El neumoperitoneo progresivo preoperatorio y la toxina botulínica tipo A son herramientas útiles en la preparación de los pacientes con hernias gigantes que han perdido el domicilio. Ambos procedimientos son armas complementarias del procedimiento quirúrgico, especialmente con el uso de técnicas protésicas sin tensión, que permiten el manejo integral de estos pacientes.
Este artículo tiene por objeto actualizar conceptos relacionados con ambos procedimientos, incidiendo en las ventajas que aportan en el manejo preoperatorio de las hernias gigantes que han perdido el domicilio.
Preoperative progressive pneumoperitoneum and botulinum toxin type A are useful tools in the preparation of patients with loss of domain hernias. Both procedures are complementary in the surgical repair, especially with the use of prosthetic techniques without tension, that allow a integral management of these patients.
The aim of this paper is to update concepts related to both procedures, emphasizing the advantages that take place in the preoperative management of loss of domain hernias.
El neumoperitoneo progresivo preoperatorio (NPP) y la toxina botulínica TB de tipo A son herramientas útiles en la preparación preoperatoria de los pacientes con hernias gigantes que han perdido el domicilio (HPD)1. Ambos procedimientos son armas complementarias del procedimiento quirúrgico, que permiten el manejo integral de estos pacientes2.
El NPP es una técnica descrita hace varias décadas que ha traído un cambio en el abordaje quirúrgico de la HPD, al posibilitar una reparación completa y reducir las complicaciones, como el síndrome compartimental abdominal y la enfermedad respiratoria restrictiva3. Goñi-Moreno decide utilizar el NPP para ampliar la cavidad abdominal en pacientes con HPD, y así poder efectuar una reducción adecuada del contenido herniario4. Aunque su uso no se ha establecido ampliamente en la mayoría de los hospitales, los grupos especializados que han incorporado el NPP han reportado buenos resultados con un riesgo aceptable5–7.
La técnica de infiltración de TB, a pesar de su relativa reciente incorporación, es una herramienta útil en la preparación prequirúrgica de la HPD, al actuar como una separación de componentes «química» reversible y con mínimas molestias al paciente8. Además, presenta la ventaja de que la acción continúa en el postoperatorio tardío, aproximadamente unos 6meses, en los que el abdomen operado va adaptando estos cambios9.
Esta revisión tiene como objetivo describir los resultados publicados en la literatura del uso del NPP y de la TB en la preparación preoperatoria de la HPD.
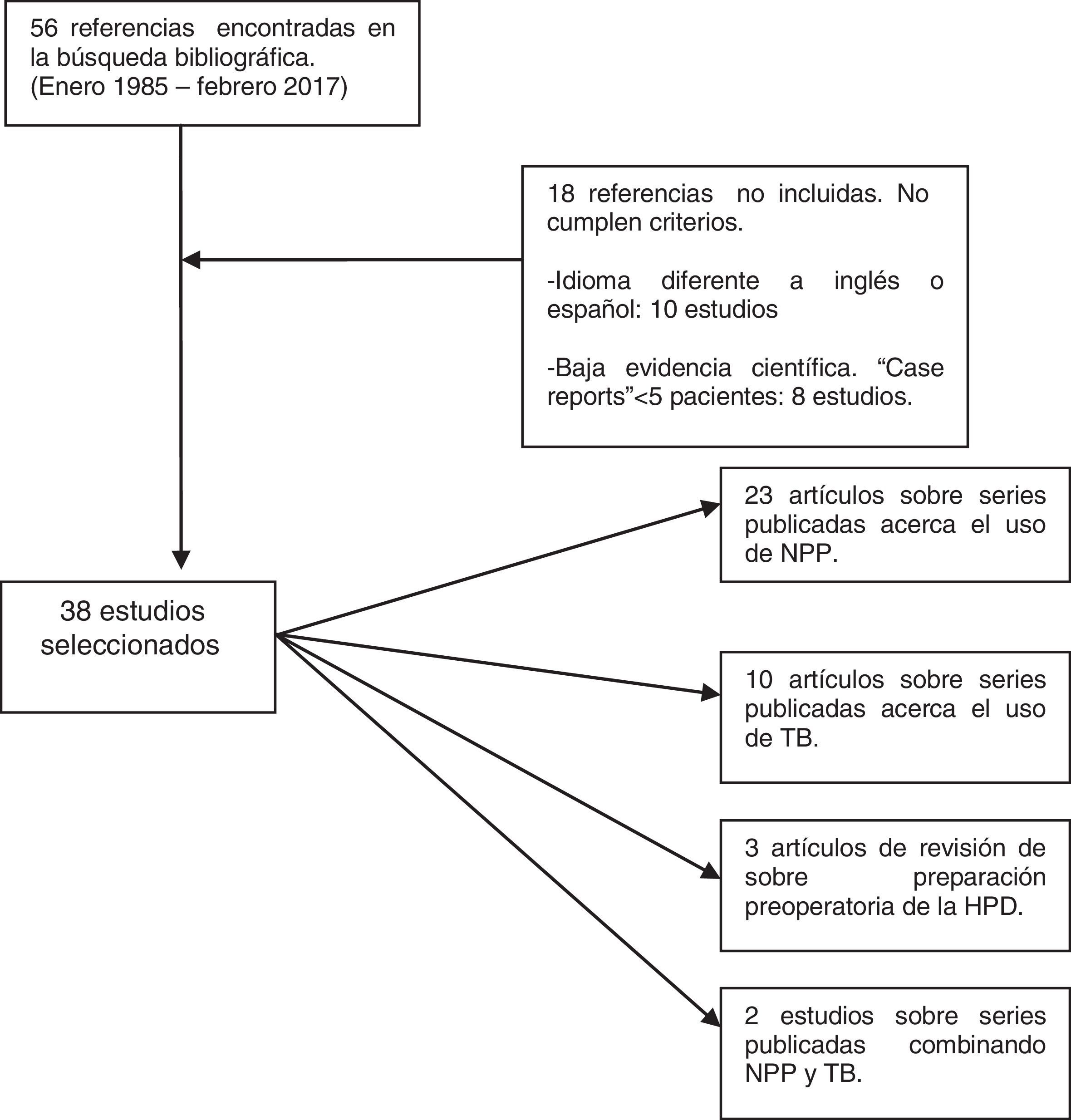
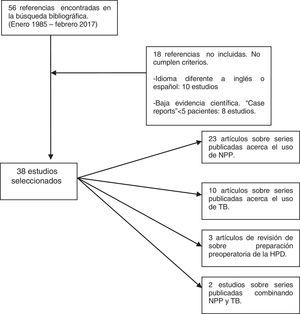
MétodoHemos efectuado una búsqueda electrónica en Pubmed y Cochrane Library (enero 1985-diciembre 2016) de artículos científicos (originales y revisiones) publicados en inglés y español con los términos «progressive pneumoperitoneum», «preoperative pneumoperitoneum», «botulinum toxin», «giant hernia», «loss of domain hernia» y «large incisional hernia». La búsqueda bibliográfica ha cumplido los criterios PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses)10. Hemos encontrado 56 referencias en común a las diferentes combinaciones de «keywords». Descartamos 18 artículos por no cumplir adecuados niveles de evidencia, ser notas clínicas con menos de 5 casos o estar escritos en otra lengua diferente al inglés o español. Finalmente hemos revisado un total de 38 artículos, valorado los «abstracts» de todos los estudios y hemos analizado en profundidad, con lectura completa de cada uno, 34 casos (fig. 1).
Neumoperitoneo progresivo preoperatorioLos objetivos que aporta el uso del NPP son11:
- 1)
Distensión progresiva de la pared abdominal para poder cerrar el defecto herniario con la menor tensión posible en el acto quirúrgico.
- 2)
Estabilizar la forma y la función diafragmática mejorando la función ventilatoria.
- 3)
Elongación de los músculos de la pared abdominal y del volumen de la cavidad abdominal.
- 4)
Disección neumática de bridas y adherencias viscerales, lo que facilita la reintroducción de las asas intestinales en la cavidad abdominal.
- 5)
Por último, está descrita la irritación peritoneal y vasodilatación local reactiva con aumento de los macrófagos los primeros días de la aplicación, lo que mejora la capacidad cicatricial.
Previamente al planteamiento de la técnica, es útil la realización de una tomografía computarizada (TC) abdominal, a ser posible en maniobra de Valsalva, para la evaluación de los diámetros y volúmenes del abdomen y del saco herniario, así como para valorar las características de la musculatura lateral y los rectos abdominales12,13. Tanaka13 fue el primer autor que proporcionó un método objetivo para calcular dichos diámetros y volúmenes con base en los hallazgos de la TC. De hecho, este autor se basa en estas medidas (volumen herniado o VIH y volumen de la cavidad abdominal o VAC) para definir «radiológicamente» la HPD. Así, una relación VIH/VAC superior al 20% es indicativa de HPD y provocaría una reintroducción traumática en la cavidad, con posible aparición de las complicaciones descritas14.
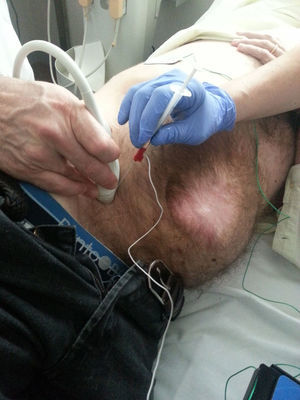
La insuflación del aire se realiza tras la inserción de un catéter que facilitará todo el proceso hasta la intervención quirúrgica. Han sido descritos diferentes procedimientos de inserción del catéter a lo largo de la evolución de la técnica15–19. La colocación puede ser guiada por ecografía, lo más frecuente, o por TC, que proporciona un mejor control de la localización20. La técnica se realiza con el paciente en ayunas y en decúbito dorsal, decidiendo el punto de punción de acuerdo con la localización de las incisiones previas y de los posibles espacios sin presencia de adherencias, preferentemente en el hipocondrio izquierdo. Grupos como el de Mayagoitia21 utilizan una aguja de Veress para la punción, similar al procedimiento laparoscópico, y un catéter subclavio de triple luz para dejarlo permanentemente en la cavidad y una jeringa de 50mm para insuflar aire ambiente. Otros grupos realizan la punción con la aguja proveniente del kit de acceso de la vía central (Cavafix®) y realizan el procedimiento de forma similar a la canalización vascular, pero a nivel abdominal1,22.
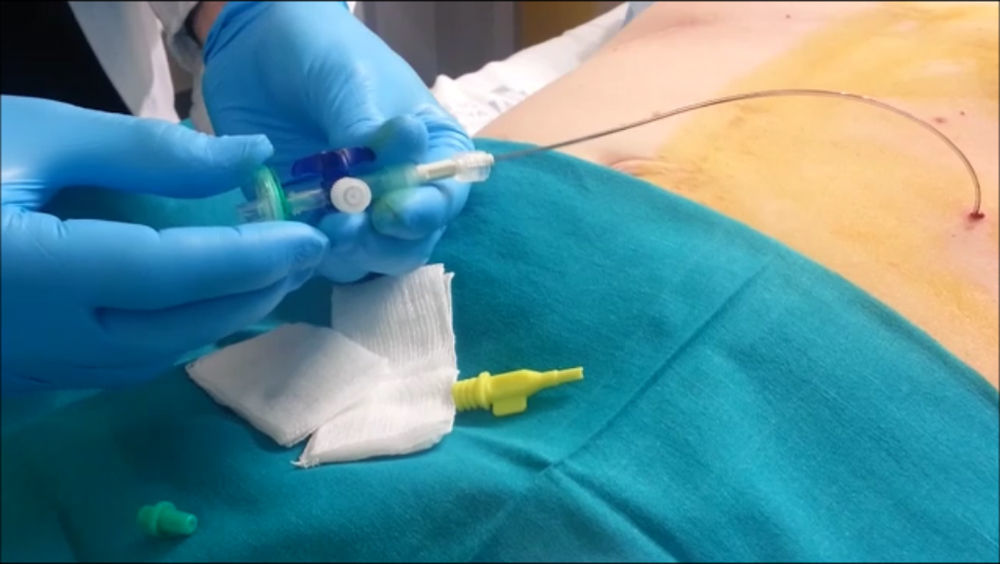
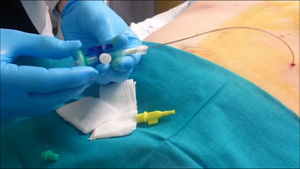
Una vez corroborada su inserción dentro de la cavidad, se prosigue con la colocación de una llave de 3vías en la luz distal del catéter y la colocación de un filtro antibacteriano (fig. 2). Así, se inicia la insuflación de la cavidad con 200-300 cc y se envía al paciente al departamento de radiología para confirmar el neumoperitoneo21. Si la radiografía muestra aire libre en ambos hemidiafragmas, se completa la insuflación de aire según el protocolo establecido previamente. Así pueden introducirse tandas diarias de 1.000-1.500 cc según la tolerancia del paciente23,24. El evento más frecuente es el dolor irradiado a la escápula, que suele ser transitorio y no precisa analgesia25.
Un aspecto interesante es la monitorización de la presión intraabdominal durante la insuflación. Aunque algún autor utiliza un esfigmógrafo conectado en la otra luz del catéter (la presión intraabdominal no debería exceder de 15mmHg)23, en general, esta comprobación ha sido abandonada, ya que la experiencia indica que es muy difícil superar los 12mmHg sin que el paciente presente severas molestias que hagan suspender la insuflación de más aire. En otras series14,25, la monitorización de la presión intraabdominal se aplica utilizando un sensor de presión laparoscópica.
Una vez terminado el procedimiento, se indica antibioterapia de amplio espectro, analgesia en caso de dolor y profilaxis tromboembólica, con medias de compresión y heparinas de bajo peso molecular. El paciente puede ser alta hospitalaria, aunque otros grupos mantienen el ingreso 24-48 h para valorar la tolerancia al NPP inicial1,23,24. Esta administración diaria puede realizarse a través de hospitalización domiciliaria o en régimen de cirugía mayor ambulatoria.
Por último, al final del proceso, se suele realizar un último control de TC abdominal, con el objeto de calcular el VAC y la nueva ratio VIH/VAC, que permitirá predecir la eficacia del procedimiento previo a la cirugía reparadora1,14,22,25,26. Algún grupo también realiza nuevas pruebas espirométricas para medir la capacidad pulmonar tras la insuflación27.
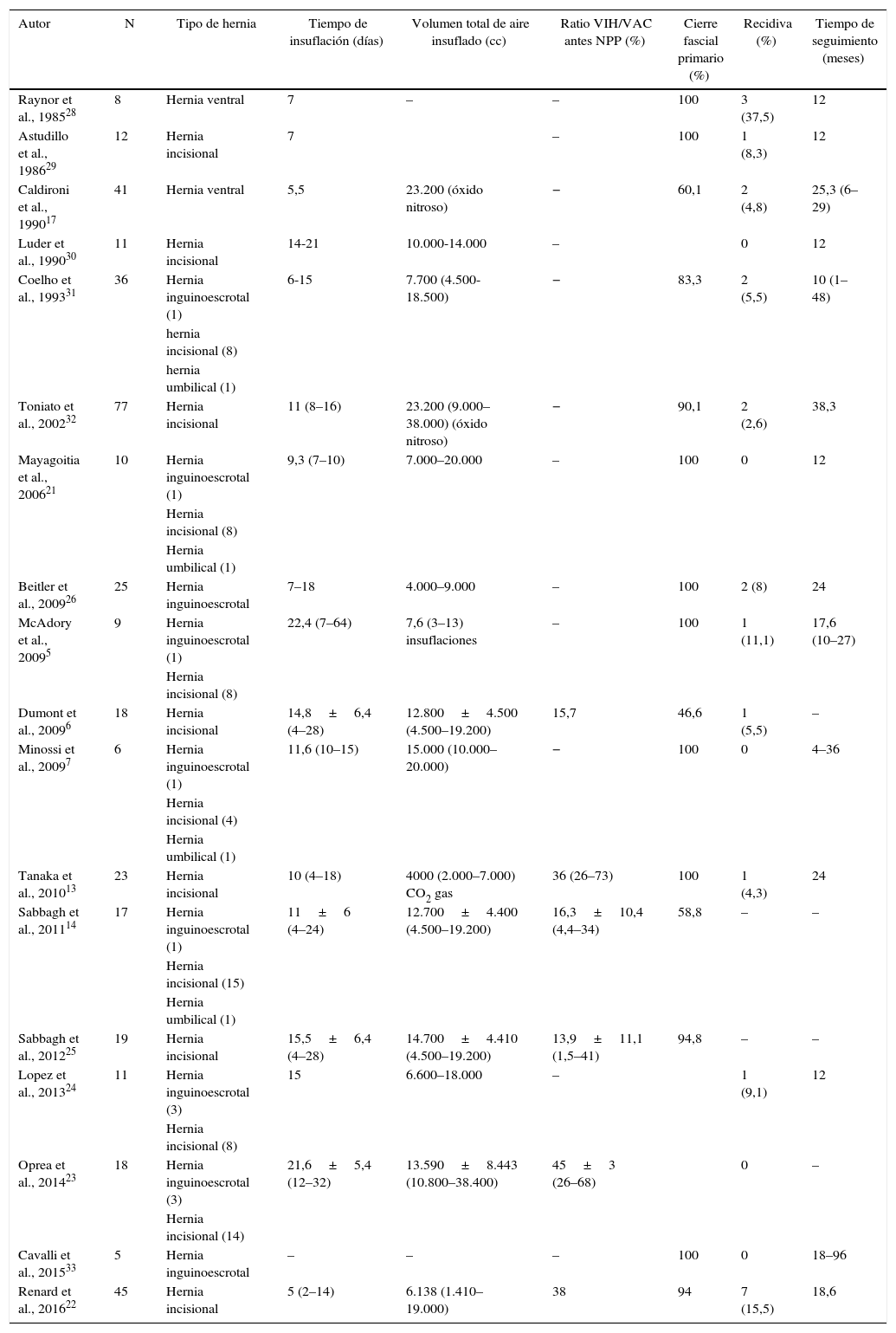
La Tabla 1 recoge las series publicadas sobre la utilización del NPP y los resultados obtenidos.
Series publicadas respecto al uso del neumoperitoneo progresivo preoperatorio en la HPD (estudios desde 1985)
| Autor | N | Tipo de hernia | Tiempo de insuflación (días) | Volumen total de aire insuflado (cc) | Ratio VIH/VAC antes NPP (%) | Cierre fascial primario (%) | Recidiva (%) | Tiempo de seguimiento (meses) |
|---|---|---|---|---|---|---|---|---|
| Raynor et al., 198528 | 8 | Hernia ventral | 7 | – | – | 100 | 3 (37,5) | 12 |
| Astudillo et al., 198629 | 12 | Hernia incisional | 7 | – | 100 | 1 (8,3) | 12 | |
| Caldironi et al., 199017 | 41 | Hernia ventral | 5,5 | 23.200 (óxido nitroso) | − | 60,1 | 2 (4,8) | 25,3 (6–29) |
| Luder et al., 199030 | 11 | Hernia incisional | 14-21 | 10.000-14.000 | – | 0 | 12 | |
| Coelho et al., 199331 | 36 | Hernia inguinoescrotal (1) | 6-15 | 7.700 (4.500-18.500) | − | 83,3 | 2 (5,5) | 10 (1–48) |
| hernia incisional (8) | ||||||||
| hernia umbilical (1) | ||||||||
| Toniato et al., 200232 | 77 | Hernia incisional | 11 (8–16) | 23.200 (9.000–38.000) (óxido nitroso) | − | 90,1 | 2 (2,6) | 38,3 |
| Mayagoitia et al., 200621 | 10 | Hernia inguinoescrotal (1) | 9,3 (7–10) | 7.000–20.000 | – | 100 | 0 | 12 |
| Hernia incisional (8) | ||||||||
| Hernia umbilical (1) | ||||||||
| Beitler et al., 200926 | 25 | Hernia inguinoescrotal | 7–18 | 4.000–9.000 | – | 100 | 2 (8) | 24 |
| McAdory et al., 20095 | 9 | Hernia inguinoescrotal (1) | 22,4 (7–64) | 7,6 (3–13) insuflaciones | – | 100 | 1 (11,1) | 17,6 (10–27) |
| Hernia incisional (8) | ||||||||
| Dumont et al., 20096 | 18 | Hernia incisional | 14,8±6,4 (4–28) | 12.800±4.500 (4.500–19.200) | 15,7 | 46,6 | 1 (5,5) | – |
| Minossi et al., 20097 | 6 | Hernia inguinoescrotal (1) | 11,6 (10–15) | 15.000 (10.000–20.000) | − | 100 | 0 | 4–36 |
| Hernia incisional (4) | ||||||||
| Hernia umbilical (1) | ||||||||
| Tanaka et al., 201013 | 23 | Hernia incisional | 10 (4–18) | 4000 (2.000–7.000) CO2 gas | 36 (26–73) | 100 | 1 (4,3) | 24 |
| Sabbagh et al., 201114 | 17 | Hernia inguinoescrotal (1) | 11±6 (4–24) | 12.700±4.400 (4.500–19.200) | 16,3±10,4 (4,4–34) | 58,8 | – | – |
| Hernia incisional (15) | ||||||||
| Hernia umbilical (1) | ||||||||
| Sabbagh et al., 201225 | 19 | Hernia incisional | 15,5±6,4 (4–28) | 14.700±4.410 (4.500–19.200) | 13,9±11,1 (1,5–41) | 94,8 | – | – |
| Lopez et al., 201324 | 11 | Hernia inguinoescrotal (3) | 15 | 6.600–18.000 | – | 1 (9,1) | 12 | |
| Hernia incisional (8) | ||||||||
| Oprea et al., 201423 | 18 | Hernia inguinoescrotal (3) | 21,6±5,4 (12–32) | 13.590±8.443 (10.800–38.400) | 45±3 (26–68) | 0 | – | |
| Hernia incisional (14) | ||||||||
| Cavalli et al., 201533 | 5 | Hernia inguinoescrotal | – | – | – | 100 | 0 | 18–96 |
| Renard et al., 201622 | 45 | Hernia incisional | 5 (2–14) | 6.138 (1.410–19.000) | 38 | 94 | 7 (15,5) | 18,6 |
No incluye «case reports», solo series con 5 o más pacientes.
No hay consenso en la literatura sobre la cantidad de aire que se debe insuflar en un programa de NPP, ni siquiera sobre cuánto tiempo debe mantenerse.
Goñi-Moreno4 termina el procedimiento cuando encuentra, por palpación, los flancos abdominales prominentes y a tensión. Como otros grupos han informado, la insuflación se detiene cuando se observa una tensión excesiva del abdomen21,27. El principal inconveniente de estos argumentos es que el cálculo del volumen no se basa en un factor objetivo y que las mediciones no son totalmente fiables ni reproducibles, por lo que únicamente es la clínica y la sintomatología del paciente tratado mediante NPP las que rigen el volumen que se insufla.
Tanaka13 administra el volumen equivalente del VIH observado en la TC preoperatoria. Recomienda el uso de NPP cuando la proporción de VIH/VAC es superior al 25%. Por el contrario, Sabbagh24 utiliza la relación entre el VIH y el contenido peritoneal total (PV); considera que el PV es predictivo del cierre de la fascia sin tensión en la HPD y representa una medida más específica del volumen de la cavidad abdominal. La relación VIH/PV es indicadora del éxito en cierre facial primario sin tensión13: si la proporción preoperatoria es superior al 20%, se puede anticipar la necesidad del NPP antes de la reconstrucción de la pared abdominal. Por último, Bueno-Lledó1 establece la necesidad de insuflar 3veces el valor de VIH, debido a pérdidas incontroladas durante el procedimiento. Posiblemente se necesitan estudios futuros para calcular el volumen correcto de insuflación de la NPP para predecir el cierre fascial sin tensión, evitando con ello el desarrollo de un síndrome compartimental abdominal.
El tiempo de insuflación del NPP será variable en cada paciente, en función del objetivo, que, según las series estudiadas, oscila entre 7 y 20 días4,5,13–17,21. Por ello, resulta necesario ajustar la capacidad respiratoria durante la duración del procedimiento, confirmando la tolerancia correcta del paciente. Habitualmente pueden insuflarse entre 1.000 y 1.500 cc diarios en cada sesión hasta que el paciente note un ligero dolor abdominal u omalgia, que suelen ceder de manera espontánea con la movilización.
El volumen total final es variable en función del tamaño del defecto y oscila generalmente entre 10 y 25 L23–37. Generalmente, el tiempo que se establece para el mantenimiento del NPP oscila entre 7 y 15 días en las hernias inguinales y de 11 a 30 días en las ventrales3,11. Según algunos grupos, la forma más precisa de saber cuándo se interrumpe el proceso de NPP y un paciente debe ser intervenido es la realización de la TC tras el procedimiento y volver a calcular los VIH y VAC1,13,14,25–27.
Toxina botulínica de tipo AEl primer estudio que informa de los beneficios de la TB sobre la musculatura de la pared abdominal fue publicado por Cakmak38. Este autor indujo artificialmente un síndrome compartimental en ratas y observó que la TB reducía la tensión de la pared abdominal y ayudaba al cierre del defecto fascial sin tensión. Aplicado al campo de las enfermedades herniarias, la neurotoxina actuaría como una separación de componentes «química», que causa una relajación de los músculos de la pared abdominal lateral.
Ibarra-Hurtado9 publica en 2009 el primer trabajo del uso de la TB en 12 pacientes con hernia ventral. El autor describe la técnica de aplicación, con la que se infiltra la TB en la musculatura lateral del abdomen. Posteriormente, Zielinski39 aporta una revisión retrospectiva de sus resultados, con administración de TB en pacientes tratados con abdomen abierto después de una laparotomía de control de daños; en todos se utilizó terapia de presión negativa para el cierre abdominal temporal hasta que se realizó el cierre fascial primario. En el 83% de estos pacientes se logró un cierre fascial precoz completo sin tensión.
Ibarra y Chávez9,40 observan una disminución significativa en el grosor y un aumento en la longitud de los músculos laterales de la pared abdominal después de la aplicación de la neurotoxina. También Farooque41 demuestra un aumento significativo en la longitud media de los músculos laterales de unos 2,8cm bilateralmente. Este grado de elongación de la pared abdominal es comparable con la separación de componentes, pero no altera la integridad anatómica de la pared abdominal, lo que preserva todas las opciones quirúrgicas para la reparación.
Otros grupos han afianzado esta técnica en pacientes con HPD y candidatos a reparación laparoscópica asistida. Así, Elstner42 aplica TB en 27 pacientes intevenidos mediante reparación intraperitoneal laparoscópica, y evidencia en la TC de control un incremento significativo en la longitud de la pared lateral de 15,7 a 19,9cm tras la administración.
Por otra parte, Zendejas43 demuestra que la administración preoperatoria de TB antes de la reparación de una hernia incisional conlleva menos necesidad analgésica opioide en el paciente, aunque no influye en otros parámetros postoperatorios como la aparición de complicaciones, en la estancia media hospitalaria ni en la recidiva.
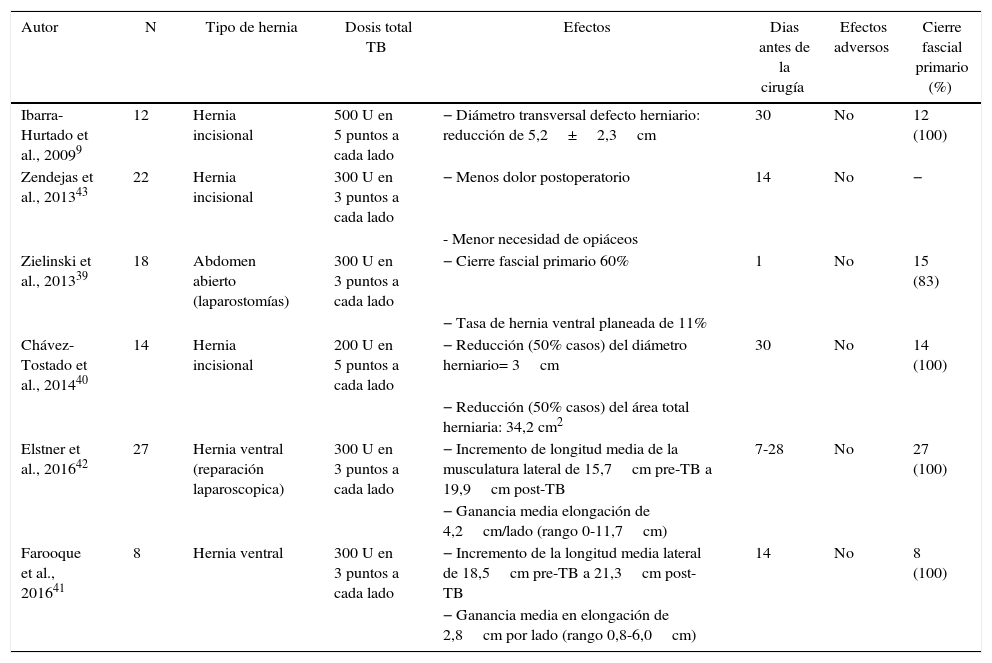
La Tabla 2 muestra las series publicadas respecto al uso de la TB en su aplicación preoperatoria.
Series publicadas respecto al uso de la TB preoperatoria en la HPD
| Autor | N | Tipo de hernia | Dosis total TB | Efectos | Dias antes de la cirugía | Efectos adversos | Cierre fascial primario (%) |
|---|---|---|---|---|---|---|---|
| Ibarra-Hurtado et al., 20099 | 12 | Hernia incisional | 500 U en 5 puntos a cada lado | − Diámetro transversal defecto herniario: reducción de 5,2±2,3cm | 30 | No | 12 (100) |
| Zendejas et al., 201343 | 22 | Hernia incisional | 300 U en 3 puntos a cada lado | − Menos dolor postoperatorio | 14 | No | − |
| - Menor necesidad de opiáceos | |||||||
| Zielinski et al., 201339 | 18 | Abdomen abierto (laparostomías) | 300 U en 3 puntos a cada lado | − Cierre fascial primario 60% | 1 | No | 15 (83) |
| − Tasa de hernia ventral planeada de 11% | |||||||
| Chávez-Tostado et al., 201440 | 14 | Hernia incisional | 200 U en 5 puntos a cada lado | − Reducción (50% casos) del diámetro herniario= 3cm | 30 | No | 14 (100) |
| − Reducción (50% casos) del área total herniaria: 34,2 cm2 | |||||||
| Elstner et al., 201642 | 27 | Hernia ventral (reparación laparoscopica) | 300 U en 3 puntos a cada lado | − Incremento de longitud media de la musculatura lateral de 15,7cm pre-TB a 19,9cm post-TB | 7-28 | No | 27 (100) |
| − Ganancia media elongación de 4,2cm/lado (rango 0-11,7cm) | |||||||
| Farooque et al., 201641 | 8 | Hernia ventral | 300 U en 3 puntos a cada lado | − Incremento de la longitud media lateral de 18,5cm pre-TB a 21,3cm post-TB | 14 | No | 8 (100) |
| − Ganancia media en elongación de 2,8cm por lado (rango 0,8-6,0cm) |
Los subtipos más usados para aplicación médica son la TB de tipo A y tipo B. La neurotoxina bloquea la liberación de acetilcolina en la terminación nerviosa y elimina por completo la actividad eléctrica que produce la contracción muscular. El efecto final es una denervación química temporal en la unión neuromuscular sin producir ninguna lesión física en las estructuras nerviosas44.
Las 2marcas comerciales de TB de tipo A más utilizadas en el mundo son el Botox® y el Dysport®. El beneficio de la neurotoxina se basa en la disminución de las fuerzas de tensión lateral sobre el defecto herniario y la elongación de los músculos laterales del abdomen con un subsecuente aumento de volumen de la cavidad abdominal, lo que permite la reconstrucción abdominal sin tensión con un período adecuado de protección8. Además, esta relajación puede disminuir la presión intraabdominal, mejorar el cumplimiento de la ventilación y reducir así la necesidad y la duración del soporte de ventilación invasiva, como reflejan varias series39,40,43. Así, la parálisis muscular se logra durante los primeros 10 días y el efecto máximo se alcanza a las 3-4 semanas, con duración decreciente los siguientes 6-9 meses43. Por lo tanto, se propone efectuar la reparación de la pared pasados 30 días, con la ventaja de tener aún 5-6 meses más de efecto de la toxina para que proteja el cierre fascial41.
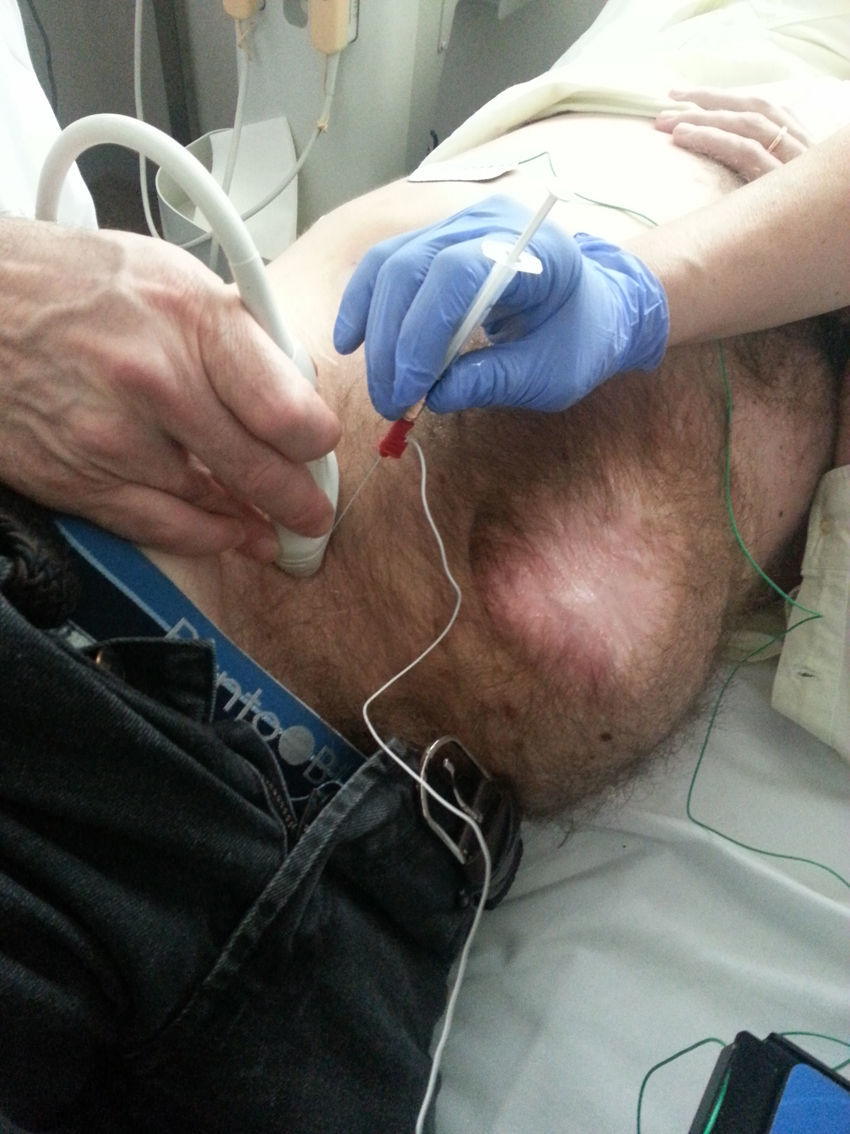
Método de aplicación de la toxina botulínica en la musculatura abdominalLa neurotoxina se aplica ambulatoriamente entre 4 y 6 semanas antes de la cirugía de reparación herniaria. Son los propios cirujanos los que la administran, aunque en algún grupo es el neurofisiólogo el que realiza la inyección1. La localización de los puntos en los que inyectar se realiza mediante control ecográfico: se visualizan las 3capas musculares laterales que se van a infiltrar (músculos oblicuo externo, oblicuo interno y transverso)40–43. Una aportación novedosa, junto a la ecografía, es la guía electromiográfica, con el objeto de identificar con precisión y confirmar si el músculo donde se aplica la neurotoxina está denervado o fibrótico según los antecedentes de la cirugía previa o el tipo de incisión, e incluso permite cambiar el punto de administración a otra zona muscular, para asegurar el efecto deseado1 (fig. 3).
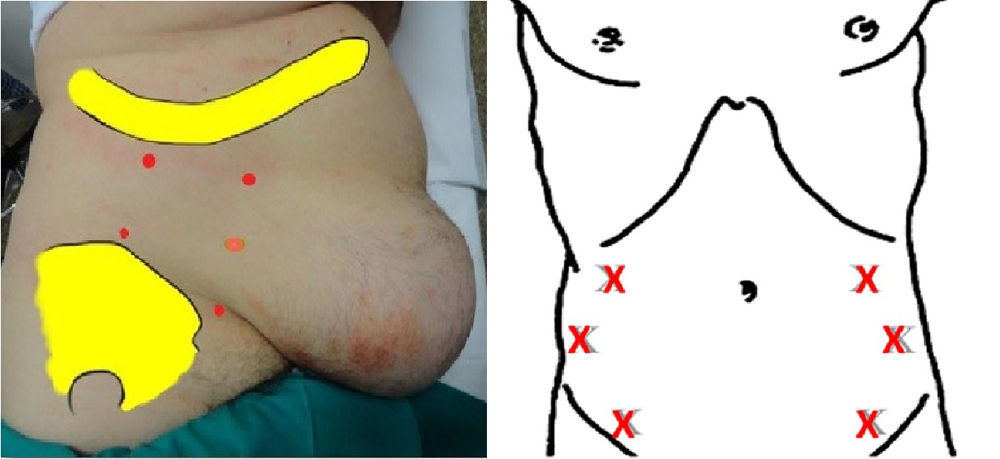
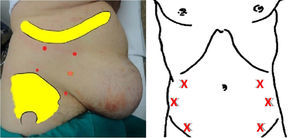
El paciente es colocado en posición lateral; siguiendo el modelo de Ibarra-Hurtado9. Generalmente se localizan 5 puntos de infiltración: 2 en la línea media axilar, a puntos equidistantes entre el reborde costal y la cresta ilíaca, y 3puntos más en la línea axilar anterior y medioclavicular entre el margen costal y la cresta ilíaca superior. Este método se repite en el lado contralateral del abdomen.
Una inyección de 5ml de Dysport® (50 unidades/5ml) o de 3ml de Botox® (30 unidades/5ml) se administra en cada punto. Si utilizamos la marca comercial Dysport®, para esta técnica se infiltran 50 U de toxina en cada uno de los 5 puntos específicos del lado derecho y 5 del izquierdo, para un total de 500 U. Si se utiliza la marca Botox®, se utilizan según la equivalencia, 300 unidades, también repartidas de igual forma.
Otros grupos de trabajo37,39,41,42 basan la localización de los puntos de infiltración según el modelo de Smooth45, a saber, 3 puntos a cada lado del abdomen, situados en la línea axilar anterior equidistante entre el borde inferior de la costilla y la espina ilíaca anterosuperior (fig. 4).
Combinación de ambas técnicas preoperatoriasDos grupos han descrito hasta el momento los beneficios de combinar el NPP y la TB (tabla 3), aunque resulta difícil analizar el efecto independiente de cada técnica preoperatoria, ya que sus efectos se superponen en el tiempo previo a la cirugía1,37.
Series publicadas con relación a la combinación de NPP y TB en el tratamiento de la HPD
| Autor | N | Tipo de hernia | Tiempo medio de insuflación (días) | Volumen total de aire insuflado (cc) | Dosis total BT (unidades) | Cierre fascial primario (%) | Recidiva (%) | Tiempo de seguimiento (meses) |
|---|---|---|---|---|---|---|---|---|
| Elstner et al., 201637 | 16 | Hernia ventral | 6,2 | – | 300 (Botox) | 100 | 0 | 21 (5–37) |
| Bueno-Lledó et al., 20171 | 45 | Hernia incisional | 7 | 8.600 (4.500–13.250) | 500 (Dysport) | 100 | 2 (4,4) | 40,5 (12–60) |
No incluye «case reports», solo series con 5 o más pacientes.
Se ha demostrado que la combinación de ambas técnicas es útil en el manejo de la HPD, para tratar diámetros y volúmenes de la hernia como preámbulo a la reparación quirúrgica. Así, Bueno-Lledó1 consigue que el VIH aumente 480 cc después de NPP y TB (p=0,003) y el VAC aumente en 2.121 cc (p=0,020). Antes y después de la NPP, la proporción VIH/VAC fue de 27,9 y 13,9%, respectivamente (p=0,001), con una reducción significativa del 14%. También se observó una disminución significativa en los diámetros longitudinales y transversales del defecto herniario. Estos valores podrían indicar el efecto beneficioso y sinérgico alcanzado por la combinación de los 2procedimientos, en comparación con los resultados obtenidos con cada técnica por separado3,9,11,21. Así, la NPP es más útil en el manejo de los 2volúmenes (directamente sobre la proporción de VIH/VAC), mientras que el efecto de la TB radica en reducir los diámetros del defecto, principalmente el transversal, al conseguir la temporal retracción de la musculatura lateral abdominal1.
También se ha planteado la hipótesis de que el uso de TB complemente el efecto de la NPP, ya que la parálisis flácida de la musculatura lateral acelera el estiramiento de la pared abdominal. Dicho efecto permite manejar mayores volúmenes de insuflación al relajar temporalmente los músculos y, por ende, acortar la duración del período de administración del NPP. Así, Elstner37 consigue el cierre fascial en 16 pacientes con hernia ventral multirrecidivada mediante laparoscopia asistida tras la combinación de ambas técnicas preoperatorias y sin objetivar recidiva herniaria tras el período de seguimiento. No obstante, resalta en su serie la aparición de complicaciones asociadas a la instauración del NPP del tipo de neumotórax, neumomediastino y acidosis metabólica, aunque pudo completar el ciclo de administración. La ganancia en el perímetro abdominal tras la combinación de BT y NPP fue del 5,6% (p<0,006), que permitió la reparación herniaria sin complicaciones postoperatorias.
Como resumen se puede afirmar que el uso del NPP y de la TB, separadamente o en combinación, son técnicas seguras, bien toleradas por el paciente y que suponen una herramienta preoperatoria eficaz en el tratamiento de la HPD. No obstante, se necesitan más estudios prospectivos que combinen o comparen ambas técnicas preoperatorias para confirmar estos resultados.
Conflicto de interesesLos autores declaran no presentar conflicto de intereses