La utilización de injertos hepáticos procedentes de donantes, en asistolia, es una de las estrategias más eficaces para incrementar la disponibilidad de órganos para trasplante1. Sin embargo, su utilidad está limitada, debido al impacto del periodo de isquemia caliente, tras la parada cardíaca, en la calidad del órgano.
La perfusión normotérmica ex vivo (MPN) puede posicionarse como una herramienta útil de valoración de la viabilidad de los órganos marginales antes de realizar el trasplante hepático y, de este modo, ayudar en la toma de decisiones. Dicha MPN permitiría evaluar el daño posreperfusión, sin comprometer la situación de un receptor en estado crítico.
El estudio prospectivo multicéntrico internacional COPE-WP2, en el cual nuestro centro ha participado, compara el efecto de la MPN y de la preservación clásica en frío, en la prevención de la lesión de preservación y de la disfunción del injerto2. Los injertos hepáticos utilizados en este estudio son procedentes de donantes en muerte encefálica y donantes en asistolia tipo 3. Con la experiencia adquirida, podemos afirmar que la utilización de la MPN es un procedimiento factible, que puede mejorar la calidad del órgano al disminuir ostensiblemente el tiempo de isquemia fría, que se limita al trabajo de banco. Este hecho justifica que la MPN pueda ser especialmente atractiva en aquellos injertos más vulnerables al daño producido por la isquemia fría, como son los donantes en asistolia tipo 2 (DA2).
Aunque los DA2 tienen un importante potencial para generar injertos hepáticos3, su utilización se ve limitada debido a los inferiores resultados postrasplante en comparación a los obtenidos con donantes convencionales4–7. Esto determina la escasa aceptación de injertos hepáticos de DA2. La utilización de perfusión regional normotérmica (PRN) asociada a MPN ha demostrado, en un modelo experimental, ser clave en la mejora de la viabilidad del injerto, y en los resultados postrasplante8. A partir de dichos resultados, nuestro centro ha iniciado un protocolo de PRN+MPN para los injertos procedentes de DA29. La fase inicial de dicho protocolo es la de perfundir aquellos injertos descartados, por no cumplir los criterios actuales de nuestro centro, y establecerlos criterios de trasplantabilidad.
En el presente trabajo, reportamos el primer caso de MPN para un injerto hepático procedente de DA2. El donante fue un paciente de 63 años de edad, que sufrió una parada cardiorrespiratoria secundaria a síndrome coronario agudo. Tras ser intubado y con 117min de maniobras de RCP avanzada, fue declarado su fallecimiento en el servicio de urgencias por el facultativo responsable, tras lo cual se inició el protocolo para posibles DA2.
Los criterios de DA2, el procedimiento de canulación y de perfusión regional normotérmica han sido previamente descritos10. Debido a que los niveles iniciales de transaminasas sobrepasaban los criterios aceptados en nuestro centro, el donante fue descartado para trasplante. Se obtuvo por parte de los familiares el consentimiento informado específico para nuestro protocolo.
La cirugía del donante sigue los pasos descritos en otros estudios10. Después de una cirugía del banco estándar, se colocan las cánulas a nivel de vena porta, arteria hepática, VCI y vía biliar. La preparación de la MPN consta en instalar el circuito desechable en la máquina, cebado con 500ml de coloide y 3 concentrados de hematíes isogrupo, y la elaboración de las soluciones de infusión (sales biliares, insulina, heparina y prostaglandinas). Al iniciar la circulación del líquido de perfusión en el circuito, se produce de forma automática su calentamiento hasta una temperatura corporal de 37°C y su oxigenación, necesarios antes de la colocación del órgano en la máquina. Una vez realizados todos estos procedimientos, el órgano se coloca en el compartimento estéril de la Organometra® y se conecta a la máquina para ser perfundido.
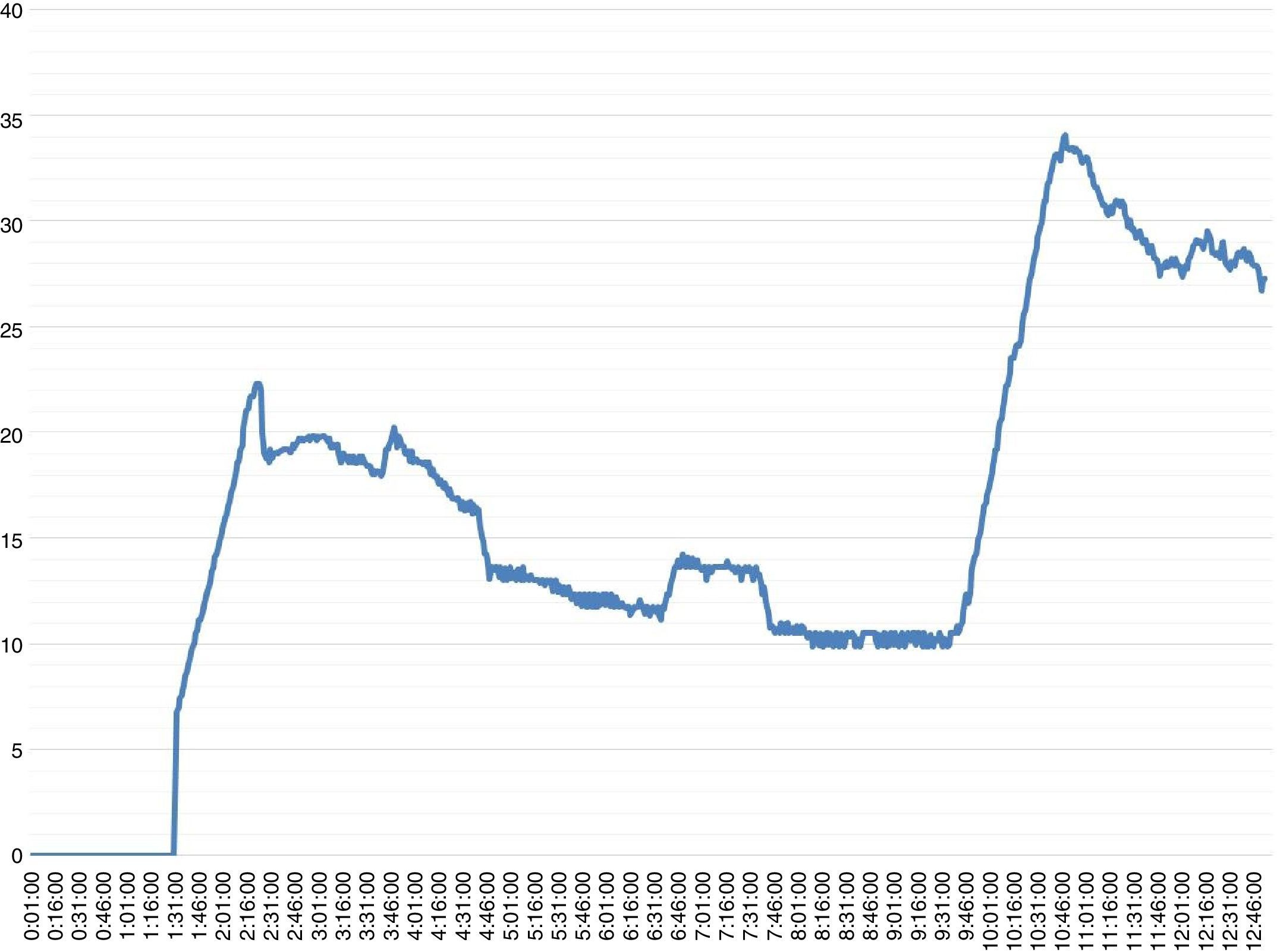
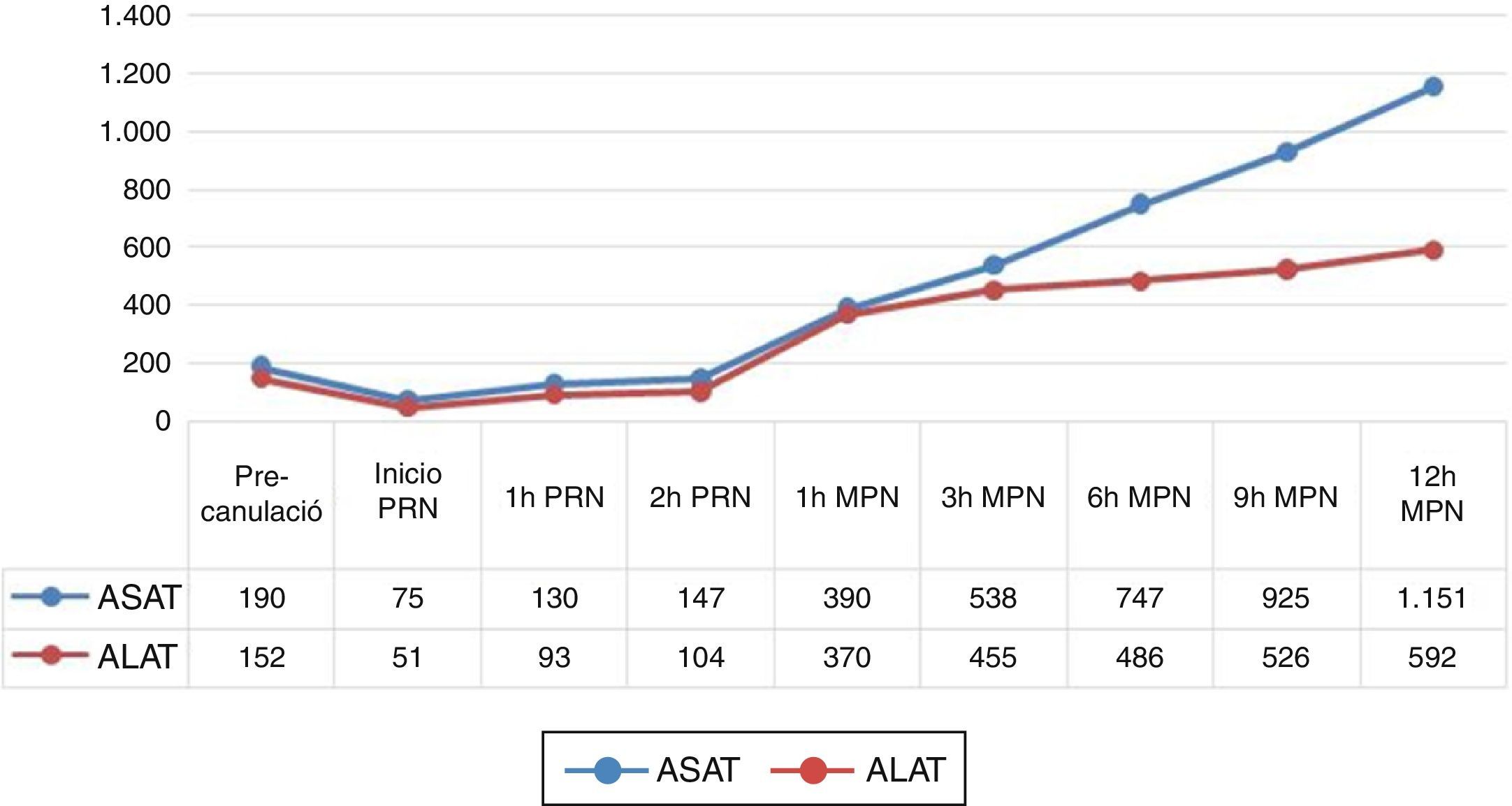
La duración de la perfusión del órgano superó las 12h. Durante la MPN, el flujo de la arteria hepática y de la vena porta se mantuvieron estables a 300ml/min y 1.200ml/min, respectivamente, mientras que el flujo biliar presentó una evolución ascendente hasta un máximo de 34ml/h (fig. 1). El pH se mantuvo constante, sin necesidad de corrección. En cuanto a los parámetros séricos, al final de la MPN, los niveles de ASAT y ALAT eran de 1.151 y 592UI/l (fig. 2), mientras que el lactato presentó una tendencia hacía la mejoría. El análisis histológico del órgano, al finalizar la perfusión, demostró mínima evidencia de necrosis hepática, con focos aislados de dilatación sinusoidal y preservación de los espacios periportales.
Los resultados de la perfusión hepática del presente caso muestran que puede existir un porcentaje de injertos descartados, siguiendo los criterios actuales de aceptación, que podrían ser rescatados para trasplante. La MPN permitiría conocer la intensidad del daño post-reperfusión y, a su vez, evitar el impacto nocivo que representa un periodo adicional de isquemia fría en estos injertos. Los resultados obtenidos en el presente estudio tendrán que ser validados posteriormente mediante el trasplante.
FinanciaciónEsta investigación ha sido financiada por la Obra Social «la Caixa».
Los autores agradecen al Servicio de Biobanco del IDIBAPS por el soporte técnico ofrecido.