Recientemente, se han descrito técnicas revolucionarias con el fin de evitar el fallo hepático secundario a hepatectomías mayores1. Robles et al.2 describieron el Associated liver torniquet and right portal vein oclussion for staging hepatectomy (ALTPS) donde se realiza ligadura portal y se coloca un torniquete sobre la línea de sección parenquimatosa, acelerando la hipertrofia y consiguiendo una regeneración eficaz en los primeros 7 días, asociando índices de morbimortalidad aceptables.
A continuación se describe un caso de ALTPS complicado con giro de la vena suprahepática (VSH) izquierda. Se trata de una paciente mujer de 57 años con antecedentes de sigmoidectomía asistida por laparoscopía en diciembre de 2014, por adenocarcinoma moderadamente diferenciado de colon sigmoides pT3 N0. Al año de la cirugía se registra una elevación del antígeno carcinoembrionario hasta 14,1ng/ml, siendo previamente normal (0-3ng/ml). Se realizó tomografía computarizada (TC) que mostró una lesión pulmonar única de 10mm en lóbulo superior izquierdo y 2 lesiones hepáticas, una en segmento IV de 18mm y otra subcapsular en segmento VII de 8mm sugestivas de metástasis. Recibió 2 ciclos de quimioterapia con leucovorina, oxaliplatino y fluorouracilo (FOLFOX), tras lo cual se realizó una nueva TC, con reconstrucción vascular y volumetría, y un PET, objetivándose un aumento del tamaño de la lesión en segmento IV a 22mm (sin compromiso de la vena cava) y estabilidad de la lesión hepática del segmento VII, y de la lesión pulmonar. Tras discutir el caso en el comité de oncología se decidió resección de las lesiones hepáticas, seguido de cirugía de lesión pulmonar en un segundo tiempo.
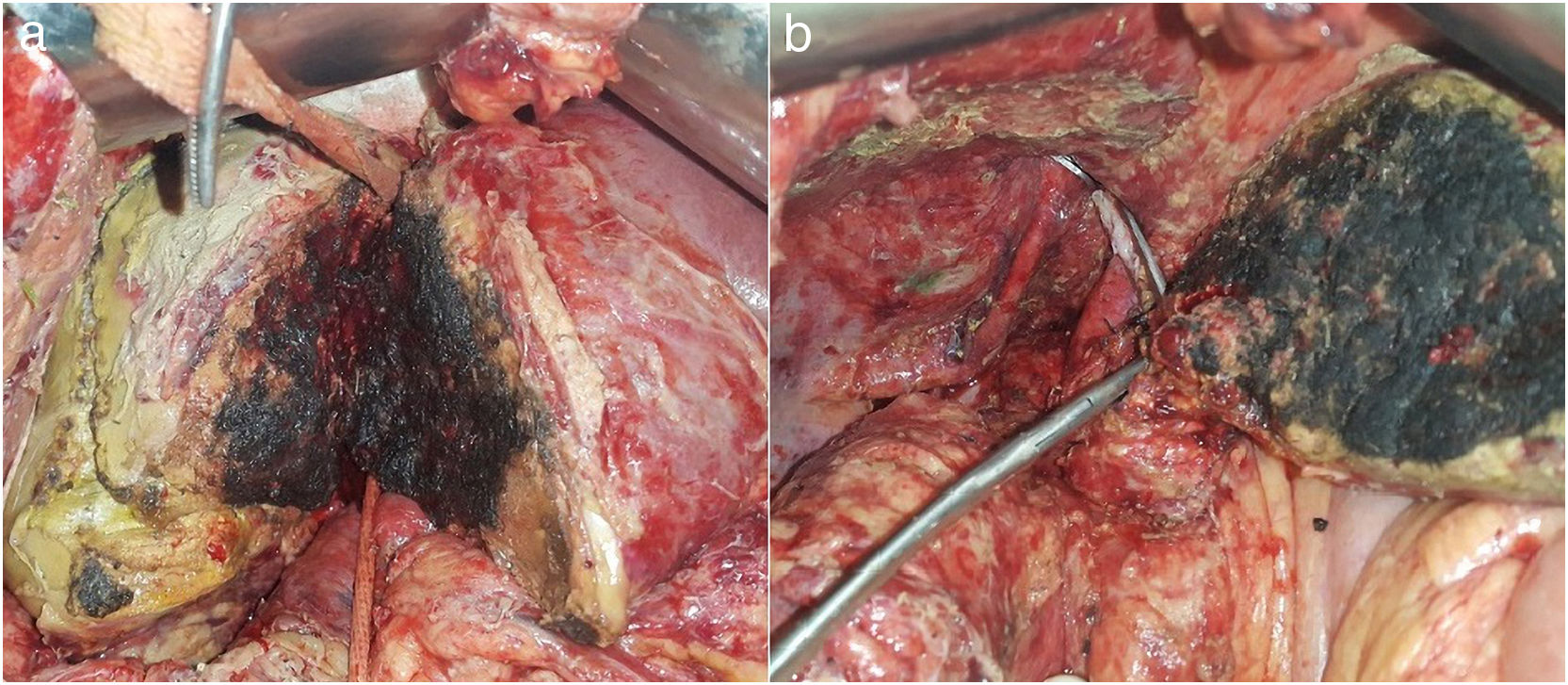
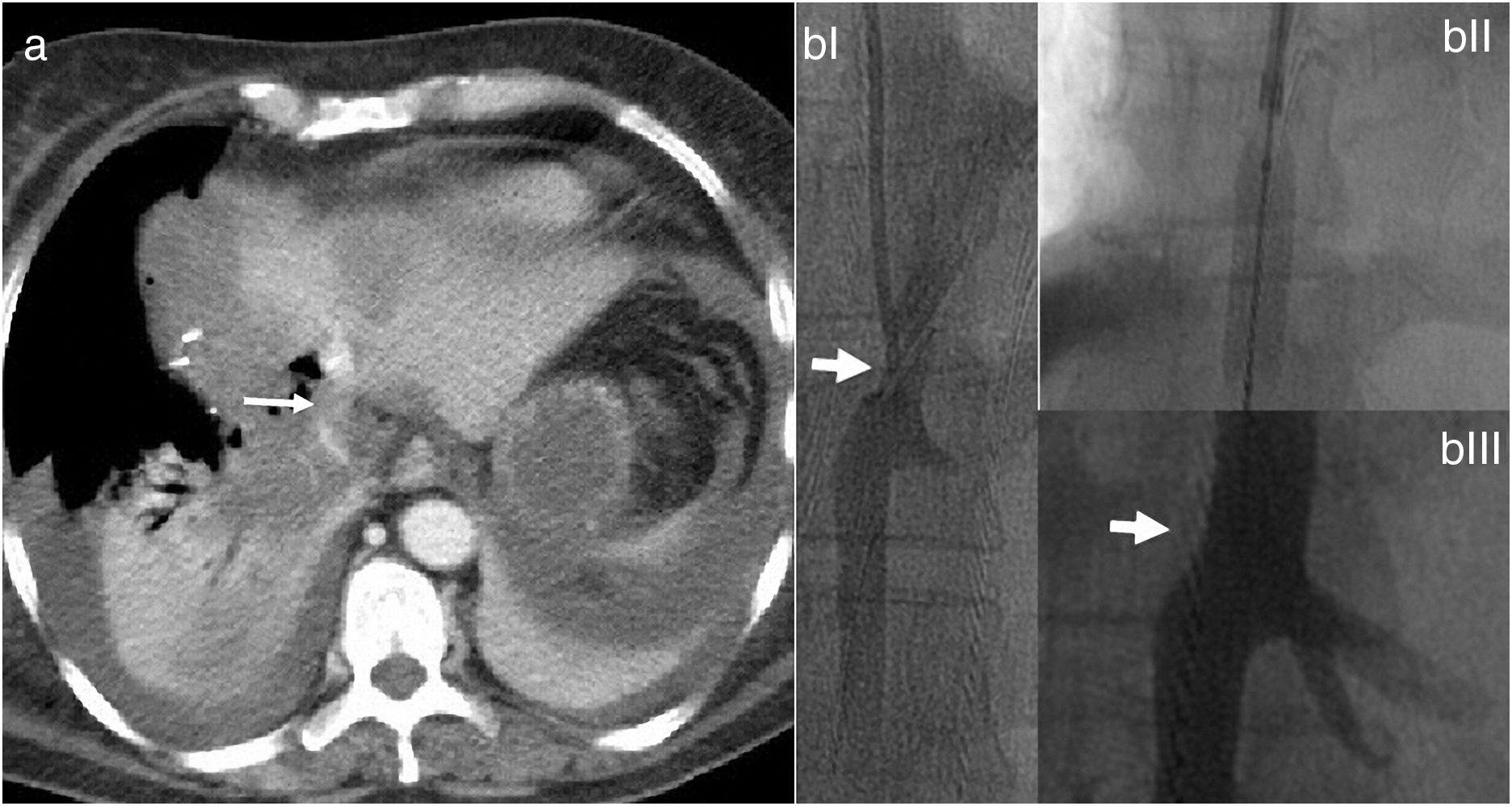
La ecografía intraoperatoria confirmó la presencia de la lesión localizada en segmento VII, siendo la lesión del segmento IV de 4cm, y en íntimo contacto con vena suprahepática derecha y media. La vena suprahepática izquierda se encontraba libre de tumor. El volumen funcional residual (VFR) del lóbulo izquierdo era de 231ml correspondiendo a un 19% (volumen hepático total de 1.178ml) para una paciente de 77kg. Se decidió realizar ALTPS siguiendo los criterios volumétricos de Morales et al.3 debido a la necesidad de una rápida hipertrofia para permitir la segunda intervención y el tratamiento de la enfermedad pulmonar en el menor plazo posible. El postoperatorio inmediato transcurrió sin complicaciones. En el décimo día se constató VFR por nueva TC de 463ml correspondiendo al 43% y se decidió segunda intervención (fig. 1a). Se observó vena cava comprometida por la lesión del segmento IV en la raíz de las VSH derecha y media. Se decidió entonces resecar el segmento de vena cava comprometido utilizando Satinsky e incluyendo origen de supra hepáticas derecha y media (fig. 1b). Se cerró el defecto de vena cava con sutura continua de Prolene® 3-0 manteniendo buen calibre y flujo. A las 12h de la cirugía, la paciente presentó inestabilidad hemodinámica y necesidad de vasopresores, requiriendo intubación. Los parámetros analíticos fueron compatibles con disfunción hepática aguda. La ecografía doppler evidenció alteración en el flujo de vena suprahepática izquierda y una TC objetivó dificultad del drenaje venoso del segmento residual de hígado compatible con torsión de vena suprahepática izquierda (fig. 2a)4. Se realizó entonces venografía que documentó estenosis de vena cava y vena supra hepática izquierda por acodamiento. Se procedió en el mismo acto a angioplastia con balón de vena cava inferior y stent 8,0×27mm en VSH (fig. 2b)5.
a) La tomografía computarizada con contraste intravenoso evidencia la dislocación del remanente hepático (la flecha señala giro de vena suprahepática izquierda); b) Venografía de estenosis a nivel de suprahepática izquierda (a). Colocación de stent (b). Resultado luego de la dilatación y la colocación del stent (c).
La evolución posterior fue favorable, se inició tratamiento con ácido acetilsalicílico (AAS) 100mg a las 48h, tras una dosis inicial de 300mg realizada durante el procedimiento. Asimismo los parámetros analíticos presentaron tendencia a la normalización (10.° día postoperatorio: GOT 50U/l, GPT 81U/l, GGT 220U/l, FAL 220U/l, bilirrubina total 1,14mg/dl y TP 15,6s, así como los controles posteriores mediante ecografía doppler. A los 15 días, la paciente fue dada de alta con doble antiagregación (AAS y clopidogrel). La anatomía patológica informó de 2 lesiones, una de 22×15×12mm con infiltración por adenocarcinoma moderadamente diferenciado con marcada necrosis, y otra de 10×10×10mm con marcada necrosis sin remanente tumoral, márgenes libres mayores a 10mm. Es posible que la necrosis tumoral y la inflamación peritumoral sean la causa de la diferencia de tamaño entre la anatomía patológica y la ecografía intraoperatoria. A los 2 meses se realizó la trisegmentectomía de lóbulo superior izquierdo pulmonar mediante videotoracoscopia, sin complicaciones. La anatomía patológica confirmó el origen metastásico de la lesión con márgenes libres y ganglios sin enfermedad. A un año y medio de seguimiento, la paciente se encuentra asintomática sin signos de recurrencia ni alteraciones en el flujo vascular.
En conclusión, se presenta un caso de insuficiencia hepática aguda en el postoperatorio inmediato tras una resección hepática debido a la rotación de la vena suprahepática izquierda diagnosticado en una unidad con experiencia en cirugía hepática y trasplante. Esta es una complicación rara, más frecuentemente observada en trasplante hepático con donante vivo que en grandes hepatectomías. En la revisión bibliográfica realizada se han encontrado 8 casos similares, sugiriendo que tras la realización de una hepatectomía derecha el lóbulo hepático remanente tiende a rotar espontáneamente alrededor de la vena cava inferior causando la oclusión del flujo venoso debido al giro de la vena suprahepática4. La incidencia de esta complicación tras hepatectomías mayores es del 0,1%6, pero en trasplante hepático con donante vivo alcanza el 5-13%7 y este aumento probablemente se deba a una hiperplasia y fibrosis intimal en los sitios anastomóticos con compresión y torsión de la anastomosis causada por la regeneración del implante8. Consideramos que, a pesar de no existir anastomosis, el crecimiento del lóbulo remante que se mantiene tras del segundo tiempo9 puede generar una rotación como la descrita ante la presencia de un gran espacio subfrénico derecho vacío y la falta de los medios naturales de fijación seccionados durante la cirugía. Además, la rápida hipertrofia con una reintervención mucho más precoz disminuyen el número de adherencias colaborando con la movilización. La utilización creciente de nuevos métodos de resección hepática puede ir asociado a un incremento en el diagnóstico de este tipo de complicaciones. Cabe aclarar que en este caso es posible que la resección parcial de la vena cava en el origen de las VSH derecha y media sea un factor favorable para la génesis de esta complicación al reducir parcialmente el calibre de la vena cava. Debería valorarse la fijación del ligamento falciforme para mantener una posición anatómica adecuada. Lógicamente, la experiencia en este tipo de resecciones es en general escasa y el tiempo marcará aspectos técnicos a mejorar para reducir al mínimo el número de eventualidades.
El diagnóstico y tratamiento temprano de la rotación de la vena suprahepática resulta clave y puede ser abordado de forma segura por hemodinamia. Las resecciones mayores y la consecuente hipertrofia hepática contralateral implican tener en cuenta esta complicación en este escenario10.