INTRODUCCION
Los alergenos son moléculas que se derivan de muchas fuentes entre las que se encuentran los ácaros del polvo de habitación, además de los pólenes, los mohos, los animales domésticos, etc.1. En la actualidad se han logrado clonar, secuenciar y expresar en diversos sistemas varios de ellos, mediante uso de la tecnología del DNA recombinante2. La mayoría de estos alergenos son glicoproteínas de variadas actividades biológicas, un gran número de estos han sido clonados, secuenciados y expresados en diversos sistemas tanto procarióticos como eucarióticos. A muchos alergenos recombinantes se les ha podido probar tanto su capacidad de unirse a la IgE como de inducir respuesta de LT, en sueros y células provenientes de individuos alérgicos, lo anterior hace vislumbrar la posibilidad de ser utilizados como herramientas diagnósticas y terapéuticas en un futuro3. Tanto en países no tropicales como en los tropicales los ácaros del polvo de habitación son la principal fuente de alergenos, siendo los del género Dermatophagoides y la Blomia tropicalis (Bt) los que ocupan los primeros lugares. La Bt se ha descrito como la principal fuente de alergenos del polvo de habitación en Cartagena.
OBJETIVO DEL TRABAJO
Probar la capacidad del alergeno rBtM de inducir una respuesta proliferativa en células mononucleares (CMSP) de pacientes alérgicos a Bt y en individuos no alérgicos.
MÉTODOS
Biología molecular
Obtención del extracto, construcción de la biblioteca de DNA complementario en el vector γgt11, aislamiento del cDNA del alergeno de Blomia tropicalis desde la biblioteca de cDNA γgt11, aislamiento de DNA de las clonas de cDNA insertadas en ggt11, subclonage del inserto en un vector plasmídico4.
Selección de pacientes
Los pacientes (seis) se seleccionaron entre aquellos que cumplieron con los criterios clínicos y paraclínicos de asma y rinitis alérgica y que además presentaron prueba cutánea positiva a un extracto del ácaro Blomia tropicalis. Como controles se utilizaron individuos sanos (cuatro) con prueba cutánea negativa.
Obtención de las muestras
A cada paciente y control se le tomaron 10 mL de sangre periférica que se disolvieron en 5 mL de RPMI-1640. Para separar la células mononucleares de sangre periférica (CMSP) por el método de Ficoll-Hypaque. Se realizó el conteo con Azul de tripano. El "pellet" se resuspendió en RPMI-1640 suplementado con 10 % se suero fetal bovino, 2 % de antibiótico (Penicilina/Estrptomicina) y 0,01 % de β2-mercaptoetanol (RPMI-10), a una concentración de 2 x 106 células/mL5.
Ensayos de linfoproliferación
En un plato de cultivo de 96 pozos fondo redondo se hicieron los cultivos con 100 μL células y 100 μL de los diferentes estímulos(RPMI-10, fitohemaglutinina (PHA) 5 μg/mL, extracto de Bt (Ext) 5 μg/mL, GST 100 μg/mL (GST1), GST 200 μg/mL (GST2), BtM 100 μg/mL (BtM1), BtM 150 μg/mL (BtM2), BtM 200 μg/mL (BtM3). Este procedimiento se aplicó a los seis pacientes y los cuatro controles por duplicado para 72 y 144 horas. Luego se incubaron a 37 °C en atmósfera de 5 % en CO2, con 20 μL de timidina tritiada a 0,5 μCi. Luego se cosechó y se hizo la lectura en el contador de centelleo beta5.
Análisis de la información
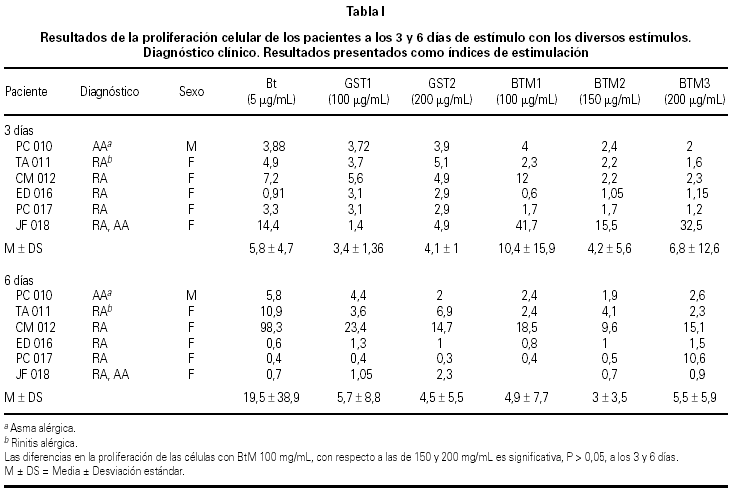
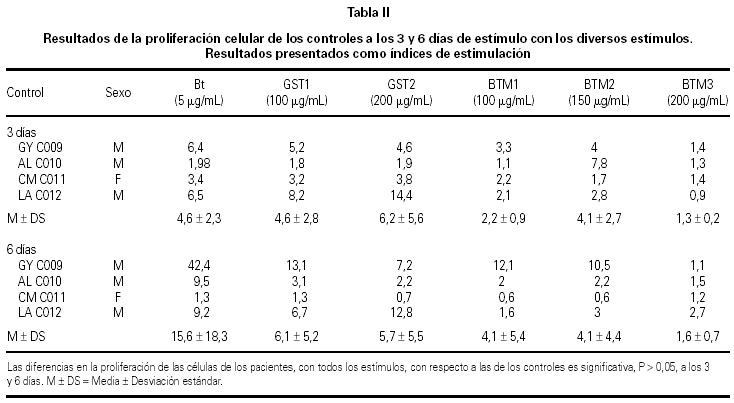
Los resultados en cpm se transformaron a Indices de Estimulación (IE)6. Junto con estos resultados, se graficó la media y la desviación estándar para cada estímulo, tanto de los pacientes a los 3 y 6 días como a los controles, así como el t de Student con una significancia del 0.05 (Pharm 4.1) (tablas I y II). Además, para determinar la diferencia entre los resultados de BtM a los 3 y a los 6 días.
RESULTADOS
Respuesta de las CMSP de pacientes alérgicos a Bt a los tres días de estímulo: Los resultados muestran como la mayoría de los pacientes respondieron de forma leve al estímulo con las tres concentraciones de BtM, solo el paciente JF018 reaccionó fuertemente a las tres concentraciones de BtM, con un valor máximo de 41,7 IE (100 μg/mL), 32,5 (200 μg/mL) de y 15.5 (150 μg/mL), valores por encima de los producidos por los demás pacientes (tabla I). Este mismo patrón de estimulación también se observó con el extracto, con un valor de 14,4 IE (tabla I). De otra parte, los resultados obtenidos con el paciente CM012, presentan una respuesta importante con un valor de 12 IE (100 μg/mL) (tabla I), valor por encima del obtenido con las otras concentraciones en el mismo experimento.
Respuesta de las PBMC de pacientes alérgicos a Bt, a los seis días de estímulo
Los resultados muestran que el paciente JF018 que había producido una fuerte respuesta a los tres días de estímulo con BtM, disminuyó significativamente (P > 0,05) a los 6 días, con valores por debajo de 1 IE (tabla I). Y el paciente CM012, que había reaccionado débilmente a las tres concentraciones de BtM, esta vez aumentó sus índices de estimulación significativamente (P > 0,05) con respecto a los tres días, 18,5 IE (100 μg/mL), 9,6 (150 μg/mL) y 15,1 (200 μg/mL). Al igual que los tres días, predomina el hecho que la concentración con mayor influencia en la proliferación de las células es la de 100 μg/mL, P > 0,05 (tabla I). Por otra parte, se destacan los valores de IE del paciente CM012 con las concentraciones de GST, de 23,4 y 14,7 (tabla I), para GST1 y GST2, respectivamente.
Respuesta de las PBMC de controles, a los tres días de estímulo
En los resultados obtenidos con los pacientes, se aprecia que las CMSP de los controles, no reaccionaron de forma considerable al estímulo con las tres concentraciones de BtM, esta diferencia en índices de estimulación es significativa, P > 0,05 (tabla II), con respecto a los pacientes, tanto a los 3 días como a los 6 días de estímulo. Se destaca la alta estimulación que produjeron las células del control LAC012 con GST, con valores de IE de 8,2 y 14,4 (tabla II), para las concentraciones de GST1 y GST2, respectivamente.
Respuesta de las CMSP de los controles, a los seis días de estímulo: En estos resultados se observa que, al igual que lo sucedido a los tres días de estímulo los valores de IE, se conservan menores que los producidos en los pacientes, con diferencia significativa (P > 0,05). A pesar de esto se destaca una ligera respuesta de estimulación del control GYC009 con el extracto, con el BtM1 y BtM2, con valores de IE 42,4, 12,1 y 10,5 (tabla II), respectivamente. También es importante el hecho que los IE del control LAC012 para GST, disminuyeron, tanto para GST1 6,7 como para GST2 12,8 (tabla II).
CONCLUSIONES
Este estudio produjo un aporte interesante para el conocimiento de la respuesta celular, que se origina a partir del estímulo de las CMSP de pacientes alérgicos a Blomia tropicalis. Como parte inicial del estudio, la capacidad de la proteína recombinante BtM de inducir una respuesta en CMSP de pacientes alérgicos a Bt, y que esta respuesta, conserva un patrón de proliferación similar a las CMSP estimuladas con el extracto de Bt, lo que se presenta como un punto de discusión interesante, al mostrar a las proteínas recombinantes como imitadoras de la respuesta inmunológica celular3,7-8. También se logró determinar que los promedios de las estimulación de las células de los pacientes a los 3 y a los 6 días, generados por el estímulo con la proteína recombinante, era de magnitud superior a la vista en los controles (P > 0,05). Resultado que va de la mano, con los datos obtenidos en las pruebas cutáneas. Esto se suma a la creencia que, la liberación de histamina por las células cebadas, después de la unión a la IgE a sus receptores en la superficie de la misma, y que es medido de manera cualitativa en la prueba cutánea, están en relación estrecha con la proliferación de las CMSP, concluyendo que la respuesta alérgica va acompañada por una producción de IgE y liberación de histamina, así como proliferación específica de linfocitos T alergeno específicos3,8. De igual forma, se destaca que no todas las CMSP de los pacientes reaccionaron de manera apreciable cuando fueron estimulados con las diferentes concentraciones de la proteína recombinante. A pesar de que los pacientes presentaron prueba cutánea positiva con el extracto de Bt. Mostrando que, a pesar que el BtM es un segmento del alergeno mayor de Bt, algunos de los pacientes muestran mayor respuesta a otros alergenos del extracto, de aquí el hecho que algunos de los pacientes de este estudio, no presentaran niveles altos de proliferación cuando fueron estimulados con la proteína recombinante. Por otro lado, es importante que la concentración de 100 μg/mL, que es la más baja de las utilizadas en el estudio, produce una proliferación significativamente mayor que las demás concentraciones (P > 0,05), lo cual hace pensar que el exceso de antígeno provoca anergia clonal dosis dependiente en las células de los pacientes, y produjeran respuestas celulares rápidas a los tres días y disminuyeran a los 6 días. Otro hecho a destacar de los resultados es lo ocurrido con el control LAC012, el cual presenta bajos niveles de proliferación con el extracto y con las diferentes concentraciones de la proteína recombinante, pero produjo altos niveles de proliferación cuando sus células fueron estimuladas con GST. Posiblemente, esté sucediendo que este individuo esté sensibilizado contra esta proteína y de allí su respuesta9. Partiendo de todo lo anterior, se puede sugerir a los alergenos recombinantes, como una buena y novedosa forma de tratamiento inmunoterapéutico, con notables resultados a nivel experimental en trabajos anteriores y en el presente estudio2,10,11.