To define the natural history of T1G3 bladder tumor not receiving intravesical Bacillus Calmette-Guerin (BCG) and to assess the diagnostic and therapeutic value of a second transurethral resection (Re-TUR) in these patients.
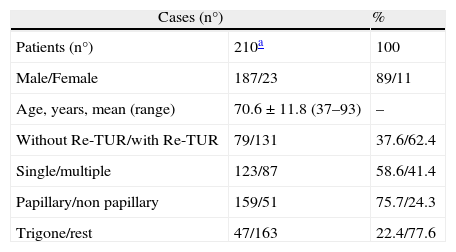
Patients and methodsRetrospective study on the natural history of 210 patients treated at two institutions for T1G3 bladder carcinoma without associated CIS. In no case was BCG administered; 79 (37.6%) received TUR alone, and 131 (62.4%) Re-TUR 4–6 weeks later; 23 (12.4%) underwent cystectomy for tumor progression.
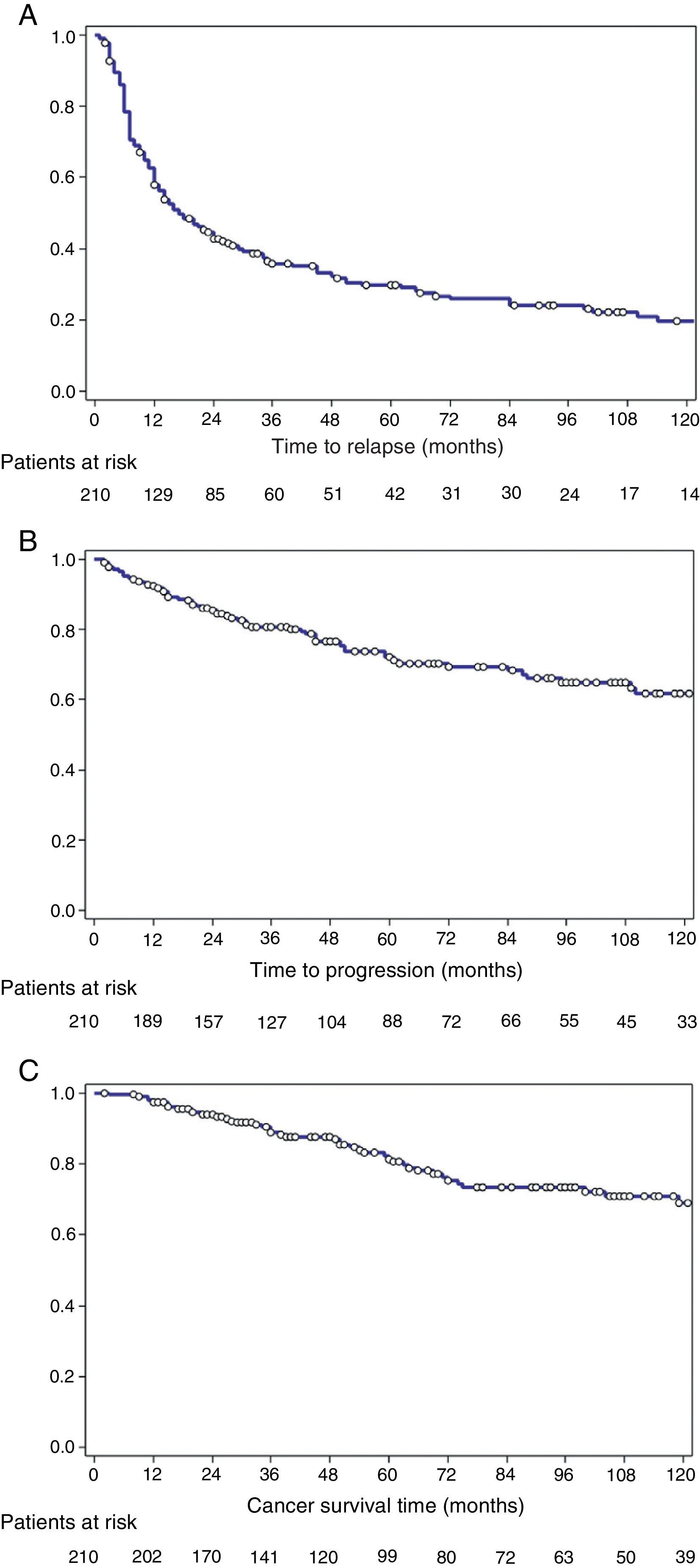
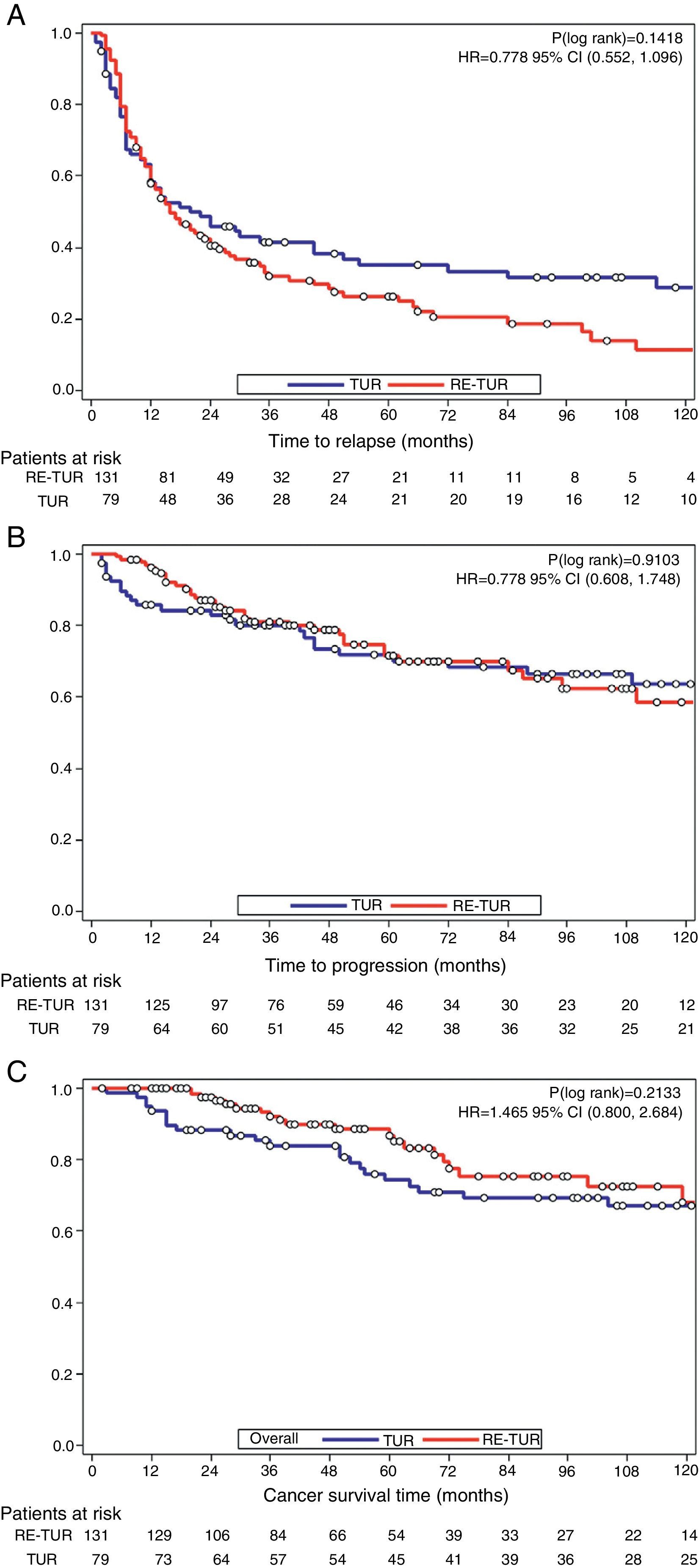
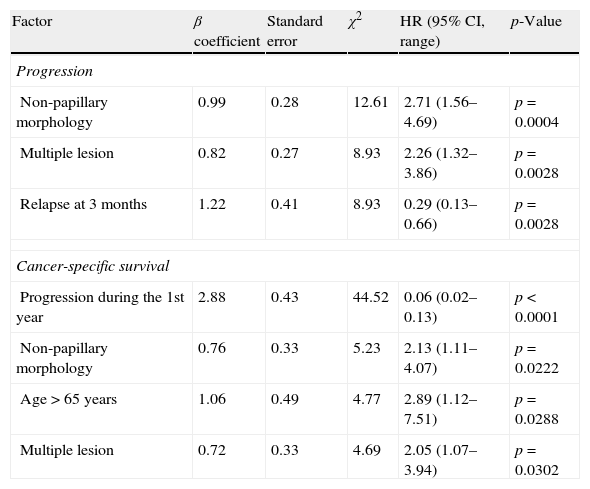
ResultsMedian follow-up was 55 (78 IQR) months, male/female ratio 8/1, and mean age 70.6±11.8 (range 37–93). 19.5% were free of recurrence at 10 years, and 61.9% free of progression. Independent prognostic factors for progression were solid pattern (HR: 2.71; p=.0004), multiplicity (HR: 2.26; p=0.003), and recurrence at 3 months (HR: 3.4; p=0.003). Cancer-specific survival was 81.5% at 5 and 69% at 10 years. Independent predictors of survival were: progression during the first year (HR: 17.9; p<0.0001), solid pattern (HR: 2.13; p=0.02), multiplicity (HR: 2.05; p=0.03), and age>65 years (HR: 2.9; p=0.03). Re-TUR avoided under-staging (7.4%), detected T1G3 residual disease (10.7%), reduced recurrence rate at 3 months (11.4–4.6%; p=0.06), and rate of progression on the 1st year (13.9–3.8%; p=.0075). However, in these patients the risk remains and no differences were detected in the long term in terms of recurrence (log-rank, p=0.14), progression (p=0.91), or cancer death (p=0.21) in patients treated with Re-TUR.
ConclusionThe recurrence in the first 3 months of a T1G3 tumor not receiving BCG is the main risk factor for progression, and progression of this type of tumors within the first year is the main factor of cancer death. The Re-TUR improves both variables but it does not change the long-term prognosis.
Definir la historia natural del tumor vesical T1G3 que no recibe bacilo de Calmette-Guerin (BCG) endovesical y evaluar el valor diagnóstico y terapéutico de una segunda resección transuretral (Re-RTU) en estos pacientes.
Pacientes y métodosEstudio retrospectivo sobre la historia natural de 210 pacientes tratados en 2 instituciones por carcinoma vesical T1G3 sin CIS asociado. En ningún caso se administró BCG; 79 (37,6%) recibieron exclusivamente RTU y 131 (62,4%) Re-RTU 4–6 semanas después; 23 (12,4%) recibieron cistectomía por progresión tumoral.
ResultadosLa mediana de seguimiento fue 55 (78 IQR) meses, la proporción hombre/mujer 8/1 y la edad media 70,6±11,8SD (37–93). Se encontraron libres de recurrencia a 10 años el 19,5%, y libres de progresión el 61,9%. Los factores pronóstico independientes de progresión fueron patrón sólido (HR: 2,71; p=0,0004), multiplicidad (HR: 2,26; p=0,003) y recidiva a 3 meses (HR: 3,4; p=0,003). La supervivencia cáncer-específica fue del 81,5% a 5 años y del 69% a 10 años. Fueron factores independientes predictivos de supervivencia la progresión el primer año (HR: 17,9; p<0,0001), el patrón sólido (HR: 2,13; p=0,02), la multiplicidad (HR: 2,05; p=0,03) y la edad>65 años (HR: 2,9; p=0,03). La Re-RTU evitó infraestadificación (7,4%), detectó enfermedad residual T1G3 (10,7%), redujo la tasa de recidiva a 3 meses (11,4 a 4,6%; p=0,06) y la tasa de progresión al año (13,9 a 3,8%; p=0,0075). Ahora bien, en estos pacientes el riesgo se mantiene y a largo plazo no se detectaron diferencias en términos de recurrencia (log-rank, p=0,14), progresión (p=0,91) o muerte por cáncer (p=0,21) en pacientes tratados con Re-RTU.
ConclusiónLa recurrencia en los primeros 3 meses de un tumor T1G3 que no recibe BCG es el principal factor de riesgo de progresión, y la progresión de este tipo de tumores en el primer año es el principal factor de muerte por cáncer. La Re-RTU mejora ambas variables, pero no modifica el pronóstico a largo plazo.