Describimos las complicaciones más frecuentes de la cirugía de implante de prótesis de pene haciendo hincapié en su manejo práctico. Hemos dividido las complicaciones en intraoperatorias y postoperatorias. Entre las complicaciones intraoperatorias destacan: La perforación de los cuerpos cavernosos durante la dilatación, el cross-over de los cilindros o colocación cruzada y la lesión uretral durante el implante. Las complicaciones más frecuentes postoperatorias son el fallo mecánico de la prótesis, la erosión de cilindros y la infección de las prótesis, haciendo énfasis en la cirugía de rescate y en las técnicas de re-implante en fibrosis de tejido cavernoso.
We describe the most frequent complications associated with penile implant surgery, paying special attention to their practical management. We have analyzed preoperative complications and postoperative complications separately. The intraoperative include perforation of the corpora cavernosa during dilation, cylinder cross-over or cross-placement and urethral injury during implantation. The most frequent postoperative complications are mechanical failure, cylinder erosion and prosthesis infection. We emphasize on rescue surgery and reimplantation techniques in cavernous tissue fibrosis.
El implante de prótesis de pene debe considerarse únicamente como el último recurso para tratar a pacientes con disfunción eréctil refractaria a tratamiento farmacológico. A pesar del coste que comportan y de su carácter invasivo, se asocian a un alto índice de satisfacción del paciente, por lo que deben contemplarse como la tercera línea de tratamiento de la disfunción eréctil1.
Existen básicamente dos tipos de prótesis peneanas: Las prótesis maleables o semi-rígidas y las prótesis hidráulicas de dos o tres componentes. Los dispositivos maleables tienen un bajo índice de fallo mecánico, aunque con ellas la longitud y el grosor del pene no cambian en las fases de tumescencia y detumescencia. Por su parte, los dispositivos inflables se basan en principios hidráulicos, lo que permite que el paciente active e inactive el dispositivo para reproducir las fases de erección2,3.
En las últimas décadas se han desarrollado diferentes mejoras en la tecnología de dispositivos hidráulicos que han reducido considerablemente las probabilidades de re-intervención por fallo mecánico de los componentes. Los datos de los que se dispone en la actualidad indican que el éxito quirúrgico que se consigue con las prótesis peneanas hidráulicas oscila entre el 95% y el 97%, mientras que la satisfacción a largo plazo del paciente se sitúa por encima del 80%4,5.
En este artículo describimos las complicaciones más frecuentes de la cirugía de implante de prótesis de pene haciendo hincapié en su manejo práctico. Hemos dividido las complicaciones en intraoperatorias y postoperatorias.
Complicaciones intraoperatoriasPerforación de los cuerpos cavernosos en la dilataciónLa perforación crural del extremo proximal del cuerpo cavernoso durante la dilatación ocurre con relativa frecuencia. Sucede fundamentalmente en pacientes con fibrosis de los cuerpos cavernosos, especialmente en la zona crural de los mismos. La causa más frecuente de fibrosis de los cuerpos cavernosos se presenta en pacientes en los que se ha tenido que retirar una prótesis previa por infección. También los pacientes con priapismo, insuficiencia vascular o enfermedad de Peyronie pueden tener cuerpos cavernosos proximales fibróticos6.
Comúnmente, el cirujano se encontrará con un «tabique» de tejido cicatricial inmediatamente por encima de la tuberosidad isquiática en estos pacientes. Si se intenta el paso de dilatadores pequeños y afilados (p. ej., Hegar #8) se puede atravesar la fibrosis bruscamente y el impulso del dilatador continuará y perforará la túnica albugínea. En realidad, en estas situaciones el cirujano básicamente está abriendo túnel en el tejido cicatricial y la perforación es muy frecuente, por lo que se debe extremar el cuidado en estos casos. Se ha informado una tasa de perforación de hasta el 50% en estos casos difíciles. Reparar formalmente la perforación tiene una gran dificultad. En principio, el paciente debe quitarse de la posición supina y reposicionarse en la posición de litotomía. Se debe hacer una incisión perineal, localizar la perforación y repararla. A menudo es difícil cerrar la perforación, ya que no existe un tejido fuerte bueno adyacente para facilitar el cierre. Debido a la dificultad de cerrar el defecto principalmente, se han adoptado métodos para mantener la base del cilindro fuera de la perforación y permitir que cicatrice, de hecho, dejando al paciente cicatrizar sobre la perforación sin intervención del médico. Todas las reparaciones tienen en común colocar una longitud de cilindro igual al lado no perforado y estabilizar de alguna manera el cilindro para que la base no migre hacia la perforación7.
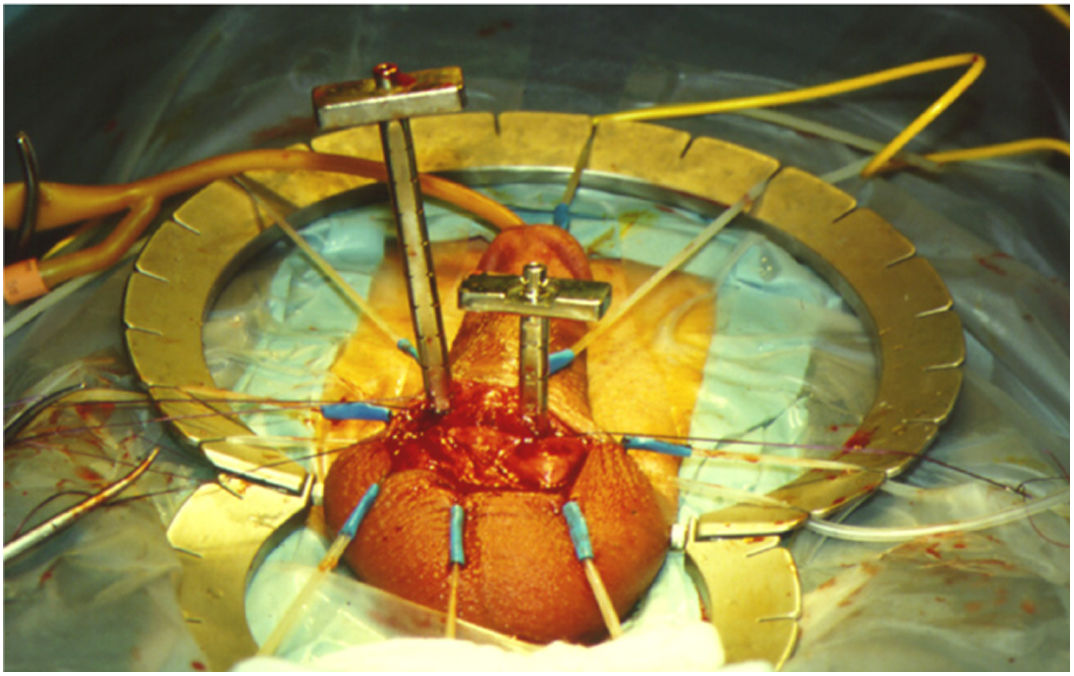
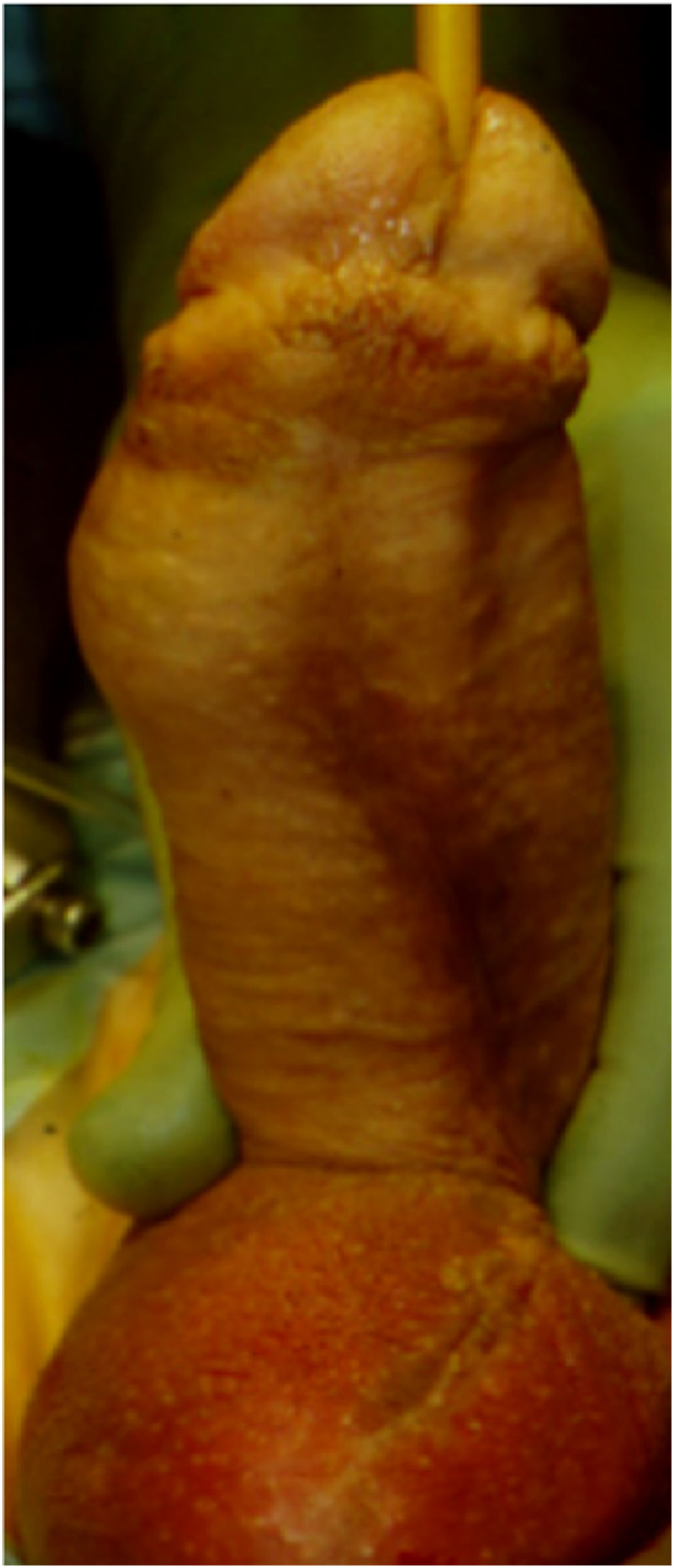
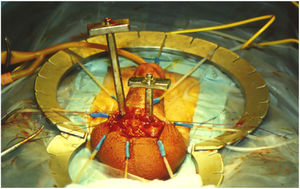
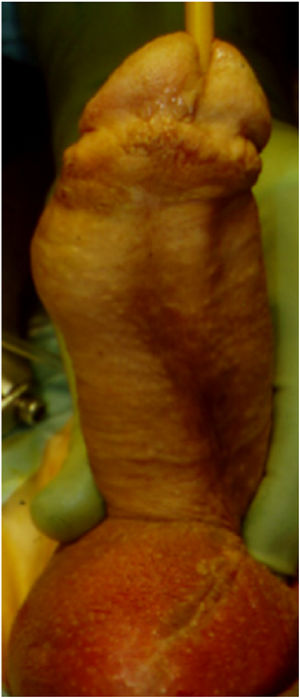
Intraoperatoriamente los dilatadores se encuentran asimétricos (fig. 1).
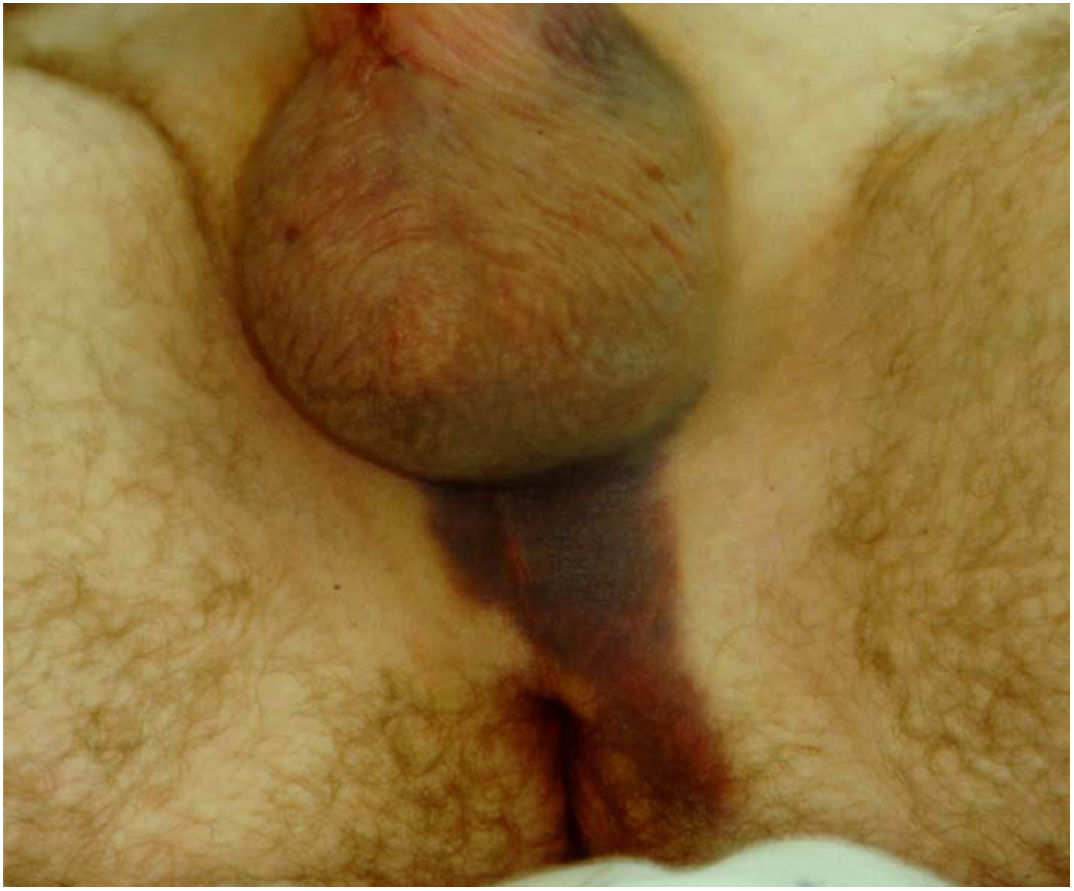
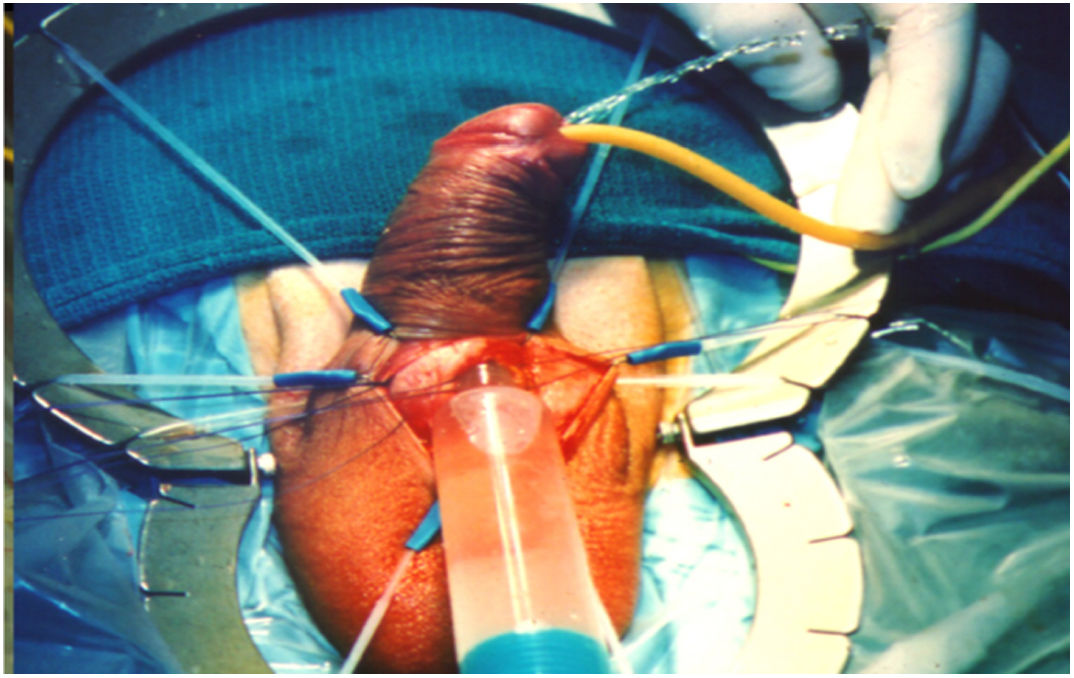
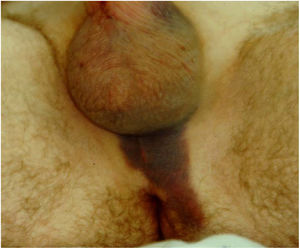
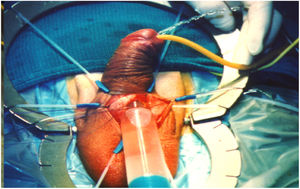
Cuando uno no detecta la perforación intraoperatoria, lo que se observa en el postoperatorio, es un cilindro más corto y un hematoma en la zona perineal (fig. 2).
Históricamente, los autores sugirieron que estas perforaciones se arreglan colocando un calcetín (windsock) de material sintético (Goretex, Dacron, etc.) alrededor de la base del cilindro y cosiendo este calcetín a la pared corporal. Varios estudios han demostrado que la adición de material de injerto a cualquier procedimiento de implante aumenta el riesgo de infección al 30%8. La razón es que tenemos un material sintético/injerto que rodea a un material sintético, el implante. Si las bacterias se interponen entre los materiales, no hay forma de que el cuerpo o los antibióticos puedan eliminar la contaminación9.
La estabilización del cilindro es fácil en un implante maleable. No hay peligro de perforación de la prótesis y se puede estabilizar con sutura no absorbible a la túnica adyacente a la corporectomía. Se sutura a través de la pared corporal, luego a través del cuerpo del cilindro maleable y nuevamente a través de la corporectomía. Finalmente se anuda la sutura después de asegurarse de que la prótesis esté bien asentada debajo del glande10.
La estabilización del cilindro también es simple con prótesis hidráulicas si sólo se ha perforado uno de los cuerpos cavernosos. Puesto que el tamaño del cilindro debe ser igual en ambos lados, se utiliza la medición del lado no perforado. Una vez colocado el cilindro debajo del glande se estabiliza el mismo pasando una sutura no absorbible a través de la pared corporal adyacente a la corporectomía y luego a través de la bota de Goretex del cilindro. Un método alternativo de estabilización es colocar una sutura no absorbible encima y debajo del tubo de entrada. Las suturas por encima y por debajo del tubo de entrada hacen que el tubo de entrada actúe como un ancla y evite que la base migre hacia la perforación. Otra técnica popular11 es utilizar el extensor proximal para que sirva de cabestrillo del cilindro.
Descripción del uso del extensor proximal para reparar una perforacion crural11 (tabla 1).
Descripción del uso del extensor proximal para reparar una perforación crural
| Extensor proximal (RTE) para la reparación de la perforación proximal |
|---|
| • Seleccionar cilindro y RTE de la misma longitud que en el lado no perforado. |
| • Usar sutura no-reabsorbible: de fuera de la corporectomía adentro. |
| • Pasar la sutura a través de la base del RTE. |
| • Pasar la sutura de Vuelta a través de la corporectomía saliendo del cuerpo cavernoso. |
| • Colocar el cilindro usando el Insertor de Furlow. |
| • Cerrar la corporectomía usando los puntos de tracción. |
| • Inflar la prótesis y ajustarla bien debajo del glande. |
| • Finalmente, anudar la sutura del RTE mientras se tracciona de los hilos conductores. |
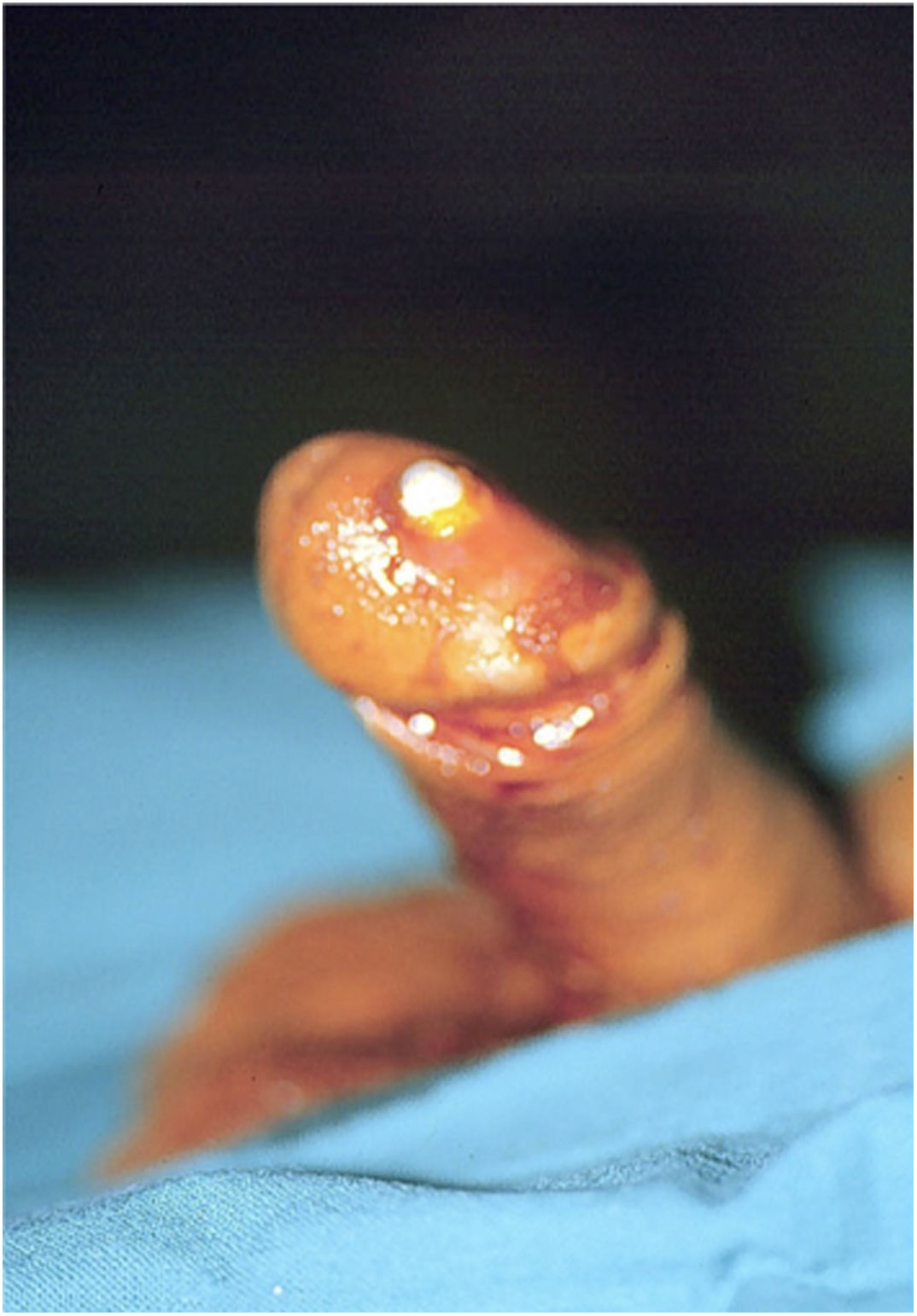
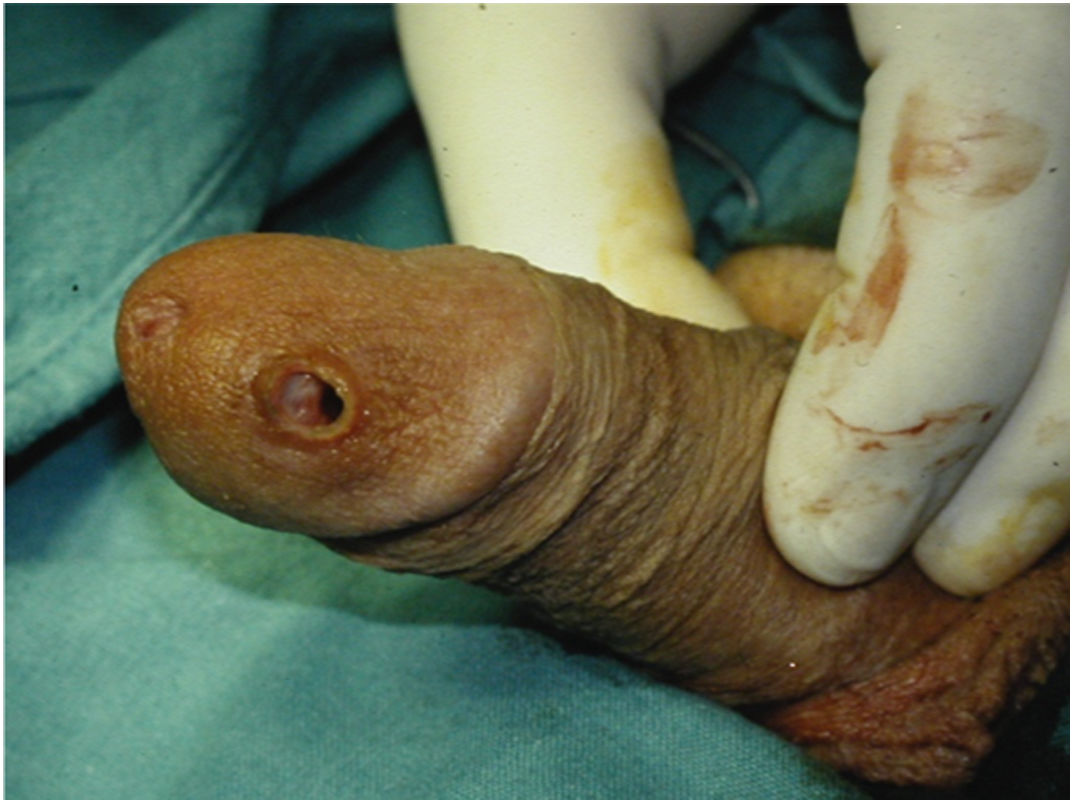
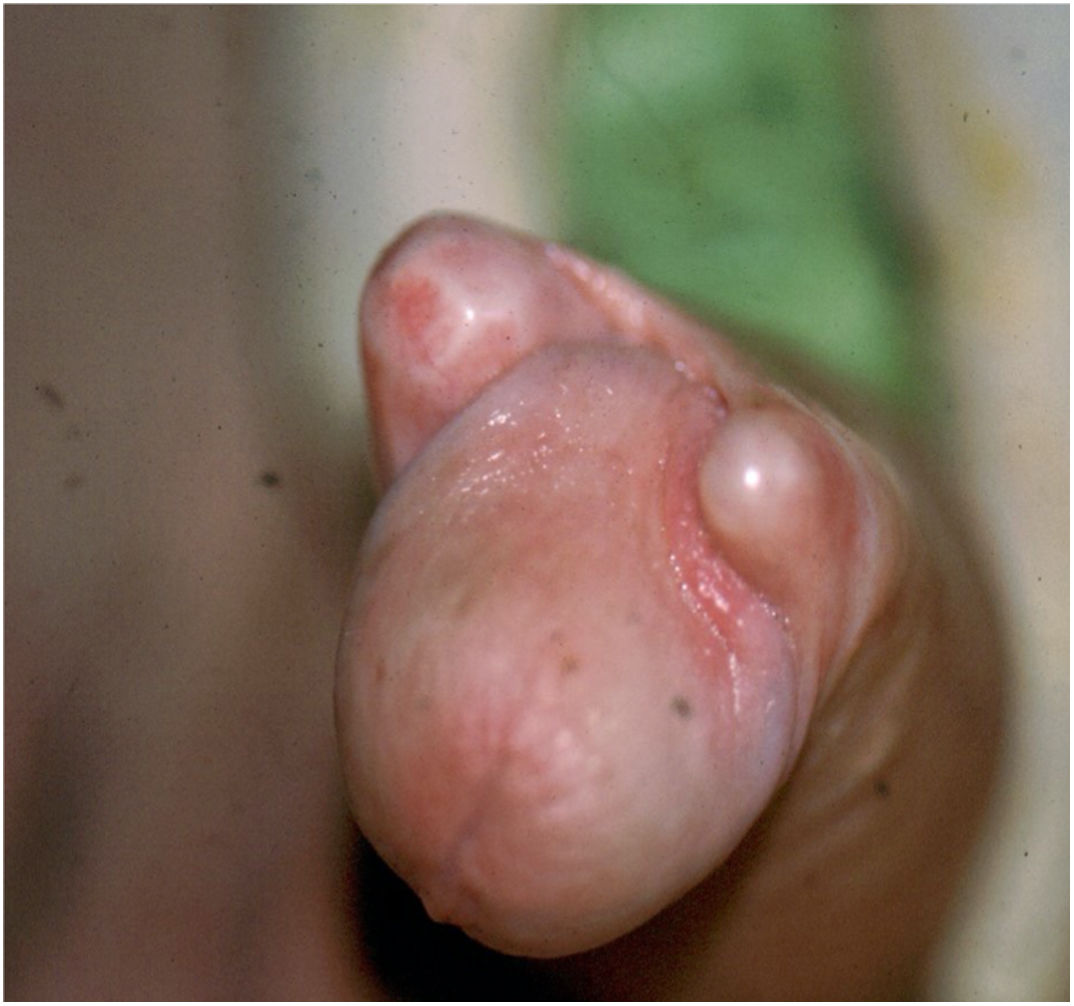
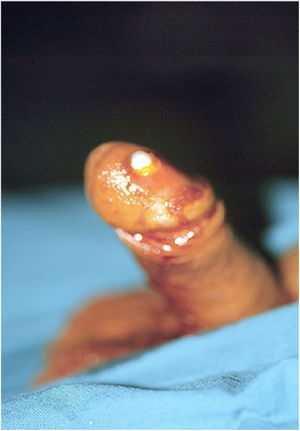
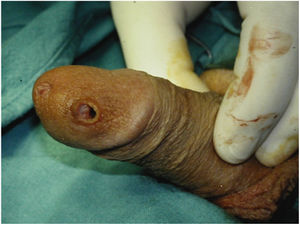
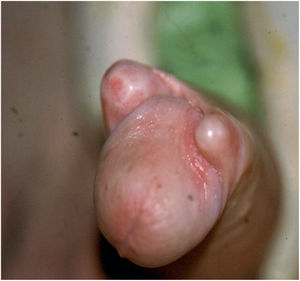
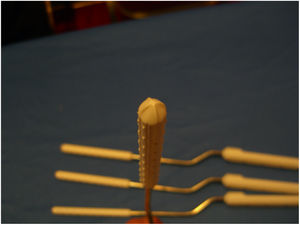
También puede existir una perforación distal pero esta es mucho menos frecuente. La perforación distal más frecuente es a través de la uretra y se tratará en la sección de perforación uretral. En los casos en los que hay fibrosis distal y además se ha debilitado el extremo distal de los cuerpos cavernosos, es decir en los casos de priapismo donde se ha hecho un shunt distal, la perforación del extremo distal de uno de los cuerpos cavernosos puede ocurrir. En estos casos el cilindro quedaría muy superficial dentro del glande corriendo el riesgo de una erosión posterior (figs. 3 y 4). En estos casos conviene disecar el extremo distal del cuerpo cavernoso y suturarlo preferiblemente sin el uso de material heterólogo, ya que favorece la infección como hemos dicho más anteriormente8.
Puede ocurrir durante el paso distal del Furlow o en la colocación proximal de los cilindros12,13. No es común que el cruzamiento de los cilindros pueda ocurrir como resultado de una migración. El septo de los cuerpos cavernosos es fenestrado. Si el cirujano no tiene cuidado durante la inserción de los cilindros puede atravesar la ventana y terminar en el lado incorrecto. A veces es difícil entender qué pasó, porque la aguja del Furlow salió por el lado del glande correcto. Lo que ocurre es que la colocación cruzada es siempre una maniobra de ida y vuelta, como el Furlow no ofrece resistencia, pasa por una ventana y sale por la otra en su viaje hacia la punta del pene14.
Normalmente la colocación cruzada se detecta en el postoperatorio cuando el paciente activa la prótesis quedando una deformidad obvia (fig. 5).
El cruzamiento distal ocurre más frecuentemente en la colocación infrapúbica de los cilindros. El pene no está estirado y el retractor no se usa para mantener el pene elongado. Si el cirujano no tiene cuidado es fácil de pasar el Furlow sobre el lado opuesto y volver al mismo lado antes de disparar la aguja a través del glande. El cruce distal del cilindro es poco manifiesto en el momento de la cirugía. Es bastante obvio después de tres meses, al inflar el lado cruzado es aneurismático y el otro lado es demasiado delgado y el pene es irregular15.
La corrección distal es fácil. No es necesario corregir el defecto del septo, ya que probablemente estuviese fenestrado antes de la colocación del cilindro (tabla 2).
Pasos para corrección del cruzamiento de los cilindros de la prótesis
| Corrección del cruzamiento |
|---|
| - Retirar ambos cilindros. |
| - Coloque un Hegar largo del lado que ambos cilindros habían ocupado. |
| - Redilatar el otro lado y pasar el Furlow con el Hegar en el lugar contralateral. |
| - Retirar el Hegar y pasar el Furlow por el lado que originalmente sostenía ambos cilindros. |
El cruzamiento proximal puede ocurrir como resultado de la escasa dilatación o en la colocación de la base de los cilindros. Parece más común en pacientes obesos y en la incisión penoescrotal que la infrapúbica. El diagnóstico del cruzamiento proximal se produce cuando el cirujano presenta extrema dificultad al asentar la base del segundo cilindro. Esto ocurre porque la primera base del cilindro pasa a través de la ventana del septum y ocupa la base del otro cuerpo cavernoso (63).
El cruzamiento proximal es fácil de corregir. No es necesario reparar el septum. Se corrige exactamente igual que el cruzamiento distal. Colocando un dilatador de Hegar en el cuerpo cavernoso proximal en el lado del cruzamiento. Luego dilatar adecuadamente y colocar el otro cilindro con el Hegar ocupando los cuerpos proximales del lado opuesto16.
Colocación del reservorio en áreas pélvica cicatricialesLa colocación habitual del reservorio es en el espacio prevesical. Si este espacio es excesivamente cicatricial después de cirugías pélvicas o de cistectomía, el reservorio puede localizarse incluso dentro de la cavidad peritoneal. Reservorios colocados dentro de la cavidad peritoneal no forman cápsula. La cavidad intraperitoneal impide la transmisión de la presión intraabdominal sobre el reservorio17.
Con las nuevas prótesis, el bloqueo valvular está presente en la bomba y en el reservorio. Esto puede prevenir que la presión abdominal cause autoinflado de la prótesis. Esto significa que el reservorio no necesita un espacio establecido como los modelos anteriores. Los reservorios pueden colocarse en la pared abdominal, anterior a las fascia pero por debajo de las capas musculares. La colocación ectópica de los reservorios ha sido probada competitivamente para la colocación de reservorio y del globo regulador de la presión del esfínter18.
La técnica para la colocación ectópica del reservorio vía infrapúbica es situándolo anterior a la fascia transversalis y con disección roma de un espacio debajo del músculo recto que pueda contener el reservorio lleno. Este mismo espacio puede ser creado vía escrotal desplazando la incisión sobre el área inguinal. Se palpa el tubérculo púbico y el dedo es insertado a través del anillo inguinal. El dedo es forzado al pasar de forma cefálica por la pared posterior del canal inguinal. Se crea un espacio anterior a la fascia transversalis y posterior a las capas musculares del abdomen moviendo el dedo hacia atrás y adelante con la yema de los dedos palpando la fascia transversalis. Una de las mayores desventajas de la colocación ectópica del reservorio es la palpación del mismo y en sujetos delgados, el abultamiento del reservorio. Debería ser menos visible con los reservorios planos. Independientemente de la palpación, muchos dispositivos (p. ej., los marcapasos) son palpables y la colocación ectópica es preferible, en nuestra opinión, a realizar una incisión abdominal separada18.
Lesión uretralSon relativamente frecuentes19. Puede ocurrir al inicio de la cirugía en la incisión peno-escrotal. El signo de esto es ver la sonda Foley colocada para vaciar la vejiga mientras disecamos los cuerpos cavernosos. Esto también puede ocurrir durante la corporectomía y también se visualizaría la sonda Foley. La uretra es muy fina en esta localización y puede repararse en dos planos y proseguir con el procedimiento. Habría que asegurarse de la reparación mediante la comprobación de la estanqueidad introduciendo líquido por el meato20.
Se aconseja dejar una sonda Foley durante tres a siete días en lugar de la retirada temprana de la sonda tras el procedimiento habitual.
El daño uretral meatal puede ocurrir durante la dilatación. Se podría encontrar resistencia con las tijeras o los dilatadores, entonces habría que forzar contra dicha resistencia. Cuando se vence la resistencia repentinamente es cuando se produce la lesión uretral. Colocando el suero a través de la corporectomía bulbar, se confirma la lesión uretral y se observa líquido a través del meato20 (fig. 6).
La porción más delgada de la túnica albugínea es al final de los cuerpos cavernosos. La disección anatómica muestra que en esta parte sólo está compuesta por dos capas a diferencia del resto de los cuerpos cavernosos que consta de tres. Si la lesión es en el meato no puede ser reparada. El cirujano debe re-programar la cirugía tres meses después. En ocasiones se podría implantar sólo un cilindro y no colocar el de lado lesionado, pero el paciente deber ser igualmente re-programado para una segunda intervención considerando los riesgos de un segundo procedimiento. En ocasiones, los pacientes quedan satisfechos con un solo cilindro. No precisa reparar el meato, tampoco prolongar el tiempo con la sonda; esto podría provocar estenosis meatal. Sin catéter la lesión repara rápidamente sin complicaciones. Cuando se realice el segundo procedimiento dos o tres meses después no habrá cicatriz y la implantación no será más complicada, casi como si no hubiera existido lesión uretral19.
Complicaciones postoperatoriasRevisión quirúrgica de los fallos mecánicosSi existe mal funcionamiento del implante el paciente, se presentará para la corrección de dicho problema. Usualmente es un implante que ha funcionado bien durante años. Uno debería saber cómo corregir la ruptura mecánica y evitar el 10% histórico de tasa de infección21.
Es importante saber que cuando el implante no funciona por rotura del mecanismo, es mejor recambiar todos los componentes después de lavar todos los espacios y recambiarlos por los nuevos recubiertos con InhibiZone22). Sin embargo, muchos cirujanos prefieren dejar los componentes funcionales y sólo cambiar el que está desgastado o roto. En 2005 se propuso reducir la tasa de infección por revisión lavando los espacios de los implantes con solución antiséptica23. La idea es que el implante roto se contaminó en la cirugía inicial de implantación con una bacteria no activa protegida por el Biofilm. Lavando los espacios con solución antiséptica y cambiando los componentes con InhibiZone se puede prevenir el 10% de tasa de infección.
Existe controversia entre los cirujanos acerca de la cantidad de las soluciones de lavado, pero todos están de acuerdo en el recambio de componentes estériles con lavados antisépticos previos24.
Mini-rescate de Wilson- -
Retirar todos los componentes si es posible. El reservorio frecuentemente es difícil de extraer y puede aumentar la morbilidad del paciente. La revisión médica aconseja dejar el reservorio en ausencia de infección. La utilización del antiguo reservorio no está del todo aconsejada. Sugerimos colocar un nuevo reservorio en el otro lado e informar al paciente que el antiguo componente queda desactivado y en caso de ocasionar problemas debería ser extraído sin compromiso de la nueva prótesis.
- -
Lavar los espacios de los implantes con soluciones recomendadas, una jeringa llena en cada lado del implante: ½ peróxido, ½ betadine, 1 g vacomincina, 80 mg gentamicina y 500 cc de suero salino.
- -
Usar drenaje con succión (p. ej., Blake o Jackson Pratt) durante 24 para facilitar la evacuación de la solución de lavado.
- -
Colocar la bomba más superficial, ya que la inflamación escrotal por las irrigaciones puede hacer más difícil utilizarla en el postoperatorio inmediato.
En el mini-rescate o en el lavado por pasos sólo se utilizan tres soluciones de lavado, el campo, los guantes y el instrumental no se cambia. Esto es porque el lavado es dirigido a eliminar las bacterias protegidas por los Biofilms en la herida y en los componentes. Esto no va dirigido a eliminar los tejidos infectados sino a prevenir la infección grave25,26.
El cambio de un componente en lugar de reemplazar todo el componente se desaconseja debido al rol del Biofilm en la prevención de las infecciones.
Es importante recordar que es mejor el uso del electrobisturí en lugar de tijera y bisturí frío. Configurar la coagulación o sólo corte. Los componentes son fáciles de disecar sin perjudicar la silicona por el corte simple en cada componente. Después de remover los cilindros es importante localizar los bordes de la corporectomía para identificar la incisión. Las referencias se pueden hacer poco apreciables con las soluciones de lavado. El reservorio es difícil de remover en particular si fue colocado por un cirujano diferente al que realiza la revisión, incrementa la morbilidad y puede ocasionar sangrado durante la revisión27. La literatura médica recomienda dejar el reservorio original. El autor aconseja eliminar el líquido del reservorio, estirar el tubo lo más alto posible y luego cortar el tubo. Nosotros asonsejamos colocar un nuevo reservorio en el otro lado28.
Infección y cirugía de rescateLa infección de la prótesis es considerada un evento catastrófico y se necesita retirar el dispositivo, a pesar de que las infecciones de la prótesis peneana raramente comprometen la vida, puede causar desfiguración y trauma psicológico. Actualmente la tasa de infecciones es menor de 1-3% para un implante en pacientes sin factores de riesgo28. Los factores de riesgo comúnmente citados son diabetes mellitus 8%, daño medular 9% y revisión quirúrgica 10%29,30. En los pacientes que toman corticoides, existe un riesgo adicional (a excepción de los transplantados renales) así como los implantes complicados requieren injertos sintéticos. Otras condiciones no consideradas factores de riesgo son la obesidad, el sitio de la incisión, circuncisión en el momento del implante y la radiación previa31. Recientemente se está poniendo mucho énfasis en las infecciones causadas por hongos reportándose un aumento en su incidencia32.
La teoría actual es que casi siempre la infección de la prótesis es causada por contaminación en el momento del implante. La diseminación hematógena es claramente rara. La bacteria trata de multiplicarse y ataca la superficie de la prótesis y el paciente en el momento usa antibióticos en el postoperatorio y el mecanismo de defensa del cuerpo para eliminar la bacteria24.
Desafortunadamente estudios recientes demuestran que a menudo cerca del 70% de las bacterias persisten, se multiplican y alcanzan suficiente cantidad para formar el Biofilm23. La bacteria puede vivir en el Biofilm inactivada por años. Viviendo en simbiosis con el huésped no dando síntomas de su existencia. Periódicamente la bacteria puede liberarse del Biofilm y esparcirse por el espacio del implante. Estas bacterias pueden producir síntomas y podrían ser eliminadas por los mecanismos de defensa del cuerpo y la administración de antibióticos usuales. La reserva de bacterias continúa protegida en el Biofilm y esto es porque la administración crónica de antibióticos muchas veces es inútil33.
El Biofilm inhibe la fagocitosis y proporciona una barrera a los antibióticos en las áreas donde las bacterias están presentes. Este es a menudo visible mientras se revisa una prótesis clínicamente no infectada por malfuncionamiento y proporciona un escondite para las bacterias. Es aún desconocido que en la revisión protésica de un implante pueda causar un 10% de infección en reservorios no contaminados por bacterias inactivadas. Por esta razón es aconsejable remover todos los componentes y lavar los espacios con soluciones antisépticas con la finalidad de disminuir la tasa de infección en las revisiones del fallo del mecanismo de las prótesis.
Se sospecha infección tras el implante en pacientes que presentan dolor crónico tras meses de la cirugía, la presencia de fiebre, eritema o la fijación de los componentes de la piel, también nos hacen sospechar una infección. La presencia de drenaje purulento a través de la herida o en zona de presión por los componentes o zonas de erosión a través de la piel es indicación de infección34.
El uso de antibiótico por intentar limpiar la zona de infección suele no ser exitoso probablemente por el fenómeno del Biofilm antes expuesto. Cuando se sospecha de una infección es mejor revisar la herida y remover todos los componentes, en el intento de dejar el reservorio muchas bacterias podrían haber migrado por el tubo y ocasionar una infección meses después. La técnica tradicional es remover todos los componentes, suturas e injertos, si se usaron. Un esfuerzo particular presentan los alargadores de las «botas» de los componentes de AMS que pueden oscurecerse por el crecimiento interno. También el alargador trasero si es dejado puede ocasionar infección persistente y requeriría otra intervención. Para seguridad de haber removido todos los componentes se podría realizar una resonancia magnética nuclear (RNM)35.
Remover los implantes sin la colocación inmediata de uno nuevo puede ocasionar pérdida de 3 5 cm de longitud peneana. Retrasar la cirugía puede representar un reto por la cicatrización después de la retirada de la prótesis. Este método nuevo fue llamado de rescate y permite la preservación del implante evitando la retracción y la dificultad quirúrgica en la reinserción de la prótesis por la cicatrización27.
Este procedimiento implica retirar todos los componentes y el material externo, lavar la herida con soluciones antisépticas y reemplazar la prótesis por material nuevo. Este procedimiento ha ganado en popularidades y en el seguimiento a largo plazo con el 80-90% de éxito.
Los miroorganismos de baja virulencia como el S. epidermidis o el S. lugdunensis causan la mayor infección de prótesis. Estas infecciones se presentan tarde en el curso clínico, al menos seis semanas y en ocasiones años después del implante. El paciente no se encuentra particularmente enfermo. Puede presentar dolor crónico, fijación de algún componente a la piel, fistulas de los tubos o cilindros. Si el escroto no está inflamado o las arrugas no están lisas, estos casos son ideales para la técnica de salvación28.
Ocasionalmente la prótesis se puede infectar muy pronto (menos de dos meses) y el paciente estará sintomático, con inflamación escrotal y eritema, drenaje purulento, fiebre, etc. La etología de estas infecciones son microorganismos más agresivos como S. aureus, pseudomona, E. coli o enterococos. La técnica de salvación es menos probable en estos pacientes posiblemente sépticos. Estas bacterias son capaces de penetrar desde el exterior al espacio del implante. Por esta razón el tejido alrededor de la prótesis y la cavidad están infectados produciendo celulitis e incluso abscesos. En estas circunstancias usar vacomicina y gentamicina durante 48-72 horas antes de la cirugía mejora los resultados de éxito. Obviamente la presencia de abscesos o fluctuaciones deben ser drenadas antes de la técnica de salvación. Si puede recolectarse líquido para cultivo, esto puede determinar un antibiótico apropiado sustituyendo a la terapia empírica usada con anterioridad36.
La ventaja de la técnica de rescate es al menos mantener la longitud peneana.
Se ha abogado por una técnica de retraso, en este caso, la prótesis es retirada y se colocan drenajes e instilaciones de antibióticos durante 72 horas. Al mismo tiempo se opta por un antibiótico más específico sustituyendo al iniciado de forma empírica. El paciente es operado después del tiempo de drenaje y la cobertura es antibiótica. Esta técnica retrasada es más costosa, con mayor estancia hospitalaria y conlleva dos intervenciones quirúrgicas. En adición que la inflamación tras 72 horas es mayor y puede ocasionar dificultad en el cierre de la herida. Inicialmente se reportaron datos de resultados similares con el implante inmediato. Subsecuentemente los autores no consiguieron sustentar su entusiasmo inicial y la técnica del recambio inmediato se ha convertido en el método preferido. Furlow y Goldeasser abogaron por un salvamento parcial. Si la herida no presenta secreción purulenta o celulitis, si la bomba es expuesta se extrae y se coloca una nueva sin cambiar el resto de los componentes. Este procedimiento no fue tan exitoso como el recambio de toda la prótesis37.
Boston Scientific y Coloplast han introducido materiales que retrasan-previenen la infección34,38,39. Resultados tempranos de estos componentes sugieren beneficios en las tasas de infección en relación con las de prótesis recubiertas en comparación con las que no lo presentan. Una recomendación importante es que con los nuevos materiales de menor tasa de infección no permite al cirujano disminuir su vigilancia al momento del implante ni el uso de antibióticos profilácticos. A pesar de los reportes iniciales y los beneficios encontrados se necesitan varios números de implantes y experiencia de centros y cirujanos para demostrar beneficios estadísticamente significativos40.
Erosión de los cilindros y deformidad en SST (Super Sonic Transport)
La protrusión o extrusión de las prótesis es inusual (fig. 7). Estas circunstancias pueden estar predispuestas por dilatación agresiva por dilatadores más pequeños o por cilindros de tamaño mayor o excesiva presión contra el final del pene durante las relaciones sexuales41. La protrusión puede ser resuelta usando un injerto natural. Se realiza una hemicircuncisión en el lado de la extrusión42. Se realiza una corporectomía en el lado de la extrusión y el cilindro es extirpado. La pared posterior de la vaina que contiene al cilindro es incidida y se desarrolla un nuevo plano detrás de la cápsula distal al final del cuerpo cavernoso. La cápsula original interior contendrá el cilindro implantado. La guía de sutura del cilindro puede ser reemplazada y pasada por esta cavidad previamente ocupada por la guía de sutura. Se crea un nuevo tracto dorsal y medial a la original cavidad del cilindro. El cilindro es guiado por esta nueva cavidad pasando la aguja de Keith a través del glande usando el Furlow. Deberá ser reforzada con sutura reabsorbible la pared externa de la cápsula a lo largo de la túnica albugínea42.
Una técnica alternativa es reparar mediante un injerto con material sintético al final de la prótesis y reemplazarla dentro de los cuerpos cavernosos reforzando la túnica albugínea. Esto interpone un cuerpo externo con otro cerca de la superficie de la piel. Carson comparó las dos técnicas y concluyó que la primera era más exitosa43.
La hipermovilidad del glande es una complicación usual. Ha sido llamada inclinación del glande, deformidad en Concorde y STT, esta última descripción hace referencia al avión supersónico (Super Sonic Transporter)42. Esto se ha visto más a menudo cuando la medida no ha sido adecuada (muy corto) para la adecuada elongación distal o cuando la prótesis ha actuado como expansor. Otros casos pueden pasar desapercibidos si la perforación es proximal con la migración del cilindro. Finalmente, el efecto concorde-SST puede aparecer en casos de correcta colocación de la prótesis y otras razones no conocidas siendo más frecuente en pacientes no circuncidados. Ocasionalmente después de un implante el glande parece muy móvil. A pesar de que la literatura recomienda fijación inmediata del glande, nuestra experiencia ha sido una subsecuente formación de cápsula alrededor de la punta del cilindro que a menudo se corrige el problema. Si el glande permanece blando después de la cicatrización puede ser fácilmente corregido con un procedimiento sencillo.
La utilización de cilindros cortos puede ser corregida con la redilatación y la colocación de extensores posteriores. Si el problema es la migración proximal del implante urinario, el implante puede ser reemplazado con un 3-piezas y el extensor posterior estabilizado mediante una sutura-cabestrillo o sutura no absorbible firmemente sujeta a la túnica albugínea. Si el tamaño del cilindro y el sitio de colocación son adecuados y sigue persistiendo el problema de la movilidad del glande o inclinación a pesar de un correcto tamaño de la prótesis, la fijación del glande debe ser planteada. Ball describió la técnica en 1980 y sigue siendo válida después de 40 años41.
Se realiza una hemi circuncisión próxima al glande y se diseca a través de la túnica albugínea. No se apertura la túnica albugínea pero se usa una guía para la disección distal por debajo del glande en cualquier lado de la línea media. En efecto la deformación en SST disminuye con la creación te estos espacios debajo del glande y la punta del cilindro sea visible en la zona distal de los cuerpos cavernosos por debajo de la túnica. Se colocan suturas no reabsorbibles por debajo del glande. Los cilindros vacíos son ordeñados en su vaina proximalmente y las suturas son colocadas en la túnica distal por encima de la punta del cilindro con cuidado de no dañar el mismo. Al anudar las suturas de la túnica distal se corrige el problema44.
Reimplante e los cilindros en fibrosis de cuerpos cavernososEl reto más difícil en la prótesis urológica es la reinserción del implante peneano en el tejido cicatricial de un implante infectado previamente o un episodio de priapismo. En estos casos, el tejido esponjoso fácil de dilatar es reemplazado por tejido fibrótico cicatricial. La fibrosis es peor distalmente en pacientes postpriapismo y proximalmente en prótesis infectadas45. El acortamiento del pene es notable particularmente en los pacientes que han tenido una infección protésica. La fibrosis desafía la dilatación con instrumentos convencionales como los dilatadores de Hegar o Brooks. El tamaño estándar de los cilindros de AMS o Mentor requiere una dilatación de 12 mm para la colocación correcta de la base de los cilindros. Para crear el espacio necesario para colocar los cilindros, la técnica tradicional precisa de resecciones corporales extensas y cubrir los defectos con material sintético. Incluso los cirujanos más experimentados reportan sólo un 50% de supervivencia del implante al año. Posibilidades de éxito en la reimplantación en estas condiciones de fibrosis son aún menores en cirujanos no experimentados46-48.
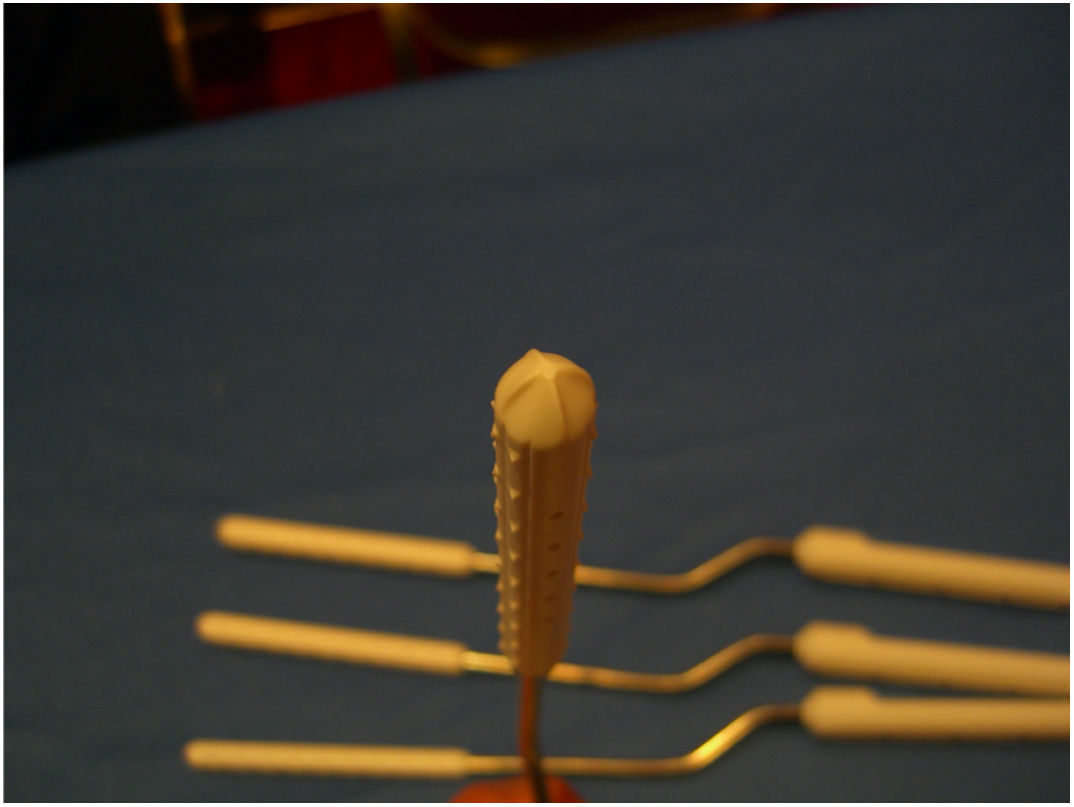
A finales de los 90, la introducción de dos instrumentos mejoró la tasa de éxito en estos casos. Primero fueron los cavernotomos de Carrion-Rossello (fig. 8).
Estos eran secuenciales (9-12 mm) dilatadores de metal con dientes que cortan hacia atrás. Se hacen avanzar de forma osciltante caminando con el dilatador dentado a través de los cuerpos cicatriciales. Con la retirada los dientes raspan el tejido cicatricial. Inicialmente usaron metal y actualmente están disponibles con dientes de plástico más afilados48.
En 1999 Moreville reportó un nuevo dilatador, el cavernotomo Uramix (fig. 9) con una cuchilla lateral, eran aún más pequeños: 6-13 mm de diámetro. Estos cavernotomos permiten al cirujano taladrar un espacio en el cuerpo cavernoso fibrótico con controles de 1 mm de corte y de este modo crear una cavidad en el tejido cicatricial40.
La minimización del tamaño de los cilindros tiene bases más estrechas y menor expansión de los cilindros. La CXM de AMS introducida en 1989 requiere dilatación de 11 mm para la inserción de la base. Esto fue la mejora sobre el tamaño estándar de los cilindros, pero los materiales recientes son incluso más estrechos30. La NB de Coloplast requiere dilatación de 10 mm y las CXR de AMS necesitan sólo 9 mm de cavidad. Combinando la creación de túneles con estos cavernotomos especiales y los implantes cada vez más finos, acompañados de la experiencia de los cirujanos permite una mayor tasa de éxito en la reimplantación de estas difíciles circunstancias45.
Mientras el cirujano consigue el éxito en estas condiciones, los pacientes están descontentos con la longitud después del implante. Típicamente los cilindros implantados son 4 a 6 cm más cortos que el de la cirugía inicial, por no mencionar que además son más pequeños en circunferencia. Los pacientes deben ser animados a la posibilidad de aceptar implantes más grandes después de utilizar unos implantes más pequeños y finos. Esto es muy parecido a la enfermedad de Peyronie y la deformidad en reloj de arena que después de usar implantes pequeños para corregir la fibrosis, ocho a 12 meses después se pueden reimplantar unos cilindros estándar de BS o Coloplast. Esto a pesar de que en el procedimiento inicial no es posiblecrear una cavidad suficiente para aceptar un diámetro estándar de cilindros. En adición, con el tiempo y el uso hidráulico, el acortamiento por el tejido fibrótico y el efecto corcorde-SST pueden ser notados debido a que los cilindros son muy cortos. Durante la reinserción de unos cilindros standard es a menudo posible incrementar la longitud 2 a 3 cm. Estos cilindros correctamente situados eliminan la hipermobilidad del glande49.
Lo pacientes postpriapismo no presentan un acortamiento severo como los pacientes con prótesis retiradas por infección. La retracción intracorpórea es menor en pacientes con fibrosis por priapismo que en pacientes con prótesis infectadas. Pacientes postpriapismo suelen tener mejora de la circunferencia, sin embargo, permite la colocación de cilinros de tamaño estándar.
ConclusionesDe todos los tratamientos disponibles actualmente para la disfunción eréctil, el implante de prótesis es el que tiene el nivel más alto de satisfacción. Estudios americanos comparan pacientes con tratamientos orales, inyecciones y bombas de vacío y posteriormente tuvieron prótesis peneana, ellos determinaron que la prótesis tiene mayor nivel de satisfacción que los tratamientos conservadores. Las prótesis peneanas están disponibles desde hace aproximadamente 40 años y representan un rol importante en el tratamiento de la disfunción eréctil. A pesar de ello las prótesis son la última opción de tratamiento, siendo incluso más confiables y duraderos. Virtualmente cualquier paciente que es informado y clínicamente apto para continuar con su vida sexual, puede ser candidato para un implante de estos dispositivos y mejorar su calidad de vida.
Conflicto de interesesI. Moncada es miembro del Global Advisory Board de BSC.