Introducción
Se han propuesto numerosos procedimientos de cirugía periodontal para el tratamiento de la recesión gingival. Entre ellos destacan los injertos gingivales libres, los injertos de tejido conjuntivo (ITC), la regeneración tisular guiada (RTG) y los colgajos pediculados. El éxito logrado con los injertos gingivales libres a la hora de cubrir las raíces denudadas dista de ser óptimo, con porcentajes que oscilan entre el 53% y el 85%1-5. La primera técnica que utilizó los ITC para el tratamiento de la recesión gingival fue presentada por Edel6 y posteriormente fue modificada por otros autores7-10. Las ventajas asociadas a la técnica del ITC son un elevado porcentaje de éxito y un elevado porcentaje de predictabilidad a la hora de lograr el recubrimiento radicular, así como un resultado estético favorable. Los estudios clínicos han demostrado que los porcentajes de éxito del recubrimiento radicular asociado al ITC oscilan entre el 80% y el 98,4%4-5. La técnica de la RTG también se ha utilizado para lograr el recubrimiento radicular. En teoría, la RTG también facilitaría la regeneración real de los tejidos periodontales en las zonas de recesión. Los porcentajes de éxito asociados al recubrimiento radicular mediante RTG oscilan entre el 54% y el 87%11. Sin embargo, aún no se ha confirmado una regeneración periodontal significativa en las raíces recubiertas con la técnica de la RTG12.
El colgajo avanzado coronalmente (CAC) es un colgajo pediculado simple que puede utilizarse para el recubrimiento radicular y no requiere la realización de un injerto. Sin embargo, algunos resultados han demostrado que el recubrimiento radicular asociado con el CAC empleado de forma aislada es inestable a largo plazo, reduciéndose del 89% tras un mes de la intervención hasta el 58,8% a los 6 meses13. Para ser más exactos, debe mencionarse que Zucchelli y De Sanctis14 demostraron resultados estables a largo plazo a los 5 años de un CAC para subsanar defectos de recesión múltiples (94% de recubrimiento radicular). Una posible limitación del CAC es la ganancia limitada en la dimensión apicocoronal del tejido queratinizado, lo cual es un importante parámetro a la hora de prevenir la recurrencia de la recesión gingival4. Así pues, los resultados indican que el uso del CAC de forma aislada es una técnica que dista de ser óptima para lograr el cubrimiento radicular a pesar de la ventaja que supone su baja morbilidad10. Sería deseable disponer de una técnica quirúrgica que pueda combinarse con el CAC para superar sus limitaciones como tratamiento de la recesión gingival. El ITC a menudo se utiliza junto con el CAC para el recubrimiento radicular con porcentajes elevados de éxito y de predictabilidad.
Varios estudios clínicos e histológicos revelan que un concepto terapéutico de concentrado plaquetario específico podría ser un medio alentador para la mejora de la cicatrización y regeneración del tejido blando en periodoncia e implantología15,16,17. La fibrina rica en plaquetas (FRP) pertenece a una nueva generación de concentrados plaquetarios con un procesado simplificado. La FRP fue desarrollada por primera vez en Francia por Choukroun y cols.15 para ser utilizada de forma específica en cirugía oral y maxilofacial. Las técnicas de preparación de la FRP no requieren la presencia de anticoagulante ni de trombina bovina. Sobre la base de la información recopilada, este estudio se diseñó para evaluar la implementación de una FRP en el tratamiento de la recesión gingival. Una membrana de FRP consiste en una matriz 3D de fibrina polimerizada en una estructura específica con la incorporación de plaquetas, leucocitos y factores de crecimiento, y la presencia de células progenitoras circulantes18,19. El análisis bioquímico de la composición de la FRP indica que este biomaterial está formado por una asociación estrecha de citocinas, cadenas glicánicas y glicoproteínas estructurales entrelazadas en una red de fibrina polimerizada lentamente15,17,18. Además, un tipo específico de polimerización de la fibrina en la FRP aumenta el tiempo de vida de estas citocinas, lo que es especialmente favorable para el proceso de cicatrización18,19.
Hasta la fecha, según la información de que disponen los autores, solamente se ha publicado un caso en relación al uso de FRP en el tratamiento de la recesión gingival20. En este estudio se evaluó si la adición de un coágulo autólogo de fibrina rico en plaquetas a un colgajo avanzado coronalmente mejoraría el resultado clínico en comparación con el uso de un CAC aislado para el tratamiento de recesiones gingivales múltiples.
El derivado de la matriz del esmalte (DME) es un preparado comercializado que consiste principalmente en amelogenina y proteínas afines derivadas de los muñones dentales porcinos. Durante el desarrollo fetal, estas proteínas de la matriz del esmalte (PME) son secretadas y depositadas de forma temporal en la superficie de la raíz por las células de la vaina epitelial radicular de Hertwig. Al parecer son esenciales para la formación del cemento acelular y el desarrollo del ligamento periodontal y del hueso alveolar21. El DME ha demostrado favorecer la formación del cemento acelular óseo y la funcionalidad del ligamento periodontal22,23.
Los resultados histológicos de la evaluación del impacto del DME en las intervenciones de recubrimiento radicular confirmaron la eficacia de esa intervención. Se ha descrito la formación de cemento y hueso nuevos tras el recubrimiento de la raíz con un injerto de tejido conjuntivo combinado con DME, aunque de forma limitada24. Otro informe que evaluó el uso combinado de CAC con DME, realizado a nivel histológico, mostró la formación de cemento nuevo, fibras de ligamento periodontal organizadas e islas de hueso cercanas a la superficie radicular tratada13.
Pilloni25 notificó mejoras significativas en un grupo con recesión gingival tratada con DME y CAC, en comparación con un grupo tratado con el CAC de forma aislada tras un periodo de evaluación de 18 meses. Por el contrario, Högelwald y cols.26 compararon el CAC con el CAC más DME y no lograron obtener diferencias significativas respecto al éxito del recubrimiento radicular entre ambas modalidades terapéuticas tras un periodo de 12 meses.
El objetivo de este estudio fue evaluar la eficacia clínica de un CAC utilizado en combinación con una FRP y compararla con el CAC combinado con DME en el tratamiento de la recesión gingival.
Materiales y métodos
Los pacientes que desearon participar en el estudio firmaron el consentimiento informado autorizado por el Comité de Ética de la Universidad de Belgrado. En el estudio se incluyeron 20 pacientes no fumadores (8 hombres y 12 mujeres) de edades comprendidas entre los 21 y los 48 años que presentaban zonas de recesión gingival bilateral similar de clase Miller I o II2 en el maxilar superior y que fueron tratados en el Departamento de Periodoncia de la Facultad de Odontología. Si la zona de tratamiento presentaba dos o más piezas adyacentes con recesión solamente, se incluyó en el estudio el diente con el mayor grado de recesión gingival, a pesar de que todos los dientes se trataron durante la misma intervención quirúrgica. Otros criterios de inclusión fueron: ausencia de caries o de restauraciones orales, antecedentes de tratamiento quirúrgico periodontal previo en la zona y ausencia de signos radiográficos de infección periapical de los dientes a tratar o de los dientes adyacentes. Las zonas de tratamiento que presentaron uno o más dientes con un índice gingival mayor de 1 tras el tratamiento inicial fueron excluidas del estudio. Los pacientes con contraindicaciones sistémicas frente a la cirugía periodontal, en tratamiento con fármacos que causan hiperplasia gingival y/o anti-coagulantes también fueron excluidos del estudio
El estudio utilizó un diseño de boca partida en el que dos dientes con recesión gingival susceptible de recubrimiento radicular fueron asignados aleatoriamente a uno de los dos grupos de tratamiento: un CAC combinado con DME (grupo DME) o un CAC combinado con FRP (grupo FRP). La distribución aleatoria se realizó mediante el lanzamiento de una moneda. Ambas intervenciones terapéuticas fueron realizadas por el mismo cirujano. Antes de la cirugía, en ambos grupos de tratamiento se realizó un tratamiento periodontal para la retirada de los cálculos y la eliminación de las manchas.
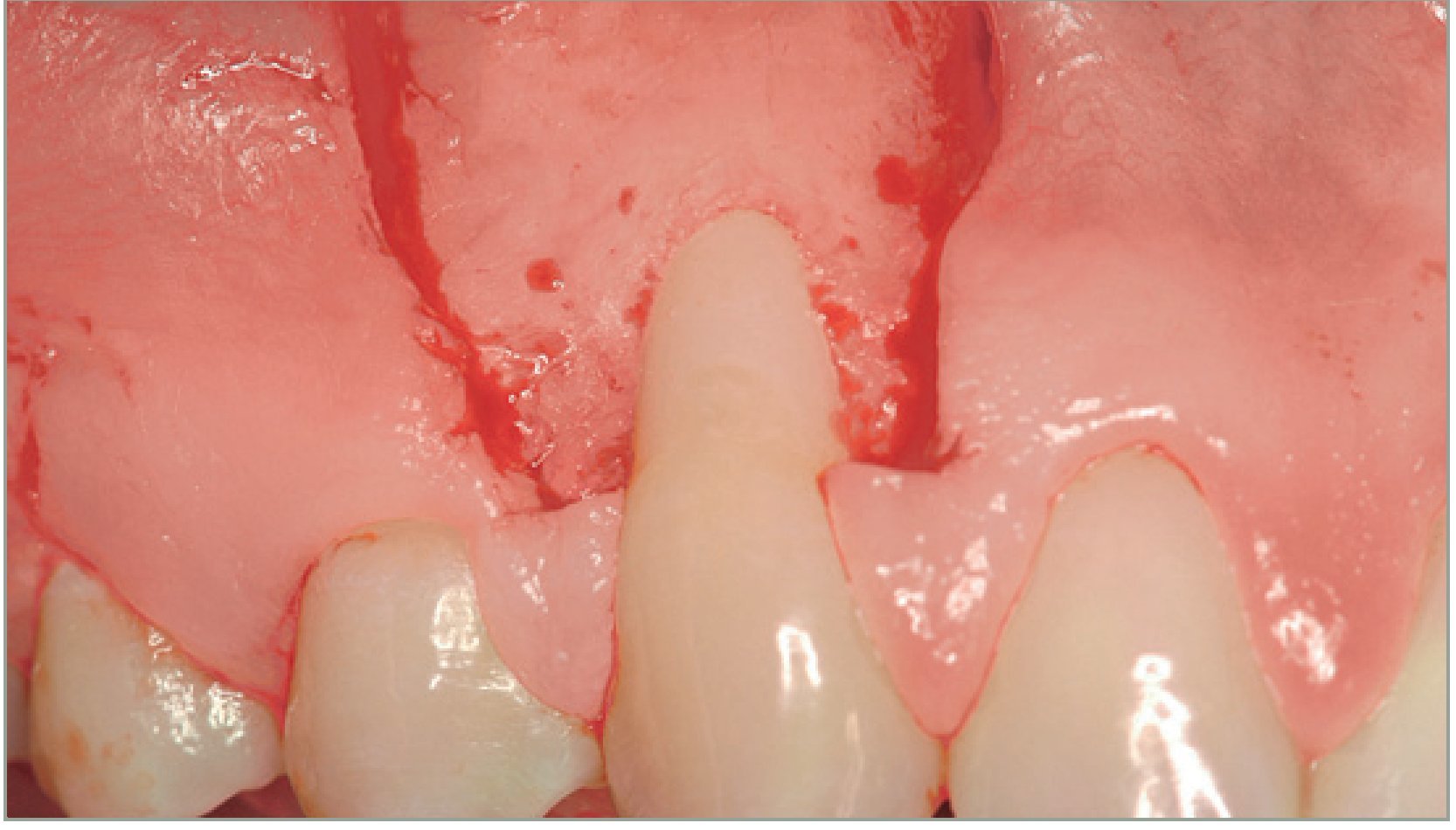
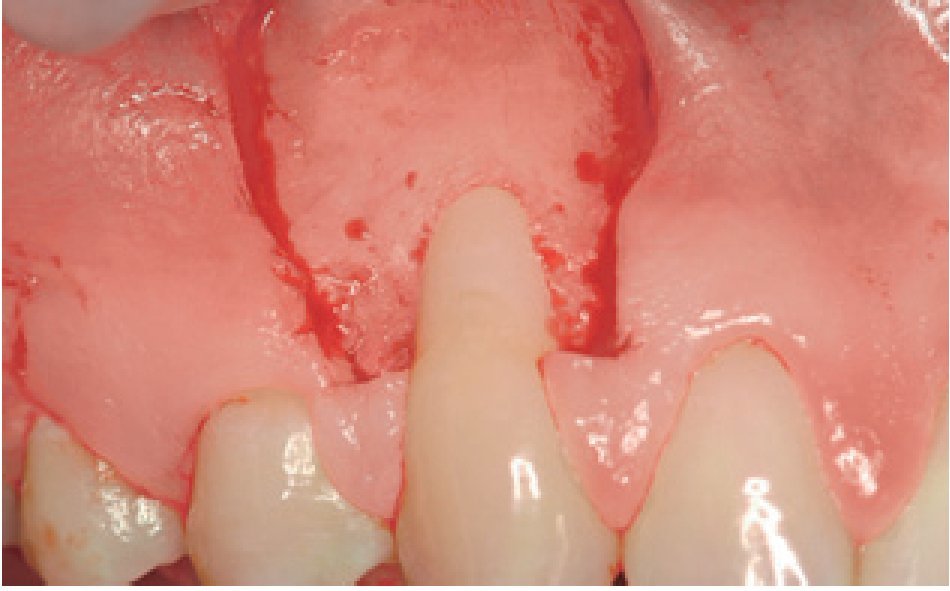
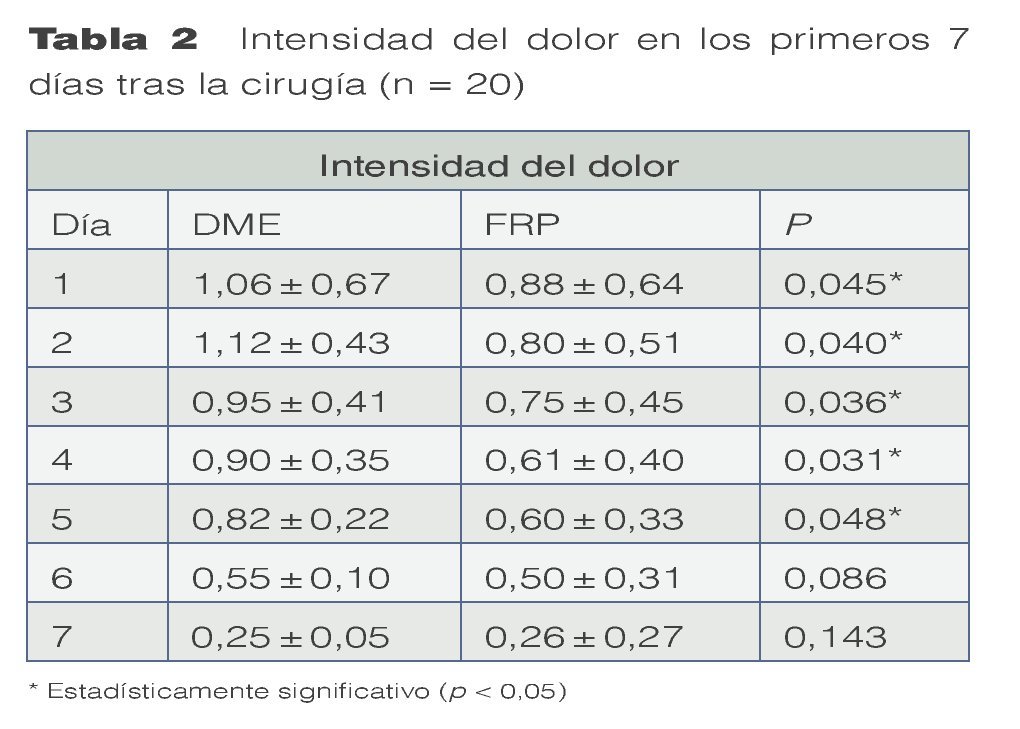
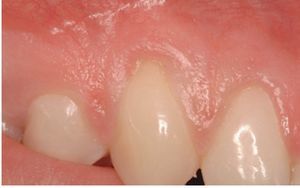
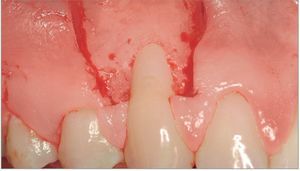
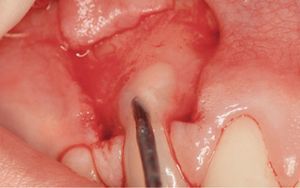
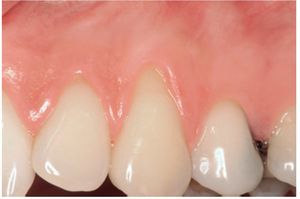
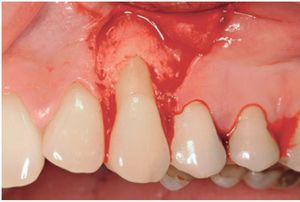
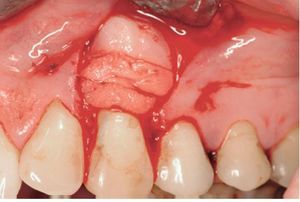
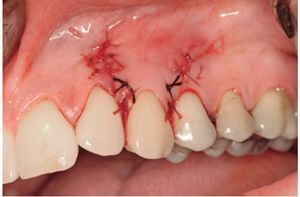
El grupo DME se trató con un colgajo avanzado coronalmente en combinación con un derivado de la matriz del esmalte (Emdogain®, Straumann, Bassel, Suiza). Tras inyectar anestésico local, se realizó el desbridamiento de la raíz con ultrasonidos y curetas manuales (figura 1). Se realizó una incisión intrasulcular con una hoja de bisturí del número 15 C en el aspecto vestibular del diente o dientes tratados. Se realizaron incisiones horizontales a nivel de la unión amelocementaria (UAC) interproximal de la papila adyacente al diente o dientes tratados. Estas incisiones horizontales fueron amplias para no afectar al borde gingival de los dientes adyacentes. Se realizaron dos incisiones oblicuas de descarga en los extremos mesial y distal de la incisión horizontal, y se prolongaron más allá de la unión mucogingival. Se levantó un colgajo de grosor total para exponer como mínimo 3 mm del hueso marginal apical a la zona de la dehiscencia (figura 2). Se realizó una incisión horizontal de descarga en el periostio de la base del colgajo para permitir el desplazamiento coronal del colgajo sin tensiones. La superficie radicular se acondicionó con un gel de EDTA (ácido etilendiamintetraacético) al 24% durante 2 minutos, se aclaró con abundante agua, se secó con una gasa de 2 x 2 pulgadas y se trató con DME de la forma recomendada por el fabricante (figura 3). El CAC se fijó coronalmente a la UAC y se suturó a la papila con suturas del 4-0 (figura 4). Las incisiones de descarga oblicuas se cerraron con puntos sueltos.
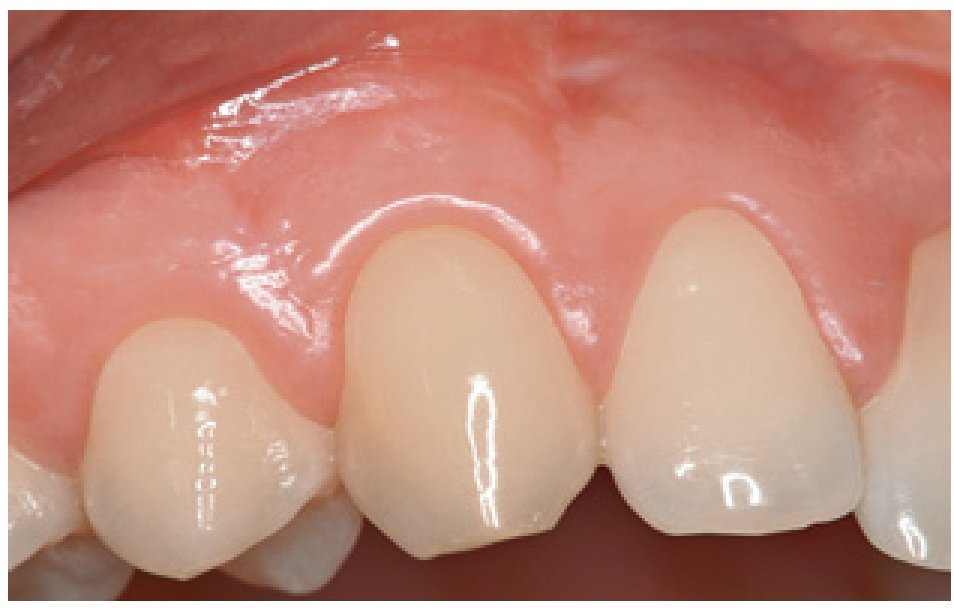
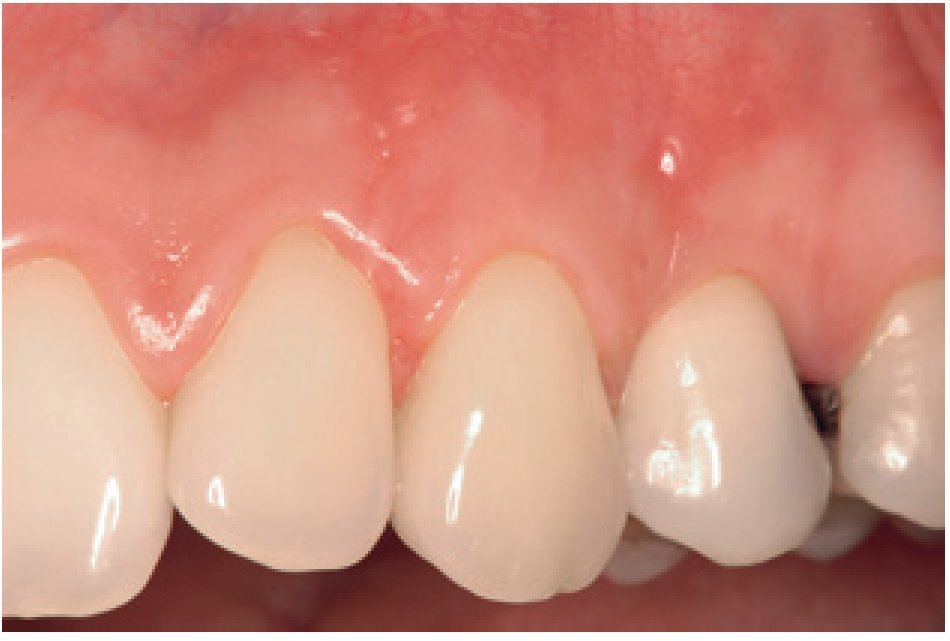
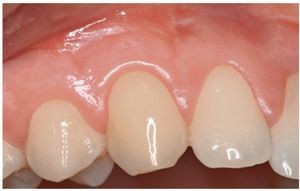
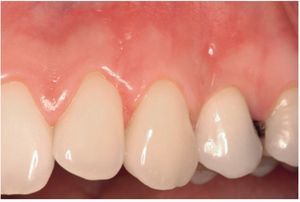
Figura 1 Grupo de tratamiento con derivado de la matriz del esmalte. Imagen preoperatoria mostrando la recesión gingival (clase de Miller I) en el diente 13.
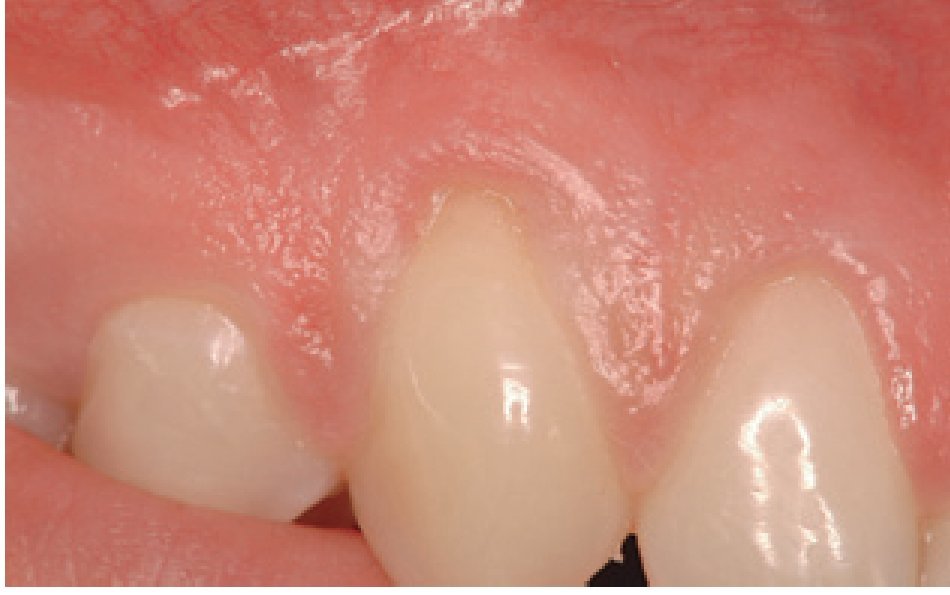
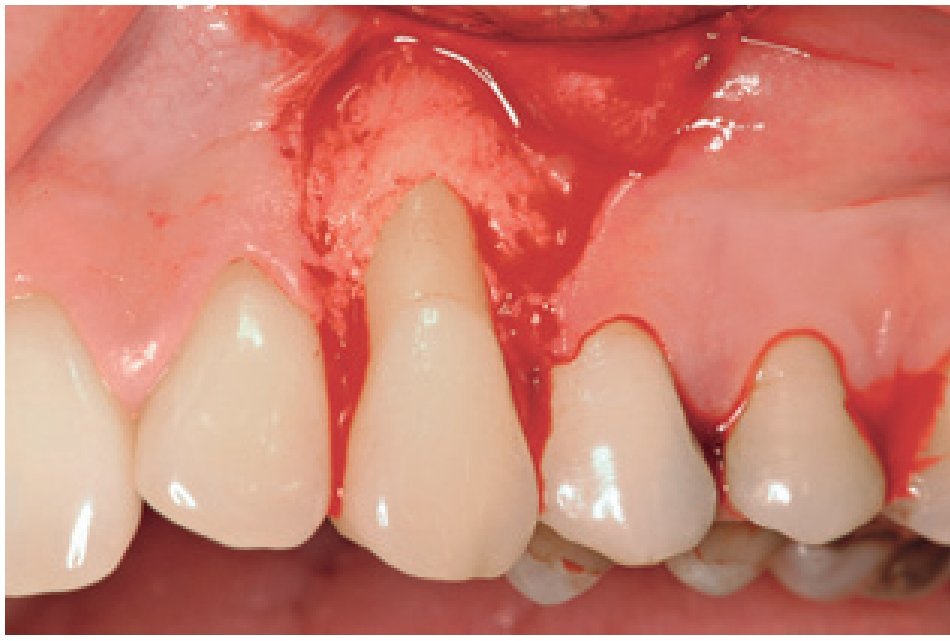
Figura 2 Grupo de tratamiento con derivado de la matriz del esmalte (diente 13). Elevación de un colgajo vestibular tras la preparación de la raíz.
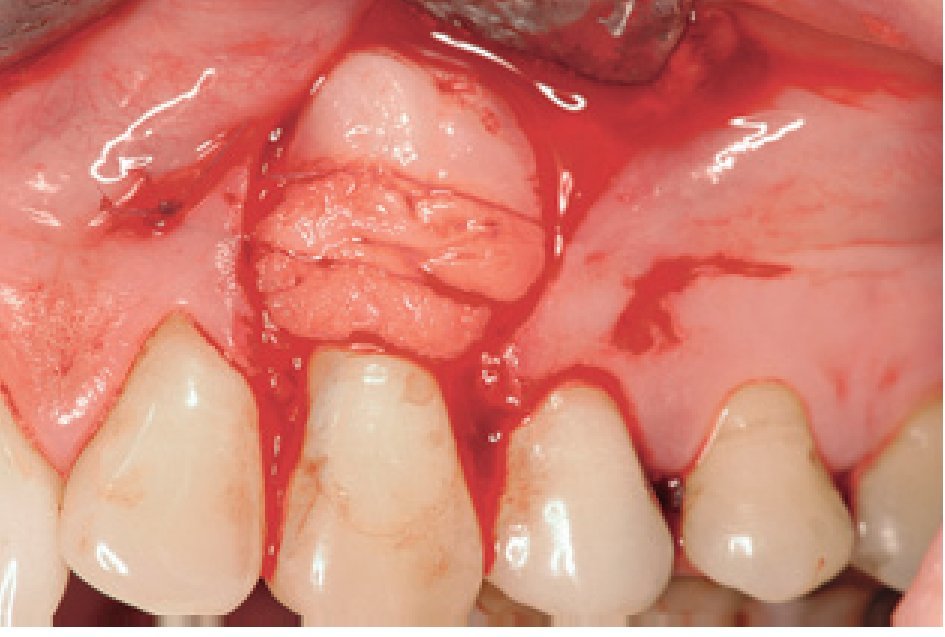
Figura 3 Grupo de tratamiento con derivado de la matriz del esmalte (DME) (diente 13). Aplicación del DME en la superficie radicular.
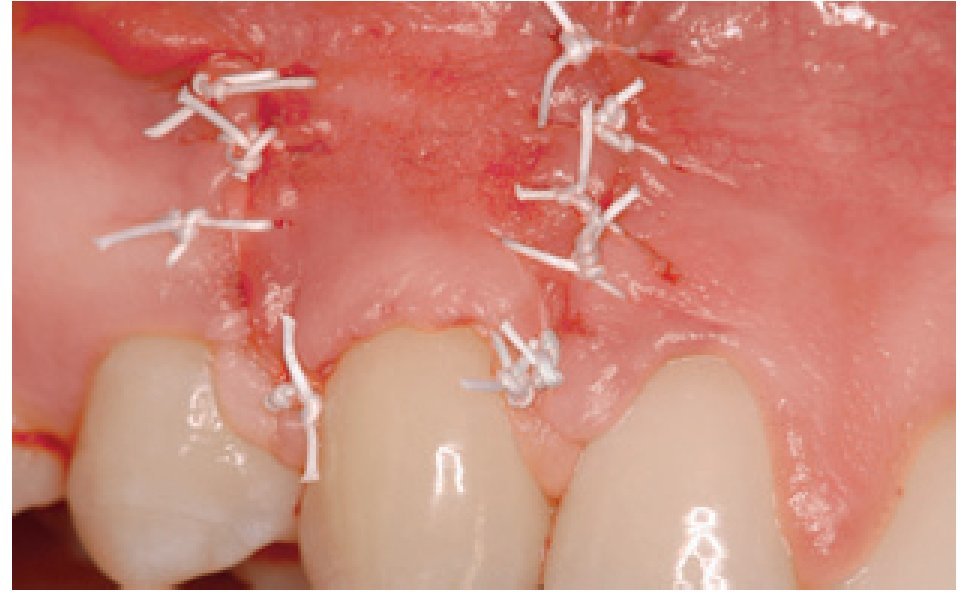
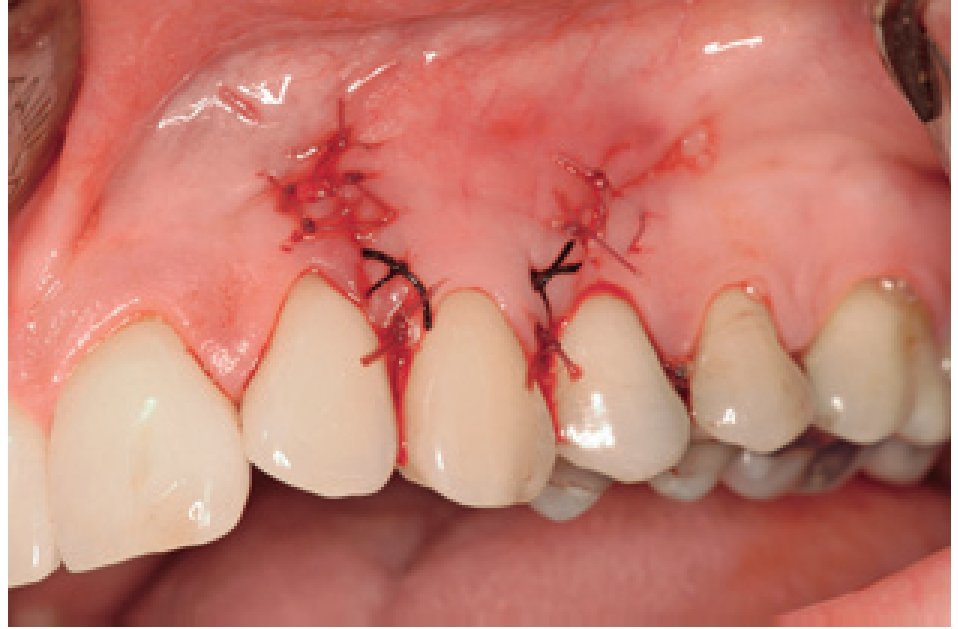
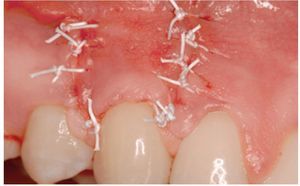
Figura 4 Grupo de tratamiento con derivado de la matriz del esmalte (diente 13). Avance coronal del colgajo y sutura con politetrafluoroetileno expandido de 4-0.
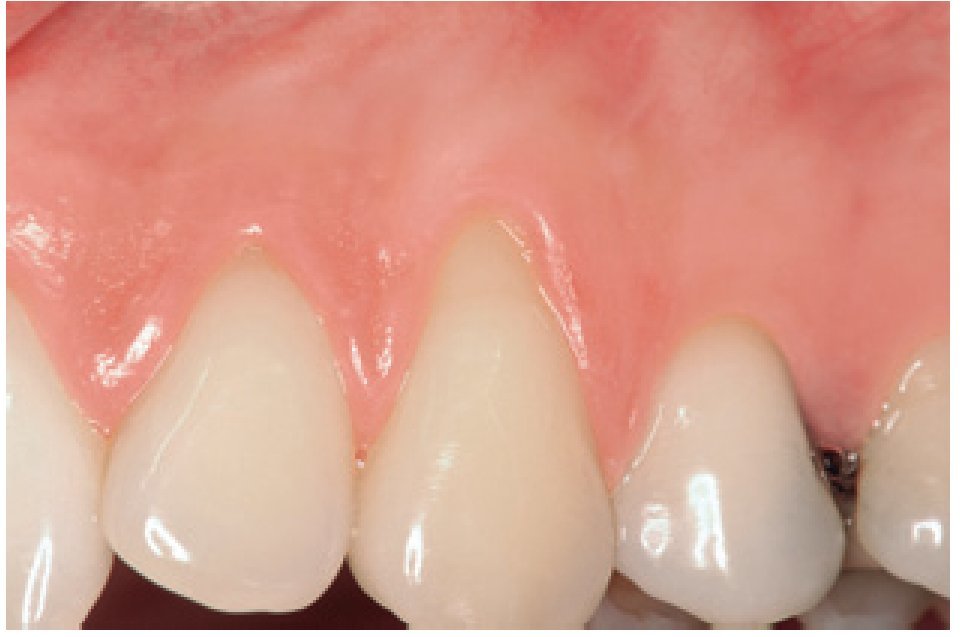
Figura 5 Grupo de tratamiento con derivado de la matriz del esmalte (diente 13). Imagen transcurridos 12 meses tras la cirugía que muestra el recubrimiento completo de la raíz.
Protocolo FRP
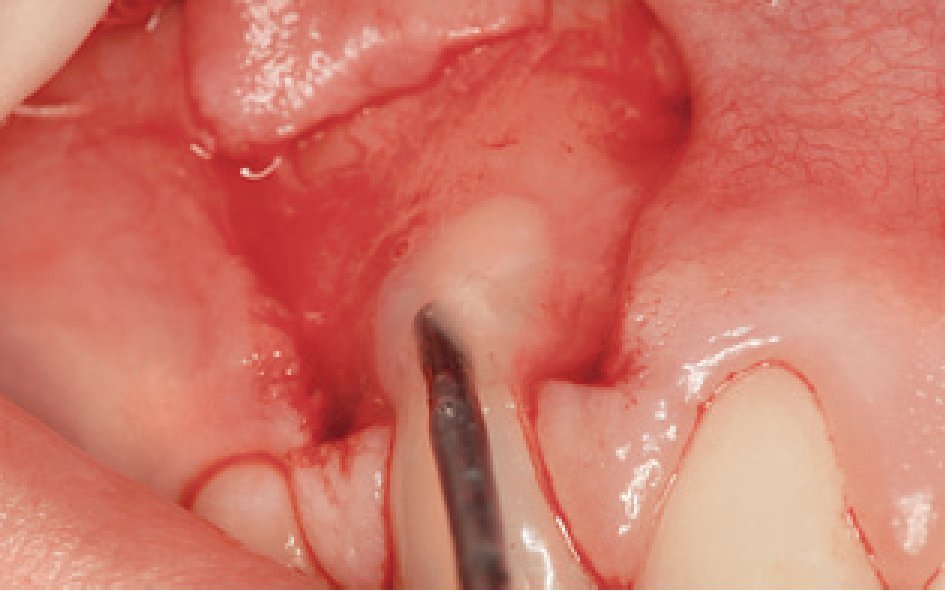
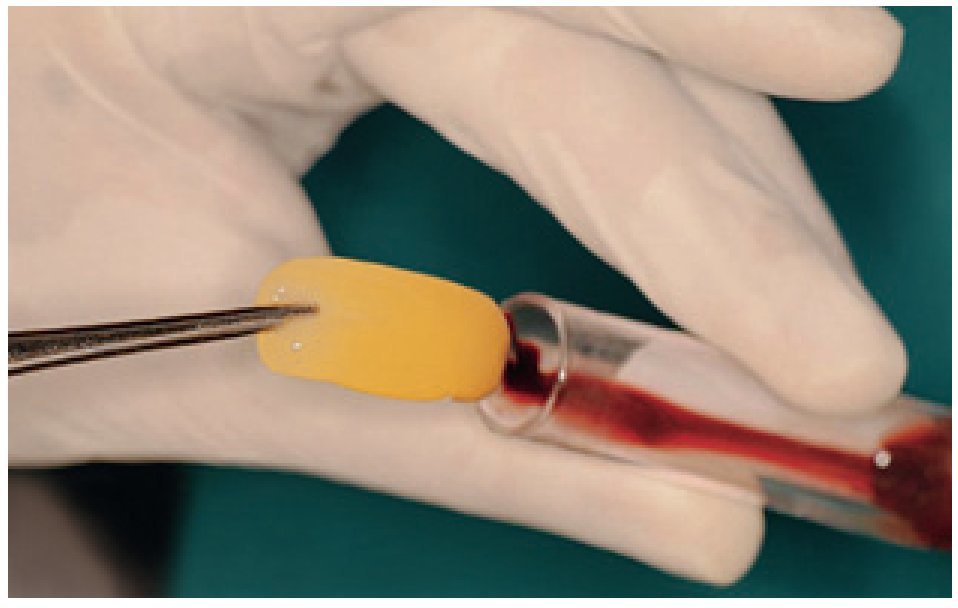
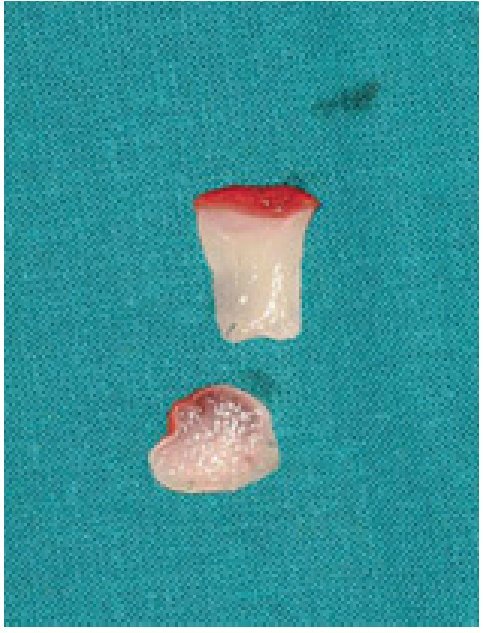
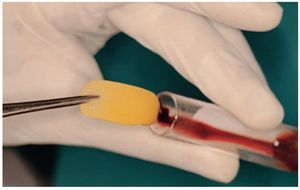
Se tomó una muestra de sangre sin anti-coagulante en un tubo de 10 ml y se centrifugó inmediatamente a 3.000 rpm (aproximadamente 400 g) durante 10 minutos. El procesado de la sangre con una centrífuga permite que el coágulo de fibrina estructurado quede en medio del tubo, justo entre los glóbulos rojos del fondo y el plasma acelular en la superficie (figura 6). Tras extraer la FRP se obtienen fácilmente membranas de fibrina autóloga resistentes retirando el suero del coágulo (figura 7).
Figura 6 Preparación de la fibrina rica en plaquetas (FRP). Retirada del coágulo de FRP.
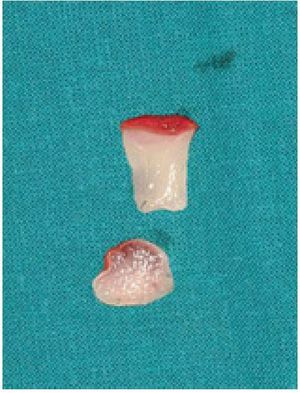
Figura 7 Membrana autóloga de fibrina rica en plaquetas obtenida retirando el suero del coágulo.
El grupo FRP se trató con algunas modificaciones de la técnica descrita por Langer y Langer7. Tras administrar anestesia local, se rasparon y alisaron las superficies radiculares de la zona situada entre el fondo del surco y la UAC mediante instrumentos manuales y ultrasónicos (figura 8). Se realizó una incisión inicial intrasulcular en la zona de la recesión del diente o dientes cuya raíz iba a recubrirse. Esta incisión se prolongó hasta los ángulos mesial y distal del diente o dientes tratados. Se realizaron dos incisiones oblicuas de descarga en los extremos mesial y distal de la incisión horizontal y se prolongaron más allá de la unión mucogingival. Se levantó un colgajo de espesor total más allá de la unión mucogingival para exponer como mínimo 3 mm de hueso apical en el margen más apical de la dehiscencia ósea (figura 9). El colgajo se levantó aún más mediante una disección nítida, liberándolo del periostio. La membrana FRP se colocó en la posición deseada y se estabilizó con puntos colchoneros horizontales (figura 10). El colgajo se avanzó para cubrir la membrana de FRP y se suturó con puntos de seda del 4-0 (figura 11).
Figura 8 Grupo de tratamiento de fibrina rica en plaquetas. Imagen preoperatoria mostrando la recesión gingival (clase Miller I) en el diente 23.
Figura 9 Grupo de tratamiento de fibrina rica en plaquetas (diente 23). Elevación de un colgajo vestibular tras la preparación radicular.
Figura 10 Grupo de tratamiento de fibrina rica en plaquetas (FRP) (diente 23). Tras la preparación de la FRP se suturó una membrana FRP en la zona receptora con seda de 4-0.
Figura 11 Colgajo avanzado coronalmente suturado sobre el injerto de tejido conjuntivo.
El protocolo posquirúrgico fue el mismo para las dos intervenciones. Se colocaron apósitos periodontales y se recetaron antibióticos (500 mg de penicilina VK cada 6 horas durante 14 días) y un colutorio de gluconato de clorhexidina (cada 12 horas durante 14 días). También se recetaron analgésicos orales (500 mg de ibuprofeno cada 8 horas si fue necesario).
Los apósitos y los puntos se retiraron a las 2 semanas de la cirugía. La herida quirúrgica se lavó cuidadosamente con gluconato de clorhexidina al 0,12% con una torunda de algodón. Los pacientes iniciaron la higiene oral mecánica, que consistió en el cepillado y la limpieza con hilo dental o el cepillado interproximal al comienzo de la tercera semana del postoperatorio. Los pacientes fueron examinados semanalmente hasta 1 mes después de la cirugía y posteriormente a los 12 meses (figuras 5 y 12). Los cuidados postoperatorios incluyeron un refuerzo de la higiene oral y la eliminación de la placa por medios mecánicos en aquellos casos en que fue necesario hacerlo.
Figura 12 Grupo de tratamiento de fibrina rica en plaquetas (diente 23). Imagen a los 12 meses de la intervención que muestra el recubrimiento radicular completo.
Las variables medidas al inicio y a los 12 meses en ambos grupos fueron: recesión gingival (RG), anchura apicocoronal del tejido queratinizado (ATQ) y profundidad de la bolsa (PS). La recesión gingival (RG) se definió como la distancia entre la UAC y el borde gingival en el aspecto mediovestibular del diente. La ATQ fue la distancia entre el borde gingival y la unión mucogingival. La PS fue la distancia entre el borde gingival y el fondo de la bolsa. Para todas las mediciones se utilizó una sonda periodontal de la Universidad de Carolina del Norte calibrada en incrementos de 1 mm. Los valores obtenidos se redondearon a los 0,5 mm más cercanos. Un examinador cualificado, que desconocía la modalidad terapéutica empleada, obtuvo los resultados al inicio y a los 12 meses de la intervención.
La evaluación clínica de la cicatrización se estimó mediante el registro del índice de cicatrización (IC). Los registros del IC se realizaron durante la primera y segunda semanas tras la intervención. El índice de cicatrización27 puntúa la cicatrización sobre la base de enrojecimiento, presencia de tejido de granulación, hemorragia y supuración y epitelización. Se otorga una puntuación de 1 a 5; el 1 se asocia con una cicatrización muy mala y el 5 excelente.
El dolor postoperatorio global de los pacientes se evaluó durante los 7 primeros días usando una escala horizontal, con el primer marcador de la izquierda indicando la ausencia de dolor (0), el marcador medio indicando dolor (1) y el marcador de la derecha indicando dolor severo (2). Se aplicó el test de Wilcoxon para comparar la intensidad del dolor durante el periodo postoperatorio. Se utilizó un nivel de significancia de 0,05 en todas las comparaciones estadísticas.
El tratamiento postoperatorio de un lado de la boca no influyó en el otro lado, porque las intervenciones quirúrgicas no se realizaron al mismo tiempo y transcurrieron un mínimo de 3 semanas entre ambas intervenciones. El procedimiento para obtener la sangre no se tuvo en cuenta en la evaluación del nivel de molestias del paciente asociado a las diferentes intervenciones quirúrgicas.Se utilizó el análisis de variabilidad de una vía (ANOVA) para comparar las mediciones clínicas pre y postoperatorias en el mismo grupo. Se utilizó el test t de Student para comparar las mediciones entre los dos grupos de tratamiento. El porcentaje de recubrimiento radicular se calculó utilizando la siguiente fórmula:
[(RG) al inicio - RG a los 12 meses) / RG al inicio] × 100
Los valores P iguales o menores de 0,05 se consideraron estadísticamente significativos.
Resultados
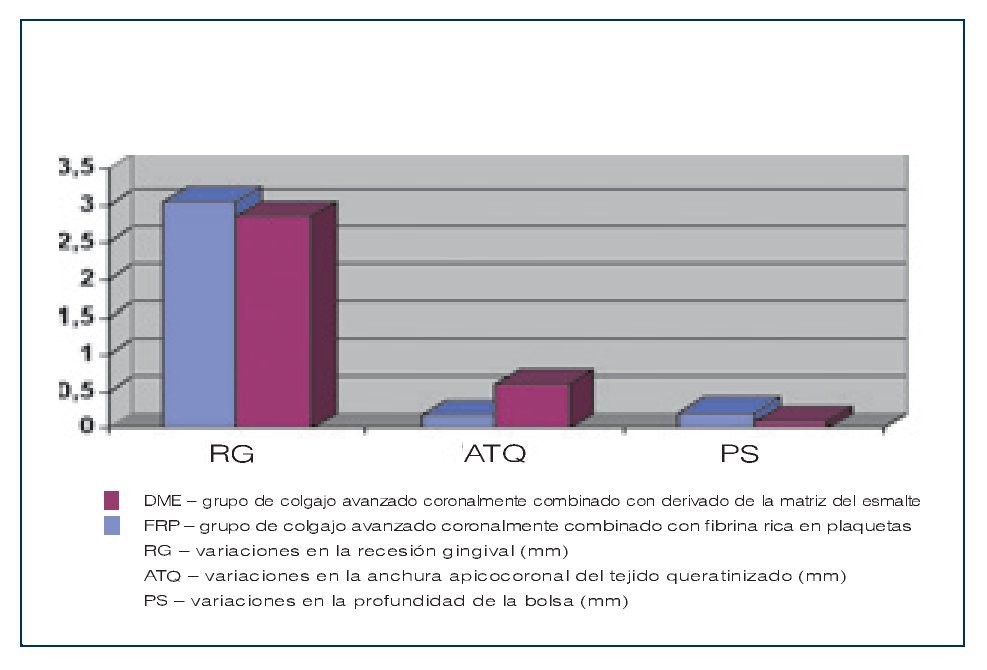
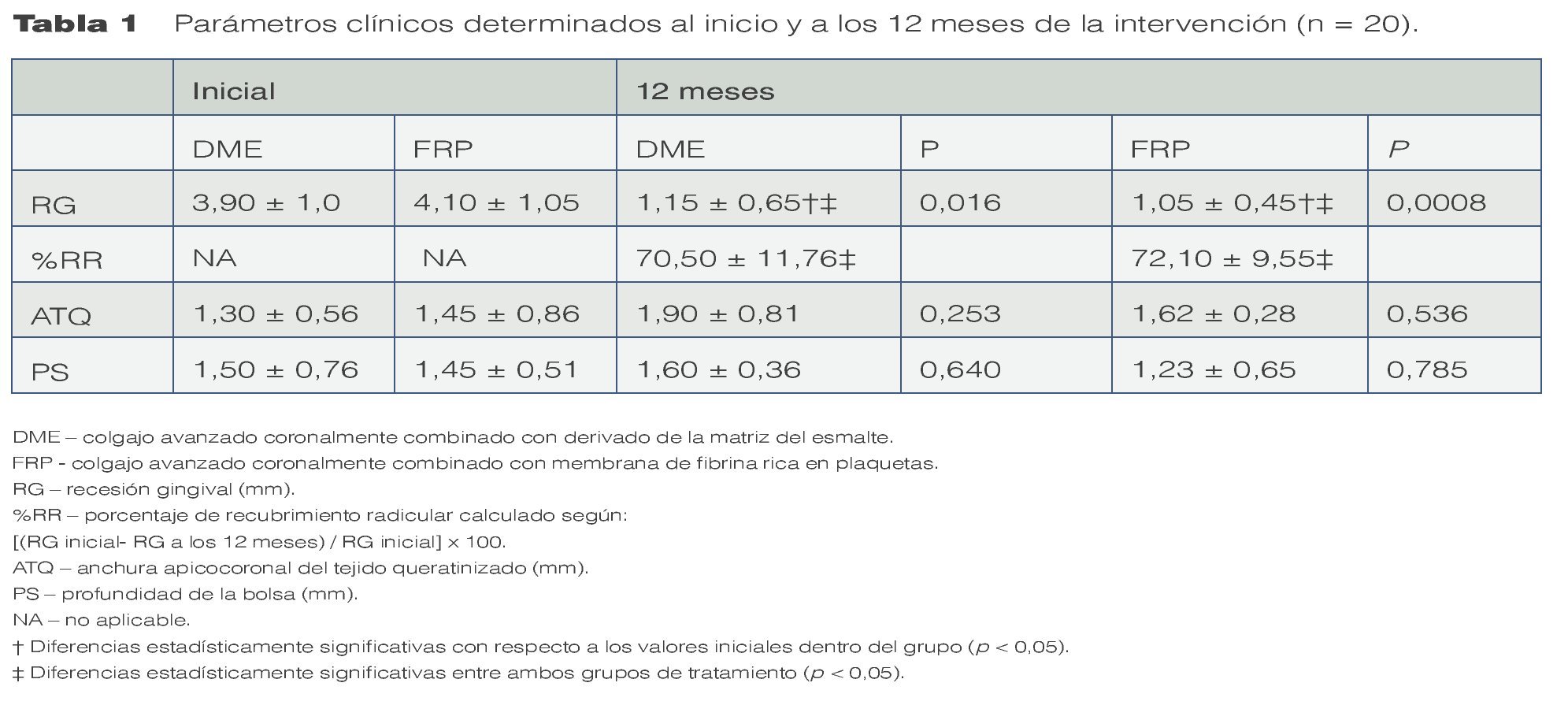
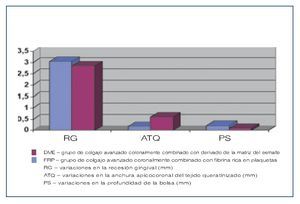
Los resultados de las mediciones clínicas pre y postoperatorias se resumen en la tabla 1. No se observaron diferencias preoperatorias significativas en cuanto a la RG, ATQ o PS entre ambos grupos. La RG se redujo de 4,10 ± 1,05 mm a 1,05 ± 0,45 mm en el grupo FRP y de 3,9 ± 1,0 mm a 1,15 ± 0,65 mm en el grupo DME. Los cambios en la RG en cada grupo (desde el inicio) y entre grupos fueron estadísticamente significativos. La reducción promedio de la RG fue de 3,05 ± 0,76 mm en el grupo FRP y de 2,75 ± 0,61 mm en el grupo DME, y esta diferencia no fue estadísticamente significativa (figura 13). El promedio del recubrimiento radicular fue del 70,5 ± 11,76% en el grupo DME y del 72,1 ± 9,55% en el grupo FRP. El recubrimiento completo de la raíz en el grupo FRP fue del 65% (13 de 20 recesiones) y del 60% en el grupo DME (12 de 20 recesiones).
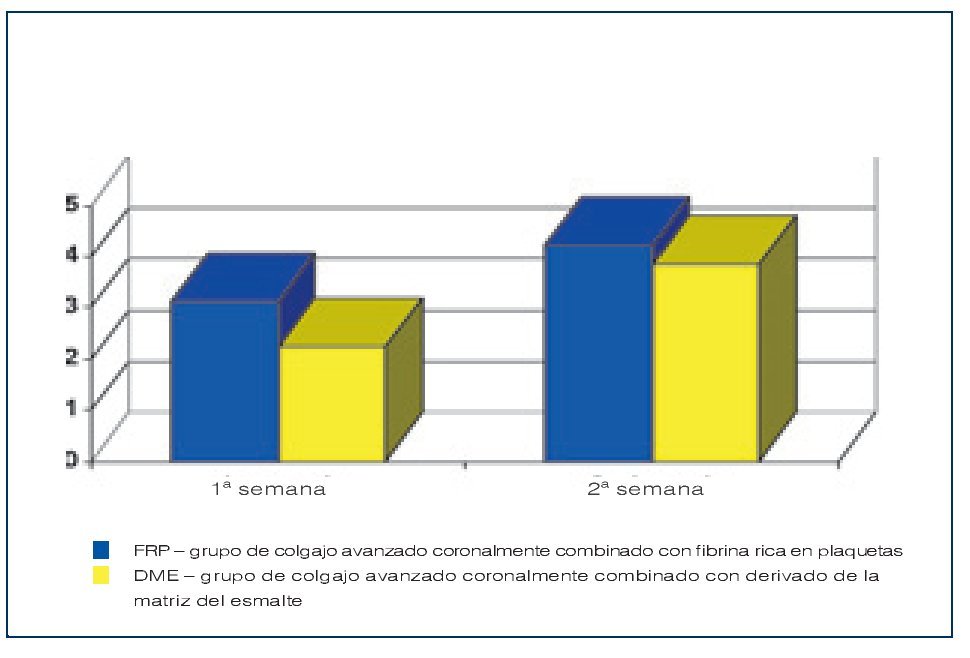
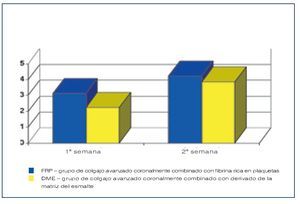
En el grupo DME, la ATQ aumentó de 1,30 ± 0,56 mm al inicio hasta 1,90 ± 0,81 mm a los 12 meses. Las zonas tratadas con FRP presentaron un aumento de la ATQ de 1,45 ± 0,86 mm al inicio hasta 1,62 ± 0,28 mm a los 12 meses. Las diferencias pre y postoperatorias en los grupos no fueron estadísticamente significativas. El aumento promedio en los 12 meses de la ATQ observado en el grupo DME fue de 0,60 ± 0,41 mm, y en el grupo FRP fue de 0,17 ± 0,28 mm (figura 13). La diferencia entre ambos grupos fue estadísticamente significativa, a favor del grupo DME. Las mediciones de la PS no fueron significativamente diferentes entre los valores iniciales y a los 12 meses en los grupos de tratamiento ni tampoco las diferencias postoperatorias entre ambos grupos.Los resultados del IC obtenidos en el grupo FRP tras 1 semana de la cirugía fueron superiores de forma estadísticamente significativa en relación a los resultados registrados en el grupo DME (p < 0,05) (figura 14). Los registros del IC obtenidos en el grupo FRP y el grupo DME dos semanas después de la cirugía mostraron un alto nivel de equivalencia (4,51 ± 0,21 y 4,29 ± 0,36; p > 0,05).
Figura 13 Variaciones promedio (mm) registradas en los grupos de tratamiento tras 12 meses.
Figura 14 Resultados del índice de cicatrización (IC).
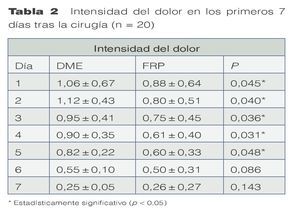
Con respecto al periodo postoperatorio, tres pacientes del grupo DME experimentaron dolor severo en comparación con uno del grupo FRP. Los 20 pacientes del grupo DME refirieron grandes molestias. La intensidad del dolor fue diferente de forma estadísticamente significativa entre los grupos durante los 5 primeros días a favor del grupo FRP (tabla 2).
Discusión
Este estudio comparó la eficacia de dos intervenciones de cirugía periodontal para lograr el recubrimiento de las raíces expuestas a causa de una recesión gingival localizada. El promedio del recubrimiento radicular logrado con el CAC combinado con el DME en este estudio fue del 70,50% a los 12 meses de la intervención. Estos resultados son muy similares a los obtenidos por Nemcovsky28, en los que el recubrimiento radicular a los 12 meses fue del 71,70%, y por Modica y cols., que obtuvieron un recubrimiento del 70,50%29. Es importante mencionar que otros estudios han informado de porcentajes de éxito más elevados en el recubrimiento radicular con el CAC combinado con DME. Pilloni y cols.25 informaron de un porcentaje de éxito promedio del 93,80% en el tratamiento de la recesión gingival tras 18 meses. El motivo de esta discrepancia entre los resultados del estudio aquí descrito y el estudio de Pilloni puede tener relación con las variaciones en los parámetros no medidos como el grosor y la tensión del colgajo.
El porcentaje de éxito en el recubrimiento de la raíz obtenido con el CAC combinado con DME en este estudio mostró una reducción significativa de la recesión gingival tratada y un elevado nivel de equivalencia con los resultados registrados con el CAC combinado con la FRP. En el estudio aquí descrito, el registro del recubrimiento radicular promedio del grupo FRP fue del 72,10% tras el periodo de observación de (12 meses). Aroca y cols. presentaron un promedio de recubrimiento radicular del 80,7% tras 6 meses utilizando FRP20. El recubrimiento radicular completo en el grupo FRP fue del 65% (13 de 20 recesiones) y en el grupo DME fue del 60% (12 de 20 recesiones). El único estudio publicado con respecto a la utilización de FRP en el tratamiento de la recesión gingival20 presentó un recubrimiento radicular completo en el grupo FRP de solamente el 52,2%.
Por tanto, no existen indicios coherentes que sugieran que las técnicas quirúrgicas que utilizan FPR sean superiores a las técnicas que utilizan DME en combinación con CAC para lograr el recubrimiento radicular.
Las posibles ventajas podrían estar relacionadas con el notable aumento en la ATQ obtenido con la técnica de DME en oposición al aumento más que modesto del mismo parámetro obtenido con el CAC más la FRP. Se ha identificado que una banda estrecha de encía insertada es un factor predisponente de recesión gingival.
El grupo DME de este estudio presentó un destacado aumento de la ATQ a los 12 meses en comparación con los valores iniciales. Ese aumento fue aproximadamente de 0,6 mm. El grupo FRP mostró un aumento promedio de 0,17 mm de ATQ tras 12 meses. Aroca y cols. no confirmaron ningún aumento de la ATQ en el grupo FRP a los 6 meses. La diferencia observada entre ambos grupos en cuanto al aumento de la anchura del tejido queratinizado a los 12 meses fue estadísticamente significativa a favor del grupo DME.
A partir de esta observación se puede inferir que el DME puede tener un efecto moderado en la inducción de la queratinización del epitelio gingival. Un informe de Högelwald26 ha sugerido un efecto de este tipo con el DME en el epitelio gingival. La capacidad del DME para aumentar la ATQ, no obstante, no es claramente tan significativa desde el punto de vista clínico como la observada con los injertos de tejido conjuntivo.
El estudio aquí descrito no proporcionó datos para evaluar los efectos adicionales del DME sobre el CAC con respecto a las intervenciones de recubrimiento radicular, dado que el grupo tratado con el CAC de forma aislada no formó parte del protocolo de investigación. Sin embargo, un estudio realizado por Del Pizzo y cols.30 reveló que una combinación de DME con CAC no provocó un recubrimiento radicular adicional en comparación con el CAC utilizado de forma aislada. Por otro lado, Pilloni25 reveló mejoras significativas de los resultados en un grupo con recesión gingival tratada con DME y un CAC en comparación con el grupo tratado con un CAC de forma aislada. La ventaja potencial asociada con el DME tiene relación con la naturaleza de la inserción entre el tejido blando y la superficie radicular. Debido a su mecanismo de acción, el DME puede favorecer el desarrollo de una inserción conjuntiva real cuando se avanza coronalmente un colgajo. Los informes histológicos, no obstante, muestran resultados controvertidos respecto a la capacidad del DME para inducir la regeneración periodontal tras las intervenciones de recubrimiento radicular13. Si bien dos estudios mostraron un grado insignificante de regeneración periodontal13,21,22, un informe describió un grado significativo de regeneración periodontal al utilizar DME en las intervenciones de recubrimiento radicular13. Estos estudios histológicos del injerto de tejido conjuntivo humano publicados se realizaron sin cálculo alguno.
El impacto biológico de las proteínas de la matriz del esmalte favorecería la cicatrización del tejido conjuntivo al aumentar la angiogénesis y la biosíntesis de la matriz durante la cicatrización de la herida21.
Los resultados del índice de cicatrización indicaron mejorías destacadas de la cicatrización temprana de la herida (primera semana tras la cirugía) en el grupo tratado con membrana de FRP en comparación con el grupo tratado con DME. Este resultado pudo estar relacionado con la densidad extremadamente elevada de las fibras de fibrina detectada en la membrana de FRP. Una densidad elevada de fibras de fibrina proporciona estabilidad adicional a la herida y favorece la rápida neoangiogénesis16. La mejora del IC lograda en el grupo FRP también podría explicarse por la acción concentrada de los principales factores de crecimiento de la FRP: PDGF, VEGF y TGF. Estos factores de crecimiento favorecerían la cicatrización del tejido conjuntivo aumentando la angiogénesis y la biosíntesis de la matriz durante la cicatrización de la herida31.
Algunos estudios recientes han hecho énfasis en que el grosor del tejido gingival es esencial para lograr un recubrimiento radicular medio o completo y la estabilidad del resultado clínico, y se ha descrito un aumento del grosor tisular tras realizar un ITC32,33. Según la información de que disponen los autores, solamente existe una publicación34 que separa el recubrimiento radicular según el tipo de patrón de cicatrización con respecto al grosor del tejido. Aroca y cols.20 mostraron un destacado incremento en el grosor gingival tras 6 meses en un grupo tratado con FRP. Esto puede ser el resultado de la proliferación de los fibroblastos gingivales y del ligamento periodontal en relación al impacto de los factores de crecimiento concentrados de la FRP. En el estudio aquí descrito, los autores no evaluaron el grosor del tejido gingival en los grupos FRP y DME antes de la cirugía y después del periodo de evaluación. Estudios futuros evaluarán este parámetro como factor predictivo potencial del recubrimiento radicular35. Estos estudios proporcionarán información adicional relacionada con la eficacia del uso de FRP en el tratamiento de la recesión gingival.
Con el objeto de ser más precisos y objetivos, hay que destacar que los resultados aquí descritos, en términos de recubrimiento radicular (porcentajes y completo) y de aumento del tejido queratinizado vestibular, no parecen ser superiores a los publicados recientemente con el CAC utilizado de forma aislada36,37.
Ambas técnicas quirúrgicas evaluadas demostraron ser clínicamente satisfactorias en el tratamiento de la recesión gingival. Las implicaciones clínicas y las pequeñas ventajas del uso de la membrana de FRP como material de injerto tienen relación con la cicatrización tisular avanzada durante la primera semana tras la cirugía y con la disminución de las molestias del paciente durante el periodo de cicatrización inicial. La ventaja de los eventos de cicatrización temprana en relación con el uso de FRP se registró solamente durante la primera semana del postoperatorio, pero aparentemente no tiene un impacto destacado en el resultado clínico al cabo de 1 año. Por otro lado, el uso del DME proporciona un mejor aumento de la ATQ.Sobre la base de los resultados logrados en esta investigación, debe destacarse que este estudio no logró demostrar ninguna ventaja clínica del uso de FRP en comparación con el DME en el recubrimiento de la recesión gingival con un CAC. Asimismo debe mencionarse que el proceso de obtención de sangre asociado a la preparación de la FRP supone una molestia adicional para el paciente.
Una posible tendencia positiva del uso de la FRP debería evaluarse mejor en estudios con un mayor número de individuos. En este estudio no se realizó ninguna evaluación histológica y, por tanto, queda por determinar el efecto de la FRP en la capacidad global de regeneración.
Correspondencia:
Dr Sasha Jankovic
University of Belgrade School of Dentistry, Department of Periodontics,
Dr Subotica #4 St, 11000, Belgrade, Republic of Serbia;
tel: +381641120674;
e-mail:drsashaj@gmail.com