El sistema inmune media numerosas patologías, por lo que es importante conocer su estructura y funcionamiento. Se clasifica en innato y adquirido. El sistema inmune innato brinda una temprana e inespecífica respuesta contra los microorganismos. El sistema inmune adquirido humoral y celular nos brinda una respuesta específica para diferentes moléculas, posee memoria frente a los antígenos y diversidad para reaccionar a una gran variedad de antígenos.
he immune system mediates numerous pathologies functions por functioning it is important to know its structure and functioning. The immune system is classified into innate and adaptive immunity. The innate immunity provides early and non-specific response against microbes. The adaptive humoral and cellular immunity gives specificy for distinct molecules and has memory to enhance response to antigen and diversity to responde to large variety of antigen
Se postula que el sistema inmune existiría porque existe la agresión endógena y exógena (1). Es así que sus principales funciones son la defensa contra microorganismos y la inmunovigilancia contra la emergencia de tumores y de enfermedades autoinmunes y alérgicas.
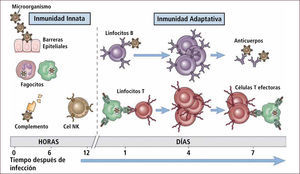
Desde el punto de vista funcional podemos clasificarlo en Sistema Inmune Innato y Adquirido (o específico) (Figura 1). Sin embargo, esta clasificación es sólo didáctica, ya que ambos sistemas funcionan de manera integrada. Esto se evidencia de dos formas:
- 1-
El sistema inmune innato activa el sistema inmune adquirido en respuesta a las infecciones.
- 2-
El sistema inmune adquirido utiliza los mecanismos efectores de la inmunidad innata para eliminar los microorganismos.
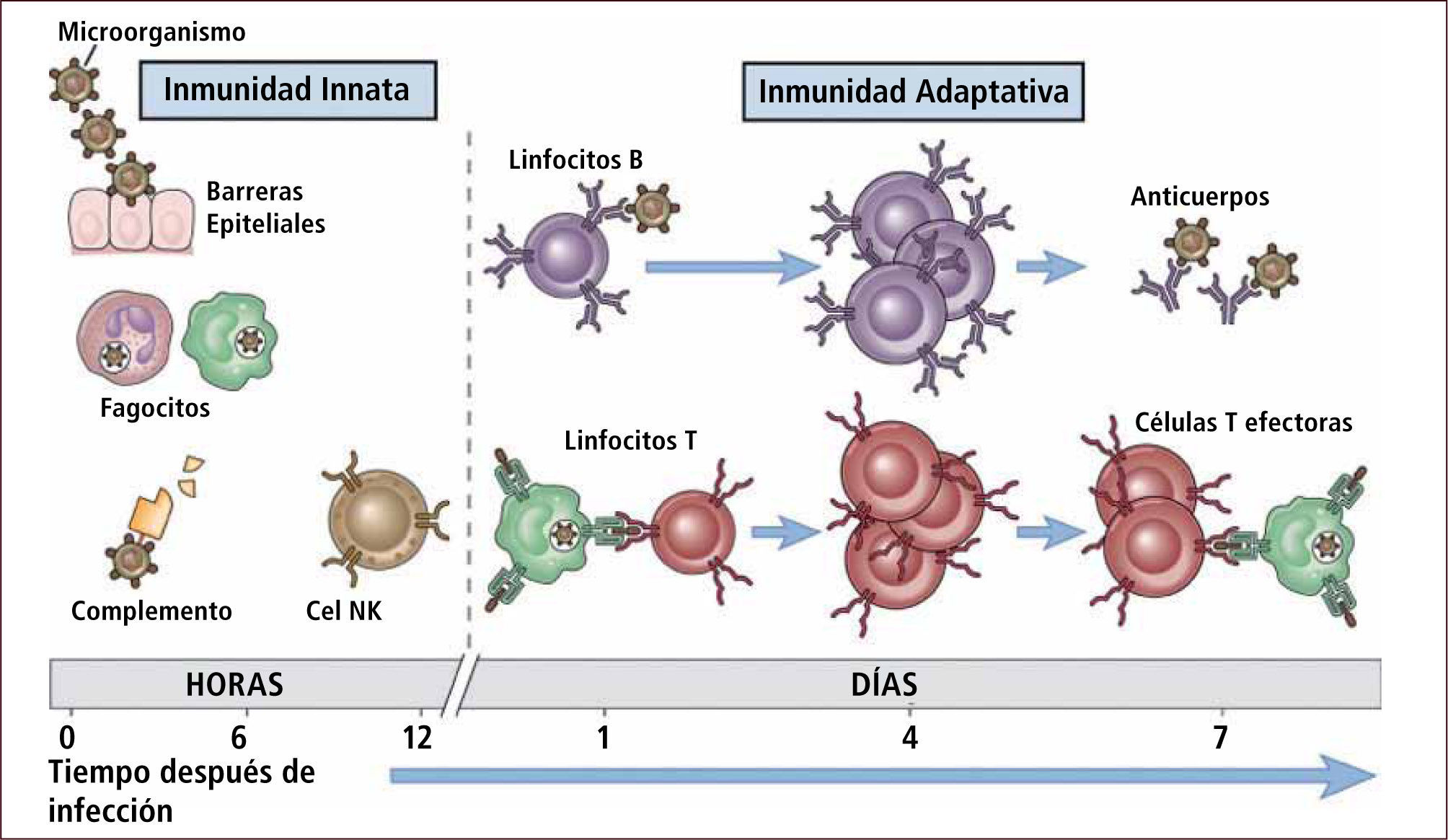
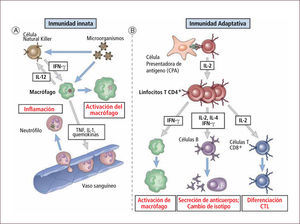
Sistema inmune innato y adaptativo
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
El Sistema Inmune Innato (SII) es la primera línea de defensa del huésped. Posee mecanismos pre-existentes que se activan de manera rápida y que preceden a la Inmunidad Adaptativa en la respuesta defensiva. El SII responde de la misma manera frente a diferentes estímulos infecciosos y posee una especificidad limitada, es decir, distingue estructuras comunes a grupos de microoganismos pudiendo no distinguir diferencias finas entre ellos (2). El SII es el más antiguo y está presente en todos organismos multicelulares, incluso plantas e insectos. Los principales componentes del sistema inmune innato se resumen en la Tabla 1.
Epitelios: impiden el ingreso de patógenos, constituyendo una barrera física (tight junctions, flujo de aires o fluidos) y química (ácidos grasos y defensinas de la piel, enzimas como la lisozima de lágrimas, sudor, saliva, la pepsina del intestino y el pH ácido del estómago).
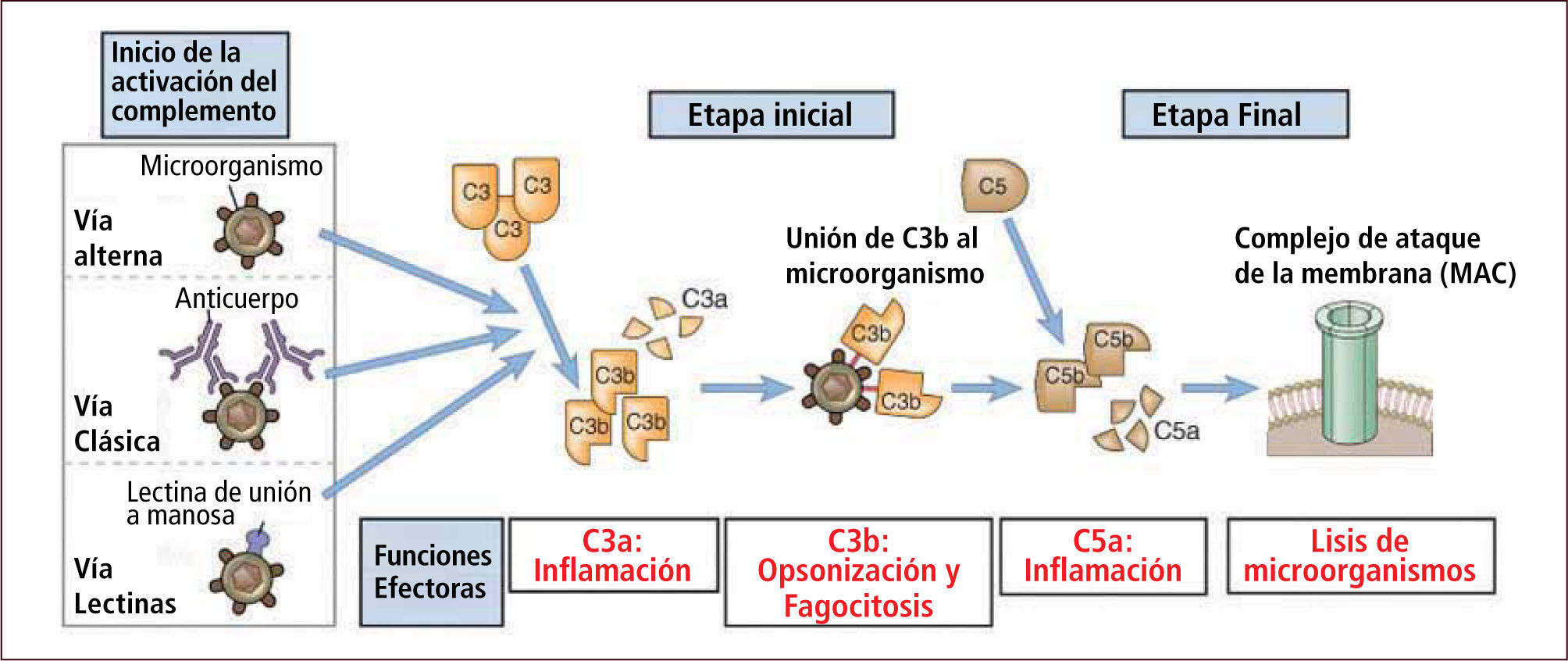
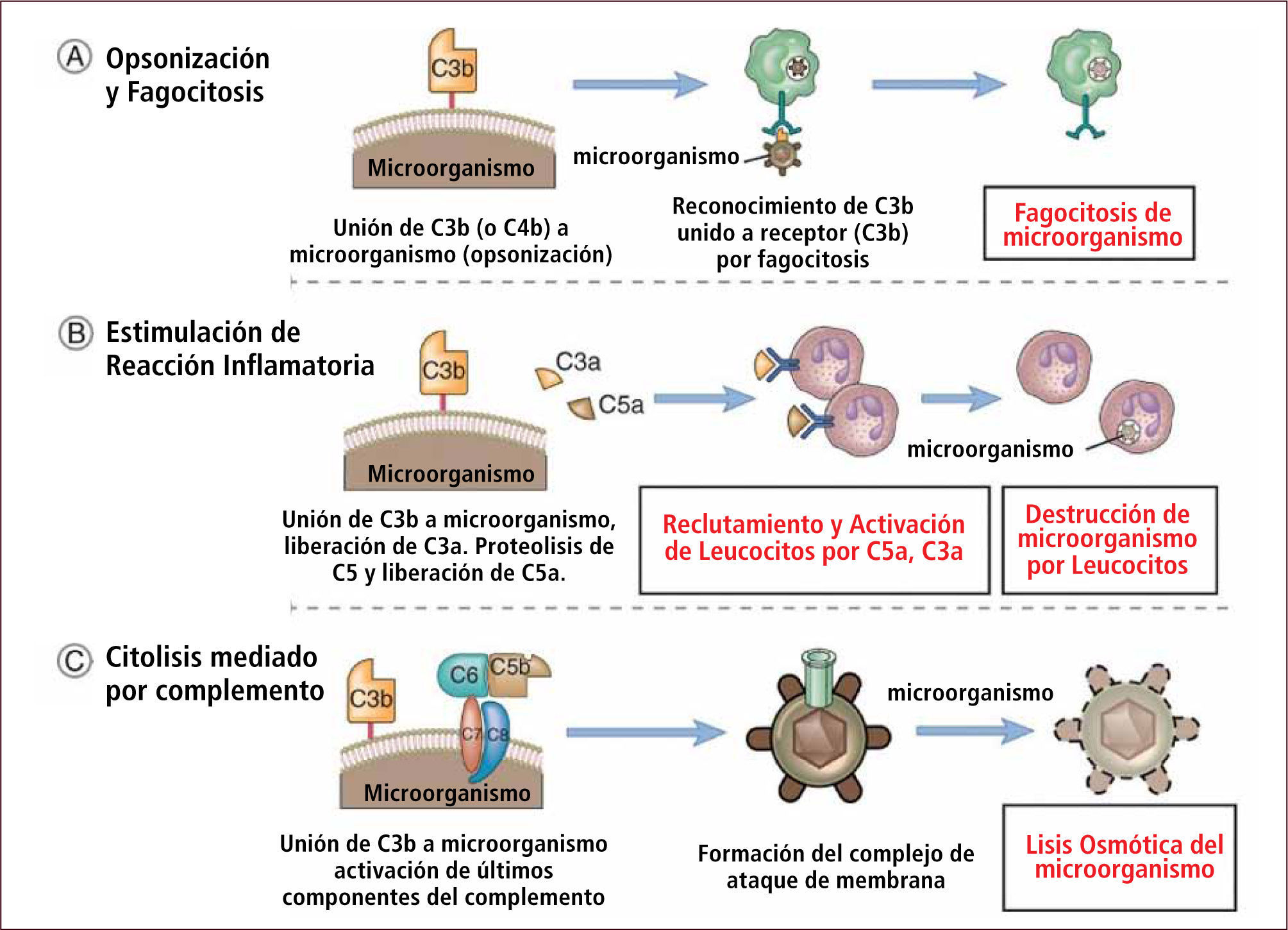
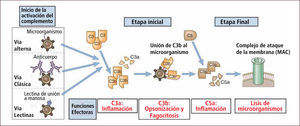
Sistema del Complemento: son proteínas que circulan inactivas en el plasma. Son sintetizadas en hígado y macrófagos. El sistema del complemento es capaz de dirigir la lisis y la opsonización sobre membranas biológicas de agresores y no de las propias debido a un estricto control a cargo de proteínas solubles y de membrana que lo impiden (3). Posee 3 vías de activación: vía clásica, alterna y de las lectinas (Figura 2). Las principales funciones del complemento son (Figura 3):
- -
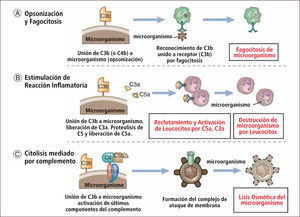
Lisis de microorganismos: mediante la formación del complejo de ataque de membrana (MAC) formado por C5 a C9 que produce canales en la membrana celular generando la lisis osmótica del patógeno.
- -
Opsonización de patógenos: al estar presente C3b y C4b sobre la superficie de las células se facilita la destrucción del patógeno por parte de las células fagocíticas.
- -
Producción de péptidos proinflamatorios: C3a, C4a C5a aumentan la permeabilidad capilar facilitando la llegada de células y potenciando la inflamación.
- -
Solubilización de complejos inmunes: C3b y C4b participan en la remoción de complejos inmunes evitando su depósito en tejidos.
- -
Activación de linfocitos: C3d y C4d se unen a los linficitos B (vía CR2) potenciando la estimulación del linfocitos B al actuar como correceptor.
Vías de activación del complemento
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
Funciones del complemento
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
Polimorfonucleares o Neutrófilos: pertenecen a la línea mieloide y constituyen la primera línea de defensa contra microorganismos. Sus principales funciones son la Fagocitosis y la Lisis de microorganismos precozmente frente a la infección. Posterior al englobamiento y fagocitosis del microorganismo su destrucción se realiza mediante sus gránulos que contienen enzimas presentes en los lisosomas y fagolisosomas.
Células NK (Natural Killer): pertenecen a la línea linfoide, son una subclase de linfocitos que destruyen células infectadas y células que han perdido la expresión de moléculas de histocompatilibidad clase I (HLA I). Producen grandes cantidades de interferón gama (INFγ) que potencian la función fagocítica del macrófago (4).
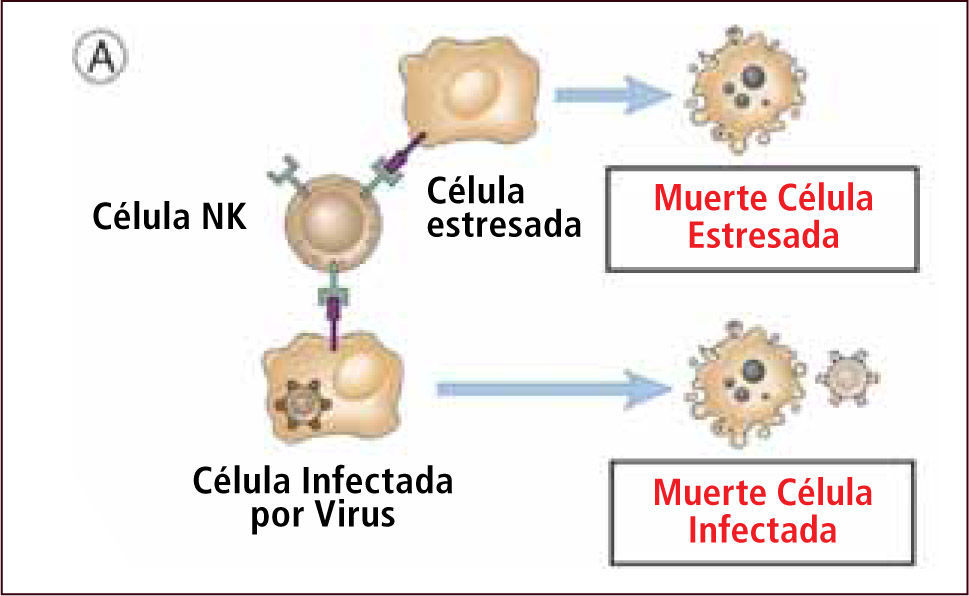
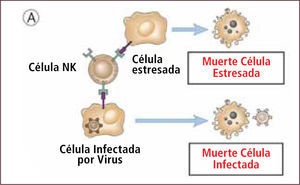
Las células NK controlan inicialmente infecciones virales y otros agentes intracelulares mediante la secreción de perforinas y granzimas (Figura 4). Reconocen y destruyen blancos celulares cubiertos por anticuerpos, mecanismo efector humoral llamado citotoxicidad dependiente de anticuerpos (ADCC). Además las células NK poseen una importante actividad antitumoral.
Control inicial de infección viral por células natural killer (NK)
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e -www.studentconsult.com
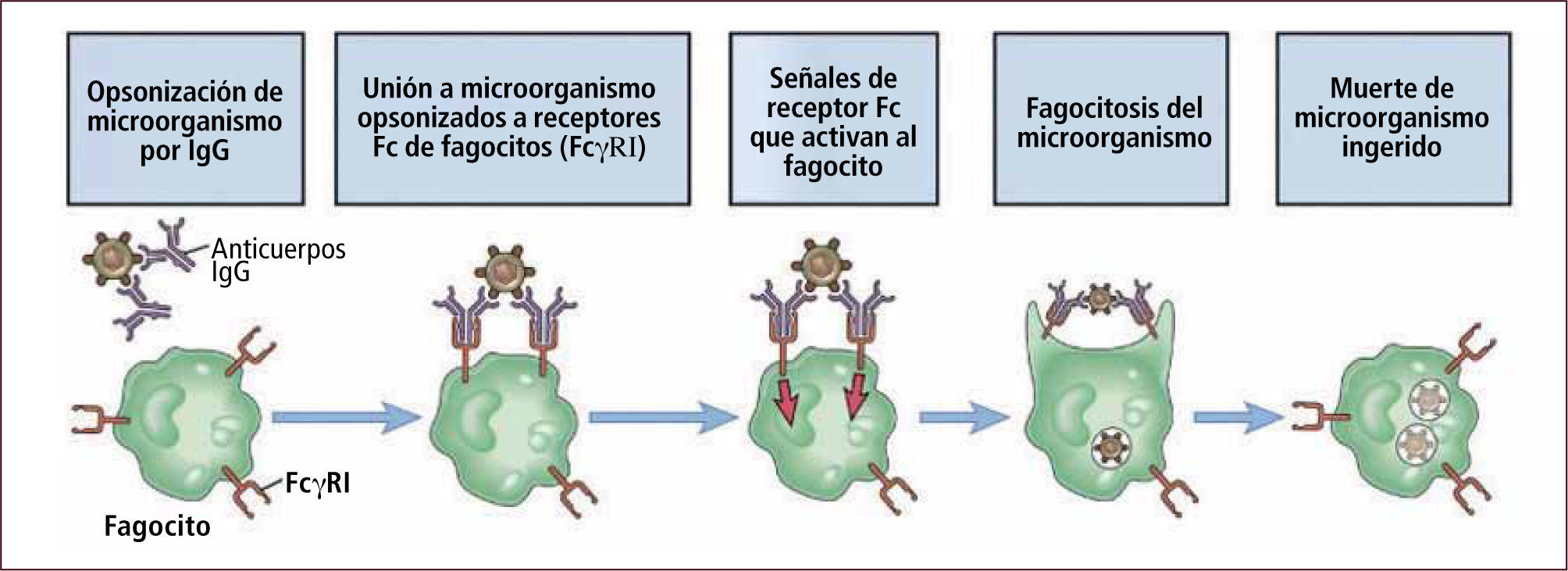
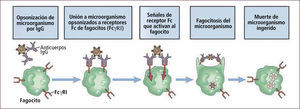
Macrófagos: son células que se encuentran como monocitos circulantes o macrófagos tisulares. Sus principales funciones son: la fagocitosis para luego producir la lisis bacteriana y degradación de antígeno a péptidos (Figura 5). Posteriormente el macrófago realiza la presentación de antígenos la cual se realiza en contexto de moléculas de Histocompatibilidad (MHC) clase I y II. El macrófago además secreta citoquinas que activan al propio macrófago a realizar más eficientemente sus funciones e inducen efectos proinflamatorios. El macrófago constituye una conexión entre la inmunidad innata y adquirida (Tabla 2).
Opsonización y fagocitosis
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
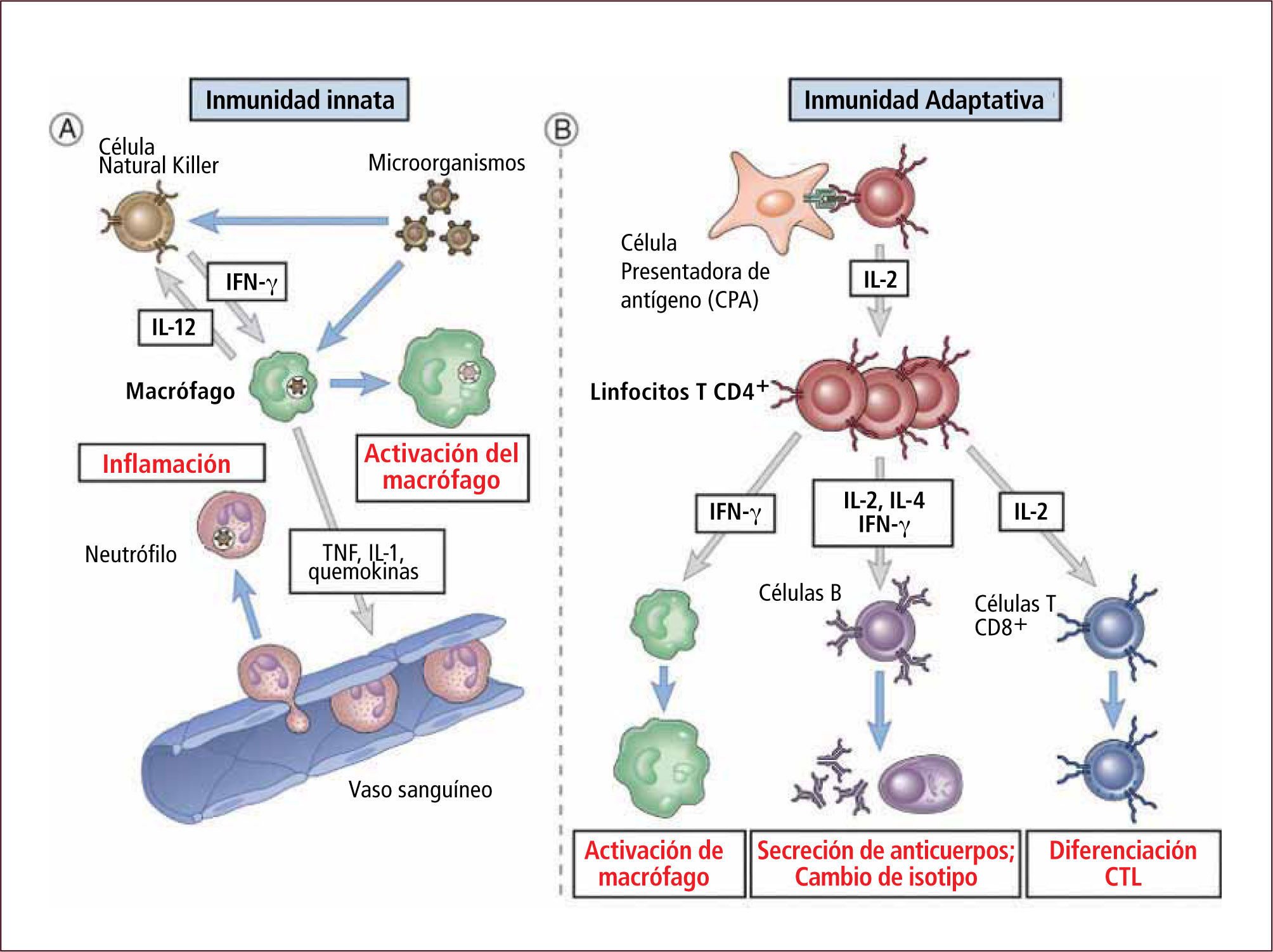
Citoquinas: o interleuquinas (IL) son proteínas secretadas por las células del sistema inmune innato y adquirido en respuesta a microorganismos y otros antígenos. Las citoquinas estimulan el crecimiento y diferenciación de los linfocitos y monocitos hacia células efectoras involucradas en la eliminación eficiente de los microorganismos y tiene un rol fundamental en la inflamación (5). Poseen una acción pleiotrópica (actúa en diferentes tipos celulares) y redundante (diferentes citoquinas inducen el mismo efecto) tanto en el sistema inmune innato y adquirido (Figura 6).
Rol de citoquinas en inmunidad innata y adquirida
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
Las citoquinas pueden estimular el desarrollo de células hematopoyéticas y además algunas poseen efectos inhibitorios. En la práctica clínica algunos antagonistas específicos de ellas son blanco terapéutico de enfermedades inmunes inflamatorias y autoinmunes. Las citoquinas pueden ejercer su acción de manera local o sistémica (Tabla 3).
Fefectos locales y sistémicos de algunas interleuquinas (IL)
| Efectos locales |
|---|
| - activación del endotelio (IL 1, TNF) |
| - quimiotaxis (IL 8) |
| - producción de anticuerpos (IL 6) |
| - activación de macrófagos (INF, IL12) |
| - activación de cel NK (IL 12) |
| Efectos sistémicos |
|---|
| - fiebre (IL 1, IL 6) |
| - proteínas de fase aguda (IL 6) |
| - shock séptico (TNF) |
Los receptores tipo Toll (RTT) son una familia de receptores que reconocen estructuras altamente conservadas de los patógenos llamados patrones moleculares de agentes microbianos (PMM), que estimulan la Respuesta Inmune (6). Estos receptores se expresan en células del sistema inmune (macrófagos, células dendríticas, neutrófilos, linfocitos T y B) y se activan al reconocer determinados PMM presente en microorganismos, destacando entre ellos los lipopolisacáridos (LPS), Nucleotidos CpG no metilados y ARN doble hebra. El efecto de la unión entre los RTT y los PMM ha puesto en evidencia la unión entre la inmunidad innata y adquirida.
La interacción entre los RTT y los PMM (presente en los patógenos) induce secreción de citoquinas (en especial interferón alfa) e inducción de moléculas coestimulatorias. Esta activación inicial del sistema inmune innato y luego adaptativo mediada por las células dendríticas se postula conllevaría al inicio y progresión de ciertas enfermedades autoinmunes. Esto se debería al quiebre de la tolerancia explicado en parte por la exposición al interferón alfa (INFα) que aumentaría la sensibilidad del sistema inmune a ligandos endógenos y exógenos, induciendo la maduración células dendríticas y activación del macrófagos. Esto conduciría a un aumento en su capacidad de activar células alogénicas con potencial generación de Linfocitos T autorreactivos y eventual autoinmunidad.
Sistema inmune adaptativoEl sistema inmune adaptivo (SIA) está presente en los vertebrados, es específico para distintas moléculas y se caracteriza por mejorar la capacidad defensiva frente exposiciones sucesivas. Los principales elementos del SIA son los linfocitos B y T que se activan frente a los antígenos (sustancias que inducen respuestas inmunes específicas).
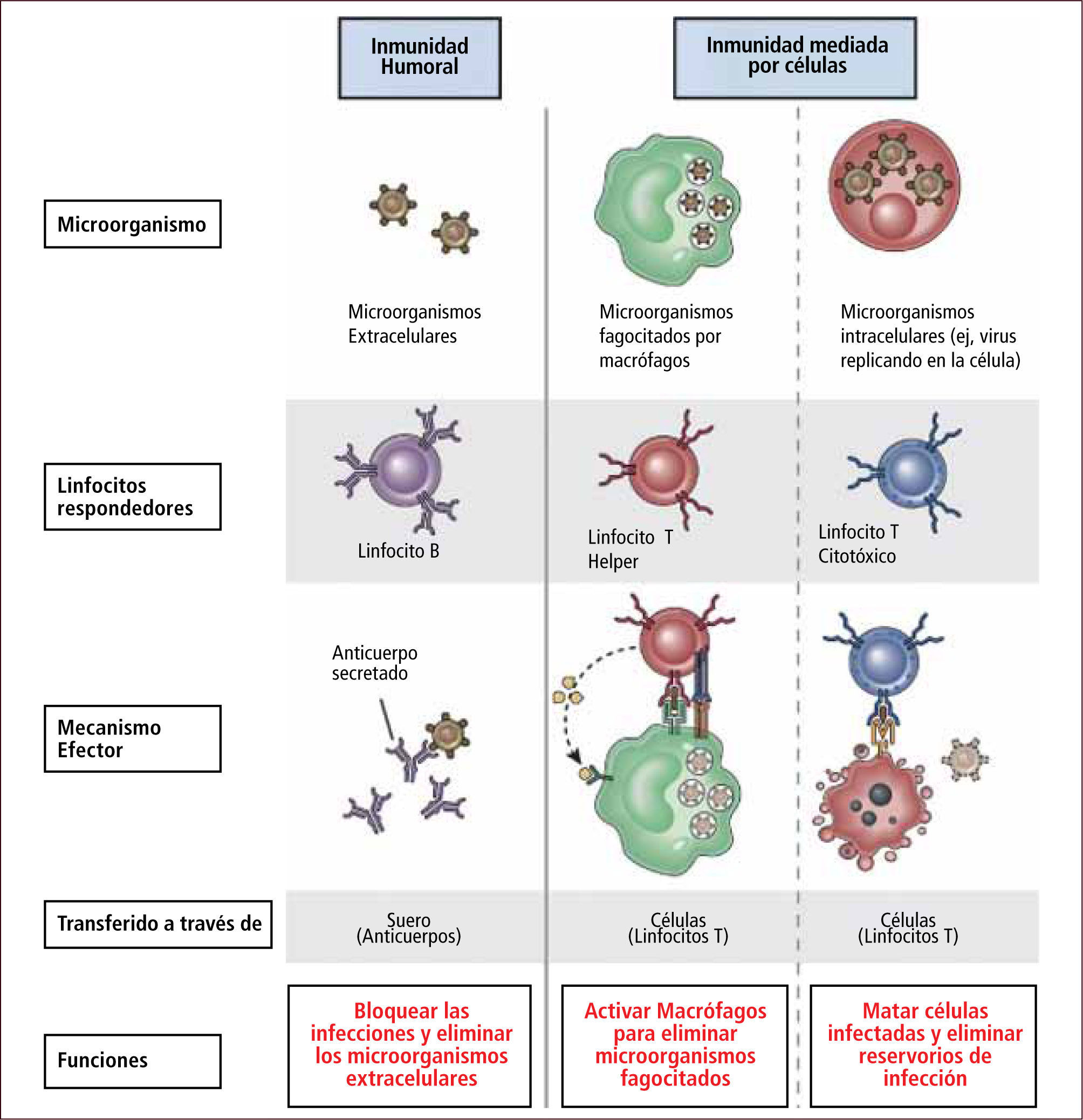
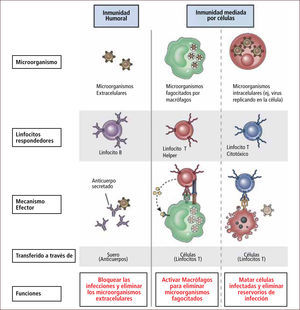
El SIA posee dos tipos de respuestas inmunes: Inmunidad Humoral e Inmunidad Celular (Figura 7).
Inmunidad adquirida humoral y celular
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
Tanto la respuesta inmune adquirida humoral como celular poseen características fundamentales que se resumen en la Tabla 4. Esta respuesta posee memoria, es decir, es “recordada” por el sistema inmune, siendo más eficaz y precoz frente a reexposiciones al mismo microorganismo (2). Además esta respuesta es específica a cada microorganismo o molécula no infecciosa, siendo capaz de distinguir de manera muy fina las características de éstas. Esta capacidad de reconocimiento específico de cada antígeno, por parte de los linfocitos, se debe a la expresión de receptores a los diferentes antígenos foráneos existentes y se denomina repertorio de linfocitos, el cual es extremadamente amplio.
Características del sistema inmune adquirido
| Especificidad: reconoce diferentes tipos de antígeno |
| Diversidad: responde a una amplia variedad de antígenos |
| Memoria: amplifica las respuesta a repetidas exposiciones al mismo antígeno |
| Especialización: genera respuesta óptimas para la defensa contra diferentes microorganismos |
| No reactivo a lo propio: previene la injuria al huésped durante la respuesta a antígenos extraños |
El repertorio de linfocitos se genera por la existencia de tres familias de receptores que mediante recombinaciones génicas son capaces de generan una diversidad que les permita reconocer a casi cualquier antígeno existente. Estos receptores son las moléculas de histocompatibilidad (HLA), los receptores de linfocitos T (TCR) y los receptores de linfocitos B (BCR). La característica anticipatoria del SIA es debida a la existencia de estos mecanismos génico presentes en estos receptores que genera cientos de millones de anticuerpos y receptores de células T y en los cuales el antígeno no juega ningún rol. En este proceso se produce un repertorio de linfocitos tolerante, sin embargo, pueden generarse clones autorreactivos, los cuales son deletados durante la ontogenia del sistema.
Inmunidad celularEs mediada por linfocitos T y constituye el principal mecanismo de defensa contra microorganismos intracelulares (virus y algunas bacterias) promoviendo la destrucción de estos en fagocitos o eliminando células infectadas. Los linfocitos T se dividen en dos subpoblaciones principales: linfocitos T CD4+ cuya principal función es la secreción de citoquinas y los linfocitos T CD8+ que eliminan células infectadas y tumorales.
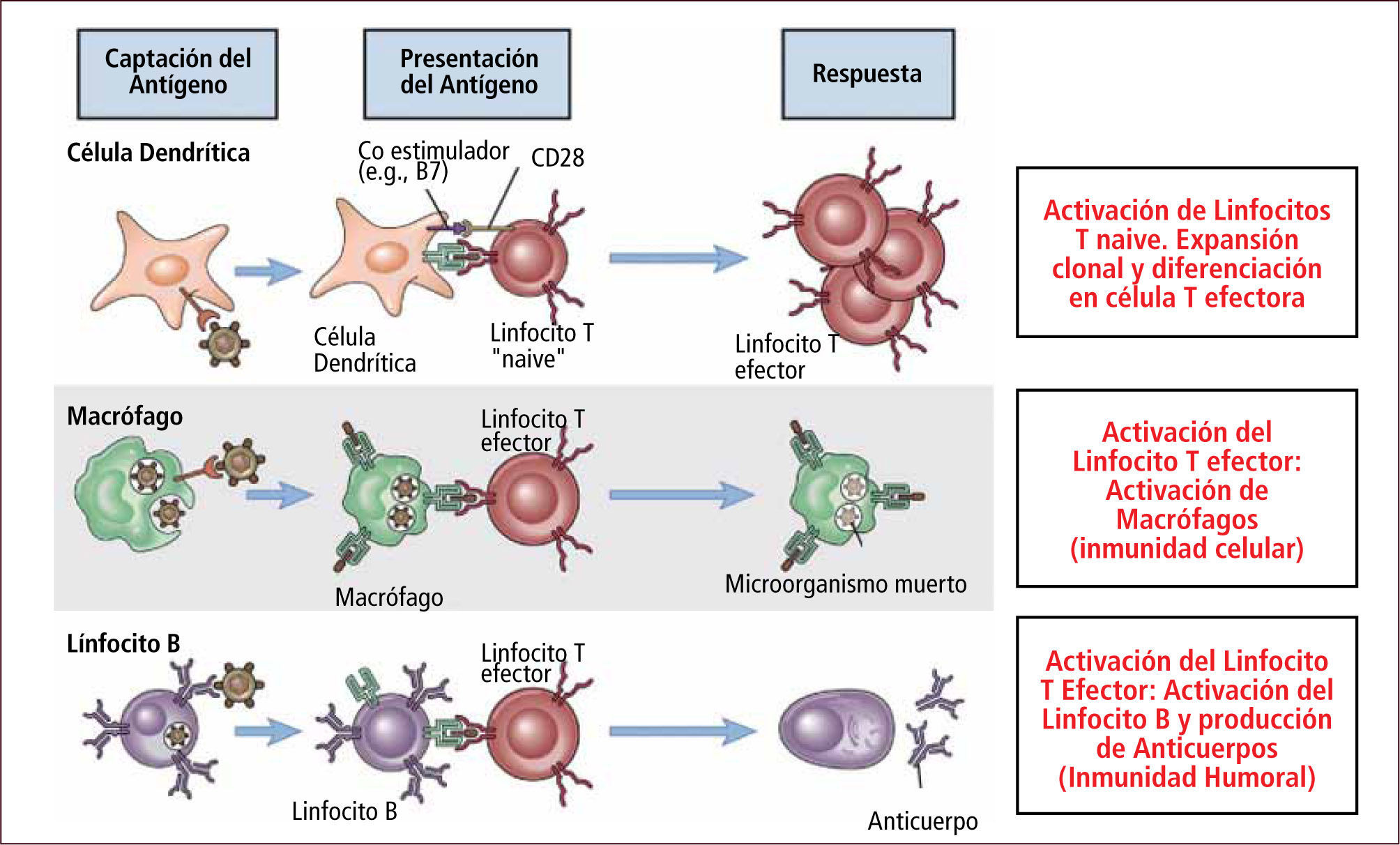
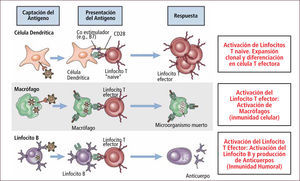
Respuesta Inmune celularAl ingresar el antígeno a través del epitelio es captado por una célula presentadora de antígeno (APC) “profesional” (célula dendrítica o un macrófago), transportado al linfonodo regional o el bazo y transformados a péptidos que se expresan en la membrana de la APC. Los linfocitos T no activados o naive recirculan a través de los linfonodo continuamente. Cuando este linfocito T encuentra su antígeno en el ganglio lo reconoce a través de su receptor (TCR) y es activado proliferando y diferenciándose a linfocitos T efectores y de memoria (7). Luego los linfocitos T efectores migran hacia los sitios de infección o inflamación encontrando el antígeno para el cual son específicos. La subpoblación de linfocitos T CD4+ efectores antígeno específico secretan citoquinas que activan (ayudan) a los macrófagos para eliminar los microorganismos fagocitados e inducen al linfocito B a diferenciarse y secretar anticuerpos que se unen a los antígenos. Por otra parte, los linfocitos T CD8+ efectores antígeno específico (también activados por las citoquinas secretadads por el linfocito TCD4+) matan células infectadas o tumorales que expresan HLA tipo I (Figura 8).
Respuesta Inmune Celular
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
Se han descrito dos grupos de linfocitos T CD4+ (helper): TH1 y TH2, ambos subsets provienen de un lineaje común de linfocitos T CD4+ que se diferencian hacia TH1 en presencia de interleuquina 12 (IL12) y amplificado por interferón gamma (INFγ) y hacia TH2 en presencia de IL 4 (7).
Estos subsets se han definido en base al tipo de citoquina predominante que secretan, lo que determina el tipo de funciones efectoras de los linfocitos.
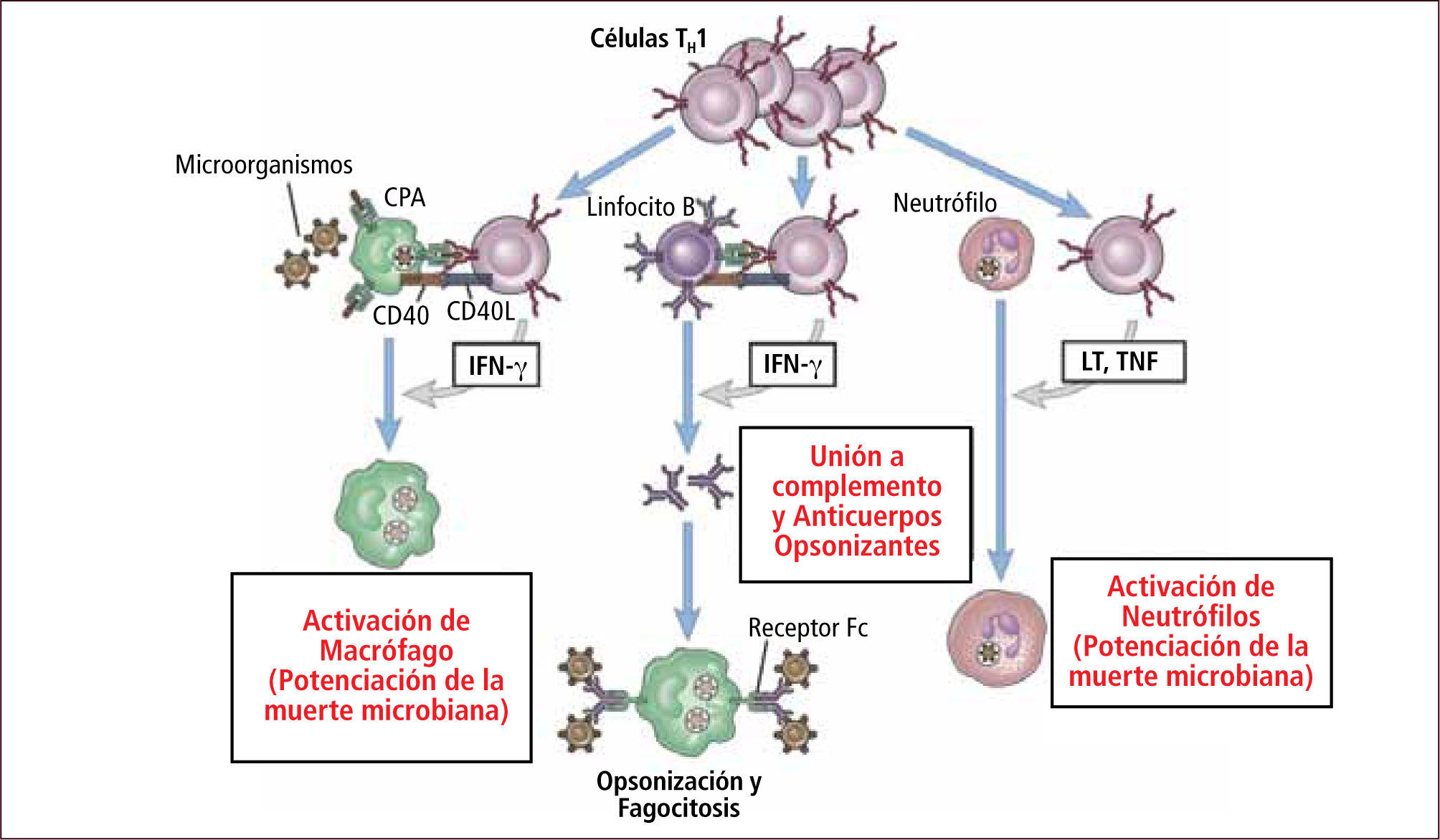
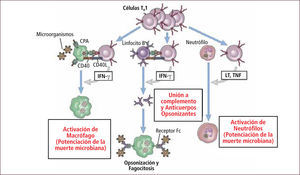
La diferenciación de linfocitos T CD4+ hacia linfocitos TH1 es estimulada por bacterias intracelulares, virus, algunos parásitos y antígenos proteicos administrados con fuertes adyuvantes que inducen la secreción de IL12 por parte de los macrófagos. Los linfocitos TH1 secretan INFγ, factor de necrosis tumoral e IL2. El INFγ activa el macrófago e incrementa la secreción de IL12, la fagocitosis y eliminación de microorganismos. El INFγ también estimula a los linfocitos B a secretar inmunoglobulina G (IgG) que actúa opsonizando los microorganismos tornando más eficiente la fagocitosis (Figura 9).
Respuesta inmune celular mediada por linfocito TH1
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
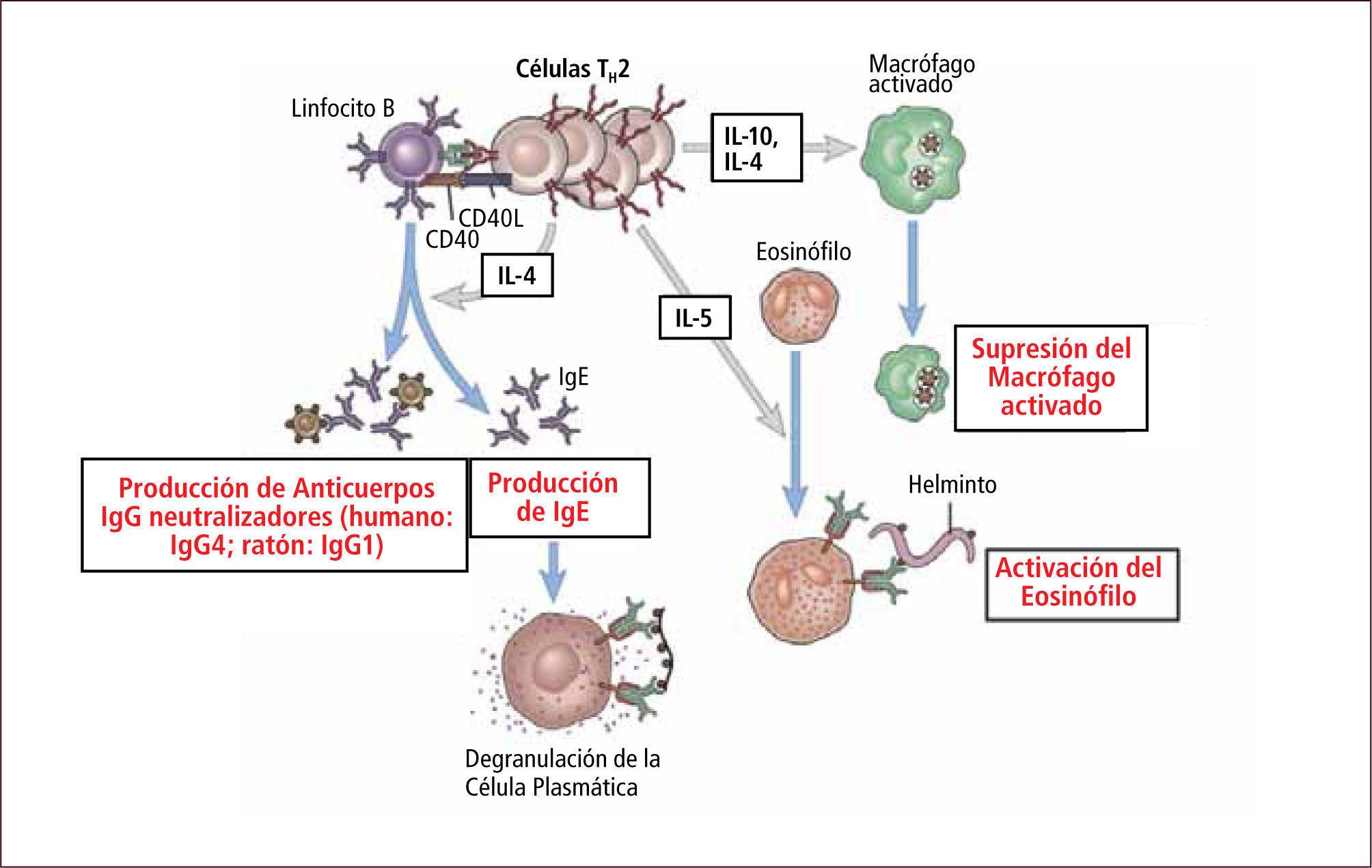
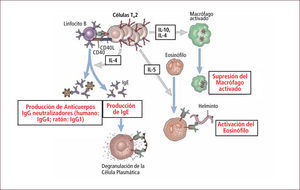
La diferenciación de linfocitos T CD4+ hacia linfocitos TH2 es estimulada por la presencia de alérgenos y helmintos que inducen la secreción de IL4. Estos linfocitos TH2 secretan IL4 e IL13 que induce el cambio de clase en el linfocito B hacia la producción de anticuerpos de tipo IgE (que media la inmunidad antihelmintos y las reacciones alérgicas). Los linfocitos TH2 también secretan IL5 que induce la maduración y llegada de eosinófilos, células también involucradas en la inmunidad antihelmintos y las reacciones alérgicas (Figura 10).
Respuesta inmune celular mediada por linfocitos TH2
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
Otro subset de linfocitos descritos más recientemente descrito son los linfocitos TH17 que corresponden a una subpoblación de linfocitos T generada por el estímulo de la IL23 que induce su diferenciación caracterizada por la secreción de IL17 (A y F), la cual gatilla efectos proinflamatorios tisulares y reclutamiento de neutrófilos cuyo rol fisiológico sería la defensa contra algunos microorganismos como Klebsiella pneumoniae y Borrelia burgdorferi entre otros (8). Estos efectos proinflamatorios son similares a los del factor de necrosis tumoral (TNF), IL1 e IL6. Debido al importante rol proinflamatorio de la IL17 se ha postulado que los linfocitos TH17 tendrían un rol en autoinmunidad. Apoyando esta teoría niveles altos de IL17 se han encontrado en pacientes con esclerosis múltiple, artritis reumatoídea y psoriasis entre otras enfermedades autoinmunes (9).
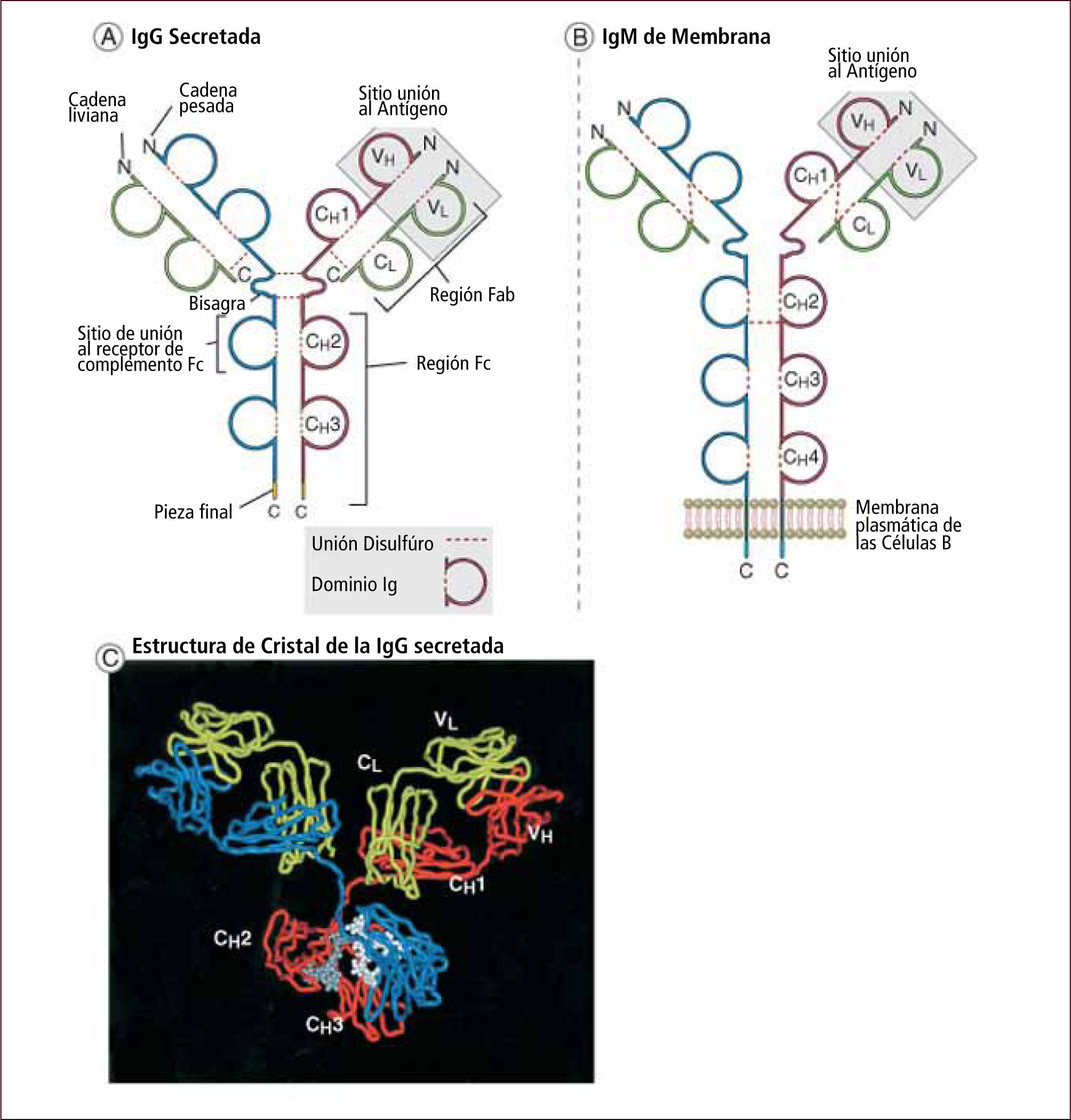
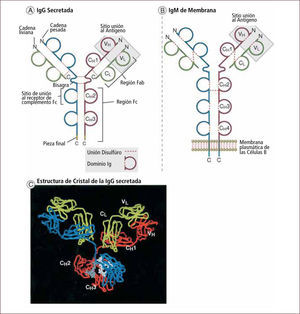
Inmunidad humoralEs mediada por anticuerpos o Inmunoglobulinas que son secretados por los linfocitos B. La inmunidad humoral constituye el principal mecanismo de defensa frente a infecciones bacterianas. Los anticuerpos o Inmunoglobulinas (Ig) son polipéptidos compuestos por dos cadenas livianas y dos cadenas pesadas. Poseen una región constante (Fc) que determina su clase (G, A, M, D y E) y funciones biológicas y una región variable (Fab) de unión al antígeno (10) (Figura 11).
Estructura de las inmunoglobulinas
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
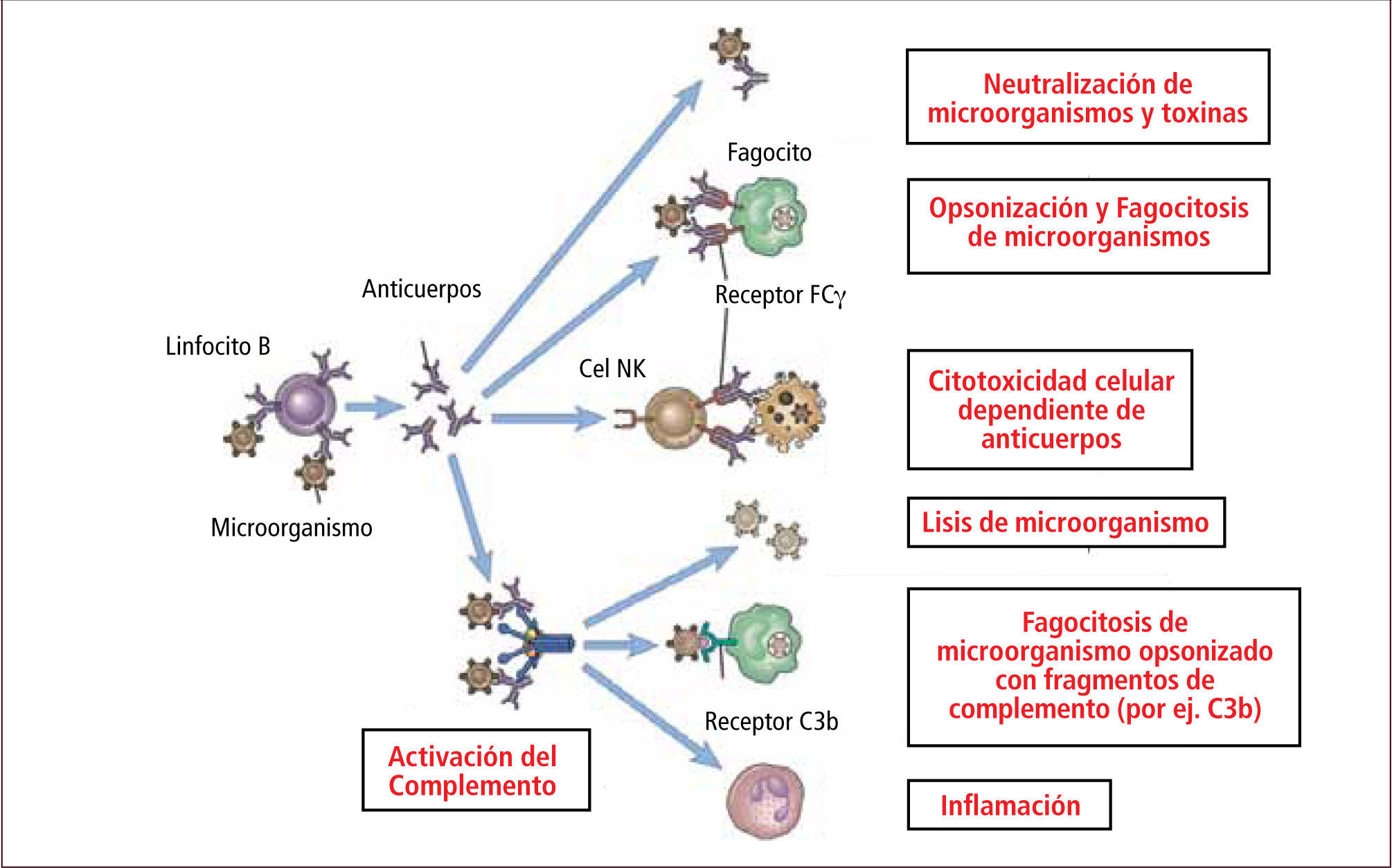
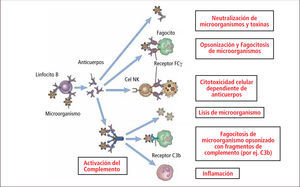
Las inmunoglobulinas reconocen y neutralizan los microorganismos mediante su región variable, gatillándose posteriormente diferentes mecanismos efectores para su eliminación (activación del complemento, opsonización) (Figura 12).
Funciones de los anticuerpos
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
Las células B residen y circulan en los linfonodos y bazo, al encontrar su antígeno, al cual es específico, se une a través de su receptor (BCR) IgM+ e IgD+ e induce la activación del linfocito B que se traduce en:
- 1-
Activación y posterior producción de anticuerpos (inicialmente IgM y luego IgG, IgE o IgA).
- 2-
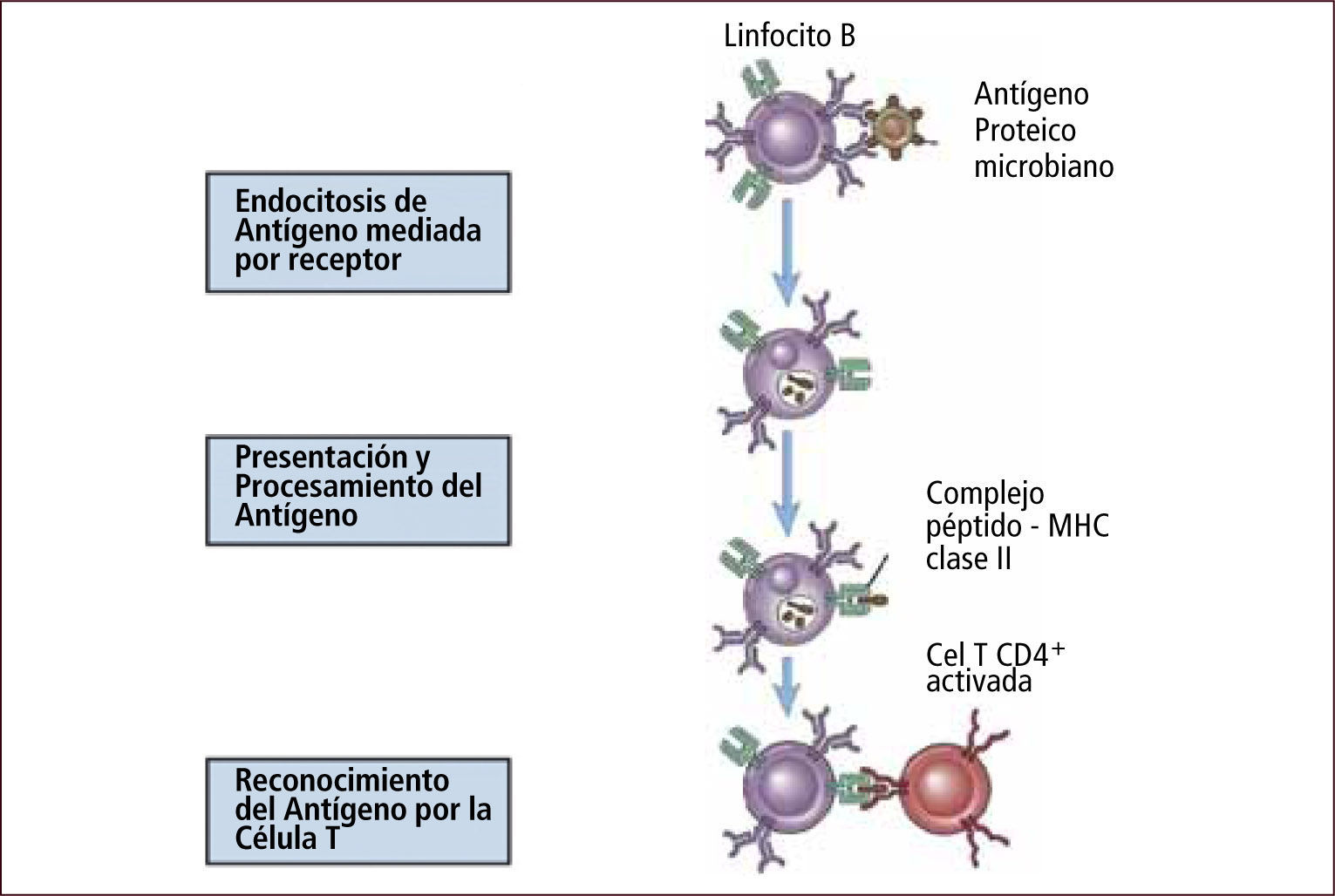
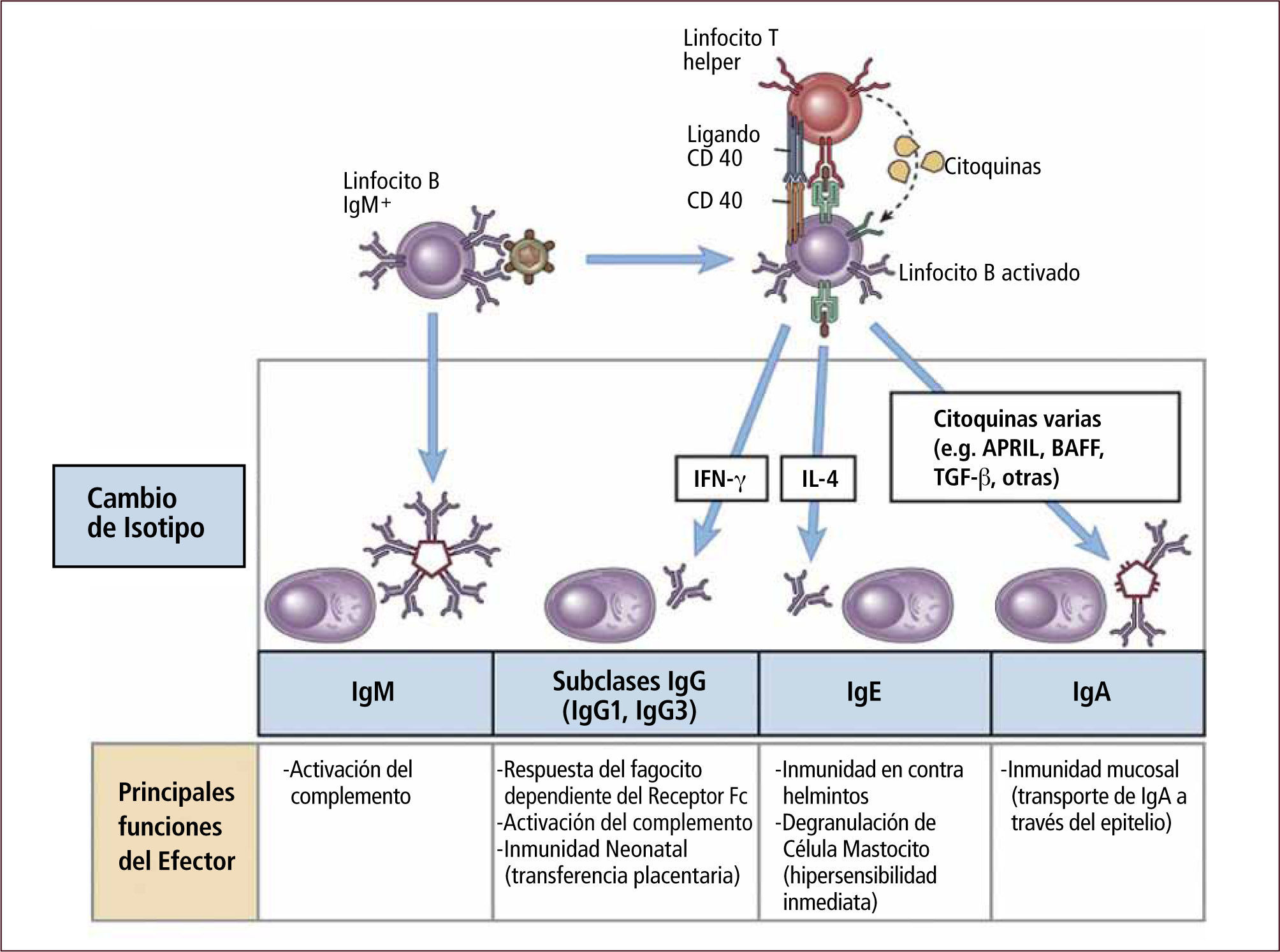
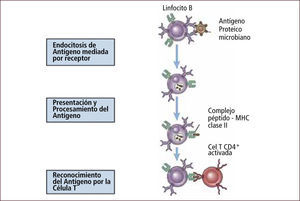
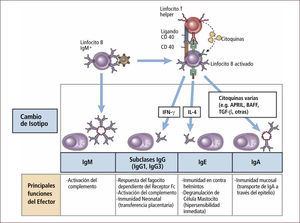
Internalización del antígeno y posterior presentación antigénica. El linfocito B entonces se torna en una APC que presenta el antígeno a su linfocito T helper específico quien secreta citoquinas (Figura 13). La presencia de moléculas co-estimuladoras como el CD40 ligando así como la secreción de citoquinas inducen un swicht (cambio) de isotipo en el linfocito B. Este cambio de clase o isotipo depende del tipo de citoquina secretada por el linfocito. Los linfocitos T helper tipo 2: (TH2) secretan IL4 que induce secreción por parte del linfocito B de IgE y los linfocitos TH1 secretan INF γ e IL12 que inducen secreción de IgG (Figura 14).
Figura 13.Reconocimiento y presentación de antígeno por linfocito B
Traducido: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
(0,14MB).Figura 14.Respuesta inmune humoral
Traducido de: Elsevier. Abbas et al: cellular and Molecular Inmunology 6e - www.studentconsult.com
(0,29MB).
La comprensión del funcionamiento del sistema inmune nos ha llevado a dilucidar los mecanismos fisiopatogénicos que subyacen a numerosas patologías. Esto ha permitido un mejor manejo y tratamientos más específicos de muchas enfermedades inmunológicamente mediadas.
La autora declara no tener conflictos de interés, con relación a este artículo.