Mientras buscamos maneras de prevenir el cáncer, la quimioprevención ha evolucionado como una herramienta para la reducción de riesgo. El uso de drogas u otras substancias que previenen o atrasan el inicio de cáncer en individuos sanos ha sido objeto de intensa investigación durante las últimas dos décadas. Aquellos individuos quienes en teoría deben beneficiarse más incluyen los con mutaciones genéticas germinales que confieren una predisposición al cáncer. Desafortunadamente, este grupo de individuos ha sido sub representado en los estudios clínicos y, por lo tanto, la evidencia para la quimioprevención en este grupo es limitada. Se presenta una revisión de la literatura sobre la quimioprevención primaria para el cáncer de colon, mama, ovario, y próstata en los portadores de mutaciones genéticas hereditarias.
As we continue to seek ways to prevent cancer, chemoprevention has evolved as an important tool for risk reduction. The use of drugs and other substances to prevent or delay the onset of cancer in healthy individuals has been the subject of intense research over the past 2 decades. Those individuals who in theory may benefit most include those with germline genetic mutations conferring a predisposition to cancer. Unfortunately, this group of individuals has been underrepresented in studies and therefore the evidence for chemoprevention in this group is limited. Herein we review the literature regarding primary chemoprevention for colorectal, breast, ovarian and prostate cancer in carriers of hereditary genetic mutations.
Según los últimos datos publicados por la Agencia Internacional para la Investigación de Cáncer (IACR), en 2012 había 8.2 millones de muertes atribuibles al cáncer al nivel mundial1. Dado el envejecimiento de la población, se estima que en el año 2030 esta cifra aumentará a 13 millones de individuos1. En nuestro país, el cáncer es igualmente letal; es clasificado como la segunda causa principal de muerte en Chile2. Tales hechos crudos obligan a encontrar tratamientos más efectivos y, sobre todo, a mejorar nuestras estrategias preventivas para el cáncer.
La quimioprevención implica el uso de drogas u otras sustancias para prevenir o suprimir la carcinogénesis efectivamente, reduciendo el desarrollo de un cáncer o retrasando su desarrollo. La quimioprevención puede ser primaria, secundaria, o terciaria. La quimioprevención primaria está dirigida al grupo de individuos sanos que está en alto riesgo del cáncer.
Aquellos que están más vulnerables al cáncer, incluye a los portadores de mutaciones germinales asociados con una predisposición al cáncer. Las estrategias para prevenir el cáncer en tales individuos se han enfocado principalmente en las intervenciones quirúrgicas como las mastectomías profilácticas para las portadoras de mutaciones en BRCA1/2 y las colectomías para pacientes con Poliposis Adenomatosis Familiar (PAF). Mientras que las cirugías de reducción de riesgo pueden ser muy efectivas para la prevención de cáncer, tienen sus propios riesgos y comorbilidades. Además, mientras que la predisposición al cáncer es generalmente una condición sistémica, la cirugía es una intervención local. Por lo tanto, sería más eficiente utilizar intervenciones que son menos invasivas y que funcionan a nivel sistémico.
La quimioprevención es una opción atractiva para pacientes de alto riesgo. Aquí revisamos los datos publicados sobre la quimioprevención en el cáncer de colon, mama, ovario, y próstata, específicamente en pacientes sanos con mutaciones hereditarias.
CÁNCER DE COLONMúltiples estudios de quimioprevención han sido publicados en cáncer colorrectal. Tales estudios se basaron en los datos publicados hace más de una década que demostraron que los adenomas colónicos sobreexpresan COX23. Esta revelación estimuló los ensayos clínicos que evaluaban el uso de los antiinflamatorios no esteroideos (AINES) para la prevención primaria del cáncer colorrectal. Ahora está claro que los AINES reducen la incidencia y recurrencia de adenomas en la población general4,5. Sin embargo, la aplicabilidad de tal quimioprevención a individuos de alto riesgo de cáncer colorrectal, como los pacientes con PAF y el síndrome de Lynch, requiere un análisis a parte. Tales pacientes han sido sujetos de investigación de los estudios del colorectal Adenoma/Carcinoma Prevention Program (CAPP).
CAPP2 fue un estudio aleatorizado y controlado placebo que comparó aspirina 600mg diario vs placebo en más de 800 pacientes con el síndrome de Lynch. Los participantes tomaron hasta 4 años la droga del estudio. El endpoint primario fue la incidencia de cáncer colorrectal. El estudio mostró que aspirina tomado por al menos dos años, pero no menos, redujo el riesgo de cáncer colorrectal en más de la mitad en este grupo de alto riesgo. Más importante, la aspirina también fue protectora de los otros cánceres asociados con el síndrome de Lynch, como por ejemplo el cáncer de endometrio6.
Un estudio observacional de pacientes con el síndrome de Lynch similarmente reveló un efecto protector de aspirina. Más de 1000 pacientes fueron incluidos en este análisis que evaluó el uso de aspirina e ibuprofeno en los portadores de mutaciones de los genes de mismatch repair. El estudio concluyó que cinco años o más de aspirina o ibuprofeno fue asociado con una reducción de riesgo de cáncer colorrectal, lo cual fue significativo (HR 0.25 and HR 0.26, respectivamente). Además, mostró que el uso de un mes – 4.9 años de aspirina o ibuprofeno también tuvo un efecto7.
La dosis óptima y la duración del uso de aspirina aún no han sido definidas. El estudio CAPP3 está en curso para dilucidar las respuestas a tales preguntas. En este estudio, los participantes estarán divididos en tres ramas, tratamiento con aspirina de baja dosis, de dosis intermedia y dosis alta. Mientras que esperamos los resultados de CAPP3, dado los estudios publicados anteriormente, el National Comprehensive Cancer Network (NCCN) recomienda considerar la aspirina para la prevención primaria de cáncer colorrectal en pacientes con el síndrome de Lynch.
Para los pacientes con PAF, la utilidad de AINES es menos evidente. En 2000 y 2003, dos estudios que evaluaron el efecto de los inhibidores de COX en los adenomas colónicos demostraron una disminución en el número y tamaño de pólipos con el tratamiento8,9. No obstante, los estudios consistieron de un pequeño número de pacientes. En 2011 un estudio multicéntrico y randomizado fue publicado, el estudio CAPP1. CAPP1 evaluó el efecto de aspirina y el almidón resistente en el desarrollo de adenomas en pacientes con PAF. Doscientos seis individuos fueron aleatorizados a recibir aspirina y/o almidón resistente y/o placebo. A pesar de los resultados positivos en los estudios previos, CAPP1 falló demostrar un efecto significativo en la cantidad o tamaño de adenomas colónicos con aspirina o almidón resistente10. Por lo tanto, los resultados han sido mixtos y no hay estudios que directamente evalúan el efecto de los AINES en la incidencia de cáncer en los pacientes con PAF. Más investigación es necesaria antes de que los AINES puedan ser considerados como quimioprevención en este grupo. El manejo estándar sigue siendo la colectomía profiláctica.
CÁNCER DE MAMA Y OVARIOLas mujeres con mutaciones en BRCA1 y BRCA2 tienen un riesgo de por vida de cáncer de mama de aproximadamente 60-80% y un riesgo de por vida de cáncer ovárico de 20-40%11. Puesto que estas cifras son varias veces mayor que las cifras en la población general, las cirugías de reducción de riesgo y el aumento de vigilancia radiológica son el estándar de cuidado en los portadores sanos de mutaciones de BRCA. Para los pacientes que no son candidatos para cirugías o que no optan por cirugía, hay mucho interés en utilizar la quimioprevención.
Tal vez los datos más informativos que tenemos sobre el uso de la quimioprevención en esta población única vienen del estudio de US Breast Cancer Prevention - P-1. El estudio P-1, publicado en 1998, fue un ensayo que comparó el uso del modulador selectivo del receptor de estrógeno tamoxifeno vs placebo para reducir la incidencia de cáncer de mama. El estudio incluyó más de 13000 mujeres quienes tenían entre 35 a 59 años con un riesgo de cáncer de mama a 5 años de 1.66% o más, o mujeres quienes tuvieron antecedentes de carcinoma lobulillar in situ o que tuvieron mayor o igual que 60 años. Mientras que el estudio original no fue diseñado para evaluar el efecto del tamoxifeno en los individuos con mutaciones germinales, un estudio subsiguiente fue publicado en 2001. En este estudio, los pacientes quienes participaban en P-1 y quienes desarrollaron cáncer de mama fueron evaluados de modo retrospectivo para mutaciones de BRCA. Doscientos ochenta y ocho casos de cáncer de mama fueron incluidos en el análisis. De los 288 casos, solo 6.6% o 19 pacientes fueron portadores de mutaciones de BRCA1/2. Desafortunadamente, dado el pequeño número de pacientes con mutaciones, no fue posible inferir un efecto del tamoxifeno en la prevención de cáncer de mama en este grupo. No obstante, se sugirió que el tamoxifeno podía tener un efecto protector, con una reducción relativa del riesgo de 62%, en los portadores de mutaciones en BRCA212. Este grupo de pacientes suelen desarrollar tumores que sobreexpresan los receptores hormonales, de allí el fundamento biológico para su utilidad13. Al contrario, los portadores de mutaciones de BRCA1 no experimentaron un beneficio del tamoxifeno en este estudio.
Los anticonceptivos orales también han sido estudiados como quimioprevención en los pacientes de alto riesgo de cáncer de mama y ovario. Varios estudios pequeños, principalmente estudios de caso-control o estudios cohortes retrospectivos, han sido publicados. Estos datos fueron compilados en una meta-análisis publicado en 2010. Este estudio evaluó la asociación entre los anticonceptivos orales y el riesgo de cáncer de mama y ovario en pacientes con mutaciones de BRCA. El análisis fue compuesto de 18 estudios, con un total de 2855 casos de cáncer de mama y 1503 casos de cáncer ovárico. El meta-análisis demostró que el uso de anticonceptivos orales fue asociado con una reducción de riesgo significativo de cáncer ovárico (SRR 0.50)14. El estudio también reveló que no había un riesgo significativo de cáncer de mama asociado con el uso de los anticonceptivos orales formulados después del año 1975, un tema muy debatido en la literatura.
Mientras que la asesoría de la reducción de riesgo para los portadores de mutaciones de BRCA1/2 debe incluir una conversación sobre las cirugías profilácticas (la mastectomía y la ooforectomía), dado estos datos y otros también se puede ofrecer el uso del tamoxifeno y los anticonceptivos orales como quimioprevención primaria. Sin embargo, es importante destacar que dado la falta de tamizaje efectiva para el cáncer de ovario la preferencia ha sido la ooforectomía preventiva sobre la quimioprevención.
CÁNCER DE PROSTATAEl cáncer de próstata es el cáncer más común en los hombres al nivel mundial15. Mientras que la gran mayoría de los pacientes con cáncer de próstata no fallecen de su enfermedad, el grupo de pacientes con una enfermedad de alto grado tienen outcomes inferiores15. Este grupo de pacientes incluye los con mutaciones hereditarias en BRCA. Los hombres con cáncer de próstata y mutaciones en BRCA típicamente desarrollan una enfermedad agresiva con una pobre sobrevida16.
Los dos estudios principales de quimioprevención para el cáncer de próstata son el estudio de Prevención de Cáncer de Próstata y el estudio REDUCE. Ambos estudios evaluaron la efectividad de los inhibidores de alfa reductasa, finasteride y dutasteride respectivamente, para reducir la incidencia del cáncer de próstata. Colectivamente, los estudios evaluaron más que 25000 individuos. Los dos estudios demostraron una disminución en el riesgo para el cáncer de próstata con el uso de los inhibidores de alfa reductasa. Sin embargo, ambos estudios también demostraron una alza en la incidencia del cáncer de próstata de alto grado en la rama experimental17,18.
La presencia de mutaciones de BRCA no fue evaluada en estos estudios y, por lo tanto, no está claro como el uso de los inhibidores de alfa reductasa aplica a esta población de alto riesgo. Sin embargo, está bien establecido que los pacientes con mutaciones en BRCA suelen desarrollar el cáncer de próstata de Gleason 8-916.Ya que los estudios indican que los inhibidores de alfa reductasa son útiles solo para la prevención del cáncer de próstata de bajo riesgo, es poco probable que serán útil en la prevención del cáncer de próstata en portadores de mutaciones en BRCA.
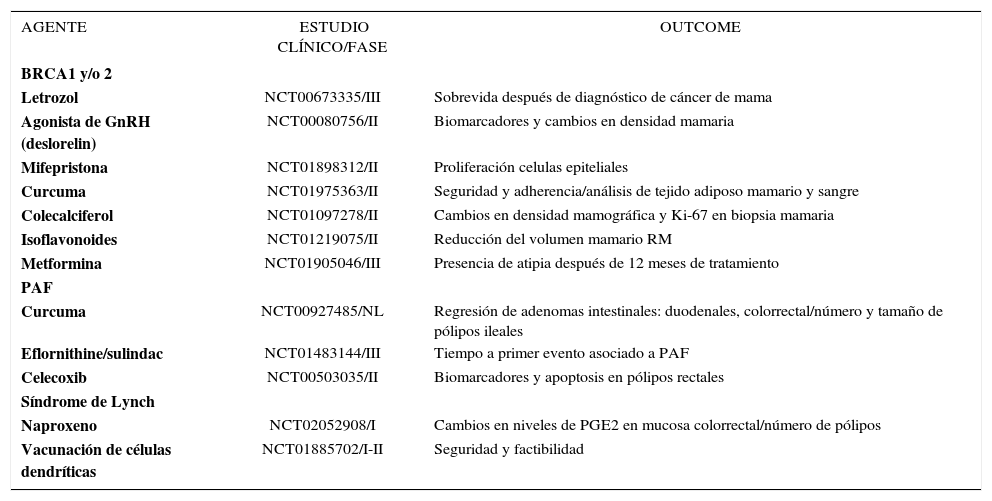
CONCLUSIONESLa quimioprevención es un área promisoria. Para los individuos de alto riesgo de cáncer, como los pacientes con síndromes hereditarias, la quimioprevención es de mayor importancia. Los AINES, el tamoxifeno y los anticonceptivos orales han demostrado tener alguna eficacia en este grupo de pacientes. Sin embargo, aún faltan datos. Actualmente se encuentran en desarrollo varios estudios clínicos con énfasis en quimioprevención, como modelo de estos pacientes con síndromes genéticos hereditarios (tabla 1). Mientras esperamos estos resultados, nuestro armamentario está limitado para este grupo de pacientes y hay que considerar las intervenciones de reducción de riesgo siempre en el contexto de las cirugías profilácticas y la vigilancia radiológica.
ESTUDIOS CLÍNICOS EN CURSO EN QUIMIOPREVENCIÓN DE SÍNDROMES GENÉTICOS HEREDITARIOS
| AGENTE | ESTUDIO CLÍNICO/FASE | OUTCOME |
|---|---|---|
| BRCA1 y/o 2 | ||
| Letrozol | NCT00673335/III | Sobrevida después de diagnóstico de cáncer de mama |
| Agonista de GnRH (deslorelin) | NCT00080756/II | Biomarcadores y cambios en densidad mamaria |
| Mifepristona | NCT01898312/II | Proliferación celulas epiteliales |
| Curcuma | NCT01975363/II | Seguridad y adherencia/análisis de tejido adiposo mamario y sangre |
| Colecalciferol | NCT01097278/II | Cambios en densidad mamográfica y Ki-67 en biopsia mamaria |
| Isoflavonoides | NCT01219075/II | Reducción del volumen mamario RM |
| Metformina | NCT01905046/III | Presencia de atipia después de 12 meses de tratamiento |
| PAF | ||
| Curcuma | NCT00927485/NL | Regresión de adenomas intestinales: duodenales, colorrectal/número y tamaño de pólipos ileales |
| Eflornithine/sulindac | NCT01483144/III | Tiempo a primer evento asociado a PAF |
| Celecoxib | NCT00503035/II | Biomarcadores y apoptosis en pólipos rectales |
| Síndrome de Lynch | ||
| Naproxeno | NCT02052908/I | Cambios en niveles de PGE2 en mucosa colorrectal/número de pólipos |
| Vacunación de células dendríticas | NCT01885702/I-II | Seguridad y factibilidad |
Ref.19.
Los autores declaran no tener conflictos de interés en relación a este artículo.