La cardiología nuclear ha sido tradicionalmente una herramienta de apoyo, principalmente en la evaluación de la cardiopatía coronaria. Los avances computacionales y desarrollo de nuevas técnicas han permitido mejorar la calidad de los estudios de cardiología nuclear, mejorando la exactitud diagnóstica. En este trabajo se revisarán los avances de los distintos equipamientos para obtención de imágenes con énfasis en la tecnología híbrida SPECT/CT y PET/CT, así como el desarrollo de nuevos trazadores y fármacos utilizados en la obtención de estas imágenes. Además, se revisan los protocolos actuales y los cambios que se debieran ver en el futuro cercano para adaptarse a los nuevos equipos y fármacos disponibles.
Nuclear cardiology has become an important tool in the clinical evaluation of coronary disease. Computer developments and the new available technology have improved the quality of the nuclear cardiology studies. This review will address the main advances in the equipments with special interest in hybrid technology of SPECT/CT and PET/CT, as well as the development of new tracers and drugs used to obtain these images. Furthermore the different acquisition protocols will be reviewed as well as the necessary adaptations that will be made in the near future to improve the use of the new available equipments, tracers and drugs.
La posibilidad de evaluar la perfusión miocárdica con un método imagenológico no invasivo se hizo realidad a mediados de la década de 1970 (1), gracias a la denominada cardiología nuclear. El principio básico de la cintigrafía de perfusión miocárdica es comparar imágenes representativas del flujo coronario en el miocardio del ventrículo izquierdo en fase de estrés y de reposo para así determinar presencia de isquemia (defectos reversibles) y/o infarto (defectos fijos) se mantiene hasta el presente. El paso de las décadas ha hecho que esta técnica madure, dejando de manifiesto su importancia en el aporte al estudio de la cardiopatía coronaria. En un comienzo, la técnica mayormente utilizada en el mundo era el estudio con 201Talio, un catión de comportamiento similar al potasio, que se administraba por vía endovenosa y permitía adquirir las imágenes estáticas del ventrículo izquierdo en tres proyecciones (anterior, lateral izquierda y oblicua anterior izquierda). Esta adquisición se realizaba luego de la administración del radiotrazador durante un estrés con ejercicio o inducido farmacológicamente, luego se volvía a adquirir con el paciente en reposo y finalmente se repetía la inyección para una nueva adquisición, de modo de aprovechar la propiedad de redistribución del 201Talio. Los buenos resultados obtenidos en series clínicas de pacientes con cardiopatía coronaria, específicamente en relación al valor pronóstico, hicieron que esta técnica ganara importancia en la práctica clínica habitual (2,3). La posterior aparición de los isonitrilos (MIBI) marcados con 99mTecnecio permitieron disminuir la dosis de radiación y mejorar la calidad de imágenes, facilitando además la disponibilidad de la técnica en nuestro país ya que se dejó de depender de la importación de 201Talio.
El desarrollo de la técnica a lo largo de las diferentes décadas hasta la actualidad tiene variados ámbitos, que se pueden resumir en cambios del equipamiento, aparición de nuevos fármacos y finalmente la actualización de los protocolos de adquisición. En este texto se pretende revisar los grandes cambios que ha presentado la técnica de perfusión miocárdica, enfocándose en la situación actual en nuestro país y los adelantos que se avizoran para los próximos años.
EQUIPAMIENTOEl evidente progreso tecnológico ha permitido el desarrollo de nuevas generaciones de equipos de detección de radiaciones utilizados en medicina nuclear (gamma-cámaras) que propiciaron beneficios significativos en los estudios de cardiología nuclear. La primera gran revolución fue en la última década del siglo pasado, con la implementación de las gamma-cámaras con capacidad tomográfica llamadas SPECT por su sigla en inglés de tomografía por emisión de fotón único. Realizar la adquisición tomográfica permitió reorientar las imágenes obtenidas ofreciendo los tres ejes (corto, largo horizontal y largo vertical), que se mantienen como formato estandarizado hasta la actualidad. Junto con la incorporación de la técnica SPECT se agregó además la posibilidad de realizar estudios gatillados mediante electrocardiograma (ECG), lo que permitió agregar información funcional al estudio: fracción de eyección (FE), motilidad global y segmentaria. Este aporte mejoró la especificidad de los estudios de cardiología nuclear, disminuyendo la cantidad de falsos positivos, y agregando además un importante factor predictor como la FE (2).
La medicina nuclear se revolucionó en este siglo con la implementación de la tomografía por emisión de positrones (PET), que ha tenido un enorme impacto en el área oncológica, y además presenta una serie de aplicaciones en la cardiología nuclear, incluyendo técnicas de perfusión miocárdica. Analizaremos finalmente el aporte de los nuevos equipos que han entrado en escena como las cámaras dedicadas para estudios cardiológicos y los equipos híbridos, que combinan los equipos de medicina nuclear (PET o SPECT) con un equipo de tomografía computada (CT) de radiología.
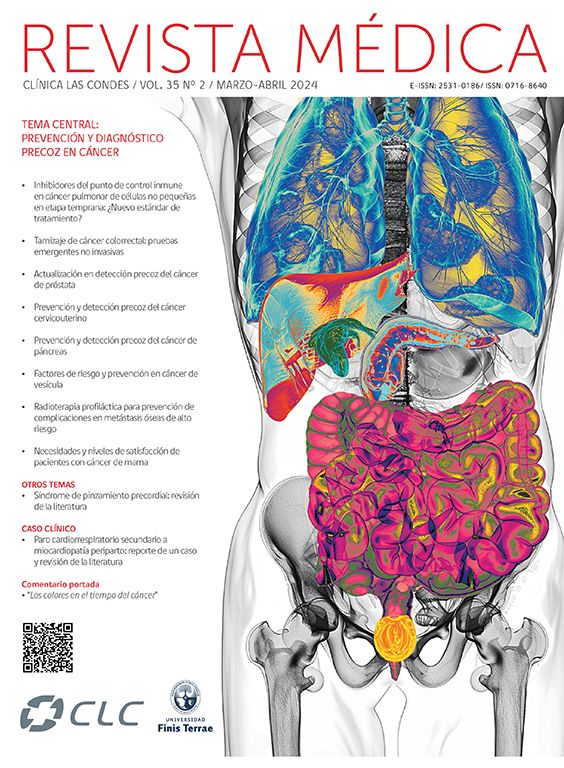
Gamma-cámaras cardiológicas dedicadasEl desarrollo de este tipo de equipos surgió de la necesidad de solucionar varios de los problemas intrínsecos de la adquisición SPECT tradicional. Una de las limitaciones técnicas del estudio de perfusión miocárdica es la interferencia de actividad extracardíaca, generalmente hepática o intestinal, que enmascara o altera la visualización del miocardio. Esto es más frecuente en pacientes donde se utiliza el dipiridamol para el estrés farmacológico, ya que a su propiedad de vasodilatación coronaria se agrega la vasodilatación esplácnica, que favorece la presencia del elemento radioactivo (eliminado por vía biliar) en las asas intestinales. En los equipos dedicados para estudios cardiológicos una de las principales características es que el paciente se realiza la adquisición de imágenes en posición sentado o semi-reclinado (Figura 1), a diferencia del SPECT tradicional donde es en posición horizontal (supino o prono dependiendo del protocolo). Al estar el paciente en posición sentado existe un descenso del hígado y de las asas intestinales, separándose del corazón, lo que mejora la calidad de la imagen.
Los equipos dedicados a la cardiología nuclear utilizan los denominados “detectores de estado sólido”, que poseen una mejor sensibilidad de detección que las gamma-cámaras SPECT tradicionales. Además, el diseño de estos detectores está especialmente adaptado al tórax, lo que permite posicionarse en mayor proximidad al corazón, por lo tanto, obteniendo una mayor cantidad de fotones lo que a su vez permite reconstruir imágenes de mejor calidad con una menor dosis de radiofármaco y/o un menor tiempo de adquisición (4). Esta es una ventaja significativa respecto a las gamma-cámaras SPECT, ya que pueden reducir hasta en un quinto el tiempo de adquisición de cada estudio, sin perder calidad de imagen. Estos equipos son de un alto costo relativo, lo que los hace ideales para funcionar en centros de imagenología cardíaca con grandes flujos de pacientes. En la realidad de los centros de medicina nuclear chilena, donde los estudios cardíacos se combinan en agendamiento diario con el resto de los estudios cintigráficos, este tipo de equipamiento dedicado no es práctico, por lo que no existe aún en el país.
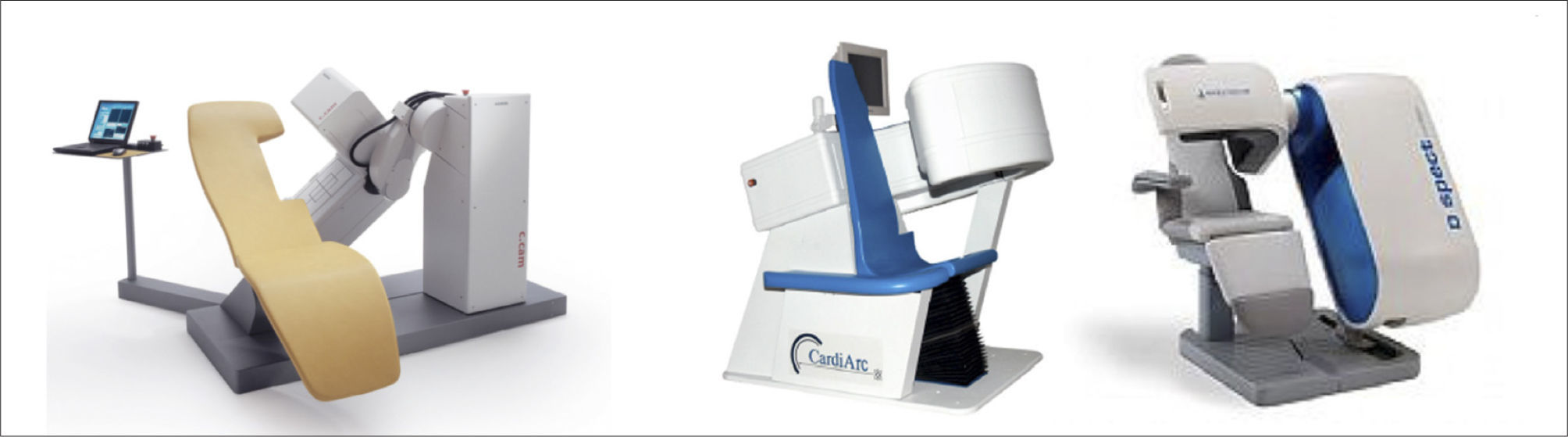
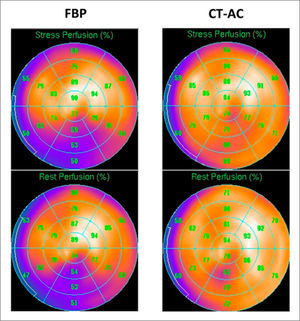
Equipos híbridosLa irrupción del PET/CT en la medicina nuclear motivó un auge de las llamadas modalidades híbridas, que combinan las imágenes funcionales o moleculares con las anatómicas. La gran ventaja de esta sinergia de técnicas de imagenología es la llamada corrección de atenuación. Para que un fotón, proveniente de un órgano específico donde se fija el radiotrazador, llegue al cristal de detección de la cámara, debe atravesar una serie de tejidos dentro del cuerpo que tienen diferentes densidades, provocando interacciones que atenúan su energía. El CT entrega una imagen tomográfica con las densidades de las diferentes estructuras, desde la que se construye un mapa de atenuación. Esto se puede lograr con una baja dosis de radiación, sin necesidad de aplicar medio de contraste. Mediante algoritmos los equipos híbridos aplican este mapa de atenuación a las imágenes de medicina nuclear, mejorando significativamente su calidad. En los estudios de perfusión miocárdica esto es evidente en los casos donde se aprecia atenuación diafragmática de la pared inferior o atenuación mamaria de la pared anterior (Figura 2) (5). La posibilidad de corrección de atenuación mejoró la exactitud diagnóstica de los estudios de perfusión miocárdica al permitir diferenciar de mejor manera un defecto de perfusión real de una menor captación producto de la atenuación (6).
Mapa polar de perfusión en estrés (Fila superior) reposo (Fila inferior)
(Fila superior) reposo (fila inferior) que muestra un artefacto por atenuación diagragmática de la pared inferior al ser reconstruido con retroproyección filtrada (FBP) y que desaparece al utilizar el mapa de corrección de atenuación del CT (CT-AC). Ref. 6.
Además de la corrección de atenuación, las imágenes de baja dosis del CT permiten obtener imágenes anatómicas que a veces pueden demostrar presencia de elementos de importancia clínica, como nódulos pulmonares, derrame pleural, adenopatías, etc. Los primeros equipos SPECT/CT híbridos contaban con componentes CT de baja dosis que se utilizaban exclusivamente para corrección de atenuación, pero las nuevas generaciones de equipos han apostado por incluir modelos con mayor capacidad diagnóstica del CT, que pueden ser utilizados para realizar estudios de Score de calcio o incluso realizar estudios coronarios con medio de contraste, además de los estudios tomográficos diagnósticos habituales. Esta tecnología se encuentra disponible en nuestro país desde fines de la década pasada, estando presente actualmente en algunos centros privados y públicos de la capital y de regiones. La tendencia actual del mercado es producir equipamiento híbrido, por lo que se vislumbra que la renovación de los equipos de medicina nuclear del país se irá inclinando por este tipo de equipamiento. Recientemente además fueron presentados al mercado la última generación de equipos SPECT/CT que incluyen como novedad los detectores de estado sólido que mejoran aún más la sensibilidad para detectar fotones, por lo que se sigue viendo progreso en esta área.
Por su parte, el PET/CT se ha consolidado como una herramienta fundamental en la etapificación y control de terapia de múltiples neoplasias, principalmente gracias al uso de un análogo de glucosa marcado con un isótopo del flúor emisor de positrones (18F-FDG). La tecnología empleada para la detección de los positrones sigue el mismo principio de los cristales utilizados en las gamma-cámaras tradicionales, con la diferencia que es un anillo de múltiples pequeños detectores en vez de los cristales de grandes dimensiones usados en los equipos SPECT. Esta particularidad hace que las imágenes obtenidas en los equipos PET/CT sean de una mejor resolución y calidad. En el ámbito cardiológico los estudios PET con 18F -FDG se utilizan para evaluación de viabilidad, disponible en nuestro país, sin embargo existe una serie de otras posibilidades de evaluaciones con PET, que se revisarán en los temas de radiofármacos y procesamiento de imágenes.
Procesamiento de imágenesLa mejoría exponencial en la capacidad y velocidad del procesamiento de datos que se ha experimentado en los últimos años ha afectado positivamente el ámbito de las imágenes médicas, y en especial a la medicina nuclear. Los sistemas computacionales que se encuentran en comercialización en la actualidad ofrecen en el ámbito cardiológico varios avances respecto a la generación previamente disponible. Uno de los avances significativos es una modificación de los algoritmos de reconstrucción que permiten obtener imágenes de similar calidad, pero desde una menor cantidad de información; es decir permitiría adquirir estudios a una mayor velocidad (menor tiempo para recolectar información) o administrando una menos cantidad de radiofármaco (menor actividad implicaría menor disponibilidad de fotones que detectar). Esto se traduce en una mayor capacidad para realizar estudios cardiológicos en los centros, menor tiempo de adquisición para los pacientes y una menor irradiación para todos los involucrados (7).
Los programas de procesamiento cardíaco que actualmente se incluyen comercialmente en las estaciones de trabajo de los distintos equipos incorporan de forma automatizada una serie de cálculos e índices que pueden ser de apoyo a la interpretación de los exámenes. Un ejemplo es el índice de dilatación isquémica transitoria (TID), que calcula la razón entre el volumen ventricular izquierdo en las imágenes de estrés sobre las de reposo. Otro índice disponible es el de excentricidad, que mide la deformación de la cavidad ventricular desde un ovoide hacia un esferoide, mediante la relación entre los diámetros de sus ejes largo horizontal y vertical. Estos índices se han relacionado con una mejor detección de enfermedad coronaria multivaso balanceada, donde la perfusión puede aparecer conservada, pero estos indicadores al igual que la caída de FE post estrés pueden estar alterados.
El análisis funcional, obtenido mediante el gatillado con ECG que previamente se mencionó, también ha presentado importantes avances. En la actualidad se dispone de programas que son capaces del análisis de fase que se aplica a los movimientos de las paredes del ventrículo izquierdo. Este análisis entrega información acerca del sincronismo con que se contraen las diversas paredes ventriculares, y ha demostrado ser de utilidad en evaluar las terapias con resincronizadores (8). Una ventaja de este análisis de sincronía es que se aplica a la adquisición tradicional del estudio de perfusión miocárdica, no requiere de imágenes extras y no altera el protocolo de adquisición.
En el ámbito PET se aplican los mismos principios a los estudios de perfusión con técnica SPECT, es decir los algoritmos de reconstrucción y los procesamientos automatizados de los diversos indicadores además del análisis de fase, con la ventaja de contar con una calidad de imagen superior debido a su mejor resolución. Un elemento diferenciador es la posibilidad de la evaluación del flujo absoluto, obtenido mediante un análisis dinámico de la actividad inyectada y de su internalización al miocardio. Esta tasa de captación se calcula en términos absolutos en ml/min/gr, y la reserva del flujo miocárdico está dada por la razón entre la tasa de captación en máxima hiperemia (estrés) y reposo. Esta información es clínicamente relevante ya que puede existir un miocardio que cuente con un flujo conservado durante el estrés pero a costa de la reserva coronaria, lo que en un estudio SPECT tradicional sería informado como normal. Por lo tanto, el PET/CT mediante el análisis de flujo coronario absoluto apuesta a convertirse en un importante indicador de enfermedad coronaria precoz, que puede permitir seleccionar a los pacientes aún asintomáticos (9). En nuestro país, si bien contamos con la potencialidad de realizar estos estudios ya que se dispone del equipamiento y del software, no tenemos a la fecha disponibilidad de trazadores PET que permitan evaluar flujo.
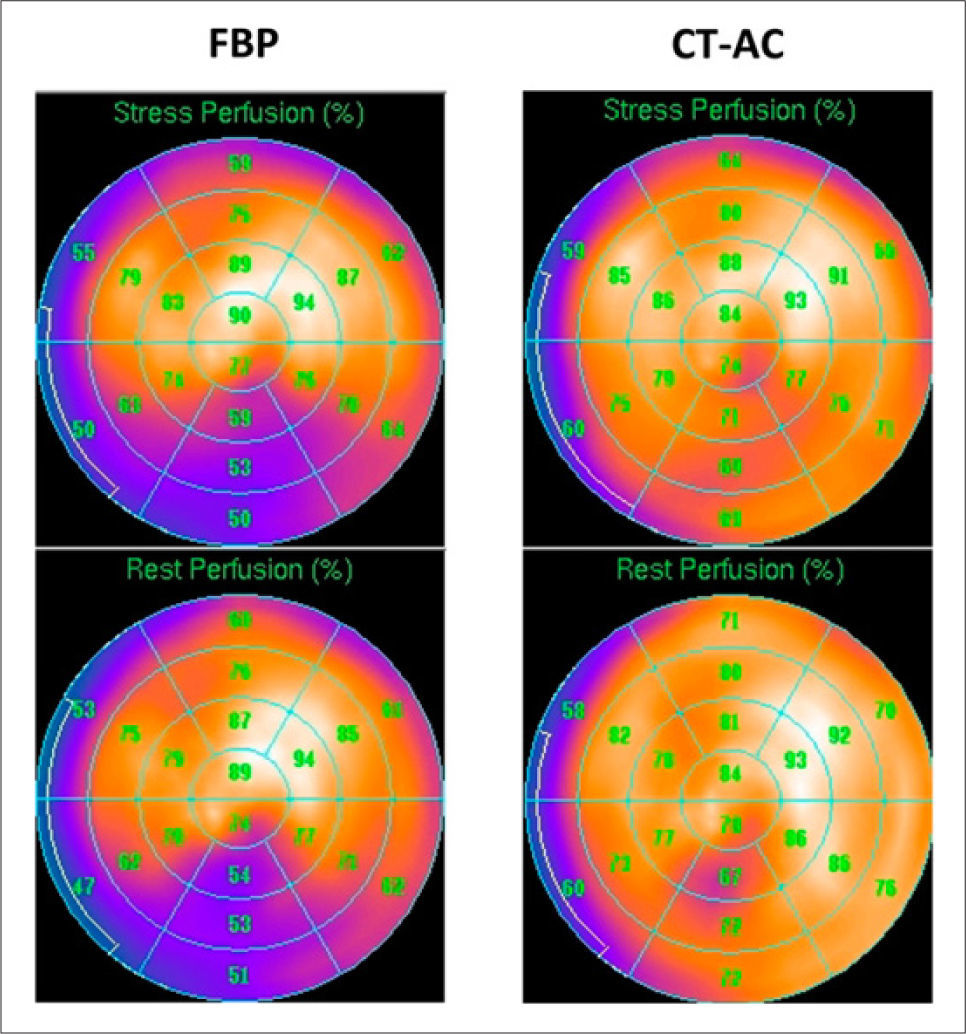
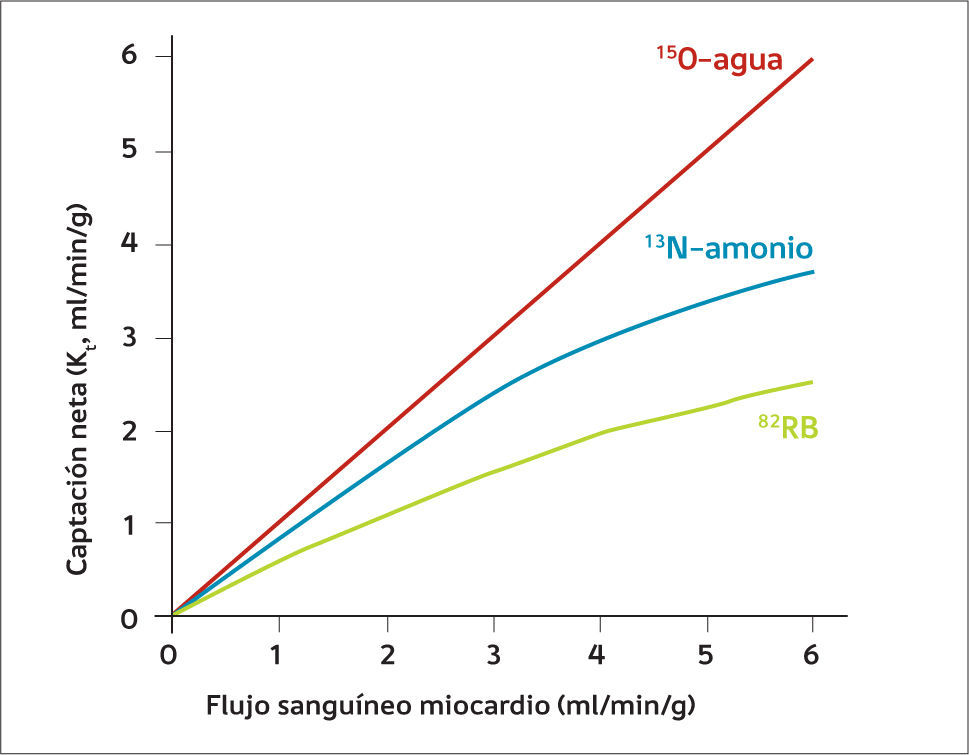
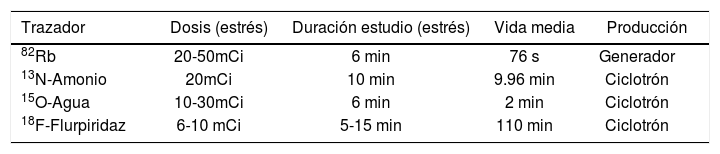
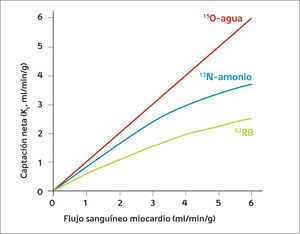
NUEVOS FÁRMACOSRadiotrazadoresEn Chile la totalidad de los estudios de perfusión miocárdica se realizan con 99mTc-MIBI como radiotrazador, con una buena disponibilidad y adecuada calidad, lo que avala su uso en los distintos centros a lo largo del territorio. Como se mencionó previamente, no existe disponibilidad local de trazadores de perfusión que emitan positrones para poder realizar estudios con técnica PET/CT, pero a continuación revisaremos las principales características de los trazadores disponibles en el exterior. El 15Oxígeno permite la marcación de moléculas de agua, que para los propósitos de análisis de perfusión miocárdica es el trazador ideal dada su farmacocinética de extracción por el miocardio de tipo lineal, pero su gran inconveniente es que para realizar estudios se necesita la presencia de un ciclotrón en el mismo centro dada su corta vida media de dos minutos. Los otros trazadores utilizados para evaluar flujo miocárdico son el amonio marcado con 13Nitrógeno (producto de ciclotrón, vida media de 10min) y el 82Rubidio, que se obtiene de un generador que es de alto costo, pero permite la independencia de contar con un ciclotrón en las proximidades. Estos dos últimos trazadores presentan un modelo de extracción miocárdica no lineal (Figura 3). En la actualidad se está desarrollando en segundo estudio de Fase III con un trazador de flujo marcado con 18F, cuya vida media de 110 min hace más factible su uso en los centros de PET/CT sin necesidad de depender de un ciclotrón cercano. Este trazador denominado 18F-Flurpiridaz ha mostrado primeros resultados alentadores, con una curva de extracción similar a las de 82Rb y 13N-Amonio, con capacidad de obtención de datos de flujo coronario absoluto y al compararlo con la técnica SPECT tradicional presenta mejor calidad de imagen y mejor exactitud diagnóstica (10). Dependiendo de los resultados de este nuevo estudio Fase III, existiría la alternativa de contar con este trazador en nuestro país ya que las características de los ciclotrones actualmente en funcionamiento permitirían su obtención. El resumen da las características de los trazadores de flujo para técnica PET se encuentra en la Tabla 1.
Relación Farmacocinética de extracción Miocárdica
K1 y el flujo miocárdico para cada trazador (9).
Los agentes más utilizados para lograr el estrés farmacológico son los vasodilatadores coronarios como la adenosina (poco utilizada en Chile por su alto valor) y un inhibidor de la recaptación de adenosina como el dipiridamol. Además se cuenta con agentes cronotropos e inotropos como la dobutamina, que se utiliza habitualmente frente a contraindicación de los vasodilatadores antes mencionados. Una de las implicancias de utilizar los vasodilatadores antes mencionados es la poca especificidad de su acción, ya que interactúan con receptores A1, A2A, A2B y A3, causando muchas veces síntomas asociados a vasodilatación periférica (cefalea, calor), broncoconstricción e incluso alteraciones de la conducción aurículo-ventricular. En los últimos años se introdujo al mercado un agente específico para los receptores A2A llamado Reganedoson, sin efecto sobre los otros receptores, por lo tanto con menores efectos secundarios y más seguro de utilizar en pacientes con antecedentes de asma bronquial y alteraciones de conducción del nodo A-V (11).
PROTOCOLOSEl formato clásico en que se realiza el test de perfusión miocárdico en nuestro país es alternar las fases de reposo y estrés, pudiendo realizarse en protocolo de un día o días separados. Cuando se realiza en un día se administra una dosis baja del trazador en la primera fase y se triplica la dosis para la segunda fase. Para definir el orden de las fases se debe tener en cuenta los siguientes factores: La fase que recibe la menor cantidad de dosis generará una imagen con menor calidad, especialmente si se requiere el análisis funcional del estudio gatillado. Si la primera fase es de estrés (físico o farmacológico), se deberá esperar idealmente 4 horas antes de iniciar la segunda fase. El protocolo de dos días se realiza con dosis menores (generalmente un 50% de la dosis que se daría en la segunda fase del protocolo de un día), iguales en ambas fases. En este caso el orden de las fases no tiene impacto. Por razones de logística se puede sugerir si se realiza un protocolo de un día iniciar con la fase de reposo administrando 8-10 miliCurie (mCi) de 99mTc-MIBI, y a continuación realizar el estudio de estrés con dosis de 25-30 mCi de 99mTc-MIBI. De esta forma la fase de estrés presenta la mayor dosis por lo tanto la mejor calidad de imagen, lo que disminuye la probabilidad de informar equivocadamente un defecto de perfusión (12).
La aparición de los nuevos equipos y programas de procesamiento antes mencionados han alterado este formato estandarizado que se promocionó por muchos años. Hoy la tendencia es a adaptar los protocolos según las características del paciente así como de la información clínica. Por ejemplo, si se dispone de un equipo que me permite realizar estudios con 1/3 de la dosis tradicional o me permite adquirir cada fase en 4 minutos (equipos tradicionales pueden demorar hasta 30 min por fase), se puede seleccionar irradiar menos a pacientes jóvenes, o subir la dosis y realizar un estudio más rápido en pacientes añosos o que tengan dificultad en mantener la posición requerida durante el estudio, evitando así movimientos involuntarios que pueden afectar la calidad de las imágenes. Otra de las posibilidades en la actualidad es realizar estudios solamente en la fase de estrés, esto estaría indicado en los pacientes con una probabilidad pre-test más bien baja, donde un estudio totalmente normal evitaría realizar la segunda fase de reposo. Aquí lo ideal sería contar con un equipo híbrido capaz de corregir atenuación, de modo de no requerir la comparación con la segunda fase en caso de encontrar atenuación diafragmática o mamaria. Además en este subgrupo, también se puede optar por realizar una adquisición más rápida con mayor dosis versus una más lenta pero con menor irradiación para el paciente dependiendo de sus características individuales (13). Los valores referenciales de dosis equivalente absorbida en miliSievert (mSv) para los protocolos tradicionales SPECT de 1 día con 99mTc-MIBI es de 10mSv, reduciéndose a 5-7mSv con los protocolos que utilizan los equipos modernos SPECT/CT. Los protocolos aceptados con técnica PET/CT con 82Rb o 13N-Amonio entregan dosis de 2-6 mSv (13).
Los protocolos que se utilizan para adquisición de estudios de perfusión con PET/CT implican necesariamente, hasta ahora, el uso de estrés farmacológico dada la corta vida media del 82Rb o 13N-Amonio. Una ventaja comparativa versus el protocolo con SPECT es que se puede realizar ambas fases del estudio en tiempos mucho más cortos, con la consiguiente menor incomodidad para el paciente. La aparición del nuevo trazador 18F-Flurpiridaz antes descrito abre la posibilidad de realizar pruebas de esfuerzo en estos protocolos.
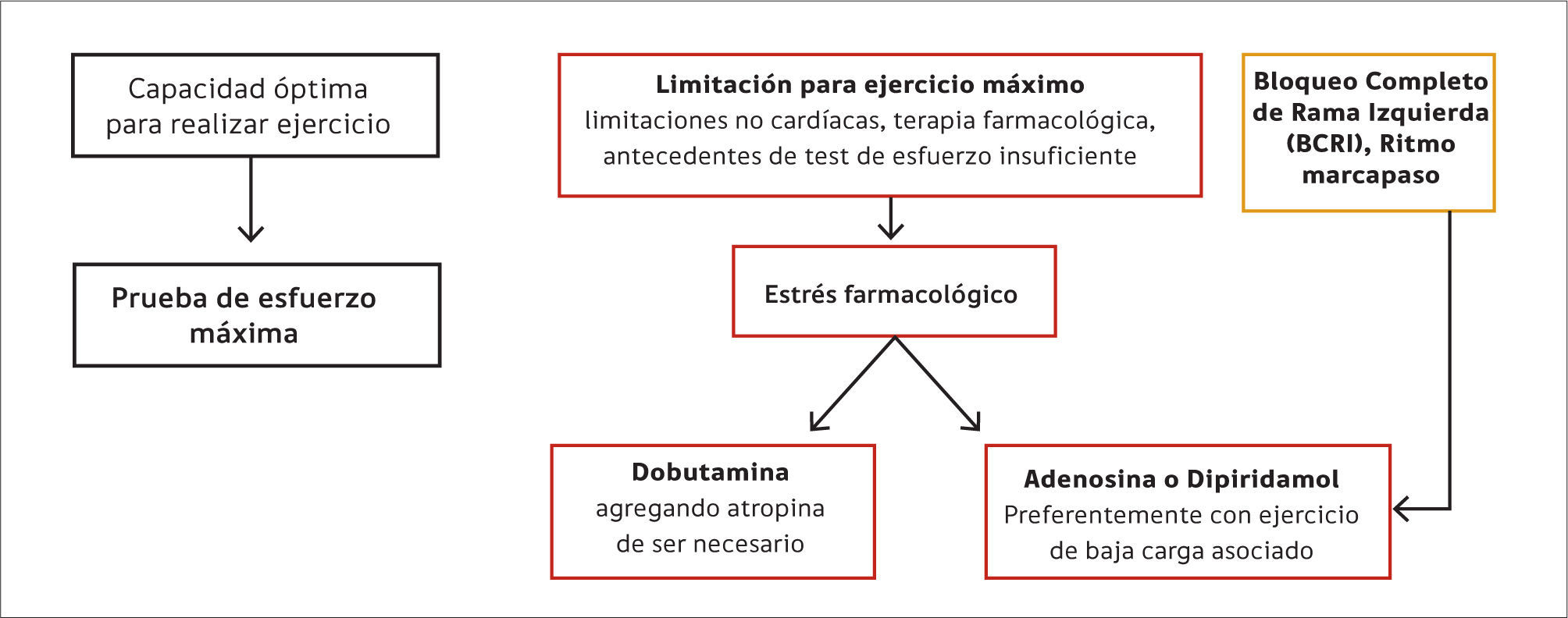
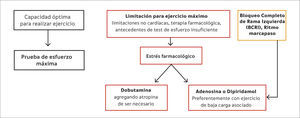
La elección del método de estrés en los estudios SPECT o SPECT/CT sigue siendo de preferencia el ejercicio físico, estandarizado como el protocolo de Bruce, siempre que el paciente sea capaz de llegar a un rango máximo de esfuerzo. En caso de no poder llegar a ese rango, por motivos propios del paciente o efectos farmacológicos, se sugiere utilizar los estresores farmacológicos. Una condición que debiera siempre requerir un estrés farmacológico es la presencia de bloqueo de rama izquierda, ya que se produce un artefacto en las imágenes de estos pacientes con el esfuerzo que pueden simular una isquemia (14) (Figura 4).
FLUJOGRAMA PARA ELECCIÓN DE MODALIDAD DE ESTRÉS
Adaptado de la guía Sociedad Europea de medicina Nuclear para estudios de perfusión miocárdica (14)
La interrupción de los medicamentos con efecto a nivel cardíaco para los estudios de perfusión miocárdico debiese ser revisada caso a caso en conjunto con el médico tratante. Puede darse la situación que la pregunta clínica es la sospecha de una cardiopatía coronaria en un paciente hipertenso usuario de beta bloqueadores, donde se podría suspender los fármacos para mejorar la capacidad diagnóstica del test. Otro caso puede ser un paciente coronario conocido, donde la finalidad del estudio es valorar el comportamiento del flujo coronario bajo las condiciones terapéuticas establecidas, en cuyo caso se puede realizar el protocolo sin suspensión de los fármacos.
CONCLUSIÓNLa cardiología nuclear sigue cumpliendo un rol preponderante de apoyo en la evaluación de la cardiopatía coronaria. La renovación tecnológica de los últimos años ha permitido aumentar significativamente la exactitud diagnóstica de la técnica, con incorporación de nuevos y prometedores indicadores como la posibilidad de medir el flujo coronario absoluto en forma no invasiva. La combinación de las técnicas de medicina nuclear y las radiológicas es el formato que llegó para quedarse, con las ventajas de reducción de dosis de radiación, menores tiempos de adquisición y mejor calidad de imagen, beneficios que se traspasan en forma directa a los pacientes.
El futuro inmediato de la cardiología nuclear es adaptarse a los requerimientos de una medicina más personalizada, con protocolos diseñados para cada paciente en forma específica. Para lograr esto es indispensable mantener un alto grado de comunicación entre los especialistas de imágenes con sus referentes clínicos, para poder optimizar el tipo de protocolo, elegir el esfuerzo adecuado según el paciente y finalmente reducir la dosis de radiación del paciente y/o mejorar su confort durante el estudio.
El autor declara no tener conflictos de interés, en relación a este artículo.