SF-36, quality of life measured by the SF-36 and EuroQol, and the domain of vitality measured by the SF-36. A model with PGA, PPA, BASFI, and vitality as independent variables explained 73% of the variance of the BASDAI scores. Cronbach's alpha of the Spanish BASDAI was 0.87. The reproducibility of the Spanish BASDAI as assessed by test-retest had a Spearman's rho = 0.92, p < 0.0001. Patients spent a mean of 60 seconds in completing the questionnaire and showed good comprehension. Conclusions: the Spanish BASDAI is reliable, valid, and feasible. It can be used to assess disease activity in Spanish patients with AS.
Introducción
El Bath Ankylosing Spondylitis Disease Activity Index (BASDAI) es un cuestionario que puede cumplimentarse de forma autoadministrada, desarrollado para medir actividad de la enfermedad en pacientes con espondilitis anquilosante (EA)1. La versión original en lengua inglesa consta de 6 preguntas que incluyen los componentes de fatiga, dolor espinal, dolor/inflamación articular, dolor en las entesis y rigidez matutina. El instrumento ha demostrado fiabilidad, validez y sensibilidad al cambio y es factible de aplicar en la práctica clínica diaria1-3.
Aunque la definición de actividad en la EA es compleja y no está completamente establecida, el BASDAI ha demostrado una adecuada validez de contenido4 y una buena correlación con los reactantes de fase aguda, como la velocidad de sedimentación globular, la proteína C reactiva, el amiloide sérico A5,6, e incluso con los valores del factor de necorsis tumoral alfa (TNF-α)7.
El BASDAI se ha utilizado en numerosos estudios8-16 y forma parte de los criterios de respuesta a corto plazo propuestos por el Grupo Internacional de Trabajo en Espondilitis Anquilosante (ASAS)17 y, asimismo, de los criterios preliminares de respuesta a tratamientos biológicos propuestos también por el grupo ASAS18. También forma parte de los criterios consensuados por el grupo ASAS para la inclusión de pacientes con EA en terapias biológicas19. Sin embargo, hasta ahora no se disponía de ninguna versión validada en español.
El objetivo de este estudio es conocer la fiabilidad, validez de constructo y factibilidad de una versión en español del BASDAI.
Métodos
Diseño y lugar de realización
Estudio transversal que se llevó a cabo en el Servicio de Reumatología del Hospital Universitario Virgen Macarena de Sevilla.
Pacientes
En Sevilla existe la Asociación de Pacientes con Espondilitis Anquilosante (EAS). En octubre de 1997 se envió una carta a todos los miembros de la EAS invitándoles a participar en un estudio acerca de su enfermedad. Se incluyó a todos los pacientes que contestaron afirmativamente, dieron su consentimiento verbal y cumplían los criterios de Nueva York modificados20 para el diagnóstico de EA.
Desarrollo del estudio
El mismo reumatólogo evaluó a todos los pacientes. Se realizó una visita en la que se registraron variables demográficas y relacionadas con la enfermedad incluyendo edad, sexo, duración de la EA, valoración global de la enfermedad por el médico y el paciente en una escala visual analógica (EVA) de 0 a 10 (0 = muy bien; 10 = muy mal) y valoración del dolor por el paciente en una EVA de 0 a 10 (0 = ningún dolor; 10 = máximo dolor).
Se aplicó la versión en español del índice de actividad BASDAI (apéndice 1). El cuestionario consta de 6 preguntas referidas a los aspectos anteriormente indicados que se contestan sobre EVA de 0 a 10. En la versión original del instrumento, la puntuación se obtiene considerando las 2 preguntas referidas a rigidez como una sola (promedio de las puntuaciones de ambas) y entonces se calcula el promedio de las 5 puntuaciones parciales correspondientes a las 4 primeras preguntas y al promedio de las 2 preguntas sobre rigidez. En la versión española, a efectos de mayor simplicidad y siguiendo el sistema adoptado por algunos autores21, la puntuación final se ha calculado como el promedio de las puntuaciones de cada una de las 6 preguntas. Dicha puntuación puede estar entre 0 (ninguna actividad) y 10 (máxima actividad). También se aplicó la versión en español del índice funcional BASFI (Bath Ankylosing Spondylitis Functional Index) (de 0 a 10, de mejor a peor función física) (apéndice 2)22,23, el índice metrológico BASMI (Bath Ankylosing Spondylitis Metrology Index) (de 0 a 10, de mejor a peor metrología)24,25 y las versiones en español de los cuestionarios genéricos de calidad de vida relacionada con la salud (CVRS) SF-3626 y EuroQol27. La puntuación de cada uno de los 8 dominios del SF-36 se transformó a una escala de 0 a 10 (de mejor a peor CVRS). Esta transformación, puramente aritmética, se realizó con el objeto de unificar los valores de puntuación del SF-36 con los de las EVA, BASDAI, BASFI y BASMI. Se obtuvo una escala física global como el promedio de los dominios de función física, dolor y limitaciones en las actividades de la vida diaria, por problemas físicos. Análogamente, la escala mental global se calculó como el promedio de los dominios de limitaciones en actividades de la vida diaria por problemas emocionales, salud mental y energía/vitalidad. La puntuación global del SF-36 se calculó como el promedio de las puntuaciones de los 8 dominios. Con respecto al perfil de salud del EuroQol, cada uno de los 3 posibles niveles de respuesta de las 5 preguntas se puntuaron como 0, 1 y 2, y se obtuvo una puntuación global promedio entre 0 y 2 (de mejor a peor CVRS). La escala visual del EuroQol se transformó en una escala de 0 a 10 (de mejor a peor estado de salud), por los motivos ya explicados a propósito de los dominios del SF-36. Se midió la expansión torácica en cm.
Validación del BASDAI
La versión original en inglés fue traducida al español de manera independiente por 2 reumatólogos bilingües familiarizados con la validación de instrumentos. Posteriormente, se analizaron cuestiones semánticas y conceptuales y se acordó una versión unificada por consenso. Esta versión fue retrotraducida al inglés por un traductor que no conocía la versión original del cuestionario. Se compararon ambas versiones inglesas y se realizaron los cambios oportunos en la versión española para asegurar la equivalencia conceptual con la versión inglesa original. La fiabilidad incluyó la medición de la reproducibilidad y de la consistencia interna. La reproducibilidad se evaluó mediante prueba testretest realizada con un intervalo de 2 h en un subgrupo de pacientes seleccionados de manera aleatoria. Este intervalo, aunque probablemente sea demasiado corto, se escogió por razones de factibilidad y también para asegurar que la situación clínica de los pacientes fuese idéntica en la prueba test-retest. Para el estudio de validez se utilizaron como constructos la valoración global de la enfermedad por el médico y el paciente. Además, se utilizaron otros constructos representativos de la enfermedad que incluyeron la función física medida por el BASFI, el índice metrológico BASMI y la CVRS medida por el SF-36 y el EuroQol. La factibilidad se evaluó por el tiempo empleado por los pacientes en contestar el cuestionario y por su grado de comprensión, a juicio del investigador.
Análisis estadístico
Se realizó estadística descriptiva. Para estudiar la asociación del BASDAI con otras variables se realizó análisis de correlación y regresión simples. Para el análisis de correlación se utilizó el doble producto momento de Pearson, ya que la distribución de la mayoría de las variables fue gaussiana. Se construyó un modelo de regresión con el BASDAI como variable dependiente en el que las variables independientes fueron aquellas que presentaron asociación significativa con el BASDAI en el análisis univariado. El análisis de reproducibilidad test-retest se realizó mediante el coeficiente de correlación de Spearman, y la consistencia interna se estudió mediante el coeficiente alfa de Cronbach. Se consideró significativo un valor de p < 0,05, sin ajuste para comparaciones múltiples.
Resultados
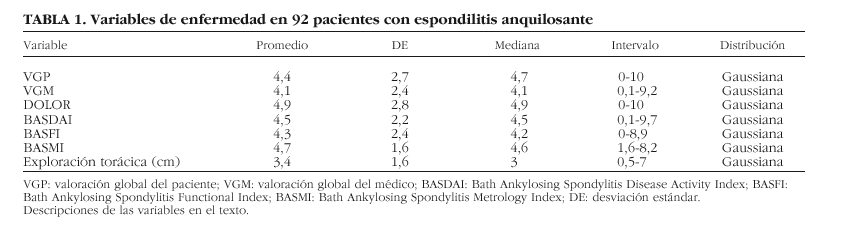
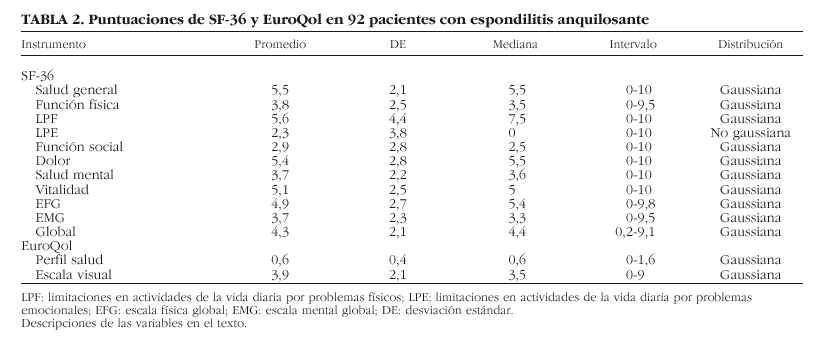
De los 130 pacientes miembros de EAS a los que se les envió la carta invitándoles a participar en el estudio, 92 respondieron afirmativamente y reunieron los criterios de inclusión. Fueron 69 varones (75%), con edad de 40,7 ± 9,1 años y duración de la enfermedad de 11 ± 7,8 años. Cincuenta y dos pacientes (56,5%) tenían afectación predominantemente axial y el resto (43,5%), de predominio periférico. El 57% de los pacientes tomaba antiinflamatorios no esteroideos en el momento de la realización del estudio, el 10% estaba en tratamiento con algún fármaco de segunda línea y el 55% recibía fisioterapia de forma habitual. En las tablas 1 y 2 se representan los valores de las principales variables de enfermedad y de los instrumentos de CVRS.
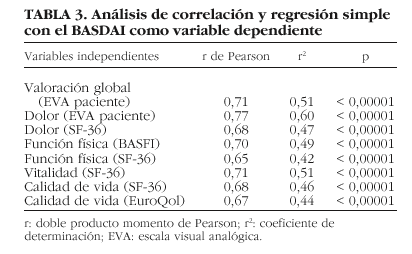
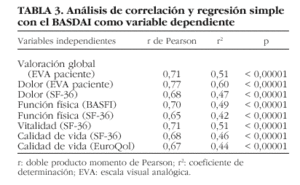
La puntuación del BASDAI mostró correlación estadísticamente significativa con r de Pearson mayores de 0,6 con la valoración global del paciente, la valoración del dolor por el paciente en EVA y medido por el SF-36, la función física medida por el BASFI y por el SF-36, la calidad de vida medida por el SF-36 y el EuroQol y la vitalidad medida por el SF-36. En la tabla 3 se muestra el análisis de correlación y regresión simple con el BASDAI como variable dependiente y con las variables citadas como independientes. El modelo de regresión que mejor explicó las variaciones en las puntuaciones del BASDAI fue el que incluyó, como variables independientes, la valoración global del paciente, la valoración del dolor por el paciente en EVA, el BASFI y la vitalidad medida por el SF-36 (tabla 4).
Las correlaciones del BASDAI con otras variables, aunque estadísticamente significativas, tuvieron r de Pearson menores de 0,6: son los casos de la valoración global del médico (r = 0,32, p < 0,002), la escala visual del EuroQol (r = 0,42, p < 0,0001) y el resto de dominios del SF-36 (con r entre 0,3 y 0,5). No encontramos correlación estadísticamente significativa con el BASMI, la expansión torácica, la edad y la duración de la enfermedad. No hubo diferencias significativas entre las puntuaciones del BASDAI en varones y mujeres.
El estudio de consistencia interna del BASDAI mostró un coeficiente alfa de Cronbach de 0,87. La reproducibilidad se evaluó mediante prueba testretest en 26 pacientes seleccionados de forma aleatoria. La correlación entre las 2 mediciones realizadas tuvo una rho de Spearman de 0,92, p < 0,00001. El tiempo empleado por los pacientes en responder el cuestionario fue de 60 s en promedio y la comprensión del mismo fue buena, a juicio del investigador.
Discusión
La definición de la actividad en EA es compleja y no está plenamente establecida. En el núcleo de medidas de desenlace propuesto por el grupo ASAS y por la reunión de expertos de OMERACT28,29 no figura como tal el dominio de la actividad pero sí algunos que pueden ser considerados sus componentes como: dolor, fatiga, rigidez matutina, reactantes de fase aguda, articulaciones inflamadas o entesopatía. Sin embargo, la inclusión de los 2 últimos citados en el concepto de actividad resulta problemática, ya que no serían adecuados en formas predominantemente axiales. Algunos estudios han evaluado la actividad de la enfermedad mediante las valoraciones globales del médico y el paciente, la valoración del dolor por el paciente y los reactantes de fase aguda30.
El BASDAI es un cuestionario que puede cumplimentarse de forma autoadministrada e incluye los principales componentes que se engloban en el concepto de actividad, valorados desde la perspectiva del paciente. Aunque no incorpora datos «duros» como pueden ser los reactantes de fase aguda ni la perspectiva del médico, por lo que podría ser considerado excesivamente subjetivo, hay varios hechos que apoyan su uso como instrumento para medir la actividad de la EA. En primer lugar, como ya se ha dicho, la versión original del instrumento ha demostrado excelentes propiedades clinimétricas1-3, por lo que puede considerarse que reúne las condiciones exigidas por OMERACT31 para los instrumentos de medida en el sentido de ser verdadero (válido), poseer capacidad discriminatoria (fiabilidad y sensibilidad al cambio) y factibilidad. En segundo lugar, el BASDAI ha demostrado una excelente correlación con los reactantes de fase aguda5,6,32. Y, por último, el buen funcionamiento del instrumento ha quedado patente con su utilización en numerosos estudios realizados en pacientes con EA, incluyendo los ensayos clínicos con terapias biológicas8-16.
De acuerdo a los resultados de este estudio, la versión en español del BASDAI demuestra validez de constructo y es fiable y factible de aplicar para medir la actividad de la enfermedad en pacientes con EA. Efectivamente, la versión española del instrumento demuestra buena correlación con diferentes constructos, algunos directamente relacionados con la actividad de la enfermedad como la valoración global del paciente, valoración del dolor por el paciente y la energía/vitalidad medida por el SF-36. Asimismo, la versión en español del BASDAI mostró una buena correlación con otros constructos representativos de otros aspectos de la enfermedad, que también pueden estar relacionados con la actividad de ésta como es el caso de la función física (medida por el BASFI y por el SF-36) o CVRS (medida por el SF-36 y el EuroQol). Precisamente, la valoración global del paciente, la valoracion del dolor por el paciente, la vitalidad medida por el SF-36 y la función física medida por el BASFI fueron las variables que mejor explicaron las variaciones en las puntuaciones del BASDAI. Por otra parte, no encontramos correlación entre el BASDAI y las medidas metrológicas incluidas en el índice BASMI (Schober, rotación cervical, distancia intermaleolar, distancia trago-pared y flexión lateral) ni con la expansión torácica. Esto puede explicarse teniendo en cuenta que la movilidad espinal y la actividad representan aspectos diferentes de la enfermedad. Por tales motivos, opinamos que estos hallazgos vienen a confirmar la validez del BASDAI. En este estudio, la correlación del BASDAI con la valoración global del médico fue pobre (r = 0,32). En este sentido, hay que recordar que dicho dominio no se incluye entre las principales medidas de desenlace recomendadas por ASAS y OMERACT para EA28,29.
El sistema de puntuación empleado en la versión española del BASDAI (promedio de las puntuaciones de las 6 preguntas) ha sido ya adoptado por otros autores21 y supone adjudicar a la rigidez un peso ligeramente superior a los demás componentes del BASDAI, en la puntuación global del instrumento. La rigidez espinal es, sin lugar a dudas, un síntoma capital en la EA y, de hecho, las 2 preguntas correspondientes del BASDAI se utilizan para medir el dominio de «inflamación» en los criterios de respuesta a corto plazo en la EA, elaborados por el grupo ASAS17. Por otro lado, los sistemas de puntuación de algunos instrumentos usados para medir la validez de constructo del BASDAI, en concreto el SF-36 y la escala visual del EuroQol, se modificaron ligeramente, pero únicamente de manera aritmética, por los motivos explicados en la sección «Métodos». En todo caso, esas modificaciones no afectan al objetivo de demostrar la validez de constructo del BASDAI. Asimismo, los resultados referidos a la correlación del BASDAI con las puntuaciones globales del SF-36 (física, mental, y global), aunque poco relevantes en nuestro estudio, deben ser tomados con cautela ya que el sentido biológico de obtener puntuaciones globales como medias aritméticas de diferentes dominios puede ser discutible.
Nuestro estudio también demuestra la fiabilidad de la versión española del BASDAI, con consistencia interna y reproducibilidad similares a las de la versión original1-3. El tiempo transcurrido entre la primera y segunda aplicación del BASDAI en la prueba test-retest fue, probablemente, demasiado corto. Ello se debió a cuestiones de factibilidad y también tuvo la finalidad de asegurar la equivalencia de la situación clínica del paciente entre la primera y la segunda aplicación del cuestionario. En todo caso, creemos que los resultados obtenidos, similares como se ha dicho a los de la versión original, son suficientemente sólidos para establecer la reproducibilidad de la versión española del BASDAI. Asimismo, los pacientes no tuvieron problemas de comprensión del cuestionario y el tiempo empleado en contestarlo fue muy bajo, lo que confirma su factibilidad de aplicación, no sólo en estudios de investigación, sino también en la práctica clínica diaria.
Este estudio tiene algunas limitaciones. En primer lugar, su diseño transversal no ha permitido estudiar la sensibilidad al cambio del instrumento. En todo caso, dada la similitud entre las propiedades métricas de la versión original y la española es esperable una buena sensibilidad al cambio del BASDAI español, que además se confirma en su aplicación a pa cientes españoles con EA en tratamiento con agentes biológicos (Hernández-Cruz B, Ariza-Ariza R, Navarro-Sarabia F, datos no publicados). En segundo lugar, en este estudio no se ha analizado la correlación del BASDAI con los reactantes de fase aguda; sin embargo, la buena asociación con otros constructos permite establecer la validez del instrumento para medir la actividad de la enfermedad. Por otro lado, la solidez de los datos de este estudio se apoya en el tamaño de la muestra, en el amplio espectro de nuestros pacientes que creemos representan adecuadamente a la población de pacientes con EA y, por último, en la consistencia de los resultados.
En definitiva, la versión española del BASDAI es un instrumento adecuado para medir la actividad de la enfermedad y se puede aplicar a pacientes españoles con EA.
Agradecimiento
Los autores desean agradecer a la Asociación de Espondilitis Anquilosante de Sevilla (EAS) y, en particular, a su presidente D. Jose Manuel Delgado Cordero, la valiosa colaboración prestada en la realización de este estudio.