Las recomendaciones del cribado de cáncer de cérvix en España incluyen la participación en programas de control de calidad externos a los laboratorios de citología. La Sociedad Española de Citología ha iniciado un programa de control de calidad de la citología ginecológica.
ObjetivoPresentar y discutir los resultados de la primera ronda del control de calidad de la Sociedad Española de Citología.
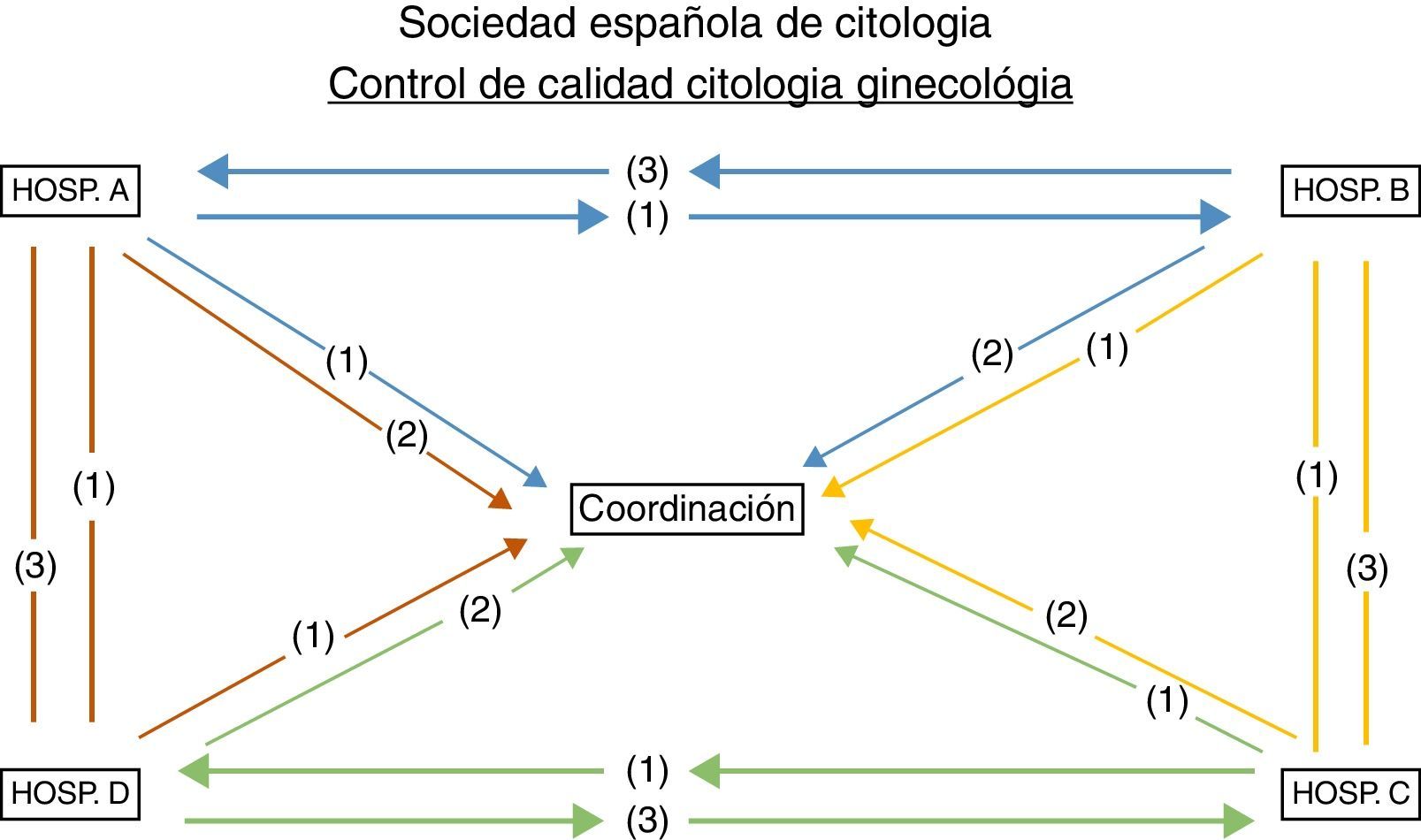
Material y métodoOrganización de los hospitales participantes según el tipo de citología. Intercambio de preparaciones de 50 casos entre los participantes: 10 negativos, 20 ASCUS-ASCH, 10 LSIL y 10 HSIL. Estudio de la correlación diagnóstica interobservador.
ResultadosTrece hospitales participantes: 6 en ThinPrep, 5 en triple toma y 2 en SurePath.
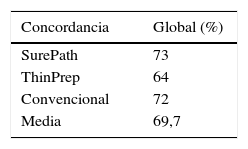
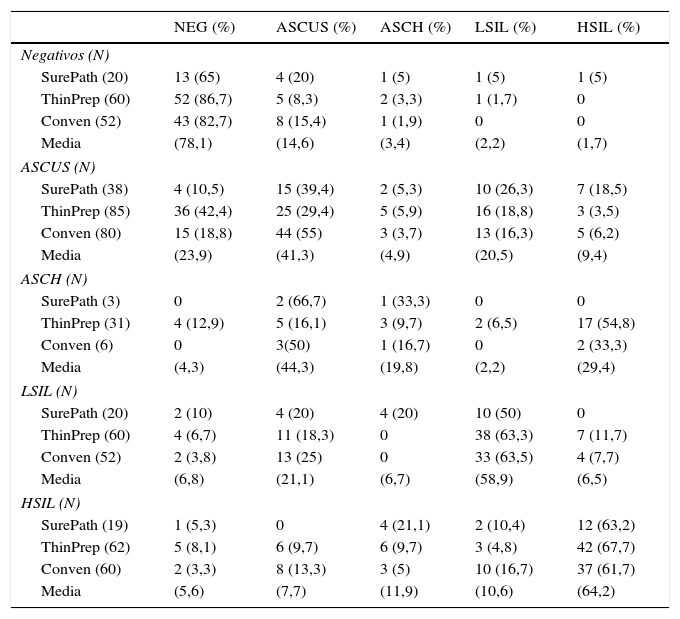
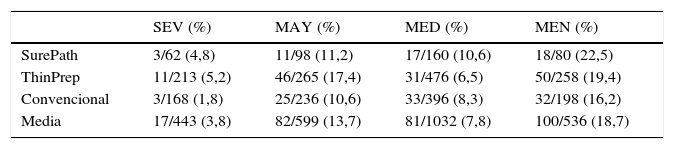
La concordancia global media fue del 69,7%. La concordancia media por tipo de lesión fue del 41,7%. La concordancia en negativos fue del 78,1%, en ASCUS del 41,3%, en LSIL de 58,9% y en HSIL del 64,2%. Los casos discordantes se diagnosticaban con mayor frecuencia como negativos, ASCUS y LSIL. Las discordancias severas (HSIL/ASCH versus negativo), alcanzaron un 3,8% de casos.
ConclusionesNuestros resultados son similares a los descritos en la literatura con muy escasas discordancias severas. El método de intercambio de laminillas utilizado no permite una formación continuada posterior, ya que no incluye la revisión de los casos con discordancias diagnósticas. Por ello, se contemplan correcciones metodológicas en sucesivas rondas.
The Spanish guidelines for cervical cancer screening recommend participating in external quality control programs. The Spanish Society of Cytology has started its own program of quality control for gynecological cytology.
AimTo describe and discuss the results of the first round of The Spanish Society of Cytology quality control for gynecological cytology.
Material and methodOrganization of participating hospitals on the basis of cytology type. Exchange of diagnostic slides from 50 cases among participants, as follows: 10 negative; 20 ASCUS-ASCH, 10 LSIL and 10 HSIL. Analysis of inter-observer correlation.
Results13 hospitals took part: 6 with ThinPrep liquid-based cytology, 5 with conventional cytology, and 2 with SurePath liquid-based cytology.
The global mean concordance was 69.7%. The mean concordance in the type of lesion was 41.7%. The concordance was 78.1% in negative diagnoses, 41.3%, in ASCUS, 58.9% in LSIL and 64.2% in HSIL The discordant cases were diagnosed more frequently as negative, ASCUS and LSIL. 3.8% of cases showed major discordances (HSIL or ASCH versus negatives).
ConclusionsOur results are similar to those reported in the literature, with very little severe discordance. The method of exchanging slides does not allows continuous training, since the review of discordant cases can not be made. Therefore, methodological corrections are contemplated for future rounds.
Artículo
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora