El síndrome compartimental agudo (SCA) o postraumático en el pie se asocia típicamente a mecanismos de alta energía, pies polifracturados, aplastamientos o atrapamientos. El diagnóstico y tratamiento precoz ante la sospecha de un SCA en un pie traumático ayudará a prevenir las secuelas de la necrosis mioneural. Aunque existen diversos métodos de monitorización de la presión compartimental, su diagnóstico es fundamentalmente clínico. La profilaxis es fundamental y el mejor tratamiento es prevenir el desarrollo de este síndrome. Para ello, es necesario de una correcta historia clínica y exploración inicial, con especial interés en dejar reflejada la exploración neurológica, vascular y muscular. La descompresión quirúrgica, mediante fasciotomías, debe ser urgente y será clave para evitar la instauración de graves secuelas. El retraso en el tratamiento puede tener consecuencias desastrosas, como la contractura, parálisis o infección, que en ocasiones pueden requerir la amputación.
Acute and post-traumatic compartment syndrome of the foot is typically associated with mechanisms of high-energy, multiple foot fractures, particularly those caused by crushing or trapping. Early diagnosis and treatment in view of the suspicion of an acute compartment syndrome in a traumatic foot will help prevent the effects of myoneural necrosis. Even though there are various methods of compartment pressure monitoring, the diagnosis is mainly clinical. Prophylaxis is essential and the best treatment is to prevent the development of this syndrome. To achieve this a correct clinical history and initial examination is needed, with special care in the nerve, vascular and muscle evaluation. Surgical decompression using fasciotomy must be urgent and will be mandatory to prevent the severe sequelae. Delayed treatment can have disastrous consequences, such as contracture and paralysis, infection, and sometimes amputation.
En 1881, Richard von Volkman realizó la primera descripción del síndrome compartimental con especial interés en las repercusiones sistémicas y funcionales en la extremidad. Describió las contracturas causadas por los vendajes constrictivos del antebrazo y de la mano, a los cuales consideró de carácter isquémico por la obstrucción prolongada de la sangre arterial. Más tarde, en 1911, Bardenheuer describe la etología del síndrome compartimental agudo (SCA), similar a la actual. Pero no es hasta 1940, durante la Segunda Guerra Mundial, cuando se generaliza la aplicación clínica de la fasciotomía para el tratamiento de lesiones en el campo de batalla.
Matsen, en 1975 definió el síndrome compartimental como el aumento de presión en un espacio osteofibroso cerrado que ocasiona la reducción del flujo sanguíneo y la perfusión tisular del mismo, lo que ocasiona dolor isquémico y puede lesionar los tejidos en el interior del compartimento1,2.
El síndrome compartimental puede ser agudo o crónico.
Los síndromes crónicos o post-ejercicio suelen ser recidivantes y se asocian a una actividad física o deportiva repetida. Las localizaciones en el pie son inusuales3. Clínicamente se caracteriza por dolor localizado en el compartimento muscular afectado, que puede asociarse a dolor neurítico o déficit neurológico irradiado por el territorio de los nervios que lo atraviesan. Estos síntomas patognomónicamente son desencadenados por el ejercicio y remiten al poco tiempo de suspender el mismo. El proceso fisiopatológico puede ser explicado por varias teorías. Una de ellas indica que la asociación de la hipertrofia muscular en el compartimento y el aumento del volumen puntual causado por el incremento del flujo sanguíneo motivado por el ejercicio, impedirían el retorno venoso aumentando, como consecuencia, el volumen sanguíneo en el compartimento, y provocando una aumento de presión intracompartimental. Esta presión intracompartimental podría continuar aumentando hasta superar a la presión de perfusión arterial, lo que impediría el aporte de oxígeno a los tejidos provocando su hipoxia. Al cesar la práctica deportiva, se disminuiría el volumen sanguíneo muscular y con éste la presión intracompartimental, revertiéndose el proceso etiológico.
El SCA o postraumático en el pie se asocia típicamente a mecanismos de alta energía, pies polifracturados, particularmente cuando han sufrido aplastamiento o atrapamiento4.
La patogénesis y el tratamiento de los síndromes compartimentales agudos en las extremidades son bien conocidos y como consecuencia de la duración y magnitud del aumento de presión intersticial se producirá una necrosis de los tejidos con alteración de la función mioneural.
Anatomía de los compartimentos del pieClásicamente se han distinguido 4 compartimentos que contienen masas musculares: interóseo (músculos intrínsecos entre 1.° y 5.° metatarsianos y nervios digitales), medial (abductor del hallux y flexor corto del hallux), central (flexor corto de los dedos, cuadrado plantar y aductor del hallux) y compartimento lateral (flexor corto 5.° dedo y abductor del quinto dedo). Manoli y Weber4,5, en un estudio anatómico con especial referencia a la descompresión del compartimento calcáneo, identifican 9 compartimentos en el pie: el medial y el lateral son iguales a los descritos anteriormente, en el central distinguen un compartimento superficial que contiene el flexor corto de los dedos y otro profundo en retropié o compartimento calcáneo que contiene el músculo cuadrado plantar, el nervio plantar lateral, el paquete neurovascular tibial posterior y el tendón del flexor hallucis longus. Finalmente, en el antepié existen 4 compartimentos interóseos y el del aductor del hallux.
EtiologíaLas causas que pueden producir un SCA son diversas. Las más frecuentes son las fracturas (abiertas o cerradas), traumatismos por aplastamiento o atrapamiento, yesos o vendajes demasiado apretados, escaras circunferenciales por quemaduras, etc.
Mubarak et al6 engloban las causas del SCA en dos grandes grupos:
- 1.
Las que provocan una disminución del compartimento:
- a.
Vendajes o yesos muy constreñidos.
- b.
Quemaduras y congelaciones que producen escaras circunferenciales inelásticas.
- c.
Cierres quirúrgicos a tensión.
- d.
Aplastamiento.
- a.
- 2.
Las que provocan un aumento del contenido del compartimento:
- a.
Edema post-isquemia: lesión arterial, tromboembolismo arterial, reimplante de miembros, excesivo tiempo de isquemia, cateterismo arterial, ergotamina.
- b.
Hematoma primitivo: hemofilia, tratamiento anticoagulante.
- c.
Hemorragias intracompartimentales: fracturas, osteotomías.
- d.
Mordedura de serpiente, venenos.
- a.
En el pie son frecuentes los síndromes compartimentales tras fracturas-luxaciones de Lisfranc o metatarsianos y en las fracturas de calcáneo7, describiéndose hasta en un 10% de los casos. También se han descrito causas no traumáticas como hemangiomas8.
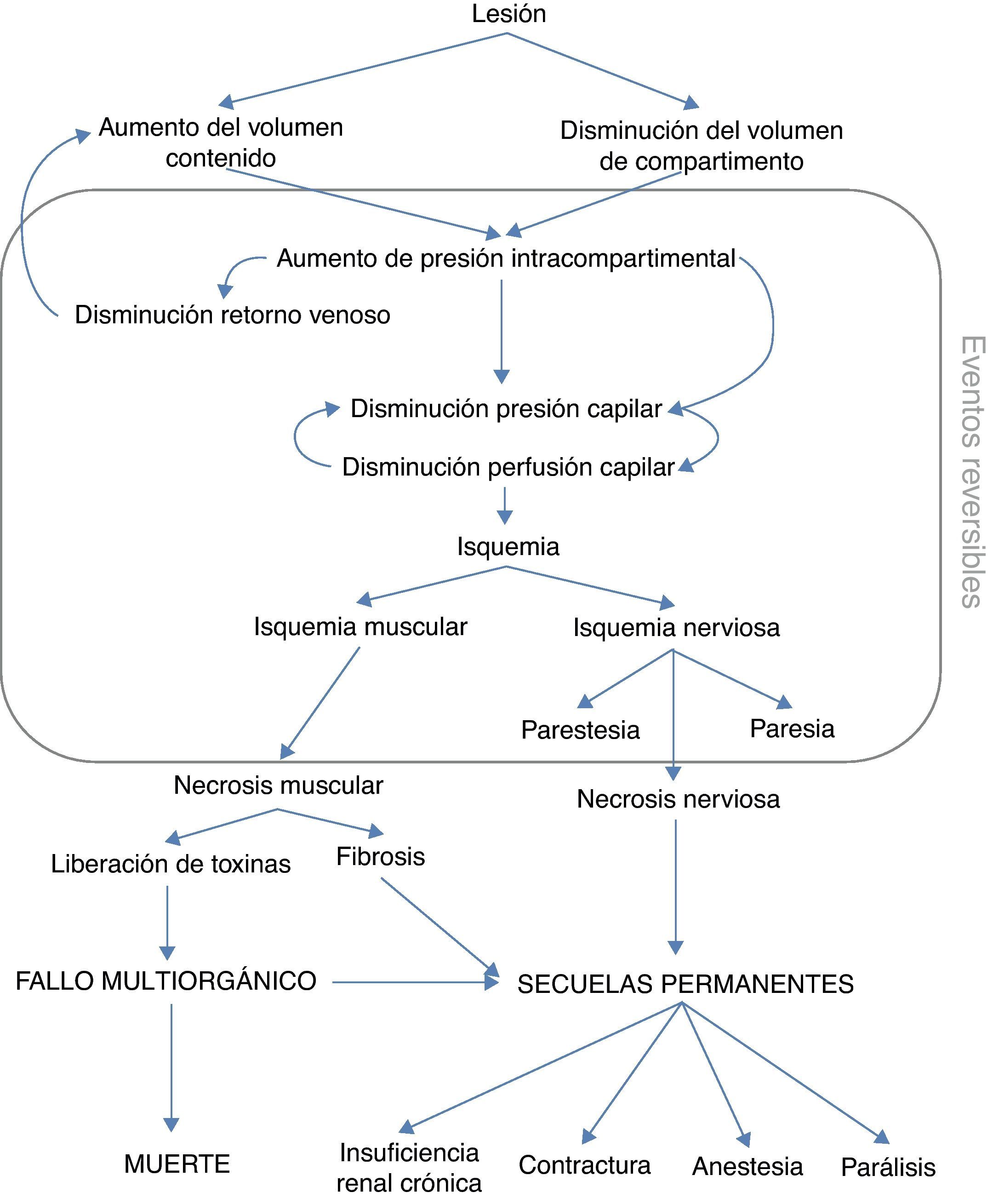
Fisiopatología del síndrome compartimentalEl SCA se caracteriza por un aumento de presión intracompartimental que puede estar provocada por múltiples causas y esto desencadena diversas lesiones (fig. 1).
El aumento de la presión intracompartimental provoca una disminución de la presión y perfusión capilar lo que conlleva a una isquemia muscular y nerviosa. Si el mecanismo lesivo continúa actuando llegará a una necrosis nerviosa y muscular.
La necrosis nerviosa ocasiona parestesias que conducirán a una anestesia total y/o paresias que llevarán a una parálisis.
La necrosis muscular provoca una degeneración de las fibras musculares que son sustituidas por tejido fibroso inelástico que ocasionará una contractura.
Además de los efectos locales sobre el miembro, el SCA puede producir efectos generales. Así, la isquemia muscular puede hacer que las células musculares dañadas liberen mioglobina. Durante la re-perfusión, la mioglobina pasará a la circulación junto a otros metabolitos inflamatorios y tóxicos. La liberación de toxinas por la destrucción celular puede provocar un fallo multiorgánico y poner en peligro la vida del paciente. El desarrollo y la extensión de los efectos sistémicos dependerán de la intensidad y duración de la afectación de la perfusión tisular, y del tamaño y número de compartimentos musculares implicados.
ClínicaEl síntoma fundamental es el dolor. Aparece pocas horas tras la lesión. Es un dolor intenso, excesivo o mayor de lo que cabría esperar, y que se incrementa con la extensión pasiva de los músculos afectos1,2,15.
El dolor se acompaña de tensión en la zona, hinchazón y alteraciones sensitivas distales.
Clásicamente, las manifestaciones clínicas se describen como las 6 «P» (por sus siglas en inglés)9,10:
Parestesias (Paresthesias)Es el primer síntoma en aparecer, sin embargo es difícil de interpretar y puede deberse a una isquemia muscular, nerviosa, un fenómeno antiálgico o una combinación de los tres. Sin tratamiento progresarán hacia la hipoestesia o anestesia.
Dolor (Pain)Fuera de proporción al tipo de lesión, se exacerba por movimiento pasivo o por compresión directa del compartimento afectado, descrito como punzante o profundo, localizado o difuso, se incrementa con la elevación de la extremidad, no cede con analgésicos. Sin embargo puede ser un indicador no fiable en síndromes compartimentales establecidos o en pacientes con déficit neurológico central o periférico añadido, ya que puede estar ausente.
Presión (Pressure)Dureza a la palpación el compartimento, que está tenso y caliente, y la piel tensa y brillante. Es el signo más precoz.
Palidez (Pallor)Es un signo tardío. La piel está fría y acartonada, y el llenado capilar es prolongado (> 3 segundos). Su aparición es rara, ocurriendo cuando el flujo arterial está muy disminuido.
Parálisis (Paralysis)Signo tardío, movimiento débil o ausente de las articulaciones dístales, ausencia de respuesta a la estimulación neurológica directa (daño mioneural irreversible).
Ausencia de pulsos (Pulselessness)Los pulsos periféricos son palpables a menos que exista una lesión arterial. La ausencia es un signo tardío, verificado clínicamente por palpación y ausencia de doppler audible.
Es de suma importancia tener en cuenta que la presencia de estas 6 P son signos y síntomas de un cuadro establecido por lo que no hay que esperar a la presencia de los mismos para el diagnóstico.
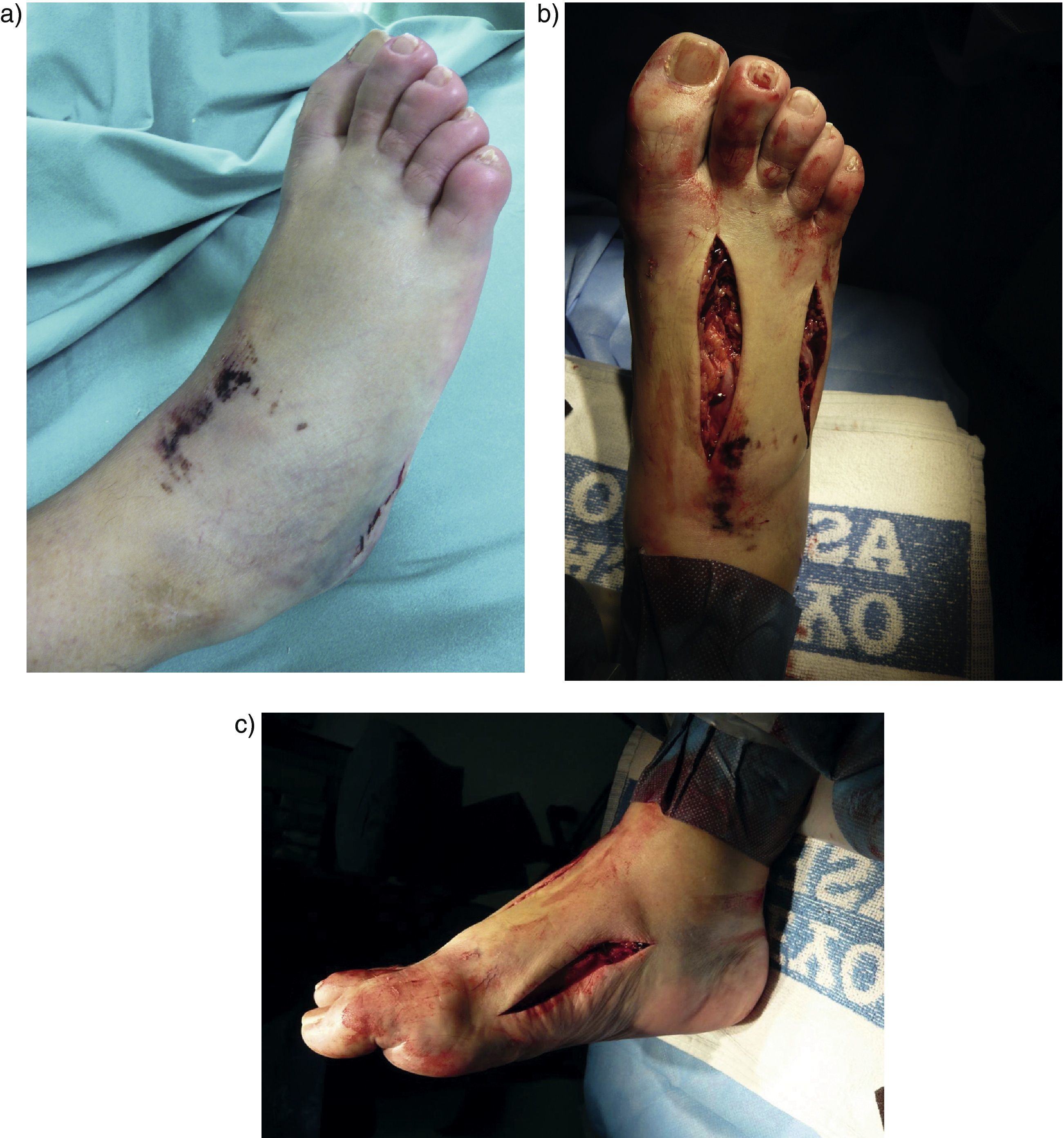
DiagnósticoPara diagnosticar el síndrome compartimental es fundamental pensar en él y realizar exploraciones seriadas. El diagnóstico clínico en el pie se sospecha cuando hay una tumefacción intensa tras un traumatismo (fig. 2a), pero resulta difícil diferenciar cual es el compartimento afectado, debiéndose evaluar minuciosamente la sensibilidad de los mismos.
Es muy importante destacar, que en estos pacientes hay un antecedente de fractura, traumatismo o cirugía ortopédica reciente, o bien de otra causa desencadenante del cuadro.
El diagnóstico es básicamente por la clínica y la exploración física. Pero en ocasiones el cuadro clínico puede ser dudoso o la exploración equívoca o difícil de realizar. En estos casos debe medirse la presión intracompartimental.
Para la medición de la presión compartimental existen diferentes métodos11,12, siendo los más utilizados los monitores de presión conectados a un catéter o los dispositivos portátiles de fácil manejo y precisión.
Una presión intracompartimental inferior a 10mmHg se considera normal. Las parestesias comienzan a aparecer entre los 20-30mmHg. Si la presión es menor de 30mmHg deberá vigilarse con monitorización continua o exámenes seriados en las siguientes 24 horas (período de mayor riesgo). Aunque no existe un consenso exacto entre los autores de cuándo realizar la descompresión quirúrgica, se considera que las presiones por encima de 30-40mmHg, o diferencias inferiores a 30mmHg entre la presión compartimental y la presión diastólica son indicación de fasciotomía. Si las presiones por encima 40mmHg se mantienen durante 8 horas se producen lesiones titulares irreversibles13–16.
Existen indicaciones aceptadas para el registro de la presión compartimental1,10:
- -
Uno o más síntomas de síndrome compartimental junto a factores de confusión.
- -
Presencia de dureza o inflamación de una extremidad en paciente al que se le ha practicado anestesia regional en el postoperatorio.
- -
Exploración no fiable en presencia de dureza o inflamación de la extremidad
- -
Hipotensión prolongada en una extremidad inflamada de dudosa dureza.
- -
Aumento espontáneo de dolor en una extremidad tras un tratamiento adecuado de dolor.
Algunas pruebas de laboratorio pueden contribuir al diagnóstico del síndrome compartimental. La elevación de la creatinfosfoquinasa (CPK) refleja la necrosis muscular, y la descompresión del compartimento mostrará una tendencia descendente. Una persistencia de cifras elevadas es indicativa de que sigue produciéndose necrosis muscular y orienta hacia una descompresión insuficiente. La mioglobinuria también confirma la lisis de las células musculares. La mioglobina es tóxica para el glomérulo renal por lo que, si el síndrome compartimental no se trata adecuadamente, producirá insuficiencia renal2,10.
TratamientoLa fasciotomía es el tratamiento de elección. El único método fiable de tratamiento de un SCA instaurado es la descompresión quirúrgica mediante fasciotomías. Se acepta por la mayoría de autores1,2,4,10,16,17, que valores superiores a 30mmHg en la presión intracompartimental o diferencias entre la presión compartimental y la presión diastólica inferiores a 30mmHg son indicativas de fasciotomía. Ante la duda y con clínica sugestiva de que pueda evolucionar a un síndrome compartimental, somos partidarios de la fasciotomía descompresiva. Por otra parte, es aconsejable la fasciotomia profiláctica sistemáticamente en casos de fracturas complejas de extremidades, traumatismos por aplastamiento, reimplante de extremidades o lesiones neurovasculares. Además del tratamiento descompresivo local, es imprescindible una hiperhidratación del paciente que ayudará a evitar la lesión de los glomérulos renales por depósito de mioblobina y metabolitos tóxicos.
En el pie, los abordajes para la descompresión se realizarán generalmente mediante dos incisiones longitudinales dorsales localizadas entre 1.° y 2.° y entre 4.° y 5.° metatarsianos, para acceder a los compartimentos del antepié (fig. 2b), y una incisión medial (fig. 2c) para la descompresión de los compartimentos calcáneo, medial, superficial y lateral, aunque a través de los abordajes dorsales también se puede acceder al compartimento lateral y superficial10,15–17. La fasciotomía comprende la incisión de la envoltura aponeurótica del compartimento, lo que permite que los tejidos se expandan sin restricciones y que la presión tisular caiga. Al practicar la fasciotomía, no sólo debe abrirse rápidamente la envoltura aponeurótica del compartimento, sino también debe abrirse la piel y tejido subcutáneo suprayacente para que los compartimentos puedan descomprimirse adecuadamente. La descompresión en un SCA no debe realizarse mediante miniincisiones o de forma percutánea. Tras la incisión debe procederse a la disección cuidadosa de todos los compartimentos, con evacuación de los hematomas retenidos, vigilando no lesionar estructuras nobles. Se debe comprobar que no existan sangrados que puedan volver a causar compresión de estructuras y debe valorarse la perfusión distal y el estado muscular. Se estabilizarán las fracturas y finalmente las heridas se dejarán abiertas sin cierre de fascias ni piel. Los puntos de aproximación de bordes que atraviesan transversalmente las heridas pueden producir decúbitos e isquemias sobre el tejido muscular, por lo que son poco recomendables. Es preferible evitarlos o colocar algún punto de sutura sin apretar y que una cada borde de la herida con la fascia o músculo subyacente. Aplicaremos sobre las heridas un apósito con gasa impregnada de pomada con sulfadiacina argéntica o nitrofurazona, que desbridan y favorecen la granulación, además de protección antibacteriana.
Tras la fasciotomía es recomendable la vigilancia estricta. Deben realizarse curas de las heridas y cambio de apósitos diariamente. En cuanto al tratamiento posterior, se siguen los principios del tratamiento primario: valorar la viabilidad del músculo, extirpar el músculo necrótico y dejar las heridas abiertas. Las fracturas deberán estabilizarse mediante fijación interna o externa. La estabilización facilita el cuidado de las heridas y permite la movilización del paciente y de las articulaciones, con lo que se reduce la aparición de fibrosis y rigidez articular. A las 24-48h se debe revisar para comprobar si se ha producido más necrosis y si precisa nueva limpieza quirúrgica18–20.
No se debe realizar el cierre de la herida hasta que se haya desbridado todo el tejido necrótico. El tipo de cierre vendrá condicionado por la naturaleza de la herida abierta. Si en la evolución posterior pueden aproximarse sin tensión los bordes de la herida se procederá al cierre primario diferido del subcutáneo y piel. Si los bordes no pueden aproximarse y hay un buen tejido de granulación, sin exposición de vasos ni nervios ni tejido óseo, se realiza cobertura mediante un injerto libre de piel. En caso de exposición ósea o tejidos nobles será necesaria la cobertura con un colgajo o con un injerto libre fasciocutáneo microvascular. Se ha comprobado la utilidad del uso de la terapia de cierre por vacío tras las fasciotomías, ayudando a una rápida resolución de la inflamación y edema de los tejidos, al mejorar el aporte local de sangre, promover la granulación del tejido e impedir la colonización bacteriana21.
Finalmente, algunos autores22 utilizan la terapia con oxígeno hiperbárico en pacientes con lesiones por aplastamiento o síndromes compartimentales precoces, pues parece que dicha terapia disminuye el riesgo de necrosis tardía e isquemia secundaria al aumentar la liberación de oxígeno en los tejidos, disminuir el edema y aumentar la función leucocitaria. Sin embargo, no queda claro cual es el momento óptimo para llevar a cabo dicha terapia ni la dosis adecuada.
El diagnóstico precoz del SCA es de suma importancia, por lo que se debe pensar en él. La profilaxis es fundamental y el mejor tratamiento es prevenir el desarrollo del SCA. Para ello es necesario de una correcta historia clínica y exploración inicial, con especial interés en dejar reflejada la exploración nerviosa, vascular y muscular.
Así mismo, la reducción y fijación correcta de las fracturas sin mucha manipulación, y la correcta colocación de vendajes y yesos, son esenciales para no agravar la lesión y evitar el compromiso compartimental.
En lesiones que puedan evolucionar con un SCA deberemos estar alerta e instaurar un control clínico periódico y estricto (dolor, movilidad, sensibilidad, pulsos, edema) junto con la monitorización de la presión intracompartimental.
El retraso en el tratamiento puede tener consecuencias desastrosas, como la contractura y parálisis, la infección y en ocasiones la amputación.
Debemos evitar cierres a tensión en casos de cirugía abierta y somos partidarios de la apertura profiláctica de compartimentos en cirugía del pie politraumático.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Nivel de evidenciaNivel de evidencia V.