En la práctica clínica de muchos reumatólogos y en algunos ensayos clínicos se ha usado colchicina en pacientes con osteoartritis primaria. A pesar de ello, su papel en el tratamiento de la misma no está claro y las guías no establecen recomendaciones al respecto.
ObjetivosEvaluar la eficacia y la seguridad del tratamiento con colchicina en pacientes adultos con osteoartritis de rodilla, tanto primaria como asociada al depósito de cristales de pirofosfato cálcico.
MétodosSe llevó a cabo una búsqueda estructurada de la literatura utilizando las bases de datos Pubmed, Embase, Cochrane Controlled Trials Register y LILACS. Se incluyeron ensayos clínicos controlados, aleatorizados, en donde se haya usado colchicina como intervención en pacientes adultos con osteoartritis de rodilla, primaria o relacionada con pirofosfato de calcio.
ResultadosSe incluyeron 5 ensayos clínicos controlados. Se observó una tendencia común en todos los estimados puntuales de los artículos a favorecer el uso de la colchicina para la mejoría del dolor y de la funcionalidad. Se observó una mayor tendencia de efectos adversos gastrointestinales con el uso de la colchicina, sin embargo, el efecto no fue estadísticamente significativo en los estudios individuales. Ninguno de los estudios evaluó calidad de vida.
ConclusionesLa colchicina parece ser una alternativa eficaz y segura para el tratamiento de pacientes adultos con osteoartritis de rodilla, tanto primaria como asociada al depósito de cristales de pirofosfato de calcio. Su uso reduce el dolor y mejora la funcionalidad, aunque puede producir síntomas gastrointestinales en algunos pacientes.
Colchicine is often used in patients with osteoarthritis in which calcium pyrophosphate crystal deposition disease is suspected. Colchicine has also been used by many rheumatologists in clinical practice, and in some trials, on patients with primary osteoarthritis (apparently unrelated to calcium pyrophosphate). However, its role in the treatment of primary osteoarthritis is not clear, and international guidelines have not established recommendations.
ObjectiveTo evaluate the efficacy and safety of colchicine for the treatment of adult patients with primary knee osteoarthritis as well as the form associated with calcium pyrophosphate.
MethodsA structured literature search was conducted using the PubMed, Embase, Cochrane Controlled Trials Register, and LILACS databases. Randomised controlled trials were included in which colchicine was used as intervention in patients with primary or pyrophosphate calcium-associated knee osteoarthritis.
ResultsThe study included 5 randomised controlled trials, all of which showed a common trend in all estimated points of the joint, favouring the use of colchicine for improvement in pain and functionality. Although the effect was not statistically significant in individual studies, there was a greater tendency of gastrointestinal adverse effects with the use of colchicine. None of the studies assessed quality of life.
ConclusionsColchicine appears to be an effective and safe alternative for treatment of adult patients with knee osteoarthritis, either primary or associated with the deposit of calcium pyrophosphate crystals. Its use reduces pain and improves functionality, but it can cause gastrointestinal symptoms in some patients.
La osteoartritis es una enfermedad crónica altamente prevalente que está asociada con mucho dolor y discapacidad funcional1. Es una condición frustrante desde el punto de vista médico, para la cual se han intentado múltiples intervenciones farmacológicas y no farmacológicas. La práctica habitual es usar analgésicos únicos o en combinación, especialmente antiinflamatorios no esteroideos, acetaminofén en altas dosis y opioides débiles, todos los cuales presentan riesgos de efectos adversos potencialmente serios, en especial en los adultos mayores2,3.
La osteoartritis es la forma más común de patología articular. El término osteoartritis posiblemente más que representar una enfermedad puede ser la vía final común de una gran variedad de condiciones con diferentes etiologías, pero con expresión morfológica y desenlaces clínicos similares. Aunque las clasificaciones de la osteoartritis en primaria y secundaria podrían ser útiles en cuidado primario y en investigación, tales distinciones son artificiales e ignoran el escenario más común de etiologías superpuestas en un mismo paciente4.
Aunque la inflamación sinovial dentro de las articulaciones afectadas por osteoartritis es frecuentemente menos intensa que en las artritis inflamatorias tradicionales (artritis reumatoide, gota, etc.), la activación de respuestas inflamatorias también ocurre en articulaciones con osteoartritis, tanto en los sinoviocitos como en los condrocitos. El cartílago anormal puede contener una gran variedad de cristales de calcio, especialmente pirofosfato de calcio, que estimulan múltiples mecanismos intracelulares de inflamación. Se puede demostrar la presencia de cristales hasta en el 70% de los especímenes de líquido sinovial de los pacientes con osteoartritis5.
Un interesante fenómeno frecuentemente observado dentro de los tejidos articulares degenerados es el depósito de cristales inorgánicos. La seudogota por pirofosfato está fuertemente asociada con la degeneración del cartílago vista en osteoartritis, y puede ser detectada en radiografías o a través del estudio del líquido sinovial. En general, la causa y la consecuencia de la presencia de condrocalcinosis en osteoartritis continúan siendo ambiguas, ya que es difícil establecer qué ocurrió primero: la degradación celular y de la matriz o la formación de los cristales. Lo más probable es que ellas se promuevan entre sí y que el trastorno metabólico conduzca a daño celular y viceversa6,7. La osteoartritis y el envejecimiento se encuentran fuertemente asociados con la artropatía por pirofosfato de calcio7,8. La fuerte interrelación existente entre los cristales de pirofosfato y la osteoartritis ha llevado a muchos a considerar a la artropatía por pirofosfato simplemente como un subgrupo dentro de las osteoartritis9.
Al igual que en la osteoartritis clasificada como primaria, en aquella asociada con pirofosfato de calcio los pacientes afectados son principalmente mujeres ancianas, siendo la rodilla el sitio más frecuentemente involucrado9. La artropatía asociada con cristales de pirofosfato de calcio puede estar asociada con características un poco más inflamatorias tales como mayor dolor, rigidez, derrame articular y discapacidad, sin embargo, tales asociaciones son marginales y no resultan útiles para el diagnóstico. Si existen o no diferencias significativas en los síntomas, la distribución articular o los desenlaces clínicos entre los pacientes con osteoartritis con o sin pirofosfato de calcio asociado requieren estudios adicionales7.
Debido a que en los pacientes clasificados con osteoartritis primaria se demuestran cristales de pirofosfato de calcio8 y de ácido úrico, así como activación del sistema inmune innato10, se encuentra soporte para la extrapolación del uso de la colchicina. Este medicamento presenta múltiples mecanismos de acción que conducen a la atenuación de diversas vías inflamatorias y modulan la inmunidad innata. Adicionalmente, se ha demostrado que posee propiedades antifibróticas y efectos diversos sobre la función endotelial11.
Las mismas modalidades de tratamiento para mejorar el dolor y los síntomas en osteoartritis primaria se usan frecuentemente en pacientes con osteoartritis relacionada con pirofosfato de calcio. Usualmente se usa colchicina en pacientes con osteoartritis en los cuales, además, se sospecha la presencia de artropatía por cristales de pirofosfato de calcio12. Sin embargo, en la práctica clínica de muchos reumatólogos y en algunos ensayos clínicos, también se ha usado en pacientes con osteoartritis primaria (aparentemente no relacionada con pirofosfato de calcio). A pesar de ello, su papel en el tratamiento de la osteoartritis primaria no está claro y las guías internacionales no establecen recomendaciones al respecto3. En general, la evidencia que soporta el uso de la colchicina en ambas formas de osteoartritis no ha sido revisada hasta la fecha de manera sistemática3,12.
Se hizo una revisión sistemática de la literatura sobre la eficacia y la seguridad del tratamiento con colchicina en pacientes con osteoartritis, tanto primaria como asociada al depósito de pirofosfato de calcio, para establecer su utilidad y que permita actualizar las guías existentes, para poder beneficiar a un mayor número de pacientes con esta intervención económica y potencialmente favorable. Según nuestro conocimiento esta es la primera revisión sistemática de la literatura que se ha realizado sobre este tema. Para llevar a cabo este trabajo se siguieron las recomendaciones PRISMA13 para el reporte de revisiones sistemáticas que evalúan intervenciones en salud.
ObjetivoEvaluar la eficacia y la seguridad del tratamiento con colchicina administrada por vía oral comparado contra placebo o control activo en pacientes adultos con osteoartritis de rodilla diagnosticada según los criterios del Colegio Americano de Reumatología14, con sospecha o no de estar asociada con enfermedad por cristales de pirofosfato de calcio, para la reducción del dolor y la mejoría de la funcionalidad, evaluados al menos un mes después del tratamiento, así como de sus efectos adversos (principalmente diarrea) y calidad de vida, mediante la evaluación de ensayos clínicos controlados, aleatorizados de brazos paralelos.
MétodosProtocolo y registroPara llevar a cabo la presente revisión no se realizó el registro del protocolo.
Criterios de elegibilidadSe incluyeron ensayos clínicos controlados, aleatorizados, en texto completo o en resumen, publicados o no, que usaran colchicina en cualquier dosis y esquema, como intervención en pacientes adultos mayores de 18 años, de cualquier sexo, con osteoartritis de rodilla, primaria o relacionada con el depósito de pirofosfato de calcio, que tuvieran un grupo de control activo o control con placebo y que evaluaran dolor o funcionalidad con un seguimiento mínimo de un mes. No hubo restricción por idioma, por año ni por estado de la publicación.
Fuentes de la informaciónSe llevó a cabo una búsqueda estructurada de la literatura utilizando las bases de datos bibliográficas electrónicas Pubmed, Embase, Cochrane Central Register of Controlled Trials (CENTRAL) y LILACS con las palabras clave «colchicine» y «osteoarthritis» que son términos Mesh, además de las palabras clave «osteoarthrosis», «osteoartritis», «osteoartrosis» y «artrosis». La estrategia exacta de búsqueda en Pubmed se reporta en el anexo 1. Se hicieron búsquedas adicionales en Google y en Google Scholar. También se realizó búsqueda manual dentro de las listas de referencias de los artículos obtenidos y se contactaron a algunos de los autores de los estudios encontrados para tratar de obtener referencias adicionales.
Selección de los estudiosLos 2 autores realizaron en forma independiente la selección de los artículos que cumplían los criterios de elegibilidad establecidos por medio de la lectura de los títulos y los resúmenes de los artículos obtenidos en las diferentes búsquedas. En algunas ocasiones fue necesario revisar el texto completo para determinar la inclusión o no de la referencia identificada. Los desacuerdos entre los autores en la selección de los estudios fueron resueltos mediante consenso.
Proceso de extracción de la informaciónSe diseñó un formato para la extracción estandarizada de la información. Los 2 autores extrajeron la información de los estudios finalmente incluidos. Los desacuerdos entre los autores con respecto a la información obtenida se resolvieron por consenso revisando las fuentes originales.
Ítems de la información extraídaLa información extraída de cada estudio fue: primer autor, país de realización del estudio, año de publicación; la población incluida fue caracterizada por medio del número total de participantes, el promedio de edad, la distribución por sexos, los criterios diagnósticos, la gravedad de la enfermedad, la proporción de pacientes con probable osteoartrosis primaria y probable osteoartrosis asociada con pirofosfato de calcio, el número de pacientes asignados a cada grupo y el número final de participantes, además de los criterios de exclusión; el tratamiento recibido por el grupo de intervención y el grupo control con respecto a la dosis y la vía de administración; además de la escala usada y el efecto observado en cada grupo con respecto a los desenlaces dolor, funcionalidad, calidad de vida, diarrea y otros efectos adversos.
Riesgo de sesgos dentro de los estudios individualesLos 2 autores en forma independiente evaluaron el riesgo de sesgo de cada uno de los artículos incluidos teniendo en cuenta las recomendaciones de la colaboración Cochrane mediante el uso de la herramienta RevMan 5.3, considerando específicamente el uso de un método adecuado de asignación aleatoria, la ocultación de la secuencia de aleatorización, el cegamiento de los participantes, el sesgo de ejecución, el sesgo de medición, el sesgo de notificación, el sesgo de deserción y otros sesgos. Además, se realizó una evaluación global de la calidad del conjunto de la evidencia utilizando el enfoque GRADE15.
Medidas de resumenLa medida resumen que se utilizó fue el OR con el método de Mantel-Haenszel bajo un modelo de efectos aleatorios, para medir los efectos observados con la intervención en los desenlaces mejoría de al menos un 30% en las escalas del dolor y funcionalidad, y en la aparición de diarrea.
Riesgo de sesgos a través de los estudiosEl sesgo de publicación fue evaluado mediante la inspección visual de un gráfico de embudo, el cual toma en cuenta el tamaño del efecto contra el inverso de la varianza. Buscamos la presencia de asimetría en el gráfico de embudo que sugiriera la posibilidad de que estudios pequeños con resultados negativos no hubieran sido publicados, teniendo en cuenta, sin embargo, que existen causas de asimetría diferentes al sesgo de publicación.
Análisis adicionalesPreespecificamos un análisis de subgrupos para evaluar la intervención en un subgrupo de osteoartritis de rodilla primaria y un subgrupo de osteoartritis de rodilla asociada con depósito de cristales de pirofosfato de calcio.
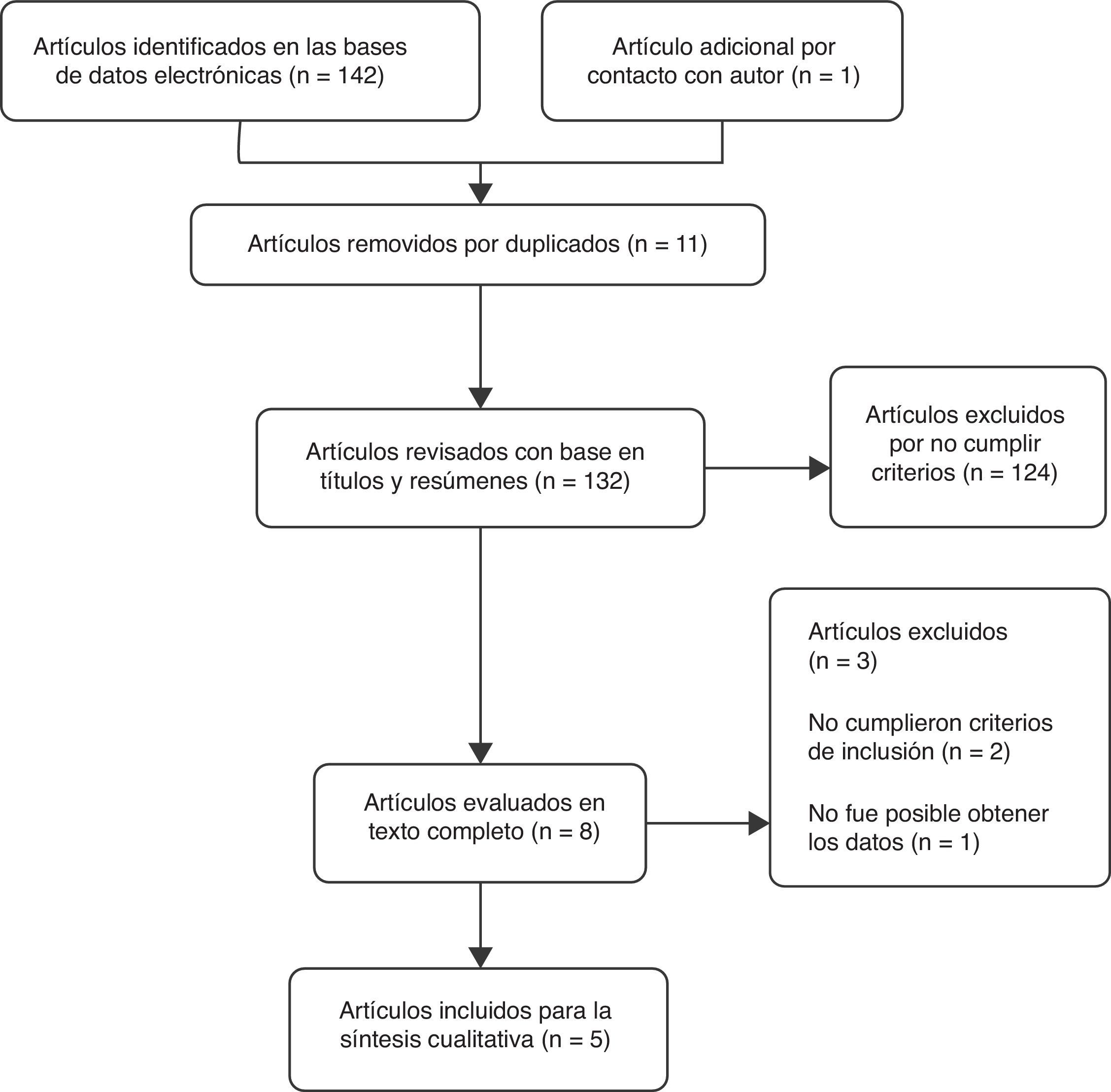
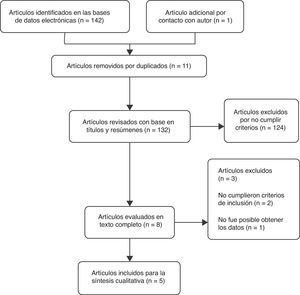
ResultadosSelección de los estudiosPara la revisión se incluyeron en total 5 ensayos clínicos controlados16–20 (fig. 1). La búsqueda en las bases de datos electrónicas Pubmed, Embase, Cochrane Central Register of Controlled Trials (CENTRAL) y LILACS arrojó en total 142 citaciones. Se encontraron 11 estudios duplicados. Después de ajustar por estudios duplicados quedaron 131. Posterior a la revisión de títulos y resúmenes se excluyeron 124 citaciones por no cumplir claramente con los criterios de inclusión. Las 7 citaciones restantes se revisaron en texto completo y 3 artículos fueron excluidos. Dos de ellos, Marra et al.21 (2012) y Koyuncu et al.22 (2010) no cumplieron criterios de inclusión. El tercer artículo Ediz et al.23 (2012) se excluyó porque no fue posible obtener la traducción al inglés ni al español y en el resumen del artículo no se encontraron los datos necesarios para la revisión. Un artículo adicional (Das et al.16 [1999]) fue obtenido al contactar al autor principal. El artículo después de su revisión en texto completo se incluyó en la revisión.
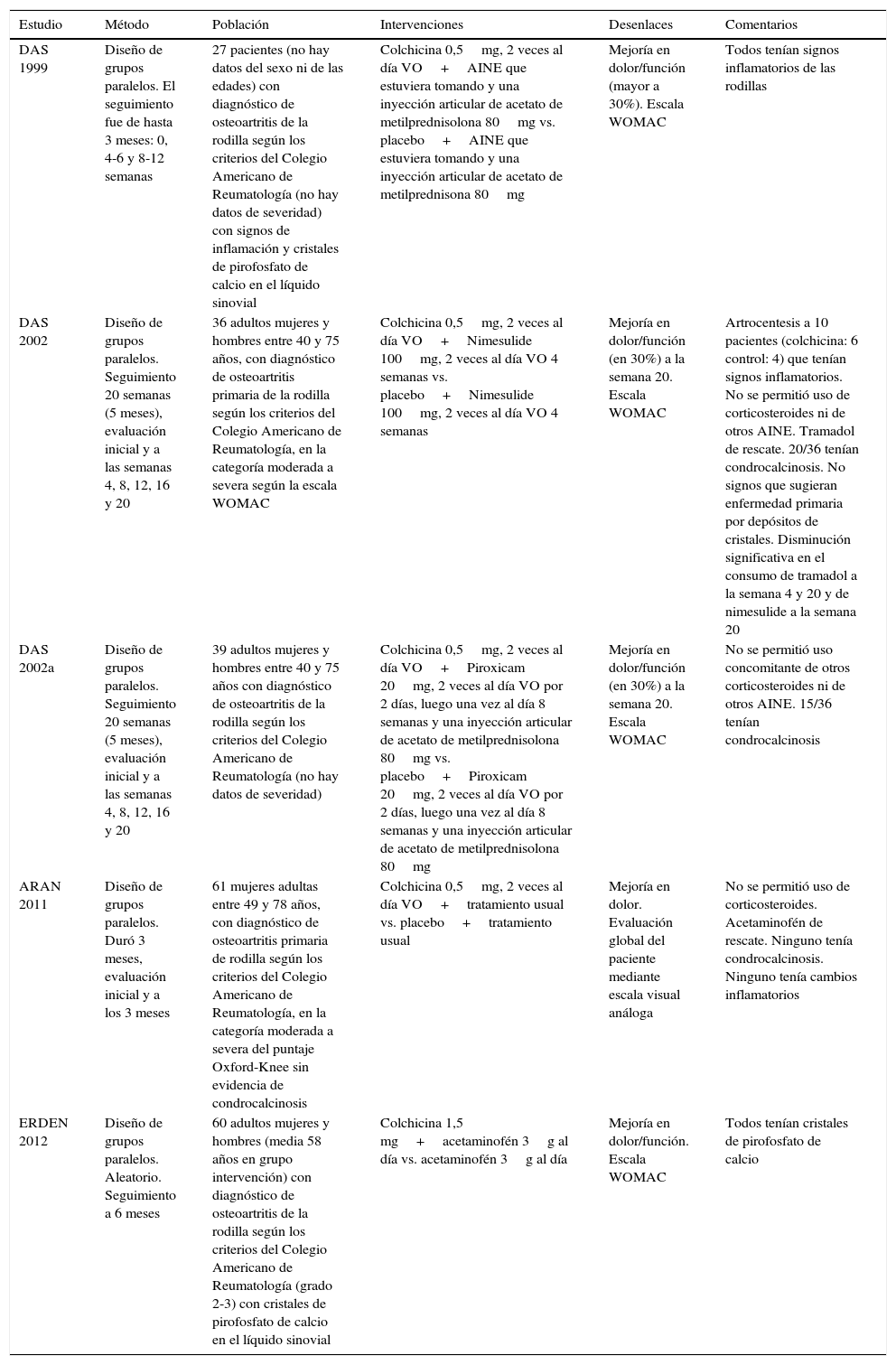
Características de los estudiosLas características de los estudios incluidos en la revisión se encuentran resumidas en la tabla 1. Todos los 5 artículos incluidos son en idioma inglés y fueron publicados entre los años 1999 y 2012. Tres de ellos son del mismo autor (Das et al.16 [1999], Das et al.17 [2012] y Das et al.18 [2012a]) realizados en la India. Otro fue realizado en Estados Unidos de América (Aran et al.19 [2011]) y el quinto fue realizado en Turquía (Erden et al.20 [2012]). Solo un estudio (Das 1999) expresa el escenario de donde fueron reclutados los pacientes, manifestando que se realizó en una clínica de Reumatología. En los demás artículos no se menciona el escenario.
Características de los estudios incluidos en la revisión
| Estudio | Método | Población | Intervenciones | Desenlaces | Comentarios |
|---|---|---|---|---|---|
| DAS 1999 | Diseño de grupos paralelos. El seguimiento fue de hasta 3 meses: 0, 4-6 y 8-12 semanas | 27 pacientes (no hay datos del sexo ni de las edades) con diagnóstico de osteoartritis de la rodilla según los criterios del Colegio Americano de Reumatología (no hay datos de severidad) con signos de inflamación y cristales de pirofosfato de calcio en el líquido sinovial | Colchicina 0,5mg, 2 veces al día VO+AINE que estuviera tomando y una inyección articular de acetato de metilprednisolona 80mg vs. placebo+AINE que estuviera tomando y una inyección articular de acetato de metilprednisona 80mg | Mejoría en dolor/función (mayor a 30%). Escala WOMAC | Todos tenían signos inflamatorios de las rodillas |
| DAS 2002 | Diseño de grupos paralelos. Seguimiento 20 semanas (5 meses), evaluación inicial y a las semanas 4, 8, 12, 16 y 20 | 36 adultos mujeres y hombres entre 40 y 75 años, con diagnóstico de osteoartritis primaria de la rodilla según los criterios del Colegio Americano de Reumatología, en la categoría moderada a severa según la escala WOMAC | Colchicina 0,5mg, 2 veces al día VO+Nimesulide 100mg, 2 veces al día VO 4 semanas vs. placebo+Nimesulide 100mg, 2 veces al día VO 4 semanas | Mejoría en dolor/función (en 30%) a la semana 20. Escala WOMAC | Artrocentesis a 10 pacientes (colchicina: 6 control: 4) que tenían signos inflamatorios. No se permitió uso de corticosteroides ni de otros AINE. Tramadol de rescate. 20/36 tenían condrocalcinosis. No signos que sugieran enfermedad primaria por depósitos de cristales. Disminución significativa en el consumo de tramadol a la semana 4 y 20 y de nimesulide a la semana 20 |
| DAS 2002a | Diseño de grupos paralelos. Seguimiento 20 semanas (5 meses), evaluación inicial y a las semanas 4, 8, 12, 16 y 20 | 39 adultos mujeres y hombres entre 40 y 75 años con diagnóstico de osteoartritis de la rodilla según los criterios del Colegio Americano de Reumatología (no hay datos de severidad) | Colchicina 0,5mg, 2 veces al día VO+Piroxicam 20mg, 2 veces al día VO por 2 días, luego una vez al día 8 semanas y una inyección articular de acetato de metilprednisolona 80mg vs. placebo+Piroxicam 20mg, 2 veces al día VO por 2 días, luego una vez al día 8 semanas y una inyección articular de acetato de metilprednisolona 80mg | Mejoría en dolor/función (en 30%) a la semana 20. Escala WOMAC | No se permitió uso concomitante de otros corticosteroides ni de otros AINE. 15/36 tenían condrocalcinosis |
| ARAN 2011 | Diseño de grupos paralelos. Duró 3 meses, evaluación inicial y a los 3 meses | 61 mujeres adultas entre 49 y 78 años, con diagnóstico de osteoartritis primaria de rodilla según los criterios del Colegio Americano de Reumatología, en la categoría moderada a severa del puntaje Oxford-Knee sin evidencia de condrocalcinosis | Colchicina 0,5mg, 2 veces al día VO+tratamiento usual vs. placebo+tratamiento usual | Mejoría en dolor. Evaluación global del paciente mediante escala visual análoga | No se permitió uso de corticosteroides. Acetaminofén de rescate. Ninguno tenía condrocalcinosis. Ninguno tenía cambios inflamatorios |
| ERDEN 2012 | Diseño de grupos paralelos. Aleatorio. Seguimiento a 6 meses | 60 adultos mujeres y hombres (media 58 años en grupo intervención) con diagnóstico de osteoartritis de la rodilla según los criterios del Colegio Americano de Reumatología (grado 2-3) con cristales de pirofosfato de calcio en el líquido sinovial | Colchicina 1,5 mg+acetaminofén 3g al día vs. acetaminofén 3g al día | Mejoría en dolor/función. Escala WOMAC | Todos tenían cristales de pirofosfato de calcio |
Las características de la población fueron diversas entre los estudios, pues se incluían mujeres en unos y hombres y mujeres en otros. El espectro de gravedad fue variable, en unos incluyendo artritis moderada-grave y en otros no se tenía en cuenta la gravedad. En unos estudios la población tenía signos inflamatorios articulares, en otros no y en otros se mezclaban ambos. Algunos autores incluyeron en su población la presencia de condrocalcinosis como signo de enfermedad articular por pirofosfato de calcio y otros excluyeron esta población. El tiempo de seguimiento más corto fue de 3 meses.
En el grupo de intervención todos tenían colchicina, 4 de ellos (excepto Erden 2012) a una dosis de 0,5mg VO, 2 veces al día. Sin embargo, las cointervenciones adicionales variaron de estudio a estudio desde AINE y acetaminofén hasta corticosteroides intraarticulares. En el grupo de comparación el tratamiento también varió de estudio a estudio.
En la mayoría de los estudios (excepto Aran 2011) se utilizó la escala WOMAC (o su modificación validada) para medir el desenlace principal. El número de participantes incluidos en los estudios es bajo, variando entre 27 y 61 participantes, incluyendo tanto al grupo intervención como al control.
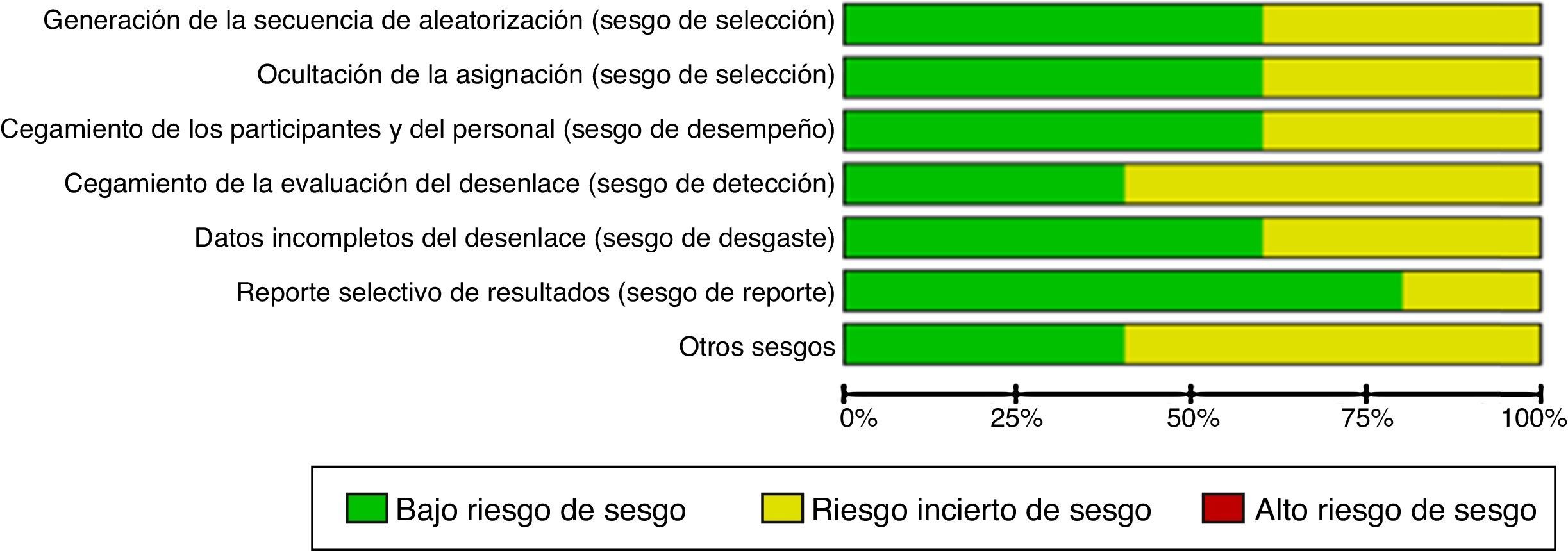
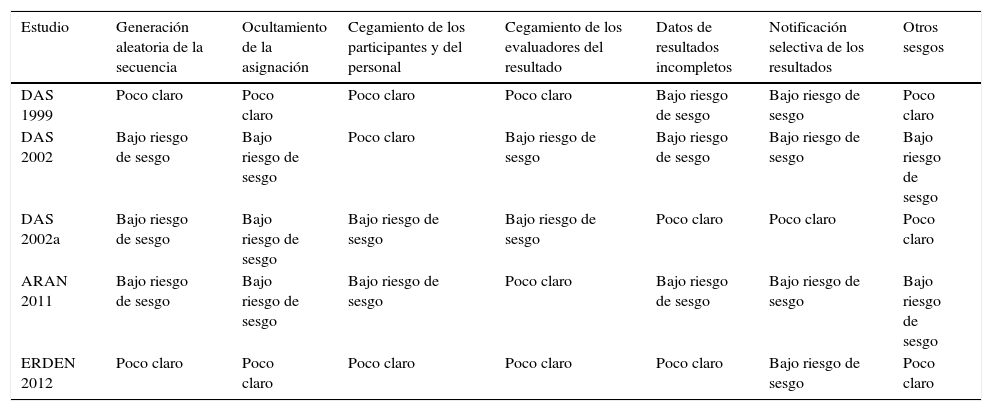
Riesgo de sesgo dentro de los estudiosEn la tabla 2 y en la figura 2 se muestra el resumen del riesgo de sesgo por cada uno de los estudios y el riesgo de sesgo por dominios, respectivamente, de acuerdo con la herramienta de la evaluación de riesgo de la Colaboración Cochrane. Tres de los estudios incluidos (Das 1999, Das 2002 y Erden 2012) tienen comprometidos dominios fundamentales que afectan la calidad.
Riesgo de sesgo dentro de cada estudio
| Estudio | Generación aleatoria de la secuencia | Ocultamiento de la asignación | Cegamiento de los participantes y del personal | Cegamiento de los evaluadores del resultado | Datos de resultados incompletos | Notificación selectiva de los resultados | Otros sesgos |
|---|---|---|---|---|---|---|---|
| DAS 1999 | Poco claro | Poco claro | Poco claro | Poco claro | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Poco claro |
| DAS 2002 | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Poco claro | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Bajo riesgo de sesgo |
| DAS 2002a | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Poco claro | Poco claro | Poco claro |
| ARAN 2011 | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Poco claro | Bajo riesgo de sesgo | Bajo riesgo de sesgo | Bajo riesgo de sesgo |
| ERDEN 2012 | Poco claro | Poco claro | Poco claro | Poco claro | Poco claro | Bajo riesgo de sesgo | Poco claro |
La calidad de la evidencia en conjunto, utilizando el enfoque GRADE, fue «muy baja». A pesar de que solo se incluyeron ensayos clínicos, factores como limitaciones en el diseño, imprecisión en los resultados y alta probabilidad de sesgo de publicación, disminuyen el nivel de la calidad de la evidencia.
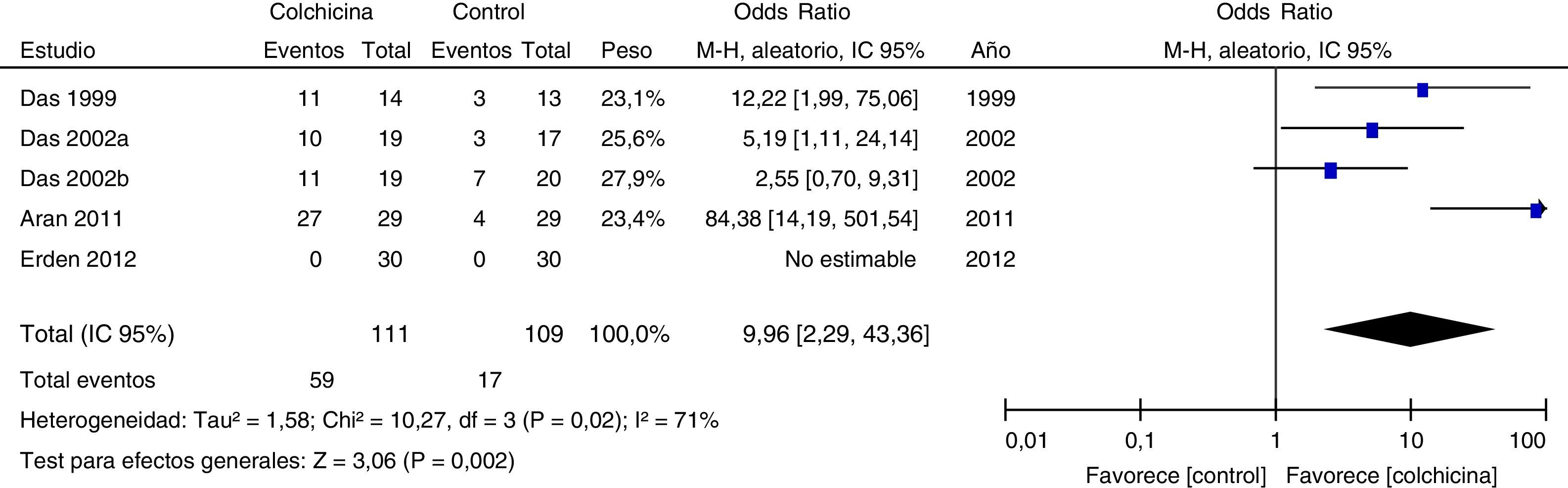
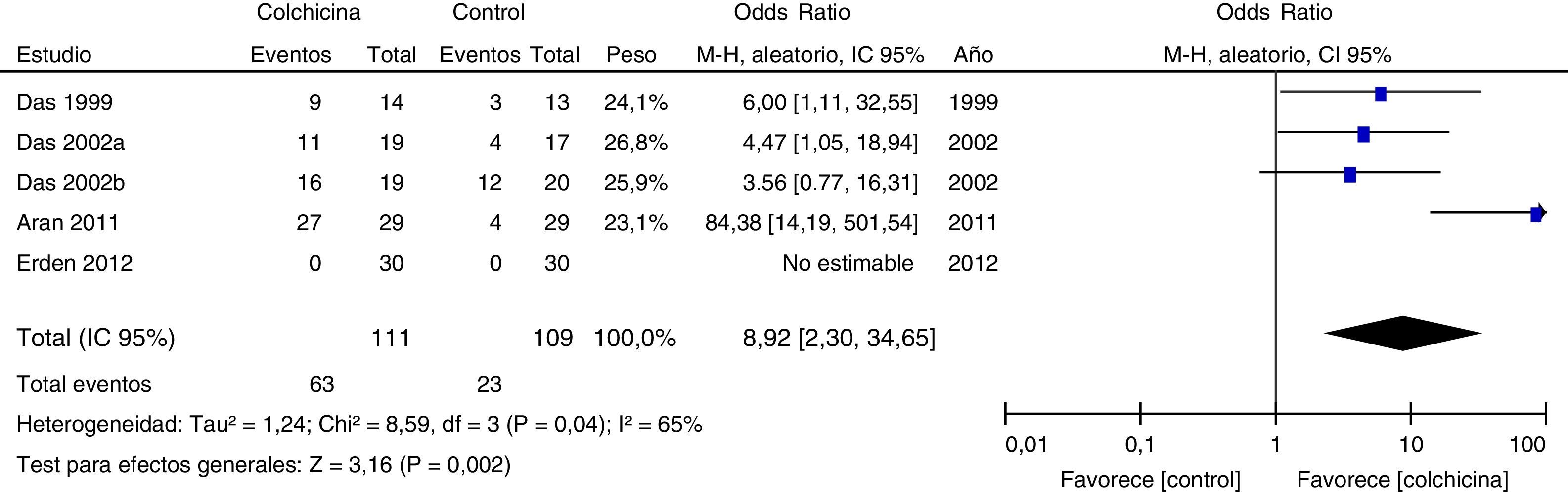
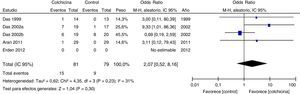
Resultados de estudios individualesEn las figuras 3–5 se muestra el resumen de los datos, la estimación del efecto y los intervalos de confianza para cada estudio incluido en la revisión, referente a los desenlaces reducción del dolor (fig. 3), mejoría de la funcionalidad (fig. 4) y efectos adversos gastrointestinales (fig. 5).
Síntesis de resultadosEn vista de que la población, sus características clínicas y las intervenciones varían marcadamente, así como también la calidad metodológica de los estudios, la revisión se enfocó principalmente en describir los estudios, sus resultados, aplicabilidad y limitaciones en una síntesis cualitativa. El metaanálisis adicional confirmó una elevada heterogeneidad entre los estudios, especialmente para los desenlaces de eficacia (figs. 3 y 4).
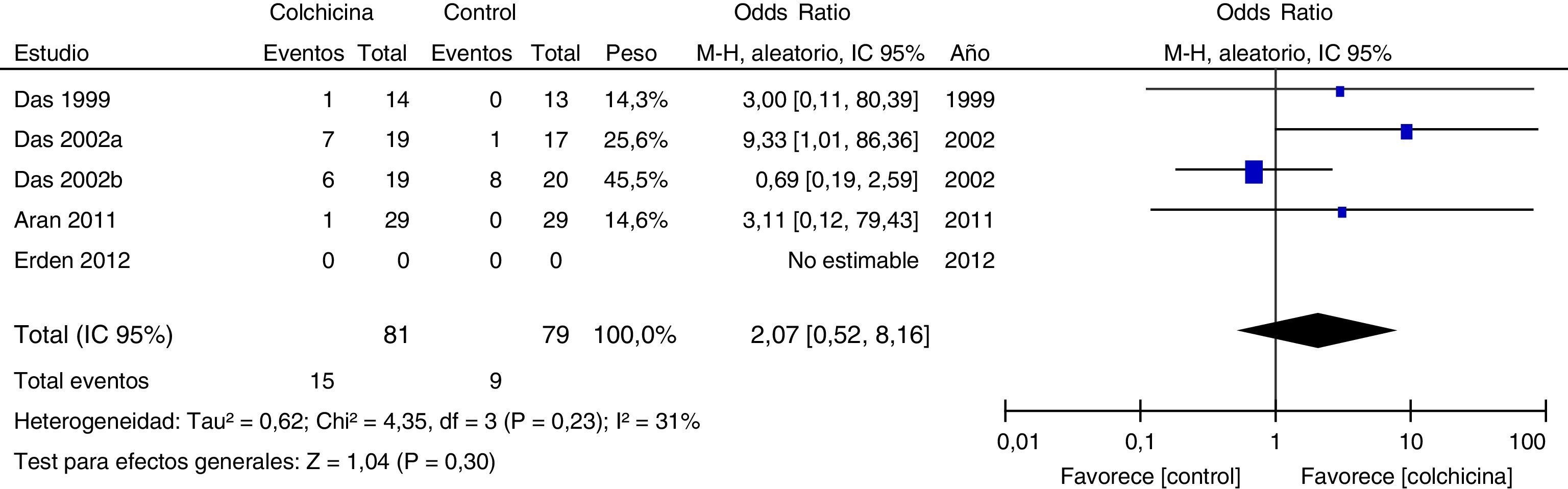
Todos los artículos incluidos en la revisión evaluaron la mejoría del dolor. En la gráfica de bosque (fig. 3) se observa una tendencia común en todos los estimados puntuales de los artículos, los cuales tienden a favorecer el uso de la colchicina para la mejoría del dolor, al ser adicionada a tratamientos convencionales comparada con solo tratamiento convencional. Una tendencia similar se observa con el desenlace mejoría de la funcionalidad (fig. 4), el cual también fue evaluado en todos los artículos incluidos.
En cuanto al desenlace efectos adversos, en 4 fue evaluado y en uno no (Erden 2012). Tres de ellos (Das 1999, Das 2002 y Aran 2011) reportaron un episodio de diarrea en cada uno, en el grupo de colchicina. En el estudio Das 2002a no se reportó diarrea sino 8 casos de síntomas dispépticos en el grupo colchicina vs. 4 casos en el grupo control. Solo Das 2002a reportó efectos adversos diferentes a los gastrointestinales; entre estos, 5 casos de infección del tracto respiratorio superior y 8 casos de aumento en el dolor musculoesquelético en el grupo de colchicina vs. un caso de infección del tracto respiratorio superior y 28 casos de aumento en el dolor musculoesquelético en el grupo control. Todos los estudios incluidos en la revisión son pequeños, con intervalos de confianza poco precisos. Ninguno de los estudios evaluó calidad de vida.
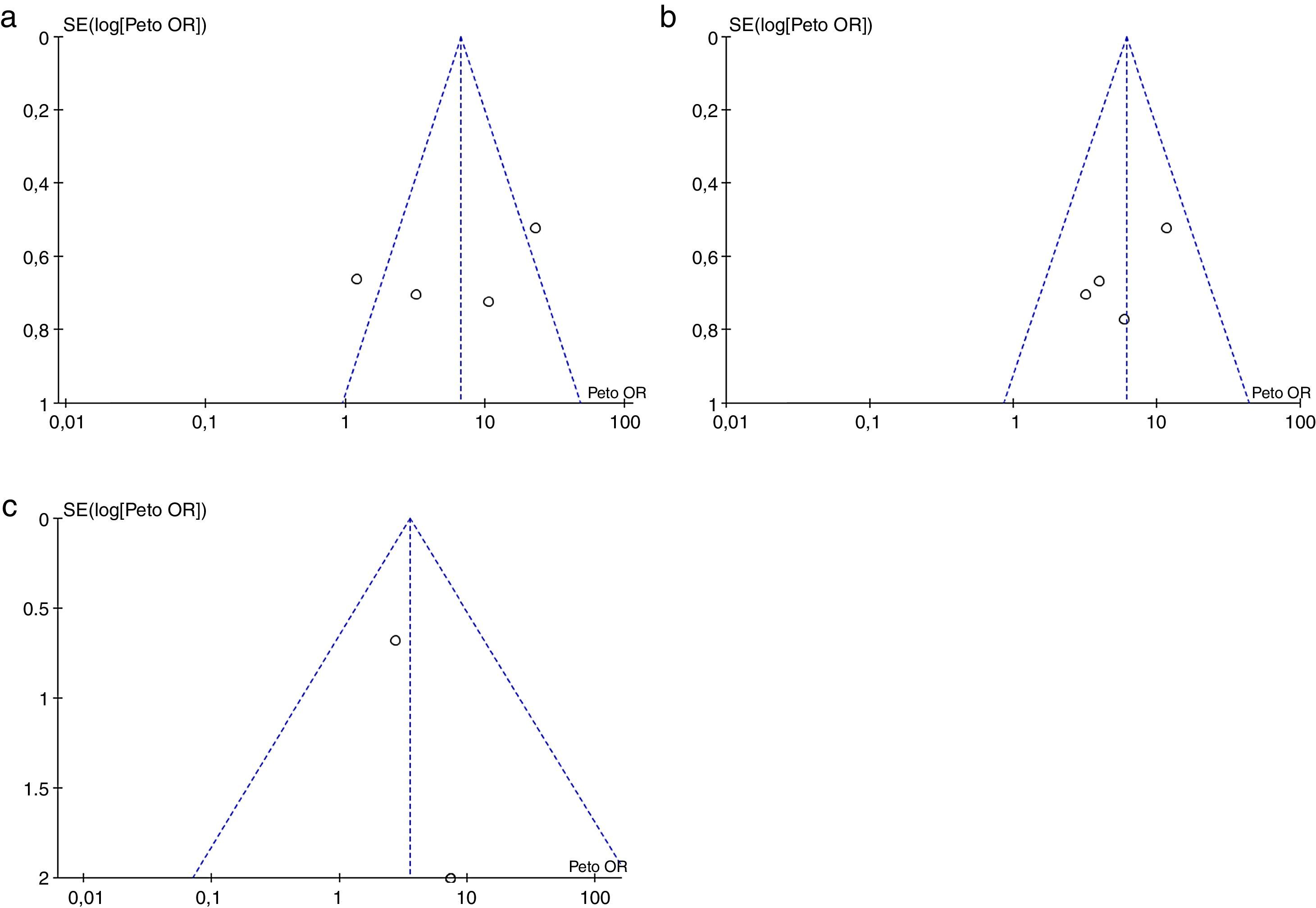
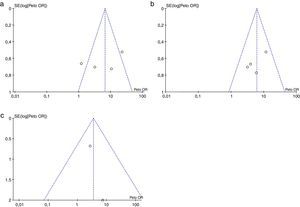
Riesgo de sesgos a través de los estudiosEn la inspección visual del gráfico de embudo para cada uno de los desenlaces evaluados, no es posible descartar la posibilidad de sesgo de publicación (fig. 6).
Análisis adicionalesPor el número reducido de estudios encontrados, no fue posible realizar análisis de subgrupos.
DiscusiónResumen de la evidenciaSe llevó a cabo una revisión sistemática de la literatura para evaluar la eficacia y seguridad de la intervención con colchicina adicionada al manejo convencional de pacientes adultos con osteoartrosis de rodilla. Debido a la variabilidad marcada en la población, sus características clínicas y las intervenciones, así como de la calidad metodológica, la revisión se enfocó en realizar una síntesis cualitativa en vez de un metaanálisis. En total solo 5 artículos cumplieron con los criterios de elegibilidad.
El hallazgo más representativo de la revisión es la tendencia a favor del uso de colchicina para la mejoría del dolor y la mejoría de la funcionalidad, comparado con el grupo control. Además, en cuanto a los efectos adversos, el gráfico de bosque muestra una tendencia a producir mayores efectos adversos gastrointestinales con el uso de la colchicina, sin embargo, la diferencia no es estadísticamente significativa en los estudios individuales. Es importante resaltar que la dosis de colchicina usada en la mayoría de los estudios fue de 0,5mg, 2 veces al día, lo cual coincide con las dosis actualmente recomendadas para el tratamiento de la enfermedad por cristales de pirofosfato de calcio12 y también para el tratamiento de gota; para esta última se ha demostrado que las dosis altas no aumentan la efectividad pero sí incrementan los efectos adversos24.
No hubo una clara declaración del escenario de los estudios, lo que puede dificultar la generalizabilidad. La fuerza de la evidencia es pobre, contándose con pocos estudios de pequeño tamaño, imprecisos y de regular calidad metodológica. Ningún estudio tuvo en cuenta la evaluación de la calidad de vida de los participantes.
Solo el estudio de Aran et al.19 (2011) fue exhaustivo en incluir solo pacientes con osteoartritis primaria de rodilla, incluyendo evaluación radiológica de la condrocalcinosis y excluyendo aquellos con cambios inflamatorios. Sin embargo, esto no descarta del todo en el estudio la posibilidad de asociación de osteoartritis con depósito de cristales de pirofosfato de calcio. El resultado de este estudio también estuvo a favor de la colchicina.
LimitacionesDentro de las limitaciones de la revisión encontramos que la calidad de la evidencia varía y ninguno de los artículos incluidos cumple todos los criterios estándar de calidad. Los estudios son pequeños y con baja precisión. No fue posible descartar sesgo de publicación para las comparaciones incluidas.
ConclusionesLa colchicina parece ser una alternativa eficaz y segura para el tratamiento de pacientes adultos con osteoartritis de rodilla, tanto primaria como relacionada con depósito de cristales de pirofosfato de calcio. Su uso reduce el dolor y mejora la funcionalidad, aunque puede producir síntomas gastrointestinales en algunos pacientes. La gran heterogeneidad clínica y metodológica de los estudios incluidos en la revisión hace inadecuado obtener una medida del efecto resumen de todos los estudios incluidos. Sería ideal llevar a cabo ensayos clínicos controlados de mejor calidad, con un mayor número de pacientes, discriminando claramente entre aquellos con osteoartritis primaria o asociada con el depósito de pirofosfato cálcico y que incluyan además desenlaces como la calidad de vida. Es importante señalar que en la actualidad aparece registrado un ensayo clínico recientemente finalizado que evalúa el uso de colchicina en osteoartritis de rodilla. Hasta la última búsqueda efectuada en noviembre de 2016 no encontramos resultados publicados25.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
- 1.
Search: «osteoarthritis»[MeSH Terms]
- 2.
Search: «osteoarthritis, knee»[MeSH Terms]
- 3.
Search: «osteoarthritis»[Text Word]
- 4.
Search: «osteoarthrosis»[Text Word]
- 5.
Search: «arthrosis»[Text Word]
- 6.
Search: «osteoartrosis»[Text Word]
- 7.
Search: «artrosis»[Text Word]
- 8.
Search: #1 OR #2 OR #3 OR #4 OR #5 OR #6 OR #7
- 9.
Search: «colchicine»[MeSH Terms]
- 10.
Search: «colchicine»[Text Word]
- 11.
Search: «colchicina»[Text Word]
- 12.
Search: #9 OR #10 OR #11
- 13.
Search: (((randomized controlled trial[pt] OR randomized controlled trials[mh] OR random allocation[mh] OR random allocat* [tw] OR randomly allocat* [tw] OR double-blind method[mh] OR single-blind method [mh] OR double blind* [tw] OR single blind* [tw] OR triple blind* [tw] OR clinical trial [pt] OR clinical trials [mh]) NOT (animal [mh] NOT human [mh])))
- 14.
Search: #8 AND #12 AND #13