El intercambio terapéutico de plasma y la plasmaféresis son procedimientos que permiten la eliminación de macromoléculas nocivas y que están indicados en algunos trastornos autoinmunes cuando está en peligro la vida o un órgano vital.
Objetivos y métodosDescribir la experiencia con el uso de la plasmaféresis y el intercambio terapéutico de plasma en patologías autoinmunes en un hospital universitario de cuarto nivel de complejidad, centro de referencia. Estudio descriptivo, retrospectivo, de una serie de casos.
ResultadosSe incluyeron 93 pacientes; 67 tenían enfermedades autoinmunes: neurológicas (66%), hematológicas (18%) y reumatológicas (12%). El 82% del grupo tuvo una respuesta favorable (61% completa y 21% parcial). La mortalidad global fue del 6%. En el subgrupo de enfermedades reumatológicas, las indicaciones más frecuentes fueron: lupus eritematoso sistémico y vasculitis asociadas a anticuerpos contra el citoplasma de neutrófilo (37,5% cada una) por compromisos: respiratorio o neurológico. Las secuelas más importantes fueron neurológicas y renales. El 63% de los sujetos no presentó ningún evento adverso.
ConclusionesLos pacientes que recibieron plasmaféresis o intercambio terapéutico de plasma por enfermedades autoinmunes con una condición crítica que amenaza la vida o un órgano vital presentaron una respuesta favorable que redundó en una mejor supervivencia a corto plazo; estas terapias son, generalmente, bien toleradas. Se requieren estudios con mayor solidez metodológica, especialmente en las enfermedades reumatológicas.
Therapeutic plasma exchange and plasmapheresis are procedures that allow the removal of harmful macromolecules, and are indicated in some autoimmune disorders, when life or vital organs are in danger.
Objectives and MethodsTo describe the experience with the use of therapeutic plasmapheresis and plasma exchange in autoimmune diseases in a tertiary reference university hospital. A retrospective descriptive study was conducted on a series of cases.
ResultsOf the 93 patients included, 67 had autoimmune diseases: neurological (66%), hematological (18%), and rheumatic (12%). A favorable response was observed in 82% of the group (61% complete and 21% partial). Overall mortality was 6%. In the subgroup of rheumatology diseases, the most frequent indications were: systemic lupus erythematosus and vasculitis associated with antibodies against neutrophil cytoplasm (37.5% each) for respiratory or neurological involvement. The most important sequelae were neurological and renal. No adverse events were reported in 63% of the subjects.
ConclusionsPatients receiving therapeutic plasmapheresis or plasma exchange in autoimmune diseases with a critical life-threatening condition or a vital organ involvement had a favorable response that resulted in better short-term survival. These therapies are, generally, well tolerated. Studies with greater methodological soundness, especially in rheumatic diseases, are required.
El intercambio terapéutico de plasma (ITP) y la plasmaféresis (PF) son procedimientos que permiten la eliminación de macromoléculas nocivas del plasma que, en patología reumatológica y otros trastornos autoinmunes parecen tener, al menos, un papel adyuvante temporal; generalmente se reservan como estrategia terapéutica cuando está en peligro un órgano vital o la vida, y aun en ese contexto, sigue considerándose una terapia con poca evidencia en la literatura1,2.
En la PF, el plasma completo es removido y separado de otros componentes sanguíneos por centrifugación o mediante una membrana de filtración; posteriormente, las células son reinfundidas con una solución de reemplazo (plasma fresco congelado, albúmina, coloides o cristaloides en el caso del ITP) o sin solución de sustitución en la PF3. Para la mayoría de condiciones, el objetivo del procedimiento es remover autoanticuerpos o toxinas consideradas deletéreas, y la meta es cambiar de 1 a 1,5 veces el volumen plasmático por procedimiento, disminuyendo, aproximadamente, del 63 al 78% los niveles de macromoléculas, respectivamente4–6.
Basados en la eficacia clínica de la PF y el ITP reportada en la literatura, la Sociedad Americana para la Aféresis las considera como tratamiento de primera línea, ya sea solas o en combinación con otras estrategias, en las siguientes patologías: síndrome de Guillain-Barré, hiperviscosidad en gammapatías monoclonales, púrpura trombocitopénica trombótica, enfermedad de células falciformes y accidente cerebrovascular agudo3,7,8. Hasta donde se sabe, hoy por hoy, se han descrito más de 100 usos racionales de PF e ITP, aunque aún son diversos y, lastimosamente, sin los mejores niveles de evidencia: la mayoría, producto de resultados anecdóticos, estudios no controlados o pequeños ensayos prospectivos de distribución aleatoria.
El propósito de este estudio es conocer la frecuencia, indicaciones, complicaciones y morbimortalidad asociadas a estos procedimientos en un hospital universitario colombiano de cuarto nivel de complejidad y centro de referencia en reumatología.
Materiales y métodosSe realizó un estudio descriptivo, retrospectivo, de una serie de casos, que incluyó a todos los pacientes sometidos a PF o ITP entre enero de 2007 y diciembre de 2012, registrados en la base de datos del banco de sangre de la institución.
Se revisaron las historias clínicas y se recolectó la información en un formulario previamente establecido, que incluyó las siguientes variables: edad, sexo, enfermedad subyacente, tiempo de evolución de esta, compromiso orgánico o vital que indicó el ITP o PF, estancia hospitalaria en días, terapias inmunosupresoras concomitantes, gravedad de la enfermedad (definida por compromiso orgánico), secuelas, técnica utilizada (PF o ITP), número de sesiones por paciente y por enfermedad, volúmenes de recambio por sesión, tipo de líquido infundido, complicaciones y eventos adversos. Los desenlaces que se debían evaluar fueron: respuesta a la terapia, mortalidad y secuelas. La estimación de la respuesta se realizó en términos de compromiso de órgano y síntomas cardinales que condicionaron la gravedad de la enfermedad y la indicación de la terapia, así: respuesta completa: recuperación total de la función orgánica comprometida y ausencia plena de secuelas; respuesta parcial: recuperación incompleta de la función orgánica comprometida. La respuesta se estimó en el momento del alta y a los 3 y 6 meses en los pacientes que continuaron en seguimiento en la institución y en quienes esta información estuviera disponible. El análisis de los resultados se hizo con estadística descriptiva, utilizando las herramientas de la hoja de cálculo de Microsoft Excel 2010.
El estudio fue previamente aprobado por el Comité de Ética de la institución.
ResultadosCaracterísticas generalesNoventa y tres pacientes fueron sometidos a PF o ITP. De ellos, 67 tenían patología autoinmune; las enfermedades neurológicas fueron las más frecuentes. Las características demográficas se muestran en la tabla 1.
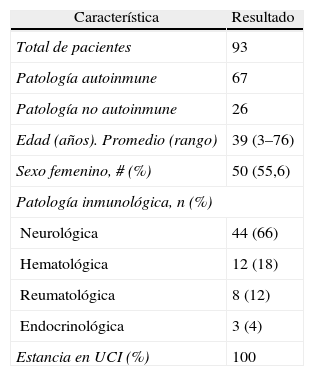
Características generales de la población sometida a intercambio terapéutico de plasma y plasmaféresis
| Característica | Resultado |
| Total de pacientes | 93 |
| Patología autoinmune | 67 |
| Patología no autoinmune | 26 |
| Edad (años). Promedio (rango) | 39 (3–76) |
| Sexo femenino, # (%) | 50 (55,6) |
| Patología inmunológica, n (%) | |
| Neurológica | 44 (66) |
| Hematológica | 12 (18) |
| Reumatológica | 8 (12) |
| Endocrinológica | 3 (4) |
| Estancia en UCI (%) | 100 |
UCI: unidad de cuidados intensivos.
Ochenta pacientes (75%) tuvieron seguimiento en la institución, al menos, hasta los 6 meses posteriores a la terapia. Veinticinco individuos (27% del grupo global) tenían indicación no inmune; de ellas, la principal fue el rechazo a trasplante renal (n=24) y, en 1 paciente, fue un síndrome paraneoplásico; estos sujetos fueron excluidos del análisis.
Características del procedimientoTodos los ITP y las PF se realizaron con el equipo Plasma Collection System PCS 2; (Haemonetics, Braintree, MA, Estados Unidos), de tipo intermitente, con un promedio de 4,3 sesiones por paciente, de 3h de duración, aféresis de 1,3 volemias por sesión. Las soluciones de reemplazo fueron con plasma fresco congelado (57 sujetos; 71%) y en 23 individuos se utilizó albúmina mezclada con solución salina (proporción 70–30) (29%). Se calculó el volumen de reemplazo según el peso corporal (40 mL/kg para ambas soluciones). El 66% de los sujetos no tuvo ningún evento adverso durante y después de los procedimientos; en el resto de la población, los efectos adversos más frecuentes fueron: hipotensión (30%) y brote (4%), los cuales obligaron a interrumpir las sesiones.
La descripción de las indicaciones de los procedimientos y el resultado global se muestran en la tabla 2.
Distribución por enfermedad y respuesta de pacientes sometidos a plasmaféresis o intercambio terapéutico de plasma
| Patología | Pacientes por enfermedad | Total | Número promedio de sesiones | Mejoría | Recurrencia |
| Neurológica | |||||
| Guillain-Barré | 17 | 44 (47%) | 4,6 | Completa 57% Parcial 27% Ninguna 16% | 16% |
| Miastenia gravis | 14 | ||||
| Síndrome de Devic | 8 | ||||
| Polineuropatía crónica inflamatoria | 1 | ||||
| Esclerosis múltiple | 1 | ||||
| Hematológica | |||||
| PTT | 6 | 12 (13%) | 3,7 | Completa 60% Parcial 0% Ninguna 40% | 0% |
| Macroglobulinemia de Waldeström | 1 | ||||
| Microangiopatía trombótica/SHU | 1 | ||||
| HPN | 1 | ||||
| Mieloma múltiple - Síndrome de hiperviscosidad | 1 | ||||
| Síndrome de Evans 1 | |||||
| Porfiria intermitente aguda | 1 | ||||
| Reumatológica | |||||
| LES/PTT | 1 | 8 (9%) | 4,5 | Completa 50% Parcial 25% Ninguna 25% | 12,5% |
| Dermatomiositis amiopática (síndrome antisintetasa) | 1 | ||||
| Granulomatosis con poliangiítis | 1 | ||||
| LES neuropsiquiátrico | 2 | ||||
| Vasculitis de SNC | 1 | ||||
| Poliangiítis microscópica | 2 | ||||
| Metabólica | |||||
| Enfermedad de Graves | 1 | 3 (3%) | 2,5 | Completa 100% | 0% |
| Hipertrigliceridemia | 1 | ||||
| Trasplante | |||||
| Rechazo trasplante renal | 25 | 27% | |||
| Neoplásica | |||||
| Síndrome paraneoplásico | 1 | 1% | |||
HPN: hemoglobinuria paroxística nocturna; LES: lupus eritematoso sistêmico; PTT: púrpura trombocitopénica trombótica; SHU: síndrome hemolítico urémico; SNC: sistema nervioso central.
El 82% de los pacientes tuvo una respuesta favorable (61% completa y 21% parcial), y el 18% no respondió. Siete de 44 sujetos con patología neurológica (16%), 1 de 8 con patología reumatológica (12,5%) y ninguno de los pacientes con etiología hematológica o endocrina presentaron recaídas. La mortalidad global fue del 6% (4 individuos): hiperviscosidad secundaria a mieloma múltiple en estadio avanzado (n=1); púrpura trombocitopénica trombótica con enfermedad cerebrovascular isquémica y transformación hemorrágica (n=1); poliangiítis microscópica con hemorragia alveolar difusa y falla respiratoria (n=1) y polineuropatía crónica inflamatoria con falla respiratoria y complicaciones infecciosas nosocomiales (n=1).
Subgrupo de enfermedades reumatológicasLa mayoría de los pacientes tenía un diagnóstico reciente; 4 de los 8 sujetos debutaron con la complicación grave que requirió PF o ITP. La edad promedio fue de 36 años; la relación hombre/mujer fue 1:1,6; hubo 3 individuos que tuvieron diagnóstico de lupus eritematoso sistémico y 3 vasculitis asociadas a anticuerpos contra el citoplasma de neutrófilo (ANCA) como patologías predominantes; en estos, 2 tenían poliangiítis microscópica con patrón de P-ANCA a la inmunofluorescencia indirecta (diluciones 1:640 y 1:320, respectivamente) y con anticuerpos antimieloperoxidasa confirmados por ELISA (123 y 80 U, respectivamente; límite > 20); el otro paciente tenía diagnóstico de granulomatosis con poliangiítis con patrón de C-ANCA por inmunofluorescencia indirecta (dilución 1:320) y con anticuerpos antiproteinasa 3 por ELISA (142 U; límite > 20 U). Los otros diagnósticos fueron: vasculitis aislada de sistema nervioso central (n=1) y dermatomiositis amiopática con enfermedad pulmonar intersticial (n=1). Tanto la recurrencia como la mortalidad fueron del 12,5%. La tabla 3 muestra las características basales de los pacientes con patología reumatológica.
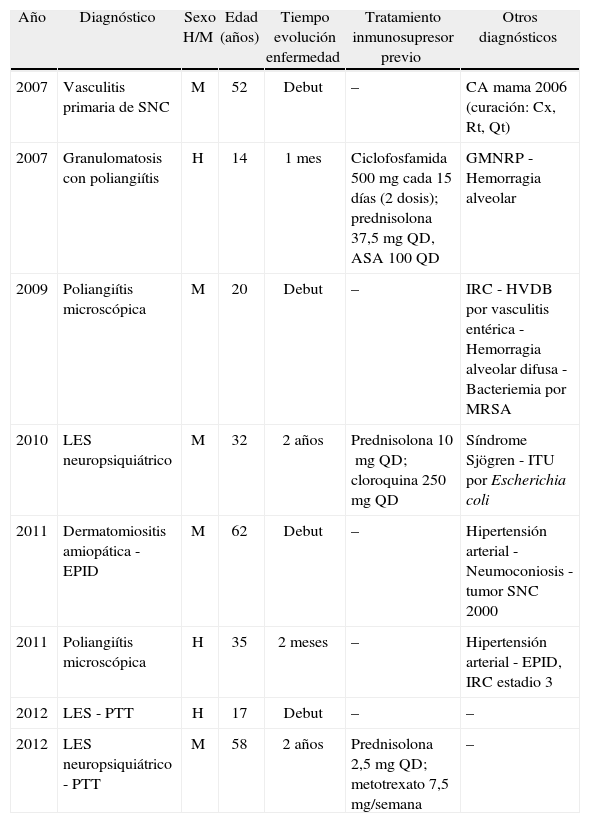
Características de los pacientes con enfermedad reumatológica que requirieron plasmaféresis o intercambio terapéutico de plasma
| Año | Diagnóstico | Sexo H/M | Edad (años) | Tiempo evolución enfermedad | Tratamiento inmunosupresor previo | Otros diagnósticos |
| 2007 | Vasculitis primaria de SNC | M | 52 | Debut | – | CA mama 2006 (curación: Cx, Rt, Qt) |
| 2007 | Granulomatosis con poliangiítis | H | 14 | 1 mes | Ciclofosfamida 500mg cada 15 días (2 dosis); prednisolona 37,5mg QD, ASA 100 QD | GMNRP - Hemorragia alveolar |
| 2009 | Poliangiítis microscópica | M | 20 | Debut | – | IRC - HVDB por vasculitis entérica - Hemorragia alveolar difusa - Bacteriemia por MRSA |
| 2010 | LES neuropsiquiátrico | M | 32 | 2 años | Prednisolona 10mg QD; cloroquina 250mg QD | Síndrome Sjögren - ITU por Escherichia coli |
| 2011 | Dermatomiositis amiopática - EPID | M | 62 | Debut | – | Hipertensión arterial - Neumoconiosis - tumor SNC 2000 |
| 2011 | Poliangiítis microscópica | H | 35 | 2 meses | – | Hipertensión arterial - EPID, IRC estadio 3 |
| 2012 | LES - PTT | H | 17 | Debut | – | – |
| 2012 | LES neuropsiquiátrico - PTT | M | 58 | 2 años | Prednisolona 2,5mg QD; metotrexato 7,5mg/semana | – |
ASA: ácido acetilsalicílico; Cx: cirugía; EPID: enfermedad pulmonar intersticial difusa; GMNRP: glomerulonefritis rápidamente progresiva; HVDB: hemorragia de vías digestivas bajas; IRC: insuficiencia renal crónica; ITU: infección del tracto urinario; LES: lupus eritematoso sistémico; MRSA: Staphylococcus aureus meticilino resistente; PTT: púrpura trombocitopénica trombótica; QD; cada día; Qt: quimioterapia; Rt: radioterapia; SNC: sistema nervioso central.
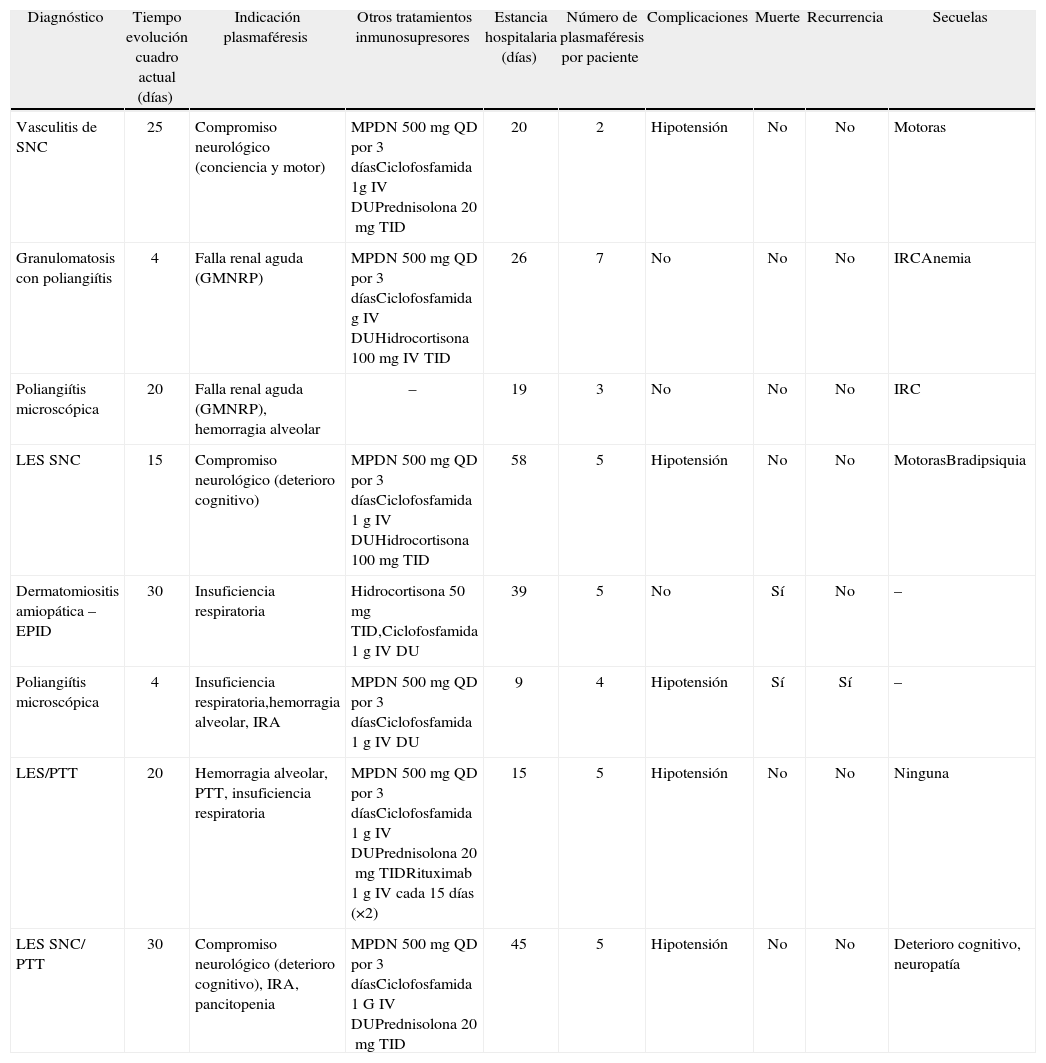
En casi todos los pacientes se utilizaron estos procedimientos de manera adjunta a la inmunosupresión con dosis altas de esteroides (en su mayoría, pulsos de metilprednisolona –MPDN–) seguidos de prednisolona, además de ciclofosfamida o rituximab, excepto en un paciente que presentó una complicación infecciosa que contraindicó la inmunosupresión. La tabla 4 ilustra, de manera detallada, los desenlaces posteriores a la PF o la ITP.
Desenlaces de los pacientes con enfermedad reumatológica que requirieron plasmaféresis o intercambio terapéutico de plasma
| Diagnóstico | Tiempo evolución cuadro actual (días) | Indicación plasmaféresis | Otros tratamientos inmunosupresores | Estancia hospitalaria (días) | Número de plasmaféresis por paciente | Complicaciones | Muerte | Recurrencia | Secuelas |
| Vasculitis de SNC | 25 | Compromiso neurológico (conciencia y motor) | MPDN 500mg QD por 3 díasCiclofosfamida 1g IV DUPrednisolona 20mg TID | 20 | 2 | Hipotensión | No | No | Motoras |
| Granulomatosis con poliangiítis | 4 | Falla renal aguda (GMNRP) | MPDN 500mg QD por 3 díasCiclofosfamida g IV DUHidrocortisona 100mg IV TID | 26 | 7 | No | No | No | IRCAnemia |
| Poliangiítis microscópica | 20 | Falla renal aguda (GMNRP), hemorragia alveolar | – | 19 | 3 | No | No | No | IRC |
| LES SNC | 15 | Compromiso neurológico (deterioro cognitivo) | MPDN 500mg QD por 3 díasCiclofosfamida 1 g IV DUHidrocortisona 100mg TID | 58 | 5 | Hipotensión | No | No | MotorasBradipsiquia |
| Dermatomiositis amiopática – EPID | 30 | Insuficiencia respiratoria | Hidrocortisona 50mg TID,Ciclofosfamida 1 g IV DU | 39 | 5 | No | Sí | No | – |
| Poliangiítis microscópica | 4 | Insuficiencia respiratoria,hemorragia alveolar, IRA | MPDN 500mg QD por 3 díasCiclofosfamida 1 g IV DU | 9 | 4 | Hipotensión | Sí | Sí | – |
| LES/PTT | 20 | Hemorragia alveolar, PTT, insuficiencia respiratoria | MPDN 500mg QD por 3 díasCiclofosfamida 1 g IV DUPrednisolona 20mg TIDRituximab 1 g IV cada 15 días (×2) | 15 | 5 | Hipotensión | No | No | Ninguna |
| LES SNC/ PTT | 30 | Compromiso neurológico (deterioro cognitivo), IRA, pancitopenia | MPDN 500mg QD por 3 díasCiclofosfamida 1 G IV DUPrednisolona 20mg TID | 45 | 5 | Hipotensión | No | No | Deterioro cognitivo, neuropatía |
DU: dosis única; EPID: enfermedad pulmonar intersticial difusa; GMNRP: glomerulonefritis rápidamente progresiva; IRA: insuficiencia renal aguda; IRC: insuficiencia renal crónica; IV: intravenoso; LES: lupus eritematoso sistémico; MPDN: metilprednisolona; PTT: púrpura trombocitopénica trombótica; QD: cada día; SNC: Sistema nervioso central. TID: cada 8h.
La distribución por grupos de patologías encontrada en nuestra población se correlaciona con las diferentes series descritas en la literatura, siendo las neurológicas (principalmente síndrome de Guillain-Barré y miastenia gravis) y las hematológicas (púrpura trombocitopénica trombótica) las entidades en las que se usa el ITP y la PF con mayor frecuencia y en las que se cuenta con mejor evidencia para su utilización.
En comparación con la publicación de Pons-Estel et al.9, en nuestra serie predomina el sexo femenino (55,6 vs. 42%), hay una menor edad promedio (39 vs. 52,9 años), menos sesiones por pacientes (4,3 vs. 6), mayor porcentaje de lúpicos incluidos (37,5 vs. 9,6%), ausencia de casos de síndrome antifosfolípido catastrófico (0 vs. 12,9%) y de crioglobulinemias asociadas al virus de la hepatitis C y esenciales (0 vs. 19,4 y 16,1%, respectivamente). En ambas series, las indicaciones principales de los procedimientos fueron: glomerulonefritis rápidamente progresiva, hemorragia alveolar y púrpura trombocitopénica trombótica; se utilizaron, de manera concomitante, esteroides, ciclofosfamida y rituximab, y hubo una tasa de respuesta similar (82 vs. 80,6%).
Con respecto a enfermedades reumatológicas específicas, la PF y el ITP fueron útiles en lupus eritematoso sistémico con compromiso neuropsiquiátrico, resultando en recuperación completa en un paciente y parcial en el otro, concordando con los resultados publicados en la literatura. La mayor serie publicada en este contexto es de Neuwelt10, quien reportó una mejoría en el 74% de los sujetos.
Dos de los pacientes con diagnóstico confirmado de poliangiítis microscópica presentaron hemorragia alveolar difusa como manifestación principal que requirió el uso de PF; uno murió y el otro recayó de manera temprana, pero nuevamente respondió. La literatura postula a la PF como una alternativa segura y efectiva para este tipo de complicaciones, pero aún es controvertida y sin evidencia suficientemente fuerte para ser recomendada como primera línea11; se esperan resultados del estudio multicéntrico, aleatorizado y controlado PEXIVAS, que podría aportar mayor solidez a la evidencia12. El fundamento de esta investigación consiste en que existen altas tasas de morbimortalidad en pacientes con vasculitis asociadas a ANCA por enfermedad no controlada y toxicidad relacionada con el tratamiento inmunosupresor; existen pequeños estudios aleatorizados que sugieren que la PF puede mejorar el control de la enfermedad, mientras que estudios observacionales indican que las dosis altas de esteroides utilizadas como manejo estándar actual se asocian a infecciones graves en estos individuos; se plantea, entonces, un estudio aleatorizado que involucra ambas estrategias, 2 a 2, factorial; este ensayo está aleatorizando, actualmente, 500 pacientes en centros de Europa, Norteamérica, Asia y Australia para recibir PF o no y dosis altas versus bajas de glucocorticoides; todos los sujetos reciben inmunosupresión concomitante con ciclofosfamida; el desenlace primario que se pretende obtener es el tiempo en que se presente un desenlace compuesto de mortalidad por todas las causas y falla renal crónica terminal.
El tercer paciente de este grupo de patologías presentó una glomerulonefritis rápidamente progresiva secundaria a granulomatosis con poliangiítis que requirió, al egreso, terapia de reemplazo renal. El estudio MEPEX (MPDN vs. PF en pacientes con nefropatía grave asociada a vasculitis ANCA), reportó un 69% de pacientes libres de diálisis a 3 meses en el brazo de PF, comparado con un 49% en el grupo de MPDN13. Otro estudio que utilizó terapia combinada con MPDN, ciclofosfamida y PF reportó un 63 y 65% de sujetos libres de diálisis a 3 meses y a un año, respectivamente14.
En Colombia, hasta donde se sabe, existe un reporte de 8 casos de pacientes con hemorragia alveolar difusa, todos ellos en el contexto de lupus eritematoso sistémico activo, en el que se utilizó PF en 50% de ellos, con una mortalidad de 12%, estando en unidad de cuidados intensivos15.
ConclusionesLos pacientes que recibieron PF o ITP por enfermedades autoinmunes con una condición crítica que amenaza la vida o un órgano vital presentaron una favorable tasa de respuesta y de supervivencia, con un perfil aceptable de seguridad.
Las principales indicaciones de estos procedimientos en patologías autoinmunes fueron las neurológicas, seguidas de las hematológicas y reumatológicas. En este último subgrupo, fue una alternativa terapéutica salvadora de la vida en varios de los sujetos, pero cuando el compromiso involucró al sistema nervioso central o al riñón, a pesar del uso de la terapia, se presentaron secuelas permanentes. Se requieren estudios que permitan incrementar y consolidar la evidencia existente en el uso de estos procedimientos, especialmente, en el grupo de enfermedades reumatológicas.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
FinanciaciónRecursos propios.
Conflicto de interesesNinguno de los autores ha recibido incentivos por parte de compañías farmacéuticas u otros patrocinadores.