El MitraClip® (Abbott Vascular, Santa Rosa; California EU), es un dispositivo de cromo cobalto, recubierto de poliéster, que se inserta por vía vena femoral y navega hasta la aurícula izquierda a través de una punción transeptal guiada por ecocardiograma transesofágico. Se implanta con el fin de atrapar las valvas anterior y posterior de la válvula mitral justo sobre el espacio donde se genera la insuficiencia mitral severa. Su objetivo terapéutico se basa en el intento de disminuirla o abolirla. Tiene además un efecto terapéutico adicional dado que al acercar las valvas crea un efecto de anuloplastia sobre el anillo valvular mitral que mejora la remodelación ventricular izquierda y disminuye los diámetros y volúmenes ventriculares.
Es una terapia actualmente aprobada en casos seleccionados por FDA, CE Mark e Invima y avalada por la Sociedad Europea de Cardiología (ESC), la Sociedad Americana del Corazón (AHA) y el Colegio Americano de Cardiología (ACC). Desde el año 2013 está disponible para uso comercial en Colombia.
MitraClip® (Abbott Vascular, Santa Rosa, California, USA), is a cobalt chromium device covered in polyester, which is inserted through the femoral vein and travels to the left atrium through a transseptal puncture, guided by a transesophageal echocardiogram. It is implanted in order to trap the anterior and posterior mitral valve leaflets precisely over the space where severe mitral regurgitation is generated. Its therapeutic objective is to decrease or eliminate the regurgitation. It has an additional therapeutic effect, since in bringing the leaflets together it creates an annuloplasty effect on the mitral valve ring, which improves left ventricular remodeling and decreases ventricular diameters and volumes.
This treatment is currently approved in selected cases by the FDA, CE Mark and Invima, and is endorsed by the European Society of Cardiology (ESC), the American Heart Association (AHA), and the American College of Cardiology (ACC). It has been available for commercial use in Colombia since 2013.
La insuficiencia de la válvula mitral es, junto con la estenosis valvular aórtica, una de las dos patologías valvulares más comunes. Su prevalencia en estudios observacionales está alrededor del 1,7% (1,5-1,9%); sin embargo, en pacientes mayores de 75 años puede aumentar hasta el 13%1. Tradicionalmente se ha clasificado según su etiología, como primaria o aquella causada por un daño degenerativo de la válvula mitral o de su aparato subvalvular y funcional o secundaria y generalmente ocasionada por dilatación del anillo valvular y/o disfunción ventricular izquierda2–4.
Estudios observacionales multicéntricos han encontrado que el manejo temprano de la insuficiencia mitral severa independiente de su etiología con cirugía cardiovascular es superior al manejo médico óptimo expectante2–6. Sin embargo, estudios observacionales adicionales muestran como un grupo de pacientes con clara indicación quirúrgica continúan con terapia médica exclusiva por ser considerados de alto riesgo o de riesgo prohibitivo en cirugía cardiovascular7. El MitraClip® (fabricado por Abbott Vascular, Santa Rosa California EU) es un dispositivo de cromo cobalto, recubierto de poliéster, que se inserta por vía vena femoral y se lleva hasta la aurícula izquierda a través de un dispositivo complejo que incluye una punción transeptal guiada por ecocardiograma transesofágico y fluoroscopia. El dispositivo se implanta con el objetivo de atrapar las valvas anterior y posterior de la válvula mitral justo sobre el espacio donde se genera la insuficiencia mitral severa. Su objetivo terapéutico se basa en el intento de disminuirla o abolirla. Tiene además un efecto terapéutico adicional dado que al acercar las valvas crea un efecto de anuloplastia sobre el anillo valvular mitral que mejora la remodelación ventricular izquierda y disminuye los diámetros y volúmenes ventriculares2,8. Según necesidad del paciente durante el mismo procedimiento puede recibir terapia con uno o más clips2,8. Es una terapia actualmente aprobada en casos seleccionados por la FDA, CE Mark e Invima y avalada por la Sociedad Europea de Cardiología (ESC) y la Sociedad Americana del Corazón (AHA) y el Colegio Americano de Cardiología (ACC)3–5. Desde el año 2013 está disponible para uso comercial en Colombia.
EvidenciaEl reparo endovascular de la insuficiencia de la válvula mitral con dispositivo MitraClip® ha sido evaluado extensivamente con estudios experimentales aleatorizados y estudios observacionales prospectivos y retrospectivos dentro de los cuales se destacan los siguientes.
Estudio experimental Everest IIEstudio multicéntrico, aleatorizado, doble ciego donde se reclutaron en relación 2:1 pacientes para manejo con reparo endovascular con MitraClip® vs. reparo quirúrgico de válvula mitral por insuficiencia mitral severa o masiva, la mayoría de origen degenerativo (74%)8. El objetivo primario de seguridad dado por aparición de eventos adversos mayores descritos como: muerte, infarto agudo del miocardio, reoperación por cirugía fallida, cirugía cardiovascular no electiva necesaria por eventos adversos, ataque cerebrovascular, insuficiencia renal, infección de tejidos profundos, ventilación mecánica por más de 48 horas, complicaciones gastrointestinales que requieren cirugía, aparición de fibrilación auricular de novo, sepsis, necesidad de transfusión de dos o más unidades de componentes sanguíneos en los primeros 30 días mostró que el reparo endovascular con MitraClip® es significativamente superior comparado con la técnica de reparo quirúrgico de la válvula mitral (9,6% vs. 57% p< 0,001)8. El objetivo primario de efectividad definido como el punto combinado de tasa libre de muerte, reoperación o persistencia de insuficiencia mitral, residual severa o masiva después de un año de seguimiento demostró que la cirugía de reparo mitral es superior al MitraClip® (73% vs. 55,2%)8. El análisis detallado del objetivo primario compuesto de seguridad muestra cómo el único criterio significativo a favor de MitraClip® fue la necesidad de transfusión de 2 o más unidades de componentes sanguíneos (13% vs. 45% p<0,001)8. Por otro lado, el análisis detallado del objetivo primario compuesto de efectividad muestra como la necesidad de reoperación fue el único criterio significativo (37% vs. 2% p<0,001)8. La mortalidad durante el primer año de seguimiento fue similar en las dos terapias (6% vs. 6% p=1)7. El seguimiento del objetivo primario compuesto de efectividad a 4 y 5 años continúa mostrando superioridad de la técnica quirúrgica (44,2% vs. 64,3% p=0,01)8,9. Sin embargo, la mortalidad en los dos grupos tratados persiste similar y sin diferencias significativas (20,8% vs. 26,8% p=0,36%)9,10.
Dentro de los objetivos secundarios se evaluó la mejoría de la clase funcional según la escala de la Asociación del corazón de New York (NYHA, su sigla en inglés). Los pacientes tratados con cirugía de reparo mitral y con MitraClip mejoraron de una clase funcional NYHA III o IV basal de 44,8% y 45,7% (p=0,11) a 13,4% y 2% (p=0,004) en el seguimiento a un año y 6,3% y 5,7% (p=0,01) en el seguimiento a 4 años9. De manera similar se encontró una diminución discreta pero significativa de los diámetros y volúmenes sistólicos y diastólicos ventriculares izquierdos en el seguimiento de 1 y 5 años10. No se evidenció un cambio significativo en la fracción de eyección en el seguimiento de ambos grupos durante todo el seguimiento, sin embargo, debe aclararse que la fracción de eyección inicial estaba dentro de límites normales10.
Estudio Realism/Everest II High Risk prospective CohortSe trata de un estudio observacional, prospectivo, multicéntrico, realizado en Estados Unidos, que evaluó la seguridad y efectividad del tratamiento con reparo endovascular de válvula mitral con MitraClip® en pacientes con insuficiencia mitral severa o masiva, la mayoría de origen funcional (71%) y alto riesgo quirúrgico (STS score > 12) durante un año de seguimiento. Se evaluaron 351 pacientes. El dispositivo fue implantado en el 95,7% de los casos con una tasa de éxito (definida como presencia de insuficiencia residual menor que moderada) del 85,3% en el alta y la cual persistió en el 83,6% de los pacientes en el seguimiento a un año11. La evaluación de eventos adversos mayores encontró una mortalidad a 30 días del 4,8%, muy inferior a la tasa de mortalidad esperada y predicha por escala STS de 7,6% (p<0,001)11. La mortalidad a un año fue del 22,8%11. Se presentó una tasa de ataque cerebrovascular en el 2,6% de los pacientes en el seguimiento a 30 días, la cual aumentó a 3,4% en el seguimiento a un año11. La progresión a falla renal se presentó en el 1,7% en el seguimiento a 30 días y en el 5,4% en el seguimiento al año11. 2,8% de los pacientes requirieron ventilación mecánica por más de 48 horas en los primeros treinta días de seguimiento11. El evento adverso mayor más común fue la necesidad de transfusión de dos o más unidades de componentes sanguíneos en el 13,4% de los pacientes tratados11. En cuanto a complicaciones del procedimiento se presentó agarre de una sola valva en 6 pacientes (1,7%), necesidad de cirugía de válvula mitral en 1 paciente (0,3%), necesidad de un nuevo procedimiento de MitraClip® en 4 pacientes (1,1%). No se presentó embolización del clip en el primer año de seguimiento. En el año de seguimiento se encontró estenosis valvular mitral severa en 3 pacientes (0,9%)11. El seguimiento clínico al año mostró clase funcional III o IV de la NYHA en solo el 17,1% de los pacientes. Fue significativa la reducción en la hospitalización por falla cardiaca. Se encontró mejoría significativa en las escalas de calidad de vida física y mental SF-36 así como en los volúmenes ventriculares sistólicos y diastólicos en el seguimiento ecocardiográfico11.
Estudio Access EUEs un estudio observacional, prospectivo, multicéntrico, postmarketing, realizado en centros de la comunidad europea, que evaluó la seguridad y eficacia del reparo endovascular de válvula mitral con MitraClip® en pacientes con insuficiencia mitral severa o masiva y alto riesgo quirúrgico, la mayoría de origen funcional (77%). 567 pacientes fueron seguidos durante el primer año post tratamiento. Se implantó MitraClip® en el 99,6% de los pacientes; el 91,2% obtuvo un resultado exitoso al alta12. La mortalidad fue del 3,4% a 30 días y 17,3% al año de seguimiento12. Se reportó un 0,7% de ataque cerebrovascular en los primeros 30 días y 1,1% en el primer año. La progresión a falla renal fue del 4,8% en los 30 días y 8,6% al año. La tasa de complicaciones vasculares fue baja: 3,9% a 30 días y 4,8% al año12. El seguimiento clínico a un año mostró que el 71,4% de los pacientes estaban en clase funcional I o II de la NYHA. Se disminuyeron en forma significativa las tasas de rehospitalización y hubo mejoría significativa en las escalas de funcionabilidad de Minessotta y en el test de caminata de 6 minutos12.
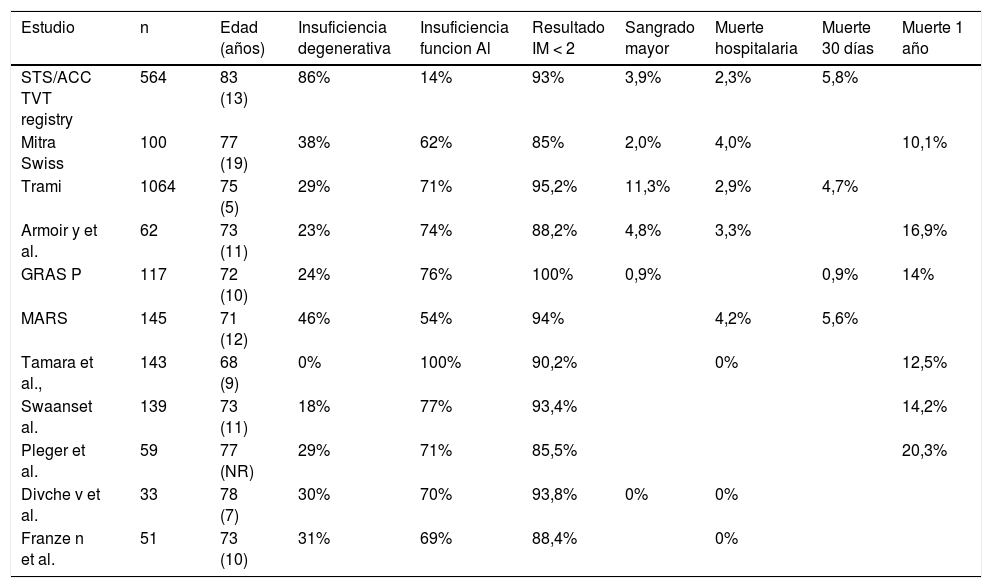
En la tabla 1 se describen otros registros observacionales con sus resultados a corto y largo plazo2,13–16.
Registros observacionales
| Estudio | n | Edad (años) | Insuficiencia degenerativa | Insuficiencia funcion Al | Resultado IM < 2 | Sangrado mayor | Muerte hospitalaria | Muerte 30 días | Muerte 1 año |
|---|---|---|---|---|---|---|---|---|---|
| STS/ACC TVT registry | 564 | 83 (13) | 86% | 14% | 93% | 3,9% | 2,3% | 5,8% | |
| Mitra Swiss | 100 | 77 (19) | 38% | 62% | 85% | 2,0% | 4,0% | 10,1% | |
| Trami | 1064 | 75 (5) | 29% | 71% | 95,2% | 11,3% | 2,9% | 4,7% | |
| Armoir y et al. | 62 | 73 (11) | 23% | 74% | 88,2% | 4,8% | 3,3% | 16,9% | |
| GRAS P | 117 | 72 (10) | 24% | 76% | 100% | 0,9% | 0,9% | 14% | |
| MARS | 145 | 71 (12) | 46% | 54% | 94% | 4,2% | 5,6% | ||
| Tamara et al., | 143 | 68 (9) | 0% | 100% | 90,2% | 0% | 12,5% | ||
| Swaanset al. | 139 | 73 (11) | 18% | 77% | 93,4% | 14,2% | |||
| Pleger et al. | 59 | 77 (NR) | 29% | 71% | 85,5% | 20,3% | |||
| Divche v et al. | 33 | 78 (7) | 30% | 70% | 93,8% | 0% | 0% | ||
| Franze n et al. | 51 | 73 (10) | 31% | 69% | 88,4% | 0% |
El tratamiento con reparo endovascular de la insuficiencia de la válvula mitral con MitraClip® se reserva para pacientes que cumplan estrictamente con los siguientes criterios17–20:
• Insuficiencia mitral severa de origen funcional o degenerativo.
• Pacientes sintomáticos (clase funcional > II NYHA) a pesar de manejo médico óptimo de falla cardiaca.
• Pacientes con riesgo alto o prohibitivo para cirugía cardiovascular.
• Pacientes que cumplan estrictamente los criterios anatómicos adecuados en la evaluación ecocardiográfica de la válvula mitral.
Los pacientes deben ser evaluados y el procedimiento debe estar respaldado por una junta médico-quirúrgica. Los miembros necesarios para su conformación se describen más adelante.
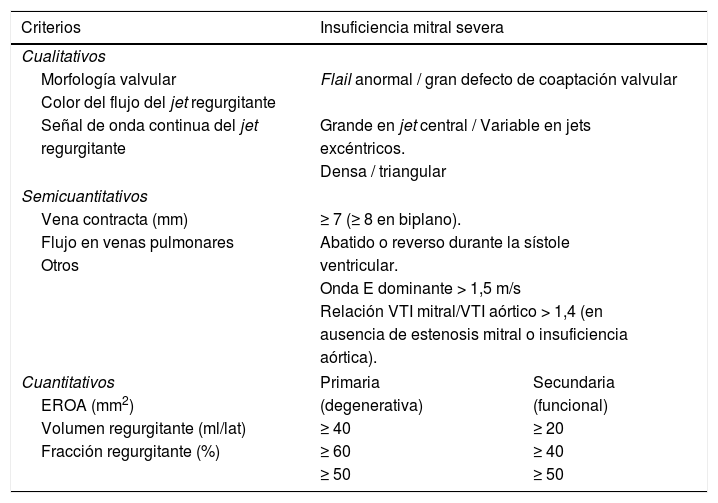
Los criterios ecocardiográficos para definir insuficiencia mitral severa de origen degenerativo o funcional se definen en la tabla 23,4,21–24.
Criterios ecocardiográficos de insuficiencia mitral severa
| Criterios | Insuficiencia mitral severa | |
|---|---|---|
| Cualitativos | ||
| Morfología valvular | Flail anormal / gran defecto de coaptación valvular | |
| Color del flujo del jet regurgitante | ||
| Señal de onda continua del jet | Grande en jet central / Variable en jets | |
| regurgitante | excéntricos. | |
| Densa / triangular | ||
| Semicuantitativos | ||
| Vena contracta (mm) | ≥ 7 (≥ 8 en biplano). | |
| Flujo en venas pulmonares | Abatido o reverso durante la sístole | |
| Otros | ventricular. | |
| Onda E dominante > 1,5 m/s | ||
| Relación VTI mitral/VTI aórtico > 1,4 (en | ||
| ausencia de estenosis mitral o insuficiencia | ||
| aórtica). | ||
| Cuantitativos | Primaria | Secundaria |
| EROA (mm2) | (degenerativa) | (funcional) |
| Volumen regurgitante (ml/lat) | ≥ 40 | ≥ 20 |
| Fracción regurgitante (%) | ≥ 60 | ≥ 40 |
| ≥ 50 | ≥ 50 | |
Se consideran pacientes con riesgo alto o prohibitivo para cirugía aquellos que presenten cualquiera de los siguientes criterios11,12:
• Escala de STS mayor o igual a 8.
• Lesiones arterioescleróticas complejas en aorta ascendente. Antecedente de irradiación de mediastino y/o tórax.
• Antecedente de mediastinitis. Cirrosis hepática.
• Dos o más cirugías torácicas previas.
• Antecedente de revascularización miocárdica con puentes permeables.
• Insuficiencia mitral funcional y fracción de eyección del ventrículo izquierdo < 40%. Edad mayor a 75 años y fracción de eyección < 40%.
Hipertensión arterial pulmonar muy severa (mayor a 2/3 de la presión arterial sistólica).
Dos o más de los siguientes factores de riesgo:
- •
Creatinina > 2,5mg/dl.
- •
Cirugía de tórax previa.
- •
Edad mayor a 75 años.
- •
Fracción de eyección del VI < 35%.
El ecocardiograma transesofágico que se realiza como parte del protocolo de evaluación y que permite declarar los pacientes como aptos para el reparo endovascular de válvula mitral debe incluir las siguientes proyecciones19,25–27:
- •
Proyección 0o superior (imagen 5 cámaras): permite visualizar segmentos A1 y P1.
- •
Proyección 0o central (imagen 4 cámaras): permite visualizar segmentos A2 y P2.
- •
Proyección 0o inferior (imagen 4 cámaras): permite visualizar segmentos A3 y P3.
- •
Proyección bicomisural (60 a 90o) rotación horaria: permite visualizar segmentos A1, A2 y A3.
- -
Proyección bicomisural (60 a 90o) posición neutra: permite visualizar segmentos P1, A2 y P3.
- -
Proyección bicomisural (60 a 90o) rotación antihoraria: permite visualizar segmentos P1, P2 y P3.
- -
Proyección tracto de salida (110-130o) rotación antihoraria: permite visualizar segmentos A1 y P1.
- -
Proyección tracto de salida (110-130o) posición central: permite visualizar segmentos A2 y P2.
- -
Proyección tracto de salida (110-130o) rotación horaria: permite visualizar segmentos A3 y P3.
- -
Proyección vena pulmonar superior izquierda (0-30o): valorar flujo con doppler pulsado y color.
- -
Proyección vena pulmonar superior derecha (90-120o): valorar flujo con doppler pulsado y color.
- -
Proyección bicava (80-110o): visualización de cava superior, septum interauricular y cava inferior.
- -
Eje corto en la base (15-45o): visualización de aorta, septum interauricular y paredes posteriores auriculares.
- -
Eje corto en transgástrico (0-20o): medición del área valvular y visualización de sitio del jet con doppler color.
- -
Proyección 3D: toma de imágenes en 3D con y sin color; ubicar válvula aórtica en meridiano 12.
- -
Para el análisis adecuado las grabaciones realizadas deben incluir al menos tres ciclos cardiacos completos con imágenes (según corresponda) en modo 2D, modo Xplane y modo 2D con color comparativo (color compare).
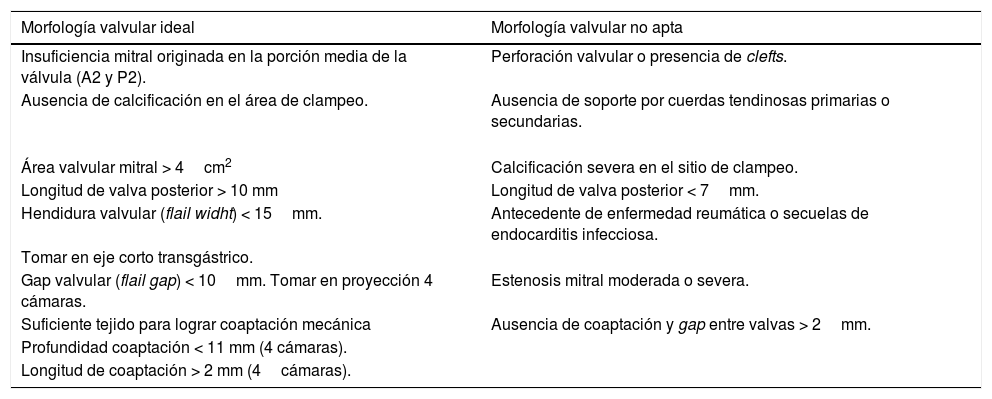
El ecocardiograma transesofágico debe aportar la información suficiente para determinar si un paciente cumple con todos los criterios anatómicos adecuados para el procedimiento, los cuales se definen en la tabla 319,28.
Morfología valvular ideal y no apta
| Morfología valvular ideal | Morfología valvular no apta |
|---|---|
| Insuficiencia mitral originada en la porción media de la válvula (A2 y P2). | Perforación valvular o presencia de clefts. |
| Ausencia de calcificación en el área de clampeo. | Ausencia de soporte por cuerdas tendinosas primarias o secundarias. |
| Área valvular mitral > 4cm2 | Calcificación severa en el sitio de clampeo. |
| Longitud de valva posterior > 10 mm | Longitud de valva posterior < 7mm. |
| Hendidura valvular (flail widht) < 15mm. | Antecedente de enfermedad reumática o secuelas de endocarditis infecciosa. |
| Tomar en eje corto transgástrico. | |
| Gap valvular (flail gap) < 10mm. Tomar en proyección 4 cámaras. | Estenosis mitral moderada o severa. |
| Suficiente tejido para lograr coaptación mecánica | Ausencia de coaptación y gap entre valvas > 2mm. |
| Profundidad coaptación < 11 mm (4 cámaras). | |
| Longitud de coaptación > 2 mm (4cámaras). |
La junta médico-quirúrgica que estudia, analiza y define si un paciente es apto para el reparo endovascular de la válvula mitral con MitraClip® debe incluir como mínimo19,29,30:
- •
Cardiólogo intervencionista (al menos uno)
- •
Cardiólogo especialista en imágenes no invasivas y ecocardiograma (al menos uno)
- •
Cirujano cardiovascular (al menos uno)
- •
Cardiólogo clínico (idealmente con entrenamiento en falla cardiaca) (al menos uno)
El reparo endovascular de válvula mitral con MitraClip® es un procedimiento de muy alta complejidad. Lo anterior sugiere que debe hacerse únicamente en centros de excelencia cardiovascular que cuenten con la tecnología y el personal médico y paramédico que se describe a continuación19,29,30:
- •
Equipo de hemodinamia de alta calidad (idealmente sala híbrida)
- •
Ecocardiograma transesofágico con capacidad de realizar imágenes 3D.
- •
Respaldo de cirugía cardiovascular.
- •
Equipo para anestesia general.
- •
Unidad de cuidado intensivo con énfasis en Patología cardiovascular.
- •
Unidad de Cardiología clínica (idealmente clínica de falla cardiaca).
- •
Unidad de Cardiología no invasiva e imágenes ecocardiográficas.
- •
De otra parte, para definir un reparo endovascular de válvula mitral con MitraClip® como procedimiento exitoso, deben cumplirse los siguientes criterios8,11,12,19,28,29:
- •
Disminución de insuficiencia mitral menor a grado II (moderado). Gradiente transvalvular mitral medio menor a 5mm Hg.
- •
Área valvular mitral efectiva mayor a 2cm2.
Ninguno.