Se presenta el caso de una paciente de 47 años de edad, remitida a nuestra institución por cuadro de la falla cardiaca aguda secundaria a la miocarditis viral, en quien se utilizó la ivabradina como terapia coadyuvante para el control de la frecuencia cardiaca en el contexto del choque cardiogénico.
The case of a 47 year-old female patient is presented. She was referred to our institution due to acute heart failure secondary to viral myocarditis, where ivabradine was used as an adjuvant therapy for controlling the heart rate in the context of a cardiogenic shock.
En pacientes con la falla cardiaca crónica, la modulación de la frecuencia cardiaca es una de las metas fundamentales del bloqueo neurohumoral. Sin embargo, en quienes no se puede titular la terapia con los betabloqueadores, el uso de la ivabradina ha demostrado beneficio en el control de la frecuencia cardiaca mejorando los desenlaces clínicos. No obstante, en el contexto de la falla cardiaca aguda y/o el choque cardiogénico, la titulación de los betabloqueadores es difícil o está contraindicado por la inestabilidad hemodinámica. Incluso más, en este grupo de pacientes la taquicardia es frecuente como mecanismo compensatorio para mantener el gasto cardiaco, llevando a un aumento del consumo de oxígeno. En estas condiciones el uso de la ivabradina puede ser una alternativa, considerando que el efecto modulador sobre la frecuencia cardiaca se traduce en una disminución del consumo de oxígeno miocárdico y la mejoría de la perfusión coronaria.
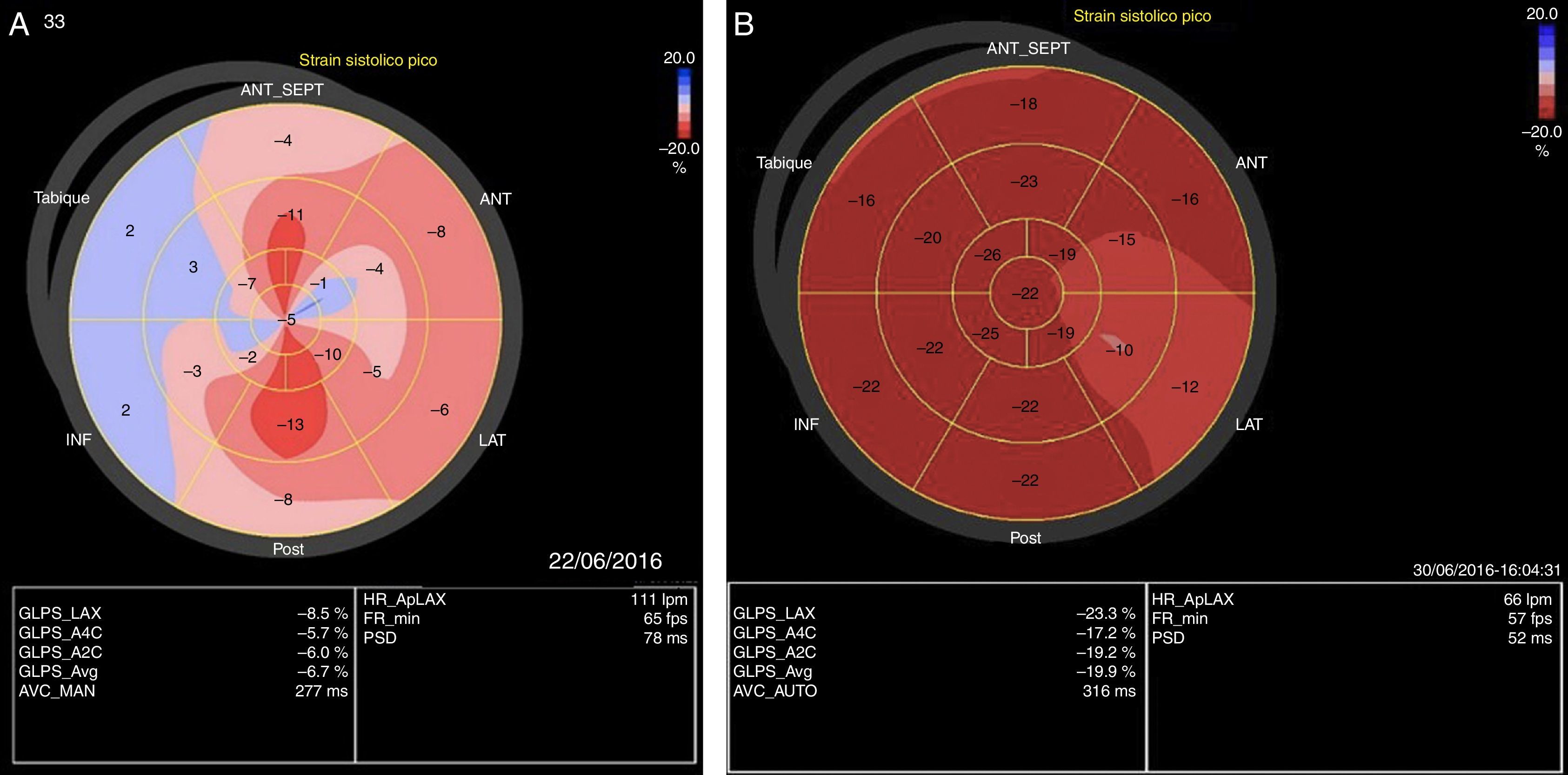
CasoSe trata de una mujer de 47 años de edad, natural y procedente de Yopal (Casanare, Colombia) quien es remitida a nuestra institución con cuadro de una semana de evolución consistente en síntomas caracterizados por: astenia, adinamia, mialgias, fiebre y deterioro de su clase funcional New York Heart AssociationIV. En el centro de origen documentan signos clínicos de la falla cardiaca aguda con evidencia de hipoperfusión que la lleva a requerir soporte vasopresor y la remiten a nuestra institución. A su ingreso, la paciente se encuentra en malas condiciones con criterios de choque cardiogénico y falla respiratoria con paraclínicos que confirman falla orgánica múltiple con compromiso de la función hepática, renal, elevación leve de troponina I (16,6n pg/ml, valor de referencia de 0,00-15,6) y gasimetría arterial que confirma disfunción pulmonar severa. El ecocardiograma de ingreso muestra hipoquinesia global moderada con función sistólica moderadamente comprometida, fracción de eyección del 35%, miocardio con aspecto edematizado y un strain longitudinal global de -8,5%. (fig. 1A). Con estos hallazgos se considera el choque cardiogénico secundario a la miocarditis aguda de etiología a establecer. Se instauró manejo con soporte ventilatorio invasivo, reanimación dirigida por metas con cristaloides isotónicos asociado a uso del vasopresor con noradrenalina a 0,5 mcg/kg/min y vasopresina a 2 unidades hora. Una vez logramos la presión arterial sistólica mayor de 90mm Hg se asoció soporte inotrópico con levosimendan a 0,1 mcg/kg/hora por 24 horas. Se inició cubrimiento antibiótico de amplio espectro, se solicitó perfil viral e inmunológico, además de policultivos. Se logró la mejoría parcial de los parámetros de perfusión tisular pero con persistencia de la taquicardia sinusal hasta de ciento treinta latidos por minuto. Se intenta control de la frecuencia cardiaca con beta-metil digoxina endovenosa, sin evidenciar respuesta. No se consideró el uso del betabloqueador dado la intestabilidad hemodinámica de la paciente. En este punto se inició la ivabradina 5 miligramos cada 12 horas para modular la frecuencia cardiaca con el objetivo de mejorar el tiempo de llenado diastólico y disminuir el consumo de oxígeno. Después de 6 horas del inicio del medicamento se obtiene disminución de la frecuencia, retiro progresivo de soporte vasoactivo, con mejoría de los parámetros de perfusión tisular (figs. 2A y 2B). Se descarta: enfermedad de Chagas, dengue, toxoplasma y mononucleosis como causa del evento. Los cultivos seriados fueron negativos. Se le realizó biopsia endomiocárdica que evidencia infiltrado linfocitario intersticial acompañado de foco aislado de cambios degenerativos del miocito, altamente sugestiva de miocarditis viral. A la paciente se le realizó el ecocardiograma transtorácico de control que evidenció mejoría importante en la contractilidad, con fracción de eyección del 55%, con strain longitudinal global de -23,3% (fig. 1B). La imagen por resonancia magnética de corazón, se realizó cuando la paciente fue retirada del ventilador, encontrando la función global preservada, con realce tardío subendocárdico y mesocárdico en los segmentos basales y medios de las paredes lateral, anterior e inferior compatibles con la miocarditis. La paciente evolucionó satisfactoriamente a clase funcional New York Heart AssociationI y es dada de alta.
Strain longitudinal global pretratamiento y postratamiento. (A) Alteración en la deformación de la fibra miocárdica principalmente en los segmentos basales y medios de la mayoría de las paredes. (B) Mejoría en la deformidad de la fibra miocárdica de forma global hasta la normalidad.
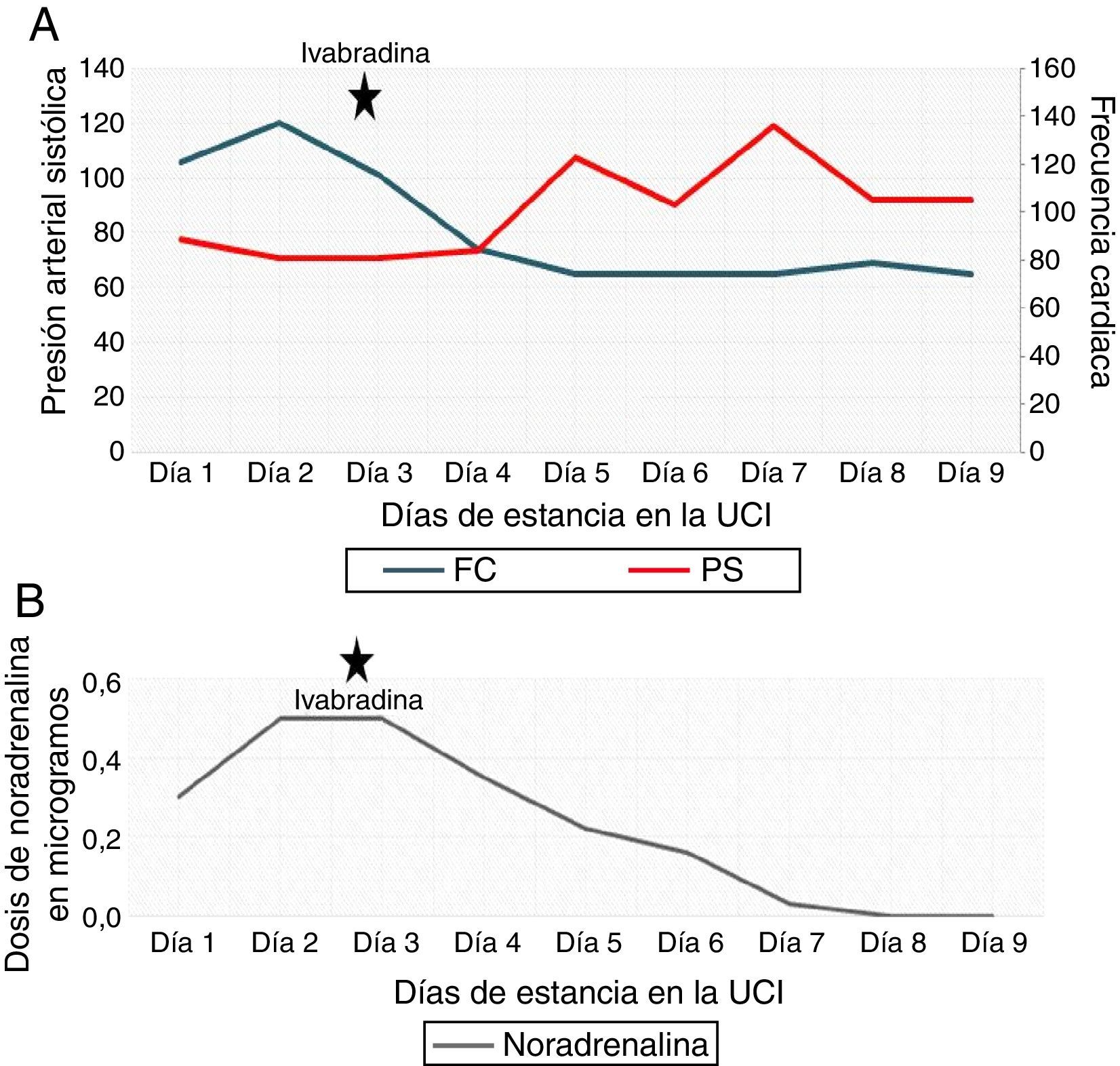
Comportamiento de la presión arterial y la frecuencia cardiaca con la ivabradina. (A) Tendencia progresiva al ascenso de la presión arterial sistólica (PS) y a la disminución de la frecuencia cardiaca (FC) posterior a la ivabradina. (B) Requerimientos de norepinefrina hasta su suspensión tras el inicio de la ivabradina.
La ivabradina es un inhibidor específico de la corriente If en el nódulo sinoauricular, cuyo efecto es disminuir la frecuencia cardiaca por un mecanismo distinto al betabloqueador. No modifica la conducción intracardiaca, la presión arterial, ni la contractilidad miocárdica, inclusive en pacientes con depresión de la función sistólica1. Su uso ha demostrado control de la frecuencia cardiaca como terapia coadyuvante en los pacientes con la falla cardiaca crónica, en quienes la titulación del betabloqueador es difícil o no se logra control de la frecuencia cardiaca, según los resultados del estudio SHIFT2. No obstante, en la falla cardiaca aguda la titulación de los betabloqueadores puede ser difícil, teniendo en cuenta los riesgos de: la inestabilidad hemodinámica, el síndrome de bajo gasto, la bradicardia o el choque cardiogénico3. En este contexto, la ivabradina podría ser considerada como el tratamiento coadyuvante en el manejo de la frecuencia cardiaca evitando el potencial compromiso hemodinámico, lo cual ha sido postulado en el estudio ETHIC - AHF, realizado en los pacientes con la falla cardiaca aguda en donde una vez se logró la estabilización hemodinámica, se adicionó la ivabradina al manejo con betabloqueadores en las primeras 24 a 48 horas, demostrando mejor control de la frecuencia cardiaca con mejoría de la fracción de eyección4. Sin embargo, en este estudio fueron excluidos los pacientes con la falla cardiaca secundaria a eventos agudos como la miocarditis, en donde consideramos que puede haber beneficio adicional, no solo en el control de la frecuencia cardiaca, sino como efecto modulador de la inflamación que está asociada a la miopericarditis per se5. En un modelo de miocarditis murino coxsackie virus B3, se estudiaron los efectos de la ivabradina y el carvedilol en los cambios histopatológicos del miocardio, el desarrollo de la fibrosis, la producción del óxido nítrico, el óxido nítrico sintasa inducible y los niveles de las citoquinas. Tanto la ivabradina como el carvedilol mostraron atenuación de las lesiones miocárdicas y a la fibrosis, inhibición de la síntesis del óxido nítrico por el óxido nítrico sintetasa inducible, y la disminución de la producción de TNF-a y IL-66. Estos hallazgos nos abren una puerta para la utilización de la ivabradina, específicamente en los pacientes con miocarditis que desarrollan falla cardiaca aguda. Se considera que la reducción de la frecuencia cardiaca con los medicamentos que no comprometan hemodinámicamente al paciente pueden influir de manera positiva en la modulación de respuesta inflamatoria, sin alterar los índices de contractilidad en las fases tempranas como terapia adyuvante, especialmente, en casos donde los betabloqueadores estén contraindicados o sea difícil su titulación, aunado a los posibles efectos fisiológicos antiinflamatorios del inhibidor de la corriente if7. No se puede concluir con esto que la ivabradina fue el medicamento con mayor impacto en la evolución positiva de la paciente; sin embargo, consideramos que los efectos fisiológicos al disminuir la frecuencia cardiaca, impactaron positivamente variables vitales de la paciente y fueron un factor importante para los resultados favorables del evento.
ConclusiónAunque en el momento no haya evidencia suficiente disponible para realizar una recomendación para el uso de la ivabradina en el contexto de la falla cardiaca aguda y el choque cardiogénico asociado a la miocarditis viral, se abren las puertas para realizar estudios que evalúen el impacto en el control de la frecuencia cardiaca y si la modulación puede tener resultados positivos en los pacientes seleccionados, especialmente en casos refractarios a otras terapias con mayor evidencia y/o el uso del betabloqueador esté contraindicado.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores manifiestan no tener conflicto de intereses.