Describir la experiencia clínica de una serie de casos de pacientes adultos con hipertensión pulmonar tromboembólica crónica, llevados a tromboendarterectomía pulmonar.
MétodosEstudio descriptivo, retrospectivo, de ocho pacientes adultos llevados a tromboendarterectomía pulmonar en la Fundación Cardiovascular de Colombia, entre febrero de 2010 y abril de 2013.
Resultadosse evaluaron 5 mujeres y 3 hombres, con promedio de edad 45±18 años, datos basales promedio de SpO2 92±2%, PaO2/FiO2 244±82, PaCO2 28,8±3,4mm Hg, presión pulmonar media 53±11mm Hg y resistencia vascular pulmonar (RVP) 999±414dyn/s/cm−5. Al tercer día postoperatorio un paciente necesitó oxigenación con membrana extracorpórea (ECMO) venoarterial por 11 días. A los 4±1días de tromboendarterectomía pulmonar, la RVP descendió 71±21% respecto al valor basal (p=0,002, IC 95%) y la presión pulmonar media disminuyó 32±27mm Hg (p=0,001). La SpO2 basal aumentó 96±3%. La sobrevida fue del 100% a los 24 meses de seguimiento, sin reingresos ni recurrencia de tromboembolia pulmonar.
ConclusionesLos resultados institucionales fueron adecuados a corto y mediano plazo. En casos de edema por reperfusión la alternativa de ECMO como soporte vital extracorpóreo es indispensable.
To describe clinical experience of a series of cases of adult patients with chronic thromboembolic pulmonary hypertension who underwent pulmonary thromboendarterectomy.
MethodsDescriptive retrospective study of eight adults who underwent pulmonary thromboendarterectomy at the Fundación Cardiovascular de Colombia between February 2010 and April 2013.
Results5 women and 3 men were assessed, with an average age of 45±18 years, with avergae baseline data of SpO2 92±2%, PaO2/FiO2 244±82, PaCO2 28.8±3.4mmHg, average pukmonary pressure of 53±11mmHg and pulmonary vascular resistance (PVR) of 999±414dyn/s/cm−5. On the third postoperative day one patient required veno-arterial extracorporeal membrane oxygenation (ECMO) during 11 days. At 4±1 days after pulmonary thromboendarterectomy, PVR decreased 71±21% with regards to baseline value (p=0.002, IC 95%) and pulmonary pressure was reduced to 32±27mmHg (p=0.001). Baseline SpO2 increased 96±3%. Survival rate was 100% after 24 months of follow-up, without readmissions or recurrence of pulmonary thromboembolism.
ConclusionsInstitutional results were adequate in the short and medium term. Cases with reperfusion edema, the alternative of ECMO as an extracorporeal life support is imperative.
La hipertensión pulmonar tromboembólica crónica es una causa común de hipertensión pulmonar, cuya incidencia es cercana al 4% (forma parte del grupo 4 de la clasificación clínica de hipertensión pulmonar de Dana Point 2008). Se calcula que del 0,1 al 0,5% de los pacientes que sobreviven a una tromboembolia pulmonar aguda, pueden desarrollar hipertensión pulmonar tromboembólica crónica1,2, entidad que se caracteriza por una obstrucción crónica causada por trombos organizados en las arterias pulmonares y sus ramas lobares y/o segmentarias, fenómeno que conduce a un aumento en las presiones pulmonares, a resistencia vascular pulmonar (RVP) y finalmente a falla del ventrículo derecho3. La hipertensión pulmonar tromboembólica crónica se define como la elevación de la presión media de la arteria pulmonar por encima de 25mm Hg, que persiste por más de 6 meses después de realizado el diagnóstico de tromboembolia pulmonar4.
Aproximadamente, 40% de los pacientes con tromboembolia pulmonar pueden ser asintomáticos, hecho que dificulta hacer el diagnóstico diferencial. Los síntomas aparecen cuando se compromete entre el 40 al 50% de la circulación pulmonar (disnea, fatiga, síncope, dolor torácico, hemoptisis e insuficiencia cardíaca derecha)5.
La hipertensión pulmonar tromboembólica crónica severa tiene un promedio de sobrevida a 3 años de menos del 20%2 y es una de las causas de hipertensión pulmonar con posibilidad de tratamiento quirúrgico potencialmente curativo a través de la tromboendarterectomía pulmonar6.
En el momento de la cirugía la anatomía patológica se categorizó según la clasificación de Jamieson7,8:
- •
Tipo I: se define por la presencia de un trombo fresco en las arterias lobares, lo que ocurre aproximadamente en el 25% de los casos y genera una mortalidad quirúrgica del 2,2%.
- •
Tipo II: se origina por el engrosamiento crónico de la íntima en la proximidad de las arterias segmentarias, lo que ocurre en cerca del 40% de casos y tiene aproximadamente 5,3% de mortalidad durante el procedimiento quirúrgico.
- •
Tipo III: es la enfermedad de la íntima, limitada a las arterias segmentarias la cual se da en cerca del 30% de casos, con una mortalidad intraquirúrgica del 5%.
- •
Tipo IV: se define como la vasculopatía arteriolar distal con enfermedad tromboembólica no visible (< 5% de casos), la cual tiene cerca del 24% de riesgo de mortalidad durante la cirugía.
La falla ventricular derecha derivada de la hipertensión pulmonar severa que le impone la vasculatura pulmonar, ha sido la principal causa de complicación de los pacientes llevados a tromboendarterectomía pulmonar. Los medicamentos usados en el manejo de la hipertensión pulmonar en esta fase, tienen una utilidad limitada debido a que el mecanismo fisiopatológico principalmente involucrado en su desarrollo es mecánico y sólo se resolverá al retirar el trombo del árbol pulmonar2.
Algunos factores de riesgo o entidades asociados al desarrollo de hipertensión pulmonar tromboembólica crónica son el antecedente de tromboembolia pulmonar, principalmente de aparición a temprana edad con grandes defectos de perfusión, trombosis venosa profunda, esplenectomía, infecciones por catéteres endovenosos o marcapasos, colitis ulcerosa crónica, enfermedades inflamatorias crónicas, lupus eritematoso sistémico, síndrome antifosfolípidos, mutación del factor V de Leiden, anomalías de la hemoglobina, aumento de los niveles de factor VIII, cortocircuitos auriculoventriculares, enfermedades neoplásicas y tratamiento sustitutivo con levotiroxina2,5.
En 1970, Nina Braunwald realizó la primera cirugía de tromboendarterectomía pulmonar con éxito en la Universidad de California en San Diego, el centro médico de mayor reconocimiento y experiencia en el mundo9,10. En dicha institución, la mortalidad global ha disminuido hasta 2,2%, teniendo en cuenta que en el subgrupo con RVP preoperatoria mayor a 1.000dyn/s/cm−5 la mortalidad fue del 4,1%, mientras que en el subgrupo con RVP prequirúrgica menor a 1.000dyn/s/cm−5 fue del 1,6%7.
Sin embargo, cabe resaltar que Jamieson et al. indicaron que para un grupo con alta experiencia en tromboendarterectomía pulmonar no hay grado de obstrucción embólica dentro del árbol vascular pulmonar que sea inaccesible y ningún grado de fallo ventricular derecho, insuficiencia tricuspídea o nivel de resistencia pulmonar que sean inoperables8.
Materiales y métodosSe realizó un estudio descriptivo retrospectivo en el que la población estuvo conformada por 8 pacientes adultos con diagnóstico de tromboembolia pulmonar crónica, que fueron llevados a tromboendarterectomía pulmonar durante el periodo comprendido entre febrero del 2010 y abril del 2013 en la Fundación Cardiovascular de Colombia, institución de cuarto nivel de atención y de referencia en el nororiente colombiano.
La información se recolectó mediante la revisión de las historias clínicas en medios electrónico y físico. Para su tabulación se utilizó Microsoft Excel 2010 y para el análisis estadístico se usó el programa IBM® SPSS® Statistics, versión 21.
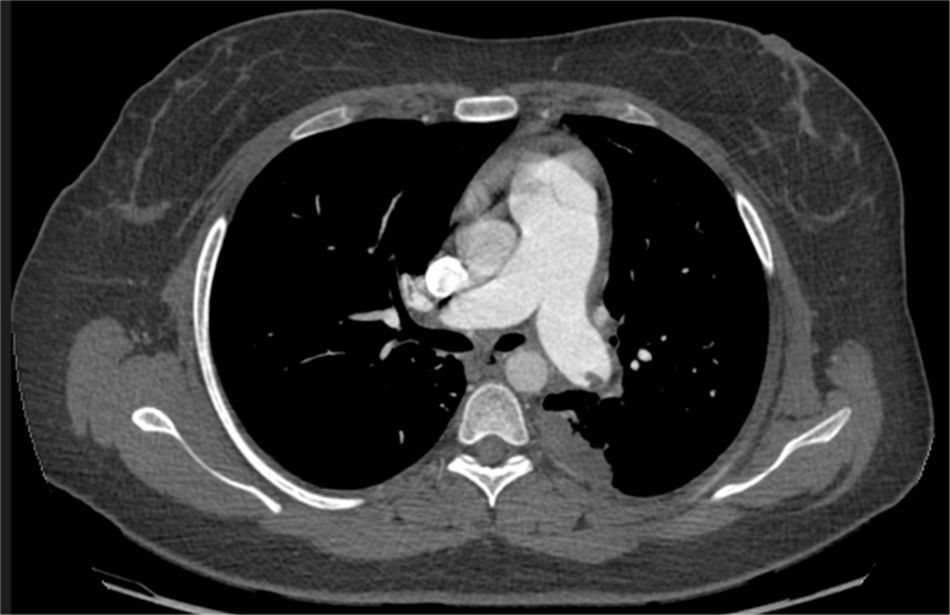
La tromboendarterectomía pulmonar estuvo indicada en pacientes sintomáticos con compromiso hemodinámico, entendido como presión arterial pulmonar media (PAPm) mayor a 30mm Hg, resistencia vascular pulmonar (RVP) mayor a 300 dynas/s/cm−5, además de compromiso respiratorio en reposo o durante el ejercicio (clase funcional II, III y IV) con evidencia de obstrucción completa de una arteria pulmonar, obstrucción proximal de arterias segmentarias o subsegmentarias (fig. 1) y ausencia de comorbilidades significativas como enfermedad pulmonar obstructiva o restrictiva, falla renal, o edad mayor a 80 años.
La única contraindicación absoluta de tromboendarterectomía pulmonar fue la presencia de una enfermedad pulmonar subyacente de alta severidad, ya fuera obstructiva o restrictiva.
Se determinó si los pacientes eran candidatos a cirugía o no, mediante la clasificación anatómica de Jamieson.
El manejo anestésico de aquellos a quienes se les hizo tromboendarterectomía pulmonar fue un reto debido a la posibilidad de colapso cardiovascular y respiratorio durante la inducción, el mantenimiento y el destete de la circulación extracorpórea.
La inducción anestésica se realizó con FiO2 del 100%, en la mayoría de casos, en posición semisentado, con una técnica balanceada, titulación lenta de midazolam y fentanilo, hasta llegar a la inconsciencia y relajación neuromuscular con pancuronio. El objetivo hemodinámico estaba enfocado en mantener unas presiones sistémicas por encima de las pulmonares para garantizar una presión de perfusión adecuada del ventrículo derecho; en todos los casos esto se logró mediante manipulación del lecho arterial sistémico con norepinefrina y/o vasopresina. La monitorización que se utilizó fue una línea arterial radial y femoral, un catéter de arteria pulmonar con medición del gasto cardíaco continuo y SvcO2, el cual sólo se avanzó hasta el ventrículo derecho en la inducción por el alto riesgo de obstrucción total del flujo pulmonar con el catéter y el trombo pulmonar. Con la medición de las presiones de las cavidades derechas se podía calcular la presión de perfusión del ventrículo derecho y a su vez inferir la presión sistólica de la arteria pulmonar; este catéter era avanzado hasta la arteria pulmonar bajo visión directa al terminar la tromboendarterectomía, justo antes del destete de la circulación extracorpórea para guiar el manejo posterior en la unidad de cuidados intensivos. En quienes el procedimiento se realizó en arresto circulatorio bajo hipotermia profunda, había 10% más de riesgo de desarrollar lesión neurológica en el postoperatorio, secundaria a las pérdidas de autorregulación cerebral, por lo cual los paros circulatorios estuvieron guiados con monitorización de suficiencia de la circulación cerebral y consumo cerebral de oxígeno utilizando un catéter yugular ascendente mono lumen 20 Fr, del cual se corroboró su colocación mediante gasimetría con saturación venosa del bulbo de la yugular (SyaO2) que debía estar entre 50-60%. El objetivo del manejo del consumo cerebral de oxígeno durante el arresto, estaba encaminado a lograr SyaO2 por encima de 90%, lo cual se obtenía con hipotermia profunda (alrededor de 25°C) y profundidad anestésica con una infusión continua de midazolam, fentanil y sevofluorano. La monitorización de la SyaO2 se realizaba cada cinco minutos, y se reanudaba la circulación extracorpórea cuando la SyaO2 caía por debajo de 70% y se perfundía hasta obtener nuevamente SyaO2 superior al 90%, y así sucesivamente hasta terminar la tromboendarterectomía.
En cuanto al manejo ventilatorio, las presiones respiratorias no debían aumentar aún más las presiones vasculares pulmonares. La instauración de una presión positiva al final de la espiración (PEEP) óptima fue fundamental, y se calculó con el punto de inflexión inferior de la curva de flujo-volumen; la PEEP óptima ayudó a disminuir las resistencias vasculares pulmonares al aumentar el área de sección transversal de la microcirculación pulmonar al reclutar los vasos extraalveolares. Se ajustaron los menores volúmenes pulmonares, la frecuencia respiratoria y la relación inspiración espiración (I:E), con los cuales se tuviese un adecuado CO2 arterial o similar al basal del paciente antes de la inducción.
El procedimiento quirúrgico se realizó mediante una esternotomía mediana con doble cánula venosa (bicava). Se colocó un aspirador de bomba en el tronco de la arteria pulmonar, dirigido a la rama pulmonar que se intervendría en última instancia, y un segundo aspirador de bomba que ingresó a través de la vena pulmonar superior derecha, dirigido hacia el ventrículo izquierdo.
En circulación extracorpórea se enfrió de manera gradual hasta obtener la SyaO2 deseada; se disecó el tronco y las ramas pulmonares y se seccionó el ligamento arterioso. Se pinzó la aorta y se pasó a cardioplejía sanguínea anterógrada y retrógrada previo a entrar en arresto circulatorio. El abordaje inicial se realizó en la rama derecha mediante incisión longitudinal y se inició la endarterectomía tratando de remover en bloque desde el tronco hacia las ramas segmentarias y subsegmentarias (con cánula de aspiración-disección de Jamieson conectada a un equipo salvador de células). Una vez finalizada la endarterectomía derecha y obteniéndose abundante reflujo sanguíneo retrógrado, se realizó plastia de la arteria pulmonar con parche de pericardio, ampliando su luz, y se pasó a realizar el mismo proceso en el lado contralateral. Se utilizó agente hemostático BioGlue® Surgical Adhesive.
Al terminar la tromboendarterectomía se inició el calentamiento gradual hasta 37°C con vasodilatación activa para asegurar que fuera homogéneo; al llegar a 36,5°C se inició la reperfusión pulmonar en donde se bajó el flujo de la bomba hasta 1,8 L/m2/min con una FiO2 de gases al oxigenador a 50%. Se pinzó la línea venosa hasta lograr una presión arterial sistólica pulmonar no mayor de 30mm Hg. El ventilador se mantuvo con una FiO2 menor de 40%, una presión pico de 21mm Hg, y capnografía de 10 – 15mm Hg, todo durante 15 minutos.
El destete de la circulación extracorpórea se realizó con milrinone y norepinefrina, y se comenzó la administración de vasodilatadores pulmonares en caso de requerirlo. El manejo estuvo encaminado a tener presiones pulmonares por debajo del 50% de las presiones sistémicas, cifra que se lograba mediante la administración de óxido nítrico o epoprostenol.
El manejo ventilatorio estuvo dirigido a disminuir el edema de reperfusión así como las presiones pulmonares, y a lograr un nivel óptimo de CO2 y oxigenación, para lo cual se ajustaron los parámetros de PEEP entre 6 - 10cm H20; la FiO2 bajó para obtener una buena oxigenación y se modificó el volumen minuto para tener un CO2 de 35 – 40mm Hg.
Siempre se tuvo disponible un circuito de oxigenación con membrana extracorpórea (ECMO) para el manejo posterior a la circulación extracorpórea.
El manejo posoperatorio se centró en los siguientes aspectos:
- 1.
Mantener ventilación mecánica hasta por 48 horas en modo presión control ajustando la PEEP de acuerdo con la tolerancia hemodinámica del paciente.
- 2.
Vigilar la aparición del edema por reperfusión, complicación que se ha descrito en el 20% de los pacientes, con una mortalidad cercana al 2%, la cual se puede presentar desde las 24 horas hasta las 72 horas posoperatorias. Se trata de un edema de tipo no cardiogénico, es decir, de gran permeabilidad, secundario a la lesión pulmonar, localizado principalmente en el área donde se realizó la endarterectomía, y en el peor de los escenarios estaba disponible la membrana de oxigenación extracorpórea.
- 3.
Hacer monitorización neurológica.
- 4.
Vigilar la aparición de hemoptisis, que podría hacer sospechar disección intrapulmonar.
- 5.
Realizar manejo cardiovascular enfocado a preservar la función ventricular derecha, para mantener así una precarga óptima y asegurar una diuresis adecuada, buscando balance acumulado negativo; para ello se utilizó hemodiafiltración veno-venosa cuando fue necesario.
- 6.
Iniciar, tan pronto como fuera posible, anticoagulación con heparina en infusión.
El postoperatorio se basó en los siguientes escenarios clínicos:
- 1.
En caso de disminución abrupta y significativa de la presión pulmonar media con aumento del gasto cardíaco y vasodilatación sistémica, el manejo consistió en administración mesurada de líquidos, normalización del gasto cardíaco y utilización de vasopresores.
- 2.
En caso de aumento de la presión media de la arteria pulmonar, del gasto cardíaco y vasodilatación sistémica que podía desencadenar edema de reperfusión e insuficiencia ventricular derecha secundaria, el manejo consistió en restricción de líquidos, normalización del gasto cardíaco y administración de diuréticos.
- 3.
En el peor de los casos, cuando la presión media de la arteria pulmonar fue muy elevada, asociada a bajo gasto cardíaco, falla cardíaca derecha y disfunción multiorgánica el manejo incluyó restricción de líquidos, diuréticos, inotrópicos, hemodiafiltración veno-venosa continua y ECMO.
Entre febrero de 2010 y abril de 2013 se diagnosticaron aproximadamente 100 casos de tromboembolia pulmonar, de los cuales 8 fueron tratados con tromboendarterectomía pulmonar. El rango de edades osciló entre 28 y 80 años (para un promedio de 45,2±18,4 años) con un 37% de hombres. El tiempo promedio desde el inicio de la sintomatología y la cirugía fue de 25,3±25,1 meses. Todos consultaron por disnea, además de síncope (25%), hemoptisis (12%), dolor abdominal (25%), lipotimia (12%) y dolor torácico (50%). La recurrencia de tromboembolia pulmonar fue confirmada en el 50% de los casos. El antecedente de trombosis venosa profunda fue documentado en el 50% de los pacientes, 25% tenía como comorbilidad síndrome antifosfolípidos y 12% lupus eritematoso sistémico (tabla 1).
Características de los pacientes al momento del diagnóstico
| Variable | Porcentaje |
|---|---|
| Hombres | 3 (37%) |
| Edad | 45,2±18,4 (28 – 80) |
| IMC | 24,1±4 (17,6 – 31,2) Bajo peso: 1 (12%), normal: 4 (50%), sobrepeso: 2 (25%), Obesidad: 1 (12%) |
| Clase funcional NYHA | III: 3 (37%) IV: 5 (62%) |
| Tabaquismo | 3 (37%) |
| EPOC | 1 (12%) |
| Filtro de Vena Cava | 8 (100%) |
| Euroscore | 6,3±3,7 (3,1 – 12,4) |
| Estadio renal MRDR | I: 2 (25%) II: 2 (25%) III: 3 (37%) IV: 1 (12%) |
| Tiempo (meses) desde el inicio de los síntomas hasta la cirugía | 25,3±25,1 (1 – 72) |
| Síndrome antifosfolípidos | 2 (25%) |
| Lupus eritematoso sistémico | 1 (12%) |
| Trombosis venosa profunda | 4 (50%) |
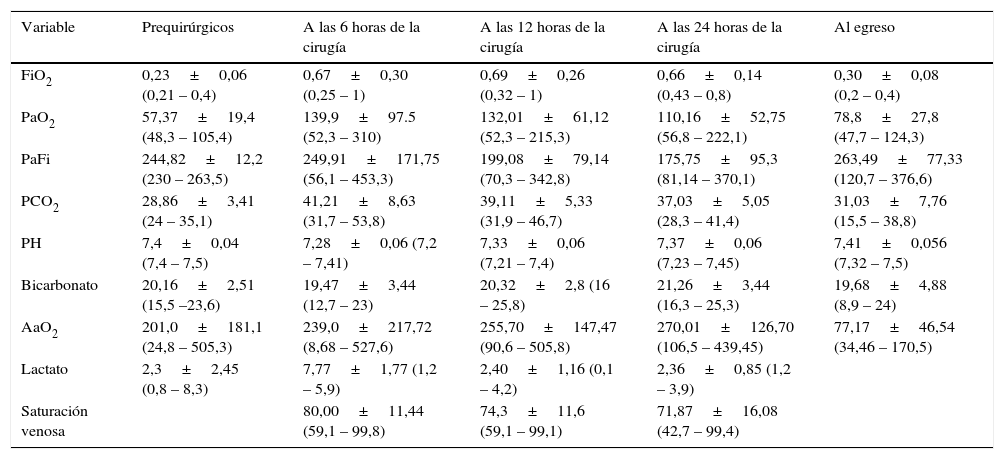
El estudio hemodinámico pulmonar mostró hipertensión pulmonar con RVP (promedio 999±414 dynas/s/cm−5) y PMAP elevadas (promedio de 53,3±12mm Hg). Tres pacientes mostraron una RVP>1000dyn/s/cm−5. Los gases arteriales antes de la cirugía mostraron una SpO2 92±2%, una PaO2/FiO2 244±12mm Hg y una PaCO2 28,8±3,4mm Hg; estos gases arteriales fueron realizados mientras se utilizaban diferentes dispositivos de administración de oxígeno a alto flujo (tabla 2).
Gases arteriovenosos
| Variable | Prequirúrgicos | A las 6 horas de la cirugía | A las 12 horas de la cirugía | A las 24 horas de la cirugía | Al egreso |
|---|---|---|---|---|---|
| FiO2 | 0,23±0,06 (0,21 – 0,4) | 0,67±0,30 (0,25 – 1) | 0,69±0,26 (0,32 – 1) | 0,66±0,14 (0,43 – 0,8) | 0,30±0,08 (0,2 – 0,4) |
| PaO2 | 57,37±19,4 (48,3 – 105,4) | 139,9±97.5 (52,3 – 310) | 132,01±61,12 (52,3 – 215,3) | 110,16±52,75 (56,8 – 222,1) | 78,8±27,8 (47,7 – 124,3) |
| PaFi | 244,82±12,2 (230 – 263,5) | 249,91±171,75 (56,1 – 453,3) | 199,08±79,14 (70,3 – 342,8) | 175,75±95,3 (81,14 – 370,1) | 263,49±77,33 (120,7 – 376,6) |
| PCO2 | 28,86±3,41 (24 – 35,1) | 41,21±8,63 (31,7 – 53,8) | 39,11±5,33 (31,9 – 46,7) | 37,03±5,05 (28,3 – 41,4) | 31,03±7,76 (15,5 – 38,8) |
| PH | 7,4±0,04 (7,4 – 7,5) | 7,28±0,06 (7,2 – 7,41) | 7,33±0,06 (7,21 – 7,4) | 7,37±0,06 (7,23 – 7,45) | 7,41±0,056 (7,32 – 7,5) |
| Bicarbonato | 20,16±2,51 (15,5 –23,6) | 19,47±3,44 (12,7 – 23) | 20,32±2,8 (16 – 25,8) | 21,26±3,44 (16,3 – 25,3) | 19,68±4,88 (8,9 – 24) |
| AaO2 | 201,0±181,1 (24,8 – 505,3) | 239,0±217,72 (8,68 – 527,6) | 255,70±147,47 (90,6 – 505,8) | 270,01±126,70 (106,5 – 439,45) | 77,17±46,54 (34,46 – 170,5) |
| Lactato | 2,3±2,45 (0,8 – 8,3) | 7,77±1,77 (1,2 – 5,9) | 2,40±1,16 (0,1 – 4,2) | 2,36±0,85 (1,2 – 3,9) | |
| Saturación venosa | 80,00±11,44 (59,1 – 99,8) | 74,3±11,6 (59,1 – 99,1) | 71,87±16,08 (42,7 – 99,4) |
El tiempo promedio de circulación extracorpórea fue de 245±34 (193 – 282) minutos. El tiempo promedio de arresto circulatorio fue de 44±20 (20 – 71) minutos. La media del tiempo de clampeo fue de 95±56 (20 – 181) minutos.
Además de la tromboendarterectomía pulmonar, en el 37% de los casos se realizó plastia tricuspídea y en el 12% cierre de foramen oral y revascularización miocárdica de un vaso. En el postoperatorio inmediato todos los pacientes pudieron ser destetados de la circulación extracorpórea con el manejo médico instaurado; sin embargo, uno requirió ECMO al tercer día postoperatorio y durante once días por presentar edema de reperfusión.
El tiempo promedio de estancia en la unidad de cuidados intensivos fue de 20,7±13 días (mediana de 21 días), en tanto que la mediana del tiempo de ventilación mecánica invasiva fue de 57,5 horas. El promedio del tiempo de estancia hospitalaria posterior a la cirugía fue de 63±49 días (mediana de 54 días).
El seguimiento promedio fue de dos años, con una sobrevida del 100%. Ese mismo porcentaje de pacientes tenía filtro de vena cava inferior previo a la cirugía.
En cuanto a medicamentos, en el 100% de los casos se usaron inhibidores de la fosfodiesterasa III, en el 75% inhibidores de la fosfodiesterasa V, en el 37% análogos de prostanoides, en el 62% óxido nítrico, en el 25% antagonistas del receptor de endotelina, en el 12% sensibilizadores de los canales de calcio y en el 12% catecolaminas, todos bajo la premisa que no existe un predictor de normalización de la presión pulmonar preoperatoria ni transoperatoria, y en consecuencia por la potencial existencia de hipertensión pulmonar residual.
Un paciente requirió traqueostomía, uno presentó mediastinitis, el 37% presentó delirium y el 12% corea con trastorno de ansiedad. Uno fue reintervenido por sangrado que requirió toracotomía por hemotórax masivo. Dos presentaron trastornos del ritmo cardíaco, una taquiarritmia supraventricular y una arritmia ventricular, que se revirtieron con medicamentos. Tres necesitaron ventilación mecánica invasiva prolongada por más de 96 horas.
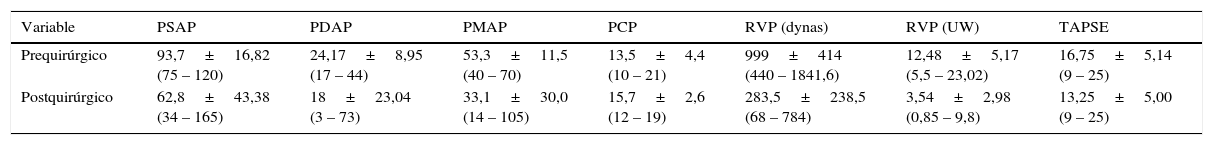
Posterior al procedimiento quirúrgico, los síntomas y los parámetros hemodinámicos mejoraron de manera sustancial: la mediana de RVP pasó de 952 dynas/s/cm−5 a 240 dynas/s/cm−5 (cambio -75%, p=0,002), disminuyó en todos los casos y mostró normalización en 5 de ellos; en los 3 restantes estuvo por debajo de 450dyn/s/cm−5. La mediana de la presión de arteria pulmonar sistólica descendió de 90 a 47mm Hg, mientras que la presión media de la arteria pulmonar cayó de 49 a 21mm Hg (p=0,001), datos obtenidos por mediciones invasivas en la unidad de cuidados intensivos en promedio a los 4±1 días de la cirugía. La presión pulmonar sistólica medida en el ecocardiograma transtorácico en promedio a los 190±367 días, disminuyó de 97±20mm Hg a 51±15mm Hg (tabla 3). La ecocardiografía mostró mejoría de los parámetros de presión y función ventricular derecha reflejados en el desplazamiento sistólico del anillo tricuspídeo (TAPSE), aunque en 3 de ellos se ha mantenido por debajo de lo aceptado como normalidad a pesar de la ausencia de hipertensión pulmonar residual y la no recurrencia de tromboembolia pulmonar durante el seguimiento. Dos pacientes mostraron persistencia de insuficiencia tricuspídea grado III/IV.
Variables hemodinámicas
| Variable | PSAP | PDAP | PMAP | PCP | RVP (dynas) | RVP (UW) | TAPSE |
|---|---|---|---|---|---|---|---|
| Prequirúrgico | 93,7±16,82 (75 – 120) | 24,17±8,95 (17 – 44) | 53,3±11,5 (40 – 70) | 13,5±4,4 (10 – 21) | 999±414 (440 – 1841,6) | 12,48±5,17 (5,5 – 23,02) | 16,75±5,14 (9 – 25) |
| Postquirúrgico | 62,8±43,38 (34 – 165) | 18±23,04 (3 – 73) | 33,1±30,0 (14 – 105) | 15,7±2,6 (12 – 19) | 283,5±238,5 (68 – 784) | 3,54±2,98 (0,85 – 9,8) | 13,25±5,00 (9 – 25) |
En el postoperatorio, el 87% de los pacientes fue evaluado con test de marcha. La SpO2 en reposo en el preoperatorio era de 91±2% mostrando un aumento a 95±2% en el postoperatorio, datos que se reflejan en normalización de la pulsoximetría en reposo sin oxígeno suplementario. Durante el ejercicio la SpO2 mínima pasó de 83±2% a 87±4%, de ahí que se resalta que en 5 pacientes hubo ausencia de desaturación ante el ejercicio, si bien a 3 de ellos fue posible realizarles dicha prueba antes de la cirugía por la disminución de la clase funcional presentada, y sólo a 7 en el postoperatorio; al paciente restante no se les realizó este test debido a dificultad en la marcha por enfermedad osteoarticular (tabla 4).
En cuanto a las pruebas de función pulmonar, es importante resaltar la ausencia de deterioro en términos de volúmenes pulmonares dinámicos o estáticos a pesar de la intervención por esternotomía o las complicaciones inmediatas. Por el contrario, las evaluaciones postoperatorias muestran que en todos los pacientes aumentaron los valores de FEV1 en una media del 24% (15-63%). No se dispone de evaluaciones de la capacidad de transferencia del CO en todos los pacientes en el periodo postoperatorio tardío, lo cual limita de evaluación de sus potenciales cambios tras la tromboendarterectomía pulmonar.
DiscusiónEl estudio incluyó la descripción de los primeros 8 casos de tromboendarterectomía pulmonar realizados en una institución cardiovascular de referencia nacional. En primer lugar, es importante resaltar el modelo de atención fundamentado en la participación y el sentido de pertenencia de un grupo multidisciplinario para el proceso, tanto diagnóstico como terapéutico, de todos los pacientes, dando origen a una Unidad Funcional para el Manejo de la tromboembolia pulmonar, tanto aguda como crónica en la que se incluye tanto personal médico como de enfermería, fisioterapia, terapia respiratoria y radiología, además de personal de apoyo asistencial y administrativo.
En segundo lugar, es necesario destacar los excelentes resultados en términos del 100% de sobrevida a largo plazo con un promedio de 24 meses de seguimiento, teniendo en cuenta que los desenlaces más robustos son proporcionales a la experiencia y el volumen de pacientes intervenidos en un centro determinado y un grupo consolidado. Específicamente, se considera que la mortalidad oscila en proporciones del 17% en los primeros 200 pacientes que fueron operados en el Centro médico de San Diego en California, el centro con mayor experiencia en esta cirugía en el mundo, y posteriormente en 1990 se realizó un cambio significativo en la técnica quirúrgica y la mortalidad bajó a 8,8% en los siguientes 500 pacientes durante 4 años, logrando una disminución de la mortalidad en 4,4% en los últimos 500 pacientes operados entre 1998 y 2002; en las últimas 500 cirugías reportadas en 2012 por este grupo, la mortalidad disminuyó a 2,2%, e incluso llegó a cero en los últimos 260 casos7,11. Los reportes de mortalidad hospitalaria en otras instituciones del mundo, varían desde 10% en 28 pacientes para el grupo de Italia12, 24% en 50 pacientes para el grupo de Dinamarca13, 10% en 69 pacientes para el grupo de Alemania14 y 15% en 41 pacientes para el grupo de Argentina5.
En nuestra institución, la ausencia de casos de mortalidad no puede ser analizada de manera aislada, sino integral, ya que se han normalizado los procesos de selección, intervención, control postoperatorio y tratamiento previo al alta con base en publicaciones y experiencias de grupos consolidados y de amplia experiencia. Por otra parte, conviene mencionar la morbilidad asociada en el período postoperatorio inmediato, la cual implicó estrategias avanzadas de tratamiento en 7 pacientes, incluyendo tratamiento específico vasodilatador pulmonar, procedimientos diagnósticos invasivos (por ejemplo, endoscopia respiratoria), antibiótico-terapia de espectro ampliado, ventilación mecánica prolongada y ECMO. A pesar de lo anterior, la hospitalización estuvo en una mediana de 21 días en UCI y 31 días en sala convencional, que debe analizarse respecto a los días reportados por centros de alto volumen de tromboendarterectomía pulmonar como en el de San Diego, con una mediana de 4 días, y en Ottawa un promedio de 11,2 días de hospitalización en UCI. En estos centros la estancia en hospitalización convencional se reportó en 10 y 19,5 días, respectivamente11,15.
En resumen, se resalta que el 100% de los pacientes tuvo mejoría funcional, hemodinámica y sintomática e incluso en algunos de ellos se normalizó la mayoría de estas variables de medición. Ningún paciente ha desarrollado hipertensión pulmonar residual a largo plazo, y la mortalidad fue nula. El tamaño muestral, sin embargo, no permite estereotipar esta respuesta ni aportar más datos con relevancia clínica potencial para la selección o exclusión del procedimiento.
ConclusionesEl programa de tromboendarterectomía pulmonar que presenta los resultados de los 8 primeros casos en la Fundación Cardiovascular de Colombia, reporta una sobrevida del 100% en un promedio de 24 meses de seguimiento. Los desenlaces hemodinámicos son favorables, sin secuelas extrapulmonares, y con mejoría de los parámetros funcionales ante el ejercicio en todos los pacientes. En caso de edema por reperfusión, la alternativa de ECMO fue adecuada.
Conflicto de interesesLos autores manifiestan no tener ningún conflicto de intereses.
A la Dra. Edna Magaly Gamboa, por su participación en el análisis de los datos.