La insuficiencia cardiaca es una de las causas prevalentes de morbimortalidad en el mundo. A pesar de la mejoría en la terapia médica y los dispositivos de estimulación cardiaca, existe un porcentaje de pacientes que progresan a falla cardiaca refractaria y sus opciones se reducen a inotrópicos, trasplante cardiaco y dispositivos de asistencia ventricular.
ObjetivoPresentar las alternativas actuales de asistencia ventricular disponibles para los pacientes con falla cardiaca avanzada.
MetodologíaRevisión narrativa de la literatura.
ConclusiónLa asistencia ventricular mecánica se ha convertido en una opción viable como puente a trasplante cardiaco o como terapia definitiva de largo plazo, ya que tiene impacto favorable en la mortalidad y la calidad de vida de los pacientes. En Colombia, la actividad relacionada con la colocación de asistencias ventriculares ha crecido notablemente en los últimos diez años y a pesar de las limitaciones derivadas de su alto costo, el país se convirtió en el primero de Suramérica en implantar un dispositivo HeartMate II para asistencia como terapia de destino. Este artículo, describe los beneficios de los dispositivos de asistencia ventricular, sus indicaciones y su disponibilidad en Colombia.
Heart failure is one of the most prevalent causes of morbidity and mortality in the world. Despite improvements in medical therapy and cardiac stimulation devices, there are a number of patients who progress to refractory heart failure and their options are reduced to inotropes, heart transplantation and ventricular assist devices.
ObjectiveTo present the current ventricular assist devices which are available to patients with advanced heart failure.
MethodologyNarrative review of the literature.
ConclusionMechanical ventricular assistance has become a viable option as a bridge to heart transplantation or as definitive long-term therapy, because it has a favourable impact on mortality and quality of life. In Colombia, the placing of ventricular assist devices has considerably increased in recent years and despite the constraints due to their high cost, the country is the first in South America to implant a HeartMate II device for assistance as destination therapy. This article describes the benefits of ventricular assist devices, its indications and availability in Colombia.
La insuficiencia cardiaca en un síndrome clínico de alta prevalencia que a pesar de los avances en la terapia médica, permanece con una mortalidad residual cercana al 50% a 5 años, lo que le confiere mayor letalidad que la mayoría de tipos de cáncer conocidos1. Cerca del 5% de los pacientes que padecen insuficiencia cardiaca son refractarios al manejo médico y persisten en clase funcional III y IV de la NYHA, lo que conlleva múltiples hospitalizaciones y alta mortalidad a corto plazo2.
Las opciones se limitan a inotrópicos endovenosos, trasplante cardiaco, asistencia ventricular o terapia paliativa, esta última en caso de que todas las demás alternativas estén contraindicadas3.
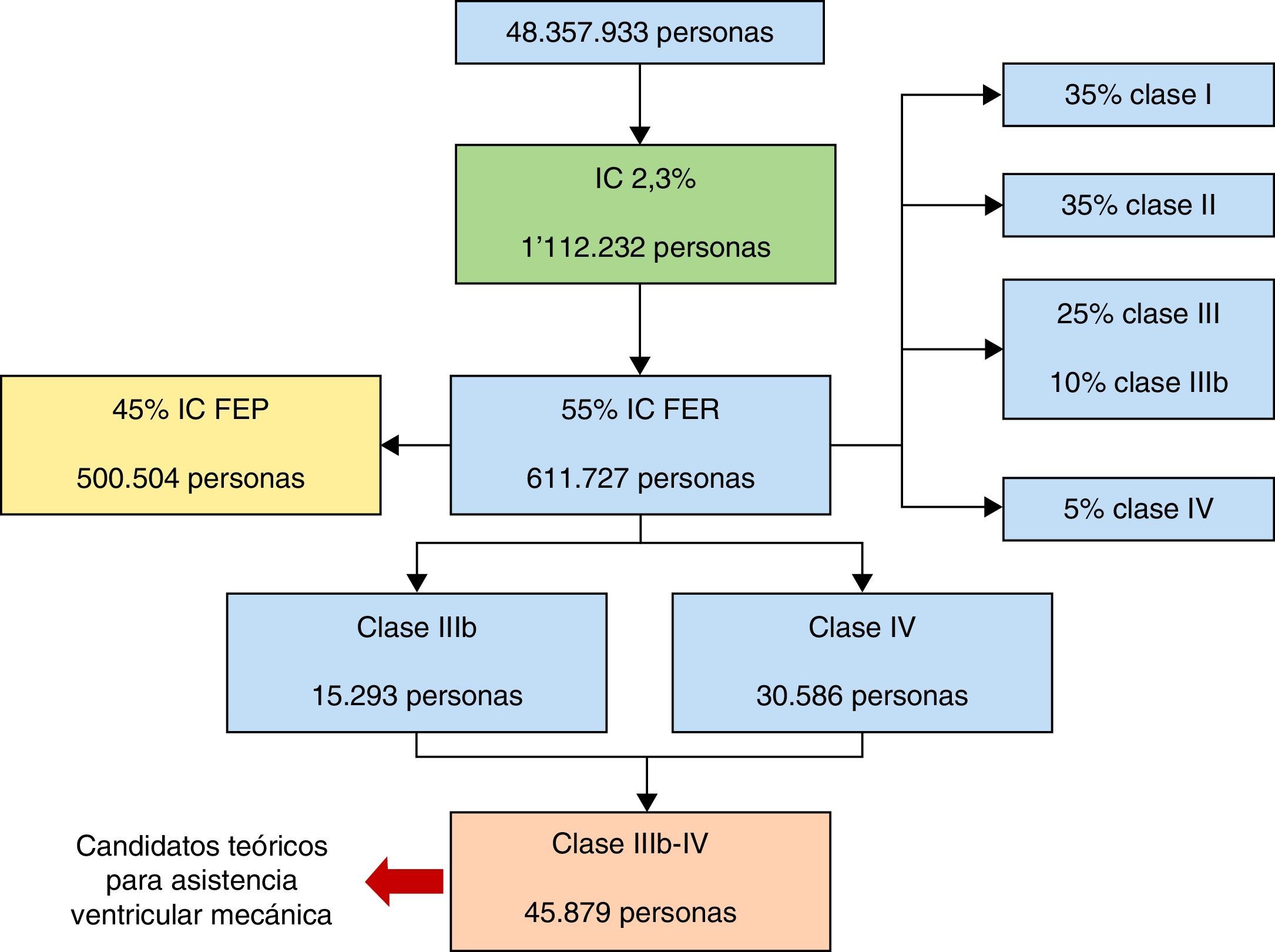
Asistencias ventriculares en ColombiaEs posible inferir una aproximación teórica de los pacientes potenciales para asistencia ventricular en Colombia teniendo en cuenta la prevalencia de la enfermedad en el país y el porcentaje de casos en los diferentes estadios de insuficiencia cardiaca reportada en la literatura (fig. 1). En general se reconocen dos escenarios de asistencia ventricular en Colombia en pacientes con insuficiencia cardiaca conocida: los que requieren asistencias de corto plazo en escenarios como choque refractario, angina intratable o tormenta arrítmica, y aquellos en falla cardiaca crónica refractaria, en cuyo caso se usan como puente a trasplante o terapia de destino.
Asistencias a corto o mediano plazoExisten dos síndromes clínicos de falla aguda a considerar en este escenario: pacientes con choque cardiogénico agudo de novo y aquellos con progresión severa de su insuficiencia cardiaca basal. El síndrome coronario agudo, la miocarditis fulminante y el choque cardiogénico después de cirugía cardiaca son las causas más frecuentes de choque cardiogénico en pacientes no conocidos con insuficiencia cardiaca4–6. El enfoque terapéutico y la indicación de asistencia mecánica circulatoria o del tipo de dispositivo a usar, varían en cada una de estas indicaciones.
En general, quienes acuden en choque cardiogénico refractario no son buenos candidatos para trasplante cardiaco o para dispositivos de asistencia ventricular implantables dada su alta mortalidad y la posibilidad de tener lesión neurológica u orgánica secundaria al choque. La principal causa de choque cardiogénico son los síndromes coronarios agudos, en especial con elevación del ST7. En estos pacientes, si la terapia de reperfusión no ha revertido el estado hemodinámico, es posible utilizar dispositivos de soporte mecánico de corta duración con el fin de esperar la recuperación cardiaca (situación ideal), la candidatura a trasplante, la asistencia ventricular como terapia de destino, o la recuperación de la función orgánica para disminuir el riesgo durante el trasplante o la implantación del dispositivo. El dispositivo más utilizado es el oxigenador de membrana extracorpórea (ECMO, su sigla en inglés) veno-arterial; con menor frecuencia se utiliza la asistencia paracorpórea con Centrimag® o Pedivas® y en casos seleccionados de síndrome coronario se utiliza el dispositivo Impella®. En un paciente isquémico que persiste hipotenso y con bajo gasto a pesar de soporte inotrópico y del tratamiento de su patología de base, se considera el uso de soporte mecánico circulatorio. Las opciones probables incluyen el balón de contrapulsación aórtico, que provee un aumento del gasto cardiaco marginal (250 a 500ml por minuto) y puede ayudar a la estabilización clínica, sin bien no ha demostrado disminuir la mortalidad en esta situación, por lo que su indicación es cada vez más controvertida8. El uso de Impella® puede proveer mayor aumento del gasto cardiaco de acuerdo con el modelo utilizado (2,5 L, 3 L o 5 L). Los dos primeros modelos son de implantación percutánea, lo cual permite un aumento del gasto cardiaco y la presión arterial, así como una disminución de la presión de fin de diástole del ventrículo izquierdo. Su utilidad se ve muy restringida en caso de disfunción biventricular o compromiso pulmonar. En Colombia varios centros han aplicado con éxito este tipo de soporte y según nuestro conocimiento el primer paciente se asistió en la clínica Country en el año 2013, y se documentó otro caso en un paciente de la Fundación Cardioinfantil en 2014. El ECMO veno-arterial percutáneo provee un soporte hasta 6 litros de gasto cardiaco permitiendo reemplazar el 100% de la función biventricular y de la función pulmonar9. Aunque no hay estudios que avalen el uso de estos dispositivos de manera contundente, pueden asegurar una estabilidad hemodinámica que permitiría una revascularización percutánea más completa y efectiva conservando la perfusión y la función orgánica. En Colombia el primer centro que utilizó ECMO fue la Fundación Santa Fe de Bogotá en dos pacientes neonatos a principios de la década del 2000. El primer uso exitoso por indicación cardiaca, se hizo en la Fundación Cardiovascular de Colombia en Bucaramanga en el año 2007, y desde el 2010 se ha empleado con éxito en varios centros de cuarto nivel en Colombia. De otro lado, las otras causas de choque cardiogénico son la miocarditis fulminante y el choque cardiogénico en cirugía cardiaca siendo la primera la de mejor pronóstico ya que con soporte mecánico circulatorio la sobrevida se aproxima al 80%10. La mayoría de estos pacientes recuperan la función ventricular una vez pasa la fase inflamatoria y lo que requieren es soporte mecánico para mantener el gasto cardiaco y la función orgánica, además de proveer reposo cardiaco. Por el contrario, en el choque cardiogénico asociado a cirugía cardiaca la sobrevida al egreso hospitalario es del 25%.
El segundo escenario de las asistencias ventriculares de corto plazo son los pacientes con falla cardiaca crónica que se descompensan agudamente y progresan con frecuencia a choque cardiogénico refractario. En este caso, el desarrollo de falla orgánica aguda o muerte son muy probables. Al contrario de las causas agudas, la probabilidad de conseguir una recuperación del corazón nativo es prácticamente nula. En esta situación es prioritario establecer si el paciente es candidato a trasplante o a terapia de destino antes de ofrecer un soporte mecánico circulatorio. En caso de que el paciente tenga contraindicación para trasplante o para dispositivo de largo término se debe proceder con manejo médico habitual y si no hay mejoría, definir manejo paliativo. Si el paciente presenta paro circulatorio o se encuentra en situación de colapso inminente, el dispositivo de elección es el ECMO veno-arterial percutáneo. Idealmente la decisión de soporte mecánico debe hacerse antes de que estos eventos ocurran y en ese caso el soporte más costo-efectivo es la asistencia ventricular paracorpórea con Centrimag® o Pedivas® si el paciente pesa menos de 15kg. Este tipo de asistencia requiere una cirugía de corazón abierto pero permite extubar rápidamente al paciente e iniciar una nutrición normal y una rehabilitación física agresiva con deambulación. El uso del dispositivo está recomendado por el fabricante hasta un mes, pero en Colombia hay pacientes que lo han soportado con éxito por más de cinco meses. El primer uso exitoso del dispositivo en Colombia data del año 2010 en la Fundación Cardiovascular de Colombia en Bucaramanga, en donde 16 pacientes han recibido la terapia. Otros centros como la Fundación Santa Fe de Bogotá, la Clínica Shaio, la Fundación Cardioinfantil, la Clínica Colombia, el Hospital San Ignacio, la Clínica DIME, la clínica CardioVid y el Hospital General del Norte, también han utilizado este tipo de soporte.
Asistencia ventricular de largo plazoLos pacientes con estadio D de falla cardiaca requieren manejo en una unidad de falla cardiaca avanzada que tenga disponibilidad de trasplante cardiaco y de asistencia ventricular.
Lamentablemente, la disponibilidad de donantes es baja y muchos pacientes se deterioran o fallecen en espera del trasplante. En cuanto a estos últimos, aquellos que se están deteriorando y/o tienen baja probabilidad de conseguir un donante deben considerarse para asistencia ventricular. Adicionalmente, algunos que tienen contraindicación para trasplante cardiaco pueden considerarse para asistencia ventricular como terapia de destino. Las indicaciones clásicas para asistencia ventricular son: pacientes que no responden a manejo médico óptimo, incluyendo inotrópicos, después de 45 a 60 días de tratamiento, o aquellos que requieren balón de contrapulsación aórtico o soporte inotrópico más de siete días y que adicionalmente tienen menos de 25% de fracción de eyección y menos de 14mL de consumo máximo de oxígeno11.
Los dispositivos de asistencia ventricular de flujo continuo ofrecen gran disminución de la mortalidad y mejoría considerable de la calidad de vida en este grupo de pacientes12.
Los resultados actuales de la asistencia ventricular son comparables con los del trasplante cardiaco sin la limitación del número de donantes y sin los inconvenientes de la inmunosupresión. Es muy probable que en un futuro próximo los pacientes con falla cardiaca estadio D que actualmente son evaluados para trasplante, sean considerados previamente para recibir asistencia ventricular y que el trasplante se reserve para aquellos con asistencia ventricular que tienen complicaciones o en quienes esté contraindicada la asistencia13.
Los dispositivos de asistencia ventricular de largo aliento en uso son bombas de flujo continuo de dos tipos: bomba axial, que tiene una turbina que rota por control magnético y posee dos soportes de rubí (HeartMate II), y bomba centrífuga, que tiene un rotor cónico que gira por control magnético y que levita en virtud de fuerzas magnéticas e hidráulicas (HeartWare II).
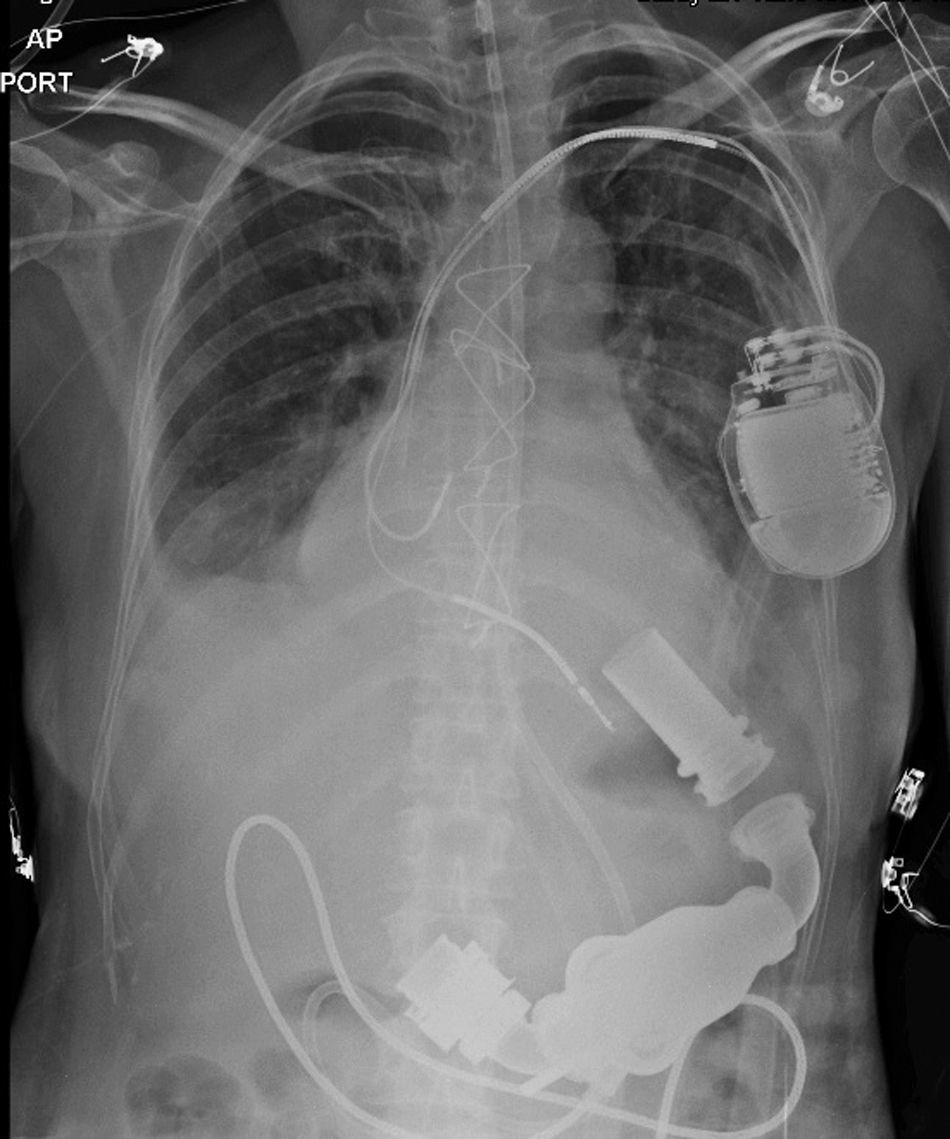
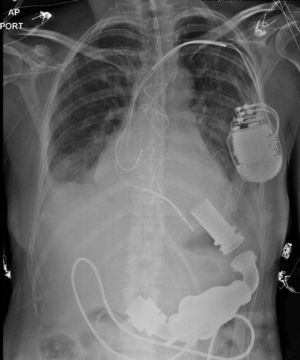
El primer implante de este tipo dispositivo en Suramérica, fue hecho en la Fundación Cardiovascular de Colombia en el año 2014 en una paciente de 52 años con insuficiencia cardiaca refractaria con contraindicación para trasplante cardiaco, en quien se implantó un HeartMate II de forma exitosa (fig. 2). En 2015 se implantaron dos nuevos dispositivos de este tipo, en el mismo centro, a pacientes de 15 y 40 años también de forma exitosa (fig. 3).
Este dispositivo se implanta en una cirugía de corazón abierto conectando una cánula de extracción en el ápex del ventrículo izquierdo y un injerto vascular de retorno en la aorta ascendente. La bomba queda puesta en un bolsillo por debajo de la reja costal y en la parte superior del abdomen. Un cable se exterioriza en la piel del abdomen (similar a un catéter de diálisis peritoneal) y se conecta a un controlador y a un sistema de dos baterías. Los pacientes deben realizarse curaciones y mantener cubierto el sitio de salida del cable y pueden cargar el controlador y las baterías en el cinturón del pantalón, en los bolsillos del pantalón, en un bolso o en un chaleco. Pueden llevar una vida normal, con actividad física habitual y retornar al trabajo o al estudio sin síntomas de falla cardiaca. Se requiere anticoagulación con warfarina (INR 2 – 3) más aspirina y deben controlarse en un centro de asistencia ventricular periódicamente (inicialmente cada mes y posteriormente hasta cada seis meses).
Estos dispositivos están diseñados para el uso por varios años (el más antiguo completa trece años con el mismo dispositivo) y en la actualidad la mayoría de pacientes que reciben esta terapia lo hacen de destino.
El uso crónico del dispositivo no está libre de complicaciones. A dos años, hasta un 20% de los pacientes han tenido infecciones del cable de control; un 10% ha tenido eventos cerebrovasculares; un 50% ha tenido sangrado nasal o gastrointestinal; un 3,8% ha tenido trombosis del dispositivo y un 4% ha tenido que cambiar el controlador. A pesar de esto, los más relevante de estos dispositivos es la mejoría de la supervivencia en cohortes históricas separadas por muy corto tiempo, con una supervivencia inicial en la primera cohorte (2005 al 2007) del 59% al año y del 56% a dos años, y en la segunda cohorte (2007 al 2009) del 85% y 70% al año y a dos años, respectivamente14,15. Esta mejoría refleja una depuración en la selección de los candidatos, un mejor entendimiento de las complicaciones y una optimización en la ingeniería, que ha solucionado progresivamente los problemas de estos dispositivos a medida que se han presentado.
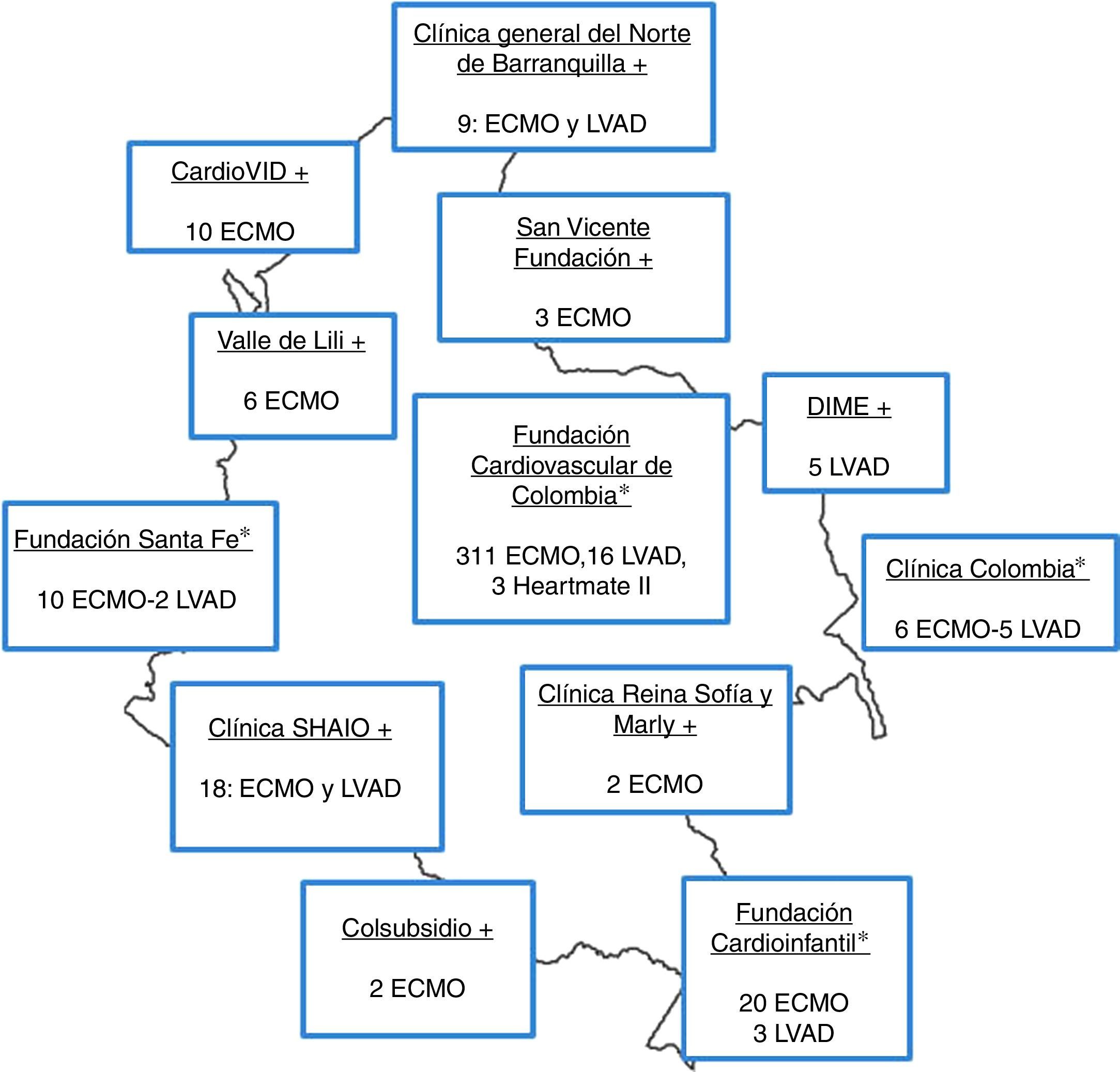
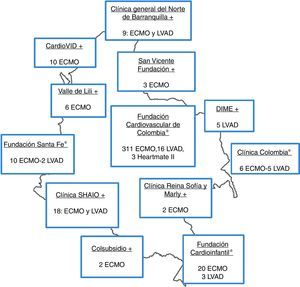
Finalmente, en la figura 4 se ilustran los centros que han realizado algún tipo de asistencia en Colombia y el tipo de dispositivo que utilizaron.
ConclusiónLos dispositivos de soporte mecánico circulatorio constituyen un avance importante en el tratamiento de los pacientes en falla cardiaca avanzada y choque cardiogénico. Su uso ha aumentado en los últimos años en Colombia. La supervivencia y la calidad de vida de los pacientes mejoran dramáticamente con el uso juicioso y bien indicado de estos dispositivos. Con la evolución de la tecnología, la disminución de las complicaciones y una reducción previsible del costo, es factible que su uso se extienda a la mayoría de los pacientes con falla cardiaca estadio D que cumplan los criterios de inclusión14,15. Por último, cabe resaltar que los pacientes de falla cardiaca avanzada y choque cardiogénico deben ser tratados por un grupo multidisciplinario en centros especializados en falla cardiaca y con disponibilidad de trasplante cardiaco y dispositivos de asistencia ventricular.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.