La gliomatosis peritoneal es una forma de extensión muy poco frecuente de los teratomas ováricos. Se caracteriza por la implantación miliar de tejido glial dentro de la cavidad peritoneal en pacientes con teratomas ováricos, generalmente inmaduros. Puede semejar un cuadro de carcinomatosis peritoneal. A pesar de su extensión intraperitoneal, la gliomatosis peritoneal no afecta adversamente al pronóstico del teratoma ovárico primario si los implantes de tejido glial se componen de tejido maduro y, por tanto, justifica tratamientos conservadores. El grado histológico del teratoma es el factor pronóstico que debe indicar el tratamiento complementario necesario. Su pronóstico es bueno, aunque se han descrito casos de malignización.
Peritoneal gliomatosis is a very rare metastatic form of ovarian teratoma, characterized by miliary dissemination of glial tissue inside the peritoneal cavity in patients with an ovarian – usually immature – teratoma. Peritoneal gliomatosis may resemble peritoneal carcinomatosis. Despite peritoneal dissemination, if the glial tissue implants are composed of mature tissue, peritoneal gliomatosis does not adversely affect the prognosis of the primary ovarian teratoma. Consequently, conservative treatment is warranted. The main prognostic factor is the histological grade of the teratoma, which indicates the required complementary treatment. The prognosis of peritoneal gliomatosis is favorable, although cases of malignant transformation have been reported.
La gliomatosis peritoneal es una forma de extensión muy poco frecuente de los teratomas ováricos. Hasta la fecha se han publicado 86 casos de esta entidad infrecuente. Se caracteriza por la presencia de implantes miliares de tejido glial dentro de la cavidad peritoneal de pacientes con teratomas ováricos, generalmente inmaduros. Los teratomas ováricos inmaduros representan menos del 1% de todos los teratomas. Contienen tejidos que derivan de las tres capas embriológicas: ectodermo, mesodermo y endodermo.
Puede ser macroscópicamente confundido con una siembra peritoneal de una carcinomatosis o con una tuberculosis peritoneal.
El diagnóstico se efectúa mediante estudio inmunohistológico de los implantes gliales. Nuestro caso además presenta implantes peritoneales en forma de otros tejidos maduros (cartílago, glándulas ecrinas y epitelio escamoso maduro), así como implantes en ganglios linfáticos.
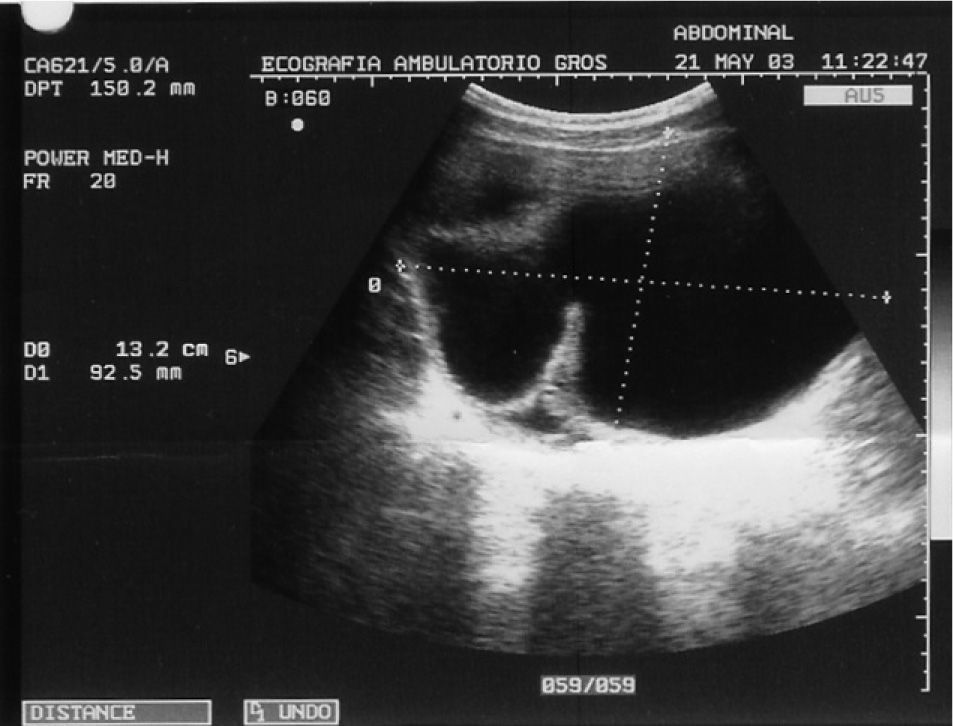
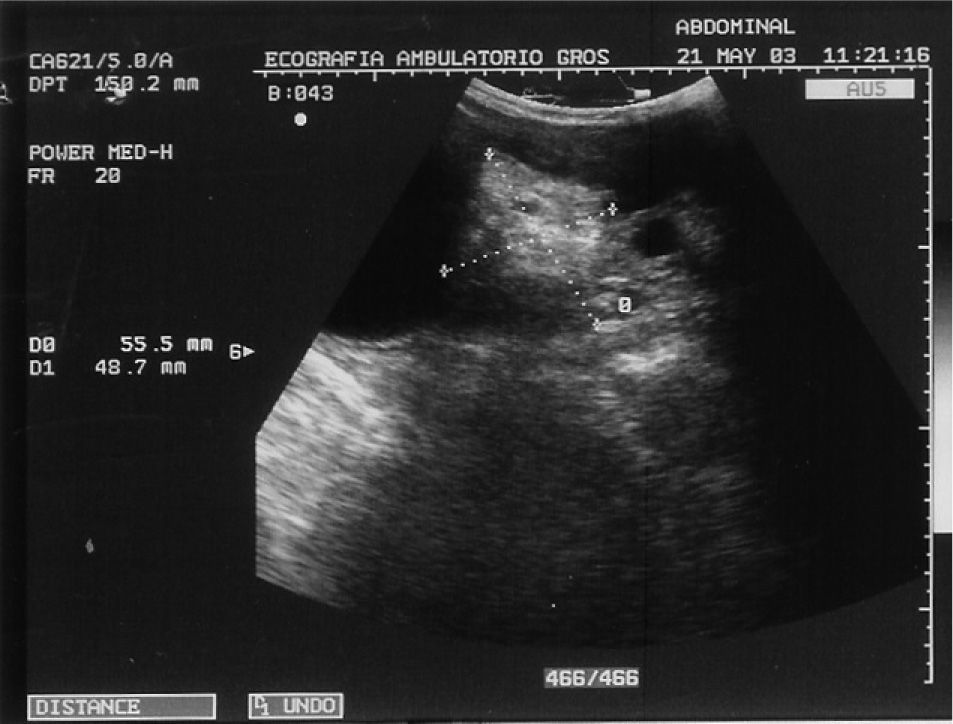
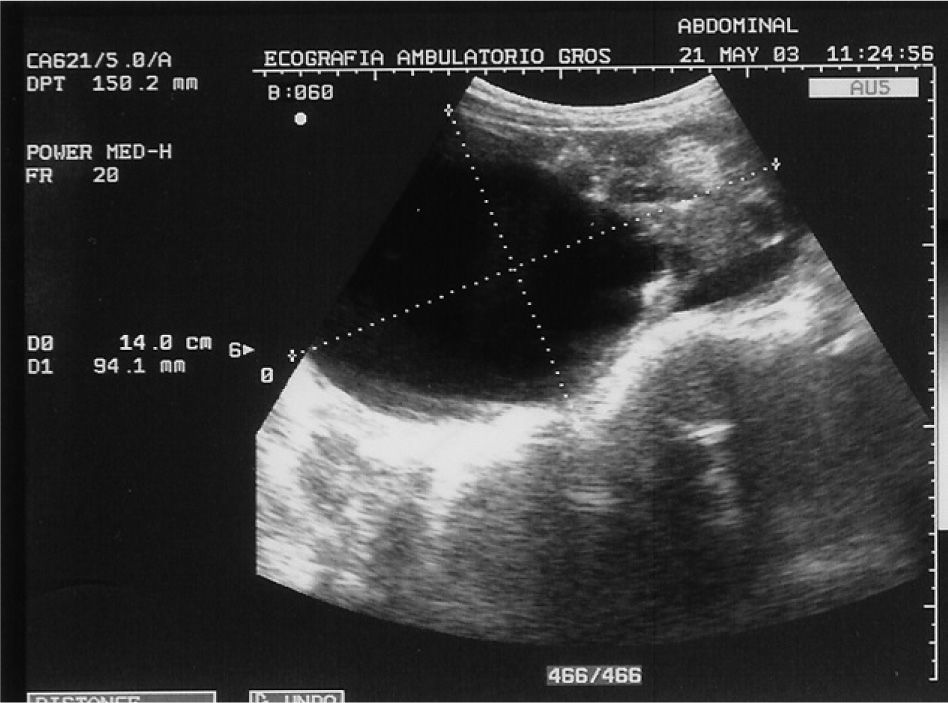
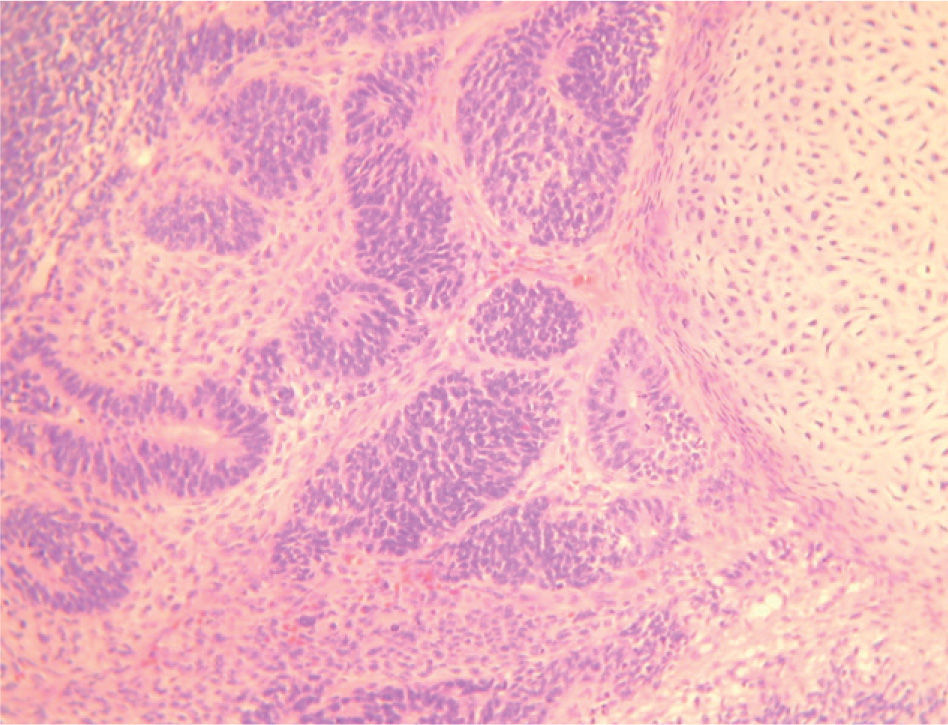
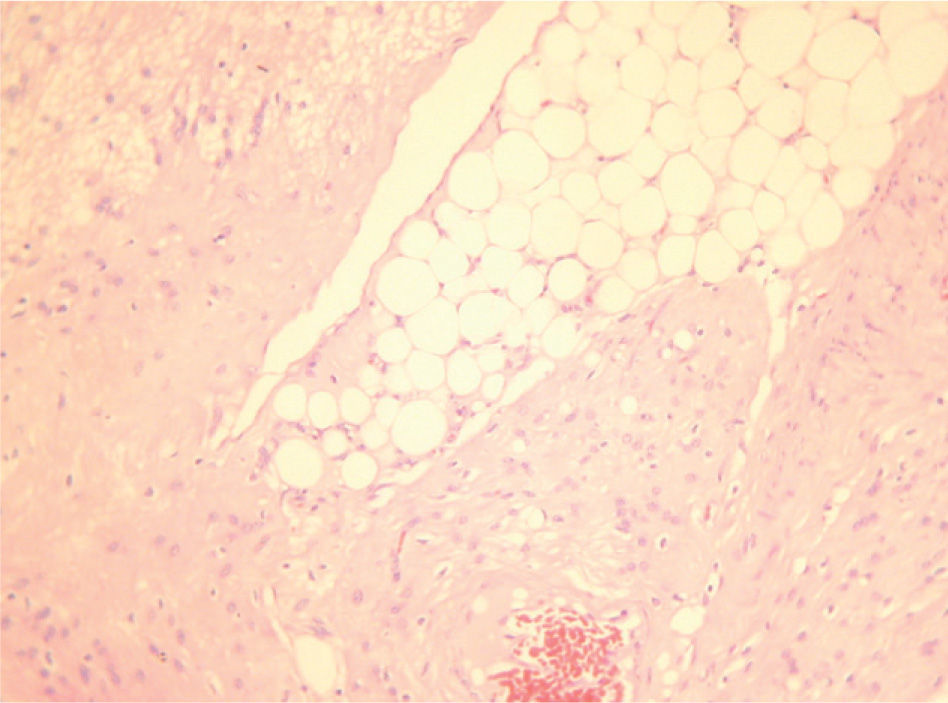
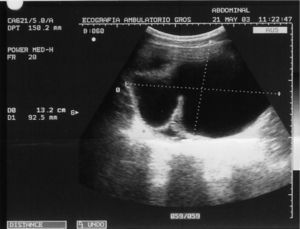
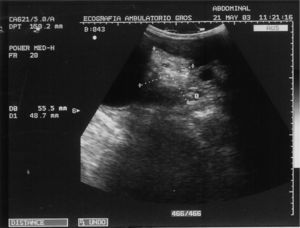
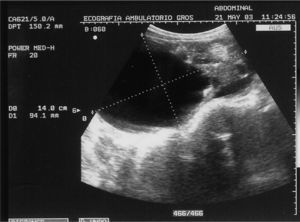
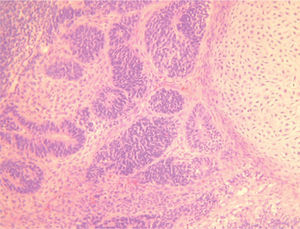
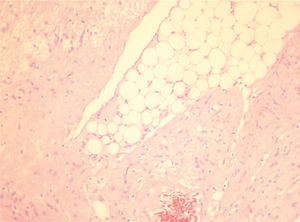
CASO CLÍNICOPaciente de 31 años que fue operada de una tumoración ovárica derecha 14 × 9,5cm con la sospecha clínica de teratoma ovárico gigante. Se le practicó una ecografía que mostró una tumoración heterogénea de 14 × 9,5cm, que en su parte inferior presentaba un componente líquido con tabiques regulares rectilíneos con flujos no sospechosos, pero que en su parte superior presentaba varias zonas sólidas e irregulares con tabiques gruesos y flujos Doppler de baja resistencia sospechosos (figs. 1, 2 y 3). Se decidió realizar una laparotomía en la que se observaron implantes metastásicos en el epiplón y en el saco de Douglas. El resultado de la biopsia intraoperatoria de la tumoración ovárica fue de teratoma inmaduro. Se efectuó una ovariectomía derecha, se resecaron los implantes en el epiplón y en el saco de Douglas y se efectuaron lavados para citología. El resultado histológico definitivo fue de teratoma inmaduro de grado III (4 campos de pequeño aumento de elementos neurales inmaduros por laminilla) con cápsula integra (figs. 4 y 5). Se describió la presencia de implantes peritoneales de gliomatosis peritoneal (tejido neural maduro) con muy ocasionales elementos ectodérmicos maduros (glándulas de revestimiento mucinoso) y se describió la existencia de un implante peritoneal maduro en el saco de Douglas (con otros tejidos maduros: cartílago, glándulas ecrinas y epitelio escamoso maduro). El lavado citológico peritoneal fue negativo. Los marcadores tumorales fueron: Ca-125: 38,2; Ca-19.9: 76,1; CEA 3,5. La gonadotropina coriónica beta (β-HCG) y AFP no se determinaron.
El comité de oncología ginecológica del hospital decidió efectuar una cirugía de estadificación completa conservando el útero y el ovario izquierdo. Se determinaron marcadores tumorales (AFP:13.4 y β-HCG normal). La citología peritoneal resultó negativa para células malignas. Las biopsias peritoneales, de sigma y mesointestinal resultaron también negativas. Se encontró tejido glial maduro en el implante de ovario izquierdo, la pelvis izquierda, el cloquet derecho, en 2 ganglios paraaórticos, el epiplón y el apéndice. El resto de la linfadenectomía pélvica fue negativa.
Posteriormente, se efectuó tratamiento quimioterápico con 4 ciclos de BEP por el grado del teratoma. Como toxicidad neurológica por platino (grado II, neurosensitiva), la paciente presentaba parestesias en las manos.
En la actualidad la paciente está libre de enfermedad en los controles efectuados, a los 3 años de la primera cirugía.
DISCUSIONLa gliomatosis peritoneal se caracteriza por la implantación miliar de tejido glial maduro sobre las superficies peritoneales. Generalmente se asocia a teratomas ováricos inmaduros, aunque de forma infrecuente pueden asociarse a teratomas ováricos maduros. Su apariencia macroscópica es similar a una carcinomatosis peritoneal. A pesar de su extensión intraperitoneal, la gliomatosis peritoneal no afecta adversamente al pronóstico del teratoma ovárico primario si los implantes de tejido glial se componen de tejido maduro1,2 y, por tanto, justifica tratamientos conservadores. A pesar de ello, se han descrito casos de transformación maligna3,4 que degeneran en tumores neuroectodérmicos malignos que semejan un gioblastoma multiforme.
Los teratomas inmaduros suponen un 1% de todos los tumores ováricos. Mayoritariamente, se trata de teratomas maduros que contienen porciones de tejido inmaduro o estructuras embrionarias. En ningún caso debe considerarse como una malignización de alguno de los componentes del teratoma maduro. Es una lesión sólida-quística de predominio sólido. Es más frecuente en mujeres jóvenes, con un pico en la segunda década de la vida. Hay que estudiar con especial cuidado múltiples porciones de este tipo de lesiones para identificar posibles focos o áreas inmaduras. Su crecimiento suele ser rápido y, por tanto, cuando se diagnostican pueden tener un volumen considerable. Son unilaterales, aunque pueden asociarse a un teratoma quístico maduro en el ovario contralateral. Clásicamente se gradúan según los criterios de Robboy y Scully5, modificados posteriormente por Thurlbeck y Scully6 y Dehner7, aunque actualmente se clasifican según el sistema de gradación de 3 niveles (tablas 1,2 y 3). Los grados 1 y 2 se comportan de forma benigna. Todos los teratomas de grado 3 que tienen un comportamiento maligno tienden a tener focos de tumores de saco vitelino (tumor germinal mixto)8. El factor pronóstico más importante de los teratomas inmaduros es el grado de la lesión. Tiene una buena correlación con la supervivencia frente a otras variables pronósticas (estadio, tamaño). El grado de tejido inmaduro se correlaciona generalmente con el potencial metastásico y la curabilidad del tumor. A mayor grado, peor pronóstico. El grado histológico del tumor primario es el mejor predictor de diseminación extraovárica y el grado de las metástasis el mejor predictor de su evolución9, aunque su reproductividad entre patólogos es tan sólo moderada10.
Grados de teratoma ovárico según Robboy y Scully, modificados por Norris et al9
| Grado | ||||
| 0 | I | II | III | |
| Mitosis | Ninguna | < 1, campo de bajo aumento | En < 3 campos microscópicos | Predominantemente |
| Sólo tejido glial maduro de tejido embrionario | Sólo tejido glial maduro | Pequeños focos de tejido embrionario o muy celular, predominando elementos maduros | Combinación de tejido maduro y embrionario de mediana cantidad | Dominancia de tejido embrionario |
Gradación de los teratomas inmaduros ováricos14
| Sistema de gradación de tres niveles | |
| Grado 1 | Tumores con escasos focos de tejido neuroepitelial inmaduro, que ocupa menos de un campo de bajo aumento (x40) en cualquier laminilla |
| Grado 2 | Tumores con elementos similares, que ocupan de 1 a 3 campos de bajo aumento (x40) en cualquier laminilla |
| Grado 3 | Tumores con gran cantidad de tejido inmaduro neuroepitelial que ocupan más de 3 campos de bajo aumento (40x) en cualquier laminilla |
La hipótesis más aceptada de su mecanismo de producción es el paso de tejido glial a través de roturas o un defecto en la cápsula del tumor ovárico5.
Existen más casos descritos en la literatura científica con elevaciones de las concentraciones de alfafetoproteína (AFP). El aumento de la AFP debe hacernos sospechar la existencia de un tumor germinal mixto, aunque se han descrito algunos casos en teratomas puros.
Debe hacerse una excisión amplia de todos los implantes gliales peritoneales para un correcto diagnóstico. Todos los implantes deben de componerse de tejido glial de grado 0 según la clasificación de Thurlbeck y Scully. Si no se encuentran otros elementos teratomatosos o tejido glial maligno en los implantes, el tratamiento debe ser el del teratoma primario. La gliomatosis peritoneal es una condición benigna que no requiere ningún tratamiento adicional al del teratoma ovárico. Se ha descrito que la presencia de gliomatosis peritoneal mejora el pronóstico11. No obstante, es fundamental que la extirpación de los implantes miliares se realice exhaustivamente y poder descartar así la presencia de implantes inmaduros, fundamentalmente tejido neuroectodérmico, que cambiaría el pronóstico. El manejo de estas tumoraciones se basa en su extirpación quirúrgica, asociando quimioterapia según el grado histológico (tabla 4). Para algunos autores la cirugía sola es curativa, independientemente del grado histológico, reservando la quimioterapia solamente para las recidivas12 con componente inmaduro. Existen evidencias de que sólo la presencia de focos microscópicos de componente de tumor del saco vitelino parece afectar al pronóstico y es un predictor de recurrencia válido13.
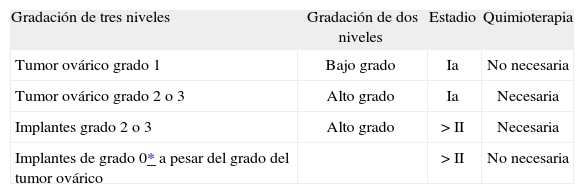
Manejo de teratomas inmaduros según el grado del tumor primario y de los implantes14
| Gradación de tres niveles | Gradación de dos niveles | Estadio | Quimioterapia |
| Tumor ovárico grado 1 | Bajo grado | Ia | No necesaria |
| Tumor ovárico grado 2 o 3 | Alto grado | Ia | Necesaria |
| Implantes grado 2 o 3 | Alto grado | > II | Necesaria |
| Implantes de grado 0* a pesar del grado del tumor ovárico | > II | No necesaria |
La gliomatosis peritoneal se asocia exclusivamente a teratomas ováricos, independientemente de su grado histológico. El grado histológico del teratoma es el factor pronóstico principal que debe indicar el tratamiento complementario necesario. Su pronóstico es bueno, aunque se han descrito casos de malignización. Resultan necesarios un seguimiento estricto y un control evolutivo.