Describir la experiencia con el uso del paracetamol en el cierre farmacológico del conducto arterioso persistente con repercusión hemodinámica.
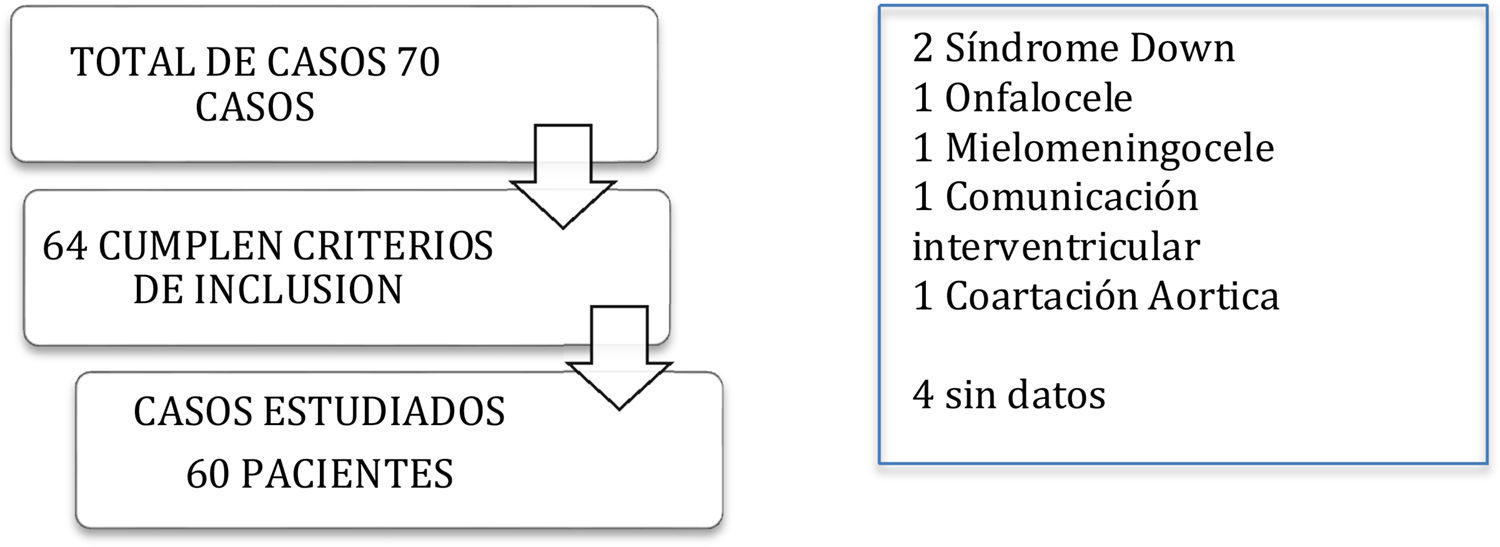
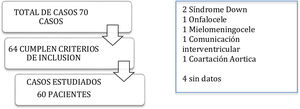
MétodosEstudio de tipo observacional retrospectivo del 1 de enero de 2014 al 1 de junio de 2017. La población estudiada fue menor de 35semanas de gestación, menores de 5días de vida, con un total de 70casos; 10 se excluyeron, para un total de 60, y de estos, a 6 se les ofreció un segundo ciclo en el que se usó paracetamol endovenoso a dosis de 15mg/kg por dosis cada 6h, hasta un total de 12dosis, por presentar persistencia del conducto arterioso con repercusión hemodinámica. Se efectuó estudio sérico de plaquetas, hepático, renal y de ultrasonido transfontanelar tomados 24h antes y después de cada ciclo; descripción del aporte hídrico del primer al quinto día.
ResultadosEdad gestacional y peso al nacimiento, sin relación con el cierre del conducto arterioso (p=0.622 y p=0.215). Se revalida el uso del corticoide prenatal como factor favorable para el cierre del conducto arterioso persistente (p<0.001). Con el total de 60 pacientes, se obtuvo una efectividad del 90%. No se presentaron datos de sangrado interventricular en el primer ciclo. Con respecto a las enzimas hepáticas y la función renal, no se mostró incremento. Dos pacientes fallecieron durante el estudio.
ConclusionesEl paracetamol para el cierre del conducto arterioso, en contraindicación de ibuprofeno, mostró una adecuada efectividad y seguridad en neonatos afectados en la ciudad de Bogotá.
To describe the experience with the use of paracetamol in the pharmacological closure of the patent ductus arteriosus with haemodynamic repercussion.
Material and methodsA retrospective observational study was conducted from 1 January 2014 to 1 June 2017, in a population of less than 35weeks of gestation, less than 5days of life. A total of 70 cases were included and 10 were excluded. Out of the remaining 60 cases, and of these, 6 were offered a second cycle of haemodynamic repercussion. Intravenous paracetamol was used at a dose of 15mg per kg every 6hours, for a total of twelve doses, on those with persistence of the ductus arteriosus, with hemodynamic repercussion. Platelets, liver and kidney function tests were performed, including a transfontanelle ultrasound at 24hours before and after each cycle, as well as a record of the fluid balance from the first to the fifth day.
ResultsGestational age and birth weight was unrelated to the closure of the ductus arteriosus (P=.622 and P=.215). The use of the prenatal corticosteroids is revalidated as a favourable factor for the closure of the patent ductus arteriosus (P<.001). An effectiveness of 90% was obtained in a total of 60 patients. There was no evidence of interventricular bleeding in the first cycle. There was no increase in liver enzymes or renal function. Two patients died during the study.
ConclusionsParacetamol for the closure of the ductus arteriosus, in contraindication of ibuprofen, showed adequate effectiveness and safety in affected neonates in the city of Bogotá.
El conducto arterioso (CA) es un vaso de gran calibre que conecta el tronco pulmonar principal (o arteria pulmonar izquierda proximal) con la aorta descendente en la vida fetal; su función esencial es derivar el flujo sanguíneo desde la circulación pulmonar con resistencia vascular elevada hacia la aorta descendente1. Al momento del nacimiento se inicia el cierre fisiológico del mismo y posteriormente el cierre anatómico. La persistencia del conducto arterioso (conducto arterioso persistente [CAP]) constituye un 10% del total de las cardiopatías congénitas, presentándose en un 45% en los menores de 1,750g y hasta en un 85% en los menores de 750g2. La incidencia, en series históricas, del CAP aislado en niños nacidos a término es de 1 en cada 2,000-2,500 recién nacidos vivos. En relación con su frecuencia, es más común en niñas que en niños (2:1)3. Las consecuencias clínicas de la persistencia del conducto arterioso están relacionadas con el grado de cortocircuito de izquierda a derecha, y a la presión diastólica, que permite una redistribución del flujo sanguíneo, reduciendo la perfusión al cerebro, al intestino y al riñón e incrementando el flujo sanguíneo pulmonar1.
El cierre farmacológico del conducto arterioso persistente es pilar del manejo, donde los antiinflamatorios no esteroideos son un determinante, promoviendo el cierre de manera efectiva mediante la reducción de la biosíntesis de las prostaglandinas vasodilatadoras4, independientemente del tratamiento quirúrgico, por lo que se sigue buscando un medicamento suficientemente efectivo que conlleve el menor número de reacciones adversas; de ahí que el paracetamol ha surgido como una opción, con gran aceptación por la comunidad científica, y cada vez hay más claridad en su mecanismo de acción y en su efectividad.
Con los diferentes estudios revisados se dispone de amplia evidencia para poder establecer el uso de paracetamol en el cierre de CAP en menores de 5días de vida y con edad gestacional inferior o igual a 35semanas, pero en este caso se busca demostrar esa efectividad en neonatos nacidos a una altura de 2,640m sobre nivel del mar, como lo es Bogotá, Colombia.
MétodosEstudio de tipo transversal, observacional, retrospectivo con base en información de historias clínicas de una serie de casos tratados consecutivamente, en los que se usó paracetamol endovenoso a dosis de 15mg/kg por dosis cada 6h, por un total de 12dosis, que tuvieran CAP con repercusión hemodinámica demostrada por ecocardiograma transtorácico, ingresados en la unidad de cuidado intensivo neonatal del Instituto Materno Infantil de la subred Centro Oriente de Bogotá, Colombia, durante el periodo comprendido entre el 1 de enero de 2014 y el 1 de junio de 2017.
Se tomaron como criterios de inclusión pacientes ingresados menores de 35semanas de edad gestacional determinado por clasificación de Ballard, con CAP, menores de 5días de vida al momento del diagnóstico y que tuvieran alguna contraindicación para uso de ibuprofeno. Como criterios de exclusión, que presentaran una o más malformaciones congénitas mayores, alguna alteración estructural cardíaca, que no sea CAP, neonatos con oliguria definida como diuresis menor de 1ml/kg/h en las 12h previas al inicio del cierre farmacológico, pacientes sin control ecocardiográfico posterior al cierre farmacológico y pacientes con datos clínicos o paraclínicos de falla hepática previa.
Se realizó descripción de edad materna, edad gestacional reportada en historia de ingreso a la unidad neonatal realizada por médico neonatólogo o pediatra, vía de nacimiento, causas de nacimiento prematuro, uso de maduración pulmonar fetal con betametasona tomando como base el tratamiento completo (dos dosis cada una con un intervalo de 24h, y nacimiento 24h después pero menor de 7días posterior a la última dosis); tratamiento incompleto: que no cumpla los anteriores condiciones pero no exceda de ellas; sobretratamiento: cuando excede de dos dosis de betametasona, durante una semana previa al nacimiento, tipo de pinzamiento (precoz, inmediato, habitual y diferido), tipo de adaptación (espontánea, conducida e inducida), evaluación de APGAR otorgada a los 5min de vida; estas variables se cruzarán con el resultado final del cierre o no del CAP posterior al ciclo de paracetamol, tanto en la población que recibió el primer ciclo como en la que recibió segundo ciclo de paracetamol. Se efectuó, además, estudio sérico de nitrógeno ureico (BUN), creatinina, alanina transferasa (ALT), aspartato transferasa (AST), hemograma completo, bilirrubina total y diferencial previo al inicio de tratamiento y 24h postratamiento.
Otras variables estudiadas fueron tipo de ventilación utilizada, concentración inspirada de oxígeno antes y después de la terminación de la terapéutica farmacológica, ultrasonido transfontanelar tomado 24h antes y después de cada ciclo, descripción del aporte hídrico del primer al quinto día de vida: en todos los casos se compararon con la variable definitiva del cierre o no del CAP.
Los ecocardiogramas fueron realizados por un cardiólogo pediatra con un equipo Vivid E9 (GE Medical Systems). Los diferentes ecocardiografistas fueron cegados a los regímenes de tratamiento. Todos los pacientes se sometieron a exámenes en las primeras 48-72h de vida para descartar cardiopatía congénita e identificar casos de CAP. El ecocardiograma se repitió al final de cada ciclo de tratamiento con paracetamol.
Para la toma de datos y resultados se accedió a las historias clínicas y se recolectaron en tablas de datos diseñadas por el autor. Se pasaron los datos a sistema STATA.14, se calcularon las tasas de prevalencia e incidencia por variable, usando como denominador el cierre del CAP. Se realizó un análisis de cada variable de modo independiente, trabajando con distribuciones de frecuencias (porcentaje total), medidas de tendencia central (media, mediana y moda) y medidas de dispersión, mediante el uso de desviación estándar.
ResultadosLa población estudiada fue un total de 70 casos, de los cuales 6 se excluyeron, quedando 64 casos —de ellos, 4 casos sin datos completos para análisis— para un total de 60 casos estudiados (tabla 1), y de ellos 6 casos estudiados con segundo ciclo de paracetamol.
Se muestra la tabla poblacional descriptiva del estudio que revalida datos descritos, como la prevalencia en población femenina, con edad gestacional promedio de 30.5semanas de gestación, muy similar a lo descrito por distintos autores4,5 (tabla 2).
Descripción de las características sociodemográficas y clínicas de las madres, el nacimiento y los neonatos
| Edad materna, años (min-max) | 24 (13-44) |
| Número de controles prenatales (min-max) | 3 (0-7) |
| Plaquetas maternas/mm3(min-max) | 273,292 (90,000-473,000) |
| Maduración pulmonar | |
| No (%) | 20 (34) |
| Sí (%) | 29 (47) |
| Incompleta (%) | 5 (9) |
| Sobretratada (%) | 6 (10) |
| Vía de nacimiento | |
| Vaginal (%) | 20 (34) |
| Cesárea%) | 40 (66) |
| Causa de nacimiento | |
| Sin causa (%) | 4 (6) |
| Preeclampsia (%) | 25 (41) |
| Corioamnionitis (%) | 14 (23) |
| Síndrome HELLP (%) | 1 (1.5) |
| Incomp. cervical (%) | 2 (3) |
| Gemelar (%) | 2 (3) |
| Placenta previa sangrante (%) | 4 (5) |
| EFI (%) | 7 (12) |
| Trillizos (%) | 1 (1.5) |
| Género neonato | |
| M (%) | 29 (48) |
| F (%) | 31 (52) |
| Pinzamiento umbilical | |
| Diferido (%), | 7 (10) |
| Habitual (%) | 25 (40) |
| Inmediato (%) | 10 (18) |
| Precoz (%) | 18 (30) |
| Adaptación neonatal | |
| Inducida %) | 14 (24) |
| Conducida (%) | 24 (39) |
| Espontánea (%) | 22 (36) |
| APGAR 5 minutos (min-max) | 6 (4-8) |
| Peso al nacimiento, gramos (min-max) | 1,315 (560-2,420) |
| Talla nacimiento, cm (ídem) | 37.8 (29-48) |
| Edad gestacional semanas (min-max) | 30.5 (26-35) |
Sobresalen madres en promedio jóvenes, con tres controles prenatales y conteo plaquetario normal; tuvieron maduración pulmonar en dos terceras partes (66%) de los casos. La vía predominante de nacimiento fue abdominal, en su gran mayoría debida a preeclampsia y a corioamnionitis.
Solo un 10% tuvo pinzamiento diferido del cordón umbilical y la adaptación fue en su mayoría espontánea o conducida. El peso y la talla promedio, para una edad gestacional promedio (30.5semanas), hacen un diagnóstico promedio de la serie de casos con «peso adecuado para la edad gestacional» entre percentil 10-50 de la curva de Fenton (2003).
Se detallan en la tabla 3 los desenlaces de cierre o no del CAP posterior a un ciclo de paracetamol; de ellos, en 6 no se obtuvo éxito (10%), y a estos se les ofreció un segundo ciclo de paracetamol.
Variables de desenlace
| Variable | Indicador |
|---|---|
| Cierre con primer ciclo, n=60 | N Exitoso 54 (90%) N No exitoso 6 (10%) |
| Cierre con segundo ciclo, n=6 | N Exitoso 2 (33%) N No exitoso 4 (66%) |
| HIV (1.er ciclo) | Ninguno |
| HIV (2.o ciclo) | 2 (33%) |
| Deterioro renal (1.er-2.o ciclo) | Ninguno |
| Elevación AST ALT (1.er-2.o ciclo) | Ninguno |
| Condición vital al mes | N Vivo 58 (96.6%) N Muerto 2 (3.33%) |
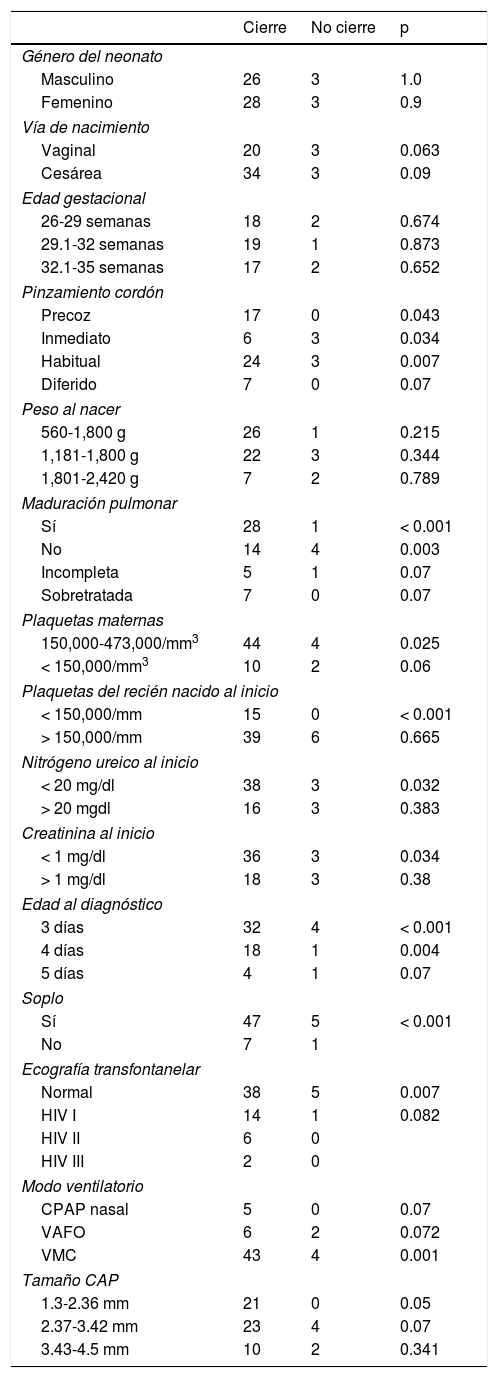
Con las variables estudiadas se realizó un análisis con el éxito o no éxito del cierre del CAP posterior al uso del primer ciclo de paracetamol (tabla 4).
Análisis bivariado para la variables de desenlace con primer ciclo de paracetamol
| Cierre | No cierre | p | |
|---|---|---|---|
| Género del neonato | |||
| Masculino | 26 | 3 | 1.0 |
| Femenino | 28 | 3 | 0.9 |
| Vía de nacimiento | |||
| Vaginal | 20 | 3 | 0.063 |
| Cesárea | 34 | 3 | 0.09 |
| Edad gestacional | |||
| 26-29 semanas | 18 | 2 | 0.674 |
| 29.1-32 semanas | 19 | 1 | 0.873 |
| 32.1-35 semanas | 17 | 2 | 0.652 |
| Pinzamiento cordón | |||
| Precoz | 17 | 0 | 0.043 |
| Inmediato | 6 | 3 | 0.034 |
| Habitual | 24 | 3 | 0.007 |
| Diferido | 7 | 0 | 0.07 |
| Peso al nacer | |||
| 560-1,800 g | 26 | 1 | 0.215 |
| 1,181-1,800 g | 22 | 3 | 0.344 |
| 1,801-2,420 g | 7 | 2 | 0.789 |
| Maduración pulmonar | |||
| Sí | 28 | 1 | < 0.001 |
| No | 14 | 4 | 0.003 |
| Incompleta | 5 | 1 | 0.07 |
| Sobretratada | 7 | 0 | 0.07 |
| Plaquetas maternas | |||
| 150,000-473,000/mm3 | 44 | 4 | 0.025 |
| < 150,000/mm3 | 10 | 2 | 0.06 |
| Plaquetas del recién nacido al inicio | |||
| < 150,000/mm | 15 | 0 | < 0.001 |
| > 150,000/mm | 39 | 6 | 0.665 |
| Nitrógeno ureico al inicio | |||
| < 20 mg/dl | 38 | 3 | 0.032 |
| > 20 mgdl | 16 | 3 | 0.383 |
| Creatinina al inicio | |||
| < 1 mg/dl | 36 | 3 | 0.034 |
| > 1 mg/dl | 18 | 3 | 0.38 |
| Edad al diagnóstico | |||
| 3 días | 32 | 4 | < 0.001 |
| 4 días | 18 | 1 | 0.004 |
| 5 días | 4 | 1 | 0.07 |
| Soplo | |||
| Sí | 47 | 5 | < 0.001 |
| No | 7 | 1 | |
| Ecografía transfontanelar | |||
| Normal | 38 | 5 | 0.007 |
| HIV I | 14 | 1 | 0.082 |
| HIV II | 6 | 0 | |
| HIV III | 2 | 0 | |
| Modo ventilatorio | |||
| CPAP nasal | 5 | 0 | 0.07 |
| VAFO | 6 | 2 | 0.072 |
| VMC | 43 | 4 | 0.001 |
| Tamaño CAP | |||
| 1.3-2.36 mm | 21 | 0 | 0.05 |
| 2.37-3.42 mm | 23 | 4 | 0.07 |
| 3.43-4.5 mm | 10 | 2 | 0.341 |
Al igual que la edad gestacional, el peso al nacimiento se dividió en tres grupos, con un peso mínimo de 560g y un máximo de 2,420g; no se evidenció relación estadísticamente significativa con el éxito en el cierre o no del CAP tras el ciclo de paracetamol (p=0.215).
Se evidencia relación entre el uso de corticosteroide antenatal con el cierre del CAP posterior al ciclo de paracetamol (p<0.001). Se buscó la relación de plaquetas maternas con el estado final del CAP, basándose en que las plaquetas del recién nacido son un factor predictor independiente del éxito del cierre o no posterior al ciclo de indometacina e ibuprofeno6,7, pero en caso del presente estudio la plaquetopenia materna, definida como menor de 150,000/mm3, no tuvo relación con el cierro o no del CAP posterior al ciclo de paracetamol (p=0.252). No se encontró relación entre los niveles de nitrógeno ureico con el estado final del CAP.
Se buscó una relación del tamaño del ductus como variable independiente y se dividió en tres grupos de acuerdo a los percentiles dados por el programa estadístico usado, con un tamaño mínimo de 1.3mm y un máximo de 4.5mm. Se demostró que conductos menores de 2.37mm (n=21) se cerraron en su totalidad (p<0.001), mientras que en el grupo2 (n=27) en 4 pacientes no se cerró, pero en el grupo3 (n=12) 2 no se cerraron tras el ciclo de paracetamol (p=0.0431).
Al comparar la edad en días al momento del diagnóstico con el éxito en el cierre o no del CAP posterior al ciclo de paracetamol se evidencia un predominio del tercer día de vida al momento del diagnóstico, acorde a lo que se reporta en la literatura8,9.
El número de plaquetas del neonato no se vio afectado; posterior al ciclo de paracetamol no existió ningún caso que pasara de tener plaquetas en cantidad normal a menor de 150,000mm3, y sin que esta variable se viera relacionada con el cierre o no del CAP.
Conociendo que el paracetamol tiene un metabolismo predominantemente hepático, se buscó conocer si con el protocolo dado de paracetamol había algún compromiso de la función hepática, que fue evaluado mediante la medición de AST y ALT, y la medición de bilirrubina sérica total y diferencial, previo al inicio. Al terminar el ciclo farmacológico no se evidenció incremento de transaminasas hepáticas (AST y ALT), pero sí un descenso significativo en la AST (p>0.001). A nivel de las bilirrubinas no se evidenció aumento significativo en nuestra descripción.
Se encontró relación entre más alto sea el aporte hídrico por día con el no cierre del CAP posterior a ciclo de paracetamol, en especial el primer y segundo día de vida. La cuantificación se hizo con el aporte de líquidos endovenosos calculados más bolos de soluciones cristaloides usadas en la mayoría de casos y líquidos usados con el paso de medicamentos. Conociendo que la mayoría de pacientes se diagnosticaron al tercer día de vida, se puede asumir que el aporte hídrico por encima de 110ml/kg de peso al día, en los dos primeros días de vida se asoció al no éxito del cierre del CAP posterior al uso de paracetamol, sin tener una significancia estadística (p=0.8).
No se evidenció el estado final de CAP con la hemorragia intraventricular (HIV), además de no apreciarse progresión de hemorragia intraventricular en ningún caso de los que recibieron el primer ciclo de paracetamol, con adecuada relevancia estadística (p<0.001), pero tampoco se demostró disminución de la severidad en HIV.
Como era de esperar, el cierre del CAP con paracetamol endovenoso se asoció a una mejoría en la ayuda ventilatoria brindada, requiriendo menos ventilación mecánica invasiva y disminución en el uso de ventilación de alta frecuencia oscilatoria invasiva.
Dentro de las repercusiones ecocardiográficas —valores por encima de 1.3mm, basándose en los criterios de Yeh10—, la mayoría pertenecía al grupo de mayor de 1.3mm (n=57); de ellos, 5 pacientes formaron parte del grupo de 6 pacientes en los que no se cerró (p=0.003).
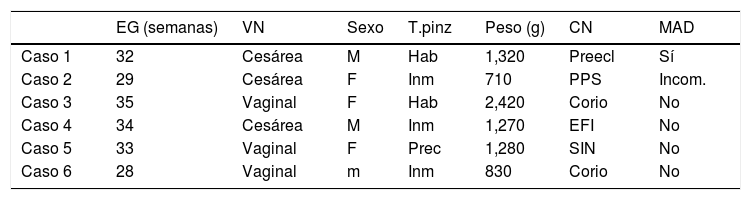
Del total de 60 pacientes estudiados, se obtuvo una efectividad del 90%, valor dentro del rango descrito entre el 77 y el 100%5,11. En un total de 6 pacientes no se obtuvo éxito en el cierre, y a estos se les ofreció un segundo ciclo de las mismas características y con mismo estudio de variables dadas en el primer ciclo (tabla 5).
Pacientes que recibieron segundo ciclo de paracetamol
| EG (semanas) | VN | Sexo | T.pinz | Peso (g) | CN | MAD | |
|---|---|---|---|---|---|---|---|
| Caso 1 | 32 | Cesárea | M | Hab | 1,320 | Preecl | Sí |
| Caso 2 | 29 | Cesárea | F | Inm | 710 | PPS | Incom. |
| Caso 3 | 35 | Vaginal | F | Hab | 2,420 | Corio | No |
| Caso 4 | 34 | Cesárea | M | Inm | 1,270 | EFI | No |
| Caso 5 | 33 | Vaginal | F | Prec | 1,280 | SIN | No |
| Caso 6 | 28 | Vaginal | m | Inm | 830 | Corio | No |
CN: causa de nacimiento; Corio: corioamnionitis; EFI: estado fetal insatisfactorio;
EG: edad gestacional; F: femenino; Hab: habitual; Incom.: incompleta; Inm: inmediado; M: masculino; MAD: Maduración pulmonar; PPS: placenta previa sangrante; Prec: precoz. g: gramos, Preecl: preeclmapsia; SIN: no causa conocida; T.pinz: tipo de pinzamiento; VN: vía de nacimiento.
A continuación se enumeran los pacientes del caso 1 al caso 6; los dos primeros fueron los casos en los que se cerró con el segundo ciclo ofrecido.
En los dos primeros casos se obtuvo éxito con el segundo ciclo, ambos nacidos por cesárea, además de que recibieron el mismo tipo de pinzamiento (habitual), pero sobresale que estos dos pacientes recibieron corticoide antenatal, de igual forma que sucedió con los pacientes a los que se les ofreció el primer ciclo.
Como se mostró en el grupo del primer ciclo de paracetamol, hubo una relación entre mayor aporte de líquidos endovenosos y CAP; en el grupo que recibió segundo ciclo de paracetamol —6casos—, los dos primeros tuvieron éxito en el segundo ciclo y fueron los que menor cantidad de líquidos endovenosos recibieron con respecto a los otros cuatro. De estos cuatro, el caso 5, a pesar de que recibió un aporte bajo el primer día de vida, al segundo y tercer día de vida su aporte fue alto comparado con los demás casos.
Con el primer ciclo de paracetamol no se evidenció incremento en casos de hemorragia, y se evidenció una mejoría en la disminución de HIV pero no significativamente estadística; con el segundo ciclo, en los 2 casos en que se obtuvo éxito las ecografías fueron descritas como normales antes y después, pero en los 4 restantes, el 50% aumentó la HIV.
De los 60 pacientes estudiados, dos fallecieron. El primero era de 29 semanas de edad gestacional, nacido por vía abdominal de urgencia por placenta previa sangrante, peso al nacimiento 710g; recibió una sola dosis de betametasona intramuscular 8h previo al nacimiento, sin hemorragia intraventricular, recibiendo los dos ciclos de paracetamol; pertenece al caso número 2 del grupo que recibió segundo ciclo de paracetamol y falleció a los 15días de vida con diagnóstico de sepsis neonatal tardía por Klebsiella oxytoca. El segundo caso fallecido, de 28 semanas de edad gestacional, había nacido por vía abdominal por preeclampsia materna; peso al nacimiento, 620g. Recibió maduración pulmonar completa y en tiempo adecuado con betametasona, con HIV gradoII antes y después del primer ciclo con paracetamol, con el que se obtuvo éxito en el cierre del CAP; falleció a los 7días de vida con diagnóstico de sepsis tardía sin aislamiento descrito.
DiscusiónAnte la necesidad del cierre oportuno del CAP, se describen distintas formas de cierre. La más usada es la farmacológica, pero los medicamentos usados pueden conllevar reacciones adversas que aumentan la morbimortalidad; de ahí que, como se mencionó anteriormente, el paracetamol haya cobrado mayor utilidad en este campo, con estudios como el realizado por Harkin et al.11, publicado en 2013, en el que el paracetamol fue estudiado para el cierre temprano y sus posibles efectos adversos en menores de 32semanas, con una dosis de carga de 20mg/kg de peso por dosis seguido con 7.5mg/kg de peso por dosis cada 6h por 4días. El principal resultado fue una disminución en el calibre ductal sin efectos secundarios, con un cierre más rápido en el grupo con paracetamol (IC95%) que con placebo, concluyendo que el paracetamol intravenoso puede promover con seguridad el cierre del conducto arterioso, o la revisión que hace el grupo de colaboración Cochrane5, donde buscan demostrar la eficacia y la seguridad del paracetamol intravenoso u oral en comparación con placebo o ninguna intervención, o con el uso de indometacina intravenosa o ibuprofeno por vía intravenosa u oral, para el cierre de un CAP en recién nacidos prematuros o de bajo peso al nacer, demostrando que no hubo diferencias significativas entre el paracetamol y el ibuprofeno, y se concluye que aunque un número limitado de niños con CAP se han estudiado en ensayos aleatorios de calidad baja a moderada de acuerdo al grado, el paracetamol parece ser tan eficaz en el cierre del CAP como el ibuprofeno.
Si bien es cierto que el paracetamol tiene un gran efectividad en el cierre del CAP, no hay que olvidar estudios que muestran la existencia de factores que favorecen o no el cierre del CAP, lo que conduce a individualizar cada caso, como se describe desde 1981 en el estudio de Gittenberger et al.12 de una serie de pacientes estudiados post mortem; algunos recibieron indometacina, pero no se evidenció una relación de la edad gestacional y el peso con el cierre o no del CAP, tanto espontáneo como de causa farmacológica, lo que lleva a pensar que existen factores que promueven o afectan el cierre; entre ellos, como se ratifica en este estudio, la betametasona antenatal es un factor a favor del cierre. Es conocido que el corticoide antenatal ha ido mostrando sus beneficios, y ya en 1981 se mencionada la relación del corticoide con el cierre del CAP13, siendo hoy en día parte del manejo de la gestante con riesgo de nacimiento prematuro. Además, hay una relación dada de la administración de corticoide antenatal, bien sea en esquema incompleto o sobretratado, con el nacimiento por vía abdominal, que estaría acorde con la aplicación de betametasona, indicada en situaciones especiales, como la prematuridad (p<0.01). La mayoría de los niños que no fueron madurados (15%) nacieron por vía vaginal, bien sea porque no dio tiempo para la aplicación (ingreso en fase de expulsivo de 6 casos) o porque no tenían indicación.
Cada vez más se describe la trombocitopenia (<150,000/mm3) del neonato como un factor independiente que se asocia con el no cierre del CAP posterior a ciclos farmacológicos con ibuprofeno e indometacina6,7. En este estudio no se encontró relación de la trombocitopenia con el cierre o no del CAP posterior al ciclo de paracetamol (p=0.665).
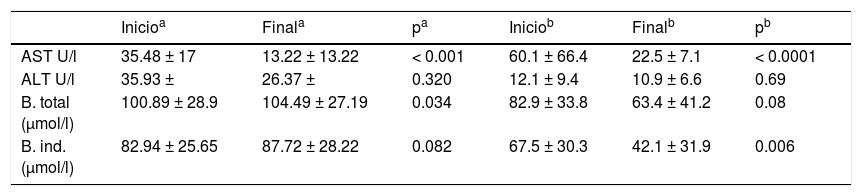
Se compararon los resultados con los obtenidos del estudio de Valerio et al.14, quienes usaron paracetamol (en contraindicación de ibuprofeno) en 30 pacientes con CAP con repercusión clínica y ecocardiográfica, con edad gestacional entre 26 y 32 semanas, en dosis iguales a las del estudio actual (15mg/kg de peso por dosis, 4 dosis diarias por 3 días). No se evidenció incremento de transaminasas hepáticas (AST y ALT) en ninguno de los dos estudios y sí un descenso significativo en la AST (p>0.001), y a nivel de las bilirrubinas no se encontró aumento significativo en nuestra descripción (tabla 6).
Comparación de niveles séricos de transaminasas y bilirrubina total y directa antes de y después de paracetamol
| Inicioa | Finala | pa | Iniciob | Finalb | pb | |
|---|---|---|---|---|---|---|
| AST U/l | 35.48 ± 17 | 13.22 ± 13.22 | < 0.001 | 60.1 ± 66.4 | 22.5 ± 7.1 | < 0.0001 |
| ALT U/l | 35.93 ± | 26.37 ± | 0.320 | 12.1 ± 9.4 | 10.9 ± 6.6 | 0.69 |
| B. total (μmol/l) | 100.89 ± 28.9 | 104.49 ± 27.19 | 0.034 | 82.9 ± 33.8 | 63.4 ± 41.2 | 0.08 |
| B. ind. (μmol/l) | 82.94 ± 25.65 | 87.72 ± 28.22 | 0.082 | 67.5 ± 30.3 | 42.1 ± 31.9 | 0.006 |
ALT: alanina transaminase; AST: aspartato aminotransferasa; B: bilirrubina; ind: indirecto.
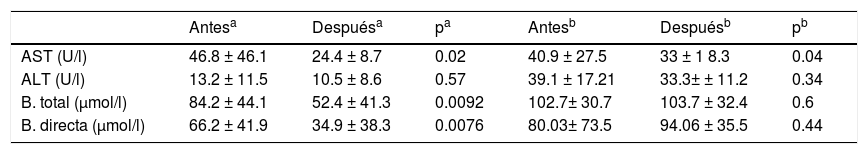
En el estudio de Valerio et al.14 también se usó el paracetamol (15mg/kg de peso por dosis, total 12 dosis) en pacientes en quienes se había usado ibuprofeno como primera línea (16 pacientes). En ninguno de los dos estudios se evidenció elevación de AST ni de ALT (tabla 7).
Comparación de transaminasas y bilirrubina antes y después del eso del paracetamol
| Antesa | Despuésa | pa | Antesb | Despuésb | pb | |
|---|---|---|---|---|---|---|
| AST (U/l) | 46.8 ± 46.1 | 24.4 ± 8.7 | 0.02 | 40.9 ± 27.5 | 33 ± 1 8.3 | 0.04 |
| ALT (U/l) | 13.2 ± 11.5 | 10.5 ± 8.6 | 0.57 | 39.1 ± 17.21 | 33.3± ± 11.2 | 0.34 |
| B. total (μmol/l) | 84.2 ± 44.1 | 52.4 ± 41.3 | 0.0092 | 102.7± 30.7 | 103.7 ± 32.4 | 0.6 |
| B. directa (μmol/l) | 66.2 ± 41.9 | 34.9 ± 38.3 | 0.0076 | 80.03± 73.5 | 94.06 ± 35.5 | 0.44 |
ALT: alanino transferasa; AST: aspartato transaminasa.
El elevado aporte de líquidos endovenosos está en relación con el cierre o no del conducto arterioso, tal como lo describe el estudio de Stephens et al.15, que demuestra que el aporte hídrico al tercer día por encima de 161ml/kg de peso al día se relaciona con una persistencia del conducto arterioso o la reapertura de este; o en la revision de New Reviews16, que informa que volúmenes superiores de 170ml/kg de peso por día se asocia a un incremento en CAP.
ConclusionesEl uso de paracetamol de forma endovenosa puede ser una opción eficaz y segura en el cierre del CAP, con una efectividad del 90% para este estudio, en pacientes con contraindicación para uso de AINE nacidos a una altura como la de Bogotá. Con la salvedad de que se requieren estudios con mayor número de pacientes y con diseño metodológico distinto.
FinanciaciónNinguna.
Conflicto de interesesLos autores declaran no tener ningún tipo de conflicto de intereses en el desarrollo del presente estudio.
AgradecimientosA todo el personal de enfermería, de terapia respiratoria y todos los colegas que laboran en el lugar del estudio por su disposición para realizarlo.