La recomendación vigente de vacunación en prematuros es iniciar a la edad cronológica independientemente del peso y edad gestacional al nacer.
ObjetivoDescribir el estado de vacunación de los infantes prematuros menores de 1500g pertenecientes al programa de seguimiento pediátrico del INPer.
Material y métodosEstudio de cohorte descriptico retrospectivo y transversal. Se incluyeron infantes que acudieron a consulta de junio del 2008 a junio del 2009 con fecha de nacimiento del 2004-2008, se obtuvo de la cartilla nacional de vacunación la fecha de la administración de la vacuna y se interrogó la causa del retraso de la administración del mismo de acuerdo al esquema vigente.
ResultadosSe incluyeron 158 infantes. El 78.5% recibieron todas sus vacunas en el sector público. Transcurrieron 54.5 ± 30.2 días entre egreso y la primera aplicación de algún inmunógeno. La cobertura de vacunación contra influenza con dos dosis en el primer año de vida fue: 18.9%, contra rotavirus dos dosis: 59.5%, pentavalente acelular tres dosis: 73.5%, neumococo tres dosis: 28.2%, BCG: 98.1%, SRP: 100% y hepatitis B tres dosis: 77.8%. Todos los inmunógenos de administraron en forma atrasada. Las tres causas más frecuentes de rechazo en la vacunación fueron: peso bajo y/o prematurez, desabasto del biológico y antecedente de transfusión.
ConclusionesLos infantes prematuros mostraron retraso en la administración de todos los inmunógenos en relación con la recomendación del esquema nacional de vacunación, se debe de revisar las indicaciones vigentes para la administración de inmunógenos en esta población.
The current recommendation for vaccination in preterm infants is to start it at the chronological age, regardless of their birthweight or gestational age.
ObjectiveTo describe the vaccination status of premature infants born under 1500g, that were part of the INPer paediatric follow-up program.
Material and methodsA retrospective, cross-sectional and descriptive cohort study, conducted on infants who attended their clinics from June 2008 to June 2009, and born between 2004 and 2008. The vaccination dates were obtained from their national immunisation record book and, where applicable, the cause of the administration delay was questioned.
ResultsThe study included 158 infants, of whom 78.5% received all their vaccines in the public sector. A total of 54.5 ± 30.2 days elapsed between discharge and the first application of some immunogen. The vaccination coverage against influenza, with two doses in the first year of life, was: 18.9%, against rotavirus with two doses: 59.5%, acellular pentavalent, three doses: 73.5%, pneumococcus, three doses: 28.2%, BCG: 98.1%, MMR: 100%, and hepatitis B three doses: 77.8%. All immunogens were administered late. The three most frequent causes of immunisation rejection were: low weight and /or prematurity, lack of vaccines, and a history of transfusions.
ConclusionsIn premature infants there was a delay in the administration of all the immunogens as regards to the national vaccination recommendation. It is necessary to review the current indications for the administration of immunogens in this population.
La vacunación es una de las páginas más exitosas de la historia de la medicina. Es una de las estrategias de mayor impacto en salud pública que más ha influido en la expectativa de vida a nivel mundial1.
Los recién nacidos prematuros, especialmente los de muy bajo peso y los de menor edad gestacional, son inmunológicamente inmaduros comparados con los nacidos de término: ellos tienen mayor riesgo de estar expuestos a enfermedades cuyo curso puede ser grave o fatal, y la mayor parte de estas enfermedades son prevenibles por vacunación2,3.
Los prematuros tienen características inmunológicas particulares que los hacen más susceptibles a contraer infecciones, ya que se encuentran inmunocomprometidos por inmadurez3–6.
A partir de la 14 semanas de gestación comienza el paso de IgG de la madre al feto vía transplacentaria, sin embargo no es sino hasta después de las 32 semanas de gestación que las concentraciones de anticuerpos son suficientes para prevenir infección. Esta transferencia natural de anticuerpos se ve interrumpida por el nacimiento prematuro. El inmunocompromiso del prematuro se acentúa por la pobre disponibilidad de recibir en forma temprana leche materna, que confiere inmunidad pasiva mediante IgA y otros inmunomoduladores7.
Hoy en día se dispone de vacunas eficaces y seguras contra más de trece enfermedades, sin embargo, su uso aún es limitado en niños nacidos prematuros4.
Desde 1994 la Academia Americana de Pediatría (AAP) emite las primeras recomendaciones de vacunación para el infante prematuro, las mismas que han sido modificadas a través del tiempo. En la actualidad se reconoce y existe el consenso de que es mayor el beneficio que el riesgo de no vacunar a esta población de riesgo8.
Las primeras indicaciones de vacunación establecieron que el infante prematuro debería recibir su primer inmunógeno a su edad cronológica independientemente de su edad gestacional y de su peso al nacer, esta indicación incluyó a los prematuros hospitalizados y con displasia broncopulmonar, poco tiempo después se incluyó también a los infantes de peso extremadamente bajo al nacer8.
Los primeros inmunógenos administrados a los prematuros incluyeron: DPT de células completas (DPTW), Haemophilus influenzae (H. influenzae) de tipo b (Hib) y vacuna contra polio virus oral (VPO). Desde entonces se advierte y se describe que la respuesta inmunológica de los prematuros era menor y directamente proporcional a la edad gestacional y al peso al nacer.
Kirmani reporta una serie de casos, donde evalúa infantes prematuros menores de 1000g y menores de 29 semanas de gestación que fueron vacunados en promedio a los 70 días de vida contra DPTw, vacuna contra polio virus oral e Hib, ellos se evaluaron a los 7 años de vida, y se encontró que si bien los niveles de anticuerpos protectores son menores que los de los infantes a término, los títulos se encontraron por encima y dentro de los rangos de protección9.
D¿Angio también informa de una serie de prematuros evaluados a los doce meses de vida y vacunados a la edad cronológica, títulos protectores para toxoide tetánico, Hib y vacuna inactiva de poliovirus.
Con respecto a los efectos colaterales de las vacunas, se ha descrito que los infantes prematuros presentan en igual proporción que los infantes de término reacciones sistémicas y locales10.
Un motivo importante de preocupación y de investigación es la descripción de lo que se ha denominado como eventos cardiorrespiratorios, que consiste en lapsos breves de apneas, desaturaciones y bradicardias que se presentan dentro de las primeras 72h posteriores a la vacunación de prematuros hospitalizados11. Estos síntomas han sido informados desde 1994 por Botham, quien describió apneas, bradicardia y desaturaciones en 19 de 97 prematuros vacunados con DPTw, siendo más frecuentes en los de menor edad gestacional, los que recibieron mayor tiempo ventilación mecánica y con diagnóstico de displasia broncopulmonar12,13.
Carbone reporta también los efectos cardiorrespiratorios en los prematuros hospitalizados con un estudio clínico controlado y aleatorizado donde evaluó a 93 infantes que recibieron DPTa, sin demostrarse el incremento en los síntomas cardiorrespiratorios en la primera dosis del inmunógeno14.
Actualmente se reconoce que el beneficio de vacunar al prematuro frágil y vulnerable ante padecimientos graves como pertusis entre otros es mayor a la no vacunación por lo que la recomendación de la AAP sigue siendo vigente, pero se advierte que la vacunación del prematuro hospitalizado debe ser monitorizada hasta 72h posteriores, en especial al paciente inestable o con diagnóstico de displasia broncopulmonar o con apneas previas a la inmunización15,16.
A pesar de las recomendaciones actuales de la AAP los médicos de primer contacto se muestran resistentes a la inmunización del prematuro, por lo que esta indicación no se lleva a cabo incluso en los países desarrollados. Esto sucede en parte por la percepción de los médicos de que sea una práctica eficaz y segura así como por el miedo y la ansiedad de los padres que influye en la decisión del médico por lo que se establecen criterios arbitrarios para el inicio de la vacunación en función de un determinado peso, edad gestacional corregida o cronológica17,18.
Langkamp en el 2001 reporta el estatus de vacunación de 4230 niños donde se evidencia que esta población tiene mayor riesgo de retraso en las inmunizaciones durante el primer año de vida y que este retraso persiste hasta los 36 meses19.
El problema del retraso de la vacunación se ve acrecentada por las infecciones agudas y rehospitalizaciones que son más frecuentes en esta población de riesgo.
El objetivo fue describir el estado de la vacunación de los infantes prematuros menores de 1500g atendidos en la consulta de seguimiento pediátrico del INPer.
Material y métodosEstudio de cohorte descriptivo retrospectivo y trasversal.
- 1.
Población de estudio. Todos los infantes que acuden a la consulta de seguimiento pediátrico de junio de 2008 a junio del 2009 cuya fecha de nacimiento fuese a partir del 2004 al 2008.
Unidad de observación. Todos los infantes egresados del INPer que acuden a la consulta de seguimiento con peso menor de 1500g al nacer.
Criterios de inclusión:
- 1.
Peso al nacimiento menor de 1500g independientemente de su edad gestacional y de sus diagnósticos.
- 2.
Que al momento de la consulta pediátrica exhiban su Cartilla Nacional de Vacunación.
- 3.
Que acudan acompañados de su madre y que responda en forma completa la encuesta.
- 4.
Se incluirán los infantes independientemente de si las vacunas se aplicaron en el sector público o en el sector privado.
- 5.
Se incluyeron infantes independientemente de su lugar de residencia.
Criterios de exclusión:
- 1.
Que el acompañante del menor no sea su madre o cuidador principal.
- 2.
Malformaciones congénitas mayores.
Durante la consulta pediátrica se realizó de manera rutinaria la revisión de la cartilla de vacunación en la cual se obtuvieron las fechas en que se aplicaron las vacunas correspondientes a la edad del paciente y de presentar algún retraso se interrogó directamente a la madre sobre los motivos por los que no fue aplicada oportunamente la vacuna. Del expediente clínico se obtuvieron datos como el peso al nacimiento y el peso al egreso hospitalario. Así como la edad cronológica al egreso.
- •
BCG.
- •
Vacuna contra poliomielitis (VOP o VIP).
- •
DPT células completas o acelular + Hib.
- •
Vacuna contra hepatitis B.
- •
Vacuna triple viral.
- •
Vacuna contra neumococo.
- •
Vacuna contra rotavirus.
- •
Vacuna contra la influenza.
- •
Edad cronológica al momento de vacunar (fecha de nacimiento – fecha de vacunación).
- •
Presencia de retraso o no retraso (de acuerdo a recomendación vigente al momento de vacunar).
- •
Motivos de NO vacunación oportuna.
- •
Se aplicó en sector público o privado.
- •
Indicación médica.
- •
Enfermedad aguda.
- •
Uso de medicamentos (esteroides antibióticos, diuréticos etc.).
- •
Uso de oxígeno.
- •
Bajo peso.
- •
Reflujo gastroesofágico.
- •
Antecedente de transfusión durante la hospitalización.
- •
Edad gestacional corregida menor a la cronológica.
Se captó en días la edad en que se administraron las dosis para cada inmunógeno como lo señala el Esquema Nacional de Vacunación. Se consideró con esquema completo cuando a los nacidos en el año 2004 cumplieron con dos dosis de influenza en el primer año de vida; a los nacidos a partir del 2007, con tres dosis de pentavalente acelular y rotavirus, y a los nacidos a partir del 2008 con dos dosis de neumococo en el primer año de vida.
La información se capturó en una hoja de cálculo con el programa SPSS 17. Los cálculos estadísticos se realizaron con el programa SPSS versión 17. Se utilizó estadística descriptiva para definir las variables sociodemográficas de la población. Este trabajo se realizó en base a los esquemas vigentes del 2004 al 2007.
ResultadosSe incluyeron un total de 158 infantes con peso al nacimiento menor de 1500g que cumplieron con los criterios de inclusión, de ellos, 121 son producto de embarazo único y 37 de embarazo múltiple.
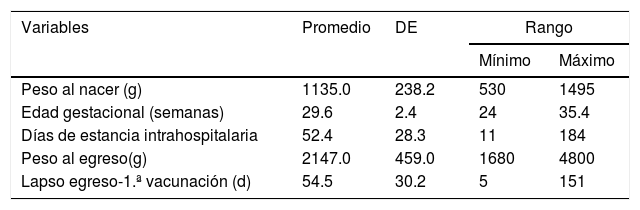
El peso promedio al nacimiento fue de 1135.8g ± 238.2. La edad gestacional de 29.6 ±2.4 semanas. Los días de hospitalización promedio de 52.4 días ± 28.3 días; se egresaron con un peso promedio de 2135.7± 485.0g, con peso mínimo de 1680 y máximo de 4800g. Transcurrieron un promedio de 54.5 ± 30.2 días entre egreso y la primera aplicación de algún inmunógeno, con un lapso mínimo de 5 días y máximo de 151 días (tabla 1).
Características generales del grupo de estudio
| Variables | Promedio | DE | Rango | |
|---|---|---|---|---|
| Mínimo | Máximo | |||
| Peso al nacer (g) | 1135.0 | 238.2 | 530 | 1495 |
| Edad gestacional (semanas) | 29.6 | 2.4 | 24 | 35.4 |
| Días de estancia intrahospitalaria | 52.4 | 28.3 | 11 | 184 |
| Peso al egreso(g) | 2147.0 | 459.0 | 1680 | 4800 |
| Lapso egreso-1.ª vacunación (d) | 54.5 | 30.2 | 5 | 151 |
El 78.5% de los infantes recibieron todas sus vacunas en el sector público, mientras que el 21.5% recibió al menos una vacuna en el sector privado (principalmente las vacunas contra el rotavirus y neumococo).
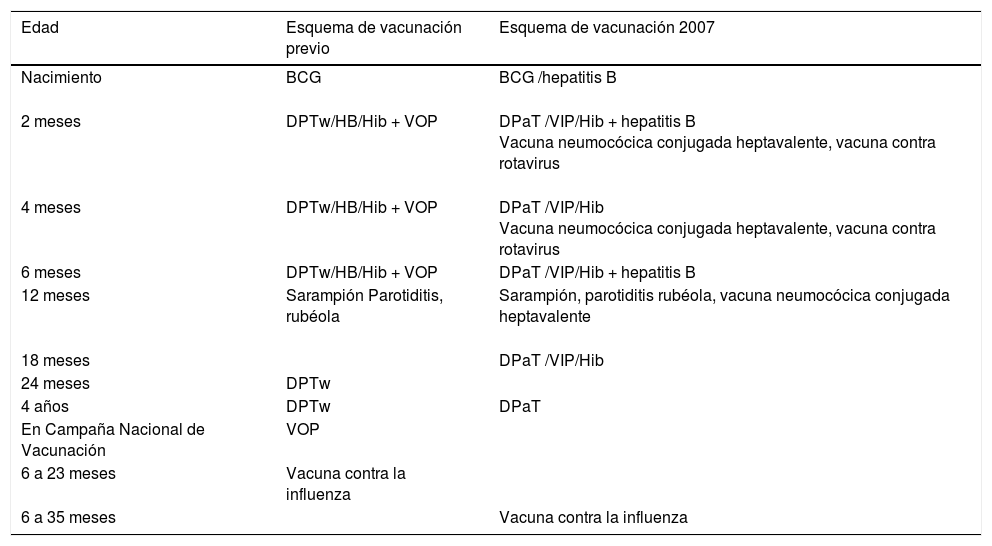
El esquema de vacunación y la cobertura fueron analizados de acuerdo a lo recomendado y disponible por la Norma Oficial Mexicana de Vacunación vigente al año de nacimiento de cada infante; en la tabla 2 se describe el esquema de vacunación a partir del año 2007 y el esquema previo.
Diferencias entre el esquema nacional de vacunación 2007 y su antecesor
| Edad | Esquema de vacunación previo | Esquema de vacunación 2007 |
|---|---|---|
| Nacimiento | BCG | BCG /hepatitis B |
| 2 meses | DPTw/HB/Hib + VOP | DPaT /VIP/Hib + hepatitis B Vacuna neumocócica conjugada heptavalente, vacuna contra rotavirus |
| 4 meses | DPTw/HB/Hib + VOP | DPaT /VIP/Hib Vacuna neumocócica conjugada heptavalente, vacuna contra rotavirus |
| 6 meses | DPTw/HB/Hib + VOP | DPaT /VIP/Hib + hepatitis B |
| 12 meses | Sarampión Parotiditis, rubéola | Sarampión, parotiditis rubéola, vacuna neumocócica conjugada heptavalente |
| 18 meses | DPaT /VIP/Hib | |
| 24 meses | DPTw | |
| 4 años | DPTw | DPaT |
| En Campaña Nacional de Vacunación | VOP | |
| 6 a 23 meses | Vacuna contra la influenza | |
| 6 a 35 meses | Vacuna contra la influenza |
Cobertura de acuerdo al esquema vigente a la fecha de nacimiento.
DPTw: vacuna contra difteria, tosferina y tétanos de células completas; DPaT: vacuna contra difteria, tosferina y tétanos acelular; VPO: vacuna contra virus poliomielitis oral; VIP: vacuna contra virus de poliomielitis intramuscular.
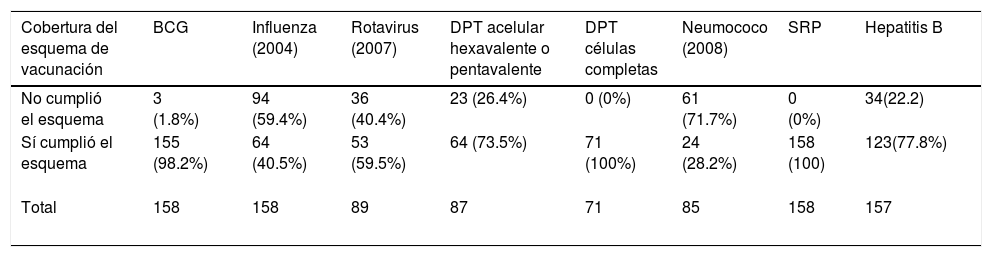
Desde el 2004 se inició la vacunación contra la influenza. Los 158 infantes debieron haber recibido la vacuna sin embargo solo 40.5%, recibieron dos dosis y solo 18.9% cumplieron el esquema de dos dosis en el primer año de vida. En el 2007 se inicia la vacunación antirrotavirus la cual se cumplió en nuestros pacientes solo en 59.5% con esquema completo de dos dosis antes del año, en el mismo año se introduce la vacunación con pentavalente acelular DPaT+ Hib+ IPV la cual se aplicó en el 73.5%, ya que el resto recibió el esquema antiguo con pentavalente de células completas (DPwT+ Hib+ HB). En el 2008 se inicia la inmunización contra neumococo lográndose solo en el 28.2% de nuestros pacientes con tres dosis (tabla 3).
Cumplimiento del esquema de vacunación vigente de acuerdo al año de nacimiento
| Cobertura del esquema de vacunación | BCG | Influenza (2004) | Rotavirus (2007) | DPT acelular hexavalente o pentavalente | DPT células completas | Neumococo (2008) | SRP | Hepatitis B |
|---|---|---|---|---|---|---|---|---|
| No cumplió el esquema | 3 (1.8%) | 94 (59.4%) | 36 (40.4%) | 23 (26.4%) | 0 (0%) | 61 (71.7%) | 0 (0%) | 34(22.2) |
| Sí cumplió el esquema | 155 (98.2%) | 64 (40.5%) | 53 (59.5%) | 64 (73.5%) | 71 (100%) | 24 (28.2%) | 158 (100) | 123(77.8%) |
| Total | 158 | 158 | 89 | 87 | 71 | 85 | 158 | 157 |
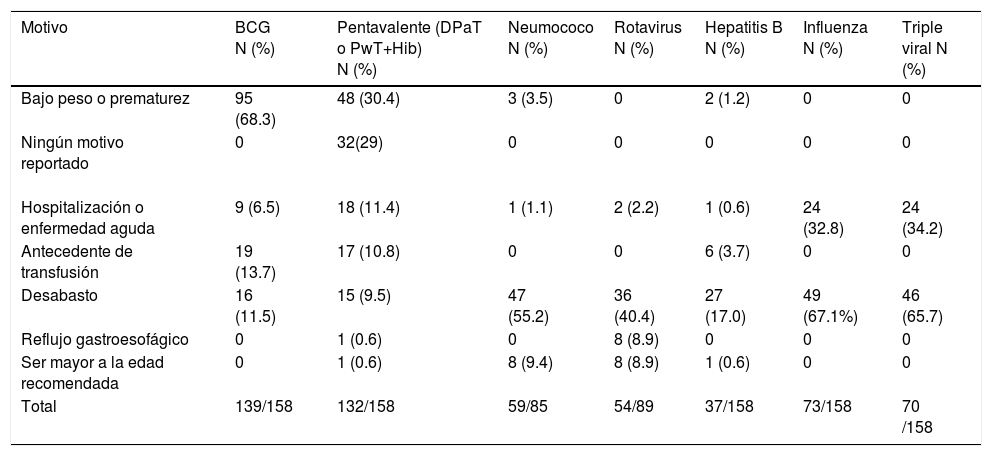
En relación a la vacuna BCG, se aplicó en 155 de los 158 infantes incluidos, con una cobertura del 98.1% de la población estudiada. La edad promedio de aplicación fue a los 119 ±65 días (3.9 meses) con una edad mínima de 27 y máxima de 386 días (12.8 meses). El bajo peso y la prematurez fue el motivo por el cual se pospuso o rechazó la administración del inmunógeno en el 68.3% de los casos, el antecedente de haber sido transfundido representó un 13.7% de los motivos de rechazo y 11.5% de las madres reportó que no se aplicó la vacuna por desabasto.
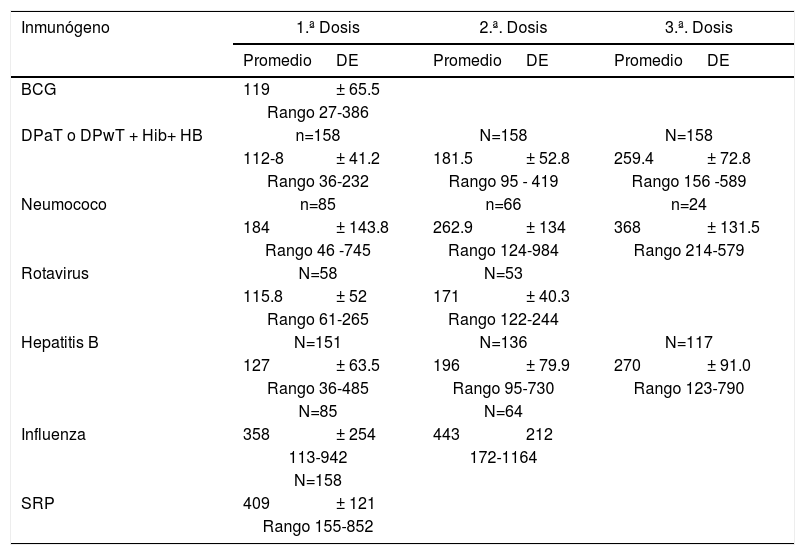
En cuanto a (DPaT o DPwT+ Hib) (difteria, tosferina, tétanos y H. influenzae) el total de infantes incluidos (158) fue vacunado con alguna de las 2 versiones de la vacuna pentavalente (acelular o de células completas). La primera dosis se aplicó a la edad promedio de 112.8±41.2 días (3.7 meses), con una edad mínima de 36 y máxima de 232 (7,7 meses) al momento de la aplicación. La segunda dosis se aplicó en promedio a los 181.5± 52.8días, (6 meses) y la tercera dosis llegó a aplicarse en promedio a los 259.4 ±75 días, (8.6 meses) con rango entre 156 y 589 días de vida (19.6 meses) los motivos para posponer la administración del inmunógeno en el 30.4% fue por bajo peso y/o prematurez, 11.4% por enfermedad aguda y/o hospitalización, 10.8% por antecedente de transfusión, 9.5% por desabasto. Con respecto a la vacuna contra el neumococo, la primera dosis se aplicó a 85 infantes del grupo estudiado, a la edad promedio de 184.2±143.8 días (6.1 meses) con rango entre 46- 745 días (24.8 meses) sesenta y seis infantes recibieron la segunda dosis, la cual se aplicó en promedio a los 262 días ± 134.3 (8.7 meses) con una edad mínima de 70 días y edad máxima de 560, (18.6 meses) solo 24 infantes (28.2%) completaron el esquema de 3 dosis antineumococo, siendo vacunados a la edad promedio de 368±131.5 días (11.5 meses) con rango entre 214 y 579 días (19.3 meses) siendo los motivos de no aplicación el desabasto en 55.2%, tener edad mayor a la que se debe vacunar 9.4%, bajo peso o prematurez 3.5% y 1.1% por enfermedad aguda. Para el rotavirus solo en 58 casos se aplicó la primera dosis, a la edad promedio de 115.8 ± 52 días (3.8 meses) con una edad mínima de 46 y máxima de 265 días (8.8 meses) solo 53 infantes completaron las 2 dosis recomendadas, y esta se aplicó a los 171 días± 40.3 de vida (5.7 meses). Las razones referidas para posponer la vacunación fueron en orden 40.4% por desabasto, 8.9% por tener edad mayor a la que se debe vacunar, 8.9% por reflujo gastroesofágico y 2.2% por enfermedad aguda y/o hospitalización. Para la vacuna antihepatitis B de los 158 niños analizados 149 (95.5%) recibió al menos una dosis de hepatitis B en forma aislada o combinada. Ciento treinta y seis (86,0%) recibieron dos dosis, y 117 (75.9%) recibieron tres dosis. La primera dosis se aplicó a la edad promedio de 127 ± 63.5 días, (4.2 meses) con una edad mínima de 36 y máxima de 485 días (16.1 meses). La segunda dosis se administró en promedio a los 196 ± 79.9 días de vida, (6.5 meses) con edad mínima de 95 y máxima de 730 días (24.3 meses) la tercera se aplicó en promedio a los 270 ± 91 días de vida (9 meses) con una edad mínima de 123 y máxima de 790 días (26.3 meses) la vacunación se retrasó en el 17% por desabasto, 3.7% por transfusión, 1.2% por bajo peso y por edad mayor a la que se debe vacunar 0.6%. La vacuna contra la influenza para los 158 niños era obligatorio administrarla, sin embargo solo se cumplió el esquema en el 40.5% con dos dosis, únicamente 18.9% lo cumplieron dentro del primer año de vida. La primera dosis se aplicó en promedio a los 358 ± 154 días de vida, (11.9 meses) con un rango que osciló entre los 180 días y los 942 días (31.4 meses) y la segunda dosis a los 443 ± 212 días (14.7 meses) con edad mínima de 172 y máxima de 1164 días (38.8 meses). La razón reportada para el retraso de la vacunación fue en el 67.1% por desabasto y 32.8% por enfermedad aguda. Por último para la triple viral (sarampión – rubeóla – parotiditis) se administró en promedio a la edad de 409 ±101-4 días de vida, (13.6 meses) siendo aplicada a la edad más temprana de 335 días de vida y la edad más tardía a los 852 días (28.4 meses). El motivo más frecuente para el retraso en la administración fue el desabasto del biológico en 65.7% y por enfermedad aguda 34.2% (tablas 4 y 5).
Edad en días de aplicación de los inmunógenos del esquema básico de vacunación durante el primer año de vida
| Inmunógeno | 1.ª Dosis | 2.ª. Dosis | 3.ª. Dosis | |||
|---|---|---|---|---|---|---|
| Promedio | DE | Promedio | DE | Promedio | DE | |
| BCG | 119 | ± 65.5 | ||||
| Rango 27-386 | ||||||
| DPaT o DPwT + Hib+ HB | n=158 | N=158 | N=158 | |||
| 112-8 | ± 41.2 | 181.5 | ± 52.8 | 259.4 | ± 72.8 | |
| Rango 36-232 | Rango 95 - 419 | Rango 156 -589 | ||||
| Neumococo | n=85 | n=66 | n=24 | |||
| 184 | ± 143.8 | 262.9 | ± 134 | 368 | ± 131.5 | |
| Rango 46 -745 | Rango 124-984 | Rango 214-579 | ||||
| Rotavirus | N=58 | N=53 | ||||
| 115.8 | ± 52 | 171 | ± 40.3 | |||
| Rango 61-265 | Rango 122-244 | |||||
| Hepatitis B | N=151 | N=136 | N=117 | |||
| 127 | ± 63.5 | 196 | ± 79.9 | 270 | ± 91.0 | |
| Rango 36-485 | Rango 95-730 | Rango 123-790 | ||||
| N=85 | N=64 | |||||
| Influenza | 358 | ± 254 | 443 | 212 | ||
| 113-942 | 172-1164 | |||||
| N=158 | ||||||
| SRP | 409 | ± 121 | ||||
| Rango 155-852 | ||||||
Motivo por el cual no se aplicó la vacunación o se retrasó su aplicación
| Motivo | BCG N (%) | Pentavalente (DPaT o PwT+Hib) N (%) | Neumococo N (%) | Rotavirus N (%) | Hepatitis B N (%) | Influenza N (%) | Triple viral N (%) |
|---|---|---|---|---|---|---|---|
| Bajo peso o prematurez | 95 (68.3) | 48 (30.4) | 3 (3.5) | 0 | 2 (1.2) | 0 | 0 |
| Ningún motivo reportado | 0 | 32(29) | 0 | 0 | 0 | 0 | 0 |
| Hospitalización o enfermedad aguda | 9 (6.5) | 18 (11.4) | 1 (1.1) | 2 (2.2) | 1 (0.6) | 24 (32.8) | 24 (34.2) |
| Antecedente de transfusión | 19 (13.7) | 17 (10.8) | 0 | 0 | 6 (3.7) | 0 | 0 |
| Desabasto | 16 (11.5) | 15 (9.5) | 47 (55.2) | 36 (40.4) | 27 (17.0) | 49 (67.1%) | 46 (65.7) |
| Reflujo gastroesofágico | 0 | 1 (0.6) | 0 | 8 (8.9) | 0 | 0 | 0 |
| Ser mayor a la edad recomendada | 0 | 1 (0.6) | 8 (9.4) | 8 (8.9) | 1 (0.6) | 0 | 0 |
| Total | 139/158 | 132/158 | 59/85 | 54/89 | 37/158 | 73/158 | 70 /158 |
Los recién nacidos prematuros especialmente los de muy bajo peso y menor edad gestacional son inmunológicamente inmaduros comparados con los nacidos a término, ellos tienen mayor riesgo de estar expuestos a enfermedades cuyo curso puede ser grave o fatal, la mayor parte de estas enfermedades son prevenibles por vacunación2,3.
Davis al analizar el estatus de vacunación de 11,580 infantes de bajo peso al nacer, observó que los prematuros tienden a presentar mayor retraso en recibir las vacunas recomendadas, lo que no sucede con los nacidos a término20. Numerosos estudios ya establecen que la respuesta inmunológica en infantes de bajo peso es eficaz y segura cuando se vacunan a la edad cronológica4,8,10,12.
Se ha descrito por diversos estudios la presencia de eventos cardiorrespiratorios secundarios a la inmunización de estos infantes, por lo que se sugiere la cuidadosa monitorización posterior al procedimiento13,16. En el presente estudio se evidencia que los infantes son aptos para vacunarse al momento del alta cuando se encuentran clínicamente estables y con bajo riesgo de apneas, pero se demuestra que transcurren en promedio 50 días en que reciben su primera vacuna, lo cual se traduce en un periodo innecesariamente prolongado de retardo para la aplicación del inmunógeno.
De acuerdo a los resultados del presente estudio, la vacuna BCG alcanzó una cobertura del 98.1%. El promedio de los infantes nacidos con peso menor a 1500g recibió la vacuna a la edad de 4 meses de vida. Negrete-Esqueda demostraron en un estudio de 84 prematuros vacunados con BCG que la respuesta inmunológica si bien podía ser disminuida, es suficiente para desarrollar protección contra enfermedad invasiva por tuberculosis en la mayoría de los casos, demostrando que, a pesar de la inmadurez o el bajo peso al nacer, la eficacia de la vacuna es adecuada21. En nuestro estudio encontramos que los infantes con peso menor de 1500g al nacer se egresan en su mayoría con peso promedio de 2000g por lo que es factible vacunarlos en el momento del egreso. El bajo peso y la prematurez no son motivos justificados para retrasar aún más la aplicación de la vacuna que en el presente estudio fue el motivo más frecuente del retraso del inmunógeno.
De las razones documentadas para no aplicar o posponer aún más la administración de DPaT-Hib-IPV o DPwT-Hib-HB, se encontró nuevamente al bajo peso y/o prematurez. En diferentes publicaciones se refiere que la vacunación debe aplicarse a la edad cronológica independiente del peso y la edad gestacional22,23. A pesar de que las 3 dosis de la vacuna se aplicaron en los 158 infantes los tiempos de aplicación se encuentran desfasados, es pertinente comentar que los infantes tuvieron una edad cronológica y peso apropiado a su egreso y pudieron haber sido vacunados, como lo establece la recomendación más reciente de la AAP, en que los infantes deben inmunizarse incluso hospitalizados para evitar el retraso y ofrecer el monitoreo adecuado especialmente a los de muy bajo peso o dependientes de oxígeno.
En el presente estudio se demuestra que los pacientes que se vacunaron con el esquema de DPwT de células completas (actualmente no vigente), que contenía la vacuna de hepatitis B, ofreció un 100% de cobertura mientras que con el esquema nuevo de DPT acelular, la vacuna antihepatitis B se aplicó en forma separada y solo el 40% completaron 3 dosis. La causa principal para la no aplicación de la segunda, o tercera dosis de este inmunógeno fue el desabasto, siendo responsabilidad del sector salud el otorgamiento del biológico.
Los hallazgos muestran que la aplicación de la vacuna pentavalente ya sea en su presentación acelular o de células completas (actualmente no vigente) demuestra que en promedio reciben su esquema básico a los 4, 6 y 9 meses de vida retardado hasta 3 meses, lo que concuerda con los resultados de Langkman y Magoon que refieren que en la población de prematuros el retraso en la inmunización se extiende hasta los 3 años de vida19,24.
A partir del 2007 se incorporan al esquema nacional de vacunación las inmunizaciones contra rotavirus y neumococo25. La Academia Americana de Pediatría estableció 3 dosis de vacuna conjugada heptavalente con un refuerzo entre los 12 a 15 meses de edad para disminuir el riesgo de enfermedad invasiva por neumococo y eliminar el estado portador, actualmente esta vacuna esta descontinuada y la que se aplica es la 13 valente23, 28.3% de los infantes cumplieron el esquema de dos dosis contemplado en ese año por el sector salud nacional de nuevo uno de los motivos para retardar la vacunación fue el desabasto del biológico.
Con respecto a la vacunación contra rotavirus, el 59.5% recibió las dos dosis, el resto no cumplió con el esquema debido al desabasto del biológico. Las recomendaciones de aplicación son a los 2 y 4 meses. En nuestros pacientes la primera dosis se aplicó tardíamente a los 4 meses de edad, otra causa interesante y no justificada para la no aplicación del biológico fue el padecer reflujo gastroesofágico.
La tasa de contagio por hepatitis B se ha incrementado notablemente en los últimos 20 años. Son varios los factores que han favorecido el aumento en la seropositividad en la población mexicana como la globalización, migración y cambio en las conductas sexuales. La transmisión vertical en el periodo perinatal cobra gran importancia debido al alto porcentaje de contagio, sin embargo es 100% prevenible por vacunación1,26,27. En el presente estudio no se cumple con la recomendación de la Academia Americana de Pediatría y de la OMS con respecto a la aplicación de la primera dosis contra la hepatitis B al nacer ni ante un estado serológico materno desconocido, como lo es en la población de los infantes estudiados.
La influenza es una enfermedad cuya epidemiología ha cambiado en los últimos años1. En México la vacunación se realiza en temporada de riesgo a todos los menores de 3 años y mayores de 60 años, además del esquema de 2 dosis cuando se inicia por primera vez la administración de este inmunógeno25. La Academia Americana de Pediatría emite además la recomendación de vacunar contra la influenza a los familiares o contactos domiciliarios de los infantes de riesgo22, la cobertura contra la influenza en los prematuros estudiados es la más baja reportada comparada con el resto de los inmunógenos, a pesar de que es la vacuna que se incluye en el esquema nacional desde 200425, solo el 40.5% de los nacidos con peso menor a 1500g recibieron dos dosis, y solo el 18.9% la recibieron en el primer año de vida, siendo la causa principal el desabasto del biológico.
Tomando en cuenta que el 81% de nuestra población estudiada depende exclusivamente del sector público para recibir las vacunas, surge la importancia de la disponibilidad en las instituciones de salud de todos los inmunógenos establecidos en la Cartilla Nacional de Vacunación y el conocimiento completo y actualizado de las contraindicaciones para la administración de inmunógenos basado en la evidencia clínica28,29.
ConclusionesEl grupo de prematuros de riesgo mostró un retraso en la administración de todos los inmunógenos que se aplican en el primer año de vida en relación con la recomendación del esquema nacional de vacunación. La población de prematuros estudiados cumplió con el requisito de edad gestacional y peso adecuados para recibir su primera vacunación oportuna. El bajo peso y el antecedente de prematurez y transfusión fueron las causas principales que provocaron el retraso aún más para la administración de la primera vacuna. La edad gestacional o el peso menor de 2kg no son contraindicaciones para ninguna vacuna. Siempre se debe valorar el beneficio ofrecido con la vacunación sobre el riesgo de aplicar el inmunógeno. Queda mucho por hacer con respecto a la práctica diaria en cuanto a la aplicación de vacunas en nuestro país, tanto a nivel intrahospitalario como extrahospitalario. Se debe garantizar por parte de las autoridades de salud la disponibilidad de los inmunógenos establecidos en el esquema nacional de vacunación.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.