El zolpidem es un hipnótico no benzodiazepínico modulador del receptor GABA que podría proporcionar beneficios en diversos trastornos del movimiento.
Casos clínicosPresentamos a 5 pacientes con enfermedad de Parkinson que experimentaron una mejoría significativa en los síntomas motores y no motores luego del tratamiento con este fármaco. Además observamos mejorías en las complicaciones motoras asociadas a levodopa y discutimos el posible mecanismo de acción.
ConclusiónLos moduladores del sistema GABA-érgico, tales como el zolpidem, podrían representar una alternativa adicional en el tratamiento de esta enfermedad. Se necesitan más estudios para determinar los beneficios y riesgos del uso de este tipo de fármacos en la enfermedad de Parkinson y otros trastornos del movimiento.
Zolpidem is a non-benzodiazepine GABA-modulator that may provide benefit in various movement disorders.
Clinical casesWe report 5 patients with Parkinson's disease who experienced significant improvement in motor and non-motor symptoms following treatment with this drug. In addition we observed improvements in levodopa-associated motor complications and discuss the possible mechanism of action.
ConclusionModulators of the GABAergic system, such as zolpidem, may offer an alternative therapeutic approach for patients with Parkinson's disease. Further studies are needed to determine the benefits and risks of using this class of drugs in Parkinson's disease and other movement disorders.
El zolpidem (ZLP) es un hipnótico no benzodiazepínico de corta acción, que se usa comúnmente en el tratamiento del insomnio. Este fármaco es un modulador alostérico positivo del receptor ácido gamma-aminobutírico tipo A (GABAA); se une al sitio benzodiacepínico de la subunidad α1 del receptor aumentando la afinidad de este por su ligando endógeno, el neurotransmisor inhibitorio GABA.
En la literatura, existen reportes de efectos beneficiosos con ZLP en los síntomas motores de la enfermedad de Parkinson (EP), en la parálisis supranuclear progresiva y en la distonía-parkinsonismo ligado al X (enfermedad de Lubag)1-6. Más recientemente, se ha observado que el ZLP podría ser también efectivo en el tratamiento del blefaroespasmo, del síndrome de Meige y de otro tipo de trastornos neurológicos6-8.
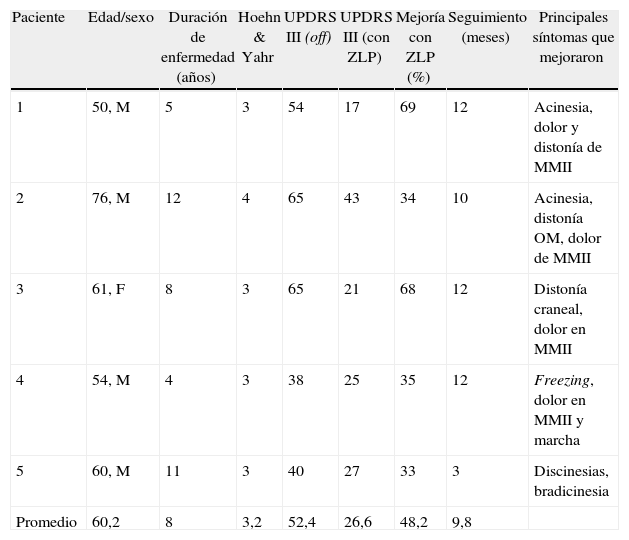
Presentamos a 5 pacientes con EP que experimentaron una considerable mejoría en los síntomas motores y no motores luego de una dosis aguda de ZLP. Los sujetos, luego de dar su consentimiento informado, fueron evaluados con la Unified Parkinson's Disease Rating Scale (UPDRS) III en el estado de off definido (12 h después de la última toma de medicación antiparkinsoniana), y 60 min después de recibir 7,5mg de ZLP. Los datos demográficos se muestran en la tabla 1.
Características clínico-demográficas
| Paciente | Edad/sexo | Duración de enfermedad (años) | Hoehn & Yahr | UPDRS III (off) | UPDRS III (con ZLP) | Mejoría con ZLP (%) | Seguimiento (meses) | Principales síntomas que mejoraron |
| 1 | 50, M | 5 | 3 | 54 | 17 | 69 | 12 | Acinesia, dolor y distonía de MMII |
| 2 | 76, M | 12 | 4 | 65 | 43 | 34 | 10 | Acinesia, distonía OM, dolor de MMII |
| 3 | 61, F | 8 | 3 | 65 | 21 | 68 | 12 | Distonía craneal, dolor en MMII |
| 4 | 54, M | 4 | 3 | 38 | 25 | 35 | 12 | Freezing, dolor en MMII y marcha |
| 5 | 60, M | 11 | 3 | 40 | 27 | 33 | 3 | Discinesias, bradicinesia |
| Promedio | 60,2 | 8 | 3,2 | 52,4 | 26,6 | 48,2 | 9,8 |
F: femenino; M: masculino; MMII; miembros inferiores; OM: oromandibular; UPDRS III: Unified Parkinson's Disease Rating Scale (puntaje motor); ZLP: zolpidem.
Sujeto masculino de 50 años, con una historia de EP de 5 años de evolución, que presentaba periodos off severos asociados a acinesia, dolor en miembros inferiores (MMII) y distonía en pies. Se encontraba medicado por su enfermedad con pramipexol 3mg/día, agregándose en los últimos 3 años levodopa hasta 750mg/día. Incidentalmente, el paciente notó que el ZLP recetado para su insomnio aliviaba también sus síntomas parkinsonianos en forma similar a la levodopa. El puntaje en la UPDRS III en off era de 54 y luego de la administración de 7,5mg de ZLP disminuyó a 17 (mejoría del 69%). Luego de un año, el paciente continúa utilizando el ZLP a dosis de 5mg 3 veces al día, con beneficio sostenido (ver Anexo 1 como material adicional online en donde se muestra el antes y el después del tratamiento con Zolpidem).
Caso 2Sujeto masculino de 76 años, con EP avanzada de 12 años de evolución, con deterioro cognitivo leve. Había utilizado agonistas dopaminérgicos, pero en los últimos 6 años su tratamiento de base era levodopa y entacapona, ambos a una dosis media de 1.000mg/día. Durante sus periodos off presentaba acinesia con distonía en pies y oromandibular, y dolor en MMII. Estaba perdiendo peso debido a sus frecuentes periodos off asociados a la distonía oromandibular. Luego de la administración de 7,5mg de ZLP el puntaje de la UPDRS III disminuyó de 65 a 43 (34% de mejoría). Se inició ZLP 5mg 3 veces por día y comenzó a ganar peso. Dos meses después, desarrolló alucinaciones visuales luego de incrementar la dosis por cuenta propia a 20mg día. A pesar de la suspensión de dicho tratamiento, el paciente admitió que ocasionalmente utilizaba ZLP como una medicación de «rescate», cuando la levodopa no aliviaba suficientemente sus síntomas (ver Anexo 1 como material adicional online en donde se muestra el antes y el después del tratamiento con Zolpidem).
Caso 3Mujer de 61 años con 6 años de enfermedad, con queja de distonía cervical dolorosa en off y dolor en MMII. Utilizó pramipexol a dosis plenas (4mg/día) y en los últimos 2 años agregó levodopa hasta 900mg/día y amantadina hasta 300mg/día. Luego de 20 min de la administración de 7,5mg de ZLP, desaparecieron dichos síntomas y la puntuación de la UPDRS III disminuyó de 65 a 21 (68% de mejoría). El inicio subsiguiente de 2,5mg de ZLP 3 veces por día redujo significativamente sus episodios distónicos diarios, manteniéndose todavía el beneficio luego de 12 meses.
Caso 4Sujeto masculino de 54 años, con historia de EP de 4 años de evolución, complicada por fluctuaciones motoras. Comenzó su tratamiento con pramipexol, llegando a una dosis de 4mg/día y en el último año se agregó levodopa hasta 500mg/día. Estando en off experimentaba dificultades de la marcha, incluyendo freezing, así como dolor en los MMII. Luego de 7,5mg de ZLP, mejoró la marcha y se resolvió el freezing, mientras que la puntuación de la UPDRS III disminuyó de 38 a 25 (35% de mejoría). Dos meses más tarde se repitió la prueba, observándose el mismo efecto beneficioso, por lo que se instauró el tratamiento a una dosis de 5mg 3 veces al día.
Caso 5Sujeto masculino de 60 años, con 11 años de enfermedad, que presentaba fluctuaciones motoras y discinesias incapacitantes en on. Utilizó pramipexol hasta 3mg/día y en los últimos 4 años se le agregó levodopa hasta 1.500mg/día y, posteriormente, amantadina hasta 300mg/día. Su estado off se caracteriza por bradicinesia y dificultades en la marcha. La administración de 7,5mg de ZLP disminuyó la UPDRS III de 40 a 27 (33% de mejoría) y la gravedad de las discinesias en on fue menor comparada con las que presentaba habitualmente con la levodopa. Posteriormente, se inició ZLP a una dosis de 2,5mg 4 veces al día, reduciendo, a su vez, la dosis total de levodopa en un 25%. En el último seguimiento, 3 meses después, sus discinesias ya no eran incapacitantes.
ComentariosLos síntomas motores mejoraron en todos los pacientes después de la administración por vía oral de 7,5mg de ZLP. Las puntuaciones en la UPDRS III mejoraron entre un 33 y 69%. Las distonías del periodo off resolvieron completamente en los 3 pacientes que las presentaban. El freezing y el dolor de MMII del periodo off mejoraron también luego del ZLP y se observó una considerable reducción de las discinesias en el on en el paciente 5.
El inicio del efecto beneficioso osciló entre 10 y 40 min, siendo óptimo para los síntomas parkinsonianos después de 1-2 h. El alivio del dolor y de la distonía fue más rápido que el efecto antiparkinsoniano. La duración media de acción fue de 4 h (rango de 2,5 a 5,5 h), y coincide con la vida media corta del ZLP (2 a 2,9 h)9. No hubo eventos adversos graves y ningún paciente experimentó somnolencia significativa durante la prueba aguda. El paciente 4 presentó somnolencia, pero fue breve y transitoria. En el seguimiento, el paciente de mayor edad (caso 2), que presentaba deterioro cognitivo leve previo, desarrolló alucinaciones visuales. Esto ocurrió luego de aumentar, por propia voluntad, la dosis diaria de ZLP a más de 20mg.
Si bien en este pequeño grupo de pacientes el ZLP fue sorprendentemente bien tolerado a las dosis administradas, es necesario tener precaución dada su indicación primaria como hipnótico y sus posibles efectos secundarios, especialmente frecuentes en ancianos9. Curiosamente, Wesensten et al. observaron que 10mg de ZLP dados durante el día eran subhipnóticos, ya que no indujeron somnolencia en 80 voluntarios sanos10. Esto está de acuerdo con observaciones anteriores que demuestran que el ZLP a dosis de 5 y 10mg fue insuficiente para promover el sueño diurno11. Por otro lado, se han utilizado dosis altas de ZLP para tratar el blefaroespasmo7, la EP y la enfermedad de Lubag2,3,5, con sorprendente buena tolerancia. Nuestros resultados confirman y extienden observaciones anteriores en relación con que el ZLP puede tener efectos antiparkinsonianos y antidiscinéticos en la EP. Además, encontramos que la distonía en off y los síntomas no motores, como el dolor en off, también pueden mejorar considerablemente con este fármaco. Estudios en animales proporcionan un fundamento para los efectos beneficiosos de ZLP. Estudios autoradiográficos en cerebros de ratas revelan una alta densidad de receptores de ZLP en áreas crucialmente implicadas en la fisiopatología de la EP, como el globo pálido (GP), la sustancia negra pars reticulata (SNR) y el núcleo subtalámico (STh)12,13. Experimentos con patch-clamp en neuronas subtalámicas, palidales, y de sustancia negra de ratones demuestran que el ZLP aumenta las corrientes sinápticas inhibitorias del receptor GABAA (Chen et al., Chen et al., Zhang et al.14-16). Por lo tanto, en la EP, el ZLP podría actuar inhibiendo la actividad excesiva en uno o más de estos núcleos. Consecuente con lo anterior, la microinyección de ZLP en la SNR y en el STh de roedores causó una rotación contralateral, mientras que la inyección en el GP (equivalente al GP externo humano) causó rotación ipsolateral. Por lo tanto, es concebible que en humanos con EP, el ZLP actúe modulando el equilibrio entre las vías directa e indirecta y, como tal, mejorando tanto los síntomas parkinsonianos como los discinéticos. En concordancia con estos hallazgos en roedores, se conoce que microinyecciones de muscimol, un agonista de GABA, en el STh o en el GP de pacientes con EP sometidos a cirugía de estimulación cerebral profunda o palidotomía, aliviaron sus síntomas17,18. Esto confirma que la inactivación de la actividad neuronal excesiva en estas áreas mediante la estimulación de las vías GABA-érgicas, mejora los síntomas motores de la EP.
En conclusión, nuestros resultados apoyan la hipótesis en relación con que el ZLP modula la neurotransmisión GABA-érgica en varias estaciones dentro de los circuitos de los ganglios basales para mejorar los síntomas motores, incluyendo la distonía en off y las discinesias inducidas por levodopa, así como otros síntomas no motores, tales como el dolor. Los agonistas selectivos GABA-érgicos, como el ZLP, podrían representar una alternativa terapéutica para los pacientes con EP, en especial aquellos con complicaciones asociadas a la L-dopa.
Se necesitan estudios controlados y aleatorizados para determinar los beneficios y riesgos del uso de ZLP u otros compuestos de esta clase de fármacos en el tratamiento de la EP y de otros trastornos del movimiento.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesEl Dr. L. Verhagen M. declara tener una beca de Parkinson's Disease Foundation Research Center. El resto de los autores no declaran conflictos de interés
Agradecemos al Dr. S.A. Rodriguez Quiroga y a Martin Frías por el apoyo técnico.
Segmento 1. Paciente 1 en estado off y luego de 7,5mg de ZLP. Se observa significativa mejoría en la marcha, en la expresión facial y en el finger-tapping luego de la administración del ZLP.
Segmento 2. Se observa al paciente 2 en estado off con acinesia asociada a síntomas no motores (dolor en miembros inferiores, disfagia, disnea y ansiedad). Luego de la administración del ZLP se resuelven los síntomas no motores y se aprecia una considerable mejoría en la expresión facial, en el fingertapping y en la marcha.