El dolor presenta elevadas tasas de prevalencia en la población con esclerosis múltiple (EM), siendo el 50% de carácter crónico y clasificándose en tipo nociceptivo, neuropático o mixto. Afecta a la calidad de vida, al sueño y a las actividades de la vida diaria. La electroterapia se presenta como una interesante alternativa o complemento en el abordaje del dolor en EM, presentando constantes innovaciones.
Material y métodosEste estudio valora la eficacia de la terapia por señales electromagnéticas pulsadas y transmitidas de manera dieléctrica monopolar (SEDM) en procesos dolorosos asociados a EM mediante un ensayo clínico aleatorizado sobre 24 pacientes a los que se les medirá el dolor mediante Brief Pain Inventory, la calidad de vida con MusiQoL, la depresión con Beck y la fatiga mediante Modified Fatigue Impact Scale.
ResultadosSe hallaron mejoras estadísticamente significativas en puntuaciones máximas y medias de dolor, así como en interferencia del dolor a nivel laboral, a nivel de relaciones personales, del sueño y el descanso. Las diferencias entre grupo de intervención y placebo no fueron significativas.
ConclusionesEl tratamiento con SEDM podría ser efectivo para reducir el dolor en pacientes con EM, siendo necesarios más estudios para mostrar su efectividad respecto al placebo y diferenciar en qué tipología de dolor puede ser más eficaz.
Pain is highly prevalent in patients with multiple sclerosis (MS); it is chronic in 50% of cases and is classified as nociceptive, neuropathic, or mixed-type. Pain affects quality of life, sleep, and the activities of daily living. Electrotherapy is an interesting alternative or complementary treatment in the management of pain in MS, with new innovations constantly appearing.
Material and methodsThis study evaluates the effectiveness of treatment with monopolar dielectric transmission of pulsed electromagnetic fields (PEMF) for pain associated with MS. We performed a randomised, placebo-controlled clinical trial including 24 patients, who were assessed with the Brief Pain Inventory, the Multiple Sclerosis International Quality of Life questionnaire, the Beck Depression Inventory, and the Modified Fatigue Impact Scale.
ResultsStatistically significant improvements were observed in maximum and mean pain scores, as well as in the impact of pain on work, personal relationships, and sleep and rest. Not significant differences were found between the treatment and placebo groups.
ConclusionsTreatment with PEMF may be effective in reducing pain in patients with MS, although further research is necessary to confirm its effectiveness over placebo and to differentiate which type of pain may be more susceptible to this treatment.
La esclerosis múltiple (EM) es una enfermedad neurodegenerativa caracterizada por la desmielinización, la pérdida axonal y la inflamación del sistema nervioso central. Aunque existe una amplia variedad de terapias, tanto sintomáticas como inmunomoduladoras, todavía no es curable ya que su etiología no es plenamente conocida1-3. La EM afecta a jóvenes y adultos de mediana edad, siendo primera causa de discapacidad neurológica de origen no traumático en España4.
Los estudios de prevalencia estiman que entre el 26 y el 86% de los pacientes con EM sufre dolor5-7 y al menos el 50% de ellos de tipo crónico6. Este hecho marca un impacto negativo sobre una variedad de dominios funcionales, incluyendo sueño, actividades ocupacionales, recreativas y actividades de la vida diaria en general, empeorando por tanto la calidad de vida8-10.
Se han propuesto clasificaciones del dolor en EM en función del mecanismo fisiopatológico subyacente6,7,11:
- –
Dolor neuropático: disestésico, que surge por lesión o enfermedad del sistema nervioso.
- –
Dolor nociceptivo: dolor músculo-esquelético asociado a lesión tisular real o potencial que responde a los mecanismos sensitivos convencionales.
- –
Dolor mixto: espasmos tónicos dolorosos y dolor muscular asociado a espasticidad.
El tratamiento convencional del dolor en EM consiste en el uso de analgésicos, antiepilépticos, antidepresivos, opiáceos y cannabinoides, que a menudo no obtienen el resultado suficiente y elevan el número de consultas al sistema público de salud, disminuyéndose además la satisfacción del paciente con la atención recibida en el control de su dolor11. Sin embargo, el abordaje del dolor en EM requiere evaluar el tipo, la intensidad y la causa que lo origina. La complejidad de su expresión y origen multifactorial requiere de diferentes estrategias para tratarlo con efectividad12, por lo que podría ser útil complementar los tratamientos farmacológicos con tratamientos de fisioterapia13.
La fisioterapia habitualmente combina diferentes abordajes, desde el acondicionamiento físico, mejora de las compensaciones posturales, educación terapéutica a técnicas estrictamente analgésicas, como la electroterapia. La electroterapia consiste en la aplicación de electricidad y sus efectos derivados (termoterapia, magnetoterapia, estimulación eléctrica…) con fines terapéuticos, habiendo demostrado varios estudios la eficacia de técnicas como la estimulación eléctrica nerviosa transcutánea (TENS) en el alivio del dolor en pacientes con EM14-17. Actualmente, existen técnicas de electroanalgesia más novedosas que suponen un importante avance respecto a la TENS en cuanto a mecanismo de transmisión y volumen de energía emitida con seguridad. Una de ellas es la terapia por emisión de señales electromagnéticas pulsadas y transmitidas de manera dieléctrica monopolar (SEDM), que combina diferentes efectos fisiológicos obtenidos por la aplicación de señales electromagnéticas moduladas digitalmente y adaptadas en intensidad, frecuencia, forma y duración para aumentar el umbral nociceptivo18,19, reducir la inflamación18,19, liberar endorfinas20,21 y movilizar las sustancias proinflamatorias y algógenas a nivel local22,23. La administración de estas señales se realiza de forma transcutánea mediante una transferencia dieléctrica y aplicación monopolar24,25, realizando depósitos energéticos focalizados25 en las áreas comprometidas en el proceso doloroso.
A día de hoy, no existen estudios sobre la eficacia de la terapia por SEDM en el tratamiento del dolor en pacientes con EM, únicamente experiencias clínicas sobre su uso en dolor neuropático, hecho que justifica la realización de estudios piloto que valoren su posible utilidad. De comprobarse la eficacia de la terapia por SEDM en los pacientes con dolor asociado a EM, se hallaría una nueva herramienta no invasiva y sin aparentes efectos secundarios que complementaría el abordaje del dolor en pacientes con EM.
El objetivo principal de este estudio es investigar el efecto de la terapia por SEDM en el tratamiento del dolor en sujetos con procesos dolorosos asociados a EM. Como objetivos secundarios se establece analizar los efectos que la posible mejora del dolor tiene en diferentes aspectos de vida del sujeto con EM, en la depresión y en la fatiga.
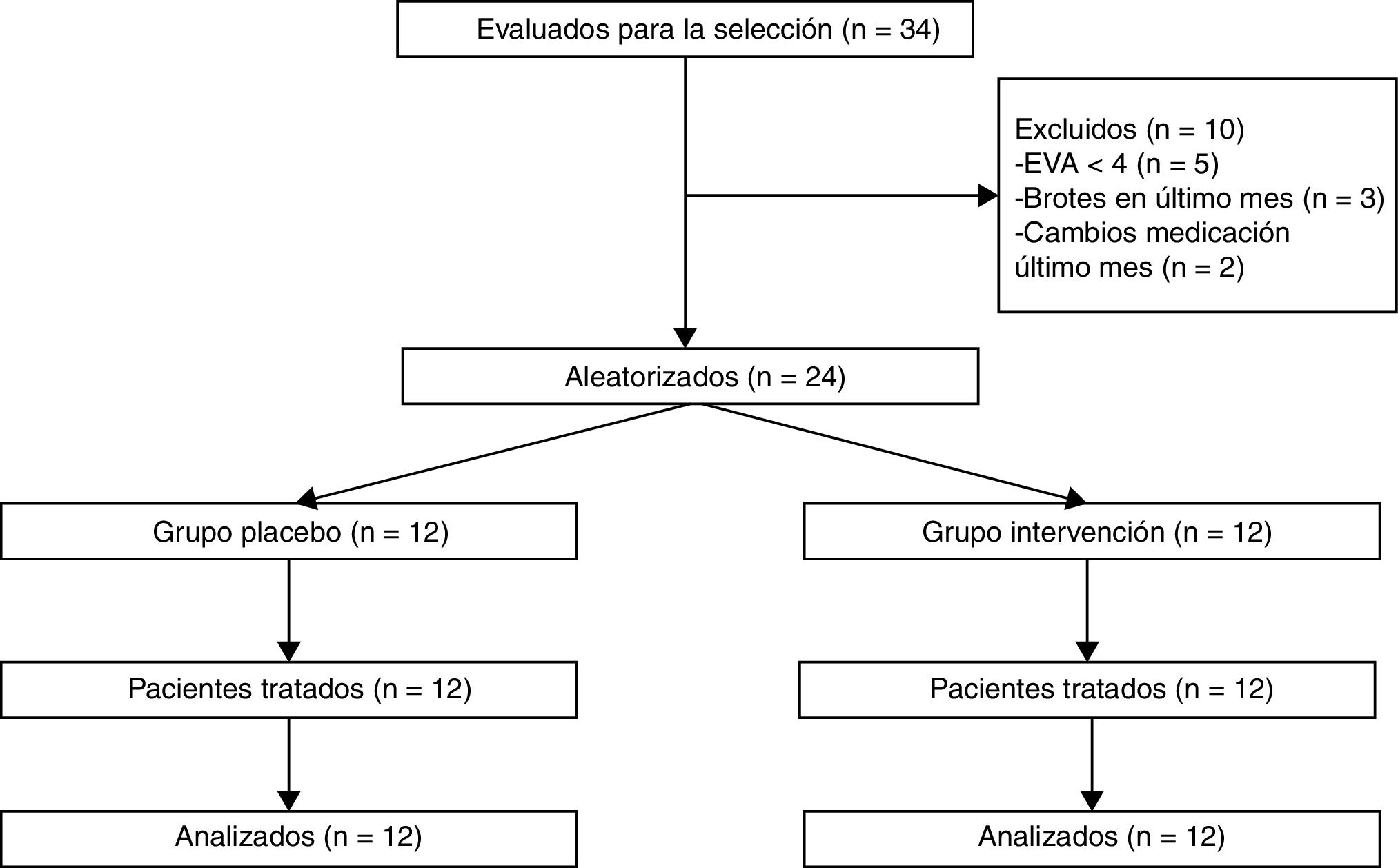
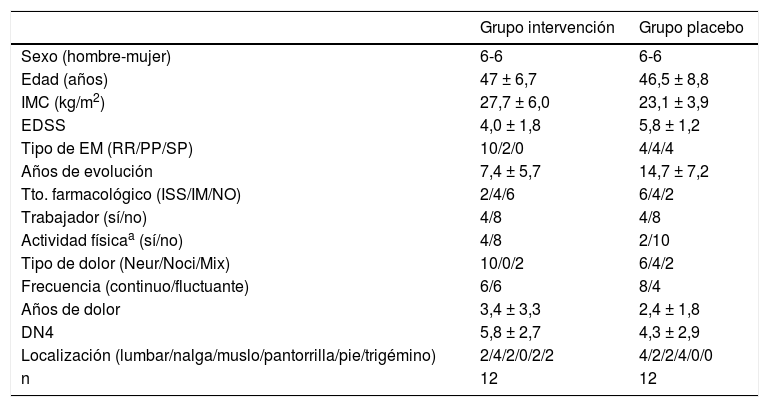
Pacientes y métodosSe realizó un estudio piloto con doble ciego para estudiar el efecto de la terapia SEDM en el dolor de sujetos con EM. Para tal objetivo, se seleccionó una muestra de 34 pacientes entre los atendidos en la Unidad de Neurofisioterapia (localización eliminada para mantener anonimato), de los cuales 24 fueron finalmente seleccionados (tabla 1) atendiendo a los criterios de inclusión y exclusión.
Estadísticos descriptivos de la muestra
| Grupo intervención | Grupo placebo | |
|---|---|---|
| Sexo (hombre-mujer) | 6-6 | 6-6 |
| Edad (años) | 47 ± 6,7 | 46,5 ± 8,8 |
| IMC (kg/m2) | 27,7 ± 6,0 | 23,1 ± 3,9 |
| EDSS | 4,0 ± 1,8 | 5,8 ± 1,2 |
| Tipo de EM (RR/PP/SP) | 10/2/0 | 4/4/4 |
| Años de evolución | 7,4 ± 5,7 | 14,7 ± 7,2 |
| Tto. farmacológico (ISS/IM/NO) | 2/4/6 | 6/4/2 |
| Trabajador (sí/no) | 4/8 | 4/8 |
| Actividad físicaa (sí/no) | 4/8 | 2/10 |
| Tipo de dolor (Neur/Noci/Mix) | 10/0/2 | 6/4/2 |
| Frecuencia (continuo/fluctuante) | 6/6 | 8/4 |
| Años de dolor | 3,4 ± 3,3 | 2,4 ± 1,8 |
| DN4 | 5,8 ± 2,7 | 4,3 ± 2,9 |
| Localización (lumbar/nalga/muslo/pantorrilla/pie/trigémino) | 2/4/2/0/2/2 | 4/2/2/4/0/0 |
| n | 12 | 12 |
DN4: cuestionario sobre dolor neuropático; EDSS: Expanded Disability Status Scale; EM: esclerosis múltiple; IM: inmunomodulador; ISS: inmunosupresor; Mix: mixto; n: número de sujetos; Neur: neuropático; NO: sin tratamiento farmacológico; Noci: nociceptivo; RR: remitente recurrente; SP: secundaria progresiva.
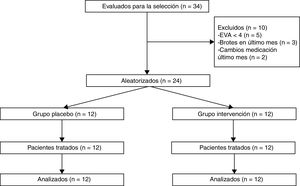
Como criterios de inclusión se determinaron: varón o mujer de 18 a 60 años de edad, diagnosticado de EM de acuerdo con los criterios de McDonald 2005, con una Expanded Disability Status Scale ≤ 7, percepción de dolor (EVA) ≥ 4 y que firmase consentimiento informado sobre su participación en el estudio. Se excluyó a pacientes que estuvieran recibiendo otra intervención fisioterápica para el dolor, que estuvieran o hubieran estado en tratamiento antitumoral durante el último año, que fueran portadores de marcapasos, que hubieran sufrido un brote o que hubiesen cambiado de medicación en los últimos 30 días previos al estudio o durante el mismo y aquellos con comorbilidad que cursen con cuadros de dolor (fig. 1).
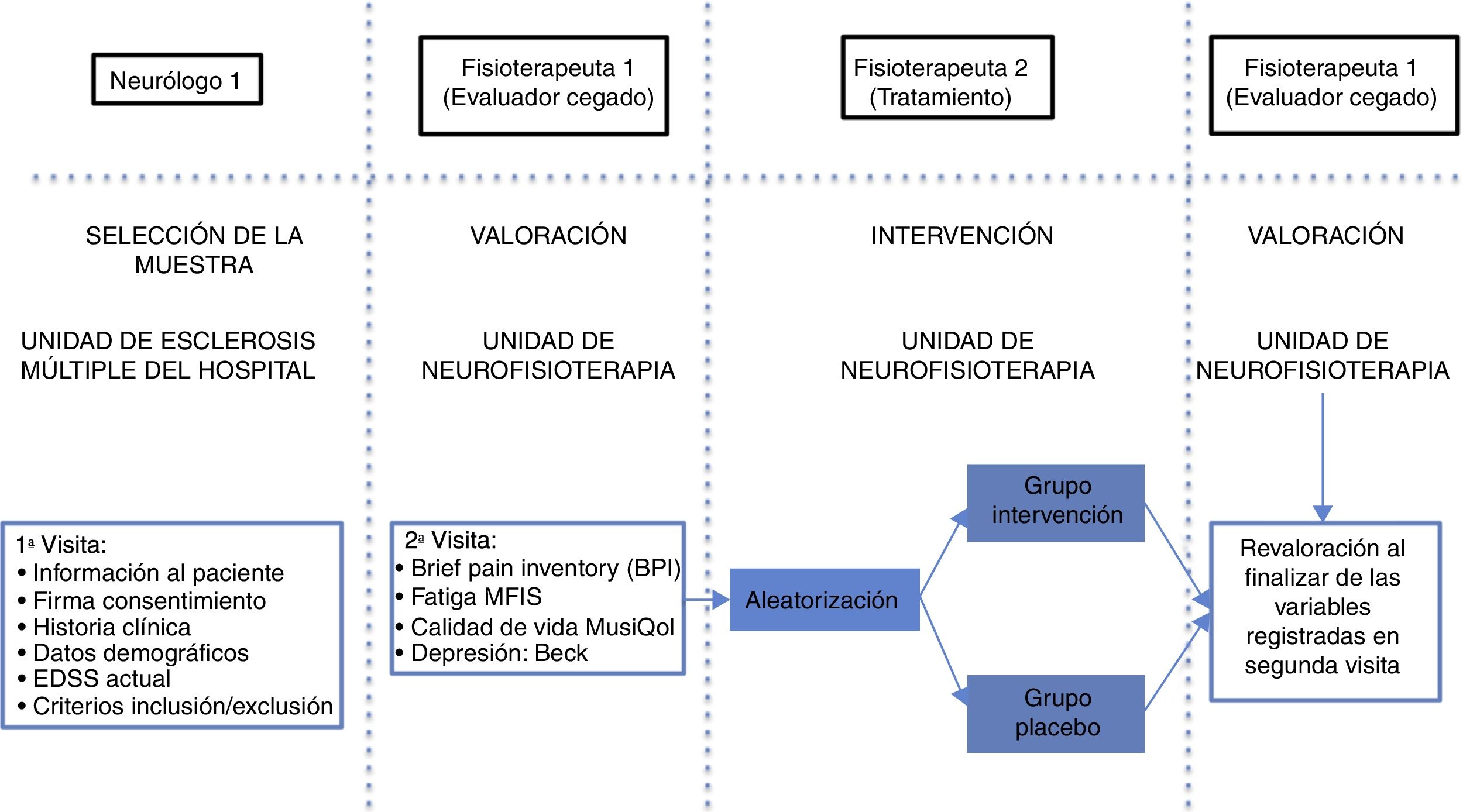
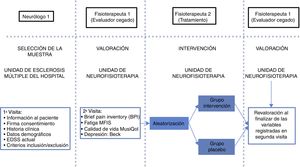
Herramientas e intervención: los pacientes fueron valorados por un fisioterapeuta 1, cegado antes de iniciar la intervención. A continuación, se distribuyeron aleatoriamente con el software Glaxo Wellcome C4-SDP versión 1.1 para Windows en el grupo intervención (tratamiento activo) o grupo placebo (tratamiento placebo).
Para diferenciar la tipología de dolor, se utilizó el cuestionario DN4, que incluye una serie de signos cuya presencia es característica del dolor neuropático26. En cuanto a la variable dolor, se utilizó el cuestionario Brief Pain Inventory (BPI), que consta de diferentes categorías sobre las fluctuaciones del dolor en el día a día (dolor máximo, mínimo y medio), así como el nivel de afectación del dolor en diferentes ámbitos de la vida diaria (relaciones personales, trabajo, descanso, etc.)27. Por otro lado, se escogió la validación al español del cuestionario MusiQoL para valorar la calidad de vida de los pacientes mediante 31 preguntas multidimensionales que suman un máximo total de 100 puntos28. La depresión fue cuantificada mediante la versión validada del Beck Depression Inventory (inventario de depresión de Beck [BDI]) versión ii (BDI-II), que mediante 21 preguntas de 4posibles respuestas indica cómo el paciente se ha sentido en las últimas 2semanas, permitiendo valorar un nivel de depresión mínima, media o severa29. Respecto a la fatiga, se escogió la versión española del cuestionario Modified Fatigue Impact Scale (MFIS), que cuenta con 3subescalas (fatiga física, cognitiva y social) con 4opciones de respuesta cada una de las preguntas que componen la escala30.
En la fase de intervención, el fisioterapeuta 1 entrevistó al paciente y lo examinó minuciosamente para conocer la historia y tipo de dolor (neuropático, nociceptivo o mixto), diferenciándolo según los criterios del cuestionario DN4 y BPI. Además del dolor, se evaluó la fatiga mediante el cuestionario autoadministrado MFIS, calidad de vida mediante MusiQoL y depresión mediante el BDI-II) (fig. 2). Se contó con una hoja de registro por paciente y sesión para registrar cualquier tipo de efecto adverso que pudiera producirse durante la intervención.
En la intervención se utilizó un dispositivo de terapia por SEDM modelo Physicalm® cedido por la empresa Biotronic Advance Develops® (C/ Horno de Abad, 12, 18002, Granada) con una emisión pulsada en rangos de frecuencia de 800-900kHz e intensidad pico de 30V. Fue llevada a cabo por el fisioterapeuta 2, distinto del que hizo la valoración y la selección de la muestra, en una cabina climatizada y separada del resto de la sala de Neurofisioterapia de la Unidad de EM. El tratamiento consistió en la aplicación SEDM durante 15 sesiones (5 días por semana durante 3 semanas) de 20 min de duración. La administración se realiza de forma transcutánea mediante un cabezal plano y redondo de 4cm de diámetro que se aplica sobre la zona de dolor con movimientos longitudinales y transversales, interponiendo 5ml de aceite 100% vegetal de almendras dulces y por tanto dieléctrico31 entre la piel y el cabezal. El tratamiento placebo empleó el mismo procedimiento, a excepción de que el cabezal del equipo, a pesar de encenderse con su característica luz verde, no emitía ningún tipo de señal electromagnética.
Dada la inexistencia de estudios previos con esta terapia, no se puedo realizar un cálculo de tamaño muestral. Los datos de este estudio servirán para establecer futuros tamaños muestrales para otros estudios con base en las diferencias halladas entre variables.
Análisis de los datosSe realizó un análisis de normalidad mediante test de Shapiro-Wilk. Al tratarse de variables cuantitativas y distribuirse los grupos con normalidad, para comparar los resultados entre los valores previos y posteriores de las variables en ambos grupos de tratamiento, se realizó una prueba t para muestras relacionadas. Posteriormente, se realizó un Anova de una vía para comparar la mejora producida entre el grupo de intervención y el grupo placebo. Asimismo, se calcularon los tamaños de efecto para cada tipo de intervención, lo que permitió determinar la relevancia clínica de los efectos del tratamiento. Para ello, se utilizará el criterio «d» de Cohen considerando el valor de 0,2 a 0,49 como tamaño del efecto pequeño, de 0,5 a 0,79 como mediano, y 0,80 o mayor como grande.
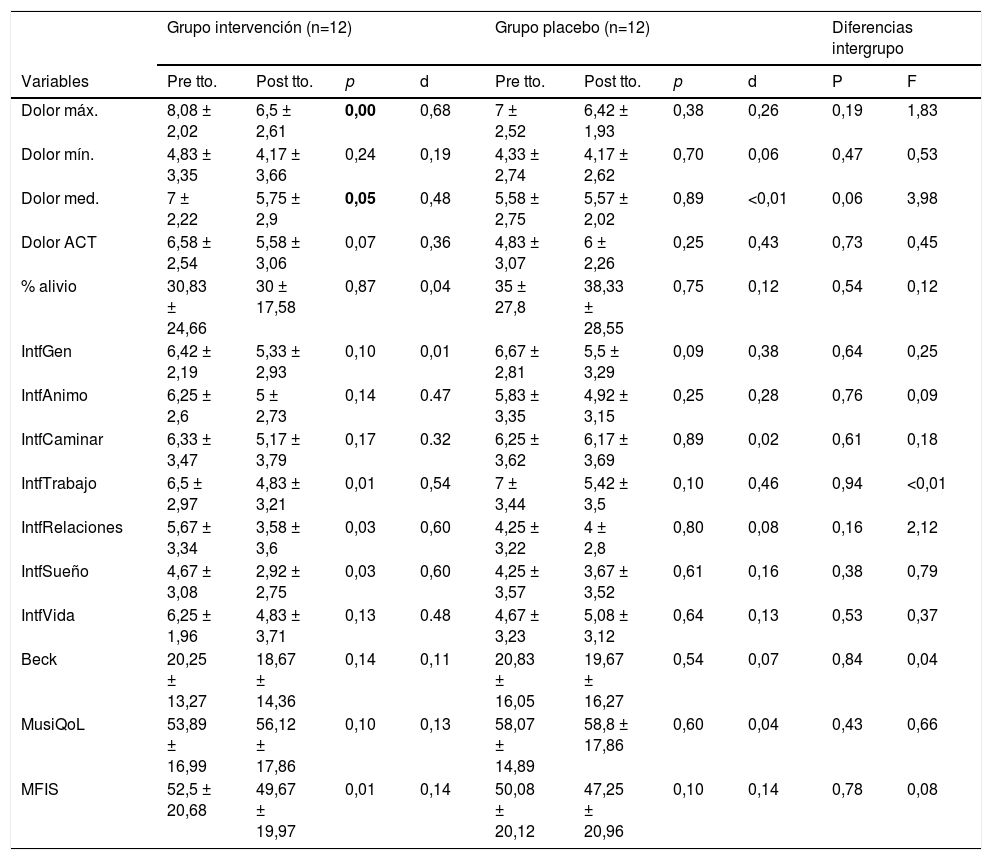
ResultadosSe hallaron diferencias estadísticamente significativas tras el tratamiento en las variables de dolor máximo, dolor medio, interferencia en trabajo, interferencia en relaciones, interferencia en calidad del sueño y en fatiga medida con MFIS en el grupo de intervención (tabla 2). El tratamiento con SEDM mostró un tamaño del efecto medio sobre las variables dolor máximo, dolor medio, interferencia en el trabajo, interferencia en relaciones e interferencia en sueño (tabla 2).
Tamaño del efecto y diferencias entre variables antes y después del tratamiento según grupo
| Grupo intervención (n=12) | Grupo placebo (n=12) | Diferencias intergrupo | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Variables | Pre tto. | Post tto. | p | d | Pre tto. | Post tto. | p | d | P | F |
| Dolor máx. | 8,08 ± 2,02 | 6,5 ± 2,61 | 0,00 | 0,68 | 7 ± 2,52 | 6,42 ± 1,93 | 0,38 | 0,26 | 0,19 | 1,83 |
| Dolor mín. | 4,83 ± 3,35 | 4,17 ± 3,66 | 0,24 | 0,19 | 4,33 ± 2,74 | 4,17 ± 2,62 | 0,70 | 0,06 | 0,47 | 0,53 |
| Dolor med. | 7 ± 2,22 | 5,75 ± 2,9 | 0,05 | 0,48 | 5,58 ± 2,75 | 5,57 ± 2,02 | 0,89 | <0,01 | 0,06 | 3,98 |
| Dolor ACT | 6,58 ± 2,54 | 5,58 ± 3,06 | 0,07 | 0,36 | 4,83 ± 3,07 | 6 ± 2,26 | 0,25 | 0,43 | 0,73 | 0,45 |
| % alivio | 30,83 ± 24,66 | 30 ± 17,58 | 0,87 | 0,04 | 35 ± 27,8 | 38,33 ± 28,55 | 0,75 | 0,12 | 0,54 | 0,12 |
| IntfGen | 6,42 ± 2,19 | 5,33 ± 2,93 | 0,10 | 0,01 | 6,67 ± 2,81 | 5,5 ± 3,29 | 0,09 | 0,38 | 0,64 | 0,25 |
| IntfAnimo | 6,25 ± 2,6 | 5 ± 2,73 | 0,14 | 0.47 | 5,83 ± 3,35 | 4,92 ± 3,15 | 0,25 | 0,28 | 0,76 | 0,09 |
| IntfCaminar | 6,33 ± 3,47 | 5,17 ± 3,79 | 0,17 | 0.32 | 6,25 ± 3,62 | 6,17 ± 3,69 | 0,89 | 0,02 | 0,61 | 0,18 |
| IntfTrabajo | 6,5 ± 2,97 | 4,83 ± 3,21 | 0,01 | 0,54 | 7 ± 3,44 | 5,42 ± 3,5 | 0,10 | 0,46 | 0,94 | <0,01 |
| IntfRelaciones | 5,67 ± 3,34 | 3,58 ± 3,6 | 0,03 | 0,60 | 4,25 ± 3,22 | 4 ± 2,8 | 0,80 | 0,08 | 0,16 | 2,12 |
| IntfSueño | 4,67 ± 3,08 | 2,92 ± 2,75 | 0,03 | 0,60 | 4,25 ± 3,57 | 3,67 ± 3,52 | 0,61 | 0,16 | 0,38 | 0,79 |
| IntfVida | 6,25 ± 1,96 | 4,83 ± 3,71 | 0,13 | 0.48 | 4,67 ± 3,23 | 5,08 ± 3,12 | 0,64 | 0,13 | 0,53 | 0,37 |
| Beck | 20,25 ± 13,27 | 18,67 ± 14,36 | 0,14 | 0,11 | 20,83 ± 16,05 | 19,67 ± 16,27 | 0,54 | 0,07 | 0,84 | 0,04 |
| MusiQoL | 53,89 ± 16,99 | 56,12 ± 17,86 | 0,10 | 0,13 | 58,07 ± 14,89 | 58,8 ± 17,86 | 0,60 | 0,04 | 0,43 | 0,66 |
| MFIS | 52,5 ± 20,68 | 49,67 ± 19,97 | 0,01 | 0,14 | 50,08 ± 20,12 | 47,25 ± 20,96 | 0,10 | 0,14 | 0,78 | 0,08 |
ACT: dolor durante la actividad; Beck: depresión medida con Beck; d: tamaño del efecto, d de Cohen; F: relación entre grupos (Anova); IntfCaminar: interferencia para caminar; IntfGen: interferencia general; IntfRelaciones: interferencia en relaciones; IntfSueño: interferencia en sueño; IntfTrabajo: interferencia en trabajo; IntfVida: interferencia en vida; IntrfAnimo: interferencia en ánimo; máx.: máximo; med.: medio; MFIS: fatiga medida con MFIS mín.: mínimo; MusiQoL: calidad de vida; p: diferencias antes y después de la intervención según tratamiento (prueba T); P: diferencias entre grupos de tratamiento (Anova); Post tto.: después del tratamiento; Pre tto.: antes del tratamiento; % alivio: porcentaje de alivio.
En negrita: resultados con significación estadística de p< 0,05.
Sin embargo, no se hallaron diferencias significativas entre la mejoría producida en el grupo de intervención respecto al grupo placebo (tabla 2).
En cuanto a la tipología de dolor, tampoco se hallaron diferencias estadísticamente significativas entre los distintos subgrupos (nociceptivo, neuropático o mixto) (p < 0,5 en todas las variables).
DiscusiónTeniendo en cuenta el elevado coste invertido en cuidados básicos, mantenimiento de la independencia y calidad de vida del paciente con EM asumido por el sistema sanitario, por el propio sujeto o el entorno familiar, un tratamiento fisioterápico que aborde estos aspectos cobra especial relevancia en estos pacientes. Si a esto unimos una condición frecuente de absentismo o incapacidad laboral, se evidencia la necesidad de investigar en la mejora del abordaje del paciente con EM desde los diferentes ámbitos sanitarios. La implementación de la tecnología en los medios de electroterapia mejora la calidad y la variedad de tratamientos que pueden llevarse a cabo desde la fisioterapia en la intervención del paciente con EM, siendo necesaria la validación de las nuevas técnicas frente a las alternativas farmacológicas6 y no farmacológicas14 antes de incluirlas en guías de tratamiento.
No existen estudios previos sobre la eficacia de la terapia por SEDM en el dolor del paciente con EM. Los estudios que abordan alternativas no farmacológicas se centran en fisioterapia y en educación del paciente para gestionar mejor su energía14. Respecto a la fisioterapia, muestra especial efectividad en el tratamiento del dolor la TENS a baja frecuencia y alta frecuencia14,17, siendo opción recomendada por Sawant et al. para tratar dolor central en EM por sus escasos efectos secundarios17. Los estudios realizados por Al-Smadi et al.16 y Warke et al.15 presentan buena calidad metodológica, sin embargo, en ellos no se realiza cegamiento del terapeuta, lo que podría comprometer parcialmente los resultados. Es por ello que para el presente estudio se ha asegurado el cegamiento de pacientes, terapeutas y evaluadores. También se ha procurado utilizar herramientas de medición más precisas que la escala visual analógica, que aportaran datos de las fluctuaciones del dolor a lo largo del día y su influencia en los distintos aspectos de la vida de los sujetos como permite el cuestionario BPI, lo cual no ha sido tenido en cuenta en otros estudios15,16. En cuanto a las variables secundarias, se han evaluado también los posibles efectos en la fatiga de los sujetos mediante cuestionario MFIS, en depresión con Beck y en calidad de vida con MusiQoL, resultado estos efectos inexistentes o muy leves.
En comparación con el TENS, la terapia por SEDM permite focalizar mejor la acción y aumentar la profundidad de emisión al utilizar mecanismo de transmisión dieléctrico y aplicación monopolar en lugar de conductivo o resistivo y bipolar como los sistemas convencionales de electroterapia25. Este hecho podría justificar los mejores resultados en analgesia de los pacientes con EM obtenidos en este estudio respecto a los revisados por Sawant et al.17 con TENS, pero la ausencia de más estudios con SEDM limita la comparación de resultados. En cuanto a la calidad de vida, no se han obtenido mejoras significativas, al igual que han determinado otros autores mediante TENS15. Tampoco se han hallado diferencias entre antes y después del tratamiento en las variables de fatiga y depresión, hecho que no se ha podido contrastar al no haberse hallado estudios con electroterapia que valoren dichas variables.
A pesar de haberse obtenido mejoras significativas en las variables de dolor en el grupo de intervención mediante el tratamiento con SEDM, no se ha podido demostrar que dichas diferencias sean significativas respecto a las cosechadas por el grupo placebo. Sin embargo, variables como dolor medio han quedado muy cercanas a valores significativos en grupo de intervención respecto a grupo placebo (p = 0,058), por lo que se piensa que un tamaño muestral mayor podría poner de manifiesto valores significativos en algunas variables.
Con base en los datos aportados en este estudio, se debe ser prudente en afirmar la efectividad de la terapia por SEDM en el tratamiento del dolor en EM. La terapia parece efectiva tanto en el tratamiento del dolor máximo como del dolor medio percibido por los pacientes y la mejora en dolor parece influir positivamente en la afectación que la EM produce en los pacientes a nivel de sus relaciones sociales (que parecen mejorar, lo que se podría asociar a reducción de la irritabilidad y mejora funcional) y sobre su descanso y sueño reparador, variables donde el impacto de la terapia alcanza un tamaño del efecto medio. Este hecho cobra especial relevancia teniendo en cuenta que los pacientes con mejor calidad del sueño tienen mejor pronóstico en dolor32, y que otros estudios no han mostrado diferencias significativas con TENS en calidad del sueño15,16. También se producen mejoras en la afectación a nivel laboral, aunque similares a las del tratamiento placebo. Las mejoras en fatiga muestran un tamaño del efecto tan leve que no resultan reseñables, siendo necesario un tamaño muestral mayor para determinar la eficacia de la terapia en esta variable. También se refleja una mejora significativa en la fatiga, pero muy leve y no generalizable con el tamaño muestral utilizado.
No se han hallado, sin embargo, diferencias significativas entre la mejora de los distintos tipos de dolor: neuropático, nociceptivo y mixto (p = 0,71). Esto puede ser debido a que el tamaño muestral no sea lo bastante potente para reflejar diferencias o que la terapia por SEDM actúe sobre puntos en común de los 3tipos de dolor. También se desconoce si cambiando la pauta de aplicación y alargando el tiempo de exposición a la terapia se podrían haber obtenido diferencias significativas entre los distintos tipos de dolor.
Uno de los principales motivos que apoyan el uso de sistemas de electroterapia como el TENS en el manejo del dolor es la ausencia de efectos secundarios respecto al tratamiento farmacológico17, la cual parece extensible a la terapia por SEDM al no haberse registrado durante el presente estudio ninguna incidencia al respecto.
A pesar de los resultados positivos, el bajo tamaño muestral disponible en la unidad en que se realizó este estudio crea la necesidad de aumentar el número de participantes y crear subgrupos de tratamiento más amplios según tipología y localización del dolor. La aparición de resultados estadísticamente significativos, a pesar del pequeño número de participantes, arroja la posibilidad de que estemos ante una eficaz alternativa para evitar una mayor polimedicación en el paciente con EM, requiriéndose más estudios para dilucidar si la tendencia a la significación de algunas variables en la comparación entre grupos se confirma. Por todo ello, este estudio resulta un buen comienzo teniendo en cuenta la inexistencia de estudios previos con SEDM, obligando sus resultados a profundizar en el tema.
Con base en los resultados de este estudio, se puede determinar que la terapia por SEDM mejora el dolor en sujetos con procesos dolorosos asociados a EM, pero no queda demostrado si de manera más efectiva que el placebo y otros tratamientos. No se han mostrado efectos claros sobre la interferencia de la mejora del dolor en la vida diaria, la depresión y la fatiga. Son necesarios más estudios para esclarecer estos hechos y diferenciar la efectividad según tipo de dolor.
Aspectos éticos de la investigaciónEstudio realizado de acuerdo con los principios de la Declaración de Helsinki, desarrollado de acuerdo con el protocolo y en cumplimiento de las normas de buena práctica clínica (BPC), tal como se describe en las normas de la ICH y con visto bueno del Comité Ético del Hospital Virgen de la Macarena de Sevilla.
El presente estudio no comporta ningún riesgo adicional para el paciente más allá de lo contemplado dentro de la práctica clínica habitual. Los pacientes incluidos en el mismo han sido informados previamente de las características del mismo, de las mediciones que se realizan en el desarrollo del mismo, sus propósitos y procedimientos. El investigador respondió a toda duda de los participantes e informó de la voluntariedad de participación. Una vez que el investigador comprobó la correcta comprensión del proceso por parte del paciente, se le facilitó la hoja de consentimiento informado y voluntario al paciente, otorgando este su consentimiento por escrito antes de ser incluido en el programa y autorizando que sus datos sean incluidos en este estudio.
Confidencialidad de los datosEl equipo investigador llevó a cabo el estudio según lo establecido en el protocolo, preservando la confidencialidad de los datos de los pacientes y garantizando la disociación de los mismos, informándose al paciente de ello tal como se establece en la LOPD 15/1999 de 13 de diciembre y en el Real Decreto 1720/2007. Los datos de los pacientes obtenidos durante el estudio se consideran confidenciales y solo fueron utilizados con el propósito de satisfacer los objetivos de investigación.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación, ni ha sido presentado a la reunión anual de la SEN ni otros congresos.
Conflicto de interesesLos autores declaran no tener conflicto de intereses.