Las posibilidades de tratamiento quirúrgico sobre la mama son múltiples y variadas: desde la exéresis de nódulos benignos hasta la cirugía del cáncer hay muchas posibilidades técnicas e indicaciones. El principio fundamental de la cirugía moderna es la correcta indicación de la técnica en cada caso, evitando generalizaciones, adaptándose a cada paciente y a sus circunstancias específicas. Traducir todo esto al campo de la senología es comprender que en todo momento debemos tener en mente la repercusión estética, psicológica y funcional que nuestra actuación tiene sobre la mujer y su seno. Por ello, el primer principio de la cirugía senológica es obtener el mejor resultado estético posible en cada caso, sin sacrificar los objetivos terapéuticos. Hemos dividido las técnicas en cuatro grandes apartados: en la cirugía de los procesos benignos y la cirugía plástica el compromiso estético es obvio. En la ciru-
gía diagnóstica y la de los procesos malignos debe mantenerse el compromiso cosmético, siempre supeditado a obtener el grado de resección suficiente para considerar la cirugía completa. En los últimos tiempos ha sido en estos dos últimos campos donde han aparecido las novedades más importantes.
En la atención primaria habitualmente no se realiza cirugía mamaria, como mucho algún procedimiento menor. Pero es en este nivel de atención donde, por el contacto y confianza del paciente con su médico, aparecen consultas sobre indicación, resultados, consecuencias. Incluso problemas o dudas en el postoperatorio. El médico de atención primaria debe tener acceso a la suficiente información para poderlas resolver con la honestidad y veracidad que caracteriza a este colectivo. A veces puede ser difícil hacer entender a la paciente que no necesariamente la exéresis más amplia se corresponde con la enfermedad más grave o de peor pronóstico: una mastectomía puede estar indicada excepcionalmente por un proceso benigno, mientras que tumores malignos del tamaño adecuado pueden ser tratados conservando el seno. Por eso es importante que en atención primaria se conozcan bien estos conceptos para evitar errores de interpretación que pueden ser transmitidos a la paciente, creándole únicamente confusión y problemas.
Cirugía de los procesos benignos
Como hemos reseñado anteriormente, es en este campo donde más importancia cobra la obtención de un resultado cosmético satisfactorio. La patología mamaria benigna susceptible de tratamiento quirúrgico puede ser dividida en varios grupos: las tumoraciones benignas (principalmente fibroadenoma, hamartoma, tumor phyllodes, tumores de la estroma como el lipoma y tumores cutáneos) y la cirugía de procesos inflamatorios (mastitis, galactoforitis); podría incluirse un tercer grupo de intervenciones correctoras de defectos congénitos o adquiridos, pero eso es tema de otro capítulo.
En la cirugía de los procesos benignos buscaremos siempre las incisiones más estéticas, de preferencia incisiones periareolares, axilares o en el surco submamario, que son las que adecuadamente tratadas y, contando con una cicatrización correcta por parte de la paciente, quedarán más disimuladas. De no ser posible una de ellas, y descartada la posibilidad de acceder a la zona a tratar a distancia utilizando una de las incisiones antes comentadas (con una técnica y experiencia adecuada habitualmente se podrá realizar), se evitarán las incisiones radiales, especialmente en los cuadrantes superointernos o «zona del escote» donde serán más visibles, de todos modos la incisión radial en cuadrantes inferiores puede ser incluso mejor que la arqueada. Una buena práctica es reconstruir el plano glandular si la exéresis ha sido amplia para evitar que queden oquedades o deformaciones del contorno mamario, procediendo a la exéresis de la piel redundante y poniendo cuidado en no desalinear excesivamente el complejo areola-pezón para no crear una asimetría que puede resultar antiestética.
La cirugía exerética de tumoraciones benignas se rige por los principios de intentar no extirpar más que el tejido necesario, evitando lesionar o extraer tejido sano. En algunos casos, como el del phyllodes, la posibilidad de que se trate de una forma maligna y la ausencia de una verdadera cápsula obligan a actuar a distancia, pasando por tejido sano, pese a que la seudocápsula ofrece un teórico plano de clivado muy atractivo. Una hemostasia adecuada, con drenajes si la hemostasia es dudosa o el despegamiento amplio (preferentemente con sistemas de aspiración por vacío en circuito cerrado), así como un vendaje modelante y compresivo son obligatorios. El postoperatorio suele ser poco doloroso; administrar paracetamol es más que suficiente en caso de necesitar analgesia; el metamizol (Nolotil®) es la alternativa más eficiente si falla el paracetamol.
Los procesos papilares precisan una cirugía delicada y precisa, identificando el conducto enfermo e intentando resecar la totalidad del lóbulo mamario asociado a él. Muchas veces puede identificarse el plano anatómico adecuado si se sigue una técnica cuidadosa. Es importante, ya que en algunos casos existen lesiones papilares malignas que pueden recidivar si queda parte del lóbulo sin extirpar: la clásica cirugía del papiloma con exéresis retroareolar demuestra así sus limitaciones y peligros. Además, estéticamente, la resección de un lóbulo pasa desapercibida, mientras que la cuña retroareolar suele dejar deformidades cicatrizales visibles.
La cirugía de los procesos inflamatorios se reserva únicamente a aquellos abscesos resistentes al tratamiento médico y que la punción evacuadora ecoguiada no es capaz de resolver.
En estos casos se procederá a desbridar el absceso, dejando un drenaje pasivo (tipo Penrose) en la zona más declive, realizando una segunda incisión si procede para asegurar un drenaje adecuado. Todo ello bajo cobertura antibiótica y siguiendo los principios generales de la cirugía «sucia» o contaminada. Es necesario un control de la herida, realizando curas y retirando progresivamente el drenaje para que la cavidad se colapse desde el interior, sin dejar espacios muertos que causarían recidivas.
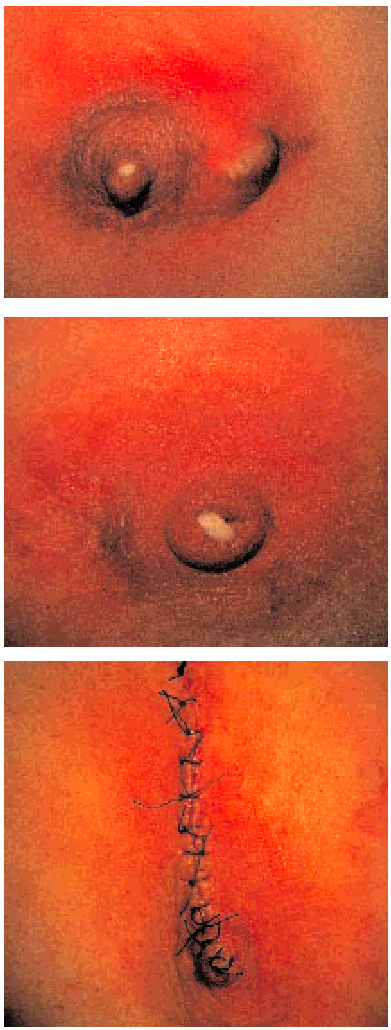
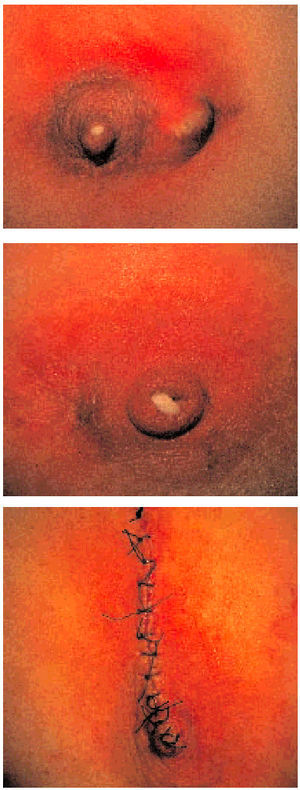
Un caso aparte merece la fistulización periareolar recidivante, que precisa una técnica totalmente diferente para solucionar el proceso (capítulo de la paciente sintomática). El tratamiento aquí consiste en la exéresis en bloque, cuando el proceso está «enfriado», de la fístula, el trayecto fistuloso y la cavidad inflamatoria así como el galactóforo enfermo, incluyendo su salida al pezón y la zona invaginada que en él crea, todo en bloque, para después suturar y evertir el pezón restante (fig. 1). Usar cualquier otra técnica para solucionar esta patología es incurrir en riesgo de mala praxis, pues no sólo no solucionaremos el problema, sino que al crear tejido cicatrizal dificultaremos la cirugía curativa definitiva, pues deberá hacerse una exéresis más amplia para eliminar el exceso de tejido fibrótico cicatrizal, que además es de menor calidad.
Fig. 1. Fistulización periareolar recidivante, tres fases del proceso: a) secreción por el pezón y absceso periareolar. b) secreción por el pezón y la fístula periareolar. c) aspecto tras la cirugía curativa, con exéresis completa de la fístula, su trayecto y el absceso así como eversión del pezón y exéresis del ducto afectado.
Cirugía diagnóstica
Por cirugía diagnóstica entendemos cualquier técnica destinada a obtener tejido mamario proviniente de una zona problema (que plantea dudas diagnósticas). Esta zona puede ser palpable o bien visible por alguno de los métodos de diagnóstico por la imagen. Pueden darse dos supuestos: obtención de la totalidad de la zona problema (biopsia escisional) o de un fragmento o fragmentos de ella que suponemos representativos de la totalidad. En este campo es donde más han incidido los avances técnicos en los últimos años: en primer lugar, por la detección de lesiones no palpables por mamografía y más tarde por ecografía; de forma más reciente son los sistemas de obtención de muestras tisulares guiados por imagen que percutáneamen te son capaces en algunos casos de eliminar totalmente la lesión.
Esta cirugía debe ser de preferencia ambulatoria y con anestesia local, aunque en ocasiones precisará de anestesia profunda y una corta estancia.
La cirugía diagnóstica clásica se basaba en la biopsia incisional o escisional de una tumoración palpable dudosa o sospechosa. Al evolucionar los métodos de diagnóstico por la imagen y aparecer lesiones sospechosas no palpables, se desarrollaron diferentes métodos para lograr su localización intraquirúrgica, siendo el más extendido hoy en día el marcado con aguja o con «arpón» (agujas especiales con un sistema de fijación en la punta o cerca de ella que impide que se mueva del lugar donde se enclavó, evitando los problemas de las agujas normales, que se mueven con facilidad, perdiendo la referencia de la lesión que buscamos), aunque existen otros métodos como marcar la piel suprayacente a la zona problema o bien inyectar algún colorante o incluso polvo de carbono dentro o cerca de la lesión para facilitar su localización.
Aparentemente, puede parecer sencilla, pero la cirugía a cielo abierto con marcaje es una de las intervenciones más difíciles que existen en patología mamaria: la ausencia de referencias anatómicas, el hecho de guiarse «a ojo» por las imágenes mamográficas o ecográficas y la fragilidad de algunos sistemas de marcaje, que con facilidad se desprenden, separándose de la zona problema hacen de esta teórica «cirugía menor» un reto en el que el cirujano-senólogo debe demostrar su habilidad y su capacidad de improvisación. Siempre que se realiza el marcado, que puede ser ecográfico o mamográfico se comprobará la pieza quirúrgica con la misma técnica de imagen diagnóstica para obtener la certeza de que la imagen problema se encuentra en el interior del espécimen. También nos será útil para comprobar si los márgenes de resección son amplios o demasiado justos y para observar si hemos erradicado toda la lesión o únicamente una parte. Por supuesto, es vital una correcta orientación de la pieza quirúrgica en el quirófano para que tanto el radiólogo como el patólogo puedan darnos información adecuada de dónde procede ampliar la exéresis, si se precisa, ahorrando de este modo extirpaciones generosas innecesarias.
Se preferirá un estudio histológico diferido, salvando casos excepcionales, por la seguridad diagnóstica que ofrece y para poder discutir con la paciente las posibilidades terapéuticas que se presenten ante un determinado proceso.
Las novedades más espectaculares se encuentran en los actuales sistemas de guiado por ecografía y por mamografía, que unidos a sistemas cada vez más sofisticados de obtención de muestras tisulares pueden llegar a permitir la total exéresis percutánea de una imagen problema mediante una nueva cirugía «a distancia» teledirigida o robótica.
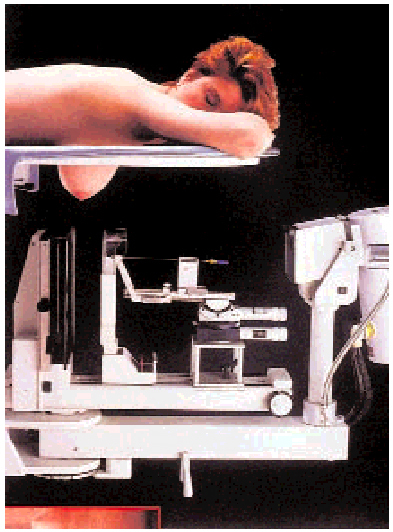
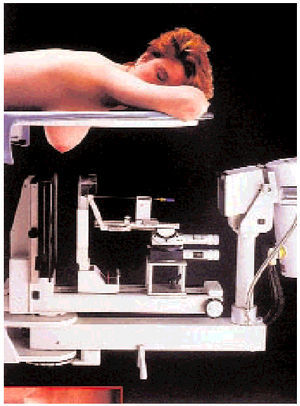
La primera revolución en este campo fue la aparición de los sistema de guía estereotáxica que, utilizando la mamografía como base, permiten dirigir la punta de una aguja, con precisión de 0,5 mm a la imagen deseada. Los primeros equipos se acoplaban sobre un mamógrafo convencional, situándose a la paciente sentada, con el seno a estudiar colocado en posición de mamografía convencional; el sistema de imagen es el mismo mamógrafo y el sistema de guía se le acopla. En la actualidad, existen aparatos o «mesas» dedicados únicamente a este propósito en los que la paciente se sitúa en decúbito prono con la mama a estudiar pendiendo por una ventana, bajo la cual se encuentra el sistema de adquisición de imágenes y el sistema de guía. Por su elevado coste, estos últimos aparatos son todavía poco habituales en nuestro medio (fig. 2). Los sistemas de adquisición de imagen digital han abreviado el proceso, permitiendo acortar el tiempo de la exploración al eliminarse el tiempo invertido en el revelado de las placas de mamografía convencional. Todos los sistemas de estereotaxia, sean mesas especialmente dedicadas o sistemas que se acoplan al mamógrafo, se basan en el mismo sistema de funcionamiento: una vez fijada la «ventana» del aparato sobre la zona del seno donde creemos que se localiza la imagen a estudiar se realizan dos proyecciones a +15° y 15°. Un vez obtenida la imagen, el radiólogo señala la zona problema en ambas, seleccionando el punto al que dirigir la punta de la aguja. Una vez hecho esto, se introducen los datos en un calculador que nos da las coordenadas en un eje tridimensional x, y, z. Dependiendo del aparato, el mismo situará la guía de la aguja en la posición adecuada o bien nosotros lo haremos manualmente hasta poner a 0 las coordenadas sobre la zona a estudiar. La guía y el calculador están calibrados para diferentes grosores, longitudes y tipos de sistema para obtener muestras tisulares. Inicialmente, se hacía punción con aguja fina obteniendo material para el estudio citológico: pronto se comprobó que la técnica así realizada tenía un bajo rendimiento. Por ello, se acoplaron sistemas de microbiopsia tipo tru-cut, prefiriéndose los de disparo con avance mecanizado por la mayor calidad de las muestras obtenidas. Inicialmente, se utilizaban agujas de 18 G; hoy en día, se utilizan de 14 G (biopsia con aguja gruesa; BAG); se considera que deben obtenerse al menos 3 e idealmente 5 o más microfragmentos para que la técnica tenga una sensibilidad y especificidad adecuadas; su inconveniente es que, aunque la muestra suele ser representativa, no obtenemos la totalidad del tejido, por lo que podemos diagnosticar un carcinoma in situ y después encontrar un carcinoma infiltrante al realizar el tratamiento definitivo. Aunque utilizada con buen criterio, es una técnica muy útil que evita biopsias quirúrgicas innecesarias e imágenes de baja sospecha, o confirma el diagnóstico en las de alta sospecha. Más recientemente, han aparecido los sistemas de biopsia de gran calibre (ABBI®) y los de biopsia asistida por vacío (Mammotome®). El sistema de gran calibre puede llegar a obtener cilindros de hasta 2 cm de diámetro, precisa anestesia local y necesita una incisión que debe ser suturada. La ventaja radica en que en casos seleccionados el sistema permite extirpar la imagen problema completa para así estudiarla adecuadamente, y en ocasiones puede llegar a considerarse que la exéresis local puede ser suficiente con esto. Este sistema tiene el inconveniente de dejar, en ocasiones, una depresión poco estética en la zona biopsiada. El sistema asistido por vacío es parecido a una aguja de tru-cut, pero un sistema de presión negativa es el que introduce el tejido que queda al lado de la «ventana» situada en el extremo de la aguja en su interior; una vez ahí, es cortado por una cuchilla y aspirado hacia el exterior, hasta una ventana donde se recoge para ser procesado. Con este sistema vamos numerando las piezas que se obtienen. Permite una enorme plasticidad, al poderse rotar la aguja y orientar la ventana hacia el punto que convenga y, casi a tiempo real, con la imagen digital, dirigir la exéresis completa de la imagen. Puede llegar a «vaciarse» completamente la imagen problema, obteniendo como media entre 12 y 16 muestras; además, la aguja de calibre 11 (hay otra del 14 G) permite la colocación de clips metálicos una vez concluida la biopsia, lo que nos permitirá completar el tratamiento, de ser preciso, en una segunda fase, dirigidos por ellos, pues el sistema suele «comerse» las imágenes completamente. El porcentaje de complicaciones es prácticamente el mismo con BAG que con Mammotome. Sus indicaciones varían según el tipo de imagen, su tamaño y la disponibilidad de estos medios. Cualquiera de ellos representa un sistema diagnóstico muy útil que puede llegar a permitir en el futuro, y hoy día ya lo permite en casos seleccionados, tratar localmente un cáncer de mama, de manera ambulatoria y prácticamente sin deformación de la mama. Lo que sí permiten en la actualidad es ahorrar biopsias convencionales excesivas, cicatrices y procedimientos innecesarios, con el consiguiente ahorro económico y personal tanto para el médico como para la paciente. Además, nos van a permitir llegar a quirófano con un diagnóstico histológico de alta fiabilidad, con lo que se puede planificar perfectamente el tratamiento, discutiendo serenamente las diferentes opciones con la paciente.
Fig. 2. Mesa para biopsia mínimamente invasiva de la mama. Obsérvese la posición de la paciente y su seno y el sistema de guía para punción.
Es posible que en un futuro no muy lejano algunos cánceres de mama de pequeño tamaño puedan ser tratados con cirugía mínimamente invasiva robotizada (cirujano + radiólogo + patólogo) y biopsia de ganglio centinela (v. siguiente apartado) (cirujano + médico nuclear + radiólogo + patólogo). Todo ello en un único acto ambulatorio. Quizás se trate de lo que el profesor Umberto Veronessi a veces llama «fantamedicina», pero en este caso creemos que, él precisamente, está convencido de que puede ser una realidad en pocos años si los estudios en curso continúan demostrando su utilidad.
Cirugía oncológica
La cirugía del cáncer de mama se encuentra en constante evolución desde que Halstead y Meyer publicaron sus primeros trabajos estableciendo las bases de la cirugía oncológica clásica o compartimental. Estos autores considerando al cáncer una enfermedad exclusivamente local que con el tiempo se podía generalizar, postularon que la exéresis de todo el compartimiento anatómico donde asentaba la enfermedad garantizaría la máxima durabilidad: nació la mastectomía radical clásica, con exéresis de todo el tejido mamario y la piel suprayacente, además de todos los ganglios axilares (los tres niveles de Berg) y de los dos músculos pectorales, que incluyen también el grupo ganglionar interpectoral o de Rotter. Durante un tiempo, las ideas fluyeron en este sentido, intentándose procedimientos cada vez más radicales para aumentar la supervivencia de las pacientes, que no aumentaba excesivamente, pensando que a más resección obtendrían mayor curación. El máximo desarrollo de esta idea fue la intervención de Prudente, que incluía la extirpación del brazo homolateral con desarticulación escapulohumeral y vaciamiento de la cadena ganglionar de la mamaria interna. Ya en su momento se alzaron voces en contra de la «suprarradicalidad» y el péndulo cambió de sentido, adquiriéndose una orientación que persiste hoy en día. Las ideas modernas se inician al considerar al cáncer una enfermedad sistémica, con una fase local que puede ser tratada sin excesiva agresividad sin menoscabar la supervivencia. Las bases del tratamiento conservador se sentaron en Europa: Amalric y Spitalier en Francia y Veronessi y Salvadori en Italia causaron incredulidad e indignación cuando se atrevieron a postular que en tumores de pequeño tamaño la cuadrantectomía o tumorectomía con vaciamiento axilar podían ser un tratamiento tan efectivo como la mastectomía. Sus trabajos demostrando la veracidad de la hipótesis y el trabajo colaborativo americano dirigido por Fischer acabaron por sentar las bases del tratamiento conservador de la mama. Pronto se comprobó que, pese a que la supervivencia era la misma, existía un número mucho mayor de recaídas locales en las mujeres que conservaban el seno frente a las mastectomizadas. La adición de radioterapia al tratamiento conservador demostró un control local mejor y una tasa de recidivas aceptable.
Técnicas actuales
Hoy en día, el tratamiento conservador del cáncer de mama está perfectamente establecido y protocolizado. Si la relación mama/tumor es favorable (es decir, si al resecar el tumor con un margen de seguridad aceptable queda un seno estéticamente correcto), si no es un cáncer localmente avanzado, con ulceración o afección cutánea ni inflamatorio, si el seno restante puede ser adecuadamente controlado, si no existe contraindicación a la radioterapia y si ésta se puede hacer, es posible conservar el seno. Evidentemente, las mujeres acogieron de forma muy favorable el tratamiento no mutilante de su enfermedad. No contentos con ello, hemos seguido buscando maneras de tratar más cánceres de mama sin alterar la silueta femenina con la supresión de un seno, que suele ser mal tolerada por la mujer en muchos aspectos. Un primer paso fue la quimioterapia de primaria o neoadyuvante: si con ella se reduce el tumor a un tamaño aceptable para poder conservar la mama, se realiza el tratamiento conservador. Aún hay voces que se alzan pidiendo cautela con este enfoque, pero lo que ha quedado claramente demostrado es que existe una evidencia aceptable de que la única utilidad de la neoadyuvancia es precisamente aumentar la tasa de tratamientos conservadores, pues la supervivencia no parece variar significativamente.
Cuando se realiza un vaciamiento axilar convencional, éste debe ser completo, es decir, debe incluir los tres niveles de Berg y la exploración y la exéresis si se palpan ganglios del grupo interpectoral o de Rotter. El vaciamiento axilar correctamente realizado tiene una morbilidad mucho menor de lo que se dice, pues hoy día, con el abandono de la radioterapia axilar, los grandes linfedemas elefantiásicos son cosa del pasado. Por tanto, como el efecto sobre la circulación linfática es el mismo, se extirpe únicamente el primer nivel o el primero y segundo o los tres, debe siempre realizarse un vaciamiento de al menos los dos primeros niveles, aunque lo aconsejable es vaciar los tres en todas las ocasiones salvo excepciones justificadas.
Otras ideas recientes para ofrecer la máxima curación con la mínima mutilación son:
La reconstrucción inmediata, en estrecha colaboración con el cirujano plástico. Tiene sus detractores, que aducen una mayor tasa de complicaciones y el hecho de que, al no haberse visto sin seno, la mujer acepta peor el seno reconstruido, que lógicamente no es como el original. Existen diversas opciones técnicas que sería prolijo describir aquí.
La mastectomía conservadora de piel. Asociada a una reconstrucción inmediata se conserva la máxima cantidad de piel sana para reconstruir el seno sin necesidad de expansión tisular.
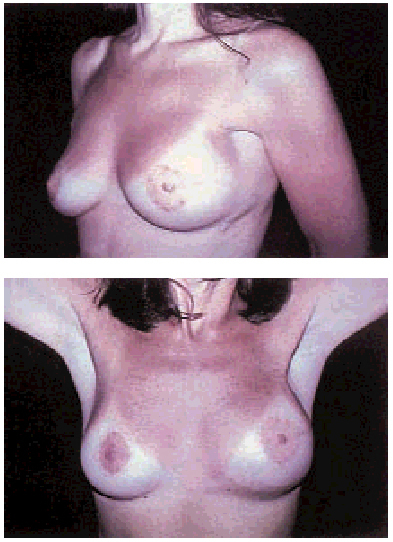
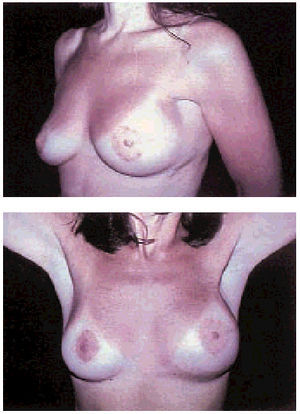
Técnicas «oncoplásticas». Englobando a las dos anteriores, se basan en las cirugías para la reducción y elevación del seno, realizando conservaciones de mama, con amplias tumorectomías y corrección estética del seno contralateral para obtener una buena simetría. Lógicamente, se asocian a la radioterapia posterior. También aquí se engloban conceptos quirúrgicos destinados a obtener el mejor resultado estético de un tratamiento conservador, remodelando la mama restante una vez realizada la tumorectomía (fig. 3).
Fig. 3. Cirugía oncoplástica. Dos visiones postoperatorias: el seno izquierdo (el de mayor volumen) es el operado; mastectomía ahorradora de piel con vaciamiento de los 3 niveles de Berg.
No sólo se tratan quirúrgicamente los tumores infiltrantes, también los tumores in situ son tributarios de cirugía. El carcinoma lobulillar in situ hoy sabemos que, además de un hallazgo habitualmente casual, sólo representa un marcador de aumento de riesgo de cáncer de mama en ambos senos. Por ello, únicamente precisa una escisión local con márgenes libres de enfermedad a ser posible.
Los carcinomas ductales in situ (CDIS) son aún motivo de polémica, pues los de alto grado, el clásico tipo «comedo», tienen una elevada tasa de recidivas, mientras que los tipos más diferenciados son poco agresivos localmente. Ello ha llevado a diferentes métodos e intentos de clasificación y tabulación para determinar qué tratamiento es el más adecuado en cada momento. El índice más utilizado actualmente el de Van Nuys, propuesto por Silverstein que, basándose en el grado hist ológico, el tamaño y la amplitud del margen de resección, divide a los CDIS en tres grupos para ser tratados de forma diferente: tumorectomía amplia, tumorectomía amplia y radioterapia o mastectomía simple. Conocer y manejar estos datos es importante en el tratamiento de esta patología, pero no debemos olvidar que Silverstein basa su clasificación en sus propios datos, por lo que si en una unidad de patología mamaria no se utiliza este índice, porque utilizan uno propio o una adaptación basada en los datos referidos a su población y experiencia, no hay que considerar en absoluto que se esté actuando de una manera indebida, sino todo lo contrario. Por ello, es importante conocer que una patología tratada adecuadamente tiene una supervivencia cercana al 100%, lo que puede ser motivo de tratamientos variados para llegar a obtener estas tasas de curación.
Pero no todas las pacientes son portadoras de tumores pequeños y poco agresivos. Cuando se nos presenta una mujer con una enfermedad localmente avanzada, la cirugía, combinada con otros tratamientos, tiene también su lugar, pensando más en el control local del proceso y la paliación de síntomas desagradables como la ulceración, la supuración, etc., que en la curación. En estos casos, el concurso del cirujano plástico es fundamental para poder cubrir con injertos grandes defectos cutáneos y de sustancia tras amplias resecciones en casos avanzados.
Un grupo de pacientes en el que parece que se enfoque la cirugía y el tratamiento oncológico de un modo diferente son las mujeres de edad avanzada, en las que su estado de salud a veces muy delicado o una esperanza de vida reducida hacen pensar en opciones light o menos agresivas que las anteriormente expuestas. El planteamiento está bien, siempre y cuando se valore correctamente la situación y se pueda ofrecer un control local y sistémico de la enfermedad que no comprometa la calidad de vida de la paciente. Por ello, en tratamientos quirúrgicos localizados citorreductores o para evitar la ulceración, el compromiso vascular o la irradiación de una parrilla costal débil o de un pulmón ya patológico están plenamente justificados.
Complicaciones
Las complicaciones más frecuentes de la cirugía oncológica mamaria se relacionan con la linfadenectomía.
El seroma de la herida axilar debe vaciarse bajo condiciones estériles tantas veces como sea necesario hasta que se resuelva, cosa que no se suele prolongar en los casos rebeldes más allá de la cuarta semana. En ocasiones la inmovilización del brazo y la compresión local ayudan a resolverlo. Una buena técnica quirúrgica, acompañada de un vendaje cuidadoso, la movilización precoz del hombro y la inmovilización relativa al alta suelen ser útiles. Hay clínicos que envían a las pacientes con los drenajes aspirativos a su domicilio, para controlarlos ambulatoriamente, nosotros nunca precisamos de ello. La infección del seroma es un hecho excepcional pero potencialmente grave que debe ser tratada con prontitud y agresividad.
La anestesia-parestesia de los nervios intercostobraquiales origina disestesias a veces molestas y que suelen mejorar lentamente durante los primeros meses en la cara interna del brazo y la axila. Habitualmente, es inevitable seccionar alguna de sus ramas al realizar la linfadenectomía, aunque en ocasiones su localización anatómica permite conservarlos sin comprometer la radicalidad del vaciado axilar.
Es importante que la paciente a la que se le ha vaciado la axila guarde una serie de precauciones en ese brazo destinadas a evitar heridas y traumatismos que pudiesen originar una linfangitis, además de una serie de ejercicios y masajes para prevenir el linfedema. La venoclisis está, en principio, reservada para las ocasiones en que no sea posible otra vía. Especial cuidado se debe tener con las pequeñas heridas, como las originadas en la manicura, al tratar con animales como los gatos, etc. Estas heridas deben ser cuidadosamente desinfectadas.
Las ideas del tratamiento conservador de la mama se han traspasado a la axila en los últimos tiempos, apareciendo el concepto de cirugía axilar conservadora o mínimamente invasiva. La idea de evitar los riesgos y complicaciones de la linfadenectomía en las pacientes con tumores de pequeño tamaño es atractiva y no es nueva. Pero el renunciar a la importante información pronóstica, y por tanto de orientación terapéutica, que proporciona el estado ganglionar no parecía técnicamente aceptable. Tras años de discusión, la reciente introducción de la biopsia del ganglio centinela promete por fin poder conservar la axila en las mujeres sin afección ganglionar, sin renunciar a la información pronóstica del estado ganglionar.
Ganglio centinela
Probablemente, entre la cirugía oncológica y la puramente diagnóstica se encuentra una técnica que proviene del tratamiento del melanoma y que es la actual vedette de los congresos de senología. La biopsia del ganglio centinela se encuentra en boca de todo el mundo y corre el peligro de ponerse de «moda». En estos momentos, y con la evidencia científica acumulada, su uso se limita a los protocolos clínicos de estudio, hasta que hayan pasado los suficientes años de seguimiento como para valorar su utilidad y seguridad como opción quirúrgica estándar. La biopsia del ganglio centinela se basa en los estudios sobre la circulación linfática que se pusieron en marcha para solucionar el problema del melanoma. A menos que se encuentre en una zona anatómicamente muy clara en cuanto a drenaje linfático, el melanoma presenta un problema, por ejemplo un melanoma toracoabdominal puede drenar a derecha y/o izquierda y a la ingle o a la axila...¿debemos realizar un cuádruple vaciamiento axilar para tratarlo? Utilizando primero colorantes vitales y después radiocoloides inyectados en la piel suprayacentre al tumor o en la periferia del mismo, se estudiaba a qué zona drenaba la linfa del tumor y sólo se vaciaba esa región ganglionar. Había nacido la técnica de biopsia centinela, que Morton introdujo para el tratamiento del melanoma en 1992. El perfeccionamiento de sondas gamma de pequeño tamaño que se pueden utilizar con facilidad en el quirófano como guía ha hecho de esta técnica una realidad, al poder guiar al cirujano hasta la zona elegida. La teoría del ganglio centinela cobra cuerpo al comprobar que siempre existe un primer ganglio al que llega el radiotrazador y que constituye la primera estación del drenaje linfático. Ampliamente validado para el melanoma, donde es ya terapia de estadificación sistemática, y si el centinela es negativo no se realiza linfadenectomía, se pensó en su posible utilidad en cáncer de mama. Tras los estudios pioneros de Giuliani et al la técnica se puso a punto. Tanto Giuliani como Veronessi y otros autores han demostrado con sus trabajos que, localizando el ganglio centinela en tumores de entre 2 y 3 cm de diámetro y vaciando la axila completamente después, la concordancia entre el estado del centinela y el del resto de la axila es del 97%, aproximadamente. Dada la baja incidencia de axila positiva en tumores de menos de 2 cm, existen varios protocolos de estudio que intentan verificar qué ocurre si únicamente se vacían las axilas con centinela positivo. Una aportación importante del ganglio centinela ha sido la introducción de técnicas de estudio histológico del ganglio mucho más exhaustivas, con hasta 40 o 60 secciones del centinela, frente a una o dos habituales. El permitir al patólogo centrarse en un solo ganglio ha aumentado notablemente la identificación de enfermedad neoplásica ganglionar. Esto ha introducido un nuevo problema, que es el significado
de las micrometástasis ganglionares y cómo debe procederse con ellas. Todo ello está siendo sometido a estudio en estos momentos. La biopsia del ganglio centinela es una técnica prometedora que probablemente consiga demostrar con el tiempo que podemos evitar la linfadenectomía axilar en algunas pacientes con cáncer de mama con la reducción de morbilidad que ello supone sin menoscabar su esperanza de vida ni el intervalo libre de enfermedad; pero aún no se ha demostrado, por lo que se trata de una técnica aplicable sólo dentro de protocolos controlados.
Cirugía plástica y reconstructora
Como en este monográfico ya existe un capítulo dedicado exclusivamente al tema, únicamente recalcaremos que en estos momentos de confusión para los pacientes, por la proliferación de centros y supuestos profesionales que ofrecen todo tipo de servicios, incluso con financiación, como si de comprar un coche o una nevera se tratara, más que incidir en técnicas e indicaciones debemos dejar claro un punto esencial: cuando una mujer se decide a realizar una cirugía de este tipo sobre su seno lo primero que debe evaluarse es su perfil psicológico, su capacidad para comprender el alcance de lo que se propone y si realmente el problema que tiene se soluciona con cirugía. Únicamente los auténticos cirujanos plásticos, con una visión no comercial sino médica y humanística de la cirugía, son capaces de acercarse a la mujer y aconsejarle qué necesita, incluso disuadiéndola de su idea primaria, desaconsejando la cirugía y proponiendo otras soluciones, incluso consultar con otros profesionales de la salud. Además, el profesional auténtico se cercionará antes de intervenir de que no exista problema alguno que contraindique la intervención, y eso incluye un estudio preoperatorio de la mama, al menos con mamografía e, idealmente, con la evaluación del seno por un senólogo, incluyendo las exploraciones que éste crea convenientes. Es muy importante en este campo de la medicina, como en muchos otros, luchar por la calidad (y aquí la lucha se inicia con un profesional adecuadamente cualificado y especializado). Pero no sólo se trata de luchar contra el intrusismo profesional, sino de aumentar y homogeneizar la calidad del especialista. Por ello, debemos aconsejar a las pacientes mucha precaución y que desconfíen de quien trivialice esta cirugía dando la impresión de una excesiva facilidad y no incida en las posibles complicaciones ni problemas que puedan surgir. En fin, el buen médico aconsejará mesura a su paciente, y si cree que realmente para ella lo mejor es operarse, la remitirá hacia otro buen médico que trate no como un objetivo financiero sino como una persona que necesita ayuda, una paciente.