Evaluar la persistencia terapéutica, el coste sanitario y las reacciones adversas en pacientes tratados con oxibutinina y mirabegrón para el tratamiento de la vejiga hiperactiva en condiciones de práctica médica habitual.
Pacientes y métodosSe diseñó un estudio observacional, multicéntrico, retrospectivo, realizado a partir de registros médicos de pacientes pertenecientes a 3 áreas geográficas distintas (Barcelona, Girona, Asturias). Se analizaron los 2 grupos de estudio (oxibutinina y mirabegrón). El seguimiento se realizó durante un año. La persistencia se definió como el tiempo (meses) sin abandono del tratamiento inicial o sin cambio a otra medicación al menos 60 días después de la prescripción inicial. Principales medidas: comorbilidad, uso de recursos sanitarios y reacciones adversas. Programa SPSSWIN; p<0,05.
ResultadosSe analizaron 1.277 sujetos. La media de edad fue de 69,3 años y el 53,2% fueron mujeres. Por grupos: 42,9% oxibutinina y 57,1% mirabegrón. Las características demográficas y la morbilidad fueron parecidas. Los pacientes en tratamiento con oxibutinina en comparación con mirabegrón presentaron una similar persistencia al tratamiento (35,0 vs. 32,2%, p=0,294), aunque menores costes (1.151,2 vs. 1.809,6€, p<0,001). Las diferencias mayores se observaron en el precio de la medicación (279,2 vs. 692,3€, p<0,001; diferencia: −413,1€) y en las reacciones adversas (9,7 vs. 4,9%, p<0,001).
ConclusionesLos pacientes en tratamiento con oxibutinina frente a mirabegrón para la vejiga hiperactiva se asociaron a una parecida persistencia al tratamiento, menores costes sanitarios y mayores tasas de reacciones adversas de oxibutinina frente a mirabegrón.
To evaluate therapeutic persistence, healthcare resources, medical costs and adverse events of oxybutynin and mirabegron treatments in patients with overactive bladder in routine medical practice.
Patients and methodsAn observational, retrospective, multicentre study was carried out using the records of patients attended to in 3 different geographic locations (Barcelona, Girona, Asturias). An analysis was made on the 2 study groups (oxybutynin and mirabegron). Follow-up time was one year. Persistence was defined as the time (months), without discontinuation of the initial treatment, or without change of treatment at least 60 days after the initial prescription. Primary endpoints: comorbidity, healthcare resources used, and adverse events. The data was analysed using the SPSSWIN Program, with a significance of P<.05.
ResultsOf the total of1,277 patients included in the study, 42.9% were on oxybutynin and 57.1% mirabegron. The mean age was 69.3 years and 53.2% were female. Demographic characteristics and morbidity were similar between the drugs and had a similar persistence (35.0% oxybutynin vs. 32.2% mirabegron, P=.294), although their costs were lower (1,151.2 vs. €1,809.6, P<.001). The biggest differences were observed in the price of medication (279.2 vs. €692.3, P<.001; a variation of: −€413.1); and adverse events (9.7 vs. 4.9%, P<.001).
ConclusionsPatients treated with oxybutynin vs. mirabegron for overactive bladder had similar persistence with the treatment, lower healthcare costs, but with higher oxybutynin vs. mirabegron adverse reaction rates.
La vejiga hiperactiva (VH) es un síndrome caracterizado por presentar síntomas de urgencia miccional con o sin incontinencia de urgencia, y frecuentemente va acompañado de un aumento de la frecuencia miccional diurna y nocturna. Consiste en una hiperactividad del músculo detrusor y puede acompañarse de disfunciones neurológicas1,2. La prevalencia en adultos varia entre un 10-20% y aumenta con la edad2–4. En población europea se estima que los síntomas de VH afectan al 16% de los varones mayores de 40 años, y al 41% de los mayores de 75 años, mientras que la prevalencia en población general mayor de 18 años es del 11,8%, similar para varones y mujeres5–7.
La VH afecta la calidad de vida de los pacientes tanto por los síntomas de llenado que la caracterizan como por las estrategias que estos adoptan para poder vivir con ellos8,9. En este sentido, muchos pacientes toman medidas extremas para evitar la frecuencia y los episodios de incontinencia, ocasionando una importante repercusión en su estado físico, la vitalidad, la vida social, el estado emocional y la funcionalidad10. No todos los pacientes buscan ayuda profesional para este problema, y solo una cuarta parte de ellos reciben tratamiento1. Además, es frecuente que los pacientes con VH no respondan adecuadamente al tratamiento farmacológico, sobre todo por falta de adherencia al mismo, pero también por falta de eficacia o problemas de tolerancia11,12; en este sentido, los medicamentos para la VH han mostrado su eficacia y seguridad, con una aceptable tolerabilidad para el tratamiento de dicha afección en diversos estudios clínicos1,2,13, que se ha acompañado de una mejora en la calidad de vida relacionada con la salud2,14.
Mirabegrón, comercializado en 2014, presenta un mecanismo de acción diferente que estimula los receptores adrenérgicos β3 en el músculo detrusor de la vejiga; mejora la capacidad de almacenamiento en la fase de llenado, por lo que reduce la frecuencia miccional de los pacientes y el número de episodios de incontinencia y de urgencia15. Por otro lado, oxibutinina está comercializada desde 2005 y es un antiespasmódico que ejerce un efecto anticolinérgico sobre el músculo liso de un modo selectivo, reduciendo la frecuencia de las contracciones, aumentando la capacidad de la vejiga y retrasando el deseo inicial de vaciado16.
Los estudios disponibles en cuanto a la comparación de medicamentos para el tratamiento de la VH relativos a la discontinuación del tratamiento son limitados en nuestro país, por lo que la realización de este análisis puede ser relevante17,18. Además, existe una creciente necesidad de llevar a cabo estudios representativos de las condiciones clínicas reales en las que se utilizan medicamentos. El objetivo primario de este estudio fue analizar la persistencia de mirabegrón y oxibutinina en el tratamiento de la VH en la práctica clínica habitual en España. Como objetivo secundario se determinó el uso de los recursos y costes sanitarios asociados, y se evaluaron las tasas de reacciones adversas a estos medicamentos.
Pacientes y métodosDiseño y población de estudioSe efectuó un diseño observacional, multicéntrico, postautorización, longitudinal y de carácter retrospectivo, realizado a partir de la revisión de los registros médicos existentes (bases de datos informatizadas, con datos disociados) de pacientes seguidos en régimen ambulatorio y hospitalario. La población de estudio estuvo formada por pacientes de 3 áreas geográficas pertenecientes a Barcelona (La Roca del Vallés), Girona (subcomarca Selva Interior) y Asturias (Avilés). Se obtuvo la participación de 18 centros de atención primaria (AP) seleccionados en función de la disponibilidad de los registros. La población asignada a los centros fue en su mayoría urbana, de nivel socioeconómico medio-bajo, con predominio industrial.
Criterios de inclusión y exclusiónSe incluyeron en el estudio todos los pacientes que demandaron atención y que iniciaron un primer tratamiento con alguno de los 2 medicamentos para la VH: mirabegron y oxibutinina, entre el 1 de enero de 2009 y el 31 de diciembre de 2014 (periodo de selección), y que reunieran los siguientes criterios de inclusión: a) edad≥18 años; b) asignados a su área de referencia; c) que se pudiera garantizar el seguimiento regular de los pacientes en los diferentes centros por presentar, al menos, 2 registros o más de sus datos sanitarios en el sistema informático del área de salud correspondiente, y d) estar en el programa de prescripciones para la obtención de las recetas con registro constatado de la dosis diaria, el intervalo de tiempo y la duración de cada tratamiento administrado. Fueron excluidos los sujetos: a) trasladados a otros centros de AP y los desplazados o fuera de zona; b) los pacientes tratados simultáneamente con 2 medicamentos para la VH durante el periodo de estudio; c) pacientes institucionalizados permanentemente y los que hayan tenido un parto o cirugía del tracto urinario inferior. El seguimiento de los pacientes fue durante el año posterior a la fecha de inicio del tratamiento para la VH.
Descripción de la vejiga hiperactivaEl diagnóstico de VH se obtuvo a partir de la Clasificación Internacional de la AP, en el componente 7 de las enfermedades y problemas de salud19 (U13), y de la codificación de las altas hospitalarias y urgencias según la Clasificación Internacional de Enfermedades, novena revisión, Modificación Clínica (596.51).
Medicación administrada y persistencia al tratamientoSe obtuvieron los medicamentos (principios activos) indicados para el tratamiento dela VH según la Anatomical Therapeutic Chemical Classification System20. La información se obtuvo de los registros procedentes de la dispensación farmacológica de medicamentos. La elección del medicamento para un paciente en concreto fue a criterio del médico (práctica clínica). La persistencia entre los principios activos se calculó desde la fecha de inicio hasta la fecha de discontinuación. La fecha de discontinuación fue aquella en que el paciente cambia a otro principio activo, se le añade otro fármaco (combinación) o abandona/interrumpe la medicación (≥60 días sin renovar la medicación y≥2 recetas). El aumento/escalado de la dosis se consideró como discontinuación o no persistencia al tratamiento. El porcentaje de cumplimiento terapéutico se definió según los criterios de la Sociedad Internacional de Farmacoeconomía y Resultados en Salud y se calculó en función de la tasa/ratio de posesión del medicamento (RPM)21. Este se evaluó desde la primera a la última prescripción y representó el número de días de medicación subministrada entre el número de días en tratamiento (a partir de la fecha índice)22. Se cuantificaron las causas de discontinuación al tratamiento (abandono, modificación de dosis, cambio a otro AM y reacciones adversas). Además, se obtuvo: a) el uso de absorbentes para la incontinencia urinaria (% de pacientes), y b) la medicación concomitante para infecciones de orina (antidepresivos, ansiolíticos/hipnóticos y antibióticos/antisépticos). El uso de absorbentes y la medicación concomitante se cuantificaron desde la fecha de inicio del tratamiento para la VH (en uso) hasta finalizar el periodo de seguimiento (en uso o nuevos fármacos).
Variables sociodemográficas y de comorbilidadLas principales variables de estudio fueron: edad (continua y por rangos), sexo, situación laboral (activo, pensionista), el tiempo desde el diagnóstico hasta el inicio del tratamiento (en años) y los antecedentes personales (Clasificación Internacional de la AP)19 de hipertensión arterial (K86, K87), diabetes mellitus (T89, T90), dislipidemia (T93), obesidad (T82), tabaquismo (P17), alcoholismo (P15, P16), todos los tipos de fallos orgánicos (cardiaco, hepático y renal), cardiopatía isquémica (K74, K75), accidente vasculocerebral (K90, K91, K93), enfermedad pulmonar obstructiva crónica (R95, obstrucción crónica del flujo aéreo), asma bronquial (R96), demencias o trastornos de memoria (P70, P20), enfermedades neurológicas: enfermedad de Parkinson (N87), epilepsia (N88), esclerosis múltiple (N86) y otras enfermedades neurológicas (N99); síndrome depresivo (P76) y neoplasias malignas (todos los tipos; A79, B72-75, D74-78, F75, H75, K72, L71, L97, N74-76, R84-86, T71-73, U75-79, W72-73, X75-81, Y77-79). Como variable resumen de la comorbilidad general, para cada paciente atendido se utilizó: a) el índice de comorbilidad de Charlson23 como una aproximación a la gravedad del paciente, y b) el índice de casuística individual, obtenido a partir de los Adjusted Clinical Groups, que es un sistema de clasificación de pacientes por uso-consumo de recursos24. El aplicativo Adjusted Clinical Groups proporciona las bandas de utilización de recursos (BUR), con lo que cada paciente en función de su morbilidad general quedó agrupado en una de las 5 categorías mutuamente excluyentes (1: usuarios sanos o de morbilidad muy baja; 2: morbilidad baja; 3: morbilidad moderada; 4: morbilidad elevada, y 5: morbilidad muy elevada).
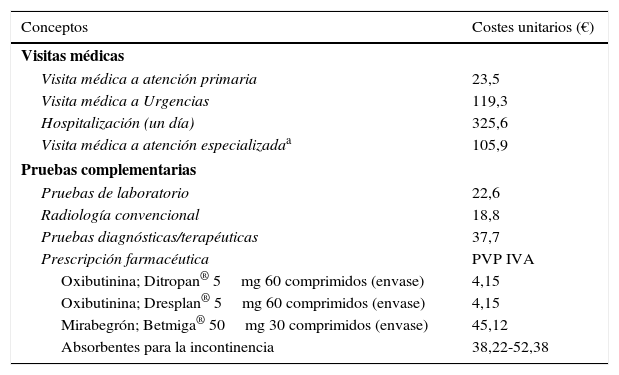
Uso de recursos y costesSe analizaron los costes sanitarios (costes directos) relacionados con la actividad asistencial (visitas médicas, días de hospitalización, urgencias, solicitudes diagnósticas o terapéuticas y medicación específica y concomitante) efectuada por los profesionales. El coste fue expresado en coste medio por paciente (promedio/unitario) durante el periodo estudio (un año). Los diferentes conceptos de estudio y su valoración económica se detallan en la tabla 1 (correspondientes al año 2015). Las tarifas se obtuvieron a partir de la contabilidad analítica de los centros, excepto la medicación. Las prescripciones (recetas médicas) se cuantificaron según el precio de venta al público por envase en el momento de la prescripción. El uso de los recursos y costes de los pacientes fue únicamente el relacionada con la VH.
Detalle de los recursos sanitarios. Costes unitarios correspondientes al año 2015
| Conceptos | Costes unitarios (€) |
|---|---|
| Visitas médicas | |
| Visita médica a atención primaria | 23,5 |
| Visita médica a Urgencias | 119,3 |
| Hospitalización (un día) | 325,6 |
| Visita médica a atención especializadaa | 105,9 |
| Pruebas complementarias | |
| Pruebas de laboratorio | 22,6 |
| Radiología convencional | 18,8 |
| Pruebas diagnósticas/terapéuticas | 37,7 |
| Prescripción farmacéutica | PVP IVA |
| Oxibutinina; Ditropan® 5mg 60 comprimidos (envase) | 4,15 |
| Oxibutinina; Dresplan® 5mg 60 comprimidos (envase) | 4,15 |
| Mirabegrón; Betmiga® 50mg 30 comprimidos (envase) | 45,12 |
| Absorbentes para la incontinencia | 38,22-52,38 |
PVP IVA: precio de venta al público con impuesto sobre el valor añadido.
Fuente de los recursos sanitarios: contabilidad analítica propia.
Estos datos se obtuvieron de la información disponible en todos los centros para las notificaciones de sospechas de reacciones adversas a medicamentos por parte de profesionales sanitarios, según las directrices emitidas por el Sistema Español de Farmacovigilancia de medicamentos de Uso Humano. Se cuantificaron en relación con el abandono de la medicación y únicamente para oxibutinina y mirabegrón.
Confidencialidad de la información y cálculo del tamaño de la muestraSe respetó la confidencialidad de los registros (anónimos y disociados) según la Ley Orgánica de Protección de Datos (Ley 15/1999 del 13 de diciembre). El estudio fue clasificado por la Agencia Española de Medicamentos y Productos Sanitarios (EPA-OD) y posteriormente fue aprobado por el Comité de Ética de Investigación Clínica de Mallorca (Baleares; expediente lB-25491/15). El cálculo del tamaño muestral se obtuvo en función de una prevalencia esperada de VH del 11,8%, asumiendo un error aleatorio del 5% y una precisión del 3%. Se tendría que seleccionar un mínimo de 442 pacientes por grupo de estudio. La potencia estadística fue del 80%.
Análisis estadísticoSe realizó una rigurosa validación de los resultados para asegurar la calidad de los registros. Se efectuó un análisis estadístico descriptivo-univariante con valores de media, desviación estándar, intervalos de confianza del 95% y de amplitud intercuartílica (mediana y percentiles 25-75 de la distribución), y se comprobó la normalidad de la distribución con la prueba de Kolmogorov-Smirnov. Para la medida de la persistencia al tratamiento se realizó un análisis de supervivencia de Kaplan-Meier (comparación: prueba de Log Rank) y el modelo de riesgos proporcionales de Cox. En el análisis bivariante se utilizaron las pruebas de ANOVA, ji al cuadrado y la correlación lineal de Pearson. La comparación del coste se realizó según las recomendaciones de Thompson y Barber25. Los modelos multivariantes utilizados fueron los siguientes: a) análisis de la covarianza (ANCOVA; procedimiento: estimación de medias marginales; ajuste de Bonferroni), para la corrección del coste sanitario (variable dependiente), y b) regresión lineal múltiple, para determinar las variables asociadas al coste sanitario (variable dependiente). Las covariables incluidas fueron: la localización, el sexo, la edad, la comorbilidad general (BUR, índice de Charlson), el tiempo desde el diagnóstico y el RPM. Se utilizó el programa SPSSWIN versión 19, estableciéndose una significación estadística para valores de p<0,05.
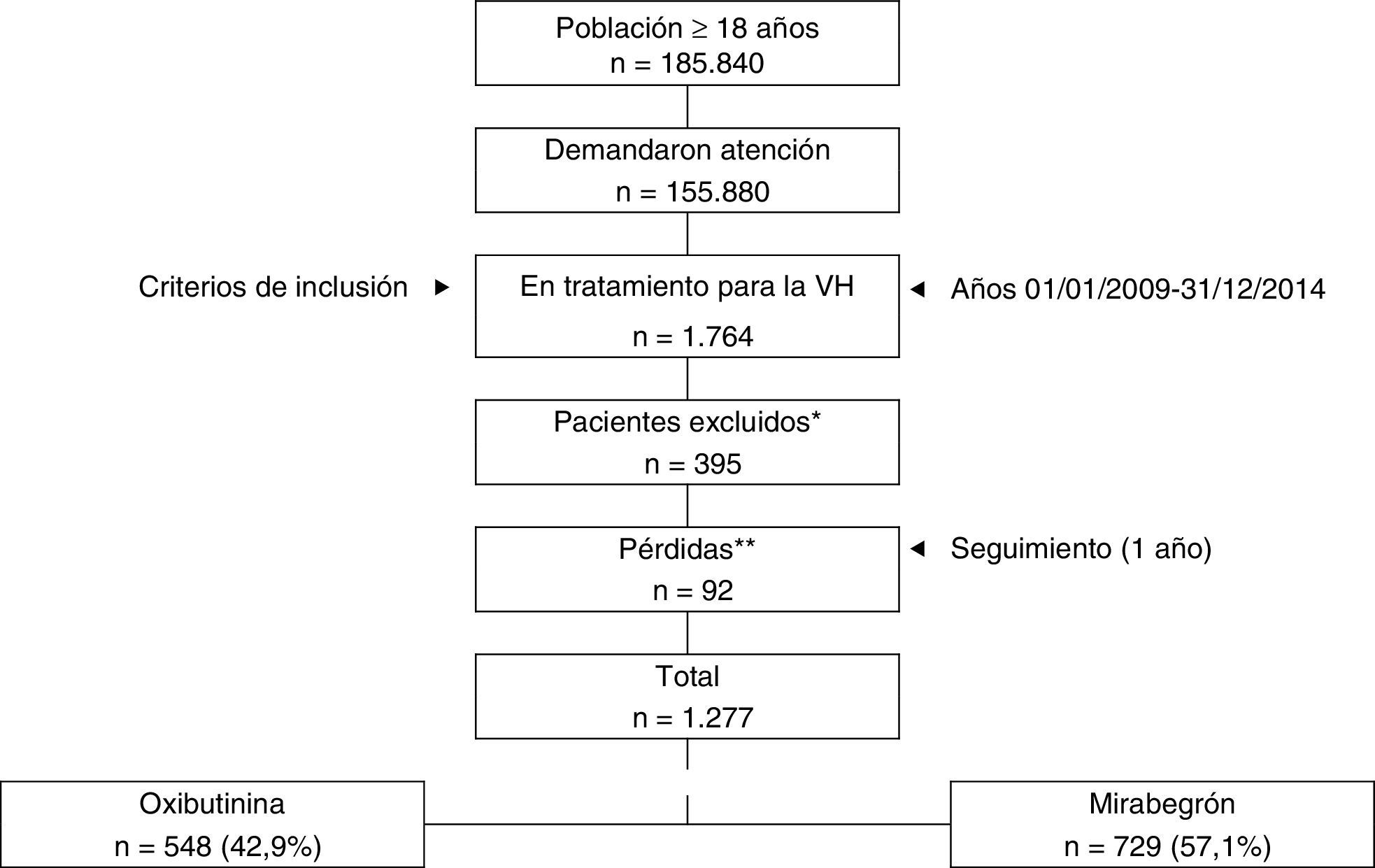
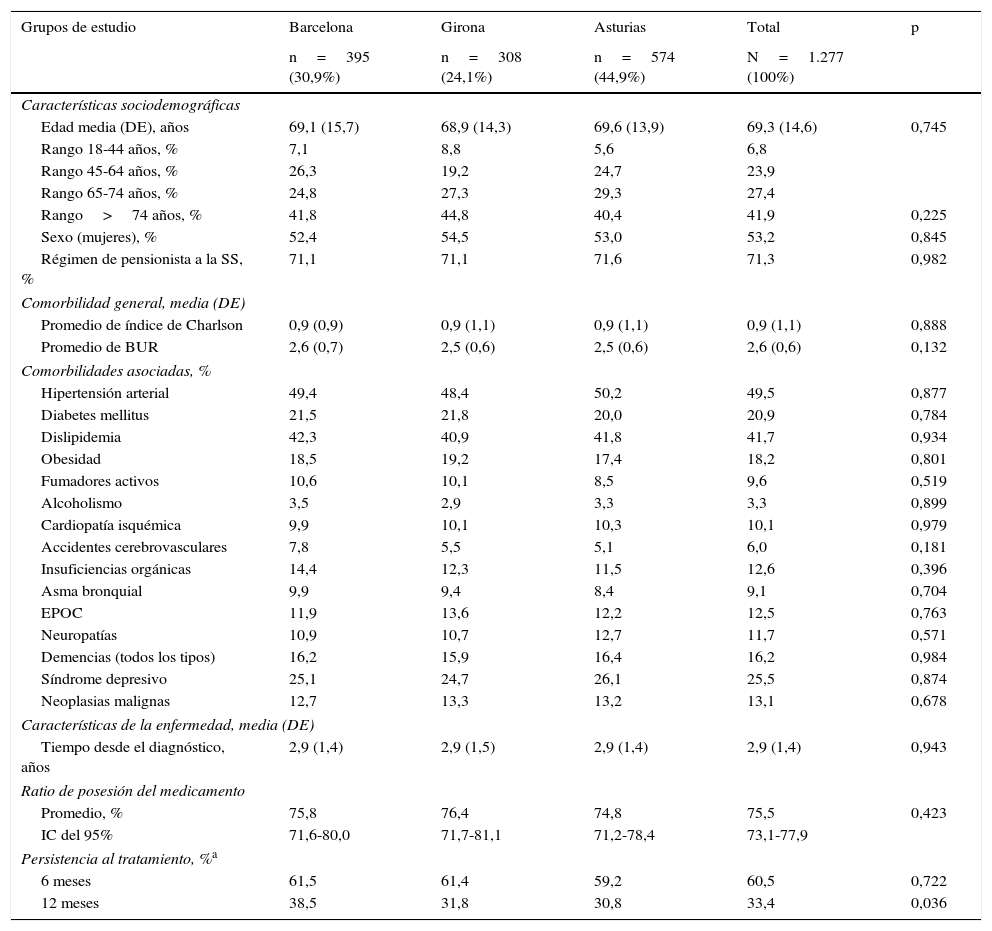
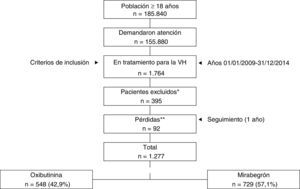
ResultadosSe analizaron 1.277 pacientes que cumplían con los criterios de inclusión/exclusión y pudieron seguirse durante el periodo de estudio. El número de pacientes seleccionado mostró la siguiente distribución: Barcelona (n=395, 30,9%), Girona (n=308, 24,1%) y Asturias (n=574, 44,9%) (fig. 1). Las características generales de la serie estudiada por áreas geográficas se detallan en la tabla 2. La media de edad de los pacientes fue de 69,3 años, y el porcentaje de mujeres fue del 53,2%. La carga de morbilidad general fue similar en todos los grupos (BUR 2,6; 2,5 y 2,5 puntos, respectivamente; p=0,132). En general, la hipertensión arterial (49,5%), la dislipidemia (41,7%), la depresión (25,5%) y la diabetes (20,9%) fueron las comorbilidades más frecuentes. El tiempo desde el diagnóstico y el RPM por áreas geográficas fueron semejantes. Destaca la persistencia a los 12 meses ligeramente superior en Barcelona frente a Girona y Asturias (38,5 frente al 31,8 y 30,8%, respectivamente; p=0,036).
Esquema general del estudio. Se efectuó un diseño observacional, multicéntrico, postautorización, longitudinal y de carácter retrospectivo, realizado a partir de la revisión de los registros médicos existentes (bases de datos informatizadas, con datos disociados) de pacientes seguidos en régimen ambulatorio y hospitalario.
VH: vejiga hiperactiva.
* Pacientes excluidos: a) inconsistencia de los datos reportados (n=261, 14,7%); b) incumplimiento de los criterios de inclusión/exclusión (n=98, 5,5%), y c) otras causas (n=36, 2,2%). ** Pérdidas durante el seguimiento: a) por desplazamiento (n=74, 4,2%), y b) por fallecimiento (n=18, 1,1%). No hubo diferencias significativas entre las áreas geográficas analizadas.
Características generales y persistencia al tratamiento por áreas geográficas
| Grupos de estudio | Barcelona | Girona | Asturias | Total | p |
|---|---|---|---|---|---|
| n=395 (30,9%) | n=308 (24,1%) | n=574 (44,9%) | N=1.277 (100%) | ||
| Características sociodemográficas | |||||
| Edad media (DE), años | 69,1 (15,7) | 68,9 (14,3) | 69,6 (13,9) | 69,3 (14,6) | 0,745 |
| Rango 18-44 años, % | 7,1 | 8,8 | 5,6 | 6,8 | |
| Rango 45-64 años, % | 26,3 | 19,2 | 24,7 | 23,9 | |
| Rango 65-74 años, % | 24,8 | 27,3 | 29,3 | 27,4 | |
| Rango>74 años, % | 41,8 | 44,8 | 40,4 | 41,9 | 0,225 |
| Sexo (mujeres), % | 52,4 | 54,5 | 53,0 | 53,2 | 0,845 |
| Régimen de pensionista a la SS, % | 71,1 | 71,1 | 71,6 | 71,3 | 0,982 |
| Comorbilidad general, media (DE) | |||||
| Promedio de índice de Charlson | 0,9 (0,9) | 0,9 (1,1) | 0,9 (1,1) | 0,9 (1,1) | 0,888 |
| Promedio de BUR | 2,6 (0,7) | 2,5 (0,6) | 2,5 (0,6) | 2,6 (0,6) | 0,132 |
| Comorbilidades asociadas, % | |||||
| Hipertensión arterial | 49,4 | 48,4 | 50,2 | 49,5 | 0,877 |
| Diabetes mellitus | 21,5 | 21,8 | 20,0 | 20,9 | 0,784 |
| Dislipidemia | 42,3 | 40,9 | 41,8 | 41,7 | 0,934 |
| Obesidad | 18,5 | 19,2 | 17,4 | 18,2 | 0,801 |
| Fumadores activos | 10,6 | 10,1 | 8,5 | 9,6 | 0,519 |
| Alcoholismo | 3,5 | 2,9 | 3,3 | 3,3 | 0,899 |
| Cardiopatía isquémica | 9,9 | 10,1 | 10,3 | 10,1 | 0,979 |
| Accidentes cerebrovasculares | 7,8 | 5,5 | 5,1 | 6,0 | 0,181 |
| Insuficiencias orgánicas | 14,4 | 12,3 | 11,5 | 12,6 | 0,396 |
| Asma bronquial | 9,9 | 9,4 | 8,4 | 9,1 | 0,704 |
| EPOC | 11,9 | 13,6 | 12,2 | 12,5 | 0,763 |
| Neuropatías | 10,9 | 10,7 | 12,7 | 11,7 | 0,571 |
| Demencias (todos los tipos) | 16,2 | 15,9 | 16,4 | 16,2 | 0,984 |
| Síndrome depresivo | 25,1 | 24,7 | 26,1 | 25,5 | 0,874 |
| Neoplasias malignas | 12,7 | 13,3 | 13,2 | 13,1 | 0,678 |
| Características de la enfermedad, media (DE) | |||||
| Tiempo desde el diagnóstico, años | 2,9 (1,4) | 2,9 (1,5) | 2,9 (1,4) | 2,9 (1,4) | 0,943 |
| Ratio de posesión del medicamento | |||||
| Promedio, % | 75,8 | 76,4 | 74,8 | 75,5 | 0,423 |
| IC del 95% | 71,6-80,0 | 71,7-81,1 | 71,2-78,4 | 73,1-77,9 | |
| Persistencia al tratamiento, %a | |||||
| 6 meses | 61,5 | 61,4 | 59,2 | 60,5 | 0,722 |
| 12 meses | 38,5 | 31,8 | 30,8 | 33,4 | 0,036 |
BUR: bandas de utilización de recursos; DE: desviación estándar; EPOC: enfermedad pulmonar obstructiva crónica; IC: intervalo de confianza; SS: seguridad social.
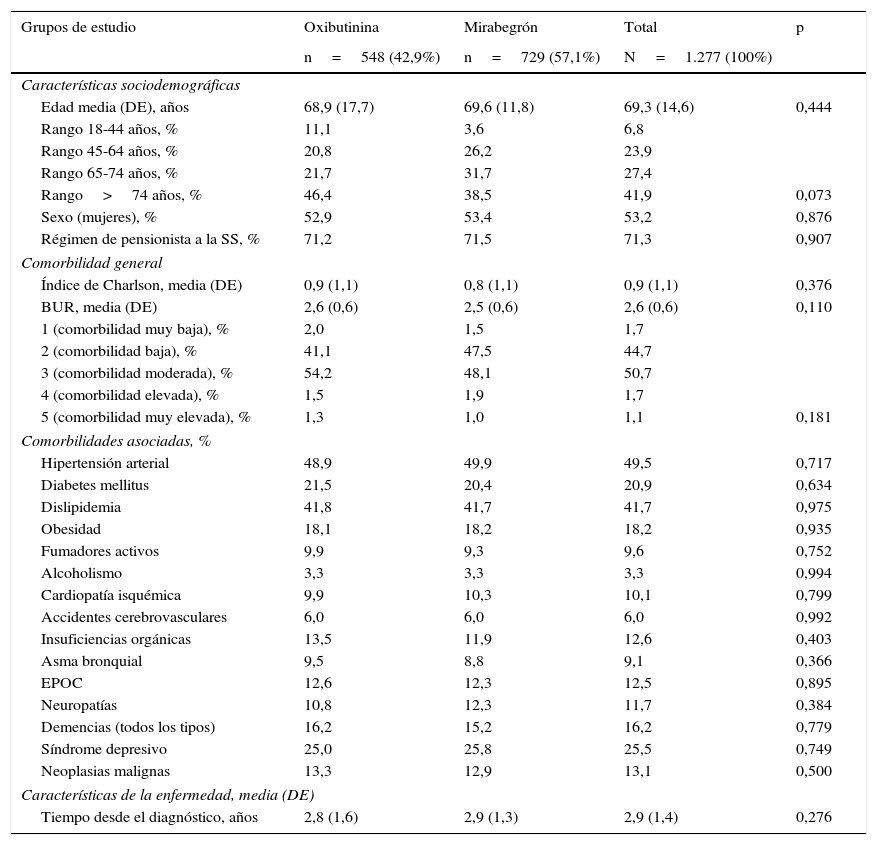
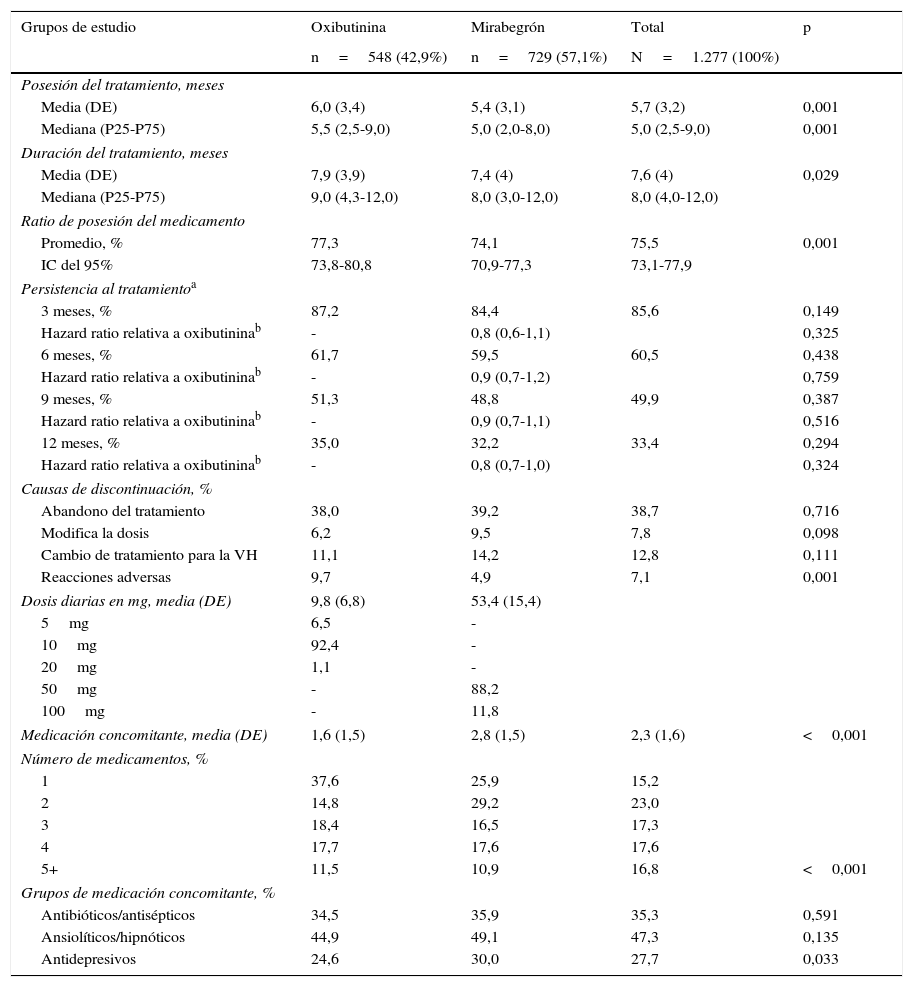
Las características generales de la serie estudiada por el fármaco analizado se detallan en la tabla 3. El número de pacientes fue el siguiente: oxibutinina (n=548, 42,9%) y mirabegrón (n=729, 57,1%). Las características demográficas y la morbilidad general/específica de los 2 fármacos analizados fueron muy similares. En la tabla 4 se detalla la persistencia al tratamiento, la RPM, las dosis administradas y la medicación concomitante por tipo de fármaco analizado. Oxibutinina en comparación con mirabegrón tuvo una duración del tratamiento (7,9 frente a 7,4 meses, p=0,029) y una RPM ligeramente superiores (77,3 frente a 74,1%, p=0,001), mientras que la persistencia al tratamiento a los 12 meses (35,0 frente a 32,2%, p=0,294) fue similar. Los porcentajes de medicación concomitante (antibióticos/antisépticos, ansiolíticos/hipnóticos), las dosis farmacológicas y la reducción de absorbentes para la incontinencia urinaria al final del periodo de estudio fueron muy parecidos.
Características generales de la serie estudiada por tipo de fármaco
| Grupos de estudio | Oxibutinina | Mirabegrón | Total | p |
|---|---|---|---|---|
| n=548 (42,9%) | n=729 (57,1%) | N=1.277 (100%) | ||
| Características sociodemográficas | ||||
| Edad media (DE), años | 68,9 (17,7) | 69,6 (11,8) | 69,3 (14,6) | 0,444 |
| Rango 18-44 años, % | 11,1 | 3,6 | 6,8 | |
| Rango 45-64 años, % | 20,8 | 26,2 | 23,9 | |
| Rango 65-74 años, % | 21,7 | 31,7 | 27,4 | |
| Rango>74 años, % | 46,4 | 38,5 | 41,9 | 0,073 |
| Sexo (mujeres), % | 52,9 | 53,4 | 53,2 | 0,876 |
| Régimen de pensionista a la SS, % | 71,2 | 71,5 | 71,3 | 0,907 |
| Comorbilidad general | ||||
| Índice de Charlson, media (DE) | 0,9 (1,1) | 0,8 (1,1) | 0,9 (1,1) | 0,376 |
| BUR, media (DE) | 2,6 (0,6) | 2,5 (0,6) | 2,6 (0,6) | 0,110 |
| 1 (comorbilidad muy baja), % | 2,0 | 1,5 | 1,7 | |
| 2 (comorbilidad baja), % | 41,1 | 47,5 | 44,7 | |
| 3 (comorbilidad moderada), % | 54,2 | 48,1 | 50,7 | |
| 4 (comorbilidad elevada), % | 1,5 | 1,9 | 1,7 | |
| 5 (comorbilidad muy elevada), % | 1,3 | 1,0 | 1,1 | 0,181 |
| Comorbilidades asociadas, % | ||||
| Hipertensión arterial | 48,9 | 49,9 | 49,5 | 0,717 |
| Diabetes mellitus | 21,5 | 20,4 | 20,9 | 0,634 |
| Dislipidemia | 41,8 | 41,7 | 41,7 | 0,975 |
| Obesidad | 18,1 | 18,2 | 18,2 | 0,935 |
| Fumadores activos | 9,9 | 9,3 | 9,6 | 0,752 |
| Alcoholismo | 3,3 | 3,3 | 3,3 | 0,994 |
| Cardiopatía isquémica | 9,9 | 10,3 | 10,1 | 0,799 |
| Accidentes cerebrovasculares | 6,0 | 6,0 | 6,0 | 0,992 |
| Insuficiencias orgánicas | 13,5 | 11,9 | 12,6 | 0,403 |
| Asma bronquial | 9,5 | 8,8 | 9,1 | 0,366 |
| EPOC | 12,6 | 12,3 | 12,5 | 0,895 |
| Neuropatías | 10,8 | 12,3 | 11,7 | 0,384 |
| Demencias (todos los tipos) | 16,2 | 15,2 | 16,2 | 0,779 |
| Síndrome depresivo | 25,0 | 25,8 | 25,5 | 0,749 |
| Neoplasias malignas | 13,3 | 12,9 | 13,1 | 0,500 |
| Características de la enfermedad, media (DE) | ||||
| Tiempo desde el diagnóstico, años | 2,8 (1,6) | 2,9 (1,3) | 2,9 (1,4) | 0,276 |
BUR: bandas de utilización de recursos; DE: desviación estándar; EPOC: enfermedad pulmonar obstructiva crónica; SS: seguridad social.
Persistencia al tratamiento, ratio de posesión de la medicación, dosis administradas y medicación concomitante por tipo de fármaco analizado
| Grupos de estudio | Oxibutinina | Mirabegrón | Total | p |
|---|---|---|---|---|
| n=548 (42,9%) | n=729 (57,1%) | N=1.277 (100%) | ||
| Posesión del tratamiento, meses | ||||
| Media (DE) | 6,0 (3,4) | 5,4 (3,1) | 5,7 (3,2) | 0,001 |
| Mediana (P25-P75) | 5,5 (2,5-9,0) | 5,0 (2,0-8,0) | 5,0 (2,5-9,0) | 0,001 |
| Duración del tratamiento, meses | ||||
| Media (DE) | 7,9 (3,9) | 7,4 (4) | 7,6 (4) | 0,029 |
| Mediana (P25-P75) | 9,0 (4,3-12,0) | 8,0 (3,0-12,0) | 8,0 (4,0-12,0) | |
| Ratio de posesión del medicamento | ||||
| Promedio, % | 77,3 | 74,1 | 75,5 | 0,001 |
| IC del 95% | 73,8-80,8 | 70,9-77,3 | 73,1-77,9 | |
| Persistencia al tratamientoa | ||||
| 3 meses, % | 87,2 | 84,4 | 85,6 | 0,149 |
| Hazard ratio relativa a oxibutininab | - | 0,8 (0,6-1,1) | 0,325 | |
| 6 meses, % | 61,7 | 59,5 | 60,5 | 0,438 |
| Hazard ratio relativa a oxibutininab | - | 0,9 (0,7-1,2) | 0,759 | |
| 9 meses, % | 51,3 | 48,8 | 49,9 | 0,387 |
| Hazard ratio relativa a oxibutininab | - | 0,9 (0,7-1,1) | 0,516 | |
| 12 meses, % | 35,0 | 32,2 | 33,4 | 0,294 |
| Hazard ratio relativa a oxibutininab | - | 0,8 (0,7-1,0) | 0,324 | |
| Causas de discontinuación, % | ||||
| Abandono del tratamiento | 38,0 | 39,2 | 38,7 | 0,716 |
| Modifica la dosis | 6,2 | 9,5 | 7,8 | 0,098 |
| Cambio de tratamiento para la VH | 11,1 | 14,2 | 12,8 | 0,111 |
| Reacciones adversas | 9,7 | 4,9 | 7,1 | 0,001 |
| Dosis diarias en mg, media (DE) | 9,8 (6,8) | 53,4 (15,4) | ||
| 5mg | 6,5 | - | ||
| 10mg | 92,4 | - | ||
| 20mg | 1,1 | - | ||
| 50mg | - | 88,2 | ||
| 100mg | - | 11,8 | ||
| Medicación concomitante, media (DE) | 1,6 (1,5) | 2,8 (1,5) | 2,3 (1,6) | <0,001 |
| Número de medicamentos, % | ||||
| 1 | 37,6 | 25,9 | 15,2 | |
| 2 | 14,8 | 29,2 | 23,0 | |
| 3 | 18,4 | 16,5 | 17,3 | |
| 4 | 17,7 | 17,6 | 17,6 | |
| 5+ | 11,5 | 10,9 | 16,8 | <0,001 |
| Grupos de medicación concomitante, % | ||||
| Antibióticos/antisépticos | 34,5 | 35,9 | 35,3 | 0,591 |
| Ansiolíticos/hipnóticos | 44,9 | 49,1 | 47,3 | 0,135 |
| Antidepresivos | 24,6 | 30,0 | 27,7 | 0,033 |
DE: desviación estándar; IC: intervalo de confianza; P: percentil; VH: vejiga hiperactiva.
La persistencia se definió como el tiempo, medido en meses, sin abandono del tratamiento inicial o sin cambio a otra medicación al menos 60 días después de la prescripción inicial.
Regresión de riesgos proporcionales de Cox (corregida por localización, edad, sexo, tiempo desde el diagnóstico, número de tratamientos concomitantes, comorbilidad y ratio de posesión del medicamento). Medicamento de referencia: oxibutinina (sin diferencias estadísticamente significativas en todos los modelos analizados).
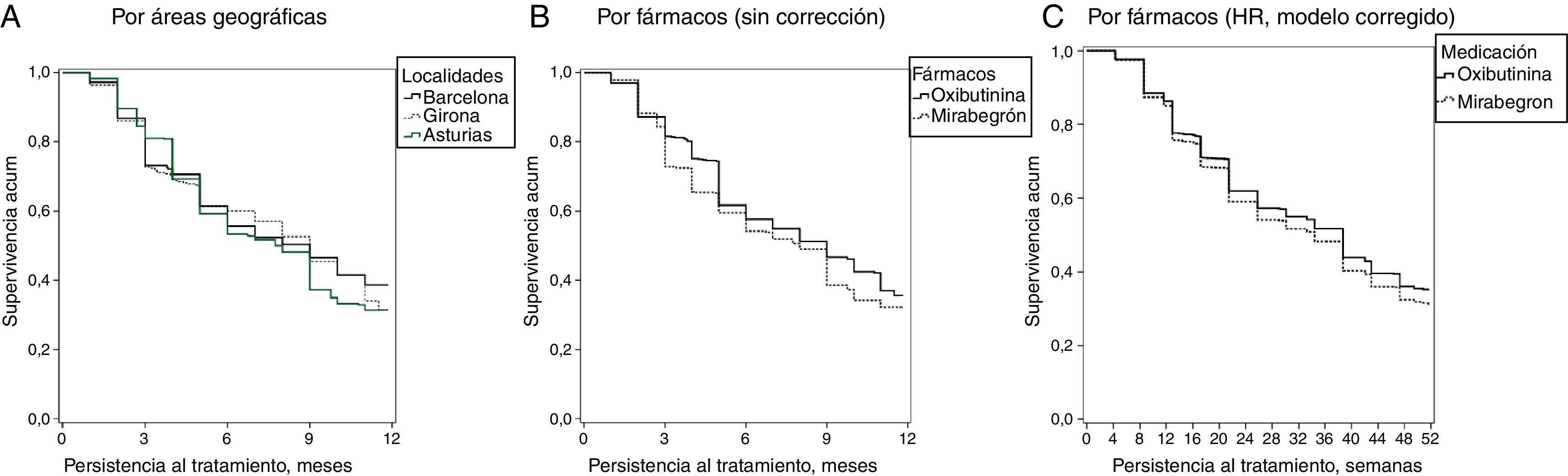
En la figura 2 se detallan las curvas de Kaplan-Meier de persistencia al tratamiento por grupos de estudio. Por áreas geográficas la persistencia al tratamiento fue similar, mientras que por los medicamentos para la VH, oxibutinina fue ligeramente superior, aunque sin alcanzar la significación estadística (comparación entre oxibutinina y mirabegrón: prueba de Log Rank-Mantel-Cox: 2,992; p=0,084). La figura 2C muestra la probabilidad acumulada de permanecer con el mismo tratamiento para la VH inicial a las 52 semanas de seguimiento, corregido por covariables (factores de confusión). La persistencia al tratamiento entre los 2 fármacos fue similar (p=0,185).
Curvas de Kaplan-Meier de persistencia y probabilidad acumulada de permanecer en el tratamiento a las 52 semanas de seguimiento.
A) Curva de Kaplan-Meier: estimación de la mediana de duración del tratamiento inicial por áreas geográficas. Comparación entre Barcelona y Girona: prueba de Log Rank-Mantel-Cox: 3,750; p=0,053. Comparación entre Barcelona y Asturias: prueba de Log Rank-Mantel-Cox: 1,652; p=0,199. Comparación entre Girona y Asturias: prueba de Log Rank-Mantel-Cox: 0,240; p=0,624.
B) Curva de Kaplan-Meier: estimación de la mediana de duración del tratamiento inicial para la VH. Comparación entre oxibutinina y mirabegrón: prueba de Log Rank-Mantel-Cox: 2,992; p=0,084.
C) Hazard ratio (HR) estimada por el modelo de riesgos proporcionales de Cox corregido por localización, edad, sexo, tiempo desde el diagnóstico, ratio de posesión de la medicación y comorbilidad. Cocientes de riesgo corregidos, persistencia de mirabegrón en relación con oxibutinina: HR=0,967 (IC del 95% 0,865-1,082), p=0,185.
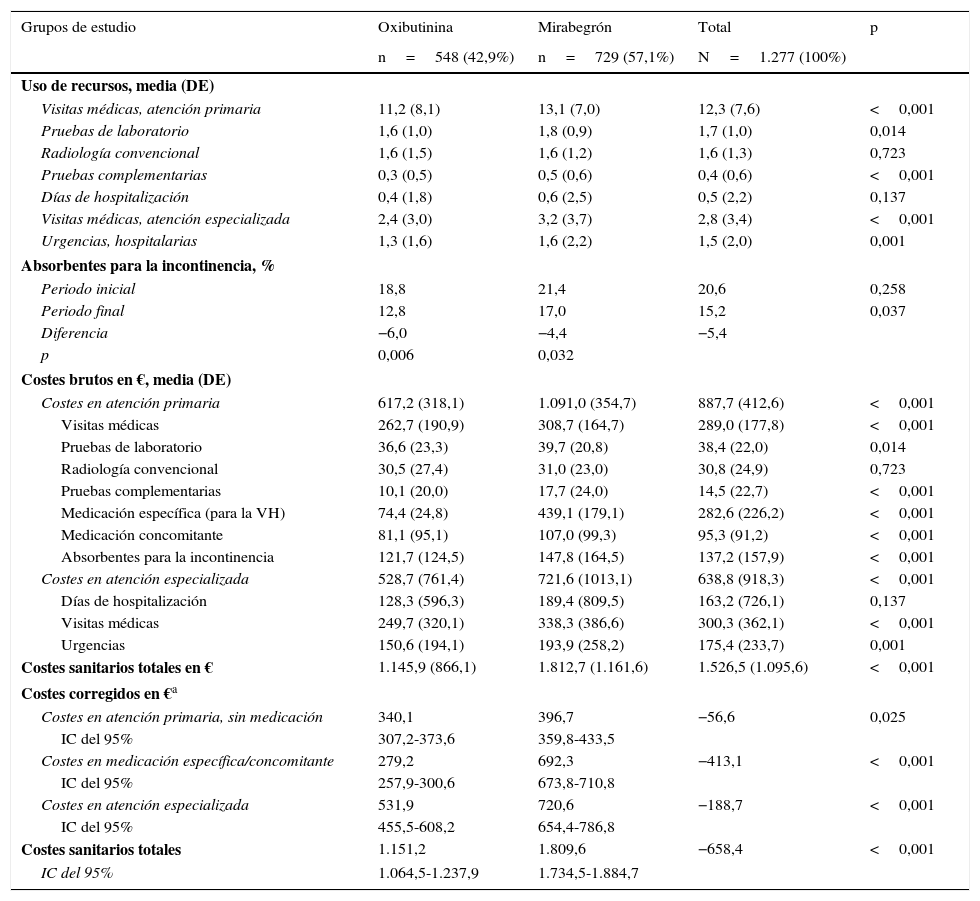
Durante el periodo de seguimiento, los pacientes en tratamiento con oxibutinina utilizaron menos recursos sanitarios, especialmente en visitas médicas en AP (11,2 frente a 13,1, p<0,001) y visitas en atención especializada (2,4 frente a 3,2; p<0,001) (tabla 5). El coste sanitario total de los pacientes incluidos en el estudio ascendió a 1,9 millones de euros, con un promedio/unitario total de 1.527€. El 58,1% de los costes se produjeron en AP y el 41,9% en atención especializada. El 33,7% del coste total fue por la medicación (específica: 18,5%; concomitante: 6,2%; absorbentes: 9,0%). En el modelo corregido, los costes totales de oxibutinina fueron inferiores a los de mirabegrón (1.151,2 frente a 1.809,6€, p<0,001). Las diferencias mayores se observaron en la medicación (279,2 frente a 692,3€; diferencia: −413,1€), p<0,001.
Uso de recursos y costes sanitarios (en €) según los grupos de estudio (durante el seguimiento de los pacientes, un año)
| Grupos de estudio | Oxibutinina | Mirabegrón | Total | p |
|---|---|---|---|---|
| n=548 (42,9%) | n=729 (57,1%) | N=1.277 (100%) | ||
| Uso de recursos, media (DE) | ||||
| Visitas médicas, atención primaria | 11,2 (8,1) | 13,1 (7,0) | 12,3 (7,6) | <0,001 |
| Pruebas de laboratorio | 1,6 (1,0) | 1,8 (0,9) | 1,7 (1,0) | 0,014 |
| Radiología convencional | 1,6 (1,5) | 1,6 (1,2) | 1,6 (1,3) | 0,723 |
| Pruebas complementarias | 0,3 (0,5) | 0,5 (0,6) | 0,4 (0,6) | <0,001 |
| Días de hospitalización | 0,4 (1,8) | 0,6 (2,5) | 0,5 (2,2) | 0,137 |
| Visitas médicas, atención especializada | 2,4 (3,0) | 3,2 (3,7) | 2,8 (3,4) | <0,001 |
| Urgencias, hospitalarias | 1,3 (1,6) | 1,6 (2,2) | 1,5 (2,0) | 0,001 |
| Absorbentes para la incontinencia, % | ||||
| Periodo inicial | 18,8 | 21,4 | 20,6 | 0,258 |
| Periodo final | 12,8 | 17,0 | 15,2 | 0,037 |
| Diferencia | −6,0 | −4,4 | −5,4 | |
| p | 0,006 | 0,032 | ||
| Costes brutos en €, media (DE) | ||||
| Costes en atención primaria | 617,2 (318,1) | 1.091,0 (354,7) | 887,7 (412,6) | <0,001 |
| Visitas médicas | 262,7 (190,9) | 308,7 (164,7) | 289,0 (177,8) | <0,001 |
| Pruebas de laboratorio | 36,6 (23,3) | 39,7 (20,8) | 38,4 (22,0) | 0,014 |
| Radiología convencional | 30,5 (27,4) | 31,0 (23,0) | 30,8 (24,9) | 0,723 |
| Pruebas complementarias | 10,1 (20,0) | 17,7 (24,0) | 14,5 (22,7) | <0,001 |
| Medicación específica (para la VH) | 74,4 (24,8) | 439,1 (179,1) | 282,6 (226,2) | <0,001 |
| Medicación concomitante | 81,1 (95,1) | 107,0 (99,3) | 95,3 (91,2) | <0,001 |
| Absorbentes para la incontinencia | 121,7 (124,5) | 147,8 (164,5) | 137,2 (157,9) | <0,001 |
| Costes en atención especializada | 528,7 (761,4) | 721,6 (1013,1) | 638,8 (918,3) | <0,001 |
| Días de hospitalización | 128,3 (596,3) | 189,4 (809,5) | 163,2 (726,1) | 0,137 |
| Visitas médicas | 249,7 (320,1) | 338,3 (386,6) | 300,3 (362,1) | <0,001 |
| Urgencias | 150,6 (194,1) | 193,9 (258,2) | 175,4 (233,7) | 0,001 |
| Costes sanitarios totales en € | 1.145,9 (866,1) | 1.812,7 (1.161,6) | 1.526,5 (1.095,6) | <0,001 |
| Costes corregidos en €a | ||||
| Costes en atención primaria, sin medicación | 340,1 | 396,7 | −56,6 | 0,025 |
| IC del 95% | 307,2-373,6 | 359,8-433,5 | ||
| Costes en medicación específica/concomitante | 279,2 | 692,3 | −413,1 | <0,001 |
| IC del 95% | 257,9-300,6 | 673,8-710,8 | ||
| Costes en atención especializada | 531,9 | 720,6 | −188,7 | <0,001 |
| IC del 95% | 455,5-608,2 | 654,4-786,8 | ||
| Costes sanitarios totales | 1.151,2 | 1.809,6 | −658,4 | <0,001 |
| IC del 95% | 1.064,5-1.237,9 | 1.734,5-1.884,7 | ||
DE: desviación estándar; IC: intervalo de confianza; VH: vejiga hiperactiva.
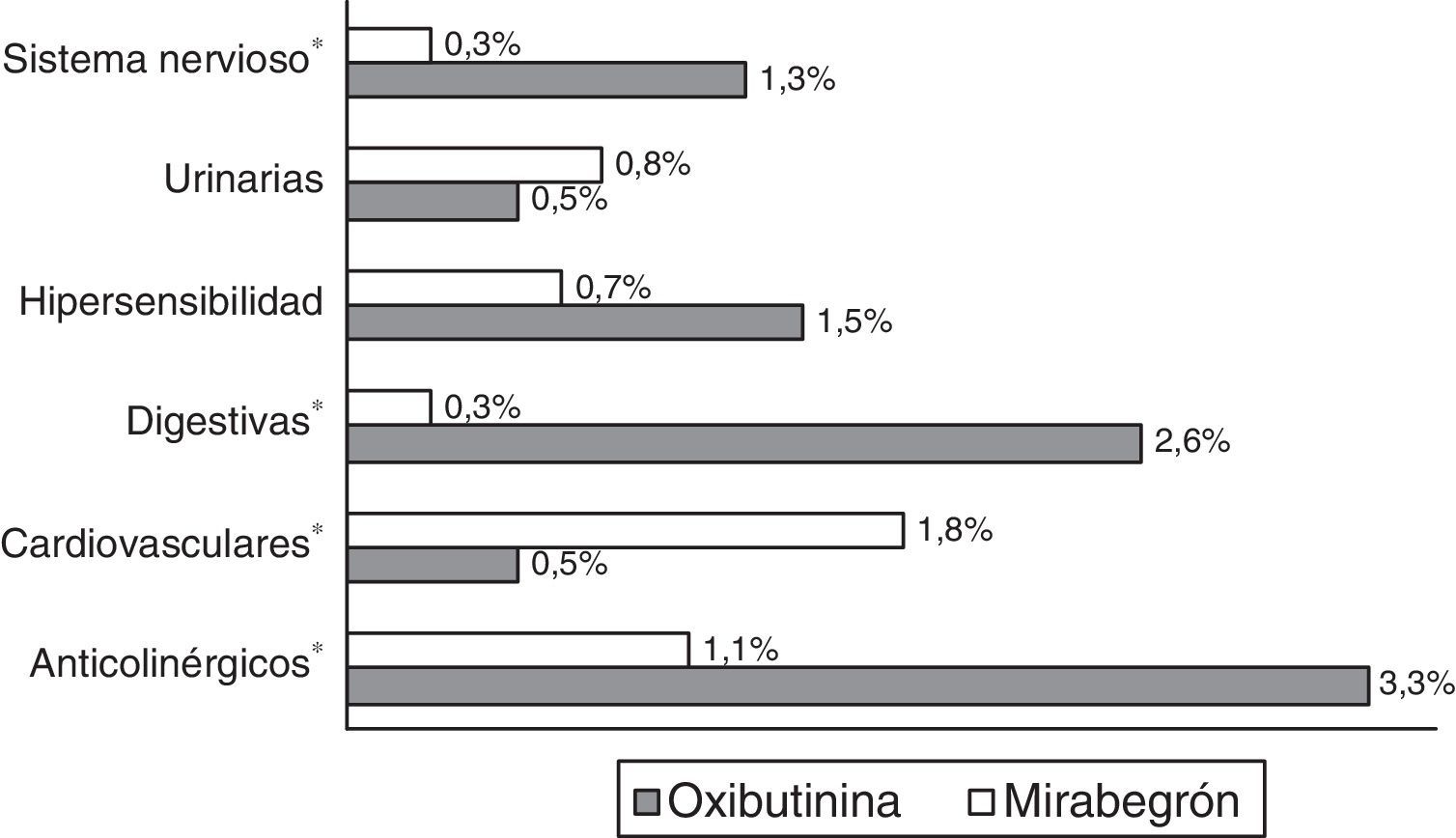
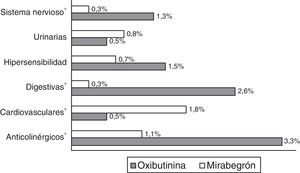
En el modelo de correlaciones binarias la edad se asoció a las BUR (r=0,362), mientras que el tipo de fármaco se asoció al coste de la medicación específica para la VH (r=0,798), p<0,001. Finalmente, en el modelo de regresión lineal múltiple (método: pasos consecutivos), el coste sanitario de la VH se asoció al tipo de fármaco específico utilizado (β=0,275), a la medicación concomitante (β=0,147), a la edad (β=0,131) y al RPM (β=−0,109), con p<0,001 en todos los casos. El coeficiente de determinación de los modelos fue del 38,6%. En la figura 3 se describen las reacciones adversas a medicamentos que motivaron las suspensión del tratamiento. Oxibutinina en comparación con mirabegrón mostró una mayor presencia de eventos adversos (menores en todos los casos; 9,7 frente al 4,9%, p=0,001). No hubo ninguna notificación o ingreso hospitalario por reacciones graves.
Reacciones adversas a medicamentos por grupos de estudio.
Reacciones adversas que obligaron a la suspensión del medicamento oxibutinina: anticolinérgicos (sequedad de boca 3,3%), digestivas (reflujo gastroesofágico 2,0%, estreñimiento 0,6%), cardiovasculares (taquicardia sinusal 0,5%), urinarias (infección del tracto urinario 0,8%), sistema nervioso (síndrome vertiginoso periférico 1,3%), hipersensibilidad (reacción alérgica 1,5%).
Reacciones adversas que obligaron a la suspensión del medicamento mirabegrón: anticolinérgicos (sequedad de boca 1,1%), digestivas (reflujo gastroesofágico 0,3%), cardiovasculares (taquicardia sinusal 1,8%), urinarias (infección del tracto urinario 0,5%), sistema nervioso (síndrome vertiginoso periférico 0,3%), hipersensibilidad (reacción alérgica 0,7%).
* Comparaciones por pares estadísticamente significativas.
Este estudio pone de manifiesto que los pacientes en tratamiento con oxibutinina frente a mirabegrón para la VH muestran una similar persistencia al tratamiento, menores costes sanitarios (especialmente farmacológicos) y mayores tasas de reacciones adversas a la medicación. Cabe destacar la existencia de pocos estudios observacionales que detallen la utilización de estos fármacos en condiciones reales, lo que dificulta la comparación de los resultados, pero en cambio debe interpretarse como una fortaleza del estudio. Este se ha realizado con una amplia muestra de pacientes, y además existe una aceptable comparabilidad inicial en cuanto a las características sociodemográficas y de comorbilidad, tanto por áreas geográficas como por los grupos farmacológicos estudiados.
En la bibliografía consultada existen algunos estudios que evalúan la carga económica de la VH, aunque las diferencias en cuanto a la metodología utilizada (estudios de simulación), las características de las poblaciones, los diferentes componentes del coste y la desigual prevalencia existente obligan a ser cautelosos en la generalización de los resultados. No obstante, la carga económica de la enfermedad aumentará en las próximas décadas debido al envejecimiento progresivo de la población. En EE. UU. se estima que los costes directos de la VH en adultos≥25 años pueden suponer un coste anual de unos 82,6 mil millones de dólares en 2020, con un coste anual por paciente de 1.925$ (1.433 directos, 66 directos no médicos y 426 indirectos)26.
Los pacientes en tratamiento con oxibutinina frente a mirabegrón se asociaron a una similar persistencia al tratamiento (35,0 vs. 32,2%, p=0,294). La revisión sistemática realizada por Veenboer y Bosch27 (N=190.279; edad media 68,5años) detalla unas tasas de persistencia al tratamiento anual con diferentes medicamentos para la VH de entre el 12,0-39,4%, y concluye que la mejora de la persistencia al tratamiento para la VH tiene que ser un reto importante, especialmente en el desarrollo de nuevos medicamentos. En este aspecto, Gomes et al.28 pusieron de manifiesto que la persistencia de oxibutinina, después de 2 años de seguimiento, fue ligeramente inferior a la de tolterodina (9,4 vs. 13,6%). D'Souza et al.29 también mostraron la alta tasa de discontinuación; al año de seguimiento la persistencia al tratamiento para oxibutinina fue del 35,2% y para tolterodina del 36,1%. Wagg et al.30 mostraron unas tasas de persistencia anual bajas (solifenacina 35%, tolterodina 28% y oxibutinina 26%); además, se describió que los pacientes≥60 años presentaron una persistencia sensiblemente superior. En un reciente estudio realizado con una metodología similar, los pacientes tratados con fesoterodina mostraron una mayor persistencia al tratamiento en comparación con solifenacina y tolterodina (40,2 vs. 34,7 y 33,6%, respectivamente; p=0,008)31. Martan et al.32, en un reciente estudio prospectivo realizado con 206 pacientes, observaron que la persistencia a los 6 meses con mirabegrón fue del 73%. Las causas de interrupción del tratamiento fueron: 43% por falta de eficacia, 53% por otras razones y 4% por efectos secundarios de carácter leve. Nuestros resultados son consistentes con la literatura revisada. Además, la variabilidad existente entre los resultados de los estudios revisados no permite establecer conclusiones relevantes; la posible relación entre efectos secundarios y persistencia al tratamiento parece ser un factor importante, pero no la única causa.
En nuestro estudio, los tratamientos con oxibutinina en comparación con mirabegrón se asociaron a unos menores costes (1.151,2 vs. 1.809,6€), especialmente por el precio de la medicación (diferencia: −413,1€). A nuestro entender, esta reducción de costes unitarios es importante desde un punto de vista de la eficiencia en la gestión clínica de este colectivo de pacientes dada la elevada prevalencia de la VH, aunque puede quedar desvirtuada por las mayores tasas de reacciones adversas (n=53 [9,7%] vs. n=36 [4,9%], respectivamente). En la literatura consultada no hemos encontrado ningún estudio comparativo del coste de la enfermedad entre estos 2 fármacos, seguramente por la existencia de otros medicamentos para la VH eficaces y por el poco tiempo de comercialización en nuestro país de mirabegrón. En estudios de evaluación económica, solifenacina parece ser más coste-efectiva que oxibutinina. Sin embargo, las diferencias entre los posibles escenarios de simulación alternativos, el gran número de abandonos, la gravedad clínica de los pacientes con VH y el riesgo de padecer reacciones adversas limita la generalización de los resultados. En algunos estudios se detalla que mirabegrón quizás es un medicamento menos efectivo en las personas mayores33,34. En general, el promedio anual del coste sanitario de los pacientes en tratamiento con oxibutinina es relativamente bajo, mientras que con mirabegrón es más elevado. A nuestro entender, la medicación concomitante puede ser un factor adicional, pero el más destacado es el coste del medicamento17,18. En cuanto a las reacciones adversas, nuestros resultados son consistentes con la bibliografía consultada34,35.
Las posibles limitaciones del estudio inciden en las propias de los estudios retrospectivos, como por ejemplo, el infrarregistro de la enfermedad/reacciones adversas o la posible variabilidad de los profesionales y de los pacientes al ser un diseño observacional. En este aspecto, la posible inexactitud de la codificación diagnóstica en cuanto al diagnóstico y otras comorbilidades, o bien la falta de alguna variable que pudiera influir en los resultados finales (eficacia del fármaco, nivel socioeconómico de los pacientes, exposición al trabajo, evolución de la dosis farmacológica prescrita, tipo de empleo, variabilidad en el uso de los recursos, exposición a otros medicamentos para la VH, etc.) deben considerarse como una limitación del estudio. También es importante considerar que el muestreo de los centros no ha sido aleatorio, sino por conveniencia (disponibilidad de los registros), y esto puede plantear un sesgo de selección y de información en los resultados. Además, oxibutinina es un medicamento utilizado mayoritariamente en el periodo de inclusión inicial (comercialización en 2005), mientras que mirabegrón lo fue en el periodo final (comercialización en 2014), circunstancia que podría ocasionar un sesgo de clasificación de carácter temporal, aunque a nuestro entender (por el diseño y la comparabilidad de los grupos), este aspecto no debería interferir en la persistencia al tratamiento y/o en la tasa de efectos adversos obtenida de los 2 fármacos evaluados (18 centros participantes). La principal limitación del estudio debe considerarse la generalización de los resultados (validez externa) por el tipo de diseño empleado.
Según la bibliografía, mirabegrón es el primero de una nueva clase de medicamentos con un nuevo mecanismo de acción, diferente al de los antimuscarínicos. Es eficaz y bien tolerado. Los estudios sobre su uso combinado con otros anticolinérgicos están en curso. Debido a su elevado coste, el lugar selectivo frente a los medicamentos para la VH actuales está aún por averiguar36,37. Las perspectivas futuras que nos ofrece este estudio se centran en replicarlo en otras instituciones sanitarias y en promover análisis a largo plazo para conocer el lugar que le corresponde desde una perspectiva coste-efectiva (colectivos específicos de pacientes).
ConclusionesLa falta de adherencia a este tipo de medicamentos es un problema de elevada magnitud. En conclusión, a pesar de las limitaciones del estudio, los pacientes en tratamiento con oxibutinina frente a mirabegrón para la VH se asociaron a una similar persistencia al tratamiento, unos menores costes sanitarios y unas mayores tasas de reacciones adversas a medicamentos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
AutoríaLa concepción y el diseño del manuscrito fueron realizados por A. Sicras-Mainar; la recogida de los datos, por A. Sicras-Mainar, M. Saez y L. Sánchez; y el análisis estadístico, por A. Sicras-Mainar. La interpretación de los datos, la redacción, la revisión y la aprobación del manuscrito remitido se llevó a cabo por todos los autores.
Conflicto de interesesEl estudio fue patrocinado por Pfizer. A. Sicras-Mainar es un consultor independiente en relación con el desarrollo de este manuscrito y que colabora con Pfizer. Los demás autores declaran no tener conflictos de intereses.