El objetivo de este documento es mostrar en detalle el posicionamiento de la Societat Catalana de Digestologia acerca de la fiabilidad y utilidad de la elastografía en el diagnóstico no invasivo de la fibrosis hepática. El documento ha sido elaborado por un grupo de expertos en enfermedades crónicas del hígado y en trasplante hepático. Se muestra el consenso alcanzado sobre la metodología e indicaciones de la elastografía transitoria. Dicho documento ha sido revisado y presentado de forma abreviada en el XX Congrés de la Societat Catalana de Digestologia y se ha incluido en la página web http://www.scdigestologia.org/index.php?link=docs_posicio
This document provides a detailed description of the position of the Catalan Society of Gastroenterology on the accuracy and utility of elastography in the non-invasive diagnosis of liver fibrosis. The document was written by a group of experts in chronic liver diseases and liver transplantation and reflects the consensus reached on the methodology and indications of transient elastography. This document was reviewed and presented in an abbreviated form at the XX Congress of the Catalan Society of Gastroenterology and included on the website http://www.scdigestologia.org/index.php?link=docs_posicio
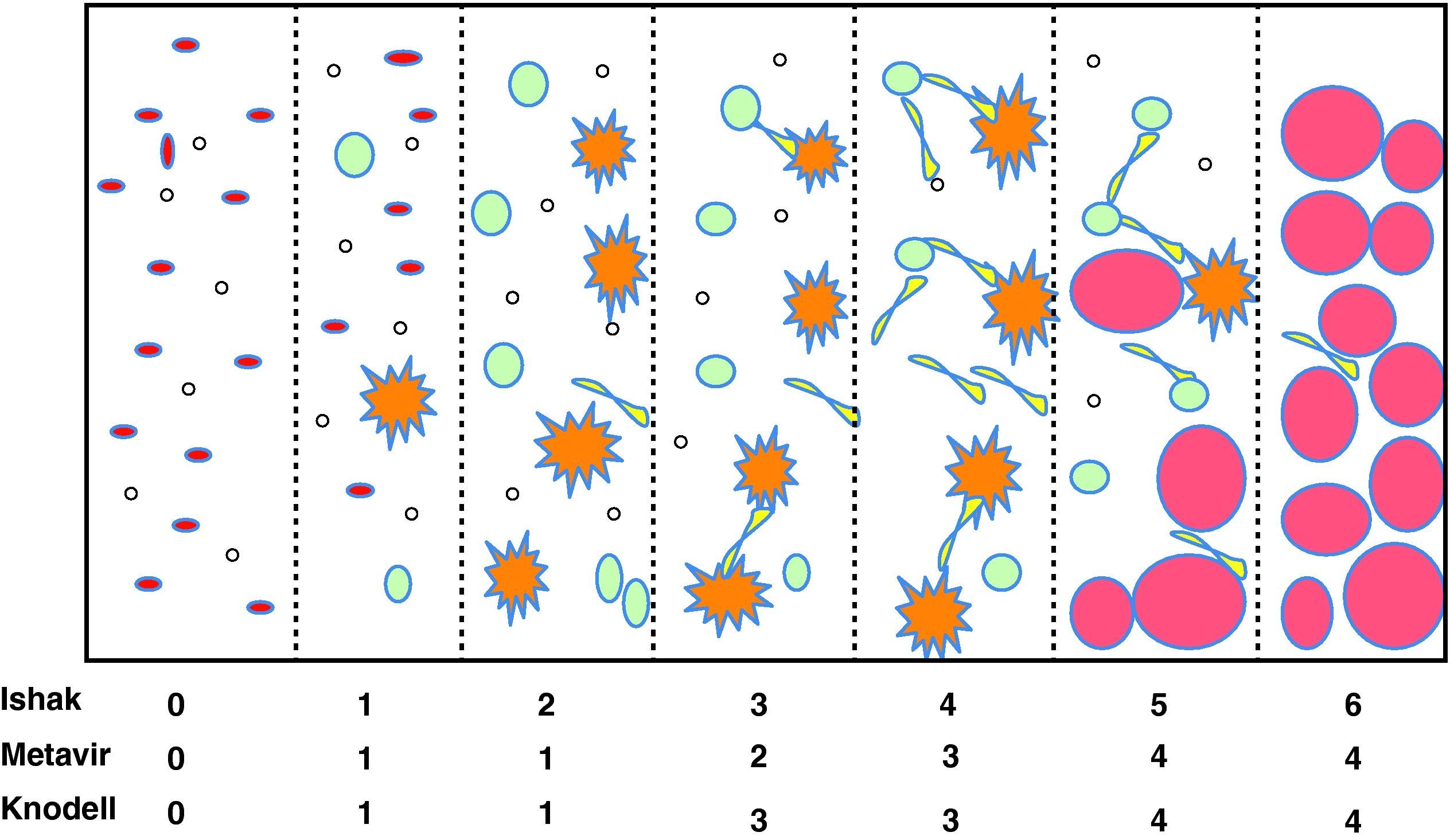
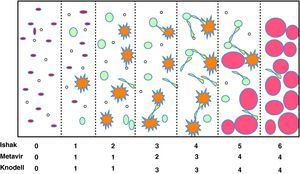
La biopsia hepática ha sido y sigue siendo una herramienta fundamental en el diagnóstico y pronóstico de las enfermedades del hígado1. La biopsia permite no solo llegar a un diagnóstico histológico, sino también excluir otras enfermedades y evaluar el grado de lesión (inflamación, fibrosis, esteatosis). La fibrosis hepática es, sin duda, la variable que más impacto tiene en el pronóstico de las enfermedades crónicas del hígado, ya sea de etiología viral (hepatitis crónica B y C) o provocada por otras causas (alcohol, enfermedades autoinmunes, metabólicas o colestásicas). La cuantificación de la fibrosis en la biopsia hepática se ha utilizado de forma frecuente para decidir el inicio del tratamiento, particularmente en las hepatitis crónicas B y C (fig. 1)2. Así pues, la presencia de una fibrosis que supera el espacio porta (F=2 según la escala METAVIR o F=3 según la escala de Ishak) se considera fibrosis significativa y, por tanto, tributaria de una intervención terapéutica (que en el caso de las hepatitis virales constituye el inicio del tratamiento antiviral).
Clasificación de la fibrosis. Adaptado de Goodman ZD et al.2
La evaluación de la fibrosis en la biopsia es semicuantitativa y controvertida por diferentes motivos. La principal razón es que el fragmento de tejido que se obtiene es muy pequeño y solo representa 1/50.000 partes del hígado. Por ello, es muy frecuente que la evaluación cuantitativa de la fibrosis sea inexacta, pudiendo clasificar de manera errónea hasta el 25% de las biopsias debido al error de muestra3. Por otra parte, la cuantificación de la fibrosis en estadios depende de la clasificación utilizada. Las clasificaciones más complejas (Ishak) pueden identificar estadios intermedios no recogidos en clasificaciones más simples (Knodell o METAVIR) haciendo difícil comparar los estudios que no utilicen una misma clasificación (fig. 1)2. Además, en aquellos casos en los que una segunda biopsia demuestra un incremento de la fibrosis, ni la cantidad de la fibra ni las consecuencias clínicas son proporcionales si comparamos los cambios que se producen entre estadios iniciales (de F0 a F1) o finales (de F3 a F4). Sin duda, la limitación más importante de la biopsia hepática es que se trata de una técnica invasiva asociada a un cierto grado de morbimortalidad. El dolor después del procedimiento es muy habitual (hasta el 80% de los pacientes) y, aunque con poca frecuencia, a veces se asocia a complicaciones graves como hematomas (1/500 casos) o hemoperitoneo (1/2.500 casos) e incluso el fallecimiento (1/10.000 casos)1.
Estos aspectos han hecho que en estos últimos 10 años se hayan dedicado esfuerzos significativos a evaluar alternativas no invasivas para identificar la cantidad de la fibrosis y evitar la biopsia hepática4. Las técnicas como la ecografía o la tomografía computarizada únicamente pueden distinguir entre formas muy avanzadas de la enfermedad (cirrosis o F4) y el resto de estadios evolutivos. Los marcadores serológicos relacionados (directos) o no (indirectos) con el proceso de fibrogénesis han demostrado una capacidad aceptable para diferenciar pacientes con fibrosis significativa (F2-F4) de aquellos con ausencia o presencia de mínima fibrosis (F0-F1) (tabla 1). La cifra de plaquetas, la gammaglutamil transpeptidasa, las transaminasas, los valores de colesterol, la macroglobulina, la haptoglobina, los productos de degradación del colágeno y algunas enzimas encargadas de su degradación como las metaloproteinasas y sus inhibidores tisulares son algunos ejemplos.
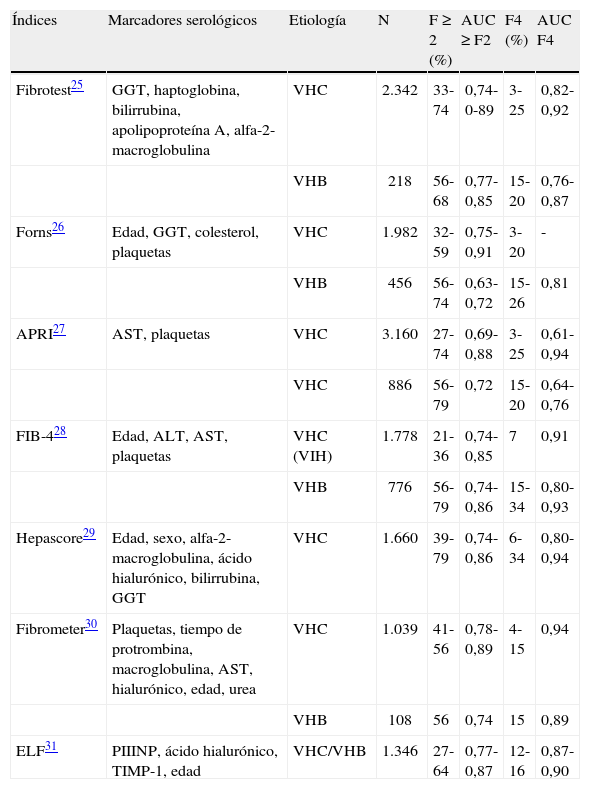
Eficacia diagnóstica de los principales índices basados en marcadores serológicos para identificar fibrosis significativa o cirrosis en pacientes con hepatitis crónica B o C
| Índices | Marcadores serológicos | Etiología | N | F ≥ 2 (%) | AUC ≥ F2 | F4 (%) | AUC F4 |
| Fibrotest25 | GGT, haptoglobina, bilirrubina, apolipoproteína A, alfa-2-macroglobulina | VHC | 2.342 | 33-74 | 0,74-0-89 | 3-25 | 0,82-0,92 |
| VHB | 218 | 56-68 | 0,77-0,85 | 15-20 | 0,76-0,87 | ||
| Forns26 | Edad, GGT, colesterol, plaquetas | VHC | 1.982 | 32-59 | 0,75-0,91 | 3-20 | - |
| VHB | 456 | 56-74 | 0,63-0,72 | 15-26 | 0,81 | ||
| APRI27 | AST, plaquetas | VHC | 3.160 | 27-74 | 0,69-0,88 | 3-25 | 0,61-0,94 |
| VHC | 886 | 56-79 | 0,72 | 15-20 | 0,64-0,76 | ||
| FIB-428 | Edad, ALT, AST, plaquetas | VHC (VIH) | 1.778 | 21-36 | 0,74-0,85 | 7 | 0,91 |
| VHB | 776 | 56-79 | 0,74-0,86 | 15-34 | 0,80-0,93 | ||
| Hepascore29 | Edad, sexo, alfa-2-macroglobulina, ácido hialurónico, bilirrubina, GGT | VHC | 1.660 | 39-79 | 0,74-0,86 | 6-34 | 0,80-0,94 |
| Fibrometer30 | Plaquetas, tiempo de protrombina, macroglobulina, AST, hialurónico, edad, urea | VHC | 1.039 | 41-56 | 0,78-0,89 | 4-15 | 0,94 |
| VHB | 108 | 56 | 0,74 | 15 | 0,89 | ||
| ELF31 | PIIINP, ácido hialurónico, TIMP-1, edad | VHC/VHB | 1.346 | 27-64 | 0,77-0,87 | 12-16 | 0,87-0,90 |
ALT: alanino aminotransferasa; AST: aspartato aminotransferasa; AUC: área bajo la curva; GGT: gammaglutamil transpeptidasa; N: número de pacientes; PIIINP: propéptido N-terminal del colágeno tipo III; TIMP-1: inhibidor tisular de metaloproteinasas-1; VHB: virus de la hepatitis B; VHC: virus de la hepatitis C; VIH: virus de la inmunodeficiencia humana.
Adaptada de Martínez S et al14.
Además de los métodos serológicos, en los últimos 5 años se ha desarrollado una nueva técnica basada en la evaluación de la elasticidad hepática llamada elastografía transitoria (FibroScan®)5. Esta técnica se basa en la medición de la elasticidad del tejido por ultrasonidos, midiendo la velocidad de propagación de una onda mecánica dentro del parénquima hepático. La elastografía ha demostrado una excelente capacidad para excluir la cirrosis y buena para identificar a los pacientes con diferentes estadios de fibrosis. La gran mayoría de estudios se han realizado en pacientes con hepatitis crónica (especialmente con hepatitis crónica C), pero también se dispone de información en hepatitis B, enfermedades hepáticas colestásicas, por consumo de alcohol, esteatohepatitis no alcohólica y hepatitis C postrasplante (tabla 2).
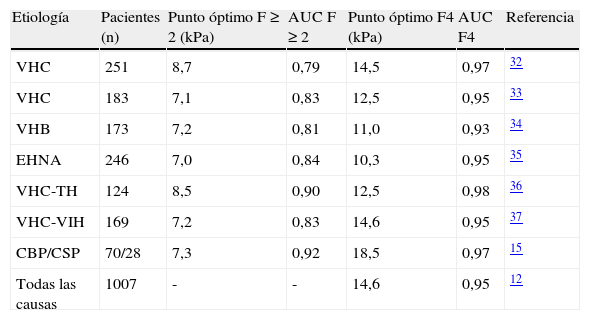
Eficacia diagnóstica del FibroScan® en diferentes enfermedades hepáticas
| Etiología | Pacientes (n) | Punto óptimo F≥2 (kPa) | AUC F≥2 | Punto óptimo F4 (kPa) | AUC F4 | Referencia |
| VHC | 251 | 8,7 | 0,79 | 14,5 | 0,97 | 32 |
| VHC | 183 | 7,1 | 0,83 | 12,5 | 0,95 | 33 |
| VHB | 173 | 7,2 | 0,81 | 11,0 | 0,93 | 34 |
| EHNA | 246 | 7,0 | 0,84 | 10,3 | 0,95 | 35 |
| VHC-TH | 124 | 8,5 | 0,90 | 12,5 | 0,98 | 36 |
| VHC-VIH | 169 | 7,2 | 0,83 | 14,6 | 0,95 | 37 |
| CBP/CSP | 70/28 | 7,3 | 0,92 | 18,5 | 0,97 | 15 |
| Todas las causas | 1007 | - | - | 14,6 | 0,95 | 12 |
AUC: área bajo la curva; CBP: cirrosis biliar primaria; CSP: colangitis esclerosante primaria; EHNA: esteatosis hepática no alcohólica; TH: trasplante hepático; VHB: virus de la hepatitis B; VHC: virus de la hepatitis C, VIH: virus de la inmunodeficiencia humana.
Queda claro que la sustitución de la biopsia hepática por métodos no invasivos es un objetivo del todo recomendable. Los pacientes prefieren no someterse a un procedimiento cruento como la biopsia, y desde el punto de vista del coste económico, a pesar de la inversión inicial que conlleva la compra de este aparato, su uso en manos expertas permite amortizar este gasto muy rápidamente. La medicina del siglo xxi va encaminada no solo a incrementar la eficacia terapéutica, sino a mejorar la calidad de vida de los pacientes. Es obvio que la utilización de pruebas menos invasivas, más rápidas, fáciles de realizar y con una buena sensibilidad y especificidad es muy recomendable.
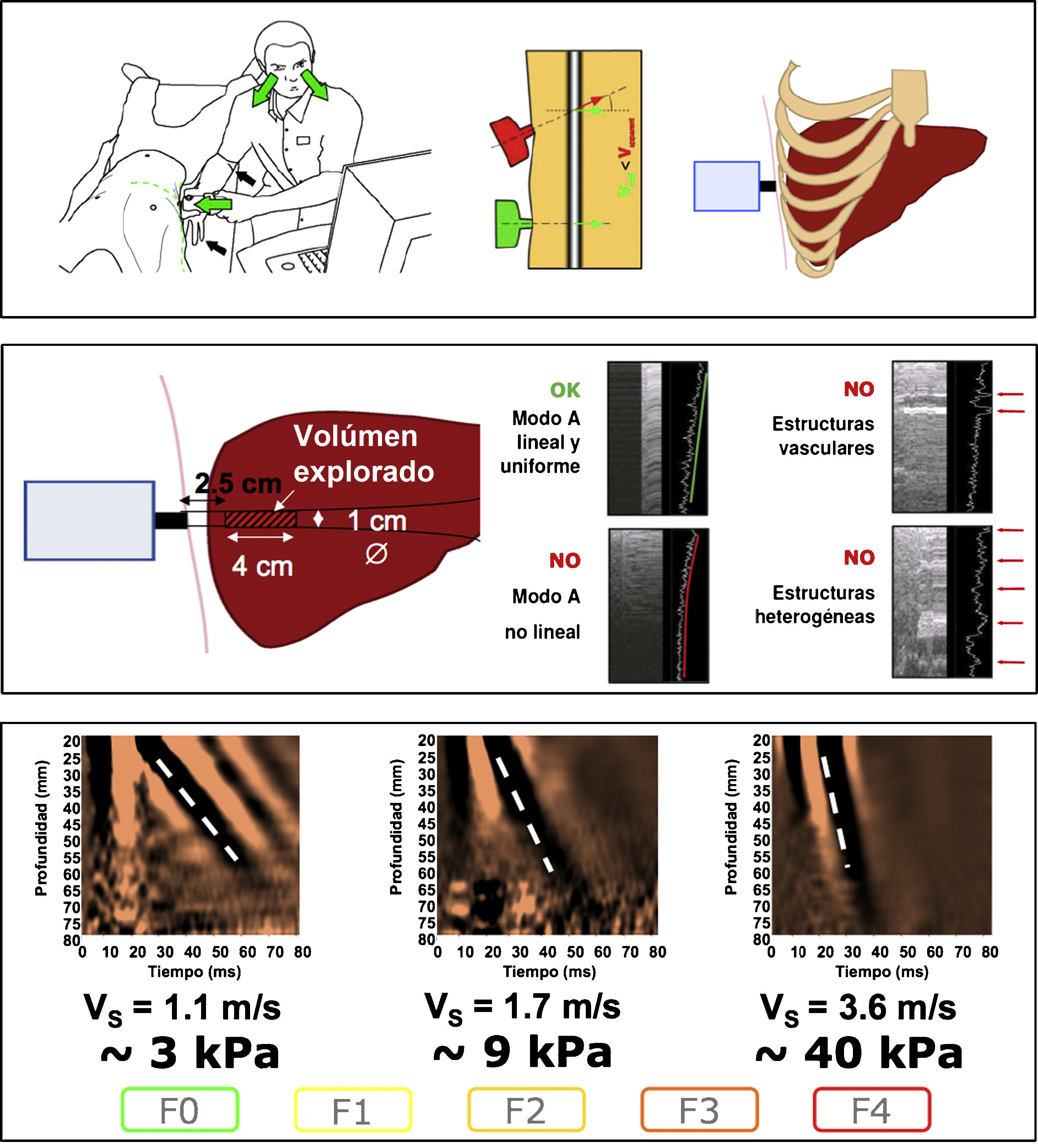
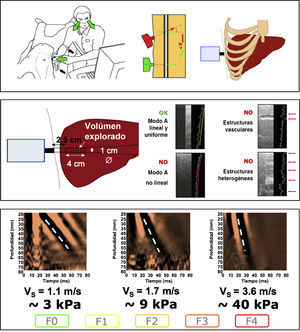
Características técnicasLa técnica es muy sencilla6. El aparato dispone de una sonda emisor-receptor que se coloca entre las costillas a la altura del hígado y que emite una onda mecánica corta de baja frecuencia. Esta onda de vibración se transmite dentro del parénquima hepático a una velocidad que depende de la rigidez del tejido, siendo más rápida cuanto más rígido es el tejido. La velocidad es detectada mediante ultrasonografía por la misma sonda y el software del aparato transforma la velocidad (m/s) en un valor de elasticidad (kilopascales o kPa). El volumen de tejido evaluado es un cilindro de aproximadamente 1cm de ancho y 4cm de longitud que se localiza entre 25 y 65mm por debajo de la piel (dentro del hígado) y es cien veces superior al volumen evaluado con una biopsia (fig. 2).
Valores obtenidosEl rango de valores de elasticidad que puede detectar el FibroScan® va desde 2,5 a 75kPa y los valores en individuos sin enfermedad hepática están alrededor de 5,5kPa. Para obtener un valor fiable de elasticidad hepática se deben realizar 10 mediciones válidas. El valor que resulta de calcular la mediana de las 10 determinaciones es el que se utiliza para establecer la rigidez (R) del hígado que es proporcional al grado o estadio de fibrosis. Es importante remarcar que el rango intercuartílico o RIQ (es decir, la diferencia entre el percentil 25 y 75 de las exploraciones realizadas) nos da una buena idea acerca de la dispersión de los valores y, por tanto, cuanto menor sea la dispersión más representativa será la mediana respecto al total de las determinaciones. Se recomienda que este RIQ sea inferior al 30% del valor mediano (R), es decir, que la proporción RIQ/R sea inferior a 0,3 o, lo que es lo mismo, que exista poca dispersión en el conjunto de valores obtenidos. También es importante el porcentaje de medidas válidas respecto al total realizadas (ratio). Se recomienda que esta ratio sea superior al 60%, esto es, que se obtenga al menos 6 determinaciones válidas.
Metodología y curva de aprendizajeEl aprendizaje es sencillo, pero hay aspectos técnicos como el posicionamiento de la sonda y la correcta interpretación de los valores artefactuados que requieren más experiencia. Desde el punto de vista técnico puede ser difícil obtener registros en pacientes con espacios intercostales pequeños o con obesidad (porque el tejido subcutáneo desplaza el hígado por debajo de la onda emitida por la sonda). Por otra parte, el registro no será posible en pacientes con ascitis y puede quedar artefactuado por cualquier proceso que incremente o atenúe la consistencia del hígado5.
El número de exploraciones requeridas para obtener resultados reproducibles y con valores aceptables de ratio y RIQ es en torno a 100-500 exploraciones7, dependiendo de la destreza de la persona que la realiza. Es esperable que los valores ratio y RIQ mejoren con la curva de aprendizaje. Además, se recomienda que el valor de rigidez, la ratio y el RIQ sean interpretados en el contexto de la enfermedad por un facultativo con experiencia y conocimientos de las características y limitaciones de la técnica.
Factores que se deben considerar y limitacionesLos factores que se han relacionado con la ausencia de registro son un índice de masa corporal elevado (IMC>30kg/m2) y la falta de experiencia del explorador7. Los factores que se asocian a un aumento de la rigidez del hígado son la necrosis hepatocelular elevada en el caso de pacientes con hepatitis aguda severa8, la congestión venosa por insuficiencia cardiaca9 y la dilatación de las vías biliares10. Los factores asociados a atenuación de la onda de transmisión son una esteatosis hepatocelular elevada11 y la presencia de cirrosis macronodular12.
Por todo ello, es recomendable repetir la exploración en los casos en que se obtengan valores de rigidez, ratio o RIQ subóptimos y es deseable utilizar otro método no invasivo o realizar una biopsia hepática en los casos con resultados incongruentes.
Indicaciones y recomendacionesLa indicación más aceptada del FibroScan® es básicamente la evaluación del estadio de fibrosis en las enfermedades crónicas del hígado6,13,14. La técnica permite identificar con una buena fiabilidad aquellos pacientes con formas más avanzadas de la enfermedad (F2-F4) y, particularmente, la presencia de cirrosis hepática (F4) (tabla 2). Dado que la gran mayoría de datos han sido generados en pacientes con hepatitis crónica C, su utilidad está bien establecida en esta enfermedad. Pese a que el número de estudios en otras enfermedades es más pequeño, la realización del FibroScan® para identificar fibrosis avanzada o cirrosis en enfermedades colestásicas crónicas (cirrosis biliar primaria)15 o en la recurrencia de la hepatitis C postrasplante hepático está también aceptada16. A título de ejemplo, el Sistema de Salud Francés considera el FibroScan® como una herramienta diagnóstica en estas indicaciones y, de hecho, financia el coste derivado de su utilización.
Hay menos consenso en las indicaciones para otras enfermedades como la hepatopatía alcohólica, la esteatohepatitis no alcohólica o la hepatitis B debido a que son enfermedades en las que pueden coexistir otros factores (además de la fibrosis) que pueden modificar la consistencia del hígado o atenuar la transmisión mecánica de la onda. Así, en estas enfermedades la elevación de las transaminasas, la presencia de esteatosis o necrosis17, la diferente distribución de la fibrosis y la presencia de macronódulos18 hacen más compleja la interpretación de los valores de rigidez hepática y su relación con el grado de fibrosis. Respecto a los valores diagnósticos, como hemos comentado anteriormente, los individuos sin enfermedad hepática tienen valores alrededor de 5,5kPa. A pesar de que pueden existir pequeñas variaciones según la etiología de la enfermedad, los metanálisis más recientes y los estudios más extensos indican un valor de 7,6kPa y de 14,6kPa como los óptimos para identificar fibrosis significativa y cirrosis, respectivamente12,19. Aparte de la capacidad para identificar la fibrosis avanzada, también se ha demostrado una buena correlación entre el valor de elasticidad (en kPa) y la presión portal (en mmHg), al menos para valores inferiores a 12mmHg. Por tanto, con esta técnica no solo se identifica la presencia de cirrhosis, sino también la de hipertensión portal20. Por otro lado, la posibilidad de repetir la exploración tantas veces como queramos nos puede permitir identificar precozmente aquellos pacientes con progresión de la enfermedad y con mayor riesgo de descompensación. Sin embargo, aún se requieren más estudios prospectivos para conocer la capacidad de la técnica a la hora de identificar los diferentes estadios de la cirrosis y el riesgo de desarrollar varices esofágicas, descompensación clínica o carcinoma hepatocelular21,22.
Análisis de costesEl coste del aparato es de unos 60.000 euros, al que hay que añadir el derivado del mantenimiento anual de la sonda de unos 2.000 euros/año. El coste de una biopsia hepática es de unos 300 euros (rango mínimo), por lo que son necesarias unas 200 exploraciones para amortizar la inversión inicial. El hecho de que la prueba se pueda realizar por una enfermera en consultas externas es importante, dado que permite una fácil implementación pues no requiere un personal adicional para su realización.
Comparación con otras técnicas no invasivasLa capacidad de la elastografía transitoria para identificar fibrosis significativa (F2-F4) es similar a la de los métodos basados en índices serológicos (tablas 1 y 2). En cambio, el FibroScan® ha mostrado una extraordinaria sensibilidad y especificidad para identificar la presencia de cirrosis (F4)12. Entre las grandes ventajas de la elastografía transitoria están su rapidez (se puede obtener el resultado en unos 5 minutos), la facilidad de su uso y su reproducibilidad como han demostrado estudios en los que 2 exploradores realizaban la técnica por duplicado23. Como todos los métodos no invasivos, se puede repetir tantas veces como sea necesario y, por lo tanto, resulta muy útil para el seguimiento de los pacientes en la consulta externa. Un dato que se debe tener en cuenta es que al utilizar ultrasonidos como método de medición de la onda mecánica podría ser utilizada en mujeres embarazadas sin que ello suponga un riesgo ni para el feto ni para la madre24.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.