Conocer la duración y los motivos de cambio de las distintas combinaciones de fármacos utilizadas como inicio del tratamiento antirretroviral en pacientes naive.
MétodosEstudio observacional y retrospectivo en el que se incluyeron todos los pacientes con infección por VIH que iniciaron tratamiento antirretroviral en un hospital universitario de referencia de alta tecnología durante el periodo comprendido entre el 1 de enero de 2003 y el 31 de diciembre de 2005. El seguimiento se realizó hasta el 31 de diciembre de 2008. Para estimar la probabilidad acumulada de interrupción del tratamiento se utilizó el método de Kaplan-Meier.
ResultadosSe incluyeron un total de 441 pacientes. La mediana de duración del primer tratamiento fue de 384 (intervalo intercuartil 84–1.290) días. Los regímenes basados en inhibidores de la transcriptasa inversa no análogos de nucleósidos y aquellos que incluían como análogos de nucleósidos abacavir o tenofovir en combinación con lamivudina o emtricitabina presentaron una duración significativamente mayor que el resto. Los principales motivos de finalización fueron las reacciones adversas aunque en un porcentaje menor que el obtenido en estudios anteriores. No se hallaron asociaciones entre el resto de características de los pacientes o del tratamiento y el riesgo de interrupción.
DiscusiónAunque la duración del primer tratamiento antirretroviral sigue siendo corta, actualmente se producen menos cambios por reacciones adversas y por pérdidas de seguimiento. Los motivos podrían ser una mejor tolerancia y una menor complejidad. No obstante, son necesarios más estudios para determinar el beneficio de un régimen frente a otro y poder generalizar estos resultados.
To determine the duration of and reasons behind changing the various combinations of drugs used for the initiation of antiretroviral treatment in naïve patients.
MethodsA retrospective observational study that included all patients with HIV infection who started antiretroviral therapy in a high-tech university reference hospital during the period from 1 January 2003 and 31 December 2005. Patients were followed until 31 December 2008. To estimate the cumulative probability of discontinuation the Kaplan-Meier method was used.
ResultsA total of 441 patients were included. The average duration of the first treatment was 384 (interquartile interval 84–1290) days. The regimen based on non-nucleoside reverse transcriptase inhibitors and those that included as nucleosides abacavir or tenofovir in combination with lamivudine or emtricitabine showed a significantly longer duration than the rest. The main reasons for termination were the side effects, although in a lesser percentage than that obtained in previous studies. No associations were found between the rest of the characteristics of the patients or of the treatment and the risk of termination.
DiscussionAlthough the duration of the first antiretroviral treatment remains short, currently fewer changes are made due to side effects and due to loss to follow-up. The reasons may be better tolerance and less complexity. However, more studies are needed to determine the benefits of one regimen or another, and to be able to generalise the results.
La introducción, a mediados de los años 90, de los inhibidores de la proteasa y, con ellos, del tratamiento antirretroviral de gran actividad (TARGA), provocó un gran cambio en la evolución de la infección por el VIH1,2. Desde entonces, prácticamente cada año han ido apareciendo nuevos fármacos antirretrovirales. En el año 2009 disponemos de 27 medicamentos comercializados además de varias moléculas en investigación.
El tratamiento de la infección por el VIH se basa en combinaciones de tres fármacos. Con ello se pretende conseguir una supresión viral máxima durante el mayor periodo de tiempo posible, restablecer o conservar la función inmunológica, mejorar la calidad de vida y reducir la morbilidad y la mortalidad relacionadas con el VIH3,4.
El número de fármacos antirretrovirales disponibles actualmente permite realizar múltiples combinaciones de tratamiento. A la hora de seleccionar el tratamiento, como muchas de estas combinaciones tienen una eficacia similar, es necesario valorar otros aspectos como el número de comprimidos, la frecuencia de administración, la aparición de reacciones adversas, la adherencia a los tratamientos previos, las interacciones farmacológicas, el coste y las recomendaciones vigentes cuando se realiza la prescripción5.
La disponibilidad de un número elevado de fármacos antirretrovirales junto con las rápidas modificaciones derivadas de los nuevos estudios hace que el tratamiento de las personas con infección por VIH sea complejo y sujeto a numerosos cambios.
A causa de la cronicidad de la enfermedad, prolongar la duración de estos tratamientos es uno de los objetivos principales, por ello, es importante conocer la duración de las distintas pautas y las causas que motivan su cambio.
Varios estudios han estimado la duración de la primera combinación de TARGA, sin embargo, la mayoría de ellos han sido realizados entre 1996 y 20006–9. Posteriormente, los inhibidores de la transcriptasa inversa análogos de nucleósidos/nucleótidos (ITIAN) que más se utilizaban en esa época, zidovudina (AZT), didanosina (ddI) y estavudina (d4T), han sido reemplazados por tenofovir (TDF) y abacavir (ABC), por presentar una menor toxicidad10–12.
El objetivo principal de este estudio es conocer en la actualidad la duración de las distintas combinaciones de fármacos utilizadas como inicio del tratamiento antirretroviral en pacientes naive. Como objetivo secundario se pretende conocer cuáles son los motivos más frecuentes de cambio de la primera combinación de tratamiento.
MétodoEstudio observacional y retrospectivo en el que se incluyeron todos los pacientes con infección por VIH que iniciaron tratamiento antirretroviral en un hospital universitario de referencia de alta tecnología durante el periodo comprendido entre el 1 de enero de 2003 y el 31 de diciembre de 2005. Se excluyeron del estudio los pacientes que iniciaron el tratamiento dentro de ensayos clínicos con fármacos no comercializados o con indicaciones no aprobadas. El seguimiento se realizó hasta el 31 de diciembre de 2008.
Las variables de resultado primarias fueron el porcentaje de pacientes que interrumpieron el tratamiento y la mediana de duración de las distintas combinaciones de fármacos hasta su interrupción.
Se definió la interrupción del tratamiento como el cese de la terapia por sustitución o por interrupción de alguno de los fármacos o de la terapia completa, tanto si fue por orden facultativa como por iniciativa propia del paciente. Los pacientes que no acudieron a las visitas médicas durante un periodo superior a 6 meses se consideraron pérdidas de seguimiento.
Las variables se obtuvieron de forma retrospectiva mediante la revisión de la historia clínica informatizada y de los registros de la unidad de farmacia ambulatoria. Se incluyeron las principales variables sociodemográficas (edad, sexo) y relacionadas con la enfermedad y su tratamiento (vía de transmisión de la enfermedad, co-infección VHC y/o VHB, fecha de inicio y de finalización del tratamiento antirretroviral) así como los parámetros basales de carga viral y linfocitos CD4.
Las diferentes combinaciones se clasificaron en regímenes basados únicamente en ITIAN, regímenes basados en inhibidores de la transcriptasa inversa no análogos de nucleósidos (ITINN) y regímenes basados en inhibidores de la proteasa (IP).
Los ITIAN utilizados dentro de cada régimen se asignaron a 3 grupos: combinaciones que incluían ddI o d4T, combinaciones que incluían AZT y combinaciones que incluían ABC o TDF. Si el régimen contenía ITIAN de más de un grupo (ej. ddI y AZT), el régimen se asignó utilizando la siguiente jerarquía: ddI o d4T, después AZT y finalmente, ABC o TDF.
El cambio de los fármacos comercializados de forma individual a los mismos fármacos en una combinación a dosis fija no se consideró como cambio de tratamiento. Tampoco se consideró cambio el paso de lamivudina (3TC) a emtricitabina (FTC) por considerarse equivalentes terapéuticos.
Respecto al análisis estadístico, se realizó un análisis descriptivo de las características de la población estudiada, el porcentaje de interrupciones y sus causas. Para estudiar la influencia de las diferentes variables en la duración del TARGA se utilizaron modelos de regresión de Cox y para estimar la probabilidad acumulada de interrupción del tratamiento a lo largo del tiempo de seguimiento se utilizó el método de Kaplan-Meier. Todos los análisis se realizaron con el programa SPSS versión 15.0.
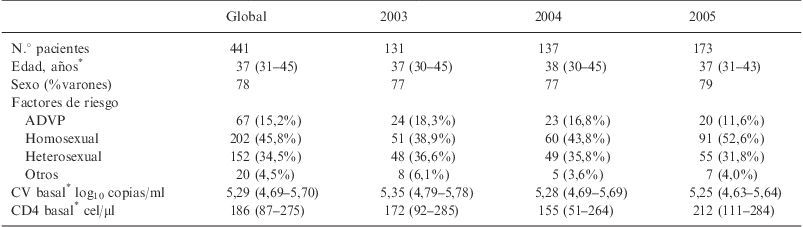
ResultadosSe incluyeron un total de 441 pacientes. De éstos, 131 iniciaron tratamiento en el 2003, 137 en el 2004 y 173 en el 2005. En la tabla 1 se muestran las características basales de esta población. El 78% de los pacientes fueron hombres y la mediana de edad fue de 37 (31–45) años. No se observaron diferencias estadísticamente significativas en estas variables durante los años estudiados. Teniendo en cuenta las distintas combinaciones de fármacos, la distribución por sexos fue similar a la global. La carga viral y el recuento de CD4 basales fueron, en mediana, de 5,06 log10 (4,69log10–5,70log10) copias/ml y 186 (87–275)células/μl, respectivamente. En cuanto a los factores de riesgo, casi la mitad de los pacientes eran homosexuales, un 35% eran heterosexuales y un 15% eran ex adictos a drogas por vía parenteral.
Características basales de la población estudiada
| Global | 2003 | 2004 | 2005 | |
| N.° pacientes | 441 | 131 | 137 | 173 |
| Edad, años* | 37 (31–45) | 37 (30–45) | 38 (30–45) | 37 (31–43) |
| Sexo (%varones) | 78 | 77 | 77 | 79 |
| Factores de riesgo | ||||
| ADVP | 67 (15,2%) | 24 (18,3%) | 23 (16,8%) | 20 (11,6%) |
| Homosexual | 202 (45,8%) | 51 (38,9%) | 60 (43,8%) | 91 (52,6%) |
| Heterosexual | 152 (34,5%) | 48 (36,6%) | 49 (35,8%) | 55 (31,8%) |
| Otros | 20 (4,5%) | 8 (6,1%) | 5 (3,6%) | 7 (4,0%) |
| CV basal* log10 copias/ml | 5,29 (4,69–5,70) | 5,35 (4,79–5,78) | 5,28 (4,69–5,69) | 5,25 (4,63–5,64) |
| CD4 basal* cel/μl | 186 (87–275) | 172 (92–285) | 155 (51–264) | 212 (111–284) |
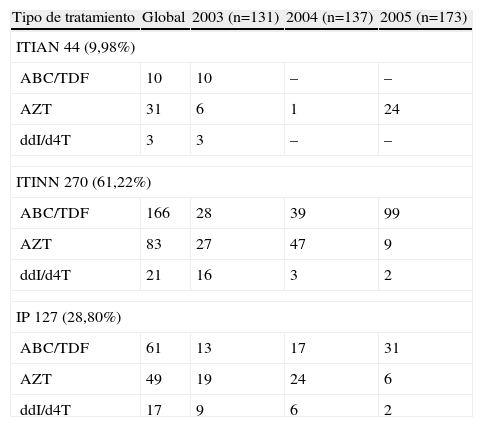
En la tabla 2 se pueden observar los esquemas de tratamiento más habituales como pauta de inicio. Respecto a los ITIAN, en un 53,7% se utilizaron como tratamiento de base regímenes que incluían ABC o TDF, seguido de AZT en un 37% y ddI o d4T en un 9,3%. Estos ITIAN generalmente se combinaron con 3TC o FTC (85% de los casos). Un 61% recibieron pautas basadas en ITINN y casi un 30% fueron basadas en IP. El ITINN más utilizado fue efavirenz (EFV), que supuso un 84,4% de los pacientes que utilizaron ITINN. El IP más utilizado fue lopinavir/ritonavir (LPV/r), en un 78,7% de los pacientes que utilizaron IP. La combinación más utilizada como pauta de inicio durante los años de estudio fue 3TC o FTC junto con TEN asociados a EFV (32%) seguido por la asociación de los mismos análogos junto con LPV/r (9%).
Combinaciones de tratamiento antirretroviral utilizadas como pauta de inicio
| Tipo de tratamiento | Global | 2003 (n=131) | 2004 (n=137) | 2005 (n=173) |
| ITIAN 44 (9,98%) | ||||
| ABC/TDF | 10 | 10 | – | – |
| AZT | 31 | 6 | 1 | 24 |
| ddI/d4T | 3 | 3 | – | – |
| ITINN 270 (61,22%) | ||||
| ABC/TDF | 166 | 28 | 39 | 99 |
| AZT | 83 | 27 | 47 | 9 |
| ddI/d4T | 21 | 16 | 3 | 2 |
| IP 127 (28,80%) | ||||
| ABC/TDF | 61 | 13 | 17 | 31 |
| AZT | 49 | 19 | 24 | 6 |
| ddI/d4T | 17 | 9 | 6 | 2 |
ABC/TDF: regímenes que incluyen como análogos abacavir o tenofovir; AZT: regímenes que incluyen como análogo zidovudina; ddI/d4T: regímenes que incluyen como análogos didanosina o estavudina; ITIAN: regímenes que sólo incluyen inhibidores de la transcriptasa inversa análogos de los nucleósidos; IP: regímenes basados en inhibidores de la proteasa; ITINN: regímenes basados en inhibidores de la transcriptasa inversa no análogos de los nucleósidos.
La mediana de duración global fue de 384 (rango intercuartil 84–1.290) días. Es decir, la probabilidad de continuar con el mismo tratamiento fue del 75% a los 84 días, del 50% a los 384 días y del 25% a los 1.290 días.
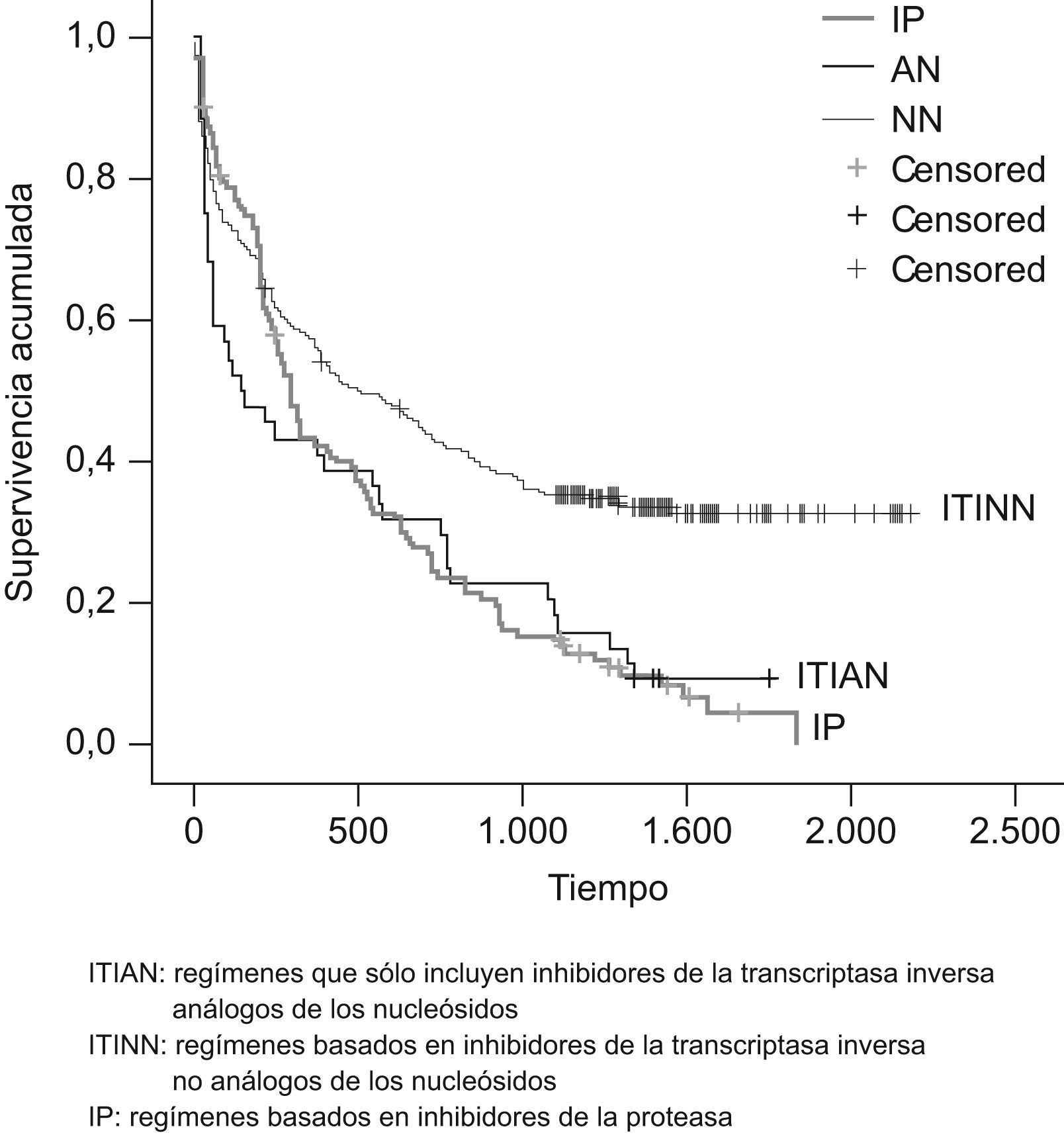
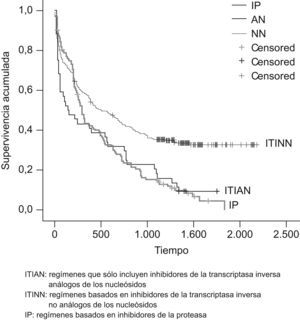
Al comparar la duración del tratamiento con las diferentes combinaciones de grupos farmacológicos (fig. 1), se observó que los regímenes basados en ITINN presentaban una mediana de duración significativamente mayor 501 días (84–.) que los regímenes basados en IP 286 días (152–722) o que sólo incluían ITIAN 137 días (31–766) (p<0,005). No se observaron diferencias estadísticamente significativas al comparar los regímenes basados en IP con las pautas que sólo incluían ITIAN.
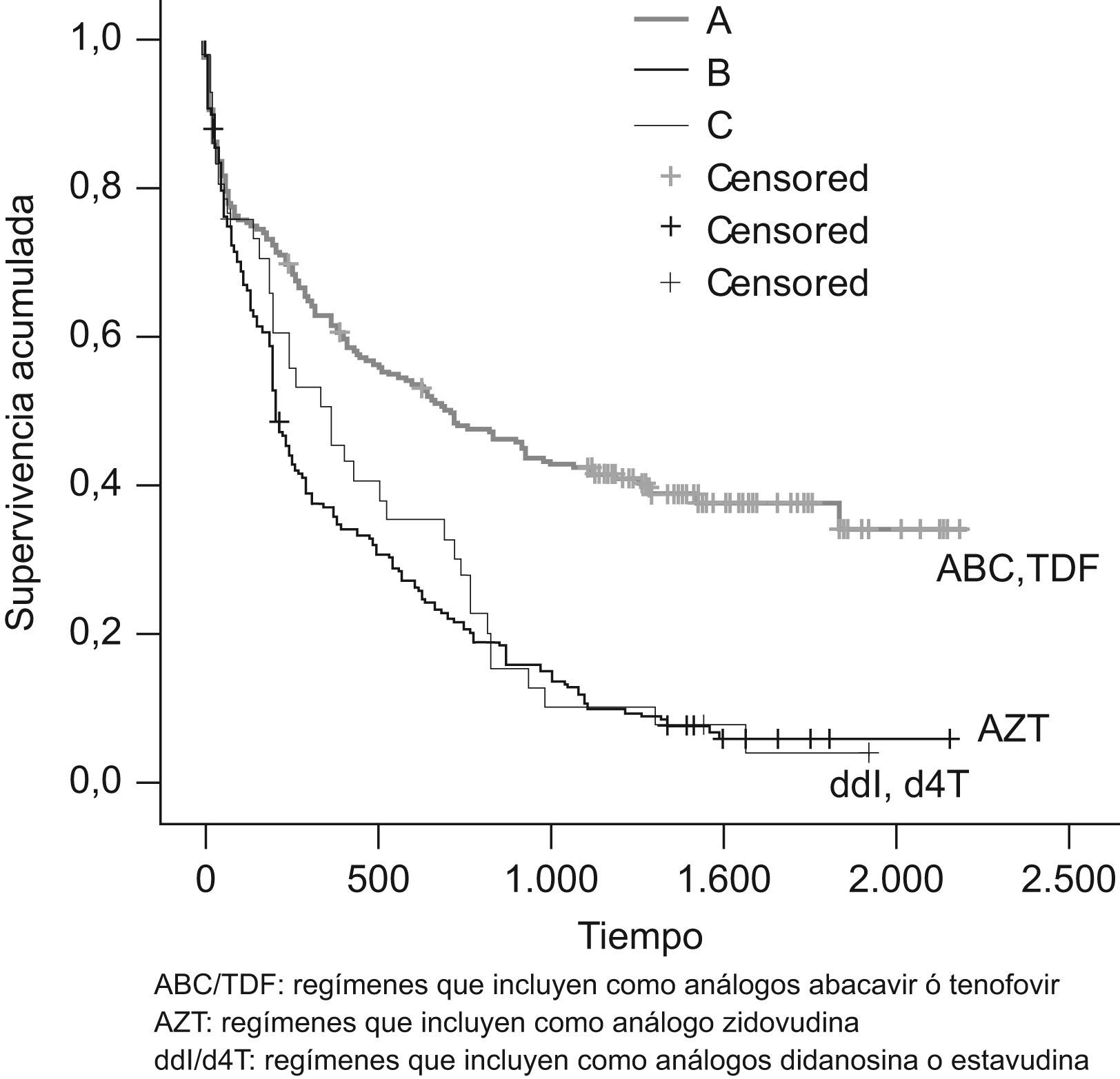
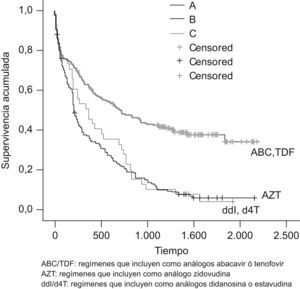
Por lo que hace referencia a los ITIAN utilizados (fig. 2), las combinaciones que incluían ABC o TDF presentaron una mayor duración 690 días (133–.) que las que incluían AZT 209 días (70–629), ddI o d4T 364 días (137–766) (p<0,005). Entre paréntesis se muestra el intervalo intercuartil. En dos casos únicamente se muestra un valor porque no había ningún caso en el primer cuartil. No se observaron diferencias estadísticamente significativas al comparar los regímenes que incluían AZT con los que incluían ddI o d4T.
No se observó una relación estadísticamente significativa entre la duración del tratamiento y el resto de variables estudiadas.
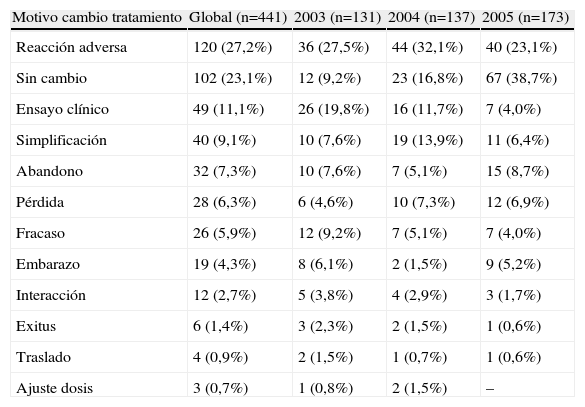
La tabla 3 resume los motivos de cambio del primer tratamiento antirretroviral. El principal motivo de cambio de tratamiento fueron las reacciones adversas, que causaron el cambio de una cuarta parte de los tratamientos iniciales. Un 7% de los pacientes abandonaron voluntariamente el tratamiento antirretroviral y un 6% fueron pérdidas de seguimiento. En un 6% el tratamiento no fue eficaz. Tan sólo una cuarta parte de los pacientes continuaban con el mismo tratamiento al final del estudio.
Motivo de finalización del primer tratamiento antirretroviral
| Motivo cambio tratamiento | Global (n=441) | 2003 (n=131) | 2004 (n=137) | 2005 (n=173) |
| Reacción adversa | 120 (27,2%) | 36 (27,5%) | 44 (32,1%) | 40 (23,1%) |
| Sin cambio | 102 (23,1%) | 12 (9,2%) | 23 (16,8%) | 67 (38,7%) |
| Ensayo clínico | 49 (11,1%) | 26 (19,8%) | 16 (11,7%) | 7 (4,0%) |
| Simplificación | 40 (9,1%) | 10 (7,6%) | 19 (13,9%) | 11 (6,4%) |
| Abandono | 32 (7,3%) | 10 (7,6%) | 7 (5,1%) | 15 (8,7%) |
| Pérdida | 28 (6,3%) | 6 (4,6%) | 10 (7,3%) | 12 (6,9%) |
| Fracaso | 26 (5,9%) | 12 (9,2%) | 7 (5,1%) | 7 (4,0%) |
| Embarazo | 19 (4,3%) | 8 (6,1%) | 2 (1,5%) | 9 (5,2%) |
| Interacción | 12 (2,7%) | 5 (3,8%) | 4 (2,9%) | 3 (1,7%) |
| Exitus | 6 (1,4%) | 3 (2,3%) | 2 (1,5%) | 1 (0,6%) |
| Traslado | 4 (0,9%) | 2 (1,5%) | 1 (0,7%) | 1 (0,6%) |
| Ajuste dosis | 3 (0,7%) | 1 (0,8%) | 2 (1,5%) | – |
Al observar los motivos de finalización del primer tratamiento antirretroviral según el año de inicio, cabe destacar que el porcentaje de interrupciones por reacciones adversas fue inferior en los pacientes que iniciaron tratamiento en el año 2005 (23%) que en los que iniciaron tratamiento en el año 2003 (27%) y 2004 (32%). Los cambios de tratamiento por reacciones adversas fueron similares para los diferentes tipos de regímenes.
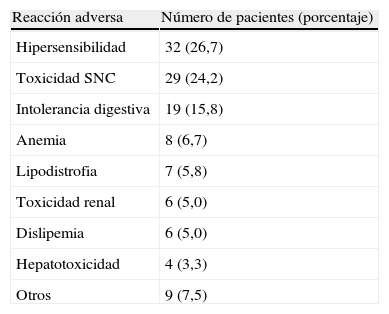
En la tabla 4 se indican las reacciones adversas que motivaron el cambio del tratamiento antirretroviral de inicio. Las principales reacciones adversas que provocaron cambios fueron las reacciones de hipersensibilidad en las pautas que incluían efavirenz, nevirapina o abacavir, la toxicidad a nivel del sistema nervioso central en las pautas que incluían efavirenz y la intolerancia digestiva, principalmente en las pautas que incluían IP.
Reacciones adversas que motivaron el cambio del tratamiento antirretroviral
| Reacción adversa | Número de pacientes (porcentaje) |
| Hipersensibilidad | 32 (26,7) |
| Toxicidad SNC | 29 (24,2) |
| Intolerancia digestiva | 19 (15,8) |
| Anemia | 8 (6,7) |
| Lipodistrofia | 7 (5,8) |
| Toxicidad renal | 6 (5,0) |
| Dislipemia | 6 (5,0) |
| Hepatotoxicidad | 4 (3,3) |
| Otros | 9 (7,5) |
Los resultados de este estudio muestran que la duración del primer tratamiento antirretroviral es corta. A pesar de que en estos últimos años los tratamientos han cambiado considerablemente, la duración ha sido comparable a la obtenida en un estudio con una metodología similar realizado en los pacientes que iniciaban tratamiento en el periodo comprendido entre 1998 y 20006. Sin embargo, se debe destacar que los motivos de cambio han sido diferentes. En el periodo anterior, las reacciones adversas supusieron casi la mitad de los motivos de cambio, mientras que en los inicios comprendidos entre el 2003 y el 2005, han supuesto menos del 30%. Por otro lado, aunque el porcentaje de abandonos ha sido similar (7%), el porcentaje de pérdidas ha sido bastante inferior al obtenido en el periodo anterior (6% vs 15%). Teniendo en cuenta estos datos, la duración del tratamiento debería haber sido superior, sin embargo, la inclusión de los pacientes en ensayos clínicos ha contribuido a acortar la duración del tratamiento. Este hecho hace que los datos no se puedan extrapolar si se compara con otros centros que presentan menos actividad investigadora.
Estudios anteriores que establecían la duración del primer tratamiento antirretroviral han referido periodos de duración de 11,8 meses a 1,6 años7–9. Chen et al7, siguieron durante casi 6 años una cohorte de 405 pacientes naive que iniciaron terapia antirretroviral entre 1996 y 2001, de los cuales un 65% recibieron una combinación con IP como terapia inicial. Estos autores hallaron una mediana de duración de 1,6 años. Palella et al8, refirieron una mediana de duración del primer tratamiento antirretroviral de 11,8 meses en los pacientes de la cohorte HOPS que iniciaron tratamiento antirretroviral entre 1996 y 1999. Las combinaciones utilizadas estuvieron basadas en IP en más del 80% de los casos. En otro trabajo, Arribas et al9 refirieron una duración del primer tratamiento de 18,5 meses en un estudio retrospectivo realizado en España entre enero de 1997 y abril de 2000, que incluyó 401 pacientes naive.
Las diferencias observadas entre estos estudios se pueden explicar, por diferencias en su diseño, si se han incluido pacientes naive y/o pretratados, el tipo de análisis estadístico (si se ha realizado un análisis de supervivencia o simplemente se ha calculado la diferencia entre la fecha de finalización y el inicio de tratamiento), tiempo de seguimiento, si se ha realizado un seguimiento posterior a la finalización del periodo de inclusión, la inclusión o no de las pérdidas de seguimiento en el análisis, la inclusión o no de los pacientes que participan en ensayos clínicos y las diferencias en las combinaciones prescritas. Por lo que hace referencia a este último punto, en la mayoría de los estudios realizados entre 1996 y 2001 las combinaciones basadas en IP fueron las más prescritas, en coherencia con las recomendaciones vigentes y la disponibilidad de fármacos en aquel periodo. Sin embargo, han pasado de representar el 92% en 1997 a representar un 20% en el 2005.
Un estudio más reciente, comparó la duración y los motivos de cambio del primer tratamiento antirretroviral en un centro americano13. Para ello contrastaron dos periodos de tiempo, el anterior y el posterior a agosto del 2004 (cuando aparecieron los regímenes de una vez al día a dosis fijas en Estados Unidos). Los datos obtenidos mostraron un mayor riesgo de discontinuación en los pacientes tratados con regímenes basados en IP y en los que incluían como análogos ddI o d4T, de forma similar a los resultados obtenidos en nuestro estudio. Estudios previos han mostrado unas altas tasas de discontinuaciones de los regímenes que contienen ZDV sobre todo debido a la supresión de la médula ósea y de d4T y ddI, a menudo relacionado con la toxicidad mitocondrial. Los nuevos ITIAN han contribuido a alargar la duración de los tratamientos debido a su menor toxicidad. En el estudio de Willig et al uno de los motivos a los que atribuyeron la mayor duración de los tratamientos en el periodo posterior a agosto del 2004 fue el cambio de ddI, d4T y AZT por ABC o TDF. Sin embargo, los resultados obtenidos en cuanto a la duración del tratamiento no son superponibles ya que en el estudio de Willig et al se excluyeron todas las interrupciones que se produjeron antes de los 14 días de tratamiento. Esta metodología excluye la mayor parte de las reacciones de hipersensibilidad que en nuestro caso han constituido uno de los principales motivos de cambio y contribuyen en acortar la duración global del tratamiento.
Por otro lado, a pesar de que el periodo de seguimiento fue menor en los pacientes que iniciaron TARGA en el año 2005, la mediana de duración fue superior a la obtenida en los años anteriores. Esto nos hace suponer que con los regímenes que se utilizan actualmente la duración del TARGA será superior debido a la menor complejidad y toxicidad de los nuevos fármacos. Teniendo en cuenta que la infección por VIH se ha convertido en una enfermedad crónica, nos interesa no interrumpir el tratamiento después de haberlo iniciado y mantenerlo activo el mayor tiempo posible.
Como ya se ha comentado, la duración fue significativamente mayor (p<0,005) en las combinaciones basadas en ITINN respecto a las basadas en IP o ITIAN y en aquellas que incluían ABC o TDF respecto a las que incluían AZT, d4T o ddI.
No se observó una relación estadísticamente significativa entre un peor estado inmunológico o virológico inicial y una menor duración del tratamiento inicial. Estos resultados coinciden con los obtenidos en otros estudios7.
Una mediana de duración del primer tratamiento antirretroviral de 384 días puede parecer corta en una infección como la producida por el VIH, que requiere tratamiento continuado. Por esta razón, es importante conocer las causas que motivan el cambio del primer tratamiento. Las reacciones adversas han sido referidas como el principal motivo de cambio del tratamiento por muchos autores, tanto en pacientes naive como en pacientes pretratados14–18. En los estudios de Chen et al7 y Arribas et al9, los efectos adversos fueron responsables del cambio del tratamiento en un 50% y 46,2% de los casos, respectivamente. En el estudio de Willig et al13 las reacciones adversas también fueron el principal motivo de cambio y mostraron una disminución en el periodo posterior a agosto de 2004 (64 vs 43% al año de seguimiento). En nuestro estudio, las reacciones adversas siguen constituyendo el principal motivo de cambio aunque en un porcentaje inferior al obtenido en los estudios realizados con anterioridad.
Las reacciones adversas que han motivado el cambio de tratamiento han sido diferentes a las descritas en otros estudios. Los cambios fundamentalmente han sido debidos a reacciones de hipersensibilidad y a toxicidad a nivel del sistema nervioso central, reacciones producidas fundamentalmente por los ITINN. Hecho esperable si tenemos en cuenta que en nuestro estudio los principales fármacos prescritos han sido los ITINN. Si nos centramos en los IP, la reacción adversa observada con más frecuencia y responsable de más del 40% de los cambios ha sido la intolerancia digestiva. Este dato es similar a los obtenidos con anterioridad en los estudios que incluían fundamentalmente pautas basadas en IP14.
Estos resultados confirman, sin duda alguna, que los efectos adversos representan un grave problema del tratamiento antirretroviral. Este hecho es sumamente importante ya que, aparte del gran número de cambios que producen, pueden provocar una disminución de la adherencia y, consecuentemente, aumentar el número de fracasos virológicos por aparición de resistencias. También se debe destacar que aunque los efectos adversos se han mantenido como principal motivo de cambio o finalización de tratamiento durante todo el periodo de seguimiento, en el año 2005 el porcentaje ha sido inferior al de los años anteriores.
Los resultados de este estudio se deben interpretar teniendo en cuenta sus limitaciones. Debido al tamaño de la muestra, no se pudo realizar una comparación de la duración de los tratamientos a nivel individual. Otra limitación es que el estudio se ha realizado en un único centro y, por tanto, no se pueden realizar generalizaciones.
En conclusión, los resultados obtenidos muestran que aunque la duración del primer tratamiento antirretroviral sigue siendo corta, actualmente se producen menos cambios por reacciones adversas y por pérdidas de seguimiento. Los motivos podrían ser una mejor tolerancia y una menor complejidad. No obstante, son necesarios más estudios para determinar el beneficio de un régimen frente a otro y poder generalizar estos resultados.