Streptococcus pneumoniae es una causa importante de morbilidad, y la vacuna es la medida más eficaz para prevenirla. El objetivo de este estudio es analizar la evolución de la enfermedad neumocócica invasora (ENI).
Material y métodosEstudio observacional de los casos de ENI residentes en la Comunidad de Madrid notificados a la Red de Vigilancia Epidemiológica entre los años 2008 y 2015. El caso de ENI se definió como la enfermedad producida por Streptococcus pneumoniae, con aislamiento, detección de ADN o detección de antígeno, en muestras procedentes de sitios normalmente estériles. Las cepas aisladas se enviaron al Laboratorio Regional de Salud Pública para la identificación del serotipo. Los serotipos se clasificaron según su inclusión en la vacuna heptavalente (VCN7), en la vacuna trecevalente pero no en la heptavalente (VCN13 adicional) y no incluidos en la VCN13 (no VCN). Se calcularon las razones de incidencia (RI) comparando los períodos 2011-2012 y 2013-2015 con el período 2008-2010.
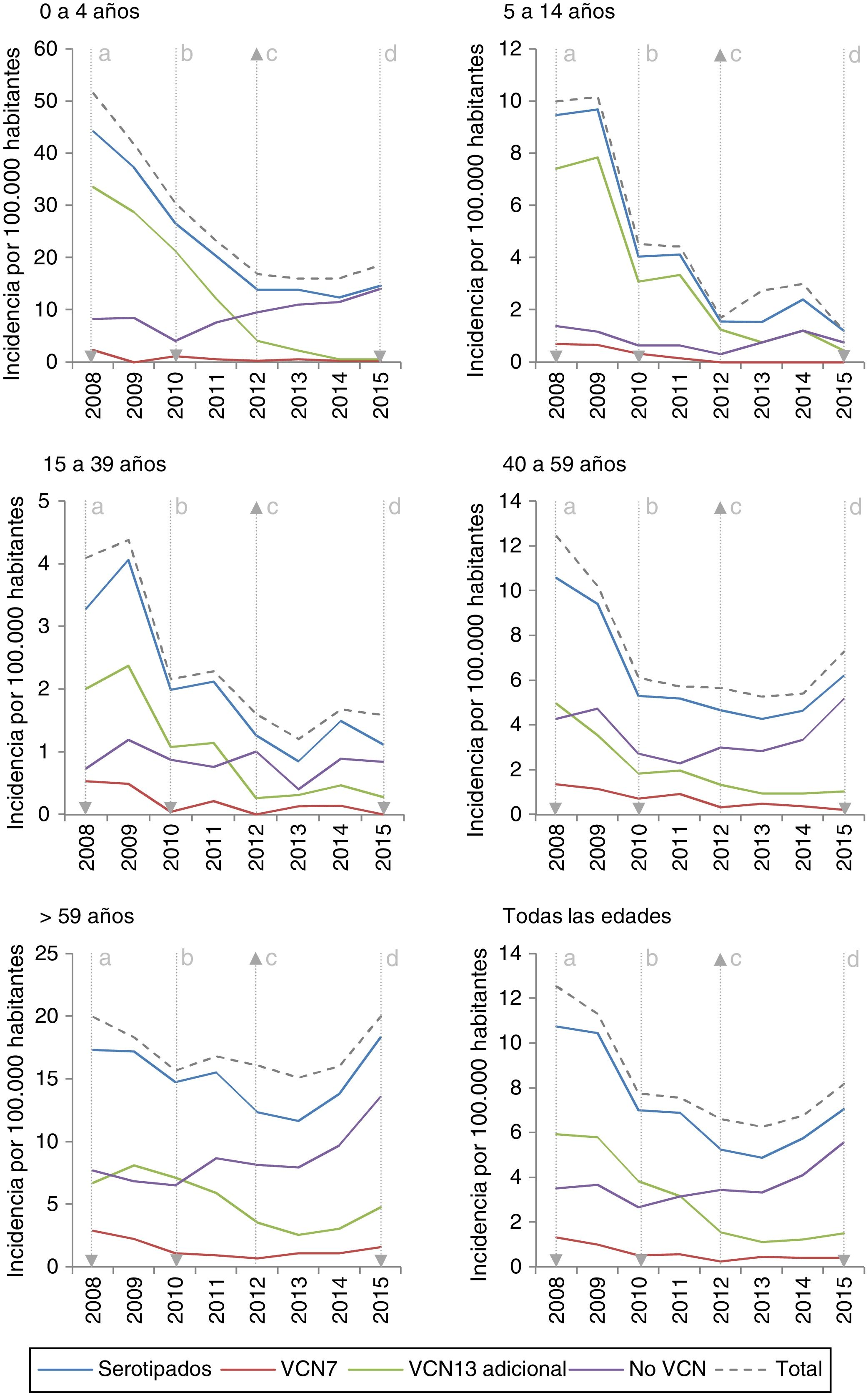
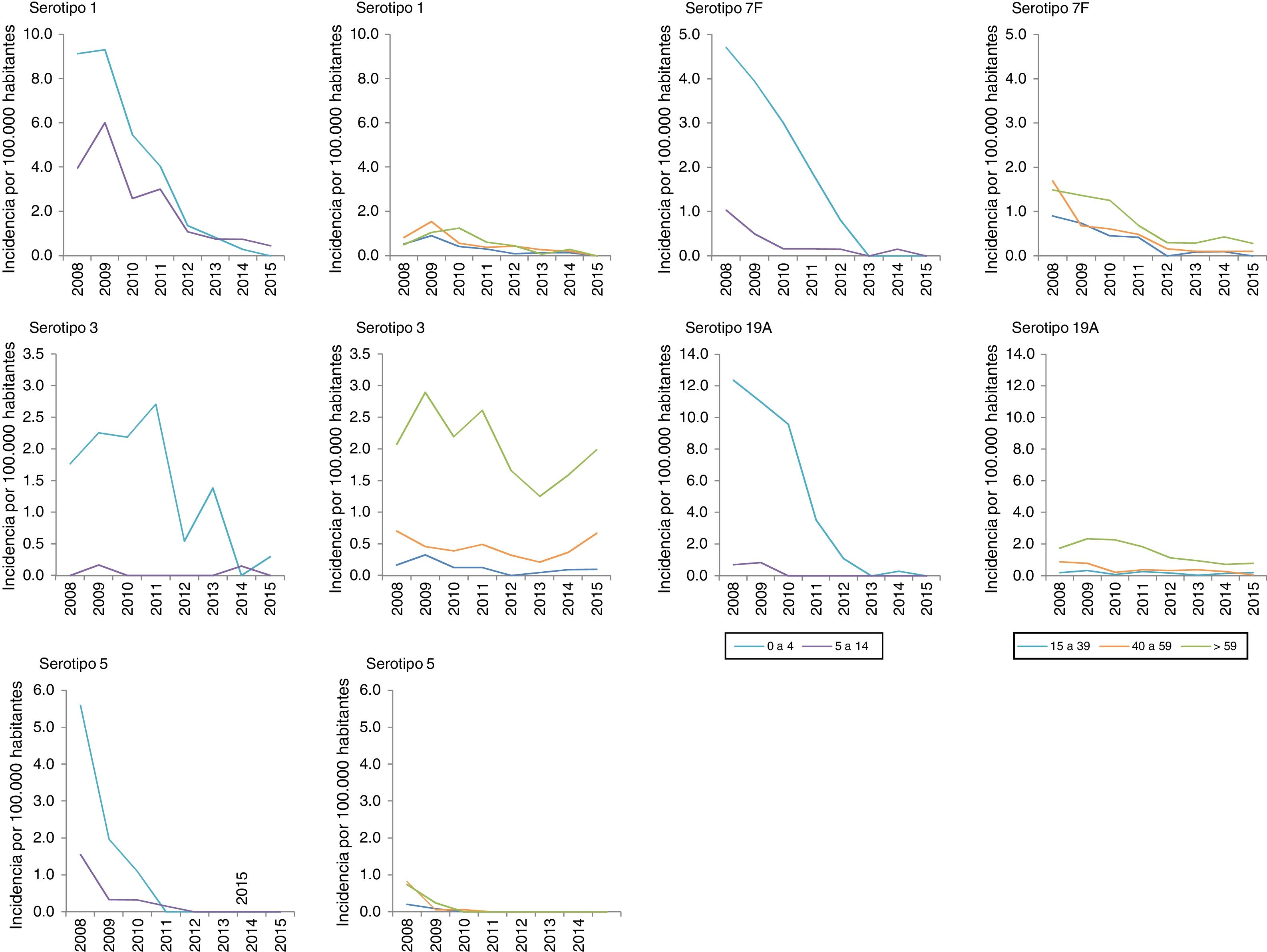
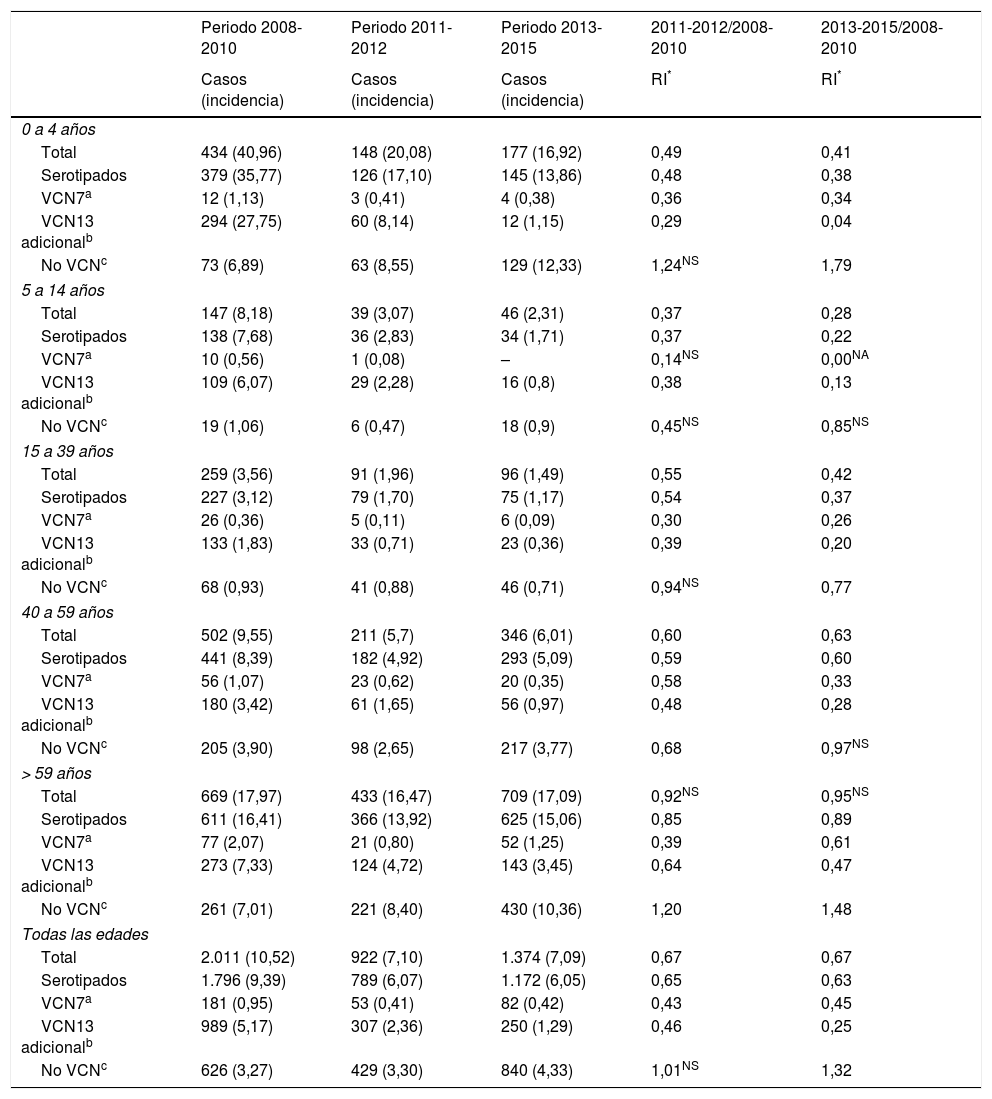
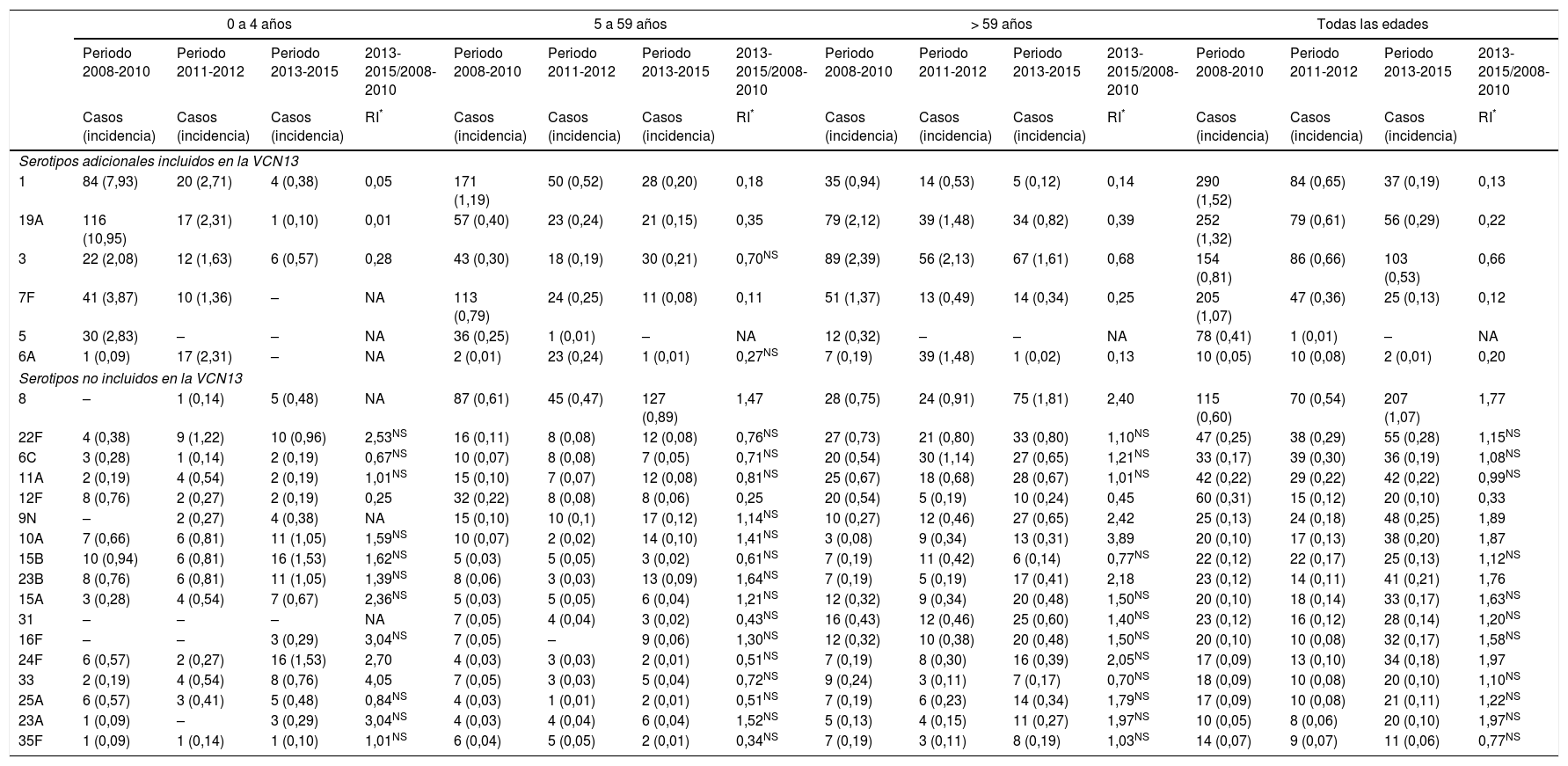
ResultadosSe notificaron 4.307 casos. El 86,6% fueron serotipados. La RI de ENI para todos los serotipos fue de 0,67 y de 0,67; la RI para los serotipos VCN7 fue de 0,43 y de 0,45; la RI para los VCN13 adicional fue de 0,46 y de 0,25, y la RI para los no VCN fue de 1,01 y de 1,32 en los períodos 2011-2012 y 2013-2015. Los serotipos 8, 9N, 10A, 23B, 24F y el serogrupo 33 incrementaron su incidencia de manera significativa en el período 2013-2015. Los serotipos 15B y 24F supusieron el 24% de los casos no VCN13 en menores de 5años, los serotipos 8 y 9N el 51% en población de 5 a 59años y los serotipos 8 y 22F el 25% en mayores de 59años.
ConclusionesLa incidencia de serotipos no incluidos en vacunas conjugadas ha aumentado, especialmente en menores de 5años, pero la incidencia total de ENI ha disminuido. Es imprescindible continuar con los programas de vigilancia epidemiológica y microbiológica para valorar el efecto de la vacunación sobre la incidencia de la ENI.
Streptococcus pneumoniae is an important cause of morbidity. Vaccination is the most effective measure to prevent it. The aim of this study is to analyse the evolution of invasive pneumococcal disease (IPD).
Material and methodsObservational study of IPD cases notified to the Epidemiological Surveillance Network of the Autonomous Community of Madrid between 2008 and 2015. The IPD case was defined as the disease caused by Streptococcus pneumoniae, with isolation and DNA or antigen detection, in samples from normally sterile sites. The isolated strains were sent to the Regional Public Health Laboratory for identification of the serotype. Serotypes were classified according to their inclusion in the 7-valent conjugate vaccine (PCV7), in the 13-valent vaccine, but not in the 7-valent vaccine (PCV13-additional) and not included in the 13-valent vaccine (non-PCV). The Incidence Rate Ratios (IRRs) were calculated comparing the 2011-2012 and 2013-2015 periods with the 2008-2010 period.
Results4,307 cases were reported. 86.6% were serotyped. The IRR of IPD was 0.67 and 0.67 for all serotypes; 0.43 and 0.45 for PCV7 serotypes; 0.46 and 0.25 for PCV13-additional serotypes, and 1.01 and 1.32 for non-PCV13 serotypes in the 2011-2012 and 2013-2015 periods. The incidence of serotypes 8, 9N, 10A, 23B, 24F and serogroup 33 increased significantly in the 2013-2015 period. Serotypes 15B and 24F accounted for 24% of non-PCV13 cases in children under 5years, serotypes 8 and 9N for 51% in the population aged 5 to 59years and serotypes 8 and 22F for 25% in the population aged over 59years.
ConclusionsThe incidence of serotypes not included in conjugate vaccines has increased, especially in children under 5years, but the total incidence of IPD has decreased. It is important to continue with the epidemiological and microbiological surveillance programmes to assess the effect of vaccination on the incidence of IPD.
Artículo
Socio de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica

Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la SEIMC, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora