El cáncer de ano (CA) es uno de los tumores no definitorios de sida más frecuentes, principalmente en hombres que tienen sexo con hombres y mujeres infectadas por VIH.
ObjetivosEvaluar la prevalencia e incidencia de lesiones precursoras (HSIL) y CA en nuestra cohorte de mujeres, y compararlas con las de cérvix; analizar el porcentaje de pacientes que adquieren y aclaran genotipos oncogénicos (VPH-AR) del canal anal; y los factores predictores para dicha infección en ano.
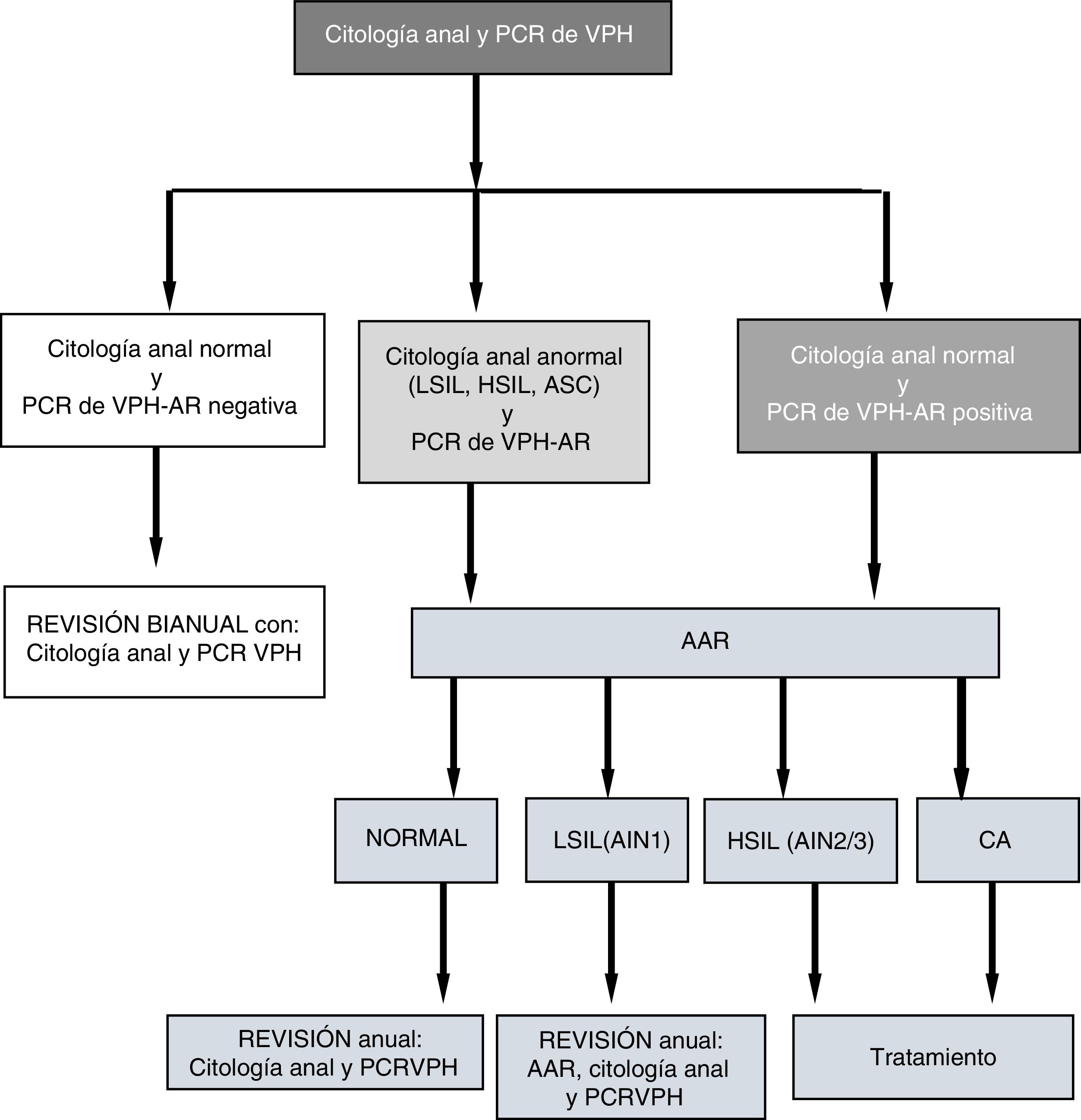
Paciente y métodosEstudio prospectivo-longitudinal (mayo de 2012-diciembre de 2016). En visita basal (V1) y posteriores se tomaban muestras de mucosa anal en medio líquido para citología, y PCR del VPH. En caso de citología anal patológica y/o PCR del VPH-AR positiva se realizaba anoscopia de alta resolución. Además, se enviaban al ginecólogo.
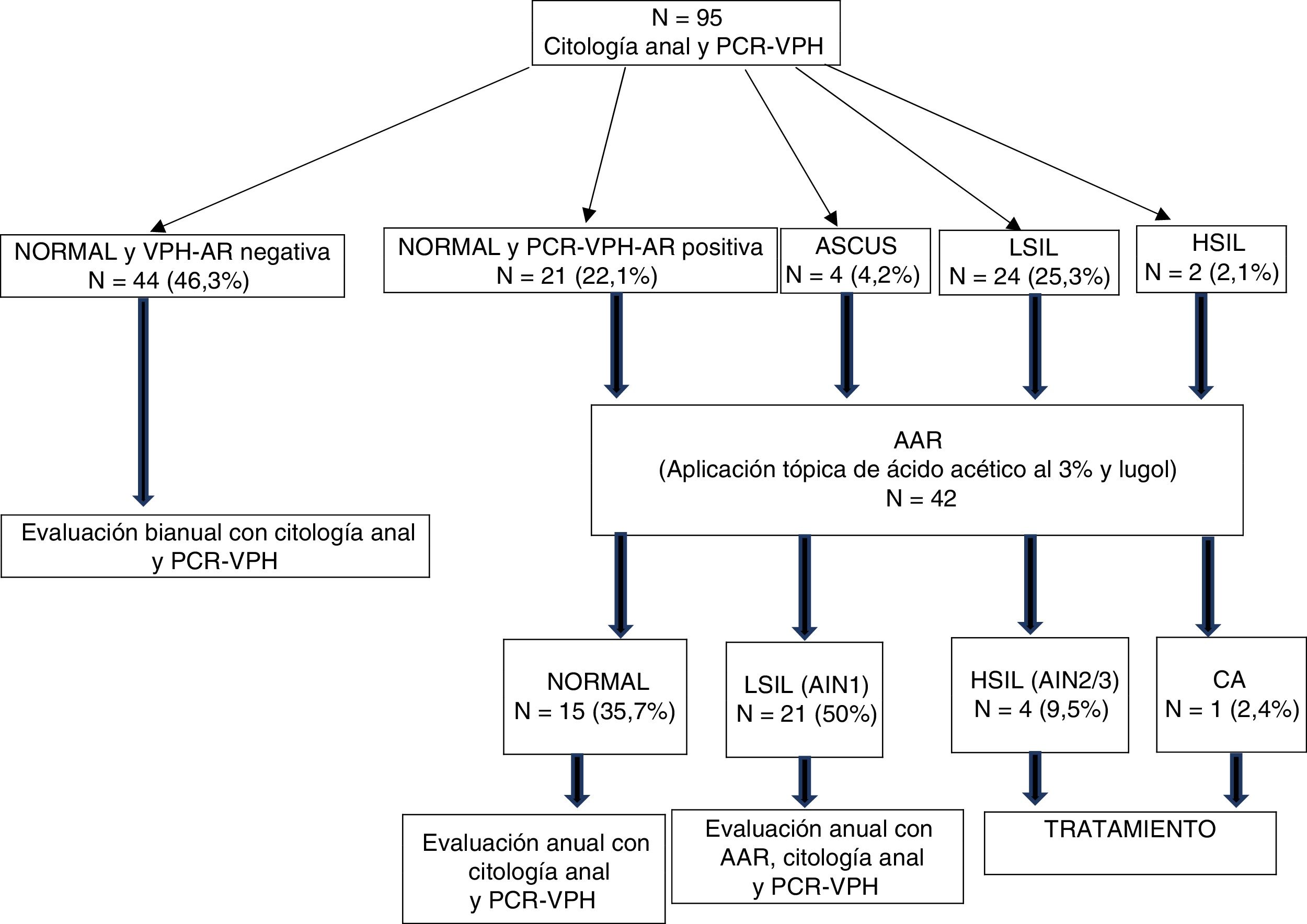
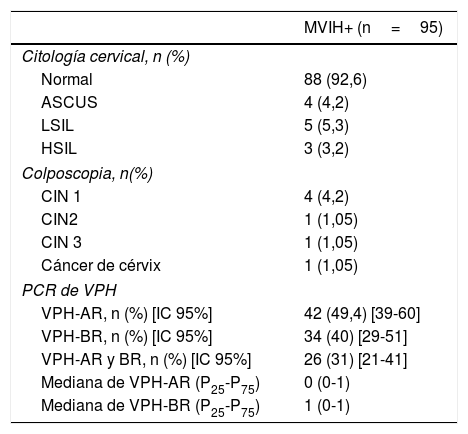
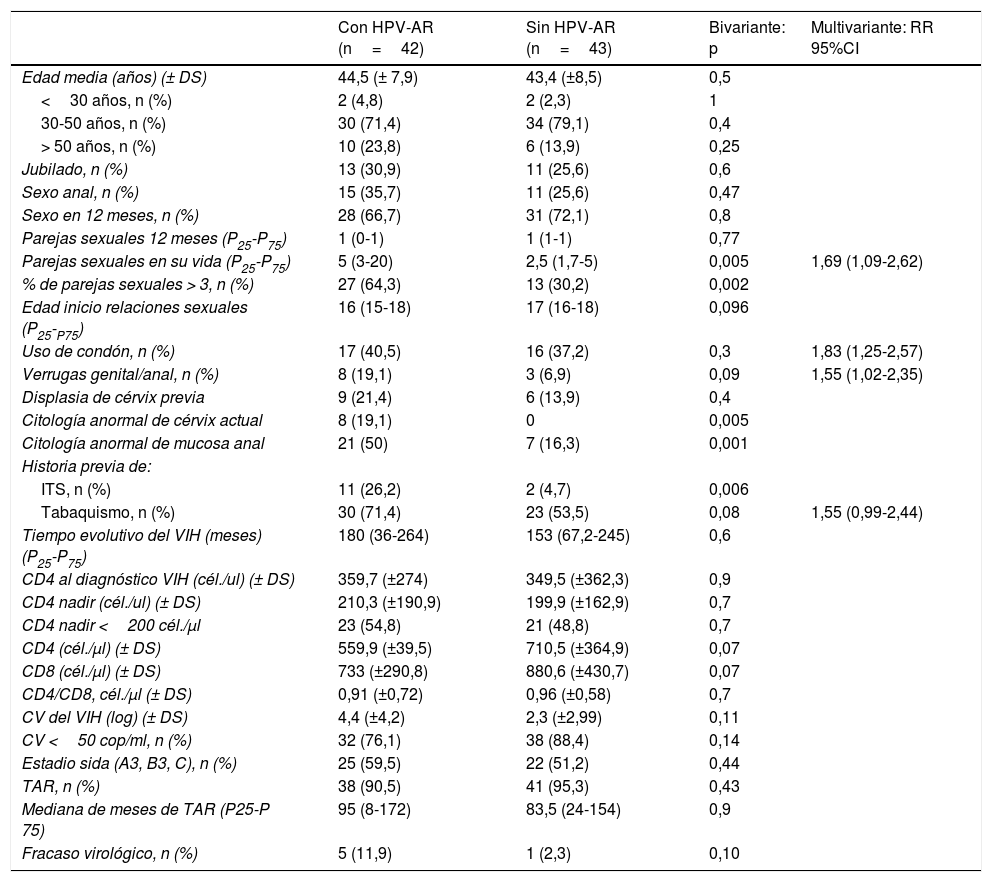
ResultadosNoventa y cinco mujeres de 43,7años fueron incluidas. En V1, el 11,6% tenían patología cervical (4,1% CIN1; 2,2% CIN2/3; 1,1% cáncer de cérvix [CC]); el 64,3% presentaban patología anal (50% LSIL/AIN1, 9,5% HSIL/AIN2/3 y 2,4% CA) y el 49,4%, infección por VPH-AR. Durante 36meses de seguimiento la incidencia de HSIL anal fue de 16×1.000 persona-año; el 14,8% adquirieron VPH-AR y el 51,2% los aclararon, p=0,007; ninguna presentó CIN1/2/3 o CC. En el análisis multivariante encontramos como factores predictores de infección por VPH-AR: tabaquismo (RR: 1,55; IC95%: 0,99-2,42), número de parejas sexuales >3 (RR: 1,69; IC95%: 1,09-2,62), displasia cervical (RR: 1,83; IC95%: 1,26-2,67) y anal (RR: 1,55; IC95%: 1,021-2,35).
ConclusionesA pesar de que el aclaramiento de genotipos oncogénicos en ano era mayor que la adquisición, la prevalencia e incidencia de HSIL era elevada, y superior a la de cérvix, por lo que quizá debería ofertarse el cribado de dichas lesiones a todas las mujeres seropositivas.
Anal cancer is one of the most common non-AIDS defining malignancies, especially in men who have sex with men and women living with HIV (WLHIV).
ObjectivesTo evaluate the prevalence and incidence of precursor lesions (high-grade squamous intraepithelial lesions [HSIL]) and anal cancer in our cohort of women and to compare them to cervical lesions; to calculate the percentage of patients that acquire and clear oncogenic genotypes (HR-HPV) in the anal canal; and to determine predictive factors for anal HPV infection.
Patients and methodsProspective-longitudinal study (May 2012-December 2016). At baseline (V1) and follow up visits, anal mucosa samples were taken in liquid medium for cytology and HPV PCR. In cases of abnormal anal cytology and/or positive HR-HPV PCR results, a high resolution anoscopy was performed. Patients were also referred to the gynaecologist.
ResultsNinety five women with an average age of 43.7years were included. At baseline, 11.6% had cervical abnormalities (4.1% CIN1, 2.2% CIN2/3, 1.1% cervical cancer), 64.3% anal abnormalities (50% LSIL/AIN1, 9.5% HSIL/AIN2/3 and 2.4% anal cancer) and 49.4% had HR-HPV genotypes. During 36months of follow up, the incidence of anal HSIL was 16×1,000 person-years; 14.8% acquired HR-HPV genotypes and 51.2% cleared them, P=.007. No patients presented CIN1/2/3/ or cervical cancer. In the multivariate analysis we found the following predictive factors for HR-HPV infection: smoking (RR: 1.55, 95%CI: 0.99-2.42), number of sexual partners >3 (RR: 1.69; 95%CI: 1.09-2.62), cervical and anal dysplasia (RR: 1.83; 95%CI: 1.26-2.67) and (RR: 1.55; 95%CI: 1.021-2.35), respectively.
ConclusionsDespite clearance rates of anal oncogenic genotypes being higher than acquisition rates, prevalence and incidence of HSIL were still high and greater than cervical HSIL. Therefore, screening for these lesions should perhaps be offered to all WLHIV.
Artículo
Socio de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica

Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la SEIMC, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora