Desde la introducción en el calendario de vacunación infantil de la vacuna conjugada frente al meningococoC (MenCC) en el año 2000, se ha modificado la pauta y se han realizado campañas de vacunación en cohortes de nacimiento específicas. El objetivo de este estudio es estimar el impacto y la efectividad de esta vacuna en Navarra hasta 2014.
MétodosEl impacto se evaluó comparando incidencia, mortalidad y letalidad de enfermedad por meningococoC en los periodos anterior (1995-1999) y posterior (2001-2014) a la vacunación. La efectividad se estimó mediante el método de cribado (Farrington) y el de cohorte indirecta (Broome). Los casos se recogieron del sistema de vigilancia de la enfermedad meningocócica en Navarra.
ResultadosEn el periodo 1995-1999 la incidencia media anual de enfermedad por meningococoC era de 1,32 por 100.000 habitantes, y de 7,18 por 100.000 en menores de 15años. El descenso de la incidencia fue contundente en los grupos de edad diana de la vacuna desde su introducción y ha sido progresivo en la población total. Entre 2011 y 2014 no se registraron casos por meningococoC. La efectividad de la vacuna para prevenir casos por este serogrupo se estimó entre el 96% (método de cribado) y el 99% (método de cohorte indirecta).
ConclusiónEl programa de vacunación con MenCC ha logrado con éxito disminuir la incidencia de la enfermedad por serogrupoC en Navarra, y los ajustes en la pauta vacunal han conseguido mantener una elevada efectividad vacunal en el tiempo.
Since 2000, when the meningococcal serogroupC conjugate vaccine (MenCC) was introduced in the childhood immunization schedule in Spain, several changes in the schedule and catch-up campaigns have been performed. We aim to estimate the impact and effectiveness of this vaccine in Navarra up to 2014.
MethodsThe impact of the vaccination program was analysed by comparing incidence, mortality and lethality rates of disease before (1995-1999) and after (2004-2014) the introduction of the MenCC. Vaccine effectiveness was estimated using the screening method (Farrington) and the indirect cohort method (Broome). Data on cases were obtained from the active surveillance of meningococcal disease.
ResultsDuring 1995-1999 the mean annual incidence of meningococcalC disease was 1.32 per 100,000, and 7.18 per 100,000 in children younger than 15years. The fall of meningococcalC disease incidence was significant in cohorts targeted for vaccination from the beginning and progressive in the general population. No cases were reported between 2011 and 2014. The estimated vaccine effectiveness was 96% by the screening method, and 99% by the indirect cohort method.
ConclusionThe MenCC vaccination program has been successful in decreasing the incidence rate of serogroupC meningococcal disease in Navarra, and schedule changes have maintained high vaccine effectiveness throughout the study period.
La enfermedad meningocócica (EM) es una infección endémica grave y potencialmente letal que causa un gran impacto médico, social y económico, por lo que es considerada una prioridad sanitaria de primer orden1,2. A su prevención se destinan sustanciales recursos materializados, fundamentalmente en programas de vacunación. Estos se dirigen de forma prioritaria a los grupos de población con mayor riesgo de enfermar, como los niños pequeños, o con un papel primordial en la transmisión del meningococo, como los adolescentes3,4.
En el año 2000 se autorizó la vacuna conjugada frente al serogrupoC (MenCC) en España, que se ha introducido a través del calendario de inmunizaciones infantil y de campañas de vacunación masiva o catch-up. La vacuna ha demostrado ser segura y tener alta eficacia, pero puede perder efectividad a los pocos años en niños vacunados a edades tempranas5-8.
En agosto del año 2000, poco antes de que se hiciera oficial la recomendación del Consejo Interterritorial del Sistema Nacional de Salud, se introdujo la vacuna en el calendario oficial de Navarra mediante la inmunización de los recién nacidos con 3 dosis en el primer año de vida9. En noviembre de ese año se implementó además una campaña de catch-up incluyendo a los menores de 6años (nacidos entre 1995 y julio de 2000). En 2004 se realizó una nueva campaña que extendió la vacunación a los menores de 17años (nacidos entre 1988 y 1994). El esquema de dosis inicial se ha modificado posteriormente en 2 ocasiones a nivel nacional10-12: en 2006 se pasó a administrar 2 dosis en el primer año seguidas de un recuerdo a partir de los 12meses, y en 2014 se acortó la primovacunación a una dosis seguida de un recuerdo a los 12meses y otro a partir de los 12años. Estos cambios, sustentados en la situación epidemiológica de la enfermedad13 y en que la vacunación a partir de la adolescencia genera una protección más duradera14, con la evidencia al mismo tiempo de que pautas cortas de primovacunación resultan igualmente inmunógenas15, han buscado reducir la pérdida de efectividad de la vacuna a largo plazo. De los 3 preparados de MenCC aprobados en España16, en Navarra se ha utilizado hasta 2004 Meningitec® (Nuron Biotech) y desde 2005 Neisvac-C® (Baxter)17.
El objetivo de este estudio es evaluar el impacto del programa de vacunación con MenCC en Navarra y estimar la efectividad de esta vacuna transcurridos 14años desde su introducción.
MétodosLa población de estudio fue la residente en Navarra entre 1995 y 2014 (unos 640.000 habitantes en 2014).
Se consideraron casos aquellos en los que se confirmó la presencia de Neisseria meningitidis serogrupoC, mediante cultivo o reacción en cadena de la polimerasa, en una muestra de un fluido corporal normalmente estéril, habitualmente sangre o líquido cefalorraquídeo. La información epidemiológica y microbiológica de los casos se obtuvo del Registro de Enfermedades de Declaración Obligatoria de Navarra, que incluye las notificaciones de casos por parte de los médicos asistenciales y las confirmaciones de laboratorio de todos los centros sanitarios. Al final de cada año se realiza un control de calidad mediante el cruce con el conjunto mínimo de datos al alta hospitalaria. En el análisis de la efectividad mediante el método de cribado se consideró fallo vacunal a todo caso confirmado por meningococoC que, habiendo recibido la pauta completa de MenCC para su edad según el esquema vacunal vigente, presentó síntomas de enfermedad al menos 14días después de la última dosis. Se consideraron correctamente vacunados, según la edad de vacunación, entre 2000 y 2005: a los niños ≤6meses con 3 dosis, a los de 7 a 11meses con 2 dosis y a los ≥12meses con una dosis; entre 2006 y 2013: a los niños ≤6meses con 2 dosis y a los de 7 a 11meses con una dosis, en ambos casos con un recuerdo después de los 12meses, y a los ≥12meses con una dosis; y en 2014 a los ≤11meses con una dosis, y con un recuerdo después de los 12meses, y a los de 12meses a 9años con una dosis, en ambos casos con un recuerdo a los 12años, y a los ≥10años con una dosis. Se excluyeron del análisis los casos parcialmente vacunados.
Para el cálculo de las tasas de incidencia y de mortalidad, se utilizó como denominador la población del padrón a 1 de enero de cada año para cada grupo de edad, según los datos del Instituto Nacional de Estadística. Para un análisis más detallado se dividió la población por grupos de edad, considerando niños a los menores de 15años y adultos al resto.
Para estimar el impacto de la vacuna, se comparó la incidencia de enfermedad en el quinquenio inmediatamente anterior a su introducción (1995-1999) con la del periodo posterior (2001-2014), que a su vez se dividió en 2 partes (2001-2003 y 2004-2014) tomando como corte el momento en el que se realizó el catch-up en adolescentes para evaluar mejor esta intervención. Se excluyó del análisis el 2000 por considerarse un año de transición. También se compararon la tasa de mortalidad, la letalidad y el porcentaje acumulado de casos según grupo de edad.
La efectividad de la vacuna se estimó mediante 2 métodos: el de cribado (Farrington)18 y el de cohorte indirecta (Broome)19. El método de cribado aplica la fórmula descrita por Farrington para comparar el estado vacunal de los casos detectados en la vigilancia, con la cobertura vacunal de la población de origen. En este análisis se utilizaron los casos detectados en las cohortes vacunadas (nacidos entre 1988 y 2014) y los datos de la cobertura de la vacunación en Navarra publicados por el Ministerio de Sanidad, Servicios Sociales e Igualdad11,20. Mediante el método de cohorte indirecta, se comparó el estado vacunal de los casos de serogrupoC con el de los casos de serogrupoB, bajo la asunción de que la vacuna MenCC no tiene efecto para prevenir casos debidos a meningococoB. En este análisis se incluyeron los casos diagnosticados entre 2meses y 24años de edad desde 1999 a 2014. Los análisis se ajustaron por sexo, grupos de edad (2-11meses, 1-4años, 5-14años y 15-24años) y periodo (1999-2004, 2005-2009 y 2010-2014).
Para la comparación de las proporciones se utilizó el test de Chi cuadrado o el test exacto de Fisher. En el estudio de cohorte indirecta se utilizaron técnicas de regresión logística no condicional convencional y exacta. La significación estadística se consideró a partir de valor de p<0,05.
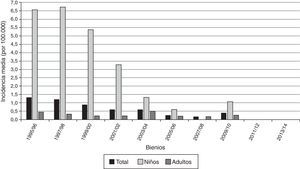
ResultadosImpacto del programa de vacunación sobre la enfermedad por meningococo CEn el periodo 1995-1999, la incidencia media anual de enfermedad por meningococoC fue de 20,81 y 14,13 casos por 100.000 en niños menores de 1año y de 1 a 4años, respectivamente. En la primera parte del periodo posvacunal (2001-2003), la incidencia se redujo un 100% en los 2 grupos de menos de 5años (p<0,001). En la segunda parte del periodo posvacunal (2004-2014) se consolidaron descensos en la incidencia del 95% en los menores de 1año (p<0,001) y del 100% en los de 1 a 4años (p<0,001) (tabla 1).
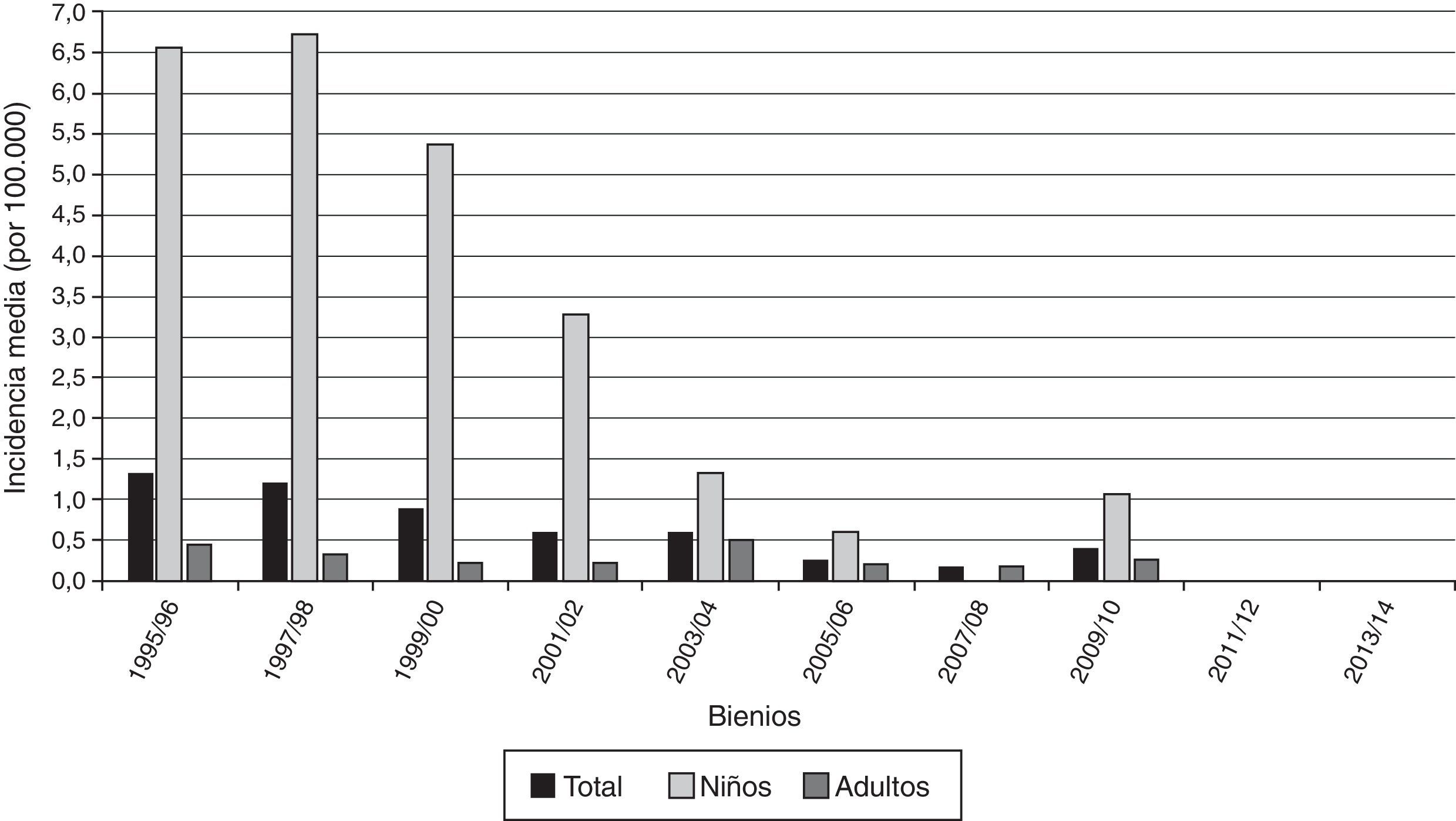
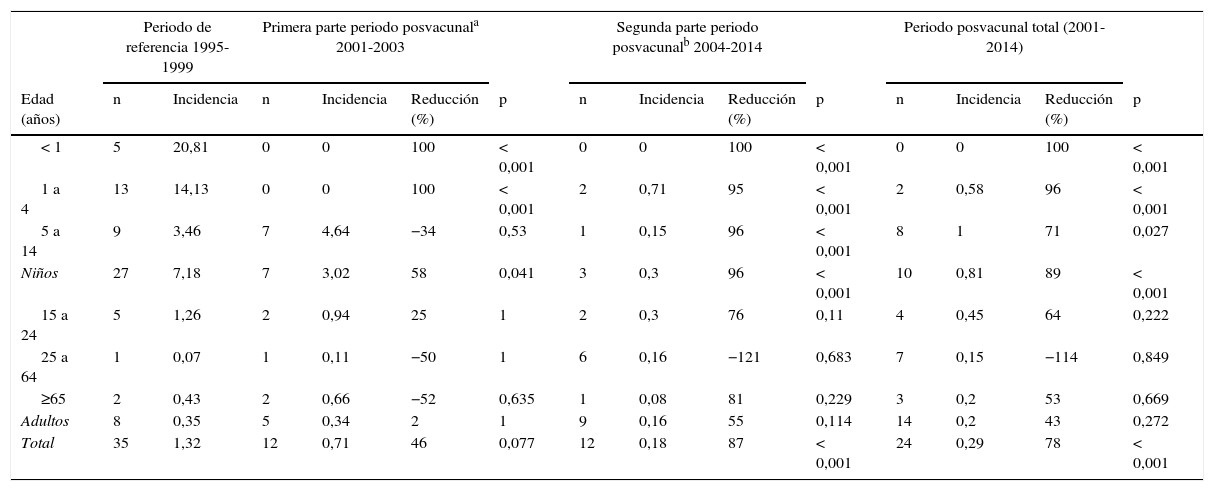
Número de casos, incidencia media anual por 100.000 habitantes y porcentaje de reducción de la incidencia de enfermedad por meningococo C en el periodo 2001-2014 (a su vez dividido en 2001-2003 y 2004-2014) respecto al periodo de referencia 1995-1999 en Navarra
| Periodo de referencia 1995-1999 | Primera parte periodo posvacunala 2001-2003 | Segunda parte periodo posvacunalb 2004-2014 | Periodo posvacunal total (2001-2014) | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Edad (años) | n | Incidencia | n | Incidencia | Reducción (%) | p | n | Incidencia | Reducción (%) | p | n | Incidencia | Reducción (%) | p |
| < 1 | 5 | 20,81 | 0 | 0 | 100 | < 0,001 | 0 | 0 | 100 | < 0,001 | 0 | 0 | 100 | < 0,001 |
| 1 a 4 | 13 | 14,13 | 0 | 0 | 100 | < 0,001 | 2 | 0,71 | 95 | < 0,001 | 2 | 0,58 | 96 | < 0,001 |
| 5 a 14 | 9 | 3,46 | 7 | 4,64 | −34 | 0,53 | 1 | 0,15 | 96 | < 0,001 | 8 | 1 | 71 | 0,027 |
| Niños | 27 | 7,18 | 7 | 3,02 | 58 | 0,041 | 3 | 0,3 | 96 | < 0,001 | 10 | 0,81 | 89 | < 0,001 |
| 15 a 24 | 5 | 1,26 | 2 | 0,94 | 25 | 1 | 2 | 0,3 | 76 | 0,11 | 4 | 0,45 | 64 | 0,222 |
| 25 a 64 | 1 | 0,07 | 1 | 0,11 | −50 | 1 | 6 | 0,16 | −121 | 0,683 | 7 | 0,15 | −114 | 0,849 |
| ≥65 | 2 | 0,43 | 2 | 0,66 | −52 | 0,635 | 1 | 0,08 | 81 | 0,229 | 3 | 0,2 | 53 | 0,669 |
| Adultos | 8 | 0,35 | 5 | 0,34 | 2 | 1 | 9 | 0,16 | 55 | 0,114 | 14 | 0,2 | 43 | 0,272 |
| Total | 35 | 1,32 | 12 | 0,71 | 46 | 0,077 | 12 | 0,18 | 87 | < 0,001 | 24 | 0,29 | 78 | < 0,001 |
En el periodo 2004-2014 también se constató un descenso en la incidencia en el grupo de 5 a 14años del 96% (p<0,001). En el conjunto de los menores de 15años la reducción fue del 96% (p<0,001). En adultos la incidencia descendió un 55%, aunque este cambio no alcanzó significación estadística (p=0,114). En el conjunto de la población la incidencia en el periodo 1995-1999 era de 1,32 casos por 100.000 personas año y descendió hasta 0,18 por 100.000 en 2004-2014, lo que supone una caída del 87% (p<0,001). Además, el descenso se ha mantenido firme, llegando a alcanzarse la incidencia de cero casos en toda la población en los últimos 4años (fig. 1).
El porcentaje de casos confirmados de menos de 5años de edad pasó del 51% en 1995-1999 al 0% en 2001-2003. El porcentaje de casos menores de 15años de edad se redujo del 58% en 2001-2003 al 25% en 2004-2014. En estos últimos años, los casos en grupos de edad no vacunados pasaron a suponer el 58% del total (tabla 1).
Los fallecidos por EM debida al serogrupoC fueron 6 en 1995-1999, 3 en 2001-2003 y otros 3 en 2004-2014. A la par que la incidencia, la tasa de mortalidad media anual disminuyó desde los 0,23 muertes por 100.000 habitantes en 1995-1999, a 0,18 y 0,05 muertes por 100.000 habitantes en 2001-2003 y 2004-2014, respectivamente, siendo el descenso significativo para la segunda parte del periodo posvacunal (p=0,03). La letalidad fue del 17% en el periodo 1995-1999 y del 25% tanto en 2001-2003 como en 2004-2014 (p=0,674). No hubo ningún fallecido por EM por serogrupoC en las cohortes vacunadas.
Estimación de la efectividad de la vacuna MenCC mediante el método de cribadoEntre 2001 y 2014 hubo 4 casos de enfermedad por meningococoC en cohortes a las que se les había ofertado la vacuna MenCC. De estos, 2 fueron fallos vacunales y los otros 2, casos no vacunados. Los 2 fallos vacunales habían sido inmunizados 5 y 8años antes de enfermar. Uno de ellos había sido vacunado con una dosis durante la primera campaña de catch-up a los 4años de edad y el otro a través de la vacunación infantil rutinaria siguiendo el esquema de 3 dosis en el primer año de vida.
La cobertura media para la vacunación rutinaria fue de 2001 a 2005 del 96,3% (mínimo 94,6% y máximo 98,5%) y de 2006 a 2014 del 95,5% (mínimo 86,8% y máximo 99,2%), siendo la media total del 95,9%. La cobertura media para el catch-up en 2000 fue del 96,0% (tanto en ≥6meses a≤12meses, como en >12meses a <6años) y del 95,8% en 2004. Aplicando el método de cribado, la efectividad estimada para la vacuna durante los 14años evaluados fue del 96% (IC95%: 69-99%) para ambas estrategias de vacunación (tabla 2).
Estimación de la efectividad de la vacuna conjugada frente al meningococoC mediante el método de cribado en cohortes de nacimiento a las que se había ofertado vacuna, según estrategia de vacunación en Navarra, periodo 2001-2014
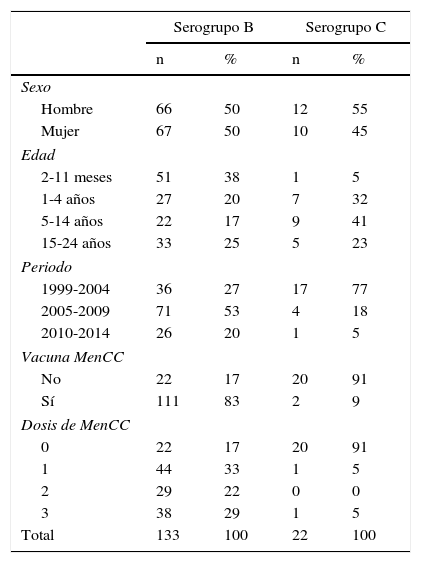
En el análisis de cohorte indirecta se comparó el estado vacunal de 22 casos de EM por serogrupoC diagnosticados entre los 2meses y los 24años de edad en el periodo 1999-2014 con el de los 133 casos por serogrupoB correspondientes a la misma edad y periodo. Entre los casos de serogrupoB el 83% habían recibido la vacuna MenCC, frente al 9% de los casos de serogrupoC. Entre los primeros, el 58% tenían menos de 5años, frente al 37% de los últimos (tabla 3).
Características de los casos de enfermedad meningocócica debida a serogrupos B y C en la población de 2 meses a 24 años en Navarra. Periodo 1999-2014
| Serogrupo B | Serogrupo C | |||
|---|---|---|---|---|
| n | % | n | % | |
| Sexo | ||||
| Hombre | 66 | 50 | 12 | 55 |
| Mujer | 67 | 50 | 10 | 45 |
| Edad | ||||
| 2-11 meses | 51 | 38 | 1 | 5 |
| 1-4 años | 27 | 20 | 7 | 32 |
| 5-14 años | 22 | 17 | 9 | 41 |
| 15-24 años | 33 | 25 | 5 | 23 |
| Periodo | ||||
| 1999-2004 | 36 | 27 | 17 | 77 |
| 2005-2009 | 71 | 53 | 4 | 18 |
| 2010-2014 | 26 | 20 | 1 | 5 |
| Vacuna MenCC | ||||
| No | 22 | 17 | 20 | 91 |
| Sí | 111 | 83 | 2 | 9 |
| Dosis de MenCC | ||||
| 0 | 22 | 17 | 20 | 91 |
| 1 | 44 | 33 | 1 | 5 |
| 2 | 29 | 22 | 0 | 0 |
| 3 | 38 | 29 | 1 | 5 |
| Total | 133 | 100 | 22 | 100 |
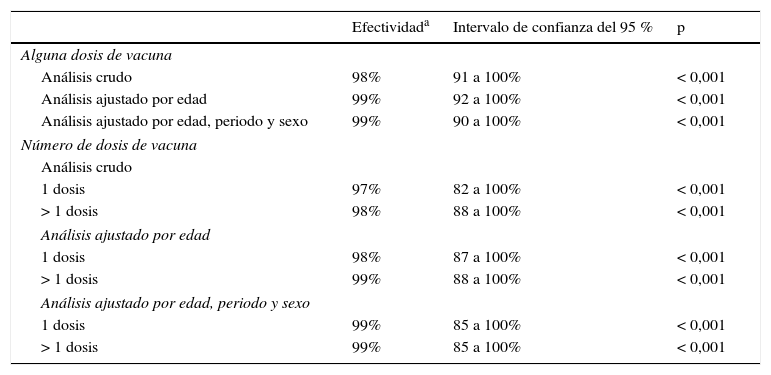
La efectividad de alguna dosis de vacuna MenCC para prevenir los casos de serogrupoC ajustada por edad, sexo y periodo fue del 99% (IC95%: 90-100%; p<0,001). Las estimaciones ajustadas de efectividad fueron igualmente del 99% (IC95%: 85-100%; p<0,001) para una o más dosis de vacuna (tabla 4).
Estimación de la efectividad de la vacuna conjugada frente al meningococo C mediante el método de cohorte indirecta en niños de 2 meses a 24 años. Comparación del estado vacunal de los casos debidos a serogrupo C tomando como grupo de comparación los casos de serogrupo B. Navarra 1999-2014
| Efectividada | Intervalo de confianza del 95 % | p | |
|---|---|---|---|
| Alguna dosis de vacuna | |||
| Análisis crudo | 98% | 91 a 100% | < 0,001 |
| Análisis ajustado por edad | 99% | 92 a 100% | < 0,001 |
| Análisis ajustado por edad, periodo y sexo | 99% | 90 a 100% | < 0,001 |
| Número de dosis de vacuna | |||
| Análisis crudo | |||
| 1 dosis | 97% | 82 a 100% | < 0,001 |
| > 1 dosis | 98% | 88 a 100% | < 0,001 |
| Análisis ajustado por edad | |||
| 1 dosis | 98% | 87 a 100% | < 0,001 |
| > 1 dosis | 99% | 88 a 100% | < 0,001 |
| Análisis ajustado por edad, periodo y sexo | |||
| 1 dosis | 99% | 85 a 100% | < 0,001 |
| > 1 dosis | 99% | 85 a 100% | < 0,001 |
El programa de vacunación con MenCC implementado en Navarra se ha seguido de un gran descenso en la incidencia de enfermedad por este serogrupo en el conjunto de la población. La caída de la incidencia se observa principalmente en los grupos de edad que han sido objetivo directo de la vacuna, como se ha descrito en otro estudio de ámbito nacional21. Desde los primeros años del periodo posvacunal (2001-2003), la incidencia en menores de 5años se redujo a cero coincidiendo con la vacunación de esas cohortes de edad. A su vez, en esos años se insinuó un repunte de los casos en adolescentes, semejante al observado en estudios de mayor potencia, probablemente debido a las ondas cíclicas propias de la enfermedad7,22. Sin embargo, la incidencia en los grupos de 5 a 14años y de 15 a 24años se redujo en los años siguientes (2004-2014), posiblemente como efecto del catch-up a los menores de 17años efectuado en 2004, al igual que ocurrió en otras comunidades autónomas23. La administración de una dosis de recuerdo en el segundo año de vida desde 2006 ha podido contribuir a que el descenso de la incidencia en menores de 15años haya alcanzado el 96% y se haya mantenido en el tiempo. En un estudio realizado con los datos de España, la población de 25-44años fue, al igual que en el presente estudio, la que presentó menos reducción de incidencia en el periodo posvacunal21.
El impacto de la vacuna sobre las cohortes vacunadas se refleja en el aumento del porcentaje de casos pertenecientes a cohortes no vacunadas (un 58% del total en 2004-2014), similar a lo publicado por Garrido-Estepa et al.21.
Parte del éxito de la vacuna MenCC se ha atribuido a su capacidad para proporcionar protección de grupo, al reducir la colonización y la transmisión bacteriana24,25. El tamaño muestral de este estudio limita el análisis del efecto en no vacunados; sin embargo, el hecho de que no se haya registrado ningún caso por serogrupoC en toda la población en los últimos 4años sugiere la existencia de cierto grado de inmunidad comunitaria, probablemente favorecida por la elevada cobertura de la vacuna.
El descenso en la tasa de mortalidad observado es consistente con la disminución de la incidencia de la enfermedad, destacando el hecho de que no ha habido fallecimientos en las cohortes vacunadas. El aumento de la letalidad media ha sido descrito por otros autores, y se ha relacionado con el aumento de la edad de los casos22.
La vacuna MenCC ha alcanzado una efectividad del 96%, según el método de cribado, y del 99%, según el método de cohorte indirecta, para prevenir casos de enfermedad por meningococoC en Navarra. Varios estudios han calculado la efectividad de la vacuna mediante el método de cribado basándose en datos epidemiológicos6,7,21. Los estudios realizados con datos españoles obtuvieron valores de efectividad equivalentes a los de este estudio para los catch-up (93-94%) e inferiores para la vacunación rutinaria (78-89%), con similares coberturas vacunales medias7,21. El preparado utilizado podría tener alguna influencia en este aspecto, ya que el conjugado con toxoide tetánico ha mostrado cierta superioridad en el mantenimiento de la protección a largo plazo frente a los conjugados con toxina diftérica26,27. Un estudio español publicado recientemente muestra que los fallos vacunales aumentan a partir del tercer año de la vacunación y que son más frecuentes en la vacunación rutinaria que en los catch-up28. El presente estudio no es concluyente sobre estos aspectos debido a que el número de fallos vacunales fue muy reducido; no obstante, en los 2 fallos vacunales habían trascurrido más de 3años desde la inmunización, siendo el porcentaje de fallos para ambas estrategias similar.
Sobre la misma población se estimó la efectividad de la vacuna utilizando 2 métodos diferentes. Aunque las estimaciones no coinciden exactamente, la similitud de los resultados obtenidos (96 y 99%) refuerza su validez y permite concluir con mayor seguridad que la efectividad de la vacuna MenCC, sin llegar al 100%, se sitúa en niveles muy altos. Los 2 métodos utilizados se basan en asunciones diferentes y se ven afectados por diferentes factores. El método de cribado compara la proporción de casos vacunados entre los casos y usa las coberturas para establecer la proporción de personas vacunadas en la población general de igual edad, pero no tiene en cuenta algunas circunstancias como la mayor frecuencia de factores de riesgo entre los casos, que podría afectar a la comparabilidad. El método de cohorte indirecta compara la proporción de casos vacunados en los casos por serogrupoC con la de los casos de serogrupoB. La comparación de casos con casos probablemente consigue mejor comparabilidad, en cuanto a la frecuencia de factores de alto riesgo, entre los 2 grupos que el método de cribado, pero podría afectarse si la vacunación frente al meningococoC modificase el riesgo de enfermedad por meningococoB. En todo caso, la similitud de las estimaciones obtenidas con métodos y asunciones diferentes apoya su validez.
En la interpretación de estos resultados han de tenerse en cuenta algunas limitaciones. Aunque el estudio abarcó a toda la población de Navarra, al tratarse de una enfermedad poco frecuente, el número de casos analizados fue suficiente para algunas comparaciones, pero no permitió profundizar en análisis más detallados. Debido al escaso número de casos, en el método de cribado se utilizó la cobertura promedio de las diversas cohortes vacunadas en cada una de las 2 estrategias; aunque las coberturas apenas variaron entre cohortes de nacimiento, la necesidad de agrupar muchas cohortes supone cierta limitación en la precisión de las estimaciones. Tampoco podemos descartar que las oscilaciones en la incidencia que puede sufrir la EM hayan podido magnificar u ocultar el impacto de la vacuna. En este sentido, Navarra fue una de las comunidades españolas menos afectadas por el incremento de casos de una cepa hipervirulenta del serogrupoC a mediados de la década de 199029. La agrupación de varios años en los análisis contribuye a mejorar la potencia estadística de las comparaciones y a suavizar cambios en la tendencia secular de la enfermedad. Por otra parte, el porcentaje de casos totales de EM confirmados durante los años que abarca el estudio fue del 92%, por lo que algún caso de meningococoC no confirmado microbiológicamente podría haber quedado excluido del análisis.
El impacto observado ha de interpretarse en el contexto de una elevada cobertura vacunal, que se mantuvo en torno al 96%, tanto en las cohortes de vacunación rutinaria como en las de catch-up. Para garantizar la continuidad de este impacto en el tiempo se han de mantener elevadas coberturas vacunales, ya que en caso contrario los avances alcanzados podrían ser reversibles.
Será necesario seguir evaluando las últimas modificaciones de la pauta de vacunación y su repercusión en un futuro. Además, aunque un cambio sustancial de la situación de la EM por este serogrupo a corto plazo parece improbable, continúa siendo primordial la vigilancia epidemiológica de los casos, la identificación microbiológica de las cepas circulantes y la elaboración de estudios de efectividad vacunal y seroprevalencia a largo plazo. Tras los grandes avances logrados en el control de la enfermedad por meningococoC, los esfuerzos han de ir dirigidos hacia el control de la enfermedad por otros serogrupos, principalmente elB30.
En conclusión, la vacunación con MenCC ha conseguido un importante impacto en la incidencia de enfermedad por meningococoC, reflejado en la ausencia de casos desde 2011, y ha presentado una alta efectividad en vacunados en Navarra. En los próximos años el mantenimiento de elevadas coberturas y los ajustes en la edad elegida para la administración de cada dosis serán los puntos clave para consolidar la eliminación de la enfermedad por meningococoC.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.