En los últimos años se está observando una reemergencia de la tos ferina en los países con amplias coberturas vacunales, con la aparición de brotes importantes. Este aumento de la incidencia tiene una distribución por edades bipolar: en los lactantes menores de 6meses, que por su edad no han iniciado la vacunación o no han completado la primovacunación, y en los adolescentes y adultos por la disminución de su inmunidad, vacunal o natural, con el tiempo transcurrido desde la inmunización o el padecimiento de la enfermedad. Estos cambios epidemiológicos justifican la adopción de nuevas estrategias vacunales con la finalidad de proteger al lactante pequeño y disminuir la incidencia de la enfermedad en toda la población.
La vacunación del adolescente y del adulto debería ser prioritaria; en el primer caso solo supone cambiar la vacuna dT por la dTpa, con un coste adicional pequeño. La vacunación del adulto puede ser más difícil de implementar, pero de la misma forma que en muchos países se revacuna cada 10años frente a la difteria y el tétanos (con la vacuna dT), debería hacerse también frente a la tos ferina (con la vacuna dTpa). La estrategia que puede tener un impacto más importante sobre la incidencia de la tos ferina en el lactante es la vacunación de las personas con quienes convive o va a convivir, lo que se conoce como estrategia del nido. Recientemente, en algunos países se ha introducido también la vacunación de la embarazada, a partir de las 20semanas de gestación, como la forma más efectiva para proteger al recién nacido.
A large increase of pertussis incidence has been observed in recent years in countries with high vaccination coverage. Outbreaks of pertussis are increasingly being reported. The age presentation has a bipolar distribution: infants younger 6months that have not initiated or completed a vaccination schedule, and adolescents and adults, due to the lost of natural or vaccine immunity over time. These epidemiological changes justify the need to adopt new vaccination strategies in order to protect young infants and to reduce pertussis incidence in all age groups.
Adolescents and adults immunization must be a priority. In the first group, strategy is easy to implement, and with a very low additional cost (to replace dT vaccine by dTap one). Adult vaccination may be more difficult to implement; dT vaccine decennial booster should be replaced by dTap. The immunization of household contacts of newborn infants (cocooning) is the strategy that has a most important impact on infant pertussis. Recently, pregnant women vaccination (after 20weeks of gestation) has been recommended in some countries as the most effective way to protect the newborn.
La tos ferina es una infección bacteriana aguda causada por Bordetella pertussis o por Bordetella parapertussis, patógenos exclusivamente humanos que pueden afectar a individuos de todas las edades. Los adolescentes y los adultos suelen presentar formas clínicas leves, pero los lactantes menores de 4meses son el grupo más vulnerable, con altas tasas de complicaciones y mortalidad. La transmisión se produce por contacto directo con las personas infectadas y su contagiosidad es muy alta, con una tasa de ataque de hasta el 90% en los convivientes susceptibles. La vacunación es la estrategia preventiva más eficaz para el control de la transmisión de la tos ferina en la población; sin embargo, ni la inmunidad natural ni la conferida por la vacunación ofrecen una protección duradera. Este documento de consenso tiene una justificación epidemiológica y preventiva. En los últimos años se está observando una reemergencia de la tos ferina en los países con amplias coberturas vacunales, con la aparición de brotes importantes. Este aumento de la incidencia tiene una distribución por edades bipolar: en los lactantes menores de 6meses, que por su edad no han iniciado la vacunación o no han completado la primovacunación, y en los adolescentes y adultos, por la disminución de su inmunidad, vacunal o natural, con el tiempo transcurrido desde la inmunización o el padecimiento de la enfermedad. Por otra parte, el descenso de la incidencia de la infección en el primer decenio de la vida, debido a las altas coberturas de vacunación, ha originado una menor circulación de B.pertussis y la ausencia del efecto booster que la infección natural induce en el adolescente y en el adulto.
Estos cambios epidemiológicos justifican la adopción de nuevas estrategias vacunales con la finalidad de proteger al lactante pequeño y disminuir la incidencia de la enfermedad en toda la población. La vacunación del adolescente y del adulto debería ser prioritaria; en el primer caso solo supone cambiar la vacuna dT por la dTpa, con un coste adicional pequeño. La vacunación del adulto puede ser más difícil de implementar, pero de la misma forma que en muchos países se revacuna cada 10años frente a la difteria y el tétanos (con la vacuna dT), debería hacerse también frente a la tos ferina (con la vacuna dTpa). La estrategia que puede tener un impacto más importante sobre la incidencia de la tos ferina en el lactante es la vacunación de las personas con quienes convive o va a convivir, lo que se conoce como estrategia del nido (cocoon strategy en inglés). En Estados Unidos, en octubre de 2011 se recomendó también la vacunación de la embarazada, a partir de las 20semanas de gestación, como la forma más efectiva para proteger al recién nacido. Esta estrategia debería implantarse conjuntamente con la del nido.
Situación epidemiológica de la tos ferina en EuropaLos sistemas de vigilancia epidemiológica de la tos ferina en Europa varían ampliamente entre países: notificación voluntaria de casos por parte del médico (sistema de enfermedades de declaración obligatoria), declaración de los laboratorios de microbiología (sistema de declaración microbiológico), sistemas de vigilancia centinela y vigilancia de las hospitalizaciones. En algunos países, como Francia, Suiza, Bélgica e Inglaterra, se utilizan simultáneamente varios de estos sistemas1.
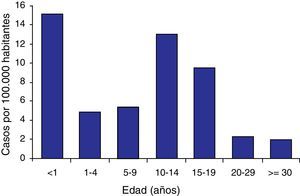
En 1998 se fundó en Europa el grupo EUVAC-NET, una red para la vigilancia epidemiológica y el control de las infecciones prevenibles por vacunas en la Unión Europea y en 3países EEA/EFA y cuyas responsabilidades las asume desde 2011 el European Centre for Disease Prevention and Control (ECDC)2. Según los últimos datos publicados, correspondientes al año 2010 y a 28países, que incluyen un total de 15.749casos registrados, la incidencia global de tos ferina fue de 3,7casos por 100.000habitantes3. Noruega y Estonia fueron los países que declararon más casos (incidencia del 73,4 y del 96,6 por 100.000, respectivamente). Las tasas de incidencia variaron en gran medida entre países, debido probablemente a diferencias en los sistemas de vigilancia epidemiológica, accesibilidad a métodos diagnósticos más sensibles, pautas vacunales, tipos de vacunas y coberturas de vacunación. La mayor incidencia se ha observado en los niños menores de un año (tasa de 15casos por 100.000habitantes), que representan el 5% del total de los casos, seguidos de los niños de 10 a 14años de edad (tasa de 13casos por 100.000) y de los adolescentes de 15 a 19años de edad (tasa de 8casos por 100.000habitantes) (fig. 1). La tasa de hospitalización fue de 87 por 1.000casos de tos ferina, y la de letalidad de 0,02 por 1.000 (el 70% de las muertes se registraron en niños menores de un año).
Incidencia de la tos ferina en Europa por grupos de edad.De EUVAC-NET, 20103.
No obstante, en realidad, la incidencia de la enfermedad es superior a la que indican los datos de vigilancia epidemiológica, debido a la existencia de una infranotificación y un infradiagnóstico importantes. Los estudios realizados en Inglaterra y en Italia sugieren que la incidencia real sería entre 3 y 7veces superior a la detectada por los sistemas de vigilancia pasivos4,5.
En los últimos años se está produciendo una reemergencia de la tos ferina en muchos países, incluso en aquellos con amplias coberturas vacunales, con un incremento notable en el número de casos en lactantes, adolescentes y adultos. En Alemania, la incidencia ha aumentado desde 7 a 10casos por 100.000 habitantes en 2002-2004 a 30casos por 100.000 habitantes en 2008; el porcentaje de casos en adultos ha pasado del 20 al 75%, con una incidencia de 160casos por 100.000 en estos grupos de edad6. En Holanda, la tasa de incidencia en el período 2002-2005 se ha incrementado el 60, el 44 y el 68% en las cohortes de 10-19años, 20-59años y mayores de 60años, respectivamente, en relación al período 1998-20017. En Inglaterra, a pesar de la disminución de la incidencia de la tos ferina asociada a la introducción de una pauta acelerada de vacunación, las tasas se mantienen altas en los niños menores de un año, en especial en los menores de 3meses (103,8casos por 100.000 en 2008), que constituyen entre el 68 y el 89% de los casos hospitalizados8; además, desde 2004 ha aumentado la incidencia de la enfermedad en los niños mayores y en adolescentes.
Los brotes recientes que se han producido en el ámbito escolar en Holanda, Alemania, Suiza y otros países han mostrado también que los adolescentes tienen un mayor riesgo de adquirir la enfermedad que los niños de otras edades9. Este aumento de casos observado en adolescentes y adultos puede explicarse, en parte, por un mayor índice de sospecha de la enfermedad, por la disponibilidad de métodos diagnósticos más sensibles, y tal vez también por una menor efectividad y una más corta duración de la inmunidad conferida por las vacunas disponibles. No obstante, desde un punto de vista de salud pública, lo más importante es que estos grupos de edad constituyen la principal fuente de infección para los lactantes que aún no han iniciado o completado la primovacunación.
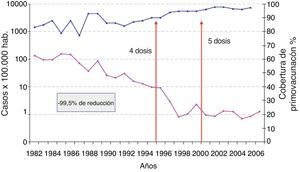
Situación epidemiológica de la tos ferina en EspañaEn España, la vacuna de la tos ferina se incluyó en el calendario de vacunación sistemática infantil en 1965. Entre 1975 y 1995 se administraban 3dosis de vacuna a los 3, 5 y 7meses de edad. En 1996 se incluyó una cuarta dosis a los 15-18meses de edad, y en 2001 una quinta dosis a los 4-6años de edad. Con la inclusión de la vacuna en el calendario nacional las coberturas de vacunación aumentaron progresivamente, y desde 1998 se mantienen por encima del 95% (97,1% para la serie primaria, 94,3% para la dosis de recuerdo de los 18meses, 81,1% para la dosis de los 4-6años y 72,5% para la dosis de dT/dTpa en adolescentes a los 14-16años, en 2011)10.
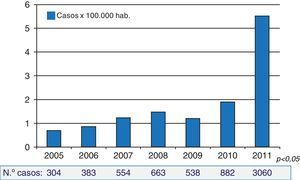
En la figura 2 se muestra la morbilidad por tos ferina declarada en España durante el período 1982-2007. Se produjo un descenso del número de casos superior al 95% entre 1982 y 1999, y desde entonces la tasa ha permanecido estable en cifras cercanas a un caso por 100.000 habitantes11. Sin embargo, a partir de 2010 se ha observado un marcado aumento del número de casos, en especial en el último año, en que la incidencia de la enfermedad se ha incrementado hasta casi 6casos por 100.000habitantes12 (fig. 3). Según datos del Centro Nacional de Epidemiología11, más del 40% de los casos son niños menores de un año, los adolescentes representan más del 14,6% y los adultos son el 12,4%.
La letalidad de la enfermedad varía entre 1,19 por cada 100casos en los menores de un año en 2001 y 1,41 en 2007 11.
Los estudios realizados en España también han confirmado el destacado papel de los contactos familiares adultos como fuente de infección de los niños13-16. Un estudio efectuado por García et al.13 demostró que en el 52% de los casos de tos ferina confirmados por el laboratorio en lactantes ingresados durante el período de mayo de 2002 a diciembre de 2004, en 4hospitales pediátricos españoles, al menos uno de los familiares investigados padecía tos ferina, con tos de más de 21días de duración que había comenzado como mínimo 10días antes del inicio de los síntomas en el caso índice. Los resultados de un estudio internacional prospectivo, en el cual han participado varios hospitales españoles, han sido similares14: el 38% de los contactos familiares de los lactantes ingresados con tos ferina confirmada por el laboratorio en los hospitales españoles participantes en el estudio fueron positivos por reacción en cadena de la polimerasa (PCR) o cultivo. En un estudio realizado para investigar quién contagió a los lactantes ingresados por tos ferina confirmada en el Hospital Vall d’Hebron de Barcelona, durante el período 2005-2008, se encontró el caso primario en el 80% de los pacientes, y en el 83% de los casos eran contactos domiciliarios15. En otro estudio llevado a cabo en el mismo hospital, que también incluyó pacientes con tos ferina no ingresados, pudo identificarse el caso primario en el 56% de los pacientes, ya que no se estudiaron los contactos no domiciliarios de los niños mayores, que muchas veces se contagian en la escuela16. Estos estudios confirman el papel de los contactos familiares, en especial de los padres, como fuente de infección de los casos de tos ferina en los niños.
Vigilancia epidemiológica de la tos ferina: una enfermedad de declaración individualizada infranotificada en EspañaLa tos ferina es una enfermedad de declaración obligatoria en España desde el año 1982 (declaración numérica entre 1982 y 1996, e individualizada a partir de 1997), por lo que las series disponibles de morbilidad declarada según grupos de edad son relativamente cortas. Al igual que ocurre con todos los sistemas de vigilancia pasivos, hay una importante infradeclaración de casos, sobre todo de los que ocurren en adolescentes y adultos17,18. A estas edades son muy pocos los casos diagnosticados, ya que los médicos de atención primaria, a diferencia de los pediatras, están poco sensibilizados con el tema, lo que conlleva un importante infradiagnóstico y la consiguiente infradeclaración.
Según un estudio retrospectivo de las hospitalizaciones por tos ferina en los niños menores de 12meses en 11hospitales de Cataluña, que comprenden más del 90% de la población pediátrica, realizado entre 1997 y 2001, la infradeclaración fue de al menos el 36,4%19.
Los datos procedentes de un programa piloto de vigilancia activa de la tos ferina realizado en Cataluña durante el período 2003-2004 y que incluía información de 40centros de atención primaria y de 11hospitales mostraron una incidencia de 14,9casos por 100.000habitantes, cifra 3veces superior a la declarada en toda Cataluña (4,6casos por 100.000habitantes)20. Estas tasas resultaron muy superiores a las registradas en 2001 y 2002, que fueron de 0,6 y 0,4 por 100.000habitantes, respectivamente. La distribución por edades de los casos declarados durante el período de estudio muestra 2valores extremos: los lactantes menores de 6meses y los preadolescentes y adolescentes de 9-13años de edad. El 81,5% de los casos confirmados en niños menores de 15 años había sido declarados al sistema de notificación microbiológica de Cataluña; por el contrario, solo lo habían sido el 9,3% de los casos confirmados en personas de 15años o más de edad21.
Hospitalizaciones por tos ferina, un indicador más preciso que la declaración individualizada de casos de enfermedades de declaración obligatoriaLa utilización de otras fuentes de información, como el conjunto mínimo básico de datos22 (CMBD) al alta, permite conocer los datos de las hospitalizaciones por tos ferina en nuestro medio y es un sistema útil de información para el estudio de la carga de la enfermedad.
Según recoge la EUVAC-NET23, el 70% de los niños menores de 12meses con tos ferina requieren hospitalización. En España se han publicado diversos estudios al respecto. El más reciente, de Gil Prieto et al.24, analiza los ingresos por tos ferina en España en el período 1999-2005 e incluye datos de 3.277 hospitalizaciones de niños menores de 12meses (tasa de hospitalización de 139,4 por 100.000niños menores de esa edad). El 93% de las hospitalizaciones correspondió a niños menores de 6meses (tabla 1). La edad media fue de 2,7meses y el tiempo medio de hospitalización, de 8,8días. La tasa de mortalidad fue de 0,5 por 100.000 habitantes y la de letalidad, del 0,4%. Estas tasas son superiores a las comunicadas por el mismo grupo para 1995-1998, con cifras de hospitalización de 78 por 100.000 en ese mismo grupo de edad25. Estos resultados sugieren, al igual que los del trabajo realizado en Cataluña por Moraga et al.19 en el período 1997-2001, con tasas de hospitalización de 48casos por 100.000habitantes al inicio del período y de 256 por 100.000 en el año 2000, que la incidencia de la tos ferina está aumentando en los niños menores de un año y especialmente en los menores de 6meses.
Distribución de las hospitalizaciones por tos ferina de lactantes según la edad, en España (1999-2005)
| Edad en meses | Número de hospitalizaciones | Porcentaje |
| 0 | 29 | 0,9 |
| 1 | 887 | 27,1 |
| 2 | 1.057 | 32,3 |
| 3 | 583 | 17,8 |
| 4 | 331 | 10,1 |
| 5 | 157 | 4,8 |
| 6 | 96 | 2,9 |
| 7 | 44 | 1,3 |
| 8 | 23 | 0,8 |
| 9 | 28 | 0,9 |
| 10 | 24 | 0,7 |
| 11 | 15 | 0,5 |
| Total | 3.277 | 100,0 |
Tomada de Gil Prieto et al.24.
Santos et al.26 han estimado también la incidencia de hospitalizaciones por tos ferina en España, en la población general, en el período 1999-2005, y han hallado que el 85,6% de los casos son niños menores de un año y el 95% tienen menos de 5años de edad.
A la vista de estos datos puede afirmarse que el CMBD es un buen indicador de la carga de la enfermedad en los niños menores de 5años, y en particular en los menores de un año, pero la incidencia de tos ferina en los niños mayores, los adolescentes y los adultos debería estimarse a partir de sistemas de vigilancia activa o programas centinela realizados en atención primaria.
Diagnóstico: importancia de la reacción en cadena de la polimerasa en tiempo realEl diagnóstico rápido de la tos ferina es fundamental para iniciar un tratamiento precoz y una adecuada profilaxis en los contactos, y lograr así la interrupción de la cadena de transmisión.
Diagnóstico clínicoEl diagnóstico de la tos ferina en ocasiones es difícil, ya que sus manifestaciones clínicas no siempre son patognomónicas, hay una gran heterogeneidad de los síntomas (sobre todo en los adolescentes y los adultos), la inmunización previa modifica el curso de la enfermedad, son frecuentes las infecciones mixtas y el grado de sospecha entre los médicos sigue siendo bajo. No obstante, hay una serie de síntomas clásicos en los lactantes y niños, en particular en los no vacunados, que suelen presentarse en 3fases diferenciadas: catarral o prodrómica, paroxística o de estado, y convalecencia. La fase catarral dura alrededor de 1-2semanas e incluye síntomas inespecíficos como rinorrea, estornudos, lagrimeo, fiebre baja y tos moderada. En la fase paroxística posterior (duración de 2-6 semanas) el niño empeora y presenta accesos de tos seca irritativa e intermitente en forma de paroxismos, estridor inspiratorio muy característico (gallo) y vómitos postusígenos; los paroxismos de tos aumentan en frecuencia e intensidad (hasta 5-10episodios de tos en una sola fase espiratoria) y puede aparecer dificultad respiratoria, apneas, cianosis y ansiedad por la sensación de asfixia. Los paroxismos pueden ser más graves durante la noche. En la tercera y última fase (convalecencia) la tos disminuye en frecuencia y gravedad, y aunque suele durar unas 2semanas, el paciente puede tardar meses hasta la recuperación completa y presentar recaídas clínicas por infecciones respiratorias virales intercurrentes. En los adultos y en los niños vacunados estas fases pueden no ser reconocibles y apreciarse únicamente una tos crónica paroxística de más de 2semanas de duración. Entre las complicaciones cabe destacar la neumonía, la otitis media, la insuficiencia respiratoria, la encefalopatía, las convulsiones y algunas secuelas físicas secundarias al esfuerzo generado por la tos27. La complicación más grave, que es causa importante de letalidad, es la tos ferina maligna, que se caracteriza por tos paroxística, pausas de apnea y fallo respiratorio progresivo con bronconeumonía e hiperleucocitosis extrema, que conduce a hipertensión pulmonar e hipoxemia rápidamente progresivas, resistentes al tratamiento convencional, que ocasionan shock y la muerte en el 70% de los casos27.
Algunos organismos internacionales, como la Organización Mundial de la Salud (OMS) y los Centers for Disease Control and Prevention (CDC) de Estados Unidos, entre otros, han publicado definiciones de caso estandarizadas para facilitar el grado de sospecha, aunque no son lo suficientemente sensibles y específicas como para conseguir una aceptable detección de los casos (en especial entre los adultos), y su uso ha sido más epidemiológico, o con fines de investigación, que clínico28-30. El último algoritmo propuesto es el de la Global Pertussis Initiative de 2012, basado solo en signos y síntomas clínicos, pero estratificado según 3grupos de edad (0-3meses, 4meses a 9años y ≥10años)31.
Diagnóstico de laboratorioEl hallazgo más característico en los niños, aunque no siempre presente, es la leucocitosis debida a una linfocitosis absoluta que se produce en las fases catarral tardía y paroxística. Su sensibilidad es del 88-89% y la especificidad, del 55-75%32. La cifra absoluta de leucocitos puede oscilar entre 15.000 y 100.000células/mm3, en función de la gravedad del cuadro, y es más frecuente en los niños no vacunados27. También puede detectarse trombocitosis, con recuentos superiores a un millón, e hipoglucemia.
Diagnóstico microbiológicoLas pruebas microbiológicas son la piedra angular del diagnóstico de confirmación de la tos ferina. La sensibilidad y la especificidad de los distintos métodos (tabla 2) depende de diversos factores: edad, exposición anterior a la bacteria, administración previa de antibióticos, inmunización recibida, fase y duración de la enfermedad, tipo de laboratorio, calidad de la muestra y su correcto y rápido transporte y procesamiento33-35. Estos 2últimos aspectos son de suma importancia para la obtención de resultados fiables. La muestra ideal es la obtenida de la nasofaringe posterior36,37. Puede tomarse con hisopo o, preferiblemente, mediante aspirado nasofaríngeo. Los hisopos deben ser de Dacron (para cultivo y PCR) o de alginato cálcico (para cultivo), pero nunca de algodón, ya que estos contienen ácidos grasos tóxicos para Bordetella spp. que invalidan la PCR38.
Diagnóstico de la infección por Bordetella pertussis
| Sensibilidad | Especificidad | Ventajas | Inconvenientes | |
| Diagnóstico clínico | + | ++ | Rápido | Baja sensibilidad en la era vacunal por la mayor proporción de casos atípicos y levesDepende de la experiencia clínica (subjetividad) |
| Cultivo | ++ | ++++ | EstandarizadoPosibilidad de tipificación molecular de la cepaPosibilidad de estudios de sensibilidad | Sensibilidad y especificidad variablesNecesidad de transporte y procesamiento rápidosNecesidad de medios de cultivo específicosLargo tiempo de incubación (7-14días) |
| PCR | +++ | +++ | Rapidez (mayor que el cultivo)No requiere que la bacteria esté viva (puede usarse en fases tardías de la enfermedad) | Posibilidad de falsos positivos (riesgo de contaminación)No estandarizada comercialmenteNo disponible en todos los laboratoriosCoste |
| IFD | + | +++ | Rápida y fácilNo requiere que la bacteria esté viva (puede usarse en fases tardías de la enfermedad) | Sensibilidad y especificidad variablesReactividad cruzada con otras bacteriasNecesidad de personal entrenado y experimentado |
| Serología (ELISA) | +++ | ++++ | FácilPermite diagnóstico en fases muy tardías de la enfermedad (convalecencia) | Solo útil en cuadros de más de 2-3 semanas de evoluciónInterferencia con anticuerpos vacunalesDifícil interpretación de los resultadosNo estandarizada comercialmente |
ELISA: enzyme-linked immunosorbent assay; IFD: inmunofluorescencia directa; PCR: reacción en cadena de la polimerasa.
El aislamiento en cultivo se considera el patrón de referencia por su alta especificidad; además, permite la tipificación molecular de las cepas circulantes, la obtención de datos para vigilancia epidemiológica y la monitorización de los patrones de sensibilidad. Sin embargo, su sensibilidad es baja, entre el 50 y el 70% en las mejores condiciones34, aunque es superior en la fase catarral y al comienzo de la fase paroxística.
Las técnicas de biología molecular, en especial la PCR, se han convertido en herramientas fundamentales no solo para el diagnóstico directo a partir de una muestra sino para la confirmación del aislamiento en cultivo. Su capacidad diagnóstica, su rapidez y su gran sensibilidad (70-99%) han hecho que tanto la OMS como los CDC la hayan incluido en sus definiciones de caso29,30,34. Además, la PCR permite la identificación del microorganismo en casos ya evolucionados (sensibilidad óptima durante las primeras 3 semanas de tos), tras iniciar el tratamiento antibiótico, en pacientes vacunados y en los que presentan síntomas atípicos de la enfermedad. No obstante, su alta sensibilidad y el riesgo de contaminación de la muestra conllevan la posibilidad de resultados falsos positivos36,38,39. Este hecho, unido a la ausencia de kits comerciales estandarizados, implica que más que tratarse de una prueba alternativa al cultivo debe emplearse siempre conjuntamente con este.
Entre las distintas técnicas, la PCR cuantitativa en tiempo real es la más prometedora al tener la capacidad de detectar menores cantidades de ácidos nucleicos, requerir menos tiempo, y tener mayor especificidad y menores tasas de contaminación que la técnica convencional40,41. Las principales dianas de las sondas de PCR en tiempo real son las secuencias IS481, IS1001 e IS1002, el gen de la toxina pertúsica, el gen de la pertactina, el gen de la porina, el gen de la adenilato ciclasa y el gen recA34. Muchos laboratorios clínicos utilizan una única secuencia, que suele ser la IS481, ya que B.pertussis presenta múltiples copias de ella y por tanto aumenta la sensibilidad del test, pero puesto que también está presente (aunque en menor cantidad) en B.holmesii y en B.bronchiseptica, aumenta la probabilidad de falsos positivos36 y debe instarse a los laboratorios a determinar múltiples secuencias para mejorar la especificidad38,39,42,43.
Las técnicas serológicas tienen utilidad diagnóstica en las fases más avanzadas del cuadro clínico, cuando tanto el cultivo como la PCR pierden rentabilidad. Las más utilizadas son el enzimoinmunoensayo (enzyme-linked immunosorbent assay, ELISA) y el inmunoensayo multiplex. Los componentes antigénicos más estudiados son la toxina pertúsica (TP) y la hemaglutinina filamentosa (HFA), aunque solo la primera es específica de B.pertussis, ya que la HFA está presente en B.parapertussis y contiene epítopos que generan reacciones cruzadas con otros microorganismos44.
Tratamiento antiinfeccioso y quimioprofilaxis postexposiciónEl tratamiento precoz, fundamentalmente durante la fase catarral, puede reducir la intensidad y la duración de los síntomas, aunque en algunos pacientes el efecto es escaso45,46 o incluso nulo si se inicia a partir de los 14-21días del comienzo de la tos46. En estos pacientes, el objetivo del tratamiento es disminuir la contagiosidad.
El tratamiento de elección son los macrólidos46-49. La eritromicina fue durante mucho tiempo la primera opción, fundamentalmente por su bajo coste. Sin embargo, la posterior aparición de macrólidos con la misma eficacia y que erradican B.pertussis de la nasofaringe, pero con mejor cumplimiento terapéutico50-52, ha hecho que las guías actuales46,53 y las opiniones de los expertos45,54 recomienden la azitromicina o la claritromicina como macrólidos de elección. En los lactantes menores de un mes es más controvertida la elección del antibiótico. La eritromicina se ha relacionado con la aparición de estenosis hipertrófica de píloro cuando se emplea a esa edad, sobre todo en los primeros 15días de vida55, con un riesgo del 1 al 5%. Los datos son escasos en relación a los otros macrólidos, pero los CDC recomiendan la azitromicina también para este grupo de edad46.
En caso de alergia o intolerancia a los macrólidos, se recomienda utilizar trimetoprim-sulfametoxazol. La dosis recomendada es de 8mg/kg al día de trimetoprim (máximo 160mg/12h), cada 12h, durante 7días53. Está contraindicada en menores de 1-2meses.
En la tabla 3 se muestran las dosis y la duración del tratamiento según el fármaco utilizado.
Posología de los antibióticos para el tratamiento y la quimioprofilaxis de la tos ferina
| Edad | Eritromicina | Claritromicina | Azitromicina |
| <1 mes | No recomendable (asociada a estenosis hipertrófica de píloro) | No recomendable (no datos) | 10mg/kg/24h5días (datos limitados) |
| 1-5 meses | 40mg/kg/día, cada 6h7días | 15mg/kg/día, cada 12h7días (datos limitados) | 10mg/kg/24h5días (datos limitados) |
| 6 meses-14 años | 40mg/kg/día, cada 6h7días (máx: 2g/día) | 15mg/kg/día, cada 12h7días (máx: 1g/día) | 1.er día: 10mg/kg (máx: 500mg/día)2.°-5.° día: 5mg/kg/día (máx: 250mg/día) |
| Adultos | 500mg/6h7días | 500mg/12h7días | 1.er día: 500mg2.°-5.° día: 250mg/día |
Según las recomendaciones de diversos organismos internacionales, deben administrarse macrólidos de forma precoz a los contactos (convivientes asintomáticos) de los casos de tos ferina. Esta indicación es especialmente importante para los niños menores de 12meses48 y sus convivientes, para las mujeres en el tercer trimestre del embarazo y para cualquier persona con una enfermedad de base con riesgo especial para la tos ferina grave46. La quimioprofilaxis no está indicada para compañeros escolares en colegios o institutos, dado el retraso habitual en el diagnóstico del caso índice y las obvias dificultades de implantación de una quimioprofilaxis correcta47.
El tipo de antibiótico y las dosis recomendadas son los mismos que para el tratamiento de los casos (tabla 3)46,49,53. Se aconseja iniciar la quimioprofilaxis lo más pronto posible, pues es más efectiva cuanto antes se instaure. Probablemente la efectividad sea muy baja si se comienza más allá de los 12días de la exposición al inicio de la tos paroxística del caso índice, y nula, y por tanto no recomendable, si han pasado ya más de 21 días46. La única excepción a esta recomendación son los neonatos, en quienes la tos ferina puede ser tan grave que no se tendrá en cuenta el tiempo que haya pasado desde la exposición46.
Aunque no hay una clara evidencia del beneficio de la quimioprofilaxis de la tos ferina para la prevención del cuadro clínico53, su utilidad en el control de la circulación de B.pertussis entre los contactos está bien establecida45.
Prevención. Vacunas actuales (DTPa/dTpa)La vacunación es la principal estrategia preventiva para el control de la tos ferina. Las vacunas antipertussis se presentan clásicamente combinadas con los toxoides tetánico y diftérico, aunque también hay preparados que también incluyen otros antígenos vacunales (poliomielitis, Haemophilus influenzae tipo b y hepatitis B). En España, desde 1998 el componente de la tos ferina es acelular (Pa), y dependiendo de la presentación comercial la vacuna contiene entre uno y 5antígenos de B.pertussis: TP, HFA, pertactina o proteína 69-KDa (PER), y uno o 2tipos de aglutinógenos (Agt) o proteínas de las fimbrias (FIM-2 y FIM-3). También pueden variar la carga de cada antígeno, el clon bacteriano de partida y el método de fabricación. Ninguno de estos factores, por sí solo, es determinante de la eficacia vacunal, aunque la mayoría de los autores coinciden en que la TP es el componente fundamental que debe contener la vacuna56. La composición de las vacunas comercializadas en España se detalla en la tabla 4.
Composición de las vacunas frente a la tos ferina comercializadas en España
| Especialidad (fabricante) | Composición |
| Infanrix® (GSK) | Tres antígenos purificados de B.pertussis: 25μg TP, 25μg HFA, 8μg PER+≥40UI toxoide tetánico+≥30UI toxoide diftéricoAdyuvante: hidróxido de aluminioConservante: 2-fenoxietanol |
| Infanrix-IPV-Hib® (GSK) | Misma composición que Infanrix+10μg polisacárido capsular (PRP) de Hib conjugado con 30μg toxoide tetánico+3tipos de virus de la polio inactivadosAdyuvante: hidróxido de aluminioConservante: 2-fenoxietanol |
| Infanrix Hexa® (GSK) | Misma composición que Infanrix-IPV-Hib+10μg HBsAgAdyuvante: hidróxido y fosfato de aluminioConservante: 2-fenoxietanol |
| Pentavac® (SP-MSD)Boostrix® (GSK) | Dos antígenos purificados de B.pertussis: 25μg TP, 25μg HFA+≥40UI toxoide tetánico+≥30UI toxoide diftérico+10μg polisacárido capsular (PRP) de Hib conjugado con toxoide tetánico+3tipos de virus de la polio inactivadosAdyuvante: hidróxido de aluminioConservante: 2-fenoxietanolTres antígenos purificados de B.pertussis: 8μg TP, 8μg HFA, 2,5μg PER+≥20UI toxoide tetánico+≥2UI toxoide diftéricoAdyuvante: hidróxido y fosfato de aluminioConservante: 2-fenoxietanol |
| Triaxis® (SP-MSD) | Cinco antígenos purificados de B.pertussis: 2,5μg TP, 5μg HFA, 3μg PER, 5μg FIM2, FIM3+≥20UI toxoide tetánico+≥2UI toxoide diftéricoAdyuvante: fosfato de aluminioConservante: fenoxietanol |
Aunque se han realizado numerosos estudios de inmunogenicidad, la comparación entre ellos es difícil porque las poblaciones y las pruebas serológicas utilizadas son distintas. En el estudio multicéntrico Multicenter Acellular Pertussis Trial (MAPT) se compararon 13vacunas acelulares y 2de células enteras57; todas produjeron aumentos significativos de anticuerpos frente a los antígenos que contenían, que en la mayoría de los casos igualaron o superaron a las concentraciones inducidas por la vacuna de células enteras de referencia. Las cifras de anticuerpos alcanzadas frente a PER, HAF, FIM-2 y FIM-3 se asociaron con la cantidad de antígeno contenido en la vacuna, hecho no observado con la TP. No existe un marcador o correlator de protección que pueda generalizarse a todas las vacunas acelulares. En un ensayo clínico aleatorizado realizado en Alemania se observó que solo la TP y la PER se asociaban significativamente con la protección58. Por otro lado, los datos de 2ensayos clínicos de eficacia realizados en Suecia indicaron que tras una exposición a B.pertussis se incrementan las concentraciones de anticuerpos frente a los antígenos contenidos en la vacuna de forma más importante que frente a otras proteínas de la bacteria, lo que sugiere que cuantos más antígenos contenga la vacuna, mayor protección podría generar59. En una reciente revisión Cochrane se han evaluado 6ensayos clínicos de eficacia y se ha estimado que con las vacunas acelulares multicomponente (con al menos 3antígenos frente a B.pertussis) la eficacia oscila entre el 84 y el 85% para la prevención de la tos ferina típica, y entre el 71 y el 78% para la tos ferina leve. Por el contrario, la eficacia de las vacunas de uno o 2componentes antigénicos es menor: del 59 al 75% para la tos ferina típica y del 13 al 54% para la tos ferina leve60.
El amplio uso, durante más de 20años, de la vacuna acelular en Japón y Suecia, tras un período sin vacunación, convierte a ambos países en buenos ejemplos para ilustrar la efectividad vacunal. En Japón, tras 100millones de dosis de DTPa administradas entre 1981 y 2003, la incidencia de tos ferina descendió de 11,3 por 100.000habitantes en 1979 a prácticamente cero en 200261. En Suecia, la incidencia de casos confirmados por laboratorio disminuyó de 121-150 por 100.000 en 1994-1995 a 12-15 por 100.000 a los 10años de introducir la vacunación sistemática62. Al comparar el año 1997 con el 2007, la incidencia de la enfermedad en los niños de 3-5meses de edad pasó de 264 por 100.000 en los niños no vacunados a 155 por 100.000 en los que solo habían recibido una dosis. En el grupo de 5-12meses de edad la incidencia fue de 526, 95 y 24 por 100.000 en los no vacunados y los inmunizados con una dosis o con 2dosis, respectivamente63. El ejemplo de Suecia indica, no obstante, que la efectividad vacunal no es óptima, y que hay factores, como la pérdida de la inmunidad con el tiempo y la expansión de clones con polimorfismo antigénico, que explican que la vacuna de la tos ferina sea quizás la de efectividad más baja de las vacunas pediátricas62.
Los efectos adversos sistémicos y locales son menos frecuentes con las vacunas acelulares que con las enteras, tanto en la serie primaria como en las dosis de recuerdo60,64. No obstante, la tasa y la intensidad de las reacciones locales a las vacunas acelulares tienden a aumentar con cada dosis de DTPa65.
Los estudios de inmunogenicidad de las vacunas DTPa combinadas con otros antígenos (DTPa-IPV; DTPa-IPV/Hib; DTPa-IPV/Hib/VHB) han mostrado no inferioridad en cuanto a seroprotección y eficacia, así como un perfil de seguridad comparable al de la administración de los componentes por separado66-68.
Se desconoce la duración de la protección, pero se sabe que la inmunidad, al igual que ocurre después de padecer la enfermedad, no es permanente y disminuye con el tiempo69. Esto justifica que para conseguir una adecuada protección en todos los grupos de edad sea necesario administrar también dosis de recuerdo a los adolescentes y los adultos.
Vacunas dTpa: inmunogenicidad, eficacia, efectividad y seguridadEn nuestro medio se dispone de 2preparados: Boostrix® (GlaxoSmithKline) y Triaxis® (Sanofi Pasteur MSD) (tabla 4). Ambos son vacunas dTpa y están indicados para la inmunización activa frente al tétanos, la difteria y la tos ferina a partir de los 4años de edad como dosis de recuerdo tras la inmunización primaria. Son una alternativa como dosis booster para los niños de 4-6años de edad.
En todos los ensayos clínicos realizados con Boostrix® se ha observado que, un mes después de la vacunación, el 80% de los adolescentes y adultos mostraron una adecuada respuesta inmunitaria70-76. Estudios realizados en niños de 4 a 6 años de edad muestran una inmunogenicidad similar a la de la vacuna DTPa, pero con un mejor perfil de seguridad77. En las personas de 40años o más de edad que no hayan recibido ninguna dosis de vacuna antidiftérica o antitetánica en los últimos 20años, una dosis de Boostrix® induce una respuesta de anticuerpos contra la tos ferina y protege frente al tétanos y la difteria en la mayoría de los casos, aunque serían necesarias 2dosis adicionales de vacuna dT, administradas uno y 6meses después de la primera dosis, para incrementar la respuesta frente a la difteria y el tétanos. Puede utilizarse para la profilaxis de heridas potencialmente tetanígenas en personas que hayan recibido previamente una serie primaria de vacunación con vacuna con toxoide tetánico y en quienes esté indicada una dosis de recuerdo frente a la difteria y la tos ferina.
Las tasas de seroprotección/índices de seropositividad observadas a los 3-3,5años y 5-6años después de la vacunación en los adolescentes y los adultos son similares a las descritas para los niños (tabla 5). Según un ensayo clínico controlado realizado en Estados Unidos, la eficacia de una dosis de esta vacuna en los adultos es muy alta (92%; intervalo de confianza del 95%: 32-99%)78. Las reacciones adversas más frecuentes asociadas con la administración de la vacuna han sido de tipo local, en el lugar de inyección (dolor, enrojecimiento e inflamación), y se han comunicado en el 50 al 92% de los sujetos69.
Tasas de seroprotección alcanzadas con la vacuna dTpa (Boostrix®) en niños, adolescentes y adultos
| Antígeno | Seroprotección/seropositividad | Adultos y adolescentes ≥10 años de edad (% vacunados) | Niños ≥4 años de edad (% vacunados) | ||
| Persistencia 3-3,5años | Persistencia 5años | Persistencia 3-3,5años | Persistencia 5-6años | ||
| Difteria | ≥0,1UI/ml | 71,2-91,6 | 84,1-86,8 | 97,5 | 94,2 |
| ≥0,016UI/mla | 97,4-100 | 94,4-99,2 | 100 | No determinado | |
| Tétanos | ≥0,1UI/ml | 94,8-100 | 96,2-100 | 98,4 | 98,5 |
| Tos ferina | |||||
| Toxoide pertúsico | ≥5UEL/ml | 81,6-90,6 | 76,8-89,5 | 58,7 | 51,5 |
| Hemaglutinia filamentosa | 100 | 100 | 100 | 100 | |
| Pertactina | 94,8-99,2 | 95,0-98,1 | 99,2 | 100 | |
Los ensayos clínicos realizados con Triaxis® muestran también que la vacuna induce una respuesta inmunógena adecuada frente a la difteria, el tétanos y la tos ferina, no inferior a la generada por las vacunas DTPa. La respuesta frente al tétanos y la difteria es similar a la inducida por una dosis única de vacuna dT62,79 (tabla 6). No se dispone de ensayos clínicos de eficacia realizados con Triaxis®, pero esta se ha estimado a partir de la correlación entre el título de anticuerpos (media geométrica de la concentración de anticuerpos) y la protección clínica frente a la tos ferina observada en los ensayos clínicos realizados en niños en Suecia en 1992-1996. La eficacia estimada al mes de la administración de una dosis en adolescentes y adultos, en comparación con la observada en niños un mes después de la vacunación primaria con una pauta de 2, 4 y 6meses de edad, es superior en todos los casos y para todos los antígenos contenidos en la vacuna62,80. El perfil de seguridad de Triaxis® es muy bueno, con una menor reactogenicidad, tanto para reacciones adversas locales como sistémicas, que la observada con la vacuna DTPa.
Inmunogenicidad de la vacuna dTpa (Triaxis®) en niños, adolescentes y adultos
| Antígeno | Respuesta inmunitaria | Seroconversión niños 4-6años (%) | Seroconversión adolescentes 11-17años (%) | Seroconversión adultos 18-64años (%) |
| Toxoide tetánico | ≥0,1UI/ml | 100 | 99,8 | 94,1 |
| Toxoide diftérico | ≥0,1UI/ml | 100 | 100 | 100 |
| Toxoide pertúsico | Respuesta de recuerdo (booster) | 91,9 | 92 | 84,4 |
| Hemaglutinina filamentosa | 88,1 | 85,6 | 82,7 | |
| Pertactina | 94,6 | 94,5 | 93,8 | |
| Fimbrias tipos2 y 3 | 94,3 | 94,9 | 85,9 |
Las estrategias de vacunación frente a la tos ferina en Europa difieren entre países (tabla 7) (puede consultarse información actualizada en la página web del ECDC81). Todos los países utilizan preparados de vacuna acelular para la primovacunación y la primera dosis de recuerdo en el primer año de vida, excepto Polonia, que es el único país que sigue vacunando con preparado de células enteras. La mayoría utilizan pautas de primovacunación con 3dosis, con diferentes esquemas (2, 4 y 6meses; 2, 3 y 4meses; 3, 4 y 5meses), menos algunos que usan pautas de 2dosis, como los países escandinavos, Islandia, Eslovaquia e Italia. La administración de la primera dosis de recuerdo se realiza en un amplio intervalo de edad (hasta los 24meses), ya que algunos países incluso vacunan antes de los 12meses (p.ej., Eslovaquia a los 10meses y Holanda a los 11meses). En el Reino Unido e Irlanda no se administra el refuerzo del segundo año de vida. En cuanto a la dosis de recuerdo de los 3-7años de edad, solo realizan vacunación con preparado de baja carga antigénica (dTpa) Alemania y España (excepto en Asturias, Castilla-La Mancha y Extremadura, que continúan usando vacuna DTPa). En Austria, Eslovenia, Francia, Letonia, Malta y Turquía no se administra la segunda dosis de recuerdo.
Esquemas de vacunación frente a la tos ferina en Europa (fuente:http://www.ecdc.europa.eu, última actualización: 30 octubre 2012)
| País | Tipo de vacuna y pauta en primovacunación (≤6meses) | Tipo de vacuna y edad del primer recuerdo (10-24meses) | Tipo de vacuna y edad del segundo recuerdo (3-7años) | Tipo de vacuna y edad del tercer recuerdo (10-18años) |
| Alemania | DTPa (3 dosis: 2, 3, 4) | DTPa (11-14) | dTpa (5-6) | dTpa (9-17) |
| Austria | DTPa (3 dosis: 2, 4, 6) | DTPa (12-24) | No | DTPa (13-16) |
| Bélgica | DTPa (3 dosis: 2, 3, 4) | DTPa (15) | DTPa (5-7) | No |
| Bulgaria | DTPa (3 dosis: 2, 3, 4) | DTPa (16) | DTPa (6) | No |
| Chipre | DTPa (3 dosis: 2, 4, 6) | DTPa (15-18) | DTPa (4-6) | No |
| Croacia | DTPa (3 dosis: 2, 4, 6) | DTPa (12-18) | DTPa (3) | No |
| Dinamarca | DTPa (2 dosis: 3, 5) | DTPa (12) | DTPa (5) | No |
| Eslovaquia | DTPa (2 dosis: 2, 4) | DTPa (10) | DTPa (5) | No |
| Eslovenia | DTPa (3 dosis: 3, 4-5, 6) | DTPa (12-24) | No | No |
| España | DTPa (3 dosis: 2, 4, 6) | DTPa (15-18) | dTpa (4-6)a | dTpa (14-16)b |
| Estonia | DTPa (3 dosis: 3, 4, 6) | DTPa (24) | DTPa (6-7) | No |
| Finlandia | DTPa (2 dosis: 3, 5) | DTPa (12) | DTPa (4) | dTpa (14-15) |
| Francia | DTPa (3 dosis: 2, 3, 4) | DTPa (16-18) | No | DTPa (11-13) |
| Grecia | DTPa (3 dosis: 2, 4, 6) | DTPa (15-18) | DTPa (4-6) | No |
| Holanda | DTPa (3 dosis: 2, 3, 4) | DTPa (11) | DTPa (4) | No |
| Hungría | DTPa (3 dosis: 2, 3, 4) | DTPa (18) | DTPa (6) | No |
| Irlanda | DTPa (3 dosis: 2, 4, 6) | No | DTPa (4-5) | No |
| Islandia | DTPa (2 dosis: 3, 5) | DTPa (12) | DTPa (4) | No |
| Italia | DTPa (2 dosis: 2-3,4-5) | DTPa (10-12) | DTPa (5-6) | dTpa (11-15) |
| Letonia | DTPa (3 dosis: 3, 4, 6) | DTPa (18) | No | No |
| Lituania | DTPa (3 dosis: 2, 4, 6) | DTPa (18) | DTPa (6-7) | No |
| Luxemburgo | DTPa (3 dosis: 2, 3, 4) | DTPa (12) | DTPa (5-6) | dTpa (15-16) |
| Malta | DTPa (3 dosis: 2, 3, 4) | DTPa (18) | No | No |
| Noruega | DTPa (2 dosis: 3, 5) | DTPa (12) | DTPa (7) | No |
| Polonia | DTPe (3 dosis: 2,3-4,5-6) | DTPe (16-18) | DTPa (6) | No |
| Portugal | DTPa (3 dosis: 2, 4, 6) | DTPa (18) | DTPa (5-6) | No |
| Reino Unido | DTPa (3 dosis: 2, 3, 4) | No | DTPa (3-5) | No |
| República Checa | DTPa (3 dosis: 3, 4, 5) | DTPa (11-18) | DTPa (5) | No |
| Rumanía | DTPa (3 dosis: 2, 4, 6) | DTPa (12) | DTPa (4) | No |
| Suecia | DTPa (2 dosis: 3, 5) | DTPa (12) | DTPa (5-7) | dTpa (14-16) |
| Suiza | DTPa (3 dosis: 2, 4, 6) | DTPa (15-24) | DTPa (4-7) | No |
| Turquía | DTPa (3 dosis: 2, 4, 6) | DTPa (18-24) | No | No |
Se recomienda una dosis de recuerdo en la adolescencia con dTpa en 21países del mundo (entre ellos Australia, Canadá, Estados Unidos, Argentina, Panamá, Paraguay, Uruguay, México y varios europeos, como Austria, Francia, Alemania, Finlandia, Islandia, Irlanda, Grecia, Israel, Italia, Luxemburgo, Suiza y Suecia)81,82. En España, la Comunidad de Madrid y las ciudades autónomas de Ceuta y Melilla la recomiendan en sus calendarios de vacunación sistemática. Austria y Francia no utilizan vacunas de baja carga antigénica para la dosis de recuerdo. La edad de administración de esta dosis es variable, entre los 9 y los 17años de edad, aunque la mayoría la recomiendan a los 14años.
Algunos países europeos recomiendan también estrategias de vacunación para adultos1. En Alemania y Francia se indica la vacunación de todos los adultos que hayan recibido la última dosis de vacuna frente a la tos ferina más de 10años antes, complementada con la estrategia del nido (cocoon strategy) y la vacunación del personal sanitario83,84. Bélgica tiene implementada una estrategia activa de cocoon strategy ampliada, con vacunación del entorno familiar del niño, de los profesionales sanitarios y de los cuidadores de guardería85.
Nuevas estrategias vacunalesVacunación del adolescenteLa infección por B.pertussis continúa presente debido a la disminución de la inmunidad adquirida tanto por la vacunación como por el padecimiento de la enfermedad, así como por la menor efectividad de las vacunas acelulares contra la tos ferina y por la potencial contribución de los cambios genéticos en las cepas circulantes de B.pertussis86. Además, hay que considerar también el reciente aumento en su atención y declaración y las mejoras en su diagnóstico gracias a la disponibilidad de la PCR.
Los adolescentes adquieren la infección y la transmiten al recién nacido y al lactante que todavía no están protegidos por la primovacunación. Esta situación epidemiológica ha hecho que en los últimos años se haya considerado en muchos países la necesidad de optimizar la inmunidad del adolescente utilizando la vacuna dTpa1. La Global Pertussis Initiative recomendó hace ya algunos años, como primer paso para afrontar el problema del desplazamiento de los casos de tos ferina hacia la adolescencia y la edad adulta en los países que han alcanzado amplias coberturas vacunales en la edad infantil, la introducción en el calendario de vacunaciones sistemáticas de la vacuna dTpa en la adolescencia, sustituyendo a la dosis de refuerzo de vacuna dT87,88.
El objetivo primario de esta recomendación es proteger al propio adolescente, y el secundario es disminuir las fuentes de infección por B.pertussis en la comunidad y con ello la incidencia de la enfermedad en los otros grupos de edad, en especial en los lactantes menores de 6meses89. Su principal ventaja es que la población diana es fácil de identificar y el programa de inmunización sencillo de aplicar, sobre todo si se realiza en el ámbito escolar; no obstante, la vacunación solo de los adolescentes no proporcionará suficiente protección ni inmunidad de grupo, y los datos sobre la efectividad y la eficiencia de dicha estrategia son escasos, ya que su introducción es relativamente reciente en muchos países. Tras incorporar dicha estrategia en la región del noroeste de Canadá90 en octubre de 2000, la incidencia de tos ferina disminuyó de 7,2casos por 10.000habitantes en el período 1997-2000, previo al programa, a 1,1casos por 10.000 en 2001-2004. En British Columbia91, la vacunación sistemática de los adolescentes de 14-16 años de edad con dTpa se introdujo en 2004, y en 2006 se observó una reducción global del 84% en la incidencia de la enfermedad en este grupo de edad. Sin embargo, aún no hay evidencias de que estos programas de vacunación en la adolescencia tengan un impacto significativo sobre la tos ferina grave del lactante92,93.
La inclusión de la vacuna dTpa en el calendario del adolescente es fácil y no tiene un coste elevado, ya que se trata de sustituir la vacuna dT. La estrategia de vacunación frente a la tos ferina a partir de los 4-6años de edad, cuando se administra la quinta y última dosis de DTPa (dTpa en la mayoría de comunidades) en los calendarios de inmunizaciones sistemáticas de España, debe proseguir con la vacuna dTpa en el adolescente. Solo las ciudades autónomas de Ceuta y Melilla y la Comunidad de Madrid han incluido una sexta dosis con vacuna dTpa a los 14años de edad, en 2002, 2008 y 2011, respectivamente.
El Comité Asesor de Vacunas de la Asociación Española de Pediatría incluyó la dosis del adolescente en el calendario de 2005, y a partir de 2012 en la franja de edad de los 11 a los 14años. En el calendario propuesto para 2013 se recomienda la vacuna combinada de baja carga antigénica frente al tétanos, la difteria y la tos ferina (Tdpa) a los 4-6años, pero obligatoriamente seguida de otra dosis de Tdpa a los 11-14años, con preferencia a los 11-12años94.
Si se tiene en cuenta que la inmunidad adquirida por la vacunación disminuye a lo largo del tiempo y a los 5años de la última dosis menos de la mitad de los vacunados mantienen la protección75, este grupo de trabajo considera también que probablemente la mejor edad para administrar dicha dosis es entre los 11 y los 12años.
Vacunación sistemática del adultoLos objetivos de la vacunación universal antipertussis de los adultos, como continuación de la vacunación pediátrica, son los siguientes: reducir la morbilidad en los adultos, desarrollar inmunidad de grupo, disminuir la transmisión a los lactantes y reducir la incidencia de la enfermedad en todos los grupos de edad. La estrategia de la vacunación sistemática del adulto tiene, sin embargo, dificultades logísticas y económicas para su aplicación. Entre las principales limitaciones cabe destacar que, a diferencia de los adolescentes, el acceso a esta población es más difícil, lo que conlleva que las coberturas vacunales sean en general bajas. La vacunación frente a la tos ferina se encuentra «indisolublemente» ligada a la vacunación antitetánica y antidiftérica. En los adultos, las políticas de vacunación frente al tétanos varían de unos países a otros: desde dosis de recuerdo decenales, generalmente con Td, hasta 2, una o ninguna dosis (todo ello en ausencia de heridas potencialmente tetanígenas). En España, las recomendaciones del Ministerio de Sanidad, Asuntos Sociales e Igualdad de 2009 contemplan, para las personas correctamente primovacunadas en la infancia, la administración de una única dosis de vacuna Td hacia los 65años de edad95. Esta estrategia, que puede ser adecuada para el tétanos y posiblemente para la difteria, no resuelve —más bien al contrario— el problema de la tos ferina. En este sentido, el recuerdo decenal con vacuna dTpa podría ser una política vacunal a considerar. Así, al menos 2estudios recientes han mostrado el buen perfil de inmunogenicidad y seguridad, en los adultos, de dosis de recuerdo de vacuna dTpa administradas cada 10años96,97.
En la ficha técnica de Boostrix® se señala que la vacunación repetida frente a la difteria, el tétanos y la tos ferina debe realizarse en los intervalos establecidos en las recomendaciones oficiales, generalmente cada 10 años69.
Vacunación del personal sanitarioLa vacunación de los profesionales sanitarios que pueden ser fuente de infección para los lactantes, a menudo con unas condiciones de salud previa más precaria (prematuridad, etc.), es una estrategia recomendada en muchos países. En los últimos años se han publicado numerosos brotes nosocomiales de tos ferina98-101, con un número de profesionales sanitarios expuestos muy alto. Se han estimado los costes totales (directos e indirectos) asociados al tratamiento de los casos secundarios y a la profilaxis del personal sanitario y de los pacientes en contacto, con cifras que oscilan entre 69.000 y 263.000dólares por brote, mucho más que el coste generado por la vacunación con dTpa de todo el personal sanitario que trabajaba en servicios o áreas de riesgo. Se dispone, por tanto, de suficientes evidencias de que los trabajadores de la salud resultan afectados en el curso de los brotes nosocomiales de tos ferina y contribuyen a propagar la enfermedad entre los pacientes que atienden. Habría que priorizar la vacunación de los sanitarios en contacto con población pediátrica. La OMS ha recomendado específicamente la vacunación del personal sanitario, en especial de maternidades y unidades pediátricas, en los países con una alta tasa de transmisión nosocomial102.
Aunque hay menos evidencia sobre la vacunación de otros profesionales, la inmunización de los trabajadores de guarderías que cuidan a niños menores de 3años también contribuiría a reducir la infección de estos profesionales y de su papel como fuentes de infección para los niños que cuidan. La vacunación del personal sanitario y de guarderías podría ser considerada en cierto modo como una «ampliación» de la estrategia del nido, centrada en la vacunación de las personas del entorno próximo de la población pediátrica más susceptible.
Estrategia del nidoDiferentes estudios han mostrado que hasta en el 84% de los casos la fuente de infección o caso primario de la tos ferina en el lactante es un conviviente domiciliario, generalmente un miembro de la familia13-16,103-108 (tabla 8). Por este motivo, entre las actuales recomendaciones de vacunación contra la tos ferina en algunos países se incluye la administración de una dosis de vacuna dTpa de recuerdo para todas las personas que tienen contacto con un lactante: padres, hermanos, abuelos y cuidadores. Aunque la madre es la transmisora más frecuente, la inmunización solo de las madres después del parto no es suficiente para reducir las infecciones por B.pertussis en los lactantes menores de 6meses109, y los esfuerzos deben dirigirse a la inmunización de todos los convivientes en el mismo domicilio. La vacunación de los contactos domiciliarios debe realizarse, al menos, 2semanas antes del nacimiento, en todos los futuros contactos de lactantes menores de 6-12meses47,110-112. Se ha estimado que cuando la estrategia del nido está bien implementada puede reducir hasta el 70% de los casos de tos ferina en los lactantes menores de 3meses113. No obstante, esta estrategia es difícil de realizar por obstáculos logísticos y económicos, como lo demuestran las bajas coberturas alcanzadas en los países que la han implementado, debido a la complejidad de acceder a todas las personas y grupos candidatos a vacunarse, y a los diversos especialistas a quienes corresponde hacerlo (obstetras, médicos de familia, pediatras, especialistas en medicina preventiva, médicos de salud laboral, geriatras…). Las estrategias dirigidas a «grupos de riesgo» (entendiendo como tales a las personas que tienen el riesgo de contagiar al lactante) no alcanzan coberturas tan altas como las vacunaciones sistemáticas. Por tanto, esta estrategia por sí sola es insuficiente para prevenir la morbilidad y la mortalidad de la tos ferina en el lactante pequeño, e influye poco en la disminución de la incidencia global de la enfermedad114.
Estudios publicados sobre la fuente de transmisión de la tos ferina
| Autor (año) | País | Casos índice (n) | Fuente identificada (%) | Principal transmisor |
| Halperin107 (1999) | Canadá | 1.082 | 40 | Hermanos |
| Renacoq108 (2007) | Francia | 1.688 | 53 | Padres |
| Crowcroft106 (2003) | Inglaterra | 33 | 42 | Padres |
| Bisgard104 (2004) | Estados Unidos | 616 | 43 | Padres |
| Wendelboe103 (2007) | Multinacional | 94 | 48-78 | Padres |
| Kowalzik14 (2007) | Multinacional | 99 | 27 | Padres |
| Iglesias15 (2009) | España | 52 | 80 | Padres |
| De Greeff105 (2010) | Holanda | 201 | 84 | Hermanos |
| Uriona16 (2012) | España | 91 | 56 | Padres |
Los estudios de coste-efectividad de la estrategia del nido son controvertidos: algunos demuestran que la vacunación de los contactos domiciliarios ahorra dinero115,116, pero otros son más críticos y ponen en duda su eficacia por considerarla ineficiente y consumir muchos recursos, estimando que para prevenir una muerte infantil es necesario vacunar por lo menos un millón de padres; para evitar un ingreso en la unidad de cuidados intensivos, 100.000 padres, y para prevenir una hospitalización infantil, más de 10.000 padres necesitarían recibir la vacuna dTpa117. La experiencia de California ha sido demostrativa, al poner en práctica la estrategia del nido en el contexto del brote de tos ferina que en 2010 tuvo una tasa de 435casos por 100.000niños menores de 6meses, con 10muertes de menores de 3meses118. Esta estrategia logró un descenso brusco de los casos de tos ferina en California (de 9.154casos de tos ferina declarados en 2010 a 2.795casos en 2011) y ha permitido revalorizar en parte la estrategia del nido.
Australia, Francia, Alemania, Canadá, Suiza y Estados Unidos recomiendan la estrategia del nido en sus programas para el control de la tos ferina.
Vacunación precoz en el neonato y en el lactanteLos primeros 3meses de vida son el período de mayor riesgo de mortalidad por tos ferina, dado que hay una mayor probabilidad para desarrollar el llamado síndrome de la tos ferina maligna. En Estados Unidos, el 80% de las muertes se producen en lactantes menores de 3meses119. La protección es escasa a esta edad, puesto que aún no han iniciado o completado la primovacunación. Por ello se han investigado diversas estrategias, como la vacunación en los primeros días de vida, para conseguir una protección adecuada lo antes posible. Solo las vacunas frente a la hepatitis B, la BCG y la polio oral están autorizadas para su administración en el período neonatal120; la edad mínima de administración de las vacunas frente a la tos ferina actualmente disponibles es de 6semanas para la primera dosis y de 10semanas para la segunda.
Se han realizado 2estudios en los que se administró una dosis de vacuna monovalente antipertúsica acelular al nacimiento y la segunda dosis a los 2-3meses de edad, con buena respuesta inmunitaria121,122. Sin embargo, el esquema que ha mostrado una mejor respuesta en el período de máximo riesgo consiste en la administración de una dosis de vacuna monocomponente acelular al nacimiento y la segunda al mes de vida119. Solo se dispone de un estudio realizado con vacuna combinada (DTPa) en el período neonatal, y se observó una peor respuesta inmunitaria frente a la pertactina, la toxina pertúsica y la difteria en comparación con el esquema convencional123.
Uno de los posibles inconvenientes de la vacunación temprana sería la interferencia de los anticuerpos maternos, pero actualmente es poco probable que, en ausencia de una dosis de recuerdo materna reciente, las madres transfieran anticuerpos de forma significativa a sus hijos. Tampoco se ha demostrado que la vacunación durante los primeros días de vida produzca una inmunotolerancia a las dosis sucesivas de vacuna, incluso tras la de recuerdo del segundo año de vida124.
Vacunación de la embarazadaLa vacunación materna durante el embarazo tiene una doble finalidad: en primer lugar, evitar que la mujer adquiera la tos ferina y contagie al neonato, lo que es una forma de estrategia del nido, pero «a tiempo», cosa que no sucede cuando se vacuna en el posparto, cuando la mujer está desprotegida durante al menos 2semanas; y en segundo lugar, la transmisión pasiva transplacentaria de anticuerpos al feto, que lo protegerán hasta que inicie la primovacunación a los 2-3 meses de edad. Se trata de una forma de inmunización que ofrece una doble protección, a la madre y al recién nacido (protección directa e indirecta)125.
En octubre de 2011, los CDC publicaron una nueva recomendación sobre la utilización de la vacuna dTpa: la vacunación de la embarazada a partir de la semana 20 de gestación para proteger al lactante, en especial al menor de 3meses110. La situación epidemiológica de la tos ferina en Estados Unidos, en concreto durante el año 2010, con importantes brotes, como el de California, que afectó a 10.000personas, y el aumento del número de muertes en el lactante hasta los 3meses de edad (en el último decenio se ha multiplicado por 3,5 en relación a la década de 1980: 175 frente a 49), ha obligado a las autoridades sanitarias a reconsiderar la prevención de la tos ferina para proteger al recién nacido y al lactante en los primeros 3meses de la vida126. La estrategia de vacunación de la embarazada, que han incorporado diversos organismos y sociedades, entre ellos el American College of Obstetricians and Gynecologists127 en marzo de 2012 y la American Academy of Pediatrics47, es el gran cambio en las medidas preventivas en esta última década. Recientemente, en septiembre de 2012, el Reino Unido ha recomendado de forma excepcional y transitoria la vacunación contra la tos ferina en todas las embarazadas entre las semanas 28 y 38 de gestación como respuesta a la epidemia de tos ferina que están padeciendo128.
Aunque la evidencia científica sobre la seguridad y la inmunogenicidad de la vacuna dTpa en la embarazada es escasa, se dispone de datos suficientes sobre el uso de la vacuna dT en gestantes que indican una buena tolerabilidad129. La incorporación del componente pertúsico probablemente no incrementa el riesgo de efectos adversos para la madre y el feto.
Se estima que la vida media de los anticuerpos antipertusis transferidos es de unas 6semanas110. Esta estrategia puede ser más efectiva y eficiente que la del nido116 y que la vacunación en el posparto antes del alta hospitalaria109. Algunos modelos matemáticos han mostrado una mayor reducción de los casos de tos ferina en los lactantes en los primeros meses de vida con la estrategia de vacunar a las embarazadas que con la estrategia del nido vacunando a madres, padres y abuelos130.
La inmunización pasiva que el recién nacido adquiere por el paso transplacentario de anticuerpos IgG específicos se espera que le proteja y modifique la gravedad de la enfermedad durante el período de máximo riesgo, que son los primeros 3 meses de vida, cuando todavía no está protegido por la primovacunación. Además, los anticuerpos maternos no interfieren con la respuesta inmunitaria a las vacunas acelulares que se administran a partir de los 2meses de edad117,130, aunque puede haber un breve período de tiempo con una menor respuesta vacunal del lactante110. El potencial beneficio de la protección conferida por los anticuerpos maternos en el lactante menor de 3 meses siempre es superior al posible riesgo de que aparezca tos ferina en el lactante mayor por la disminución de la inmunogenicidad de la serie primaria.
La vacunación de la embarazada debe recomendarse junto con la estrategia del nido, vacunando a los futuros contactos del lactante al menos 2semanas antes del nacimiento110.
Recomendaciones del grupo de trabajoLa situación epidemiológica actual de la tos ferina en España obliga a plantear la necesidad de incorporar nuevas estrategias vacunales para un mejor control de la infección. En la tabla 9 se resumen las nuevas estrategias de vacunación frente a la tos ferina.
Recomendaciones del grupo de trabajo sobre las nuevas estrategias de vacunación frente a la tos ferina
| Estrategia | Nuevas estrategias de vacunación frente a la tos ferina | ||
| Objetivo primario | Objetivo secundario | Población diana | |
| Adolescentes | Reducir la morbilidad en adolescentes y desarrollar inmunidad de grupo | Reducir la transmisión a lactantes | Todos los adolescentes (a los 11-14años, preferentemente a los 11-12años) |
| Adultos | Reducir la morbilidad en adultos y desarrollar inmunidad de grupo | Reducir la transmisión a lactantes | Todos los adultos (cada 10años) |
| Personal sanitario | Reducir el riesgo de transmisión nosocomial | Reducir la morbilidad en el personal sanitario | Todo el personal sanitario (prioridad personal de servicios pediátricos y de obstetricia) |
| Cuidadores de guardería | Reducir la transmisión a lactantes y niños pequeños | Reducir la morbilidad en cuidadores | Todos los cuidadores |
| Convivientes (estrategia del nido) | Reducir la transmisión a lactantes | Reducir la morbilidad en la familia y convivientes | Contactos familiares y convivientes de recién nacidos (vacunar como mínimo 15días antes del parto) |
| Embarazada | Protección a los recién nacidos por paso transplacentario de anticuerpos protectores y reducción del riesgo de transmisión madre-hijo | Reducir la morbilidad en las embarazadas | Todas las embarazadas (tercer trimestre de gestación) |
MC ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline y Sanofi Pasteur MSD, y ha colaborado como investigador en ensayos clínicos desarrollados por GlaxoSmithKline y Sanofi Pasteur MSD.
DMP ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline y Sanofi Pasteur MSD.
AGM ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline y Sanofi Pasteur MSD.
FAML ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline y Sanofi Pasteur MSD.
JAF ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline y Sanofi Pasteur MSD.
JMB ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline y Sanofi Pasteur MSD, y ha colaborado como investigador en ensayos clínicos desarrollados por GlaxoSmithKline y Sanofi Pasteur MSD.
FGR, AGM y LSS declaran que no existe ningún conflicto de intereses.
Este documento está avalado por las siguientes sociedades científicas: Asociación Española de Pediatría; Asociación Española de Vacunología; Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica; Sociedad Española de Ginecología y Obstetricia; Sociedad Española de Infectología Pediátrica; Sociedad Española de Medicina Preventiva, Salud Pública e Higiene; Sociedad Española de Médicos Generales y de Familia; Sociedad Española de Quimioterapia: Infección y Vacunas.
Las recomendaciones del documento están basadas en los datos y resultados de los estudios disponibles hasta el momento de la publicación.
Este artículo se publica simultáneamente en la revista Medicina Preventiva (Edimsa, Madrid).