Dar soporte a los profesionales no especialistas en el tema a la hora de tratar a pacientes que presentan una patología urgente derivada de la infección por el virus de la inmunodeficiencia humana (VIH).
MétodosEstas recomendaciones se han consensuado por un panel de expertos de la Secretaría del Plan Nacional sobre el Sida, de la Sociedad Española de Medicina de Urgencias y Emergencias y del Grupo de Estudio de Sida. Para ello se han revisado los resultados de eficacia y seguridad de ensayos clínicos, estudios de cohortes y de farmacocinética publicados en revistas biomédicas (PubMed y Embase) o presentados en congresos. La fuerza de cada recomendación (A, B, C) y la gradación de la evidencia que la sustentan (I, II, III) se basan en una modificación de los criterios de la Infectious Diseases Society of America.
ResultadosSe especifican los datos que deben ser recogidos en la historia clínica de urgencias con el objetivo de reconocer al paciente en riesgo de infección por el VIH. Se incide en el conocimiento de los principios básicos del tratamiento antirretroviral (TAR) y su importancia en términos de descenso de morbimortalidad de los pacientes VIH+ y derivar al especialista en VIH para su control cuando proceda, así como de las interacciones farmacológicas. Manejo de las diferentes situaciones de urgencia que se pueden presentar en el paciente con infección por el VIH.
ConclusionesEl profesional no especialista en VIH encontrará las herramientas necesarias para el abordaje del paciente con infección por el VIH con una patología de urgencias.
Supporting non-HIV specialist professionals in the treatment of patients with urgent diseases resulting from HIV infection.
MethodsThese recommendations have been agreed by an expert panel from the National AIDS Plan Secretariat, the Spanish Society of Emergency Medicine, and the AIDS Study Group. A review has been made of the safety and efficacy results of clinical trials and cohort studies published in biomedical journals (PubMed and Embase) or presented at conferences. The strength of each recommendation (A, B, C) and the level of supporting evidence (I, II, III) are based on a modification of the criteria of the Infectious Diseases Society of America.
ResultsThe data to be collected from the emergency medical history in order to recognize the patient at risk of HIV infection were specified. It stressed the basic knowledge of ART principles and its importance in terms of decline in morbidity and mortality of HIV+ patients and referring to the HIV specialist for follow-up, where appropriate, including drug interactions. Management of different emergency situations that may occur in patients with HIV infection is also mentioned.
ConclusionsThe non-HIV specialist professional, will find the necessary tools to approach HIV patients with an emergency disease.
Los servicios de urgencias (SU) son la piedra angular de nuestra sanidad y, por tanto, no pueden permanecer indiferentes a los avances que se han producido en la infección por el virus de la inmunodeficiencia humana (VIH) y que ha cambiado radicalmente el panorama de la enfermedad; así, su actualización entre los especialistas en urgencias no solo es necesaria sino que es imprescindible.
El objetivo de este documento es dar soporte a los profesionales —básicamente no especialistas en el tema— a la hora de tratar a pacientes que presentan una patología urgente derivada de la infección por el VIH o relacionada con ella.
MetodologíaPara la elaboración de este documento, en octubre de 2010 se constituyó un grupo de expertos y expertas designados por la Secretaría del Plan Nacional sobre el Sida, la Sociedad Española de Medicina de Urgencias y Emergencias y la Junta Directiva de GESIDA, siendo el rol de las 3 instituciones de coordinación.
Este grupo está compuesto por especialistas de medicina interna con experiencia en el ámbito del VIH, expertos en urgencias, en pediatría y en psiquiatría, y 3 miembros del panel que actúan como coordinadores. Cada miembro del panel ha emitido un informe de conflicto de intereses depositado en la Secretaría del Plan Nacional sobre el Sida (SPNS) (Anexo 1). Todos ellos han aceptado participar de forma voluntaria y altruista.
Cada redactor/a ha realizado una revisión de la evidencia científica (última revisión, julio de 2012) disponible de cada uno de los aspectos que se incluyen en el documento y, con ella, ha escrito su capítulo, que ha sido discutido y revisado por el revisor asignado. Una vez recopilado todo el documento, se ha remitido a todos los miembros del panel para su discusión. Posteriormente se ha realizado una reunión de consenso de todo el panel y se ha sometido a la revisión externa, exponiéndose durante un periodo de tiempo en la web de las entidades promotoras para que los y las profesionales a los que va dirigido y cualquier persona interesada pudiera sugerir matices o cambios, decidiendo el panel a posteriori su inclusión o no dentro del documento definitivo.
La clasificación de la fuerza y la calidad de las recomendaciones se ha realizado aplicando una adaptación del sistema utilizado por la Sociedad Americana de Enfermedades Infecciosas (IDSA) y el Servicio de Salud Pública de Estados Unidos, tal y como se refleja a continuación:
Fuerza de la recomendación
Nivel A: buen nivel de evidencia para apoyar la recomendación de uso.
Nivel B: moderado nivel de evidencia para apoyar la recomendación de uso.
Nivel C: escasa evidencia para apoyar la recomendación de uso.
Calidad de la recomendación
I: evidencia procedente de al menos un ensayo clínico aleatorizado.
II: evidencia procedente de al menos un ensayo no aleatorizado, bien diseñado, o bien de estudios de cohortes, o de estudios analíticos de casos y controles (preferiblemente de más de un centro), o de series temporales, o de resultados concluyentes obtenidos en estudios experimentales no controlados.
III: evidencia de opiniones de expertos, basadas en la experiencia clínica o en estudios descriptivos.
Para la realización de los capítulos se ha llevado a cabo una búsqueda bibliográfica en las siguientes bases de datos: Medline, Pubmed, UpToDate y MD Consult, incluyendo artículos desde el año 2000 al 2012. Los idiomas de los artículos seleccionados fueron el inglés y el español, y las referencias utilizadas para la elaboración de estas recomendaciones incluyen revisiones sistemáticas, guías clínicas, ensayos clínicos, guías de práctica clínica y estudios de investigación cuantitativa, así como libros escritos por personas expertas sobre los temas elaborados. Está prevista la actualización del presente documento con carácter anual, siendo cada uno de los autores responsable de realizar su capítulo.
Historia clínica de urgenciasLa infección por el VIH presenta una serie de particularidades con respecto al resto de la población, por lo que se hace necesario recoger en la historia clínica de urgencias una serie de datos que se especifican a continuación.
El primer paso en la evaluación de un paciente es determinar la posibilidad de que se encuentre infectado por el VIH. Se puede determinar preguntando al paciente si se ha realizado recientemente una serología para el VIH o si conoce su estatus serológico1. Se debe realizar una aproximación de riesgo, mediante un interrogatorio directo al paciente con preguntas relativas a sus hábitos sexuales, al uso de métodos de barrera o al uso de drogas intravenosas u otras drogas que favorezcan la no utilización de medidas preventivas. En pacientes en los que no se puede obtener su historia, la determinación del riesgo debe basarse en las características demográficas y en la evaluación clínica.
La detección de una infección aguda es importante, ya que ocurre entre la primera y la sexta semana tras la exposición al VIH2. El cuadro simula un síndrome mononucleósido. Una cuarta parte de los pacientes experimentan la aparición de un exantema de predominio en el tronco y que puede ser maculopapular, morbiliforme o urticarial. En todo caso es indistinguible de otras infecciones virales, por lo que el conocimiento de las posibles conductas de riesgo del paciente es fundamental para sospechar la infección.
En un paciente con serología positiva conocida el médico de urgencias debe realizar las siguientes acciones:
- •
Preguntar sobre la fecha del diagnóstico de la infección VIH y, a ser posible, sobre la fecha aproximada del momento de la infección. Se debe investigar sobre la existencia de análisis previos negativos, la fecha del inicio de la práctica de riesgo o la fecha de aparición de la clínica sugestiva de la primoinfección.
- •
Seguimiento en consulta especializada: ayuda a predecir el cumplimiento de un determinado paciente frente a los tratamientos o la continuidad en el seguimiento a lo largo de la enfermedad.
- •
Conocer la situación inmunológica: es imprescindible conocer la cifra actual de linfocitos CD4, dado que de ello va a depender nuestra actitud diagnóstico-terapéutica. Además constituyen un indicador pronóstico de progresión clínica y supervivencia. Igualmente, son necesarios para indicar o no profilaxis de infecciones oportunistas.
- •
Características sociodemográficas: la visita a países en los que pueden existir microorganismos endémicos podría ayudar en la sospecha diagnóstica de infecciones como histoplasmosis o coccidioidomicosis. Del mismo modo, es interesante valorar la posibilidad de que el paciente se haya infectado en zonas geográficas en las que se sabe de la existencia de cepas de VIH no-B o con resistencia primaria a antirretrovirales.
- •
Mecanismo de transmisión: orienta hacia la búsqueda de infecciones que comparten la misma forma de transmisión, como infecciones de trasmisión sexual, hepatitis B o C, etc.
- •
Historia médica pasada: se interrogará al paciente sobre complicaciones o comorbilidades asociadas al VIH que incluyan infecciones oportunistas, tumores e historia de enfermedad o riesgo cardiovascular, y sobre el estado vacunal y la correcta inmunización.
- •
Medicación habitual y tratamiento antirretroviral: debe incluir regímenes antirretrovirales actuales y pasados, causas del cambio terapéutico, duración de los tratamientos y respuesta a cada uno de ellos. El conocimiento del tratamiento nos posibilita la sospecha diagnóstica de efectos secundarios de los mismos y de posibles interacciones con otros fármacos. Se deberá incluir medicación convencional, incluyendo tratamiento con metadona y suplementos dietéticos o de herbolario que han demostrado interacciones con los antirretrovirales. Se interrogará sobre el uso de otras drogas de abuso o recreativas y sobre prácticas de drogadicción.
El mejor predictor de riesgo de infección oportunista es la cifra de linfocitos CD4 absoluta y su porcentaje3,4. Cifras de linfocitos CD4 por debajo de 200células/mm3 se asocian con un riesgo muy elevado de aparición de enfermedades oportunistas. Entre las causas más frecuentes de asistencia a los SU por parte de los pacientes con infección por el VIH se encuentran las infecciones oportunistas y en especial las neumonías (bacterianas, por Penumocistis jiroveci, micobacterias) y las infecciones del sistema nervioso central (SNC) (toxoplasmosis, criptococo). Estas, junto con las bacteriemias, son las 3 causas más importantes y potencialmente tratables en el SU.
La exploración debe ser exhaustiva y basarse en: a)valorar si existen adenopatías significativas; b)examen de la cavidad oral para buscar lesiones de candidiasis, leucoplasia oral vellosa, sarcoma de Kaposi, aftas, verrugas o enfermedad periodontal, que indiquen situaciones de inmunosupresión avanzada; c)examen de la piel, por si muestra alteraciones que pueden estar relacionadas con la infección por el VIH, como la dermatitis seborreica, el sarcoma de Kaposi, lesiones de psoriasis, Molluscum contagiosum, herpes simple grave oral o anogenital, sarna, etc.; d)exploración anal con tacto rectal en los varones homosexuales y bisexuales, dada la creciente incidencia de carcinoma anal de células escamosas; e)buscar activamente hepatoesplenomegalia y soplos cardíacos, sobre todo en los usuarios de drogas por vía parenteral; f)los déficits neurológicos y los trastornos de la conducta pueden alertar de la existencia de un complejo sida-demencia, y g)la exploración debe completarse con la realización de algún test de demencia5.
Recomendaciones- •
En los SU se debe estar alerta ante los posibles casos de primoinfección o patologías asociadas al VIH con el fin de disminuir el diagnóstico tardío (A-II).
- •
En los pacientes con serología ya conocida es fundamental conocer el estado inmunológico, ya que esta nos orientará hacia las exploraciones y pruebas complementarias necesarias para buscar patología oportunista relacionada (B-III).
Las recomendaciones actuales de tratamiento antirretroviral (TAR) para pacientes con infección crónica por el VIH incluyen a aquellos con recuentos de CD4<500células/mm3, historia de enfermedad definitoria de sida, determinadas comorbilidades (hepatitis B, nefropatía asociada a VIH) y las mujeres embarazadas para prevenir la transmisión materno-fetal6,7 (véase «Documento de consenso de GESIDA/Plan Nacional sobre el Sida (PNS) respecto al tratamiento antirretroviral en adultos infectados por el VIH» Actualización enero 2013, disponible en: http://www.msssi.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/publicaciones/profSanitarios/docTARGesidaPNS2013Def.pdf.).
La complejidad del TAR hace imprescindible un manejo especializado. Deben conocerse en profundidad las características particulares de los fármacos y su comportamiento en combinación con otros, así como el perfil de efectos adversos y sus interacciones farmacológicas. La toxicidad aguda por el TAR es un potencial motivo de consulta en urgencias y podría llegar a requerir el cambio del fármaco implicado si este es fácil de identificar.
La prevención y el tratamiento de las infecciones oportunistas en pacientes con infección por el VIH llevan parejo el uso de determinados antimicrobianos cuyo empleo es menos frecuente en la era del TAR. No obstante, en pacientes que se diagnostican tardíamente o en los poco adherentes al TAR es todavía habitual contemplar su uso. Asimismo, las comorbilidades que acompañan a la infección por VIH también suelen requerir el manejo de un número limitado de fármacos que el especialista debe conocer en profundidad. No debe olvidarse el potencial de interacciones farmacológicas del TAR (especialmente los inhibidores de la proteasa [IP] y los inhibidores de la transcriptasa inversa no análogos [ITINN]) y ante la eventual prescripción de un nuevo medicamento a un paciente con infección por el VIH en TAR8.
Recomendaciones- •
El médico de urgencias debe conocer los principios básicos del TAR y su importancia en términos de descenso de la morbimortalidad de los pacientes VIH+ y derivar al especialista en VIH para su control cuando proceda (A-III).
- •
Se recomienda consultar las interacciones farmacológicas cuando se decida prescribir un nuevo fármaco en un paciente en TAR en los SU (A-III).
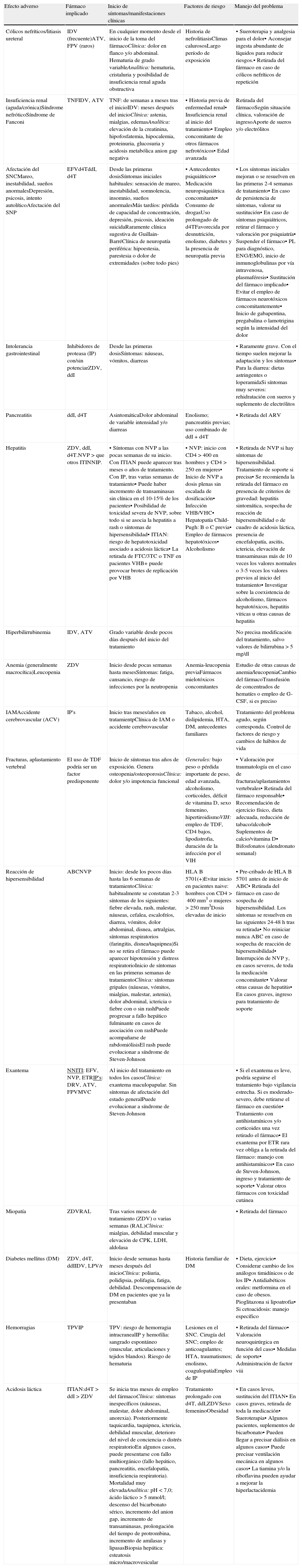
Los efectos secundarios del TAR constituyen la principal causa de cambio de tratamiento y de pérdida de adherencia. Podemos distinguir desde efectos secundarios de inicio a largo-medio plazo, como la dislipidemia, la resistencia a la insulina, la diabetes o la redistribución de la grasa corporal, pero habitualmente se detectan en los controles realizados en la consulta especializada, mientras que los efectos secundarios de inicio precoz son los que con más probabilidad van a generar consultas a los SU6,9. En la tabla 1 se resumen los efectos adversos más importantes.
Efectos adversos más importantes
| Efecto adverso | Fármaco implicado | Inicio de síntomas/manifestaciones clínicas | Factores de riesgo | Manejo del problema |
| Cólicos nefríticos/litiasis ureteral | IDV (frecuente)ATV, FPV (raros) | En cualquier momento desde el inicio de la toma del fármacoClínica: dolor en flanco y/o abdominal. Hematuria de grado variableAnalítica: hematuria, cristaluria y posibilidad de insuficiencia renal aguda obstructiva | Historia de nefrolitiasisClimas calurososLargo período de exposición | • Sueroterapia y analgesia para el dolor• Aconsejar ingesta abundante de líquidos para reducir riesgos.• Retirada del fármaco en caso de cólicos nefríticos de repetición |
| Insuficiencia renal (aguda/crónica)Síndrome nefróticoSíndrome de Fanconi | TNFIDV, ATV | TNF: de semanas a meses tras el inicioIDV: meses después del inicioClínica: astenia, mialgias, edemasAnalítica: elevación de la creatinina, hipofosfatemia, hipocalemia, proteinuria, glucosuria y acidosis metabólica anion gap negativa | • Historia previa de enfermedad renal• Insuficiencia renal al inicio del tratamiento• Empleo concomitante de otros fármacos nefrotóxicos• Edad avanzada | Retirada del fármacoSegún situación clínica, valoración de ingresoAporte de sueros y/o electrólitos |
| Afectación del SNCMareo, inestabilidad, sueños anormalesDepresión, psicosis, intento autolíticoAfectación del SNP | EFVd4TddI, d4T | Desde las primeras dosisSíntomas iniciales habituales: sensación de mareo, inestabilidad, somnolencia, insomnio, sueños anormalesMás tardíos: pérdida de capacidad de concentración, depresión, psicosis, ideación suicidaRaramente clínica sugestiva de Guillain-BarréClínica de neuropatía periférica: hipoestesia, parestesia o dolor de extremidades (sobre todo pies) | • Antecedentes psiquiátricos• Medicación neuropsiquiátrica concomitante• Consumo de drogasUso prolongado de d4TFavorecida por desnutrición, enolismo, diabetes y la presencia de neuropatía previa | • Los síntomas iniciales mejoran o se resuelven en las primeras 2-4 semanas de tratamiento• En caso de persistencia de síntomas, valorar su sustitución• En caso de síntomas psiquiátricos, retirar el fármaco y valoración por psiquiatría• Suspender el fármaco• PL para diagnóstico, ENG/EMG, inicio de inmunoglobulinas por vía intravenosa, plasmaféresis• Sustitución del fármaco implicado• Evitar el empleo de fármacos neurotóxicos concomitantemente• Inicio de gabapentina, pregabalina o lamotrigina según la intensidad del dolor |
| Intolerancia gastrointestinal | Inhibidores de proteasa (IP) con/sin potenciarZDV, ddI | Desde las primeras dosisSíntomas: náuseas, vómitos, diarreas | • Raramente grave. Con el tiempo suelen mejorar la adaptación y los síntomas• Para la diarrea: dietas astringentes o loperamidaSi síntomas muy severos: rehidratación con sueros y suplemento de electrólitos | |
| Pancreatitis | ddI, d4T | AsintomáticaDolor abdominal de variable intensidad y/o diarreas | Enolismo; pancreatitis previas; uso combinado de ddI + d4T | • Retirada del ARV |
| Hepatitis | ZDV, ddI, d4T.NVP > que otros ITINNIP. | • Síntomas con NVP a las pocas semanas de su inicio. Con ITIAN puede aparecer tras meses o años de tratamiento. Con IP, tras varias semanas de tratamiento• Puede haber incremento de transaminasas sin clínica en el 10-15% de los pacientes• Posibilidad de toxicidad severa de NVP, sobre todo si se asocia la hepatitis a rash o síntomas de hipersensibilidad• ITIAN: riesgo de hepatotoxicidad asociado a acidosis láctica• La retirada de FTC/3TC o TNF en pacientes VHB+ puede provocar brotes de replicación por VHB | • NVP: inicio con CD4 > 400 en hombres y CD4 > 250 en mujeres• Inicio de NVP a dosis plenas sin escalada de dosificación• Infección VHB/VHC• Hepatopatía Child-Pugh: B o C previa• Empleo de fármacos hepatotóxicos• Alcoholismo | • Retirada de NVP si hay síntomas de hipersensibilidad. Tratamiento de soporte si precisa• Se recomienda la retirada del fármaco en presencia de criterios de gravedad: hepatitis sintomática, sospecha de reacción de hipersensibilidad o de cuadro de acidosis láctica, presencia de encefalopatía, ascitis, ictericia, elevación de transaminasas más de 10 veces los valores normales o 3-5 veces los valores previos al inicio del tratamiento• Investigar sobre la coexistencia de alcoholismo, fármacos hepatotóxicos, hepatitis víricas u otras causas de hepatitis |
| Hiperbilirrubinemia | IDV, ATV | Grado variable desde pocos días después del inicio del tratamiento | No precisa modificación del tratamiento, salvo valores de bilirrubina > 5 mg/dl | |
| Anemia (generalmente macrocítica)Leucopenia | ZDV | Inicio desde pocas semanas hasta mesesSíntomas: fatiga, cansancio, riesgo de infecciones por la neutropenia | Anemia-leucopenia previaFármacos mielotóxicos concomitantes | Estudio de otras causas de anemia/leucopeniaCambio del fármacoTransfusión de concentrados de hematíes o empleo de G-CSF, si es preciso |
| IAMAccidente cerebrovascular (ACV) | IP's | Inicio tras meses/años en tratamientpClínica de IAM o accidente cerebrovascular | Tabaco, alcohol, dislipidemia, HTA, DM, antecedentes familiares | Tratamiento del problema agudo, según corresponda. Control de factores de riesgo y cambios de hábitos de vida |
| Fracturas, aplastamiento vertebral | El uso de TDF podría ser un factor predisponente | Inicio de síntomas tras años de exposición. Genera osteopenia/osteoporosisClínica: dolor y/o impotencia funcional | Generales: bajo peso o pérdida importante de peso, edad avanzada, alcoholismo, corticoides, déficit de vitamina D, sexo femenino, hipertiroidismoVIH: empleo de TDF, CD4 bajos, lipodistrofia, duración de la infección por el VIH | • Valoración por traumatología en el caso de fracturas/aplastamientos vertebrales• Retirada del fármaco responsable• Recomendación de ejercicio físico, dieta adecuada, reducción de tabaco/alcohol• Suplementos de calcio/vitamina D• Bifosfonatos (alendronato semanal) |
| Reacción de hipersensibilidad | ABCNVP | Inicio: desde los pocos días hasta las 6 semanas de tratamientoClínica: habitualmente se constatan 2-3 síntomas de los siguientes: fiebre elevada, rash, malestar, náuseas, cefalea, escalofríos, diarrea, vómitos, dolor abdominal, disnea, artralgias, síntomas respiratorios (faringitis, disnea/taquipnea)Si no se retira el fármaco puede aparecer hipotensión y distress respiratorioInicio de síntomas en las primeras semanas de tratamientoClínica: síntomas gripales (náuseas, vómitos, mialgias, malestar, astenia), dolor abdominal, ictericia o fiebre con o sin rashPuede progresar a fallo hepático fulminante en casos de asociación con rashPuede acompañarse de rabdomiólisisEl rash puede evolucionar a síndrome de Steven-Johnson | HLA B 5701(+)Evitar inicio en pacientes naive: hombres con CD4>400mm3 o mujeres >250mm3Dosis elevadas de inicio | • Pre-cribado de HLA B 5701 antes de inicio de ABC• Retirada del fármaco en caso de sospecha de hipersensibilidad. Los síntomas se resuelven en las siguientes 24-48h tras su retirada• No reiniciar nunca ABC en caso de sospecha de reacción de hipersensibilidad• Interrupción de NVP y, en casos severos, de toda la medicación concomitante• Valorar otras causas de hepatitis• En casos graves, ingreso para tratamiento de soporte |
| Exantema | NNITI: EFV, NVP, ETRIP's: DRV, ATV, FPVMVC | Al inicio del tratamiento en todos los casosClínica: exantema maculopapular. Sin síntomas de afectación del estado generalPuede evolucionar a síndrome de Steven-Johnson | • Si el exantema es leve, podría seguirse el tratamiento bajo vigilancia estrecha. Si es moderado-severo, debe retirarse el fármaco en cuestión• Tratamiento con antihistamínicos y/o corticoides una vez retirado el fármaco• El exantema por ETR rara vez obliga a la retirada del fármaco: manejo con antihistamínicos• En caso de Steven-Johnson, ingreso y tratamiento de soporte• Valorar otros fármacos con toxicidad cutánea | |
| Miopatía | ZDVRAL | Tras varios meses de tratamiento (ZDV) o varias semanas (RAL)Clínica: mialgias, debilidad muscular y elevación de CPK, LDH, aldolasa | • Retirada del fármaco | |
| Diabetes mellitus (DM) | ZDV, d4T, ddIIDV, LPV/r | Inicio desde semanas hasta meses después del inicioClínica: poliuria, polidipsia, polifagia, fatiga, debilidad. Descompensación de DM en pacientes que ya la presentaban | Historia familiar de DM | • Dieta, ejercicio• Considerar cambio de los análogos timidínicos o de los IP• Antidiabéticos orales: metformina en el caso de obesos. Pioglitazona si lipoatrofia• Si cetoacidosis: manejo específico |
| Hemorragias | TPVIP | TPV: riesgo de hemorragia intracranealIP y hemofilia: sangrado espontáneo (muscular, articulaciones y tejidos blandos). Riesgo de hematuria | Lesiones en el SNC. Cirugía del SNC; empleo de anticoagulantes; HTA, traumatismos; enolismo, coagulopatíaEmpleo de IP | • Retirada del fármaco• Valoración neuroquirúrgica en función del caso• Medidas de soporte• Administración de factor viii |
| Acidosis láctica | ITIAN:d4T>ddI>ZDV | Se inicia tras meses de empleo del fármacoClínica: síntomas inespecíficos (náuseas, malestar, dolor abdominal, anorexia). Posteriormente taquicardia, taquipnea, ictericia, debilidad muscular, deterioro del nivel de conciencia o distrés respiratorioEn algunos casos, puede presentarse con fallo multiorgánico (fallo hepático, pancreatitis, encefalopatía, insuficiencia respiratoria). Mortalidad muy elevadaAnalítica: pH<7,0; ácido láctico>5mmol/l; descenso del bicarbonato sérico, incremento del anion gap, incremento de transaminasas, prolongación del tiempo de protrombina, incremento de amilasas y lipasasBiopsia hepática: esteatosis micro/macrovesicular | Tratamiento prolongado con d4T, ddI,ZDVSexo femeninoObesidad | • En casos leves, sustitución del ITIAN• En casos graves, retirada de toda la medicación• Sueroterapia• Algunos pacientes, suplementos de bicarbonato• Pueden llegar a precisar diálisis en algunos casos• Puede precisar ventilación mecánica en algunos casos• La tiamina y/o la riboflavina pueden ayudar a mejorar la hiperlactacidemia |
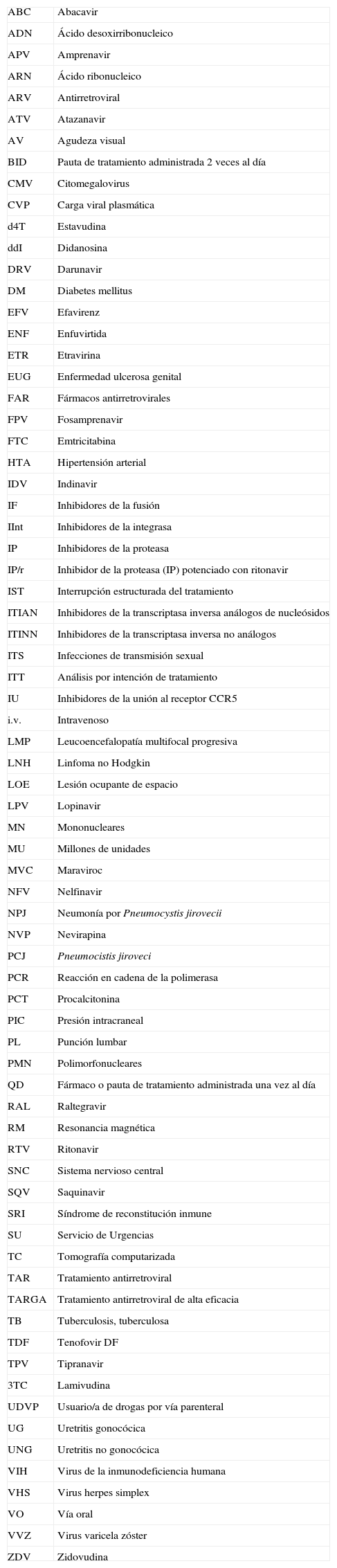
Véase la tabla de abreviaturas en el Anexo 2.
La edad creciente de nuestros pacientes está provocando un incremento de comorbilidades (hipertensión arterial [HTA], diabetes, dislipidemia, cardiopatía…) que podrían precisar de nuevos tratamientos. Asimismo, deberemos estar muy atentos a las posibles interacciones medicamentosas, que pueden variar la farmacocinética tanto del TAR como la del resto de fármacos.
Recomendaciones- •
Se recomienda seguimiento en 2-4 semanas, tanto clínico como analítico, para control de tolerancia y presencia de efectos adversos (B-III).
- •
Deben tenerse en cuenta todos los fármacos que toma el paciente, para prevenir y valorar las posibles interacciones/efectos adversos (B-III).
- •
Se recomienda incluir en los controles analíticos un cálculo de tasa de filtrado glomerular y un estudio elemental de orina (A-III), sobre todo en pacientes en tratamiento con tenofovir (A-II). En caso de filtrado glomerular <50, no debería emplearse tenofovir (A-III).
- •
Se recomienda un test del HLAB5701, previo al inicio de un tratamiento con abacavir (A-I).
- •
Durante las primeras 2-4semanas después de iniciar un tratamiento con efavirenz (EFV) suelen presentarse trastornos del sueño, mareos, dificultad de concentración, cefalea, que no constituyen motivo de retirada, dado que habitualmente suelen desaparecer (A-II). Se desaconseja el uso de EFV en pacientes con antecedentes psiquiátricos (A-III).
La fiebre es la manifestación clínica más frecuente en los pacientes infectados por el VIH. En aproximadamente el 90% de los casos se llega a un diagnóstico etiológico tras un estudio sencillo. Estos síndromes febriles suelen ser de corta duración y autolimitados. El control inmunológico y virológico de la infección consecuencia del TAR disminuye de manera muy importante la posibilidad de presentar este síndrome.
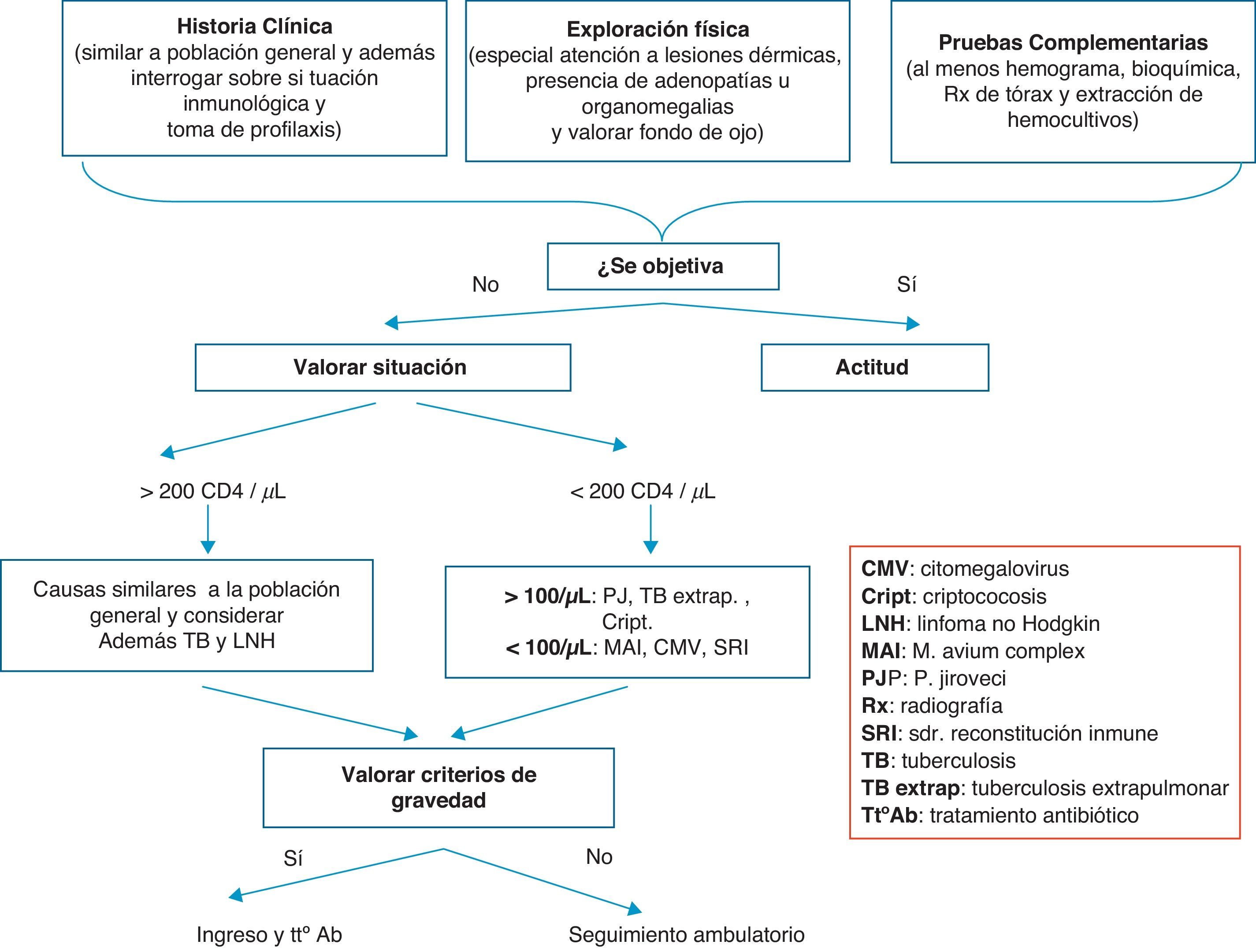
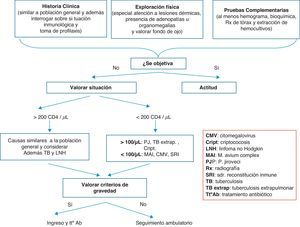
La infección más frecuentemente diagnosticada en los casos de fiebre sin foco en pacientes con infección por el VIH es la tuberculosis (TB). En líneas generales, las causas de fiebre sin foco en un paciente con más de 200CD4/mm3 son las mismas que en la población general, a excepción de la TB y el linfoma no Hodgkin. En pacientes con menos de 200CD4/mm3, el diagnóstico diferencial es más amplio10. Las causas más frecuentes de fiebre sin foco son: el propio VIH, especialmente durante la primoinfección y en fases finales de la enfermedad; infecciones oportunistas, neoplasias sólidas y hematológicas, causas comunes en la población general, tanto causas infecciosas como otras (p.ej., enfermedades del tejido conectivo…), fármacos; y a tener en cuenta el síndrome de reconstitución inmune (SRI). Este síndrome es más frecuente en los pacientes que comienza el TAR más inmunodeprimidos y con cargas virales más elevadas que coinciden con algún episodio oportunista. En la tabla 2 se recogen las causas más frecuentes de fiebre sin causa aparente. En la figura 1 se resume la actitud a seguir en urgencias en el paciente VIH que acude por fiebre sin foco evidente.
Causas de fiebre más frecuentes
| Frecuentes | Infrecuentes |
| Tuberculosis | Otras micobacterias (M. avium intracellulare, M. kansasii) |
| VIH | Sepsis por Salmonella spp. |
| Fiebre medicamentosa | Citomegalovirus |
| Linfoma no Hodgkin | Sífilis |
| Endocarditis | Pseudomonas auroginosa |
| Criptococosis | Leishmaniosis |
| Síndrome de reconstitución inmune | Pneumocistis jirovecii |
| Toxoplasma gondii | |
| Histoplasma capsulatum | |
| Campylobacter spp. | |
| Coccidioides immitis | |
| Rhodococcus equi | |
| Streptococcus pneumoniae | |
| Haemophilus influenzae | |
| Brucelosis | |
| Bartonella henselae y B. quintana | |
| Candidiasis diseminada | |
| Neoplasias (sarcoma de Kaposi, linfoma de Hodgkin y otras neoplasias) | |
| Polimiositis | |
| Vasculitis y enfermedades del tejido conjuntivo | |
| Acidosis láctica e hiperlactatemia sintomática |
Algoritmo de manejo del paciente con infección por el VIH con fiebre sin foco.
CMV: citomegalovirus; Cript.: criptococosis; LNH: linfoma no Hodgkin; MAI: M. avium complex; PJ: P. jiroveci; SRI: síndrome de reconstitución inmune; TB: tuberculosis; TB extrap.: tuberculosis extrapulmonar; Tt° ab: tratamiento antibiótico.
- •
Ante la presencia de fiebre sin foco en pacientes con infección por el VIH independientemente de la cifra de CD4 y dada la alta prevalencia en nuestro medio, se debe descartar una TB (B-II).
- •
En pacientes con CD4>200células/mm3, ademas de descartar los mismos cuadros patológicos que en la población general, se deben incluir la TB y el linfoma no Hodgkin (B-II).
En los pacientes con infección por el VIH, la disnea es uno de los síntomas que con mayor frecuencia llevan al paciente a consultar en urgencias. El origen de la disnea puede agruparse en 4grandes causas: respiratoria (infecciosa o no), cardíaca, metabólica y psíquica. En los pacientes con VIH, las enfermedades pulmonares son las más frecuentes en la clínica diaria, y constituyen una de las principales causas de morbimortalidad11,12.
La conducta recomendable ante un paciente con infección por el VIH con disnea sería:
- -
Exploración física detallada (signos de venopunción, adenopatías, etc.) y una anamnesis detallada que incluya:
- -
Averiguar el estado inmunitario del paciente.
- -
Conocimiento de si existe drogadicción activa.
- -
Existencia de afecciones pulmonares previas.
- -
Tratamientos terapéuticos o profilácticos llevados a cabo.
- -
Forma de presentación clínica.
- -
Coexistencia de fiebre, expectoración o dolor torácico.
- -
Existencia de pérdida de conocimiento previo (sospecha de neumonía aspirativa).
- -
Exploración física detallada.
Se deben asimismo, realizar pruebas complementarias básicas: gasometría arterial basal y radiografía de tórax de frente y perfil.
En la tabla 3 se recoge la actuación ante un paciente VIH+ con disnea.
Actuación en un paciente VIH+ con disnea
| Anamnesis |
| Descartar: obstrucción de la vía aérea respiratoria alta; abuso/intoxicación por opiáceos u otras sustancias adictivas |
| Valorar la gravedad (frecuencia respiratoria, coloración de piel y mucosas, PA, FC, temperatura, flapping, tiraje, incoordinación toracoabdominal, aleteo nasal) |
| EF, GSA y RxT: Normales | GSA pO2<75mmHg y RxT normal | GSA Normal/anormal y RxT anormal | ||
| Patrón radiológico | ||||
| Etiología | Etiología | Intersticial | Alveolar | Pneumotórax |
| Traqueobronquitis agudaAnemiaAnsiedad/Sociopatía | Tromboembolismo pulmonarAsmaTrastornos metabólicosFármacosConsiderar NPJ y TBC | Bilateral y difusoNPJSarcoma de KaposiReticulonodulillarTBC | BilateralesIC-EAPEndocarditis/embolia sépticaFocal-NeumoníaNeumococoH. influenzaeS. aureus (>%ADVP)LegionellaPseudomonasCMVCriptococoSarcoma de KaposiTBAspergillusToxoplasmaLeishmaniaCavitadasTBM. kansasiPseudomonasNocardiaS. aureusNPJRhodococcusSerotipos de neumococo | NPJ si tratamiento con pentamidinaTBDerrame pleuralTBMetaneumónicoSarcoma de Kaposi (hemático)NeoplasiasLinfomasCarcinoma broncogénico |
| Actitud | Actitud | Actitud: Ingeso hospitalario |
| Valorar determinación de Hto.Macrólido, Amoxixilina + ácido clavulánico | Ingreso hospitalario OxigenoterapiaTratamiento etiológico | Analítica (LDH)HemocultivosZiehl y Gram de esputoAntigenuria para Legionella y neumococoTratamiento empírico o tratamiento específico |
ADVP: adictos a drogas por vía parenteral; CMV: citomegalovirus; EAP: edema agudo de pulmón; FC: frecuencia cardíaca; GSA: gasometría; Hto: hematócrito, IC: insuficiencia cardíaca; NPJ: neumonía por Pneumocystis jirovecii; PA: presión arterial; RxT: radiografía de tórax; TB: tuberculosis.
- •
En pacientes con inmunodepresión moderada-severa (CD4<200células/mm3) y disnea, los cuadros tanto infecciosos como no infecciosos sueles ser graves, con elevada mortalidad, por lo que deberá actuarse de forma rápida para identificar lo antes posible la causa e iniciar tratamiento específico (C-III).
- •
En la mayoría de los casos se recomienda iniciar tratamiento empírico de las patologías más frecuentes hasta tener confirmación diagnóstica (C-III).
El 20% de los pacientes infectados por el VIH van a tener una presentación clínica en forma de complicación neurológica, y con frecuencia acudirán a un SU por este motivo. El diagnóstico ha de ser siempre individualizado y basado en: la historia clínica, cifra de linfocitos CD4, si está o no con TAR, la historia epidemiológica, si la enfermedad afecta a otros órganos, etc. (tabla 4).
Afectaciones neurológicas frecuentes en pacientes con infección por el VIH
| Afectación cerebral no focal |
| Encefalopatía por VIH-Demencia asociada a sida |
| Encefalopatías metabólicas y tóxicas |
| Encefalitis por CMV y herpéticas |
| Sífilis |
| Afectación cerebral focal |
| Toxoplasmosis cerebral |
| Linfoma primario del SNC |
| Tuberculomas |
| Criptococomas |
| Nocardiosis |
| Leucoencefalopatía multifocal progresiva (LMP) |
| Afectación meníngea |
| Meningitis bacteriana |
| Meningitis criptocócica |
| Meningitis tuberculosa |
| Linfomatosis meníngea |
| Primoinfección aguda |
| Afectación medular |
| Mielopatía vacuolar |
| Linfomas |
| Neuropatías periféricas |
| Neuropatía sensitiva asociada al VIH |
| Polirradiculopatía por CMV |
| Síndrome de Guillain-Barré |
| Mononeuritis múltiple |
| Neuropatía tóxica |
| Miopatías |
| Otros procesos |
| Lesiones vasculares |
| Trastornos metabólicos y nutricionales |
| Síndrome de reconstitución inmune |
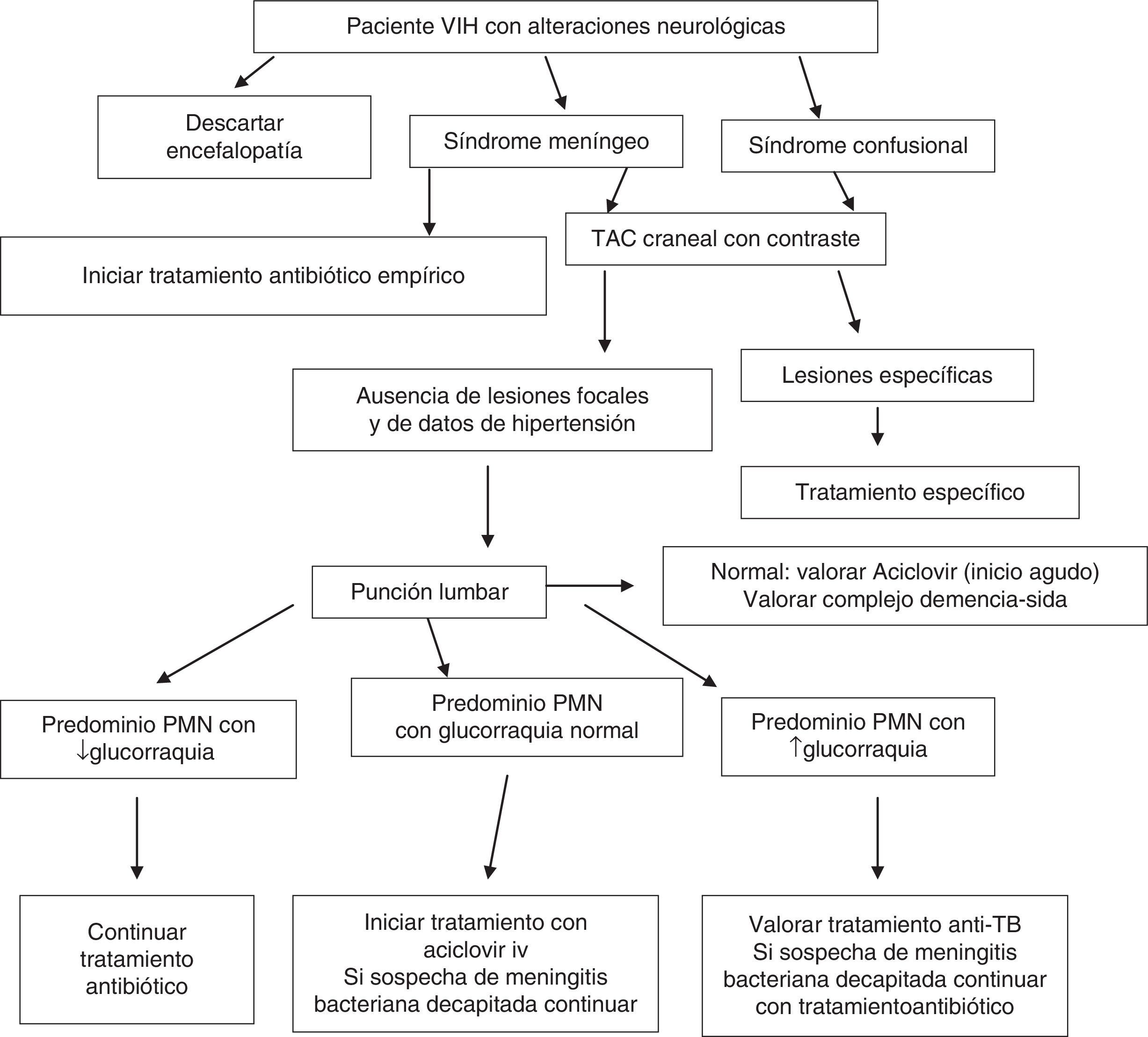
En muchos casos estará indicado realizar una resonancia magnética (RM) craneal o medular, pero en la mayoría de los SU solo existe disponibilidad de tomografía computarizada (TC), que, junto con la punción lumbar (PL), serán los pilares del diagnóstico13,14. En los pacientes con infección por el VIH, por estar inmunodeprimidos, siempre se debe realizar una TC craneal previa a la PL. En el líquido cefalorraquídeo (LCR) se determinarán la glucorraquia, la proteinorraquia, el recuento de leucocitos y diferencial, los hematíes, las tinciones de Gram y Ziehl-Neelsen, el cultivo, la detección de Cryptococcus neoformans (tinta china o aglutinación en látex), las serologías, la reacción en cadena de la polimerasa (PCR), etc. Por otro lado, el estudio de fondo de ojo, además de revelar la existencia de papiledema, puede descubrir una retinitis por citomegalovirus (CMV), Toxoplasma gondii o indiferenciada por el propio VIH.
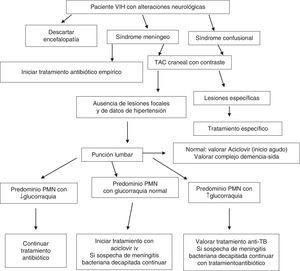
En la figura 2 se recoge el algoritmo de actuación ante un paciente VIH+ con síntomas neurológicos.
- •
La etiología más frecuente de encefalitis es el CMV, y aunque actualmente no es muy frecuente, se deberá descartar especialmente en pacientes muy inmunodeprimidos (A-II).
- •
Ante una disminución del nivel de consciencia y/o una exploración neurológica con presencia de algún dato de afectación focal, se debe pensar en la existencia de una lesión ocupante de espacio (LOE) cerebral (A-II).
- •
En los pacientes con infección por el VIH, siempre se debe realizar TC craneal previa a la PL (B-III).
- •
La causa más frecuente de LOE con captación de contraste es la toxoplasmosis; así, ante este cuadro clinicorradiológico cabe iniciar tratamiento empírico contra esta infección (A-II).
El síntoma gastrointestinal más frecuente en el paciente con infección por el VIH es la diarrea, y el 50-90% la han presentado en algún momento de su curso evolutivo15,16.
En la anamnesis de la diarrea de estos pacientes deben constar siempre: la duración (aguda/crónica), las características de las deposiciones, la investigación del uso de fármacos y drogas, el tipo de dieta, las condiciones de vivienda y el consumo de aguas no purificadas. Preguntar sobre viajes recientes al extranjero y prácticas sexuales y grado de inmunosupresión para predecir etiologías probables.
La situación clínica y analítica del paciente determinara sí existe indicación de ingreso.
El tratamiento empírico puede estar justificado cuando hay bacteriemia y afectación severa del estado general. A la espera de los resultados de los cultivos cursados, se pautarán quinolonas (ciprofloxacino, 500-750mg/12h por vía oral, o 200-400mg/12h intravenosa) o cotrimoxazol. El tratamiento sintomático se realizará con reposición de líquidos por vía parenteral y se valorará el uso de fármacos antidiarreicos convencionales como la loperamida. En caso de sospechar diarrea por antirretrovirales, estos se retirarán y se remitirán a la mayor brevedad posible a la consulta especializada para valorar su reintroducción o bien su sustitución definitiva. Si el dolor es importante, se deberá pautar analgesia (paracetamol oral o por vía parenteral).
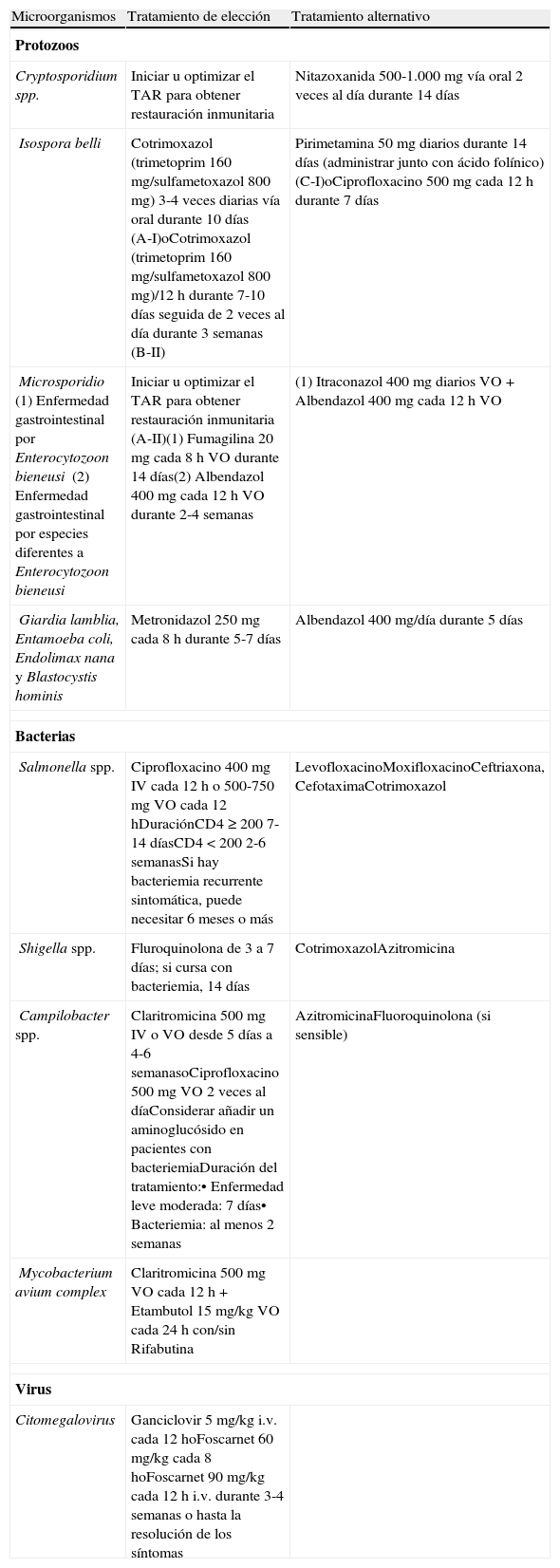
En la tabla 5 se recogen el tratamiento de las causas más frecuentes de diarrea en el VIH+.
Tratamiento de las causas más frecuentes de diarrea
| Microorganismos | Tratamiento de elección | Tratamiento alternativo |
| Protozoos | ||
| Cryptosporidium spp. | Iniciar u optimizar el TAR para obtener restauración inmunitaria | Nitazoxanida 500-1.000 mg vía oral 2 veces al día durante 14 días |
| Isospora belli | Cotrimoxazol (trimetoprim 160mg/sulfametoxazol 800mg) 3-4 veces diarias vía oral durante 10 días (A-I)oCotrimoxazol (trimetoprim 160 mg/sulfametoxazol 800mg)/12h durante 7-10 días seguida de 2 veces al día durante 3 semanas (B-II) | Pirimetamina 50 mg diarios durante 14 días (administrar junto con ácido folínico) (C-I)oCiprofloxacino 500 mg cada 12h durante 7 días |
| Microsporidio(1) Enfermedad gastrointestinal por Enterocytozoon bieneusi(2) Enfermedad gastrointestinal por especies diferentes a Enterocytozoon bieneusi | Iniciar u optimizar el TAR para obtener restauración inmunitaria (A-II)(1) Fumagilina 20 mg cada 8h VO durante 14 días(2) Albendazol 400 mg cada 12h VO durante 2-4 semanas | (1) Itraconazol 400 mg diarios VO + Albendazol 400 mg cada 12h VO |
| Giardia lamblia, Entamoeba coli, Endolimax nana y Blastocystis hominis | Metronidazol 250mg cada 8h durante 5-7 días | Albendazol 400 mg/día durante 5 días |
| Bacterias | ||
| Salmonella spp. | Ciprofloxacino 400 mg IV cada 12h o 500-750mg VO cada 12hDuraciónCD4≥200 7-14 díasCD4<200 2-6 semanasSi hay bacteriemia recurrente sintomática, puede necesitar 6meses o más | LevofloxacinoMoxifloxacinoCeftriaxona, CefotaximaCotrimoxazol |
| Shigella spp. | Fluroquinolona de 3 a 7 días; si cursa con bacteriemia, 14 días | CotrimoxazolAzitromicina |
| Campilobacter spp. | Claritromicina 500mg IV o VO desde 5 días a 4-6 semanasoCiprofloxacino 500 mg VO 2 veces al díaConsiderar añadir un aminoglucósido en pacientes con bacteriemiaDuración del tratamiento:• Enfermedad leve moderada: 7días• Bacteriemia: al menos 2semanas | AzitromicinaFluoroquinolona (si sensible) |
| Mycobacterium avium complex | Claritromicina 500mg VO cada 12h + Etambutol 15mg/kg VO cada 24h con/sin Rifabutina | |
| Virus | ||
| Citomegalovirus | Ganciclovir 5 mg/kg i.v. cada 12hoFoscarnet 60 mg/kg cada 8hoFoscarnet 90mg/kg cada 12h i.v. durante 3-4 semanas o hasta la resolución de los síntomas | |
- •
En caso de sospechar diarrea por fármacos antirretrovirales, estos se retirarán y se remitirán a la mayor brevedad posible a la consulta especializada para valorar su reintroducción o bien su sustitución definitiva (B-II).
- •
El tratamiento empírico puede estar justificado cuando hay bacteriemia y afectación severa del estado general, a la espera de los resultados de los cultivos cursados (B-III).
Los pacientes VIH+ con elevada frecuencia acuden a los SU médicos o psiquiátricos con algún motivo de consulta relacionado con la salud mental. Alrededor del 2% de las visitas realizadas en una unidad de urgencias psiquiátricas correspondieron a pacientes VIH+17.
Los principales motivos de consulta a urgencias médicas son los siguientes: síndrome depresivo (intento de suicidio, síntomas físicos inespecíficos, anorexia); suicidio (ante la presencia de pensamientos de suicidio es aconsejable siempre una valoración psiquiátrica); síndrome ansioso (inquietud y nerviosismo, síntomas vegetativos: palpitaciones, disnea, etc. sensación de muerte); síndrome maniaco y síndrome psicótico (inquietud y nerviosismo, síntomas vegetativos: palpitaciones, disnea, etc., sensación de muerte), y síndrome confusional (alteración del nivel de conciencia, signos neurológicos, agitación psicomotora)18. Para mayor información, véase documento extenso en http://www.msssi.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/publicaciones/profSanitarios/UrgenciasVIH17Julio2012.pdf
Recomendaciones- •
Es importante diagnosticar y tratar los trastornos psiquiátricos de los pacientes VIH+, dado que pueden complicar el pronóstico de la enfermedad (B-III).
- •
Es necesario descartar que los síntomas psiquiátricos puedan ser debidos a la misma infección, a enfermedades oportunistas o a los tratamientos médicos (B-III).
- •
Los aspectos generales a considerar en relación al tratamiento psicofarmacológico en los pacientes VIH+ son:
- -
Administración de dosis iniciales más bajas e incremento más lento. Suele haber mayor sensibilidad (menor tolerancia) (B-III).
- -
Programación de la posología lo menos compleja posible para facilitar el cumplimiento del tratamiento (B-III).
- -
Tener en cuenta el perfil de efectos secundarios para evitar sucesos adversos innecesarios. Conviene vigilar los efectos serotoninérgicos y los antidopaminérgicos (B-III).
- -
Considerar vías metabólicas y de eliminación del fármaco para reducir a mínimos tanto las interacciones entre medicamentos como las lesiones en el órgano diana (B-III).
- -
La prevalencia de las complicaciones oculares se correlaciona con el recuento de linfocitos CD4 y el estadio clínico según la OMS (pacientes con niveles de CD4<100células/mm3 y estados clínicos 3 y 4 presentan mayor prevalencia de manifestaciones oculares)19.
Más del 50% de los pacientes con infección por el VIH presentan complicaciones del segmento anterior, y estas incluyen procesos relativamente benignos, como la blefaritis o la queratoconjuntivitis seca, infecciones corneales (queratitis), herpes zóster oftálmico, Molluscum contagiosum, afectaciones de la cámara anterior (iridociclitis), efectos secundarios de los antirretrovirales (nevirapina, indinavir), o incluso procesos malignos como el sarcoma de Kaposi, entre otros20.
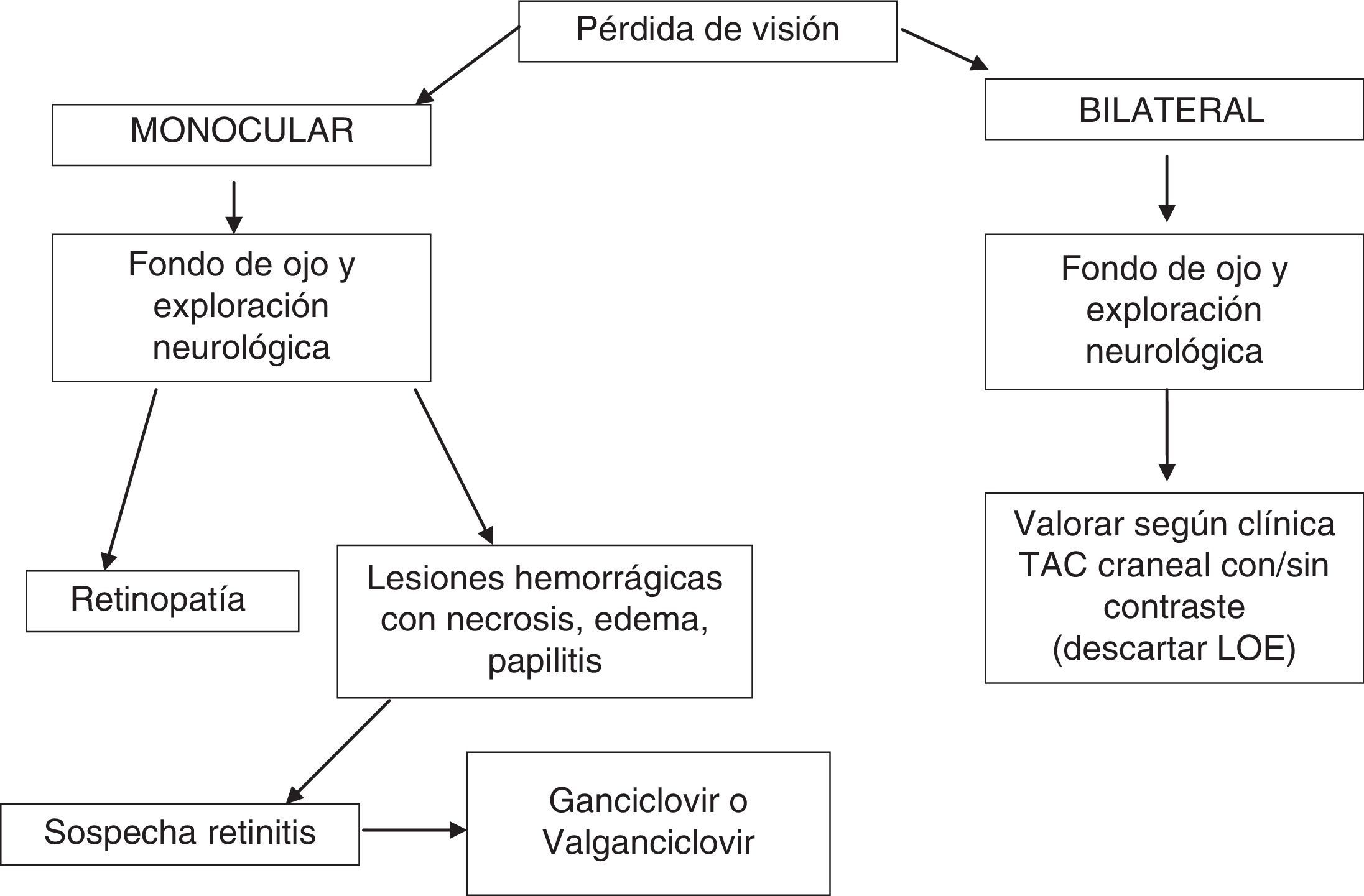
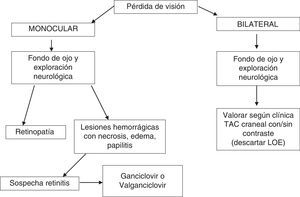
Las manifestaciones del segmento posterior relacionadas con el sida se pueden dividir en 4 categorías: vasculopatía retiniana, infecciones oportunistas, tumores inusuales y anomalías neuro-oftalmológicas21. En la anamnesis en el SU se preguntará si la pérdida es monocular o binocular, el momento del inicio del TAR y si se acompaña de otra sintomatología sistémica como fiebre, cefalea y/o focalidad neurológica (fig. 3). En la exploración física es imprescindible la realización de un fondo de ojo y de una exploración neurológica. Ante la pérdida de visión binocular, en ausencia de lesiones en la cámara posterior se deberá realizar una prueba de imagen (TC o RM craneal) para descartar LOE.
- •
Ante una lesión ocular en un paciente con infección por el VIH se deberá realizar un fondo de ojo y una exploración neurológica (B-III).
- •
En los casos en los que se sospeche una retinitis, y debido a su repercusión, se iniciará tratamiento empírico (B-II).
- •
Se recomienda remitir al paciente a un especialista en oftalmología, especialmente en los casos en los que exista afectación del segmento posterior (B-II).
En el mundo desarrollado el porcentaje de ingreso de los pacientes con infección por el VIH en las unidades de cuidados intensivos (UCI) varía entre el 5 y el 10%. La principal causa de ingreso es la insuficiencia respiratoria, fundamentalmente secundaria a la neumonía por Pneumocistis jirovecii (NPJ)22.
La toma de decisión sobre el ingreso del paciente con infección por el VIH en la UCI debe tomarse, al igual que en la población general, basándose en el pronóstico, considerando a este respecto tanto el proceso agudo que motiva el ingreso como la enfermedad de base, en este caso la infección por el VIH. No obstante, es importante reseñar que la situación inmunológica y virológica puntual del paciente no debe excluir el ingreso en la UCI por sí misma, ya que el TAR puede modificar esta situación de manera sustancial. Los niveles de CD4 no se relacionan con el pronóstico vital del paciente23.
La mortalidad en la UCI se asociaría más a la gravedad inicial del cuadro que motiva el ingreso. Sin embargo, la mortalidad a medio y largo plazo en los supervivientes al episodio que motivó el ingreso en la UCI parece relacionarse más con el estadio y la gravedad de la infección por el VIH.
Recomendación- •
Los criterios de ingreso en la UCI no difieren de los de la población general, y se deben realizar en relación al pronóstico del paciente, y no deben ser excluidos por presentar una situación inmunovirológica comprometida (B-III).
El niño con diagnóstico de VIH en el SU debe ser valorado de manera detenida, incidiendo fundamentalmente en la situación clínica e inmunovirológica actual. Es importante conocer el tratamiento específico, pues existe toxicidad diferente según los antirretrovirales que esté recibiendo, y es también importante saber si alguno de los antirretrovirales se ha introducido recientemente, pues las primeras semanas tras la introducción de la medicación es cuando más riesgo hay de efectos adversos. Se debe también preguntar si el niño está recibiendo cotrimoxazol de manera profiláctica, pues podría indicar situación de inmunodepresión actual o reciente.
Debido a la buena situación inmunovirológica del niño con infección VIH en España, la mayoría de las visitas al SU pueden tener un motivo no relacionado con la infección por el VIH o con la medicación antirretroviral, sino tratarse de la patología común del niño no infectado. Sin embargo, se debe estar atento a algunos síntomas de alarma que indican inmunodepresión, como la candidiasis oral, la diarrea prolongada o la pérdida importante de peso reciente. Los efectos secundarios de la medicación antirretroviral pueden ser motivo de consulta en el SU pediátrico. Se deben distinguir los cuadros inespecíficos o poco graves de los cuadros que pueden resultar muy graves. El caso más claro es el de los vómitos asociados a dolor abdominal y otros síntomas inespecíficos que pueden ser los síntomas iniciales de la acidosis láctica, la complicación más grave asociada a TAR, que si no se identifica de manera precoz puede progresar a un cuadro irreversible y en ocasiones fatal24. Existe una explicación detallada en las Recomendaciones de seguimiento del paciente pediátrico con infección VIH25.
En ocasiones, en los resultados de la analítica realizada en el SU se encuentran alteraciones de laboratorio significativas. En general, si la alteración no es grave y el niño está asintomático, se puede remitir al paciente a la consulta del especialista en VIH infantil para seguimiento preferente en 24-48h.
Las infecciones más frecuentes en el niño pequeño son infecciones respiratorias de las vías altas de etiología viral, así como también otitis, neumonías, gastroenteritis e infecciones urinarias. Otras causas menos frecuentes son varicela (niños no inmunizados) y meningitis, y en inmunodeprimidos, infección por CMV, micobacterias atípicas y NPJ. En la tabla 6 se recogen los criterios de ingreso hospitalario en el niño VIH con cuadro infeccioso.
Criterios de ingreso hospitalario en el niño con cuadro infeccioso
| • Situación de inmunodepresión (<15% CD4) |
| • Afectación importante del estado general con signos clínicos de insuficiencia respiratoria o mala perfusión periférica o mal estado de hidratación |
| • Alteración analítica con neutropenia severa o alteración de la coagulación |
| • Sintomatología neurológica |
| • Fiebre prolongada |
| • Sospecha de síndrome de reconstitución inmune |
- •
En el niño con infección por el VIH que acude al SU es fundamental conocer la medicación antirretroviral que toma y su situación inmunovirológica reciente (C-III).
- •
La acidosis láctica es una complicación grave asociada a la medicación antirretroviral que requiere la suspensión urgente de la medicación (B-II).
- •
Con el TAR, las infecciones oportunistas en el niño con infección VIH han disminuido de manera muy significativa, por lo que el enfoque del niño con fiebre debe hacerse a partir de su situación inmunológica más reciente (B-II).
La decisión de iniciar profilaxis postexposición ocupacional o no ocupacional se basa en la probabilidad o riesgo de transmisión del agente infeccioso en cada escenario.
La exposición laboral requiere una evaluación urgente, y en ocasiones exige una profilaxis sin demora.
Los escenarios en los que pueden producirse exposiciones no ocupacionales son relaciones sexuales (consentidas o no), transfusión de sangre o hemoderivados (algo extremadamente infrecuente en nuestro medio), accidentes con agujas u objetos cortantes, contacto con fluidos o tejidos infectados y mordeduras.
Es importante señalar que la efectividad de la profilaxis nunca es del 100%. Todas las profilaxis deben iniciarse antes de las 72h y han de ser controladas por un experto en las primeras 72h de la exposición26.
Recomendaciones- •
En los SU debe existir un protocolo consensuado de actuación frente a exposición a agentes biológicos tanto ocupacional como no ocupacional, así como métodos de diagnóstico rápido y con accesibilidad de 24h a los fármacos utilizados en la profilaxis postexposición (PPE) (A-III).
- •
La indicación de PPE se realizará tras la valoración de la fuente, del estado serológico del receptor y de las las características de la exposición (A-III).
- •
El inicio de la PPE debe ser precoz (idealmente en las 4 primeras horas), hasta las 72h. Su duración será de 4 semanas (A-II).
- •
No se recomienda efectuar PPE pasadas 72h (A-III).
- •
Cuando esté indicada la PPE, se recomienda una pauta convencional de 3 fármacos, recomendándose combinaciones fijas (TDF/FTC o ZDV/3TC) junto a un IP. En caso de no poder administrar un IP potenciado con ritonavir (IP/r), este puede ser sustituido por EFV o bien por una terapia con 3 ITIAN (ZDV/3TC+TDF/FTC) (A-III).
- •
Debe supervisarse por un experto en el manejo de la infección por VIH-1, reevaluando su indicación a las 24-72h del inicio (B-III).
- •
La PPE no ocupacional debe recomendarse en situaciones incluidas dentro del denominado «riesgo apreciable», siempre que se den las siguientes condiciones: instauración precoz, ausencia de contraindicación para tomar fármacos antirretrovirales y garantía de seguimiento clínico y analítico (B-III).
- •
En los casos de exposición sexual, se valorará el riesgo de infecciones de transmisión sexual (ITS) y embarazo (A-III).
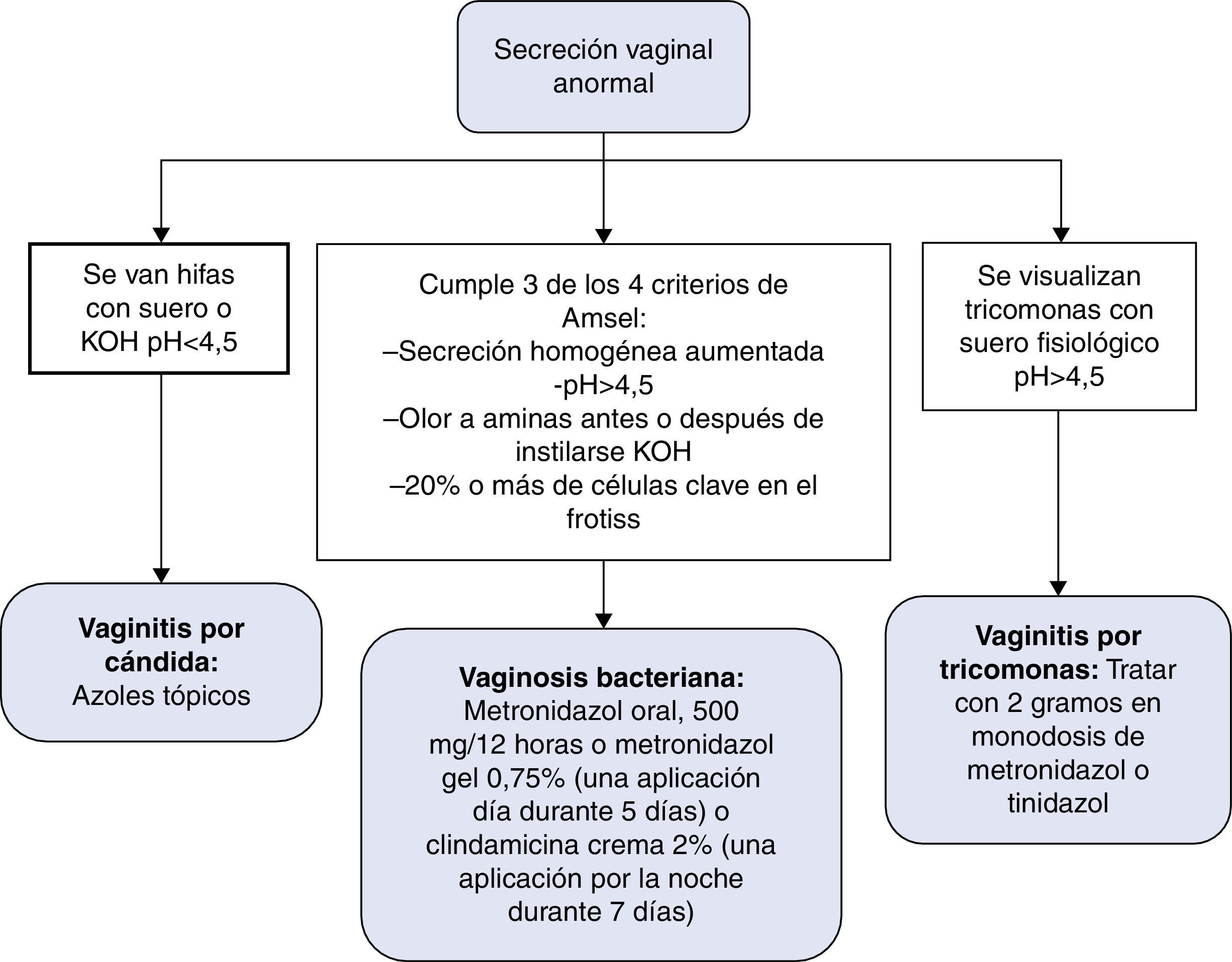
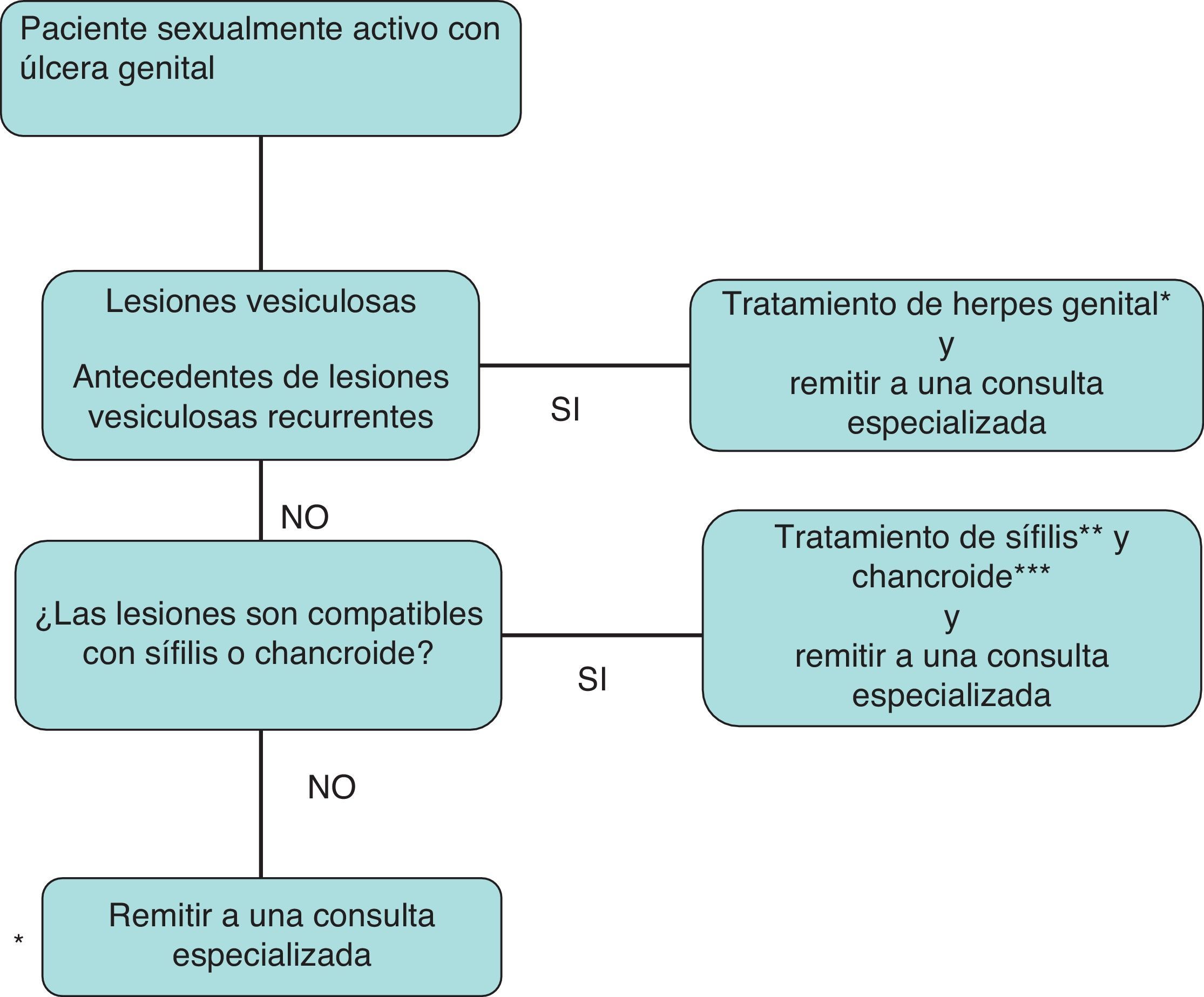
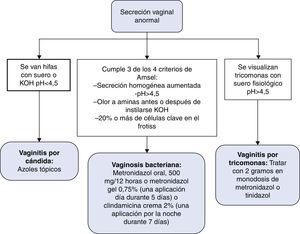
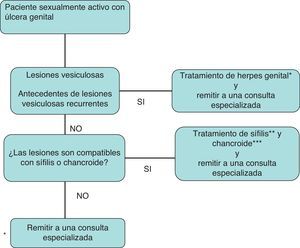
Las ITS son uno de los problemas de salud pública más importantes. La infección por el VIH está claramente interrelacionada con las ITS, no solo por compartir la vía de transmisión, sino también por el aumento de riesgo de transmisión del VIH26,27. En la figura 4 se recoge el algoritmo de diagnóstico y tratamiento de la secreción vaginal anormal. En la figura 5 se recoge el algoritmo de tratamiento empírico de la enfermedad ulcerosa genital.
Algoritmo de tratamiento empírico de la enfermedad ulcerosa genital.
*Aciclovir, 400mg/8h; famciclovir, 250mg/8h, o valaciclovir, 1g/12h, todos por vía oral, 7-10días. Casos graves: aciclovir 5mg/kg/8h intravenoso, 5-10días.
** Penicilina benzatina, 2,4millonesUI por vía intramuscular en monodosis.
***Azitromicina, 1g por vía oral; ceftriaxona, 250mg por vía intramuscular, ambas en monodosis; ciprofloxacino, 500mg/12h por vía oral, 3días, o eritromicina, 500mg/8h por vía oral, 7días.
- •
Deben tratarse todos los pacientes sintomáticos con uretritis o cervicitis, incluso cuando la observación al microscopio sea no diagnóstica (C-III).
- •
Las mujeres que son contactos de un hombre con uretritis gonocócica (UG) o uretritis no gonocócica (UNG) por Chlamydia deben ser tratadas empíricamente (B-II).
- •
A las 3 semanas del tratamiento de una uretritis o cervicitis debe realizarse una entrevista para asegurar el cumplimiento del mismo y la resolución de los síntomas (B-III).
- •
Ante una úlcera genital, se recomienda la toma de muestras en la medida de lo posible para establecer un diagnóstico etiológico a partir de los exámenes microbiológicos (A-III).
- •
Se recomienda acudir a algoritmos de diagnóstico y tratamiento sencillos de la enfermedad ulcerosa genital (EUG). Se debe garantizar el seguimiento del paciente en una consulta especializada para evaluar la respuesta terapéutica y realizar cribado de otras ITS (A-III).
- •
Se debe mantener la abstinencia sexual hasta la curación total de la ulceración genital (A-III).
- •
Todo paciente sexualmente activo con EUG debe ser testado frente al VIH (A-III).
- •
Los pacientes con infección por el VIH deben ser tratados con el mismo régimen terapéutico que los pacientes seronegativos, siendo la penicilina el tratamiento de elección (A-II).
- •
En las embarazadas la penicilina es el tratamiento de elección, incluso en las alérgicas, en quien habría que hacer una desensibilización y tratamiento con penicilina (A-III).
- •
En todo paciente con clínica neurológica y/o fracaso terapéutico está indicada la realización de una PL para descartar la posibilidad de neurosífilis (A-III).
El uso de drogas ilegales y de alcohol se asocia a conductas de riesgo de infección y transmisión del VIH. Un reciente metaanálisis ha demostrado que el consumo de alcohol es un factor de riesgo independiente para mantener relaciones sexuales sin protección, relacionándose directamente con la transmisión de VIH y otras ITS28,29.
Respecto a la asociación entre consumo de drogas por vía parenteral e infección por VIH, los datos son alentadores, pues según los registros existentes ha disminuido de forma progresiva el número de nuevos diagnósticos de VIH en esa población. Parece que la caída en el número de infecciones en este grupo se debe más al descenso de los usuarios que se inyectan drogas que a una disminución de las conductas de riesgo para la transmisión del VIH. Es por ello que debemos seguir prestando atención a la transmisión sexual y a las parejas de los usuarios de la vía parenteral seropositivos.
En general, el abordaje en urgencias de las intoxicaciones agudas por drogas debe hacerse desde un enfoque sindrómico, debido fundamentalmente al uso combinado de sustancias y el cuadro clínico polimórfico resultante.
En los SU cercanos a aeropuertos de zonas turísticas o con vuelos transcontinentales suelen presentarse casos de body-packers (transportadores de drogas —cocaína o heroína— en el interior del tubo digestivo, ingeridas en forma de pequeñas bolas muy bien embaladas, en gran cantidad y con una enorme pureza, o bien introducidas vía anal o vaginal) o los body-stuffers (pacientes que se tragan la droga cuando van a ser detenidos, para ocultarla). En ambos casos la extracción con endoscopio debe obviarse, por el riesgo de rotura de los envoltorios.
Recomendaciones- •
En caso de sospecha de ser víctima de sumisión química, un test de drogas negativo no excluye la posibilidad de agresión sexual, por lo que deben adoptarse las medias preventivas frente al riesgo de infecciones de transmisión sexual (C-III).
- •
En casos de body-packers, debe pautarse tratamiento con soluciones de polietilenglicol por vía oral, hasta su expulsión completa. En caso de que el paciente presente clínica tóxica o un test urinario inicialmente negativo que vire a positivo, es indicación de laparotomía urgente, al ser sugestivo de rotura de las bolas de droga, con el consiguiente riesgo de muerte (B-III).
La solicitud y la interpretación de pruebas complementarias en el SU deben basarse siempre en la historia clínica y en la exploración física del paciente; por ello, estas pruebas nunca podrán sustituir un juicio clínico.
En nuestro medio casi el 40% de los nuevos diagnósticos de VIH se producen en situaciones de lo que llamamos presentador tardío (cuando la cifra de linfocitos CD4 está por debajo de las 200células/ml de plasma o con el diagnóstico simultáneo de una infección oportunista diagnóstica de sida). Esto implica un exceso de morbimortalidad para el individuo y un riesgo elevado de transmisión mantenida para la sociedad. En función de la gravedad del cuadro que presente el paciente o del destino del mismo, el médico de urgencias puede recomendar la realización de la prueba en su centro de atención primaria para los pacientes que no requieran ingreso, la realización de forma diferida durante el ingreso hospitalario o la realización de un test rápido para los pacientes cuyo cuadro clínico requiera del conocimiento de la situación serológica respecto al VIH de forma no diferible30.
Recomendación- •
Ante la sospecha clínica de infección por el VIH en un paciente que no conozca su situación serológica, el médico de urgencias debe recomendar la realización de la prueba, ya sea de forma urgente o diferida, en función de la gravedad del cuadro (B-III).
La realización de este documento ha sido financiada con fondos propios de la SPNS.
Conflicto de interesesCon el fin de evitar y/o minimizar los posibles conflictos de intereses, las personas que forman el panel de expertos han realizado una declaración formal de intereses. En esta declaración parte de los/as autores/as han recibido financiación para participar en congresos y para la realización de investigaciones, y también han recibido pagos como ponentes por parte de instituciones públicas y laboratorios farmacéuticos. Estas actividades no afectan a la claridad del presente documento al no entrar lo recomendado en conflicto de intereses con los honorarios y/o las ayudas recibidas. Cabe resaltar que con respecto a los fármacos, en el documento solamente se habla de principio activo y no de marca comercial.
Rosa Polo Rodríguez. Especialista en Medicina Interna. Secretaría del Plan Nacional sobre el sida. MSSSI. Madrid.
Enric Pedrol Clotet. Especialista en Medicina Interna. Hospital de Sant Pau i Santa Tecla. Tarragona.
Vicente Abril López de Medrano. Especialista en Medicina Interna. Consorcio Hospital General Universitario. Valencia.
Jordi Blanch Andreu. Especialista en Psiquiatría. Hospital Clínic. Barcelona.
Guillermo Burillo-Putze. Especialista en Medicina Familiar y Comunitaria. Hospital Universitario de Canarias.
Jose Ramón Blanco Ramos. Especialista en Medicina Interna. Hospital San Pedro. Logroño.
Sonsoles Callejas Pérez. Especialista en Medicina de Familiar y Comunitaria. Hospital Universitario. Fuenlabrada.
Ramón Canet González. Especialista en Medicina Interna. Hospital Can Misses. Ibiza.
Antonio Delegido Sánchez-Migallón. Especialista en Medicina Interna. Hospital de Sant Pau i Santa Tecla. Tarragona.
Carlos Dueñas Gutiérrez. Especialista en Medicina Interna. Complejo Asistencial Universitario. Burgos.
Oscar Luis Ferrero Beneitez. Especialista en Medicina Interna. Hospital de Basurto. Bilbao.
Inmaculada Gisbert Civera. Licenciada en Psicología. Master en Salud Pública. Madrid.
Juan González del Castillo. Especialista en Medicina Interna. Hospital Clínico San Carlos. Madrid.
Marisa Navarro Gómez. Especialista en Pediatría. Hospital Gregorio Marañón. Madrid.
Josep M. Guardiolo Tey. Especialista en Medicina Interna. Hospital de la Santa Creu i Sant Pau. Barcelona.
Agustín Julian Jimenez. Especialista en Medicina Interna. Hospital Virgen de la Salud. Toledo.
Rosario Palacios Muñoz. Especialista en Medicina Interna. Hospital Virgen de la Victoria. Málaga.
Rafael Perelló Carbonell. Especialista en Medicina Familiar y Comunitaria. Servicio de Urgencias. Hospital Clínic. Barcelona.
Pablo Rojo Conejo. Especialista en Pediatría. Hospital 12 de Octubre. Madrid.
Ignacio de los Santos Gil. Especialista en Medicina Interna. Hospital Universitario de la Princesa. Madrid.
Oscar Miró Andreu. Especialista en Medicina Interna. Hospital Clínic. Barcelona.
| ABC | Abacavir |
| ADN | Ácido desoxirribonucleico |
| APV | Amprenavir |
| ARN | Ácido ribonucleico |
| ARV | Antirretroviral |
| ATV | Atazanavir |
| AV | Agudeza visual |
| BID | Pauta de tratamiento administrada 2 veces al día |
| CMV | Citomegalovirus |
| CVP | Carga viral plasmática |
| d4T | Estavudina |
| ddI | Didanosina |
| DRV | Darunavir |
| DM | Diabetes mellitus |
| EFV | Efavirenz |
| ENF | Enfuvirtida |
| ETR | Etravirina |
| EUG | Enfermedad ulcerosa genital |
| FAR | Fármacos antirretrovirales |
| FPV | Fosamprenavir |
| FTC | Emtricitabina |
| HTA | Hipertensión arterial |
| IDV | Indinavir |
| IF | Inhibidores de la fusión |
| IInt | Inhibidores de la integrasa |
| IP | Inhibidores de la proteasa |
| IP/r | Inhibidor de la proteasa (IP) potenciado con ritonavir |
| IST | Interrupción estructurada del tratamiento |
| ITIAN | Inhibidores de la transcriptasa inversa análogos de nucleósidos |
| ITINN | Inhibidores de la transcriptasa inversa no análogos |
| ITS | Infecciones de transmisión sexual |
| ITT | Análisis por intención de tratamiento |
| IU | Inhibidores de la unión al receptor CCR5 |
| i.v. | Intravenoso |
| LMP | Leucoencefalopatía multifocal progresiva |
| LNH | Linfoma no Hodgkin |
| LOE | Lesión ocupante de espacio |
| LPV | Lopinavir |
| MN | Mononucleares |
| MU | Millones de unidades |
| MVC | Maraviroc |
| NFV | Nelfinavir |
| NPJ | Neumonía por Pneumocystis jirovecii |
| NVP | Nevirapina |
| PCJ | Pneumocistis jiroveci |
| PCR | Reacción en cadena de la polimerasa |
| PCT | Procalcitonina |
| PIC | Presión intracraneal |
| PL | Punción lumbar |
| PMN | Polimorfonucleares |
| QD | Fármaco o pauta de tratamiento administrada una vez al día |
| RAL | Raltegravir |
| RM | Resonancia magnética |
| RTV | Ritonavir |
| SNC | Sistema nervioso central |
| SQV | Saquinavir |
| SRI | Síndrome de reconstitución inmune |
| SU | Servicio de Urgencias |
| TC | Tomografía computarizada |
| TAR | Tratamiento antirretroviral |
| TARGA | Tratamiento antirretroviral de alta eficacia |
| TB | Tuberculosis, tuberculosa |
| TDF | Tenofovir DF |
| TPV | Tipranavir |
| 3TC | Lamivudina |
| UDVP | Usuario/a de drogas por vía parenteral |
| UG | Uretritis gonocócica |
| UNG | Uretritis no gonocócica |
| VIH | Virus de la inmunodeficiencia humana |
| VHS | Virus herpes simplex |
| VO | Vía oral |
| VVZ | Virus varicela zóster |
| ZDV | Zidovudina |