Staphylococcus aureus resistente a meticilina (SARM) ST398 es una línea genética asociada con ganado que puede causar infecciones en humanos.
MétodosSe presentan 4 casos de lesiones cutáneas por SARM ST398 en 3 pacientes, dos de ellos trabajadores de granja de cerdos. Asimismo, se estudió el estado de portador nasal de los pacientes y sus familiares convivientes. Las cepas SARM fueron tipadas (SCCmec, spa, agr y MLST) y se determinó su fenotipo y genotipo de resistencia a antimicrobianos y la presencia de los genes de virulencia.
ResultadosSe aislaron 20 cepas SARM ST398 de lesiones de 3 pacientes y de muestras nasales de 2 pacientes y 5 familiares. Los aislados se tiparon: spa-tipo t011 o t108; agr-tipo I y SCCmec IVa o V. Las cepas fueron todas resistentes a tetraciclina y 15 de ellas presentaron un fenotipo de multirresistencia, pero no genes de virulencia.
ConclusionesSARM ST398 está emergiendo en nuestro medio, frecuentemente asociado a infección de piel y partes blandas en individuos con relación profesional con granjas de cerdos. La resistencia a tetraciclina es un marcador importante para la detección de estas cepas.
Livestock-associated methicillin-resistant Staphylococcus aureus (LA-MRSA) of sequence type ST398 is a genetic lineage also described in human infections.
MethodsCutaneous infections related with MRSA ST398 are described in 3 patients, two of them pig farmers. The MRSA nasal carriage by patients and their relatives was also studied. MRSA ST398 strains were typed (SCCmec, spa, agr and MLST) and the antimicrobial resistance pattern and virulence genes were determined.
ResultsTwenty MRSA ST398 isolates were recovered in lesions of three patients, and in nasal samples of two patients and five relatives. Isolates were typed: spa-type t011 or t108; agr-type I and SCCmec IVa or V. MRSA strains were tetracycline-resistant and 15 of them showed a phenotype and genotype of multi-resistance, but they were free of tested virulence genes.
ConclusionsLA-MRSA ST398 is an emergent problem in our country, mainly associated with skin and soft tissue infections in people with professional relationships with pig farms. Tetracycline resistance is an important marker for MRSA ST398 detection.
En la década pasada, las cepas de Staphylococcus aureus (S. aureus) resistentes a meticilina adquiridas en la comunidad (SARM-CO) fueron un problema creciente en los EE. UU., hasta representar en la actualidad una endemia y constituir el agente etiológico de la mayoría de las infecciones de piel y partes blandas (IPPB) de ese país1. La prevalencia de SARM-CO en Europa no ha seguido el mismo patrón y continúa siendo baja, aunque es objeto de estrecha vigilancia. Se han detectado casos de SARM-CO en la práctica totalidad de los países europeos incluyendo Holanda y los países nórdicos que, como ya es conocido, presentan tasas muy bajas de SARM hospitalario. No obstante, en países como Grecia las tasas de SARM-CO en algunos centros se aproximan peligrosamente a las cifras de EE.UU2. En contraste con América del Norte, donde el clon USA300 (ST8-IV) es el predominante, los SARM-CO en Europa se caracterizan por una heterogeneidad clonal y las cepas más comunes pertenecen al llamado clon Europeo (ST80-IV), aunque los aislados de USA300 están aumentado.
Algunos de los clones de SARM-CO que están emergiendo en Europa están relacionados con los animales, especialmente con los cerdos. Este fenómeno se ha estudiado sobre todo en países como Holanda, Alemania o Dinamarca: es el llamado SARM asociado al ganado (SARM-AG) que incluye principalmente cepas pertenecientes a la línea clonal 398 (ST398) y de origen porcino3–5. Este tipo de cepas también se ha detectado en nuestro país6,7, y generalmente las cepas son resistentes a tetraciclina (TETR). El conocimiento de la epidemiología de estos nuevos SARM es esencial para implementar nuevas iniciativas de control que prevengan su potencial diseminación en Europa2.
Relatamos la experiencia de 4 casos de infecciones cutáneas comunitarias relacionadas con SARM ST398 en 3 pacientes, dos de ellos con contacto profesional con ganado porcino, realizándose la caracterización y tipado molecular de las cepas, el estudio del fenotipo y genotipo de resistencia a antimicrobianos y su posible repercusión, tanto clínica como epidemiológica.
MétodosDetección de los casos clínicosSe estudiaron durante un período de 3 años (1 de junio 2008-1 de junio 2011) las muestras procedentes de cultivos dermatológicos, piel y tejidos blandos y exudados procedentes de consultas externas de Dermatología y Urgencias del Hospital Royo Villanova de Zaragoza. En este intervalo se aisló S. aureus en 121 pacientes, y en 15 de ellos se identifico SARM, siendo 10 de los casos considerados como SARM-CO y en 6 de ellos las cepas presentaron el fenotipo TETR. Las cepas de los 6 pacientes con SARM-TETR fueron tipadas como ST398, describiéndose en este estudio los datos clínicos relacionados con 3 de estos pacientes, ya que otros han sido publicados con anterioridad6,7.
Casos y pacientesSe incluyeron en este estudio 4 casos de 3 pacientes con lesiones cutáneas:
Caso A Paciente 1Mujer de 45 años de edad, trabajadora de una granja de cerdos, con antecedentes personales dermatológicos de eccema. El motivo de consulta fue una lesión en el cuello, consistente en una placa eritematosa y pruriginosa.
Caso B Paciente 2Varón de 46 años de edad, trabajador de una granja de cerdos. Consultó por una paroniquia intensa en varios dedos de las manos de largo tiempo de evolución. Había sido tratado con antifúngicos tópicos y orales con resultados poco satisfactorios.
Caso C Paciente 2El mismo paciente del caso B, un año después de consultar por las lesiones ungueales, consultó por una nueva lesión de tórpida cicatrización en la cara, de varias semanas de evolución.
Caso D Paciente 3Mujer de 48 años de edad que acudió al servicio de urgencias del hospital por presentar exudado ótico y dolor local. Entre sus antecedentes refería eccema de conducto auditivo externo de años de evolución. La paciente no tenía relación con ganado ni con animales domésticos.
Obtención de muestras e identificación y caracterización de las cepasEn las lesiones de los 4 casos presentados se obtuvo un cultivo abundante de estafilococos que fueron identificados como S. aureus. La resistencia a oxacilina y el patrón de resistencia a otros 18 antimicrobianos fue determinado mediante microdilución (paneles comercializados Vitek2, BioMérieux) y difusión en agar. Se realizó la caracterización genética de las cepas SARM (MLST, tipado de spa, agr y SCCmec), el estudio de factores de virulencia (lukS-PV/lukF-PV, tst, eta, etb y etd) y de genes de resistencia a antimicrobianos (mecA, tetK, tetL, tetM, ermA, ermB, ermC, msrA, ant(4′), aph(2′)-acc(6′), y dfrK) mediante PCR y secuenciación6.
Una vez conocida la identificación definitiva, se instó a los pacientes a volver al laboratorio de Microbiología, donde se repitieron las tomas (aunque en el caso D ya no existía exudado ótico, probablemente por estar bajo tratamiento antimicrobiano), y se tomaron frotis nasales para conocer el estado de portador. En el caso B, el paciente 2 fue visitado en varias ocasiones para ver su evolución y en cada una de ellas se recogieron muestras de sus lesiones y frotis nasales. Se obtuvieron asimismo hisopados nasales de los familiares que convivían con los pacientes. Las cepas SARM obtenidas de los frotis nasales de pacientes y convivientes fueron caracterizadas y tipadas como se ha comentado anteriormente.
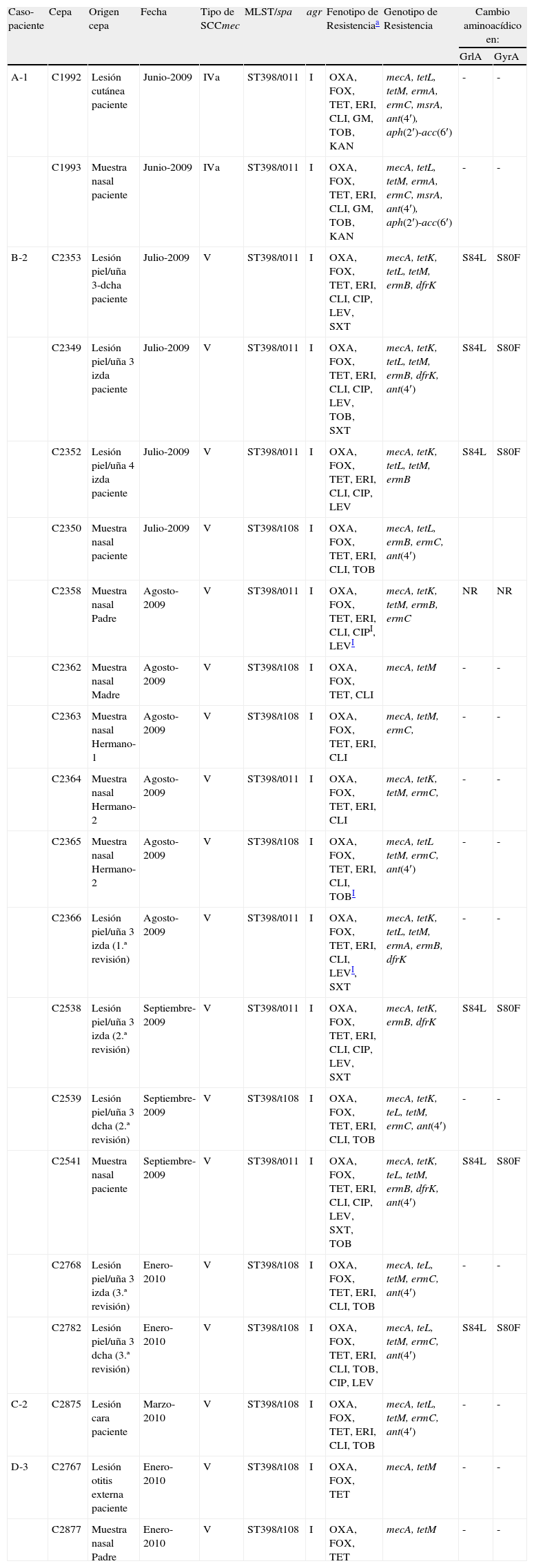
ResultadosLas características de las cepas aisladas de las lesiones en cada caso y de los frotis nasales de pacientes y familiares se muestran en la tabla 1 (una cepa por muestra, total: 20 cepas SARM). Como puede observarse, en las muestras de las lesiones de los 4 casos se aisló SARM ST398, y los pacientes 1 y 2 fueron asimismo portadores nasales. Los tipos spa detectados en las cepas clínicas y nasales de los pacientes fueron t011 (mayoritario) y t108. También se aislaron cepas SARM ST398 pertenecientes a los spa-tipos t011 y t108 en muestras nasales de 5 familiares de los pacientes 2 y 3 (tabla 1). Es interesante reseñar que en el paciente 2 se detectaron cepas con spa-tipo t011 y t108 en las lesiones, y asimismo, ambos tipos spa fueron detectados en las muestras nasales de los convivientes.
Características de las 20 cepas de SARM ST398 aisladas a partir de los 4 casos de infecciones cutáneas de los pacientes y los frotis nasales de los 3 pacientes y sus familiares
| Caso-paciente | Cepa | Origen cepa | Fecha | Tipo de SCCmec | MLST/spa | agr | Fenotipo de Resistenciaa | Genotipo de Resistencia | Cambio aminoacídico en: | |
| GrlA | GyrA | |||||||||
| A-1 | C1992 | Lesión cutánea paciente | Junio-2009 | IVa | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, GM, TOB, KAN | mecA, tetL, tetM, ermA, ermC, msrA, ant(4′), aph(2′)-acc(6′) | - | - |
| C1993 | Muestra nasal paciente | Junio-2009 | IVa | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, GM, TOB, KAN | mecA, tetL, tetM, ermA, ermC, msrA, ant(4′), aph(2′)-acc(6′) | - | - | |
| B-2 | C2353 | Lesión piel/uña 3-dcha paciente | Julio-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, CIP, LEV, SXT | mecA, tetK, tetL, tetM, ermB, dfrK | S84L | S80F |
| C2349 | Lesión piel/uña 3 izda paciente | Julio-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, CIP, LEV, TOB, SXT | mecA, tetK, tetL, tetM, ermB, dfrK, ant(4′) | S84L | S80F | |
| C2352 | Lesión piel/uña 4 izda paciente | Julio-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, CIP, LEV | mecA, tetK, tetL, tetM, ermB | S84L | S80F | |
| C2350 | Muestra nasal paciente | Julio-2009 | V | ST398/t108 | I | OXA, FOX, TET, ERI, CLI, TOB | mecA, tetL, ermB, ermC, ant(4′) | |||
| C2358 | Muestra nasal Padre | Agosto-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, CIPI, LEVI | mecA, tetK, tetM, ermB, ermC | NR | NR | |
| C2362 | Muestra nasal Madre | Agosto-2009 | V | ST398/t108 | I | OXA, FOX, TET, CLI | mecA, tetM | - | - | |
| C2363 | Muestra nasal Hermano-1 | Agosto-2009 | V | ST398/t108 | I | OXA, FOX, TET, ERI, CLI | mecA, tetM, ermC, | - | - | |
| C2364 | Muestra nasal Hermano-2 | Agosto-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI | mecA, tetK, tetM, ermC, | - | - | |
| C2365 | Muestra nasal Hermano-2 | Agosto-2009 | V | ST398/t108 | I | OXA, FOX, TET, ERI, CLI, TOBI | mecA, tetL tetM, ermC, ant(4′) | - | - | |
| C2366 | Lesión piel/uña 3 izda (1.ª revisión) | Agosto-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, LEVI, SXT | mecA, tetK, tetL, tetM, ermA, ermB, dfrK | - | - | |
| C2538 | Lesión piel/uña 3 izda (2.ª revisión) | Septiembre-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, CIP, LEV, SXT | mecA, tetK, ermB, dfrK | S84L | S80F | |
| C2539 | Lesión piel/uña 3 dcha (2.ª revisión) | Septiembre-2009 | V | ST398/t108 | I | OXA, FOX, TET, ERI, CLI, TOB | mecA, tetK, teL, tetM, ermC, ant(4′) | - | - | |
| C2541 | Muestra nasal paciente | Septiembre-2009 | V | ST398/t011 | I | OXA, FOX, TET, ERI, CLI, CIP, LEV, SXT, TOB | mecA, tetK, teL, tetM, ermB, dfrK, ant(4′) | S84L | S80F | |
| C2768 | Lesión piel/uña 3 izda (3.ª revisión) | Enero-2010 | V | ST398/t108 | I | OXA, FOX, TET, ERI, CLI, TOB | mecA, teL, tetM, ermC, ant(4′) | - | - | |
| C2782 | Lesión piel/uña 3 dcha (3.ª revisión) | Enero-2010 | V | ST398/t108 | I | OXA, FOX, TET, ERI, CLI, TOB, CIP, LEV | mecA, teL, tetM, ermC, ant(4′) | S84L | S80F | |
| C-2 | C2875 | Lesión cara paciente | Marzo-2010 | V | ST398/t108 | I | OXA, FOX, TET, ERI, CLI, TOB | mecA, tetL, tetM, ermC, ant(4′) | - | - |
| D-3 | C2767 | Lesión otitis externa paciente | Enero-2010 | V | ST398/t108 | I | OXA, FOX, TET | mecA, tetM | - | - |
| C2877 | Muestra nasal Padre | Enero-2010 | V | ST398/t108 | I | OXA, FOX, TET | mecA, tetM | - | - | |
Todas las cepas de pacientes y convivientes presentaron resistencia a tetraciclina y portaban diferentes combinaciones de los genes tetM, tetL y tetK. Las cepas procedentes de los pacientes 1 y 2 mostraron un fenotipo de multirresistencia con una gran diversidad de genes de resistencia; sin embargo, las cepas del paciente 3 (caso D) solo presentaron resistencia a tetraciclina, además de a oxacilina (tabla 1). Todas las cepas SARM del estudio fueron negativas para los genes de virulencia analizados (lukS-PV/lukF-PV, tst, eta, etb y etd).
DiscusiónSARM ST398 fue descrito por primera vez en 2005 en países del centro de Europa3. Se relaciona con animales de producción y en especial con cerdos, siendo un riesgo también para el ser humano4. Desde entonces se ha aislado en otros países europeos, así como en América y Asia. En 2007, un tercio de todos los SARM en Holanda fueron ST3985. En otros países europeos, la situación no es bien conocida, pero la prevalencia de estas cepas en muestras ambientales de granjas de porcino se ha demostrado muy elevada en países como el nuestro, y en otros como Alemania y Bélgica8. Este hecho constituye un factor de riesgo para la colonización nasal y cutánea del personal en contacto con los animales, lo que puede conducir a su vez a una mayor probabilidad de infección en los portadores de estos microorganismos. Aunque, en general, las infecciones producidas por SARM-AG son de piel y tejidos blandos superficiales, como en estos casos y otros publicados6, no se debe bajar la guardia pues se han visto también implicados en infecciones graves como endocarditis, neumonías asociadas a ventilación mecánica, etc.4,9.
Las veinte cepas de SARM ST398 de este estudio fueron aisladas de lesiones cutáneas de 3 pacientes y de la investigación de portadores nasales en los propios pacientes y sus familiares/contactos más próximos. Dos de los 3 pacientes eran granjeros de porcino, claro criterio epidemiológico para la aparición de cepas de SARM ST398. Sin embargo, la paciente 3 no tenía relación profesional con animales, aunque su padre (con el que no convivía) sí había sido granjero de cerdos hacía 10 años. Aunque se desconoce la razón y origen de esta adquisición de SARM ST398, no se puede descartar la posibilidad de un estado prolongado de portador y transmisión interhumana.
En cuanto a la caracterización molecular de las cepas, se han detectado ST398 con dos tipos diferentes de spa (t011 y t108). Ambos tipos, junto con el t034 corresponden a los mayoritariamente encontrados hasta el momento4,7. No obstante, según algunos trabajos recientes parece que otros tipos de spa se están expandiendo7, lo que indica una probable evolución de esta línea genética.
Por otro lado, en este estudio se han hallado dos tipos de SCCmec (IVa y V), los cuales han sido previamente detectados en SARM ST39810. Algunos autores proponen una relación entre el spa tipo t011 y el SCCmec IVa y entre el spa tipo t108 y el SCCmec V10. En nuestro estudio todas las cepas con SCCmec IVa fueron t011 pero la mayoría de las que presentaron el spa tipo t011 fueron SCCmec V. Este hecho ya ha sido observado en otros estudios11.
La mayoría de los aislados SARM ST398 presentaron fenotipo de multirresistencia. Se han detectado una gran diversidad de genes de resistencia a tetraciclina (tetL, tetM y/o tetK), macrólidos y lincosamidas (ermA, ermB y ermC), aminoglucósidos (ant[4′]) y trimetoprim (dfrK); siendo este último gen descrito por primera vez en una cepa de SARM ST39812. Los aislamientos de SARM-AG suelen ser sensibles a la mupirocina y al ácido fusídico lo que facilita el tratamiento de infecciones cutáneas con estos antimicrobianos.
Todas las cepas incluidas en este estudio fueron negativas por PCR para las toxinas estudiadas, incluida la leucocidina de Panton-Valentine. Es conocido que SARM-AG tiene menos factores de patogenicidad que otros SARM de diferentes líneas genéticas13, aunque se han descrito algunas cepas ST398 positivas para la leucocidina de Panton-Valentine, tanto en SARM como en SASM14.
Todos los SARM ST398 del estudio fueron resistentes a la tetraciclina, y esta característica es común a esta línea genética, por lo que puede ser un buen marcador inicial de sospecha en aislados de S. aureus implicados en IPPB, especialmente si existe relación profesional con animales,4,6-8. De hecho, en nuestro estudio, todos los aislados de SARM comunitarios TETR procedentes de lesiones de piel y tejidos blandos fueron ST398, y en 5 de 6 pacientes existía el antecedente epidemiológico de contacto estrecho y reiterado con ganado porcino. En este sentido, podría ser pertinente la inclusión de una pregunta en la historia clínica sobre el posible contacto profesional del paciente con animales en aquellos casos de sospecha epidemiológica de SARM ST398.
Por último, este estudio constata la peculiar ecología de S. aureus en los pacientes que están en contacto próximo con ganado porcino y sería recomendable extremar las medidas de higiene y protección en las granjas. En nuestro ámbito, aquellos casos en los que se encontraron cepas de SARM-AG en lesiones cutáneas se asociaron generalmente con colonizaciones nasales y con un patrón de resistencia múltiple que incluía tetraciclinas, macrólidos, lincosamidas, aminoglucósidos, y ocasionalmente quinolonas y cotrimoxazol, lo que hace su tratamiento difícil sin la guía de un cultivo y un estudio de sensibilidad. Asimismo, pensamos que, de igual modo que ya sucede en otros países como Holanda, la relación profesional de los pacientes con el ganado –especialmente porcino− debería añadirse a los habituales factores de riesgo para estar colonizado por SARM.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Este trabajo ha sido financiado en parte por el proyecto SAF2009-08570 del Ministerio de Ciencia e Innovación y Feder. Carmen Lozano tiene una beca predoctoral del Ministerio de Ciencia e Innovación de España.