La diabetes es una de las complicaciones metabólicas más frecuentes de la gestación y se asocia a un incremento del riesgo de morbimortalidad maternal y fetal, que pueden evitarse y/o reducirse con un adecuado control. En la diabetes pregestacional, la preparación específica previa a la gestación es indispensable para intentar conseguir un control glucémico lo más próximo a la normalidad, evaluar complicaciones y revisar las pautas de tratamientos farmacológicos. En el caso de la diabetes gestacional, el tratamiento de esta entidad ha demostrado disminuir la tasa de complicaciones maternas y perinatales, por lo que su diagnóstico está justificado. En relación con la estrategia diagnóstica, ante la falta de consenso y la controversia desatada tras la aparición de los nuevos criterios IADPSG, el grupo ha decidido mantener la misma estrategia diagnóstica en 2 pasos y con los mismos puntos de corte hasta disponer de datos sólidos que avalen la introducción de nuevos criterios.
Diabetes is one of the most common metabolic complications of pregnancy, and is associated with an increased risk of maternal and foetal morbidity and mortality that can be prevented and/or reduced with adequate glycaemic control. In pre-gestational diabetes, specific preparation prior to the pregnancy is essential in order to achieve glycaemic control near to normal as possible and to evaluate complications and review pharmacologic treatment prescription. The treatment of gestational diabetes has been shown to decrease the rate of maternal and perinatal complications, thus its diagnosis is justified. As regards the diagnostic strategy and due to the lack of consensus and the controversy arising after the publication of the new International Association of the Diabetes and Pregnancy Study Groups (IADPSG), the group has decided to keep the same diagnostic strategy in two stages, and with the same cut-off points, until there are solid data available that support the introduction of new criteria.
Uno de los objetivos del grupo de Diabetes y Embarazo (GEDE) desde su formación en 1994 es mejorar la asistencia de la gestante con diabetes y de su hijo, así como estimular la investigación en este campo. Por este motivo, uno de los primeros cometidos del grupo fue el desarrollo y la publicación de la primera guía asistencial que vio la luz en 19951. De ella se han realizado ya 2 actualizaciones en los años 20002 y 20063, y la que nos ocupa es la última revisión.
Desde su última edición, se han introducido nuevos formulaciones terapéuticas y se han publicado múltiples trabajos, algunos de ellos sólidos, que han motivado en algunos casos cambios en la práctica clínica habitual. Entre ellos cabría destacar que la utilización cada vez más generalizada de los análogos de insulina se ha visto avalada por estudios observacionales y ensayos clínicos que no evidencian inferioridad, la utilización creciente de los antidiabéticos orales en el tratamiento de la diabetes gestacional, la necesidad de optimizar aún más el control pregestacional con objeto de disminuir la aparición de malformaciones congénitas, y por último, pero no por ello menos importante, el debate abierto en torno a los nuevos criterios diagnósticos de la diabetes gestacional desarrollados en base a los resultados del estudio Hyperglycemia and Adverse Pregnancy Outcomes (HAPO). Este último ya fue merecedor de un editorial en el que se explicaban los motivos por los que no se consideraba adecuado el cambio en el 20104. Por este motivo, se ha considerado oportuno realizar una revisión de la guía.
Esta guía es fruto del consenso de todos los miembros del grupo, integrado mayoritariamente por endocrinólogos y obstetras y auspiciado por la Sociedad Española de Diabetes (SED) y la Sociedad Española de Obstetricia y Ginecología (SEGO), revisada por el Dr. Ricardo Closa, miembro de la Sociedad Española de Pediatría (Sección de Neonatología), y pretende ser un elemento de ayuda tanto en el tratamiento y el seguimiento de las mujeres con diabetes que desean una gestación como de aquellas diagnosticadas en el curso de esta.
IntroducciónLa diabetes mellitus (DM) constituye la alteración metabólica que más frecuentemente se asocia al embarazo, afectando al pronóstico de la madre y al de su futuro hijo. Aproximadamente un 1% de todas las mujeres embarazadas presentan DM pregestacional (DMPG) y hasta un 12% de los casos, dependiendo de la estrategia diagnóstica empleada, presentará diabetes gestacional (DMG) en el transcurso del embarazo5,6.
La diabetes mellitus durante el embarazo es un factor de riesgo para el desarrollo de complicaciones en la madre y en la descendencia:
Repercusión de la diabetes mellitus sobre la gestación- •
Infecciones urinarias, candidiasis vaginal, polihidramnios, estados hipertensivos del embarazo y prematuridad.
- •
Diabetes mellitus pregestacional: malformaciones y/o abortos (periodo de organogénesis) y crecimiento intrauterino restringido (CIR) en situaciones de vasculopatía materna.
- •
En ambos tipos de diabetes (DMPG y DMG) y como consecuencia del hiperinsulinismo fetal secundario a hiperglucemia materna:
- –
Macrosomía (distocias, traumatismo obstétrico y aumento de la tasa de cesáreas).
- –
Riesgo de pérdida de bienestar fetal ante o intraparto.
- –
Miocardiopatía hipertrófica.
- –
Inmadurez fetal que puede manifestarse como síndrome de distrés respiratorio o alteraciones metabólicas.
- –
- •
Diabetes mellitus pregestacional: los cambios hormonales fisiológicos del embarazo son los responsables de las modificaciones en las necesidades insulínicas, que habrá que adecuar a lo largo del embarazo. Así mismo, el embarazo puede favorecer el inicio y/o la progresión de determinadas complicaciones vasculares específicas de la DMPG (retinopatía).
- •
Diabetes mellitus gestacional: los cambios hormonales fisiológicos del embarazo constituyen el factor desencadenante de la intolerancia glucídica responsable de la aparición de la diabetes.
La aparición de DMG constituye un marcador de prediabetes, dada la frecuencia de desarrollo posterior de DM tipo2 y síndrome metabólico (dislipidemia, obesidad e hipertensión arterial [HTA] asociadas). Ocasionalmente la DMG está manifestando una disminución de reserva pancreática secundaria a destrucción autoinmune de la célula beta (DM tipo1 latente), dando lugar posteriormente a una DM tipo1.
Pronóstico de la descendenciaLos niños que durante el periodo intrauterino han estado expuestos a un ambiente metabólico hiperglucémico tienen más riesgo de desarrollar obesidad, alteraciones del metabolismo de los hidratos de carbono y síndrome metabólico en la vida adulta7.
Clasificación de la diabetes en relación con el embarazo8,9Diabetes mellitus pregestacionalEs toda diabetes diagnosticada antes del inicio del embarazo.
- •
Diabetes mellitus tipo 1 (destrucción de la célula β, generalmente con deficiencia absoluta de insulina).
- •
Diabetes mellitus tipo 2 (déficit en la secreción de insulina en presencia de resistencia a la insulina).
- •
Otros tipos específicos de diabetes (defectos genéticos de la función de la célula β, defectos genéticos de la acción de la insulina, enfermedades del páncreas exocrino, endocrinopatías, fármacos u otras sustancias químicas, infecciones, formas poco comunes de diabetes de naturaleza inmune, otros síndromes genéticos ocasionalmente asociados a diabetes).
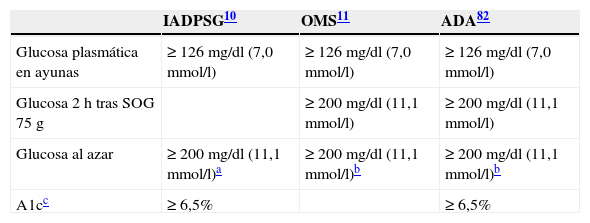
Se define como tal a toda diabetes diagnosticada por primera vez durante el embarazo, independientemente de la necesidad de tratamiento insulínico, del grado de trastorno metabólico o de su persistencia una vez finalizada la gestación. Recientemente la Asociación Internacional de Grupos de Estudio de Diabetes y Embarazo (IADPSG)10 ha definido la diabetes franca o diabetes manifiesta durante la gestación para aquellas mujeres con hiperglucemia marcada en la primera visita prenatal definida como: glucemia basal ≥126mg/dl (7,0mmol/l), A1c (HbA1c estandarizada para NGSP/DCCT en % e IFCC en mmol/mol) ≥6,5% (47,5mmol/mol) o glucemia plasmática al azar ≥200mg/dl (11,1mmol/l) tras confirmación con glucemia basal o A1c. La Organización Mundial de la Salud (OMS) ha incorporado también la categoría de diabetes mellitus durante la gestación. La definición se diferencia respecto a los criterios IADPSG en que no considera la HbA1c pero en cambio considera también diagnóstica una glucemia ≥200mg/dl a las 2h de una sobrecarga con 75g de glucosa11 (tabla 1).
Criterios diagnósticos de diabetes en la gestación
| IADPSG10 | OMS11 | ADA82 | |
|---|---|---|---|
| Glucosa plasmática en ayunas | ≥126mg/dl (7,0mmol/l) | ≥126mg/dl (7,0mmol/l) | ≥126mg/dl (7,0mmol/l) |
| Glucosa 2 h tras SOG 75g | ≥200mg/dl (11,1mmol/l) | ≥200mg/dl (11,1mmol/l) | |
| Glucosa al azar | ≥ 200mg/dl (11,1mmol/l)a | ≥200mg/dl (11,1mmol/l)b | ≥200mg/dl (11,1mmol/l)b |
| A1cc | ≥6,5% | ≥6,5% |
SOG: sobrecarga oral de glucosa.
- -
Determinar, en función de las complicaciones maternas secundarias a la diabetes, el riesgo que conlleva una gestación y prevenir y/o reducir las complicaciones maternofetales con un adecuado control y cuidado médico antes de la concepción.
- -
Proporcionar información a la futura gestante y a su pareja sobre la necesidad, en primer lugar, de valorar la situación de la DM materna para detectar posibles circunstancias que hicieran desaconsejable una gestación y, en segundo lugar, expresar la conveniencia de una participación activa de ambos para la consecución de los objetivos preconcepcionales, comunicando a la pareja la mutua repercusión entre DM y embarazo, haciendo referencia expresa a las posibles complicaciones que pueden surgir, así como a los métodos para prevenirlas.
- -
Niveles de A1c>10% (85,8mmol/mol).
- -
Nefropatía grave (creatinina plasmática >2mg/dl o proteinuria >3g/24h y/o HTA de difícil control).
- -
Cardiopatía isquémica.
- -
Retinopatía proliferativa grave, con mal pronóstico visual.
- -
Neuropatía autonómica grave.
Caracterización de la DM. Se intentará catalogar el tipo de diabetes que presenta la mujer mediante la realización de una historia clínica completa, estudio de la reserva pancreática y determinación de autoanticuerpos.
Valoración de las complicaciones de la DM y patologías asociadas (tiroidopatía, obesidad, HTA o dislipidemia). Para ello es precisa una exploración física completa que incluya somatometría (peso, talla y perímetro de cintura/cadera) y toma de la presión arterial. Además, se investigará la existencia de complicaciones de la DM mediante las exploraciones correspondientes:
- -
Retinopatía diabética: exploración del fondo de ojo mediante oftalmoscopia previa dilatación pupilar o retinografía con cámara no midriática.
- -
Nefropatía diabética: determinación de excreción urinaria de albúmina y, si precisa, cuantificación de proteinuria y aclaramiento de creatinina.
- -
Neuropatía: con especial interés en valorar la presencia de neuropatía autonómica en mujeres con DM de larga duración (>20años).
- -
Macroangiopatía: se aconseja realizar el cribado de cardiopatía isquémica y de vasculopatía periférica en mujeres con factores de riesgo cardiovascular (DM de larga duración, nefropatía establecida, dislipidemia, HTA, hábito tabáquico).
- -
Enfermedades asociadas: en mujeres con diabetes mellitus tipo1 es recomendable la valoración de la función tiroidea y el cribado de otras alteraciones autoinmunes si hay datos clínicos de sospecha (enfermedad celíaca u otras). En mujeres con diabetes mellitus tipo2, valorar la presencia de otros componentes del síndrome metabólico (HTA, dislipidemia, obesidad).
- -
Corregir desviaciones del peso para obtener una adecuada situación ponderal.
- -
Alcanzar previamente a la concepción una cifra de A1c lo más cercana posible a la normalidad, intentando evitar hipoglucemias, ya que no existe un umbral por debajo del cual no exista riesgo de malformaciones15. Si tenemos en cuenta que el límite alto de la normalidad para A1c se encuentra entre 5,7-5,9% (38,8-41mmol/mol), parece razonable recomendar niveles de A1c<6% (4,1mmol/mol)), intentando no sobrepasar un valor de 6,5% (47,5mmol/mol). Los objetivos de control glucémico durante el control pregestacional serán mantener una glucemia basal entre 70 y 95mg/dl (3,9-5,3mmol/l) y una glucemia posprandial (1h) entre 90 y 140mg/dl (5,0-7,8mmol/l), siempre intentando evitar la aparición de hipoglucemias.
- -
Adecuada educación terapéutica diabetológica, que deberá adaptarse a los conocimientos de base de la mujer.
- -
Intensificación de la frecuencia del autocontrol glucémico, siendo imprescindible el empleo de lectura instrumental (glucómetros), recomendándose la utilización de programas informáticos para la valoración de resultados.
- -
Instauración de tratamiento nutricional y ejercicio físico adaptado al tipo de DM y situación ponderal.
- -
En las mujeres con DM tratadas con insulina se instaurarán programas de tratamiento insulínico que permitan conseguir un adecuado control metabólico. Se recomienda la utilización preferente de dosis múltiples de insulina en pauta bolo-basal o sistemas de infusión continua subcutánea de insulina. Por lo que respecta al tipo de insulina a utilizar, se recomienda la insulina humana; sin embargo, varios estudios apoyan tanto la seguridad como la eficacia de los análogos de insulina rápida (lispro y aspártica) en el embarazo16-27, consiguiendo los objetivos de control posprandiales con menor riesgo de hipoglucemias.
- -
Así mismo, hay diferentes estudios con el uso de análogos de insulina lenta en el embarazo28-37, destacando entre ellos un metaanálisis de insulina glargina en el que no se encuentran un aumento de efectos adversos en los resultados perinatales en comparación con NPH34, y un ensayo clínico con insulina detemir que demuestra la seguridad y la eficacia de esta insulina en el embarazo y tiene aprobada la indicación en el embarazo por la Food and Drug Administration (FDA)35,37. Por este motivo, las mujeres que estén en tratamiento con análogos de insulina basales y tengan un buen control glucémico antes de la gestación podrían seguir con el tratamiento durante el periodo preconcepcional y durante la gestación.
- -
En las mujeres con DM tipo 2 tratadas con antidiabéticos orales, por el momento, se recomienda suspender estos fármacos antes de la concepción, instaurándose, si es preciso, tratamiento mediante programas de insulinoterapia. En el capítulo de diabetes gestacional se trata con más detalle el uso de los antidiabéticos orales. En el caso concreto de la metformina, se valorará el riesgo-beneficio de su uso, sobre todo si hay historia de abortos de repetición, infertilidad o en aquellas situaciones donde la mejoría del control glucémico ofrecido por la metformina supera los riesgos38.
- -
En todos los casos se debe ajustar el tratamiento dietético y farmacológico de acuerdo con los objetivos establecidos de control metabólico.
- -
Retinopatía diabética. Valorar la necesidad de realizar tratamiento fotocoagulador de la retinopatía diabética antes de la gestación. En mujeres con DM de larga evolución, retinopatía diabética y mal control glucémico, la normalización glucémica debería realizarse de forma paulatina para evitar un potencial empeoramiento de la retinopatía diabética39.
- -
Nefropatía e hipertensión arterial. En pacientes con HTA se utilizarán los fármacos antihipertensivos con menor riesgo para el feto (alfa-metildopa, labetalol, diltiazem, hidralazina, clonidina). En pacientes con nefropatía en tratamiento con IECA o ARAII, se deben suspender antes de la concepción o lo más precozmente, tras la confirmación de la misma20,40. Sería recomendable que las mujeres que deseen gestación mantengan niveles de presión arterial<130/8041.
- -
Dislipidemia asociada. Dado el posible riesgo teratogénico, se recomienda suspender el tratamiento con fármacos hipolipemiantes antes de la gestación20,42.
- -
Yodo. Además de una dieta adecuada con sal iodada, se recomienda iniciar la suplementación de yodo periconcepcional a dosis de 100-200μg/día, para disminuir el riesgo de alteraciones en el desarrollo neurológico fetal secundario a hipotiroxinemia43,44.
- -
Ácido fólico. Se recomienda iniciar la suplementación periconcepcional para prevenir los defectos del tubo neural (DTN), al menos un mes antes de la concepción, y continuar durante las primeras 10-12semanas de la gestación. Aunque la dosis óptima que reduce el riesgo de aparición de los DTN es desconocida, en las mujeres de alto riesgo, como son las mujeres con diabetes, parece prudente recomendar 4mg/día, sobre todo si el control glucémico es insuficiente, además de una dieta equilibrada45-47. No se recomienda el uso de preparados multivitamínicos, ya que para conseguir la dosis necesaria de folatos podemos incrementar en exceso el aporte de otras vitaminas (A o D) con potenciales riesgos para la madre y el feto. Finalmente, dada la controversia existente en la actualidad sobre la seguridad de un tratamiento prolongado con altas dosis de folatos (futuras neoplasias en la madre), parece prudente reducir la dosis de suplementación, si el periodo preconcepcional se prolonga en el tiempo48.
Se ajustará al protocolo de la Sociedad Española de Ginecología y Obstetricia (SEGO) sobre asistencia preconcepcional14, que se basa en el empleo de 3 instrumentos básicos:
Historia clínica y exploración ginecológicaSe valorarán especialmente los siguientes aspectos:
- -
Existencia de otras patologías.
- -
Riesgo de cromosomopatías.
- -
Historia familiar propia o en la pareja de enfermedades hereditarias: posibilidades de transmisión y diagnóstico prenatal.
- -
Uso de fármacos u otros tóxicos como factores de riesgo confirmados, a fin de proteger al embrión-feto frente a su exposición.
- -
Hábitos, estilo de vida y actividad laboral de la mujer.
- -
Antecedentes reproductivos y método anticonceptivo empleado, asegurándose que se utilizará de forma efectiva hasta el momento en que se consiga el deseado control metabólico y demás circunstancias favorables.
- -
Revisión ginecológica con periodicidad igual que en la población general.
- -
Estudio básico de esterilidad si hay sospecha clínica o se prevé un seguimiento largo en la clínica preconcepcional.
- -
Recomendadas a todas las gestantes (además de la analítica incluida en el control endocrinológico): grupo sanguíneo, factor Rh y test de Coombs indirecto, investigación de anticuerpos frente a antígenos irregulares y serología para detección de rubéola, lúes y VIH.
- -
Insistir en la necesidad de evitar el consumo de alcohol, tabaco y drogas y exposición a teratógenos farmacológicos o ambientales desde el período preconcepcional.
- -
Utilización de un método anticonceptivo adecuado, hasta que se considere la instauración del embarazo.
- -
Enfatizar la importancia de la consulta prenatal precoz.
Aunque no es lo deseable, puede ocurrir que la paciente no haya sido evaluada preconcepcionalmente. Si ello es así, se abordará la correspondiente cualificación de la DMPG, así como la valoración de la existencia de complicaciones específicas de la misma, de acuerdo con lo expresado en la etapa preconcepcional.
Control diabetológicoControl metabólicoTiene como objetivo el mantenimiento de normoglucemia durante el embarazo, intentando la obtención de valores de glucemia capilar semejantes a los de la gestante sin diabetes, evitando la hipoglucemia:
- -
Glucemia basal: entre 70 y 95mg/dl (3,9-5,3mmol/l).
- -
Glucemia posprandial (1h): entre 90 y 140mg/dl (5,0-7,8mmol/l).
- -
A1c: media+2DE (A1c 4,8-5,7% o 29-38,8mmol/mol).
- -
Ausencia de cetonuria e hipoglucemia.
- -
Adecuar la dieta al peso de la paciente, a las necesidades de la gestación, a las preferencias de la mujer y al esquema terapéutico insulínico. El reparto de los diversos principios inmediatos, en cuanto al aporte calórico global, deberá guardar los siguientes porcentajes: hidratos de carbono (40-50%), proteínas (20%) y grasas (30-40%), con predominio de monoinsaturadas. Es previsible que el número de ingestas aumente por deseo de la paciente o para prevención de cetogénesis/hipoglucemias.
- -
Recomendar la práctica de ejercicio físico moderado diario (más importante en la DM tipo2).
- -
En cuanto al tratamiento farmacológico adicional a la dieta y el ejercicio (hipoglucemiantes orales e insulina), se seguirán los mismos criterios expresados en el control metabólico de la diabetes en la etapa preconcepcional. El inicio de tratamiento con infusor continuo de insulina durante el embarazo solo debe valorarse en caso de no conseguir los objetivos de control glucémico, debido al potencial riesgo de empeoramiento transitorio del control glucémico, cetoacidosis e hipoglucemia. Habrá que tener presente el aumento de sensibilidad a la insulina al final del primer trimestre y el aumento de la resistencia a la insulina en la segunda mitad de la misma, con los consiguientes cambios en los requerimientos.
- -
Autocontrol domiciliario: se valorará la glucemia capilar mediante glucómetro. Se aconseja la realización de 3 glucemias preprandiales diarias y 3 glucemias posprandiales diarias, con una determinación nocturna según necesidades. Se recomienda también realizar análisis de cetonuria o cetonemia en situaciones de enfermedad o si glucemia >200mg/dl para descartar cetosis/cetoacidosis; y basal de forma ocasional.
- -
Proporcionar glucagón para utilizar en caso de hipoglucemia severa.
- -
Determinación de A1c cada 4-8semanas.
- -
El seguimiento de la paciente deberá realizarse conjuntamente por el obstetra y el diabetólogo. La frecuencia de las visitas se adaptará a la situación clínica de la gestante, siendo aconsejable que tengan lugar cada 2-4semanas.
- -
Examen del fondo de ojo: antes o al inicio y en la segunda mitad de la gestación, alrededor de las 28 semanas. En las mujeres con retinopatía, las exploraciones se programarán a juicio del oftalmólogo.
- -
Fotocoagulación retiniana con láser si se considera preciso.
- -
Evitar en lo posible la práctica de fluoresceingrafía retiniana.
- -
Determinación de excreción urinaria de albúmina en el primer, segundo y tercer trimestre de la gestación.
- -
Suspender tratamiento con IECA, antagonistas del receptor de la angiotensinaII (ARAII), estatinas y otros fármacos potencialmente nocivos, si no se hubieren retirado en el periodo preconcepcional. Los niveles de presión arterial deben intentar mantenerse por debajo de 130/80mmHg41.
- -
Confirmar la gestación y fijar la edad gestacional.
- -
Valorar la viabilidad embriofetal.
- -
Descartar patología obstétrica y/o ginecológica asociada.
- -
Aunque actualmente no hay evidencia suficiente para recomendarlo en la DM tipo1 que no presenta otros factores de riesgo vascular50-52, dada su efectividad en gestantes de alto riesgo de preeclampsia se podría valorar el uso de ácido acetilsalicílico a dosis bajas.
- -
Revisión de la historia clínica y exploración obstétrico-ginecológica (características uterinas, cervicales, anexiales y mamarias). Toma para citología si no se ha realizado en la consulta preconcepcional.
- -
Estudio ecográfico con el fin de establecer la cronología de la gestación, constatar la vitalidad y la normalidad del embrión (o en su caso del feto) y su ubicación en la cavidad uterina, así como las características de los anejos.
- -
Vigilar el bienestar materno y descartar complicaciones asociadas.
- -
Valorar el crecimiento y el bienestar fetal, así como la presencia de posibles complicaciones.
- •
Control obstétrico habitual. Valoración de la frecuencia cardiaca fetal, circunferencia abdominal, altura uterina y movimientos fetales. Control de peso y presión arterial.
- •
Estudio de anomalías congénitas. Están sometidas a mayor riesgo de malformaciones, y por tanto deben ser objeto de especial atención, las pacientes en las que se asocie alguna de las siguientes circunstancias:
- -
Obesidad.
- -
A1c superior a la media+7DE en el primer trimestre (8% o 63,9mmol/mol).
- -
Biometría embriofetal por debajo de la media.
- -
Hidramnios.
- -
Cetoacidosis.
- -
Nefropatía diabética grave.
- •
Seguimiento ecográfico.
- -
Ecografía entre las semanas 11 y 14, igual que en todas las embarazadas, para evaluar la viabilidad, el número de fetos, datar la gestación, calcular el riesgo de cromosomopatías mediante la medición de la sono-translucencia nucal en combinación con determinaciones bioquímicas y una evaluación morfológica precoz en los casos en que sea posible si existen los medios disponibles.
- -
Sería recomendable realizar una exploración ecocardiográfica precoz entre las 14-16semanas, en especial en las gestantes con diabetes que presenten un incremento del riesgo de malformaciones.
- -
Ecografía a las 20-22semanas de gestación para el cribado de malformaciones, igual que en todas las gestaciones, siguiendo los criterios de la SEGO.
- -
Valorar la realización de ecocardiografía fetal para estudio de una eventual miocardiopatía, habitualmente entre las 28 y 32semanas.
- •
Dado que las gestantes con diabetes no tienen un mayor riesgo de cromosomopatías, se seguirán a este respecto las mismas pautas que en la población general53.
- •
Valoración del crecimiento fetal y características de los anejos ovulares. Determinación seriada de biometrías fetales, volumen del líquido amniótico y de las características placentarias, mediante ecografías mensuales a partir de las 28-30semanas.
- •
Valoración del bienestar fetal: mediante estudio cardiotocográfico, en cada visita a partir de las 36-38 semanas, en las pacientes con buen control y en ausencia de vasculopatía. En cualquier caso, la semana de inicio y la cadencia dependerán del control metabólico materno y del estado del feto. El método habitual será el cardiotocográfico. Se usarán otros métodos, tales como estudio de perfil biofísico o doppler, cuando se considere oportuno. El doppler tiene mayor utilidad en los casos de preeclampsia y de sospecha de crecimiento intrauterino retardado.
- -
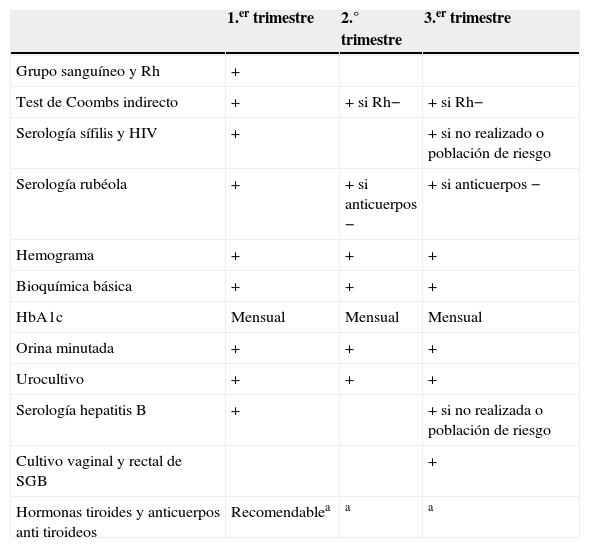
En la tabla 2 se recogen las determinaciones analíticas recomendadas.
Determinaciones analíticas
| 1.er trimestre | 2.° trimestre | 3.er trimestre | |
|---|---|---|---|
| Grupo sanguíneo y Rh | + | ||
| Test de Coombs indirecto | + | + si Rh− | + si Rh− |
| Serología sífilis y HIV | + | + si no realizado o población de riesgo | |
| Serología rubéola | + | + si anticuerpos − | + si anticuerpos − |
| Hemograma | + | + | + |
| Bioquímica básica | + | + | + |
| HbA1c | Mensual | Mensual | Mensual |
| Orina minutada | + | + | + |
| Urocultivo | + | + | + |
| Serología hepatitis B | + | + si no realizada o población de riesgo | |
| Cultivo vaginal y rectal de SGB | + | ||
| Hormonas tiroides y anticuerpos anti tiroideos | Recomendablea | a | a |
a Si disfunción y/o autoinmunidad tiroidea, a lo largo de la gestación se realizarán los controles de función tiroidea precisos para cada entidad83.
Complicaciones graves con repercusión materno-fetal:
- -
Mal control metabólico, absoluto (cetosis clínica, hipoglucemia grave) o relativo (control metabólico irregular).
- -
Nefropatía y/o estados hipertensivos, no controlados.
- -
Pielonefritis.
- -
Amenaza de parto pretérmino o rotura prematura de membranas.
- -
Sospecha de riesgo de pérdida del bienestar fetal.
- -
Otras indicaciones obstétricas.
Siempre que exista un correcto control metabólico, ausencia de complicaciones y garantías de control ambulatorio del bienestar fetal, no será necesario el ingreso de la paciente hasta el momento del parto.
Finalización de la gestaciónCon un control metabólico correcto y vigilancia adecuada del bienestar fetal, se debe dejar evolucionar la gestación hasta el inicio espontáneo del parto. A partir de la semana38 se puede plantear la inducción del parto en mujeres con buenas condiciones obstétricas. Si en la semana40 el parto no se ha iniciado, se valorará la finalización del embarazo.
En las restantes situaciones, cuando no exista garantía de un adecuado seguimiento y control obstétrico-diabetológico, se procurará terminar el embarazo a partir de la semana37, o antes si se considerase preciso. Si fuera necesario finalizar la gestación antes de la semana34+6, deben administrarse corticoides para acelerar la maduración pulmonar fetal, teniendo en cuenta la correspondiente adecuación del tratamiento insulínico. En el anexo 1 a esta guía se incluye una pauta orientativa de ajuste del tratamiento insulínico durante el tratamiento con corticoides.
En caso de riesgo de pérdida del bienestar fetal, la finalización de la gestación será inmediata.
En el tratamiento de la amenaza de parto pretérmino, el fármaco de elección es el atosibán, pudiendo utilizarse como alternativa los antagonistas del calcio (nifedipino), aunque hay que tener en cuenta que la amenaza de parto pretérmino no figura entre las indicaciones para las que está aceptado el uso del fármaco. Los β-miméticos no son recomendables por su efecto hiperglucemiante.
Vía del partoLa vía de elección del parto será la vaginal. Las indicaciones de cesárea son las mismas que para las gestantes sin diabetes, a excepción de que el peso fetal estimado supere los 4.500g o exista el antecedente de una distocia de hombros en una gestación anterior.
La retinopatía diabética no es una contraindicación para el parto vaginal. En el caso de mujeres con retinopatía diabética proliferativa grave se recomienda evitar maniobras de Valsalva que puedan propiciar el desarrollo de hemorragias retinianas, aconsejándose la utilización durante el parto de anestesia locorregional.
Para la inducción del parto se recomienda:
- -
Con cérvix favorable (índice Bishop >6): amniotomía, monitorización cardiotocográfica y perfusión de oxitocina.
- -
Con cérvix desfavorable: maduración cervical previa con prostaglandinas.
- -
Control del bienestar materno y fetal.
- -
Monitorización de la dinámica uterina y de la frecuencia cardíaca fetal.
- -
Ante la sospecha de riesgo de pérdida del bienestar fetal, se valorará la utilización de otro método de control fetal: tecnología STAN o estudio del equilibrio ácido-base.
- -
Mantener la glucemia capilar entre 70-110mg/dl (3,9-6,1mmol/l) sin cetonuria.
- •
Protocolo de perfusiones intravenosas:
- -
Perfusión continua de glucosa (p.ej., 500cc suero glucosado al 5 o 10%, cada 6h).
- -
Administración sistemática de insulina de acción rápida por vía intravenosa, preferentemente con bomba de infusión, y ajustar ritmo de infusión según glucemias y protocolo interno del centro.
- -
Control horario de glucemia capilar para ajustar el ritmo de las perfusiones.
- -
El hijo de madre con diabetes (HMD) es un neonato de riesgo elevado por las frecuentes complicaciones que presenta. Todas ellas son más habituales en los hijos de madre con DMPG y más intensas en caso de un mal control metabólico durante la gestación.
Problemas específicos del hijo de madre con diabetes- •
Metabólicos:
- -
Hipoglucemia (glucemia <40mg/dl; <2,21mmol/l). Es la complicación más frecuente en las 2 primeras horas de vida por caída brusca del aporte de glucosa.
- -
Hipocalcemia (calcemia <7mg/dl; <1,75mmol/l). Aparece entre las 24 y 72h de vida. Se atribuye en parte a un hipoparatiroidismo funcional transitorio; por ello, coexiste en ocasiones con una hipomagnesemia (magnesio sérico <1,5mg/dl; <0,67mmol/l).
- -
Macrosomía/peso elevado para la edad gestacional.
- -
A consecuencia de la macrosomía son más frecuentes los traumatismos durante el parto, sobre todo parálisis braquial, fracturas de clavícula y asfixia perinatal.
- -
Los HMD tienen visceromegalias, y es frecuente el aumento de grosor del miocardio a nivel del septum interventricular (>5mm) (miocardiopatía hipertrófica), que desaparece entre los 2 y 6meses. Es poco habitual que presenten sintomatología de hipertrofia septal por obstrucción del tracto de salida, que cursa con insuficiencia cardíaca y soplo y suele ser autolimitada.
- -
Restricción de crecimiento intrauterino. En mujeres con diabetes que presentan vasculopatía y flujo placentario disminuido.
- -
Inmadurez funcional. El efecto del retraso de la maduración morfológica y funcional de algunos órganos (pulmones, paratiroides e hígado) ha sido atribuido al hiperinsulinismo fetal. Por ello, la incidencia de dificultad respiratoria por inmadurez (enfermedad de la membrana hialina), así como la ictericia, están aumentadas en este grupo de pacientes.
- -
Malformaciones congénitas. Son más frecuentes que en la población general. Aunque la más característica es el síndrome de regresión caudal, las más frecuentes son cardiopatías (comunicación interventricular, transposición de los grandes vasos, coartación de aorta…), anomalías intestinales (colon izquierdo hipoplásico), renales (agenesia), del sistema nervioso central, etc.15.
- -
- •
Hematológicos:
- -
Poliglobulia. El aumento del hematocrito puede producir hiperviscosidad y dar complicaciones trombóticas. La más frecuente es la trombosis venosa renal.
- -
Ictericia secundaria a la policitemia asociada y la inmadurez hepática.
- -
- •
Se dispondrá en la sala de partos de los medios humanos y técnicos necesarios para la asistencia y reanimación de un recién nacido producto de un parto de alto riesgo.
- •
Posteriormente, se realizará una exploración física cuidadosa para descartar malformaciones.
- •
Se harán determinaciones de:
- -
Glucemia cada 30min en las 2 primeras horas de vida y luego a las 3, 6, 12, 24, 36 y 48h.
- -
Calcemia a las 24h si el recién nacido presenta estigmas de HMD o sintomatología específica. Si aparece hipocalcemia, se determinará la magnesemia.
- -
Hematocrito/bilirrubina si aparece sintomatología.
- -
Se practicarán exploraciones complementarias (radiografía de tórax, ecografías cerebral, renal, cardíaca y/o de columna lumbosacra) según la clínica del paciente.
- -
Se valorará en cada caso la conveniencia de un alta precoz.
- -
- •
Alimentación precoz (antes de las 2h de vida) con lactancia materna o artificial.
- •
Hipoglucemia:
- -
Si aparece hipoglucemia en un HMD asintomático, se administrará leche o glucosa 10% por vía oral (5-10ml/kg) y se realizará nuevo control de glucemia a los 20-30min. Si la glucemia es >40mg/dl se continuará con alimentación cada 2 o 3h. Si la glucemia es <40mg/dl, se ingresará para administración de glucosa intravenosa.
- -
Hipoglucemia sintomática: se ingresará al recién nacido y se administrará glucosa por vía intravenosa.
- -
- •
Hipocalcemia: si los niveles son <7mg/dl, debe tratarse con gluconato cálcico intravenoso, y si resulta difícil de corregir, debe sospecharse hipomagnesemia y corregirla al mismo tiempo.
Se recomienda la lactancia materna.
Se adaptará la dieta materna a las necesidades nutricionales de la lactancia.
En caso de necesidad de inhibir la lactancia, se utilizarán drogas dopaminérgicas.
Los requerimientos de insulina descienden en el posparto inmediato, por lo que es preciso reducir la dosis diaria aproximadamente a un 50% de la que venía siendo empleada en el tercer trimestre, manteniendo también en este periodo una estrecha automonitorización del control glucémico.
Los controles puerperales se llevarán a cabo de la manera habitual como en las puérperas sin diabetes.
Es recomendable la determinación de tiroxina libre, TSH y anticuerpos antitiroideos a los 3 o 4 meses posparto para la detección y tratamiento, si procede, de la disfunción tiroidea posparto (más frecuente en la diabetes mellitus tipo1)55.
Consideraciones especiales en diabetes pregestacional y edad fértilCriterios para la interrupción legal del embarazo- -
Malformación fetal grave.
- -
Cardiopatía isquémica, nefropatía y/o neuropatía autonómica graves.
- -
Concomitancia de retinopatía proliferativa activa y grave, con mal pronóstico visual.
- -
Otras circunstancias no dependientes de la DMPG.
- -
Las indicaciones y la eficacia de los diferentes métodos anticonceptivos disponibles para las gestantes con DMPG son similares a las de la población general. No existen contraindicaciones para el uso de anticonceptivos hormonales ni dispositivos intrauterinos, si bien el uso de los primeros debe ser tomado con precaución ante la presencia de vasculopatía.
- -
Cuando estas mujeres ya han completado su deseo genésico, se les asesorará (como a todas las mujeres con enfermedades de riesgo para el embarazo) sobre la utilización de un método anticonceptivo definitivo.
Si en la primera consulta prenatal la gestante presenta criterios diagnósticos de DM no es necesario realizar ninguna prueba y se considerará diabetes franca o manifiesta10 (tabla 1).
CribadoSe realiza mediante la prueba de O'Sullivan (anexo 2).
Primer trimestre en gestantes de alto riesgo9- -
Edad >35años.
- -
Obesidad (índice de masa corporal >30kg/m2).
- -
Antecedentes personales de DMG u otras alteraciones del metabolismo de la glucosa.
- -
Resultados obstétricos previos que hagan sospechar una DMG no diagnosticada (p.ej., macrosomía).
- -
Historia de diabetes mellitus en familiares de primer grado.
- -
Grupos étnicos de riesgo (afroamericanas, asiático-americanas, hispanas, indio-americanas).
En todas las gestantes no diagnosticadas previamente.
Tercer trimestreEn gestantes que no han sido estudiadas en el 2.° trimestre y en aquellas que aunque el estudio resultara negativo, posteriormente desarrollan complicaciones que característicamente se asocian a la DMG (macrosomía fetal o polihidramnios). En estos casos se obviará la prueba de cribado y se acudirá directamente a la realización de una sobrecarga oral de glucosa (SOG).
Cuando la prueba de O'Sullivan resulte positiva, se procederá a la confirmación diagnóstica mediante la práctica de SOG.
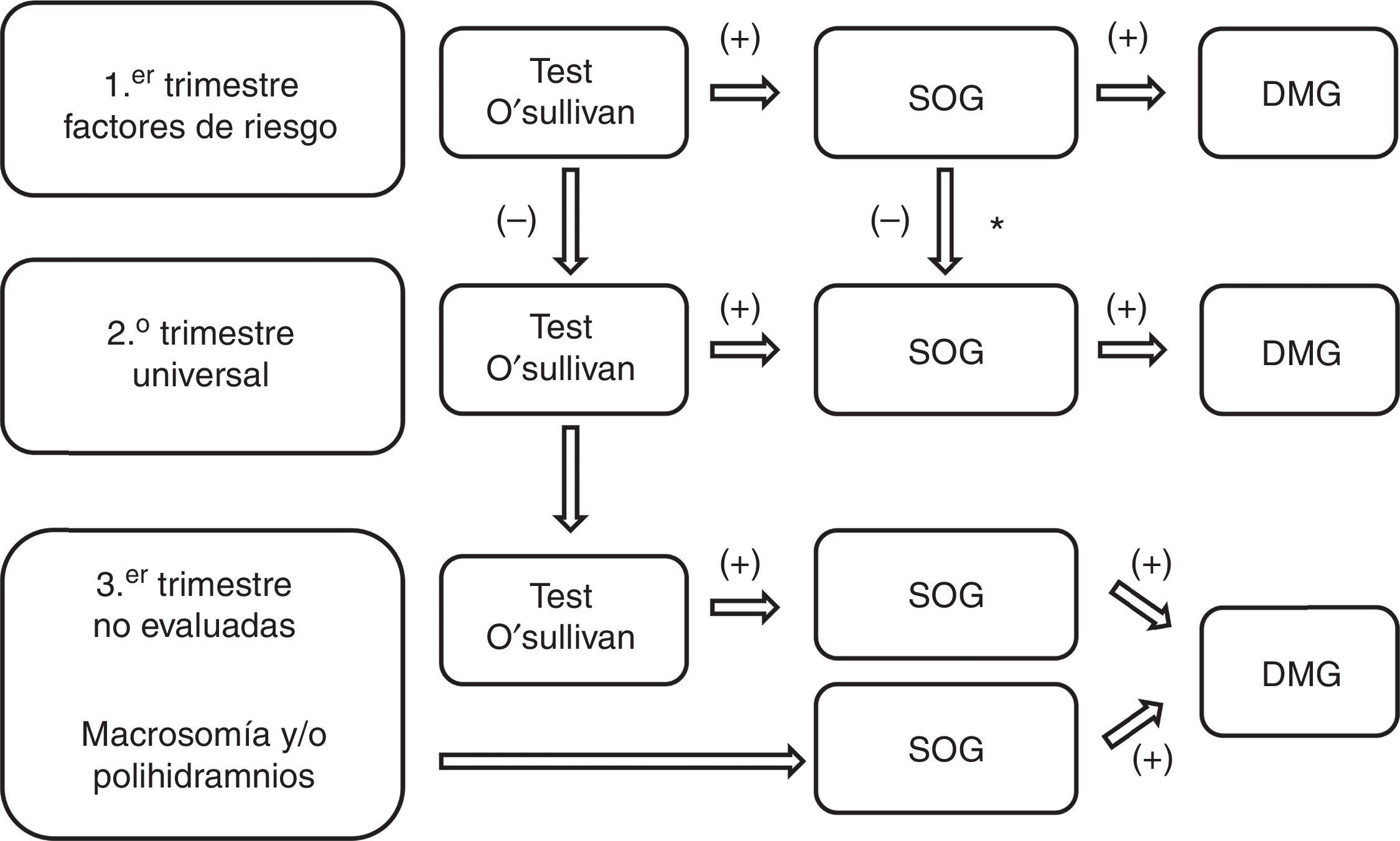
Prueba diagnósticaSe realiza mediante SOG (anexo 3). En la figura 1 se muestra un esquema de la estrategia diagnóstica a seguir durante la gestación.
Estrategia diagnóstica de diabetes gestacional en el embarazo.
SOG: sobrecarga oral de glucosa de 100g; * Opcionalmente se puede realizar test de O'Sullivan3.
Antes de realizar una SOG, debe prestarse atención a las siguientes consideraciones:
- •
Dos glucemias basales ≥126mg/dl (7,0mmol/l) en días diferentes, o una glucemia al azar >200mg/dl (11,1mmol/l), ratifica el diagnóstico de DMG y excluye la necesidad de realizar una SOG.
Se recomiendan los criterios diagnósticos del National Diabetes Data Group (NDDG)56 y del 3rd Workshop-Conference on Gestational Diabetes Mellitus57. El estudio multicéntrico español realizado en nuestra población5,58 no demostró diferencias en los resultados de mujeres tratadas con DMG según criterios del NDDG vs mujeres no tratadas con los criterios de Carpenter y Coustan59 propuestos por la 4th Workshop-Conference on Gestational Diabetes Mellitus60 y la ADA61, por lo que en la última Guía se desestimó el cambio3.
En 2010, basándose en los resultados del estudio Hyperglycemia Adverse Pregnancy Outcomes (HAPO)62, la IADPSG propuso el diagnóstico de DMG en un solo paso (SOG de 75g) con puntos de corte claramente más bajos (93-180-153mg/dl o 5,1-10-8,5mmol/l)10. En el momento actual, el GEDE no considera adecuado cambiar a los criterios diagnósticos derivados del estudio HAPO, tanto por su aplicabilidad a nuestra población como porque no han sido testados en un ensayo clínico4. Según los criterios del Estudio Multicéntrico Español5, siendo la categoría de referencia las mujeres con tolerancia normal a la glucosa, la OR asociada a la categoría de Carpenter y Coustan (95-180-155-140mg/dl o 5,3-10-8,6-7,8) era 1,44, lo que supone un riesgo inferior al 1,75 de los criterios IADPSG. Por los datos previos en nuestro medio, se presupone que los criterios IADPSG diagnosticarían un grupo de gestantes con una morbilidad inferior a la que pretenden identificar. Esto supondría una prevalencia de hiperglucemia gestacional probablemente superior al 17%, con la correspondiente necesidad de aumentar los recursos sanitarios destinados a este fin63.
Además, en la actualidad no existe consenso sobre la utilización de los nuevos criterios64. En publicaciones recientes, algunos autores proponen reflexión sobre los nuevos criterios antes de aceptarlos65-68. A fecha de hoy son de destacar el pronunciamiento de la OMS aceptando los criterios, aunque concede que la evidencia es débil11, y la National Institute of Health Consensus Conference, que no los acepta con la evidencia actual69.
Control durante el embarazo y partoUna vez efectuado el diagnóstico de DMG la paciente debe iniciar tratamiento lo antes posible, por lo que debe ser remitida a la unidad de diabetes y embarazo correspondiente.
Control metabólico- -
Tratamiento dietético. Las recomendaciones dietéticas son similares a las establecidas para la DMPG. La dieta será normocalórica, excepto en las embarazadas con obesidad importante, en las que se puede indicar una cierta restricción calórica, evitando la aparición de cetonuria.
- -
Ejercicio físico. Es recomendable la práctica, con asiduidad, de ejercicio físico moderado (p.ej., paseo de una hora diaria).
- -
Automonitorización. Se recomienda la práctica de controles de glucemia capilar tanto preprandiales como especialmente posprandiales63, así como cetonurias, para el ajuste de la cantidad y el reparto adecuado de los hidratos de carbono.
- -
Objetivos del control metabólico.
- -
Glucemia basal: <95mg/dl (5,3mmol/l), sin hipoglucemias.
- -
Glucemia posprandial (1h): <140mg/dl (7,8mmol/l).
- -
Glucemia posprandial (2h): <120mg/l (6,7mmol/l).
- -
Tratamiento adicional.Aunque ha existido controversia sobre la necesidad de diagnosticar y tratar a las mujeres con DMG70, hay evidencia originada en estudios controlados y aleatorizados que dejan pocas dudas al respecto71-74. Cuando a pesar del establecimiento de la dieta y el ejercicio no se consigan los objetivos del control metabólico, será necesario el tratamiento adicional. También podría valorarse en el caso de macrosomía fetal sugestiva de hiperinsulinismo intraútero. En este caso se considera suficiente la sospecha de un crecimiento fetal excesivo (circunferencia abdominal >p70-p75 para su edad gestacional).
Aunque hay estudios que describen resultados perinatales satisfactorios en gestantes con DMG tratadas con glibenclamida75,76 o metformina76-78, la insulina es el fármaco que ha demostrado de forma más consistente la reducción de la morbilidad maternofetal cuando se añade al tratamiento nutricional. Ninguno de los laboratorios titulares de glibenclamida o metformina ha modificado las fichas técnicas autorizadas por la Agencia Española del Medicamento y Productos Sanitarios (AEMPS), por lo que esta agencia recomienda la insulina para el control de la diabetes durante la gestación, limitándose el uso de antidiabéticos orales a ensayos clínicos autorizados. Respecto al tipo de insulina a utilizar, valen las consideraciones hechas para la DMPG.
Control obstétricoEl seguimiento y control obstétrico será similar al efectuado en la gestante normal, con las siguientes matizaciones:
- -
A los estudios ecográficos habituales de la gestación normal, se recomienda añadir uno entre la 28.ª-32.ª semanas para detectar la presencia de macrosomía.
- -
La finalización y la asistencia al parto de estas pacientes no debe diferir de las gestantes normales. Pero dado que bajo la etiqueta de DMG se agrupan pacientes que van desde mujeres con diabetes gestacional leve hasta DM tipo2 no diagnosticada, la finalización de la gestación en estas pacientes dependerá de la gravedad del cuadro. En las pacientes con una DMG leve los criterios de finalización no diferirán de los empleados en la población obstétrica general, mientras que en las que se sospeche una DMPG no diagnosticada o que requieran insulina o presenten macrosomía fetal se aplicarán los criterios de la DMPG. Sin embargo, deben mantenerse los mismos objetivos de control intraparto que en la DMPG, por lo que se precisará la oportuna monitorización glucémica, junto con el establecimiento ocasional de tratamiento insulínico, preferiblemente mediante la utilización de perfusión intravenosa.
- -
Los cuidados del recién nacido difieren de los establecidos en la gestante normal en la necesidad de prevenir, detectar y tratar la hipoglucemia neonatal.
- -
Tras el parto se suspenderá el tratamiento y se realizarán controles glucémicos para confirmar la situación metabólica en el posparto inmediato.
Se realizarán los controles puerperales habituales.
Se recomendarán hábitos de vida saludables (dieta, ejercicio, abstención de tabaco).
Se procederá a la reclasificación metabólica de la diabetes gestacional. Para ello, a partir de las 6-8semanas tras el parto y/o una vez finalizada la lactancia, se llevará a cabo una sobrecarga oral de glucosa (75g). Los resultados se valorarán de acuerdo con los criterios del Comité de Expertos de la ADA8 (anexo 4).
Se recomienda revisión metabólica anual en los casos de categorías de aumento de riesgo de diabetes (glucemia basal alterada [GBA] o de intolerancia a la glucosa [ITG] o A1c ≥5,7 y <6,5%) (anexo 4) y cada 3años en caso de situación glucídica normal. Las revisiones de las mujeres con antecedentes de DMG deben valorar además una somatometría completa (índice de masa corporal y cintura), presión arterial y perfil lipídico, dada la frecuente asociación de la DMG con otros componentes del síndrome metabólico.
Unidades de diabetes y embarazoEl adecuado control y seguimiento de las mujeres con DMPG y DMG precisa unidades especializadas en las que se contemplarán 2 niveles de complejidad asistencial, lo que permitirá conseguir una adecuada y racional asistencia. Estas unidades estarán formadas por equipos multidisciplinarios cuyo núcleo central lo constituyen diabetólogos, obstetras y educadores en diabetes.
Las funciones a desarrollar en los 2 niveles asistenciales son las siguientes:
Nivel A. Asistencia primaria y especializada extrahospitalaria- -
Diagnóstico de la DMG.
- -
Control y seguimiento durante el embarazo de la DMG, en conexión con el nivel B.
- -
Seguimiento posparto de las mujeres con DMG.
- -
Información a las pacientes con diabetes en edad fértil sobre la necesidad de programación de su embarazo, remitiéndolas para este fin al nivel B (clínica preconcepcional).
- -
Envío al nivel B, para correcto control y seguimiento, de todas las gestantes con DMPG o DMG de difícil control.
- •
Tratamiento de la DMPG:
- -
Preconcepcional.
- -
Embarazo, parto y posparto.
- -
- •
Tratamiento de la DMG:
- -
Asistencia en el embarazo, parto y posparto de las mujeres con DMG diagnosticadas en este nivel o remitidas desde el nivel A, ante la imposibilidad de un adecuado control.
- -
Formación y reciclaje de profesionales sanitarios relacionados con Unidades de Diabetes y Embarazo.
- -
Establecimiento de un control de calidad de la asistencia a las mujeres con diabetes gestantes en ambos niveles promoviendo la creación, el desarrollo y la actualización de los oportunos protocolos clínicos y registros.
- -
Participación en proyectos de investigación sobre temas relacionados con la diabetes y gestación que puedan contribuir a un mejor conocimiento de este problema, así como a mejorar el cuidado de estas pacientes.
- -
RC declara que ha recibido honorarios de Medtronic y Roche en concepto de consultoría. Los otros autores declaran no tener ningún conflicto de intereses en relación con la redacción de esta guía.
A Sanofi por su colaboración en el patrocinio del GEDE y a Ricardo Closa Monasterolo por la revisión de los apartados relativos a la evaluación neonatal
- •
Tratamiento esteroideo más habitual: betametasona 12mg i.m. cada 24h (2 dosis).
- •
Hora de administración preferente: 13-16h.
- 1.
DMG en tratamiento con dieta. Si glucemia >95mg/dl preprandial o >140mg/dl 1h posprandial: iniciar insulina 0,3UI/kg de peso pregestacional en pauta bolo-basal y ajustar según evolución.
- 2.
DMG insulinizada y DMPG. Aumentar las dosis de insulina previa, según el siguiente esquema:
- 1.
Si glucemia >250mg/dl en 2 ocasiones y/o cetonuria 3-4+ o cetonemia >1,5mmol/l, inciar perfusión de insulina i.v.
- -
Determinación de glucemia en plasma venoso, una hora después de la ingesta de 50g de glucosa, en cualquier momento del día e independientemente de la ingesta previa de alimentos.
- -
Se acepta como resultado positivo una cifra de glucemia ≥140mg/dl (7,8mmol/l).
- -
Los 3 días anteriores a su realización se recomendará a la embarazada la ingesta de una dieta que no sea restrictiva en hidratos de carbono, o por lo menos con un aporte diario de hidratos de carbono superior a 150g.
- -
El día de la prueba y tras ayuno previo de 8 a 14h, se extraerá sangre y acto seguido se administrarán por vía oral 100g de glucosa en un vehículo acuoso de 300ml en el transcurso de 5min. Posteriormente la mujer deberá permanecer sentada y sin fumar y se tomarán muestras de sangre venosa tras 1, 2 y 3h.
- -
Se determinará la glucemia en plasma venoso, adicionando fluoruro sódico u otro agente similar cuando el análisis no se haga con inmediatez.
- -
Se considerará diagnóstico de DMG el hallazgo de 2 o más puntos iguales o superiores a los siguientes valores11
Estos criterios corresponden a los recomendados por el 3th Workshop-Conference on Gestational Diabetes Mellitus57, no habiéndose adaptado a los del 4th Workshop60, ni a los de la IADPSG10, a raíz de los estudios realizados por el grupo5,58.
:- -
Basal: 105mg/dl (5,8mmol/l).
- -
Una hora: 190mg/dl (10,6mmol/l).
- -
Dos horas: 165mg/dl (9,2mmol/l).
- -
Tres horas: 145mg/dl (8,1mmol/l).
- -
Categorías de aumento de riesgo de diabetes (prediabetes):
- -
Glucemia basal alterada (GBA): glucemia basal >100mg/dl (5,6mmol/l), o
- -
Tolerancia alterada a la glucosa (ITG): glucemia a las 2h de administrar 75g de glucosa >140mg/dl (7,8mmol/l) y <200mg/dl (11,1mmol/l), o
- -
A1c22
Valores estandarizados NGSP/DCCT-IFCC.
5,7-6,4% (38,8-46,4mmol/mol).
Criterios de diabetes mellitus (DM):
- -
A1c≥6,5% (47,5mmol/mol), o
- -
Glucemia basal ≥126mg/dl (7mmol/l)33
En ausencia de hiperglucemia inequívoca, los valores deben ser confirmados en una segunda ocasión.
, o - -
Glucemia a las 2h de administrar 75g de glucosa ≥200mg/dl (11,1mmol/l)3, o
- -
Sintomatología clínica de diabetes y glucemia al azar ≥200mg/dl (11,1mmol/l).
Los miembros del Grupo Español de Diabetes y Embarazo (GEDE) se presentan en el Anexo 5