The study of the Spin crossover (SCO) materials began in the early 1930's. After eight decades, different research groups developed strategies for the synthesis of SCO materials. Recently Gütlich has proposed a few rules as requirement for designing SCO materials. In this paper we present a brief description of the main strategies, their relation to Gütlich's rules and their respective validation according to Crystal-field theory and Molecular Orbital theory, including the definition of the Cooperativity Model. It is briefly exposed the state of the art and future perspectives of SCO materials and their applications.
El estudio de los materiales con entrecruzamiento de espín (SCO) inició al principio de la década de 1930. Luego de ocho décadas de estudios, varios grupos de investigación han desarrollado diferentes estrategias de síntesis de estos materiales. Recientemente Gütlich propuso algunas reglas para el diseno de estos materiales. En este artículo se presenta una breve descripción de las estrategias más importantes, su relación con las reglas de Gütlich y su respectiva correspondencia con las teorías de Campo Cristalino y de Orbitales Moleculares, incluyendo el modelo de Cooperatividad. Se exponen brevemente las perspectivas de investigación y de diseño de los materiales con entrecruzamiento de espín y sus aplicaciones.
El estudio de los materiales con propiedad de entrecruzamiento de espín (SCO, spin-crossover), se inició cuando Cambi y Szegö (1931) sintetizaron una serie de compuestos de coordinación derivados de hierro(III) que cambiaban sus propiedades magnéticas cuando se sometían a variaciones continuas de temperatura; se encontró que dicho comportamiento era reversible. Años después, Pauling (1936) reconoció la existencia del SCO cuando hizo estudios del comportamiento magnético de la hemoglobina inspirado por un trabajo de Faraday.
El cambio en las propiedades magnéticas de estos compuestos inspiró la investigación para sus posibles aplicaciones; sin embargo, las temperaturas necesarias para verificar dicho fenómeno (menores a 100K) volvieron su utilización práctica poco factible.
En 1925 se inició el desarrollo de modelos teóricos gracias a la aportación de Ising resolviendo el correspondiente hamiltoniano para estructuras unidimensionales en el cual se introducen las constantes de cooperatividad y el espín “ficticio”. A partir de entonces, varios científicos como Onsager, Wajnflasz y Pick, han resuelto la ecuación de Ising mediante pequeñas modificaciones. A mediados de los 80, Rao, MacGarvey y Ganguli propusieron la introducción de la Energía libre de Gibbs de la mezcla de estados HS y LS (alto espín, bajo espín), por lo cual abordan el fenómeno desde un punto de vista termodinámico. Además, se han hecho cálculos teóricos mediante métodos como Montecarlo y DFT (funcionales de la densidad).
Desde 1980 se abrió un nuevo panorama con respecto a la investigación de compuestos con SCO cuando se descubrió el fenómeno conocido como LIESST (Light-Induced Excited State Spin Trapping, atrapamiento de los estados excitados de espín inducido por luz) por Gütlich y colaboradores (Gütlich y Hauser, 1990).
La búsqueda de nuevas estrategias de síntesis de estos materiales basados en la sinergia —esto es, la combinación de distintas propiedades, como propiedades estruc tu rales, condiciones de síntesis— con SCO dependiente de la temperatura, aunado al desarrollo de los modelos teóricos que explican este comportamiento han sido los herederos en el renacimiento del estudio de los compuestos de Cambi.
Este artículo tiene como propósito describir brevemente las estrategias de sinergia más estudiadas hasta el momento, presentar y explicar la validez de las reglas de Gütlich con base en la Teoría de Campo Cristalino y Teoría de Orbitales Moleculares (Ribas, 2008), así como mencionar las perspectivas de las investigaciones correspondientes.
¿Qué es el entrecruzamiento de espín?Desde 1999 la IUPAC definió el entrecruzamiento de espín como “un tipo de magnetismo molecular que resulta de la inestabilidad electrónica debida a fuerzas externas que inducen a cambios estructurales a nivel molecular y de red” (Minkin, 1999). En otras palabras, sería el cambio de las propiedades magnéticas de un compuesto de coordinación inducido mediante la variación de un campo eléctrico o magnético, temperatura, etc.
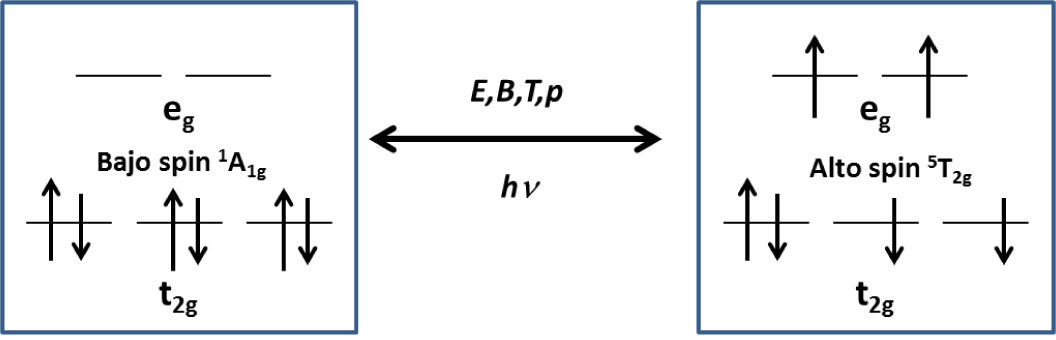
En la figura 1 se muestra el esquema del desdoblamiento energético de los orbitales de un centro metálico d6 en un compuesto de coordinación con simetría octaédrica. La flecha de doble cabeza en el medio muestra las influencias externas que favorecen las configuraciones de alto y bajo espín, T es la temperatura, p es la presión, B es un campo magnético, E representa un campo eléctrico y hv representa la irradiación de luz de una determinada longitud de onda.
Esquema del entrecruzamiento de espín (SCO). La posición de las líneas horizontales simbolizan el desdoblamiento energético de los orbitales axiales eg y los orbitales interaxiales t2g. El cuadro izquierdo muestra la configuración de Bajo spin representada por el término 1A1g el cual indica que el material presenta un singulete (ningún electrón desapareado) en su configuración electrónica. El cuadro derecho muestra la configuración de Alto spin representada por el término 5T2g el cual indica que el material presenta un quintuplete (cuatro electrones desapareados) en su configuración electrónica.
Para poder entender el SCO es necesario primero introducir la Teoría de Campo Cristalino, que explica la geometría de los compuestos de coordinación como efecto de interacciones electrostáticas entre el ligante y el ion metálico de acuerdo con el sitio de acción, es decir, la dirección (interaxial o axial) por la cual el ligante con su par de electrones se aproxima al centro metálico (Ribas, 2008). Dicha teoría supone que un compuesto de coordinación es una entidad química formada por un catión metálico y un conjunto de ligantes aniónicos o polares (δ−) cuyos electrones enlazantes actúan como cargas puntuales negativas que interaccionan repulsivamente con los electrones del catión. La teoría surgió de los estudios de Bethe y Van Vleck cuando pretendían describir los efectos del desdoblamiento energético de los orbitales de un ión libre (Na+) cuando éste se sometía al efecto del campo electrostático de la red cristalina de NaCl y de aquí se deriva el nombre de Teoría de Campo Cristalino.
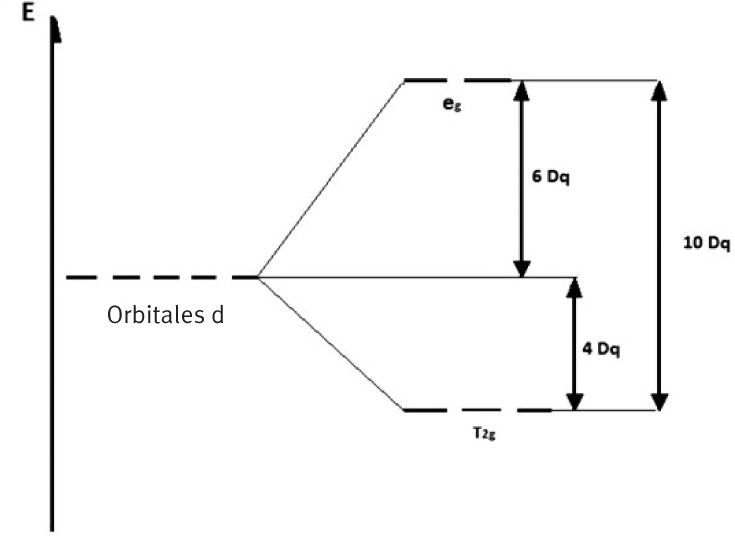
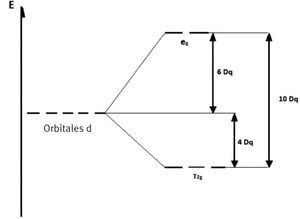
Como se observa en la figura 2, en un compuesto de coordinación octaédrico los orbitales que reciben mayor influencia del ligante son los axiales dx2-y2,dz2, por lo cual su energía potencial aumenta (eg); sin embargo, el sistema se estabiliza con la disminución en energía necesaria de los orbitales interaxiales (t2g). La suma algebraica entre el aumento en energía de los orbitales eg y la correspondiente disminución de los orbitales t2g se conoce como 10Dq. Es importante señalar que de acuerdo con el desdoblamiento de estos orbitales, producido por la interacción con los ligantes, si la energía 10Dq es mayor a la energía de apareamiento de los electrones (P), el sistema adquirirá una configuración de bajo espín (LS), es decir, la mayor cantidad de electrones estarán en los orbitales t2g; si, por el contrario, dicha energía es menor que la de apareamiento de electrones, entonces el sistema adquirirá una configuración de alto espín (HS), distribuyendo los electrones en todos los orbitales a fin de tener el mayor número posible de e− desapareados. Cuando la energía de apareamiento de los electrones (P) es similar al valor de 10Dq en centros metálicos, con configuración electrónica entre d4 y d7, se hace posible el fenómeno de SCO.
Esquema del desdoblamiento de orbitales d en un compuesto de coordinación con simetría octaédrica. Los orbitales eg son los orbitales axiales dz2y dx2-y2 y los orbitales t2g son los orbitales interaxiales dxy,dxz,dyz. La energía total del desdoblamiento se representa como 10Dq, energía relativa de la diferencia entre los valores de energéticos de eg y t2g, los cuales son 6Dq y 4Dq, respectivamente.
En un trabajo reciente, Gütlich resumió las características necesarias para que un compuesto de coordinación sea candidato para presentar el fenómeno de SCO, entre éstas se encuentran:
- 1)
Los compuestos con metales de transición de la primera serie 3d4−7 deben tener simetría octaédrica.
- 2)
Incrementar el estado de oxidación de un ion complejo octaédrico, mientras se mantengan las demás características iguales, incrementa el 10Dq en un 40–80%. En otras palabras, el efecto del SCO se puede obtener al aumentar la interacción entre el ligante y el centro metálico, como consecuencia del cambio en el estado de oxidación.
- 3)
El SCO dependiente de la temperatura se debe a una competencia favorable entre la energía de estabilización de campo cristalino (10Dq) y la energía de apareamiento de electrones (P).
Los ligantes más utilizados en el estudio de materiales que presentan SCO son aquellos que tienen por lo menos un nitrógeno como el átomo que se coordina, y dependiendo de la naturaleza del ligante se puede modificar el carácter covalente del enlace de coordinación, lo que se traduce en una reducción en la distancia de enlace entre el ion metálico y el ligante (fuerza del ligante).
Estrategias de síntesis de materiales con entrecruzamiento de espínEntre las estrategias más importantes que han presentado un avance significativo en el estudio de las posibles aplicaciones de estos compuestos encontramos:
a)SCO dependiente de la temperaturaLos complejos que se han estudiado con base en esta característica han sido en su mayoría complejos de FeII y FeIII. Este proceso es termodinámicamente conducido por la entropía del sistema, ya que una configuración de alto espín con electrones desapareados tiene una alta densidad de estados vibracionales y un alto número de degeneración de sus microestados espectroscópicos.
En este fenómeno se aprovecha la propiedad de transición de acuerdo a la temperatura ya que a temperaturas muy bajas, la energía del desdoblamiento 10Dq es mayor que la energía de apareamiento de los electrones, debido a que baja la intensidad de las vibraciones de éstos.
Se considera una distribución de población con base en la fracción molar presente en el sistema siendo γHS y γLS las fracciones molares de la configuración de alto espín y bajo espín, respectivamente. Por ello, se estudia la variación de γ como función de la temperatura.
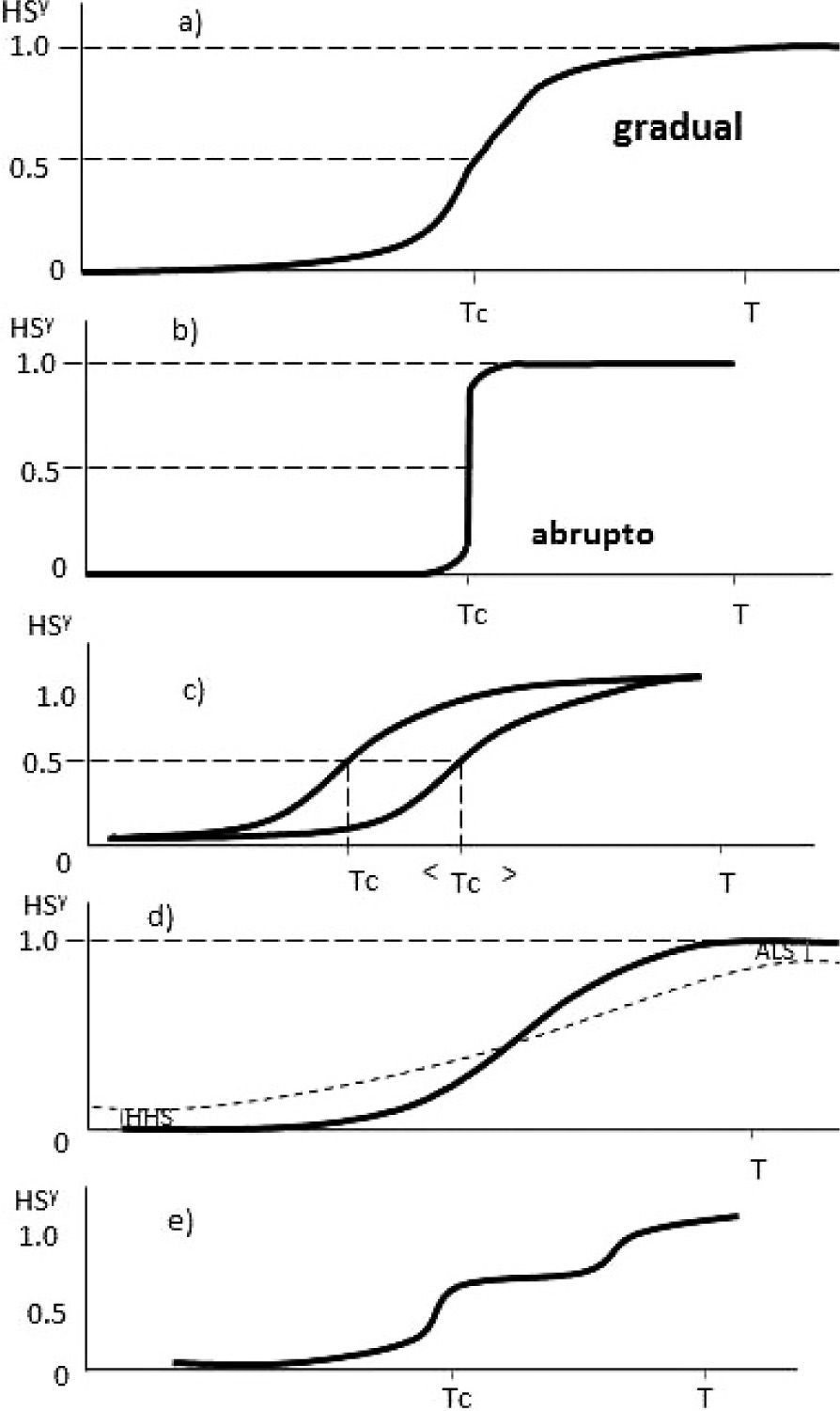
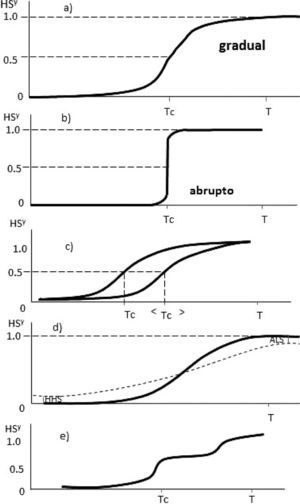
Este fenómeno ocurre en sólidos cristalinos, amorfos o en soluciones líquidas, siendo el modelado del comportamiento de los complejos en estado sólido el más estudiado. Se pueden observar distintos comportamientos de los modelos de acuerdo con las interacciones de SCO en los compuestos de coordinación por sí mismos y en las estructuras de la red. Este efecto se conoce con el término cooperatividad, que se puede definir como la modificación de las interacciones intercentrales (ion metálico-ligante), lo cual equivale a modificar la fuerza del ligante (Pavlik y Boča, 2013). Esto se refleja en las distintas formas de las curvas de las gráficas de γHS vs T (figura 3), siendo γHS la fracción molar de la configuración de alto espín del complejo y T, la temperatura. Existe una temperatura denotada como Tc la cual es la temperatura a la que γHS y γLS son iguales (0.5) y muestra el momento en que ocurre la transición de espín. Esta temperatura Tc se encuentra por debajo de los 100K.
Posibles tipos de SCO dependientes de la temperatura en estado sólido: a) gradual, b) abrupto, c) con histéresis, d) con zonas residuales, e) con meseta. Estas gráficas se obtuvieron a partir de datos experimentales con técnicas de susceptibilidad magnética, respaldada por espectroscopía de Mössbauer y capacidad térmica (modificado de Gütlich y Hauser, 1990).
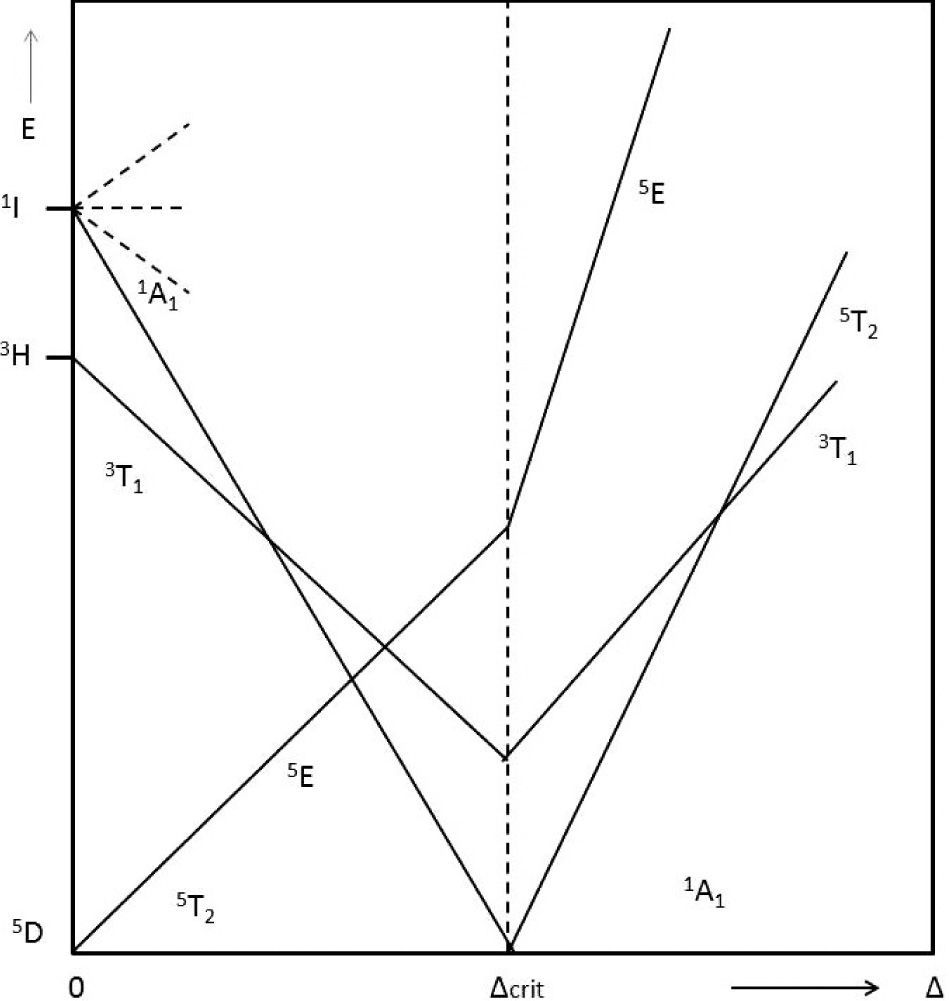
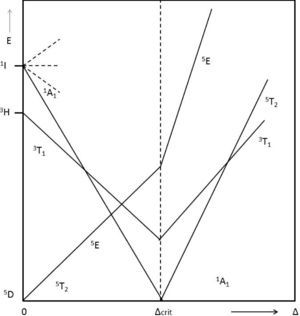
Algunos ejemplos de compuestos que presentan SCO dependiente de la temperatura son: complejos de FeII como el sistema [Fe(Rtz)6](BF4)2 donde Rtz es 1-R-tetrazol, siendo R cualquier sustituyente alquilo (CH3−, C3H7−, etc.); [Fe(2-pic)3X2]·Sol, donde 2-pic es 2-picolilamina, X=Cl,Br y Sol=H2O, 2H2O, MeOH o EtOH; [Fe(dppen)2X2] donde dppen es cis-12-bis(difenilfosfino)etileno, X=Cl, Br y los compuestos de Cambi de FeIII como [Fe(R2NCS2)3] siendo R2NCS2 un N,N-R2-ditiocarbamato y R es un grupo alquilo. Todos estos compuestos tienen una geometría octaédrica. Para el caso de FeII, un sistema 3d6, de acuerdo con el diagrama de Tanabe-Sugano se aprecia que puede presentar una configuración de alto espín con un campo ligante débil, con electrones desapareados y término espectroscópico 5T2g, o de bajo espín en un campo ligante fuerte, con electrones apareados y término espectroscópico 1A1g (véase la figura 4).
Diagrama de Tanabe-Sugano simplificado para un sistema d6. Del lado izquierdo se observan las transiciones electrónicas para compuestos de alto espín, mientras que del lado derecho se observan las posibles transiciones electrónicas en un complejo de bajo espín. Cada una de las líneas corresponde a un término espectroscópico relacionado con la energía, mientras que en el eje de las ordenadas se encuentra el desdoblamiento de campo cristalino relativo.
Si las fuerzas del ligante de ambas configuraciones están próximas a un valor crítico (Δcrit), entonces se observará una transición de espin térmica. El diagrama de Tanabe-Sugano describe sólo la energía electrónica de un sistema como una función de 10 Dq, y como se menciona arriba, el desdoblamiento energético de los orbitales depende de las características del ligante que se coordina con el ion metálico, pero también es función de la distancia de enlace entre el metal y el ligante. De tal manera que el punto de entrecruzamiento en un diagrama de Tanabe-Sugano significa simplemente que, de acuerdo al ligante, existe una configuración electrónica para la cual las energías correspondientes a bajo espín y alto espín son similares.
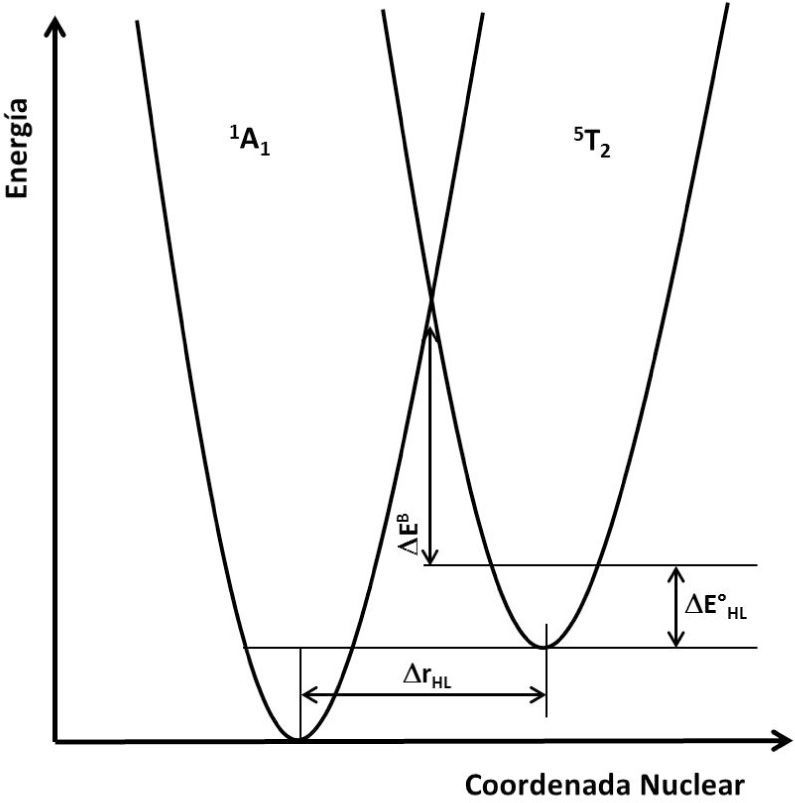
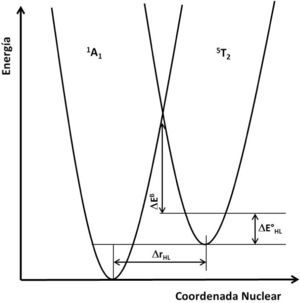
La distancia metal-ligante (coordenada nuclear) aporta información sobre el arreglo interno del compuesto de coordinación y relaciona una componente energética con pozos de potenciales correspondientes a estados de alto (5T2g) y bajo (1A1g) espín de forma que se puede observar si es factible que ocurra SCO (figura 5). Un factor importante a considerar es la distancia entre los mínimos energéticos de estos pozos, que refleja la energía debida a la diferencia en la longitud del enlace entre el ion metálico y el ligante. Esta diferencia representa la barrera energética que debe superar el sistema para el SCO, la cual se modifica por la temperatura y por ende se alcanza un estado metaestable.
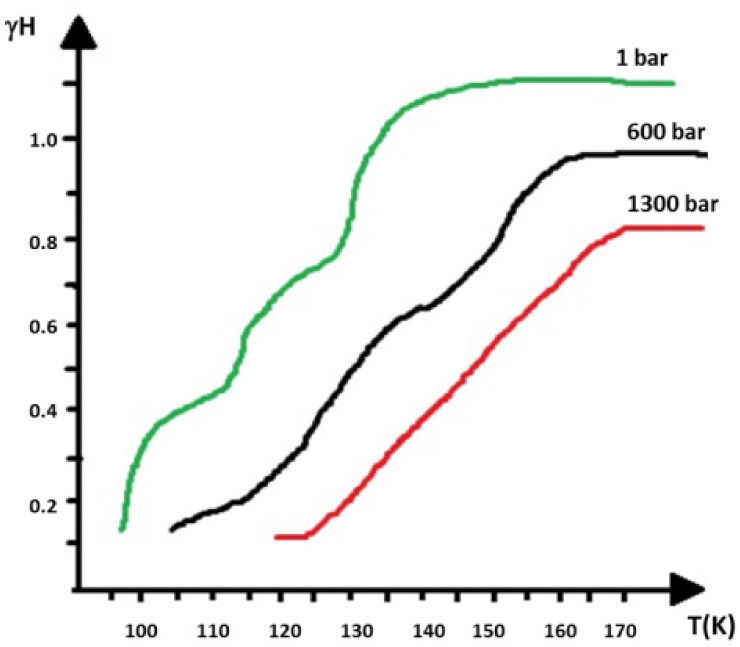
b)PresiónEl SCO depende de la distancia de enlace entre el ion metálico y el ligante, ya que gracias a sus correspondientes interacciones internucleares se observa el fenómeno. Cuando existe una diferencia en el volumen de una celda unitaria de un compuesto que tiene una configuración de alto espín y una con bajo espín, afirma Gütlich, se puede esperar que la presión favorezca el entrecruzamiento de espín (SCO) y sobre todo la estabilización de la configuración de bajo espín. En la figura 6 se observa una gráfica de γHS vs T, del compuesto [Fe(2-pic)3]Cl2·EtOH (Gütlich y Hauser, 1990). En dicho estudio se aplicaron diferentes presiones con el objetivo de desplazar la temperatura Tc hacia temperaturas más altas. Esto es importante ya que se pretende dar aplicación a estos materiales como switches moleculares o como dispositivos de almacenamiento de memoria masivo, por lo que es necesario que la temperatura Tc sea manejable, es decir, que el fenómeno ocurra a temperatura ambiente.
Gráficas de γHS vs T, aplicando diferentes presiones. El sistema estudiado fue [Fe(2-pic)3]Cl2.EtOH (modificado de Gütlich y Hauser, 1990).
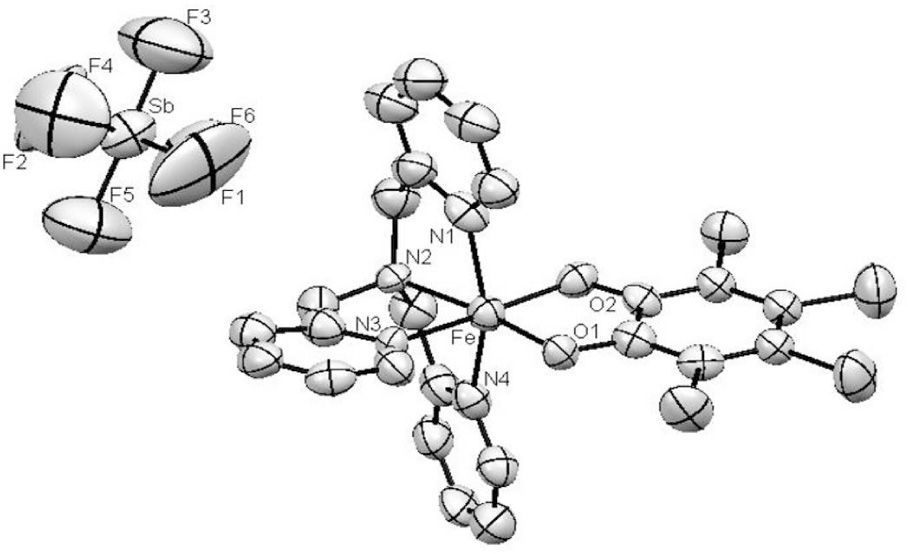
Recientemente, el grupo de Antoine Tissot realizó un estudio de las propiedades magnéticas y la conversión entre los estados de alto y bajo espín en los compuestos [Fe(TCC) (TPA)]MF6, siendo TCC=3,4,5,6-tetraclorocatecolato, TPA = N,N,N-tris(2-piridilmetil)amina y M = P, Sb. La geometría del átomo de FeIII es octaédrica en ambos casos; en la figura 7 se muestra la estructura de [Fe(TCC)(TPA)]SbF6, donde se aprecia dicha geometría (Tissot, 2013). Se encontró que la variación en el volumen de la celda unitaria del compuesto con PF6-, inducida por presión o temperatura es un factor importante en el entrecruzamiento de espín en dicho compuesto.
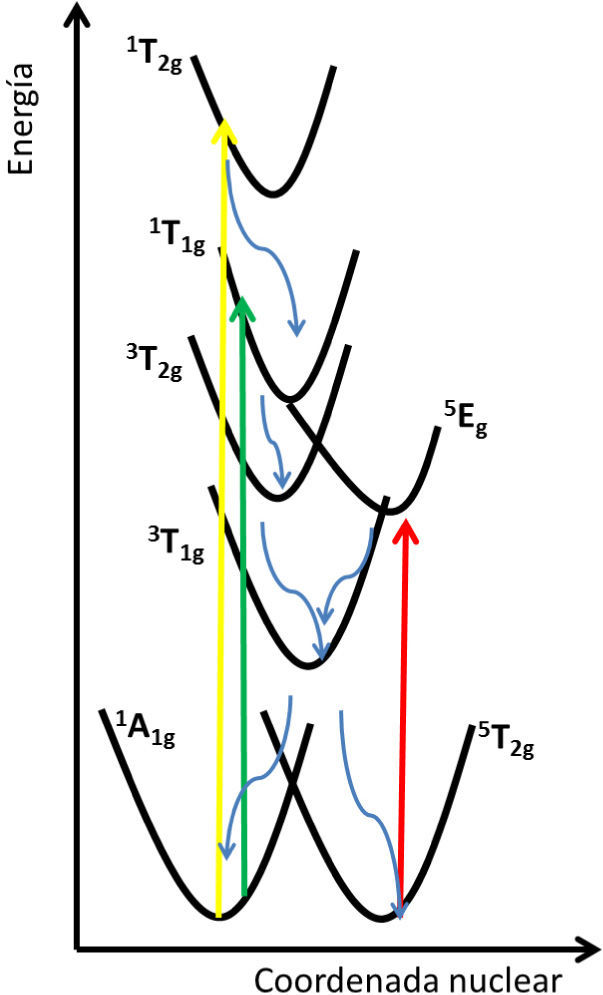
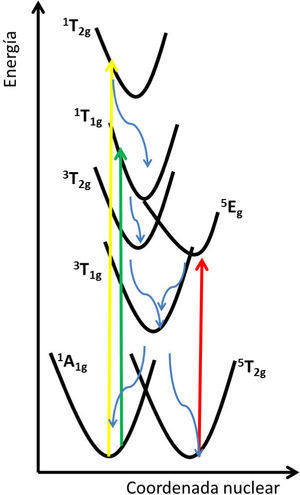
c)LIESST (Light-Induced Excited Spin State Trapping, atrapamiento de los estados excitados de espín inducido por luz)La influencia que ejerce la luz sobre el comportamiento de entrecruzamiento de espín en un compuesto de coordinación de FeIII se puede explicar con base en la figura 8; el mecanismo está descrito por Gütlich y Hauser (1990).
El fenómeno que se observa en la figura 8 muestra las transiciones permitidas por espín para un sistema 3d6(1T1g ←1 A1g y 1T2g ←1A1g). Si se irradia una muestra a bajas temperaturas, se induce una transición permitida por espín (1T1g ←1A1g) la cual es de corta duración y decae rápidamente hacia el estado base; sin embargo, existe una alternativa posible debido al acoplamiento de espín-órbita que permite una transición prohibida en el sistema (3T2g ←1T1g) que permite el decaimiento a un pozo de potencial en los estados 3T1g y posteriormente 3T2g. A partir de aquí, vuelve a decaer por medio de otra transición prohibida en el sistema ya sea al singulete 1A1g o al estado metaestable de quintuplete 5T2g. El sistema permanece atrapado en la configuración de alto espín por largo tiempo si la temperatura es lo suficientemente baja, de tal manera que la barrera energética entre los potenciales de HS y LS no pueda ser superada. Dichos potenciales están separados por la gran diferencia en la longitud de enlace entre ion metálico y el ligante de acuerdo con las respectivas configuraciones de alto y bajo espín. Ya que los pasos de entrecruzamiento en las transiciones electrónicas son rápidos, el sistema confluye en el estado de alto espín. El entrecruzamiento se puede revertir mediante la radiación de una longitud de onda que promueva la transición (5Eg ←5T2g).
El fenómeno de LIESST se descubrió con el compuesto [Fe(ptz)6](BF4)2, siendo ptz=1-propiltetrazol y se han estudiado los sistemas [Fe(Rtz)6](BF4)2, siendo R = metil-, etil-, propil-, etc. Sin embargo se han reportado ejemplos de compuestos polinucleares como los sistemas diluidos [FexM1−x(Rtz)6](BF4)2, en el que M=Zn y [FexM1−x(terpy)2] (ClO4)2 siendo M = Mn y terpy=2,2':6',2″-terpiridina (Gütlich, García y Woike, 2001).
d)LD-LISC (Ligand-Driven Light Induced Spin Change, Cambio de espín promovido por el ligante e inducido por luz)El equipo de Boillot ha diseñado esta estrategia de SCO para que los estados electrónicos de espín del ion metálico sean controlados por la alteración fotoquímica de los ligantes. Eso es debido a que cambios relativamente pequeños en las distancias de enlace en los compuestos de coordinación pueden cambiar el desdoblamiento del campo cristalino lo suficiente como para que otro estado de espín sea el estado basal del sistema. La alteración fotoquímica que proponen, es una reacción de fotoisomerización (cis-trans) del ligante 4-stypy (4-estirilpiridina) (Boillot, et al., 1999).
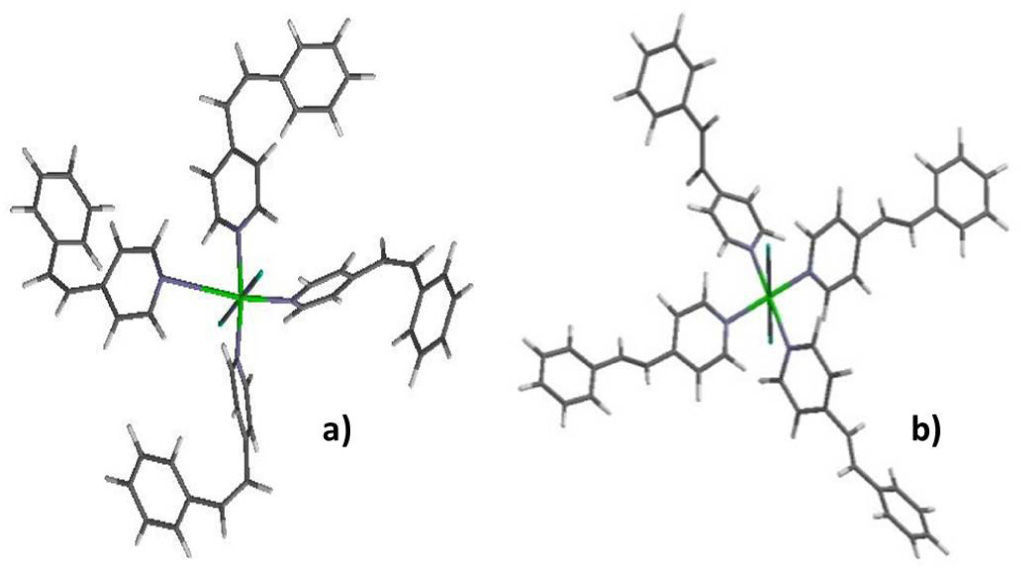
En la figura 9 se observan las estructuras de los compuestos que componen al sistema [Fe(4-stypy)4(NCS)2]. Se propone que una de las especies estudiadas presente un SCO dependiente de la temperatura, mientras que la otra presente en cualquier rango de temperatura una configuración alto espín. Otros sistemas cis-trans estudiados por el grupo de Boillot son [Fe(trans-hsbpy)2](NCS)2 siendo trans-hsbpy = 4-heptadecil-4'-trans-estiril-2,2'-bipiridina y [Fe(4-stypy)4(NCBPh3)2] (Boillot, et al., 1999).
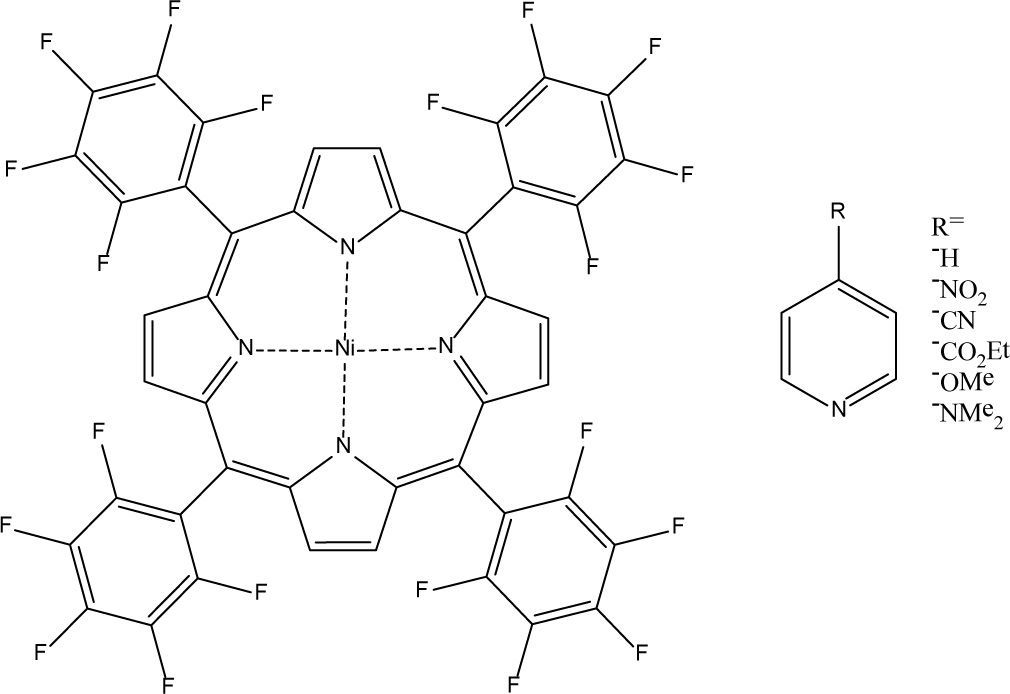
e)CISCO (Coordination-Induced Spin Crossover, entrecruzamiento de espín inducido por coordinación)En 2010 el grupo de Steffen Thies propuso esta estrategia para favorecer el SCO. El principio es muy simple: se busca aumentar el número de coordinación de un ion metálico que se encuentre en una geometría cuadrada plana (no viable según las reglas de Gütlich) para conseguir la geometría octaédrica. En la figura 10 se observa el sistema estudiado por este equipo: el compuesto de partida es un Ni2+ coordinado a una porfirina tetrasustituida (izquierda) al que se le añaden los ligantes mostrados a la derecha a fin de formar el compuesto [Ni(TPFPP)L2] siendo TPFPP = tetrakis(pentafluorofenil)porfirina y L=3-R-piridina y promover el CISCO (Thies, et al., 2010).
Sistema estudiado por el grupo de Thies. Se trata de un Ni d8 que está coordinado a una porfirina tetrasustituida y los ligantes que se adicionaron aparecen en lista a la derecha de la imagen. El sistema es el [Ni(TPFPP)L2] (izquierda) siendo TPFPP = tetrakis (pentafluorofenil) porfirina y L = 3-R-piridina (modificado de Thies, et al., 2010).
Por lo anterior, se observa que la primera regla de Gütlich puede no cumplirse como en el caso anterior, es decir, este fenómeno no es exclusivo de los metales con electrones de valencia nd4–7.
Adicionalmente, el equipo de Thies ha estudiado una serie de compuestos que presentan entrecruzamiento de espín al combinar los efectos de LD-LISC y CISCO.
Hasta ahora se han expuesto las estrategias pioneras en el estudio y diseño de compuestos de coordinación con SCO. En estas estrategias se han observado ciertas similitudes en sus principios: todos los compuestos estudiados presentan geometría octaédrica y el ion metálico participante tiene electrones de valencia pertenecientes a los orbitales 3d.
PerspectivasDesde 1980 se han estudiado las posibles aplicaciones de los compuestos de SCO gracias a sus propiedades magnéticas y al control tipo switch que se puede ejercer sobre éstas. Kahn propuso su uso como dispositivos de almacenamiento de memoria masivo o pantallas de cristal líquido, aunque también pueden servir como sensores ultrasensibles de temperatura (Kahn y Martínez, 1998).
Gütlich y colaboradores, por ejemplo, han llegado a la conclusión de que es posible mejorar el desarrollo de la computación cuántica con base en estudios de la óptica no lineal (Gaspar, et al., 2005).
Sin embargo, estas posibles aplicaciones siguen en estado de desarrollo ya que aún no se encuentran las condiciones adecuadas de temperatura para la funcionalidad de estos materiales.
Para finalizar, ejemplos de materiales con SCO y el desarrollo de modelos teóricos sobre este fenómeno, así como de las nuevas propuestas de síntesis, se encuentran ampliamente descritos en el libro Spin Crossover Materials (Halcrow, 2013).





![Gráficas de γHS vs T, aplicando diferentes presiones. El sistema estudiado fue [Fe(2-pic)3]Cl2.EtOH (modificado de Gütlich y Hauser, 1990). Gráficas de γHS vs T, aplicando diferentes presiones. El sistema estudiado fue [Fe(2-pic)3]Cl2.EtOH (modificado de Gütlich y Hauser, 1990).](https://static.elsevier.es/multimedia/0187893X/0000002500000004/v1_201412221031/S0187893X1470062X/v1_201412221031/es/main.assets/thumbnail/gr6.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)
![Estructura cristalina del compuesto [Fe(TCC)(TPA)]SbF6 Estructura cristalina del compuesto [Fe(TCC)(TPA)]SbF6](https://static.elsevier.es/multimedia/0187893X/0000002500000004/v1_201412221031/S0187893X1470062X/v1_201412221031/es/main.assets/thumbnail/gr7.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)
![Estructuras de: a) [Fe(cis-4-stypy)4(NCS)2] y b) [Fe(trans-4-stypy)4(NCS)2]. Estructuras de: a) [Fe(cis-4-stypy)4(NCS)2] y b) [Fe(trans-4-stypy)4(NCS)2].](https://static.elsevier.es/multimedia/0187893X/0000002500000004/v1_201412221031/S0187893X1470062X/v1_201412221031/es/main.assets/thumbnail/gr9.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)
![Sistema estudiado por el grupo de Thies. Se trata de un Ni d8 que está coordinado a una porfirina tetrasustituida y los ligantes que se adicionaron aparecen en lista a la derecha de la imagen. El sistema es el [Ni(TPFPP)L2] (izquierda) siendo TPFPP = tetrakis (pentafluorofenil) porfirina y L = 3-R-piridina (modificado de Thies, et al., 2010). Sistema estudiado por el grupo de Thies. Se trata de un Ni d8 que está coordinado a una porfirina tetrasustituida y los ligantes que se adicionaron aparecen en lista a la derecha de la imagen. El sistema es el [Ni(TPFPP)L2] (izquierda) siendo TPFPP = tetrakis (pentafluorofenil) porfirina y L = 3-R-piridina (modificado de Thies, et al., 2010).](https://static.elsevier.es/multimedia/0187893X/0000002500000004/v1_201412221031/S0187893X1470062X/v1_201412221031/es/main.assets/thumbnail/gr10.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)