El uso de un stent metálico autoexpandible como puente a la cirugía del cáncer de colon izquierdo en oclusión se ha señalado como tratamiento alternativo a la cirugía de urgencia. El objetivo del presente estudio fue comparar la morbimortalidad, el coste-beneficio y los resultados oncológicos a largo plazo de ambas opciones terapéuticas.
MétodosSe trata de un estudio prospectivo, comparativo, controlado y no aleatorizado (2005-2010) realizado en una unidad especializada. El estudio agrupó a 82 pacientes con cáncer de colon izquierdo en oclusión tratados mediante stent como puente a la cirugía (n=27) o cirugía de urgencia (n=55), intervenidos con intención curativa local. Las principales variables del estudio (morbimortalidad postoperatoria, coste-beneficio, tasa de estomas y resultados oncológicos a largo plazo) fueron comparados sobre la base de un análisis «con intención de tratar».
ResultadosNo se encontraron diferencias estadísticamente significativas entre los dos grupos en términos de datos preoperatorios y características tumorales. La tasa de éxito técnico en la colocación de la endoprótesis fue del 88,9% (con un 11,1% de perforaciones derivadas del stent), y el éxito clínico fue del 81,4%. No se observó diferencia alguna en cuanto a los índices de morbimortalidad postoperatoria. La tasa de anastomosis primaria fue superior en el grupo «stent como puente a la cirugía», en comparación al grupo «cirugía de urgencia» (77,8% frente a 56,4%; p=0,05). Los costes medios por paciente en el grupo «cirugía de urgencia» resultaron ser más elevados (+1.391,9€) que en el grupo «stent como puente a la cirugía». No se produjeron diferencias estadísticamente significativas en cuanto a resulados oncológicos a largo plazo.
ConclusionesEl uso de stents metálicos autoexpandibles como puente a la cirugía constituye una opción segura para el tratamiento urgente del cáncer de colon izquierdo en oclusión, con resultados oncológicos similares a largo plazo en comparación a la cirugía de urgencia, con menor coste económico y una tasa superior de anastomosis primarias, evitando numerosos estomas.
The use of a self-expanding metallic stent as a bridge to surgery in acute malignant left colonic obstruction has been suggested as an alternative treatment to emergency surgery. The aim of the present study was to compare the morbi-mortality, cost-benefit and long-term oncological outcomes of both therapeutic options.
MethodsThis is a prospective, comparative, controlled, non-randomized study (2005-2010) performed in a specialized unit. The study included 82 patients with left colon cancer obstruction treated by stent as a bridge to surgery (n=27) or emergency surgery (n=55) operated with local curative intention. The main outcome measures (postoperative morbi-mortaliy, cost-benefit, stoma rate and long-term oncological outcomes) were compared based on an “intention-to-treat” analysis.
ResultsThere were no significant statistical differences between the two groups in terms of preoperative data and tumor characteristics. The technically successful stenting rate was 88.9% (11.1% perforation during stent placement) and clinical success was 81.4%. No difference was observed in postoperative morbi-mortality rates. The primary anastomosis rate was higher in the bridge to surgery group compared to the emergency surgery group (77.8% vs. 56.4%; P=.05). The mean costs in the emergency surgery group resulted to be €1,391.9 more expensive per patient than in the bridge to surgery group. There was no significant statistical difference in oncological long-term outcomes.
ConclusionsThe use of self-expanding metalllic stents as a bridge to surgery is a safe option in the urgent treatment of obstructive left colon cancer, with similar short and long-term results compared to direct surgery, inferior mean costs and a higher rate of primary anastomosis.
Aproximadamente el 7-29% de las neoplasias colorrectales malignas se presentan como obstrucción intestinal, produciéndose el 70% de ellas en el colon izquierdo. Este es el motivo principal de la cirugía de urgencia (CU) en el cáncer de colon1-3. A pesar de los avances médicos y quirúrgicos, esta CU sigue presentando una elevada morbilidad (30-60%) y mortalidad (10-30%) en comparación con la cirugía electiva (tasa de mortalidad inferior al 5%)4-8. Esta diferencia podría deberse a dos razones: en primer lugar, en la CU el paciente no está debidamente preparado y optimizado en términos de situación nutricional, equilibrio electrolítico, etc. En segundo lugar, se realiza, a menudo, por parte de cirujanos generales no especializados en cirugía colorrectal, con un efecto derivado negativo resultante de la variable «factor cirujano»9. Además, en estos casos el colon se halla distendido y no preparado, lo que muchas veces imposibilita una anastomosis primaria en un mismo tiempo quirúrgico, siendo necesario realizar un estoma terminal. Por ello, los pacientes requerirían otra cirugía para el cierre del estoma y la reconstrucción del tránsito intestinal, con la consecuente morbimortalidad añadida, lo cual, junto a la edad avanzada de los mismos, hace que muchos de ellos no se intervengan10. En otros casos, dado el mal estado del resto del colon, los pacientes pueden requerir una cirugía mayor, como una colectomía subtotal o total, lo que supondrá, como sabemos, una peor calidad de vida futura.
Otra cuestión muy importante es el incremento del riesgo de dehiscencia anastomótica en la CU, en casos de obstrucción del colon y con cirujanos no especializados en cirugía colorrectal, con el consiguiente impacto oncológico y en la calidad de vida a largo plazo, demostrado ampliamente en la literatura8,9,11,12. Sin embargo, Frago et al.13 han demostrado buenos resultados de morbimortalidad tras la resección quirúrgica de urgencia, aunque únicamente en casos seleccionados y realizadas por cirujanos especializados en cirugía colorrectal.
En 1991, Dohmoto14 introdujo el uso del stent metálico autoexpandible como tratamiento paliativo en la obstrucción maligna del colon izquierdo. La elevada morbimortalidad en estos pacientes tras la CU ha redundado en un uso más amplio del stent. Tejero et al.15 reportaron el uso de endoprótesis en el cáncer de colon izquierdo previa a la cirugía electiva. Conocido como stent «puente a la cirugía» (PC), aporta tiempo para mejorar la situación clínica, optimizar las comorbilidades y la situación nutricional del paciente y realizar los estudios preoperatorios necesarios. Todo ello reduce la morbimortalidad y el número de colostomías realizadas, según se ha reportado en estudios recientes6,7. Otras indicaciones de las endoprótesis son el tratamiento paliativo definitivo en el cáncer metastásico avanzado y en pacientes quirúrgicos de alto riesgo14.
Sin embargo, no en todos los centros puede realizarse la implantación de stents, debiéndose tener también en cuenta su coste. Por otro lado, a pesar de que las diferentes publicaciones reportan que es una técnica beneficiosa y segura, con índices de morbimortalidad bajos, no está exenta de complicaciones, como la perforación, la migración o la re-obstrucción6,16,17. Por ello, en la actualidad es objeto de gran controversia por el efecto negativo que la perforación pueda tener sobre la supervivencia de estos pacientes. De hecho, 3 de 4 ensayos clínicos aleatorizados publicados recientemente se han interrumpido prematuramente a causa de los resultados desfavorables a corto plazo en uno de los brazos del estudio, que no siempre era el mismo. Por tanto, la literatura actual no aclara cuál es la mejor opción de tratamiento para estos pacientes18-21.
La hipótesis del presente estudio se basa en que en los pacientes con cáncer de colon izquierdo en oclusión el uso de endoprótesis como «PC» puede mejorar los resultados a corto plazo sin tener un impacto negativo sobre los oncológicos a largo plazo. Ello podría justificarse por la optimización de la situación del paciente, la preparación intestinal y la posibilidad de realizar una estadificación adecuada del tumor. Además, la cirugía podría ser realizada por parte de un especialista colorrectal.
El principal objetivo del presente estudio fue evaluar la morbimortalidad postoperatoria del stent como «PC» y realizar la comparación con la «cirugía de urgencia» (CU) en pacientes con cáncer de colon izquierdo en oclusión, tratados con intención curativa. Los objetivos secundarios fueron el análisis de los costes, la tasa de estomas definitivos y los resultados oncológicos a largo plazo en cada grupo.
MétodosSe trata de un estudio prospectivo, controlado, comparativo y no aleatorizado, realizado en el Departamento de Cirugía General y Digestiva del Hospital Clínico Universitario de Valencia. Los datos fueron recogidos en una base de datos entre enero de 2005 y diciembre de 2010.
Se incluyeron los pacientes con obstrucción intestinal secundaria a cáncer de colon del lado izquierdo, situado distalmente al ángulo esplénico del colon, incluyendo también sigma y unión recto-sigma a más de 11cm del margen anal medido por rectoscopia rígida. El diagnóstico de oclusión intestinal aguda se basó en la clínica y en la radiografía de abdomen, donde se objetivó la dilatación colónica. El diagnóstico de cáncer se confirmó mediante colonoscopia flexible y TAC abdominopélvica.
En el estudio excluimos a: 1)los pacientes con peritonitis y/o perforación; 2)las resecciones locales paliativas; 3)los stents definitivos en pacientes con mal estado general o con enfermedad en estadioiv no aptos para cirugía curativa (stents paliativos), y 4)los pacientes que rechazaron la cirugía.
Se dividió a los pacientes en dos grupos: el grupo «cirugía de urgencia» (CU) cuando se realizó este tipo de intervención, y el grupo «puente a la cirugía» (PC) cuando se empleó un stent seguido de una cirugía diferida.
El determinante primario para la colocación de un stent y la asignación de grupo dependió de la disponibilidad de un endoscopista con capacidades de implantación de endoprótesis, independientemente de las características y de la comorbilidad de los pacientes, y del cirujano de guardia.
El comité de ética local aprobó el estudio, y todos los pacientes otorgaron su consentimiento informado y escrito antes de la inclusión.
Implantación de la endoprótesisEn los pacientes del grupo PC se practicó la colocación de un stent. Tras la realización de un enema rectal, se realizó una colonoscopia flexible bajo sedación, para confirmar el diagnóstico. Se utilizó un endoscopio con doble canal, introduciéndose por un canal una guía a través de la estenosis y, por el otro, un catéter por el que se introduce contraste hidrosolube. Haciendo uso de la guía se introduce el catéter portador del stent y se deja alojado en la estenosis. La correcta localización de la prótesis se comprueba con fluoroscopia y endoscopia. Se utilizaron dos tipos de endoprótesis: Wallstent® y Wallflex®, dependiendo de las preferencias del endoscopista.
El éxito técnico se definió como la colocación correcta del stent confirmada mediante fluoroscopia. El éxito clínico se definió como la resolución del cuadro de obstrucción tanto clínico como radiológico, con capacidad de aplazamiento de la cirugía durante un mínimo de 7días. En caso de éxito clínico de la colocación del stent, la cirugía electiva se realizó en un plazo máximo de 2semanas. Durante este periodo el paciente permaneció hospitalizado. En caso de producirse un suceso adverso, se indicó CU.
Técnica quirúrgicaLa cirugía consistió en la resección oncológica con intención curativa, con o sin restauración de la continuidad intestinal, de acuerdo con la decisión del cirujano de guardia. Se utilizó un abordaje laparoscópico en pacientes seleccionados, fundamentalmente en el último periodo del estudio.
Variables del estudioSe recogieron los datos siguientes: características demográficas de los pacientes, localización y estadificación del tumor, resultados y complicaciones de la colocación del stent, características de la cirugía y complicaciones postoperatorias dentro de los primeros 30días.
Además, se evaluaron los costes directos en ambos grupos. Para calcular el coste financiero utilizamos el método Alcántara18, basado en la estancia hospitalaria, tiempo de la intervención y materiales utilizados. La información requerida se adquirió del Sistema de Información Financiera del Hospital Clínico Universitario de Valencia en 2010. El coste para cada paciente se calculó utilizando la siguiente fórmula: (días en la unidad de cuidados críticos) ×1.518,15€ +(duración de la intervención) ×11,18€/min +(días en planta) ×335,07€. En los pacientes que precisaron múltiples ingresos (incluyendo readmisión por complicaciones y admisión para restaurar la continuidad intestinal) el coste total se calculó añadiendo el coste de cada ingreso. En el grupo PC el coste del stent (1.500€) fue añadido al coste total.
Los resultados oncológicos (recidiva local [RL] y sistémica [RS]) fueron recogidos a los 2 y 5años de seguimiento. La RL se definió como la presencia de tumor a nivel anastomótico, peritoneal en vecindad o pélvico, documentada mediante examen proctoscópico, radiológico o histopatológico. La RS se definió como la evidencia de enfermedad en cualquier otra localización. La RL incluyó tanto a los pacientes afectados únicamente de RL como a aquellos con RL y RS. El seguimiento de los pacientes se realizó mediante visitas médicas ambulatorias y valoración del CEA cada 3meses durante el primer año, cada 6meses durante el segundo año, y anualmente a partir de entonces. La tomografía computarizada toracoabdominal se realizó cada 6meses durante los primeros 2años. La colonoscopia se realizó al cabo de un año y a los 3-5 años desde entonces, dependiendo del riesgo individual del paciente. De sospecharse recidiva, se utilizaron métodos diagnósticos adicionales, según la necesidad. El oncólogo, dentro del equipo multidisciplinar, actuó como observador independiente para confirmar la presencia de recidiva de la enfermedad.
Análisis estadísticoEl análisis realizado fue según la intención de tratamiento.
Las variables continuas fueron descritas mediante media, desviación estándar, mediana y primer y tercer cuartiles, y mediante frecuencias relativa y absoluta en el caso de las variables categóricas. Las variables categóricas se compararon utilizando las pruebas de chi-cuadrado y exacta de Fisher. Las variables continuas se compararon utilizando pruebas de significación paramétricas (prueba t de Student) y no paramétricas (U de Mann-Whitney), según el caso.
Se utilizó la regresión logística multivariable para evaluar las diferencias entre los grupos, en cuanto a la morbilidad postoperatoria y los datos quirúrgicos. Para cuantificar las variables de confusión tales como edad, sexo, hipertensión, diabetes y localización y estadio tumoral, se calculó una puntuación de propensión utilizando dichas variables, añadiéndose como covariable a los modelos. Se utilizaron las curvas de Kaplan-Meier y la prueba de Log-Rank para investigar los factores pronósticos sobre la RL, la supervivencia libre de enfermedad y la supervivencia específica del cáncer. Se utilizaron métodos de regresión gradual (criterios de inclusión de variables cuando p<0,1) para el modelo anterior.
Las diferencias en cuanto a los costes medios entre ambos grupos se evaluaron mediante dos métodos: la transformación logarítmica de los valores de costes seguida de una prueba t, y la aleatorización muestral utilizando 10.000 nuevos muestreos. También se compararon los costes utilizando la prueba de Wilcoxon, para valorar las diferencias de ubicación.
La significación estadística se estableció en α=0,05.
Se utilizó el software Statistical Package for Social Sciences (SPSS versión 22.0.0; IBM SPSS Statistics, IBM Corporation, Armonk, NY, EE.UU.) para realizar los análisis descriptivo y estadístico. El análisis y las gráficas de costes se realizaron utilizando el software R (versión 3.0.2).
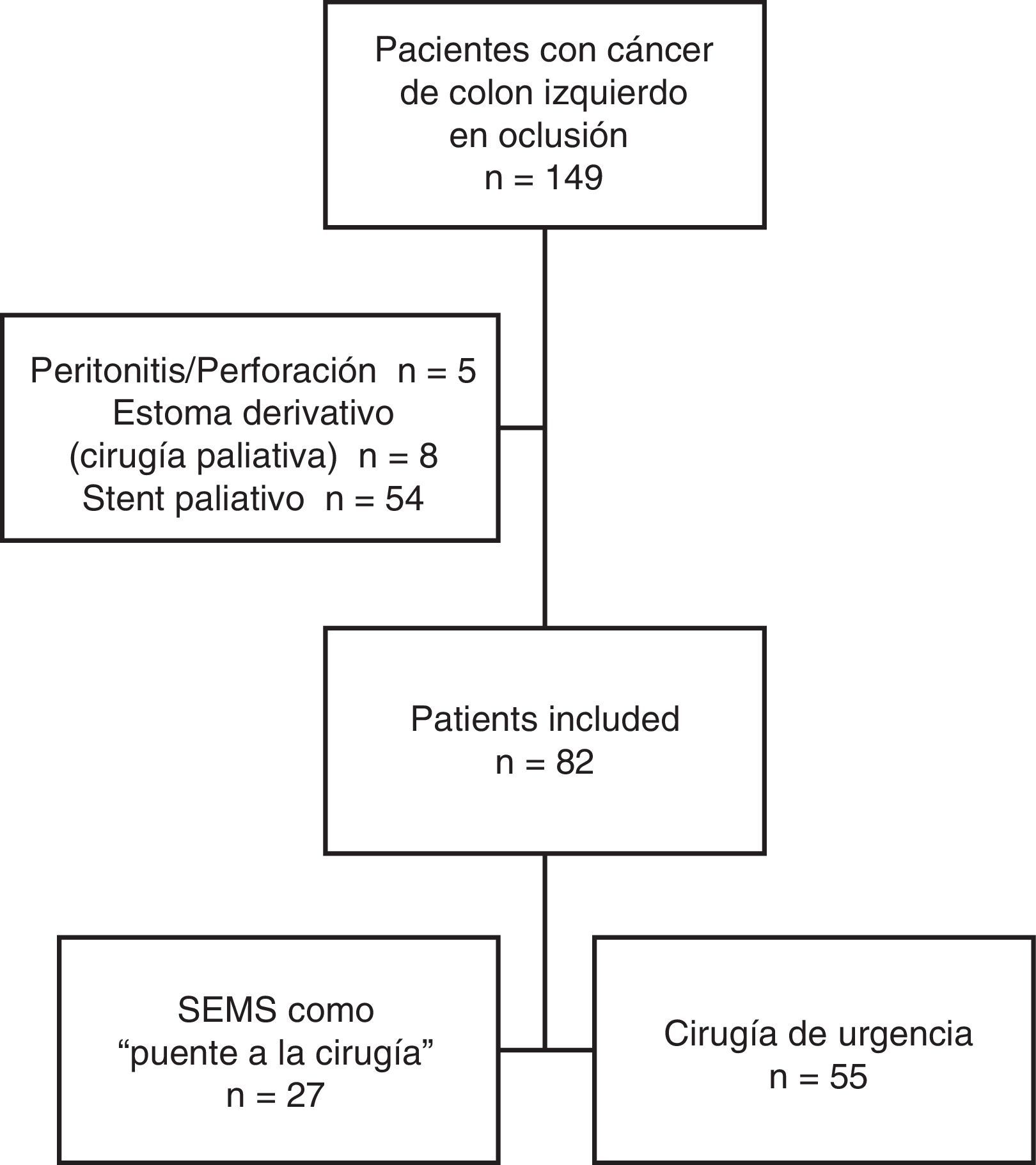
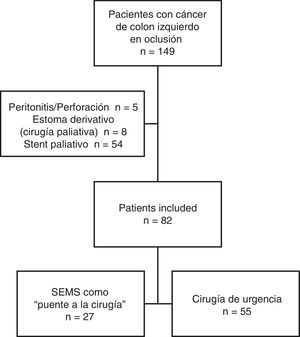
ResultadosCaracterísticas de los pacientesDesde enero de 2005 hasta diciembre de 2010, un total de 149 pacientes se presentaron con cáncer de colon izquierdo en oclusión. De ellos, 54 fueron excluidos del estudio debido a que el stent fue paliativo, 5 por perforación tumoral y peritonitis, y 8 debido a cirugía paliativa. Una vez aplicados los criterios de inclusión y exclusión, se incluyó finalmente a 82 pacientes en el estudio: 27 fueron tratados inicialmente con endoprótesis (grupo «PC») y 55 pacientes fueron sometidos a CU (grupo «CU») (fig. 1).
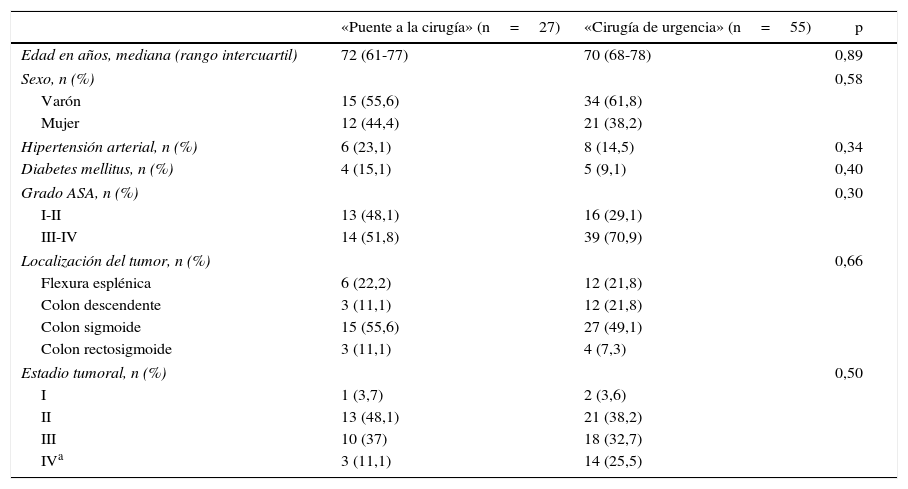
No se encontraron diferencias estadísticamente significativas entre los dos grupos en términos de edad, sexo, hipertensión arterial, diabetes mellitus, grado ASA (American Society of Anesthesiologists), localización del tumor y estadificación tumoral (mínimo p=0,30) (tabla 1).
Características demográficas y oncológicas de los pacientes
| «Puente a la cirugía» (n=27) | «Cirugía de urgencia» (n=55) | p | |
|---|---|---|---|
| Edad en años, mediana (rango intercuartil) | 72 (61-77) | 70 (68-78) | 0,89 |
| Sexo, n (%) | 0,58 | ||
| Varón | 15 (55,6) | 34 (61,8) | |
| Mujer | 12 (44,4) | 21 (38,2) | |
| Hipertensión arterial, n (%) | 6 (23,1) | 8 (14,5) | 0,34 |
| Diabetes mellitus, n (%) | 4 (15,1) | 5 (9,1) | 0,40 |
| Grado ASA, n (%) | 0,30 | ||
| I-II | 13 (48,1) | 16 (29,1) | |
| III-IV | 14 (51,8) | 39 (70,9) | |
| Localización del tumor, n (%) | 0,66 | ||
| Flexura esplénica | 6 (22,2) | 12 (21,8) | |
| Colon descendente | 3 (11,1) | 12 (21,8) | |
| Colon sigmoide | 15 (55,6) | 27 (49,1) | |
| Colon rectosigmoide | 3 (11,1) | 4 (7,3) | |
| Estadio tumoral, n (%) | 0,50 | ||
| I | 1 (3,7) | 2 (3,6) | |
| II | 13 (48,1) | 21 (38,2) | |
| III | 10 (37) | 18 (32,7) | |
| IVa | 3 (11,1) | 14 (25,5) | |
ASA: Sociedad Americana de Anestesiólogos.
En 24 pacientes (88,9%) el stent se implantó técnicamente con éxito. En los 3 pacientes restantes (11,1%) se produjo perforación durante la colocación del stent, por lo que precisaron CU (2 procedimientos de Hartmann y una resección anterior con anastomosis e ileostomía en asa). Se demostró éxito clínico en 21 (de 27) pacientes (77,8%), dentro de las 48h posteriores a la implantación del stent en 19 pacientes, y dentro de las 72h en los otros 2 pacientes. En un paciente con éxito clínico inicial se produjo la migración del stent transcurridos 7días, originando oclusión intestinal que precisó CU (resección anterior con anastomosis e ileostomía en asa). No se produjeron complicaciones de sangrado o re-obstrucción en el grupo PC.
Resultados quirúrgicosNo observamos ninguna diferencia estadísticamente significativa en cuanto a técnica quirúrgica (laparotomía frente a laparoscopia) y tiempo de intervención (tabla 3). La estancia media hospitalaria fue superior en el grupo PC (16 frente a 11; p=0,005).
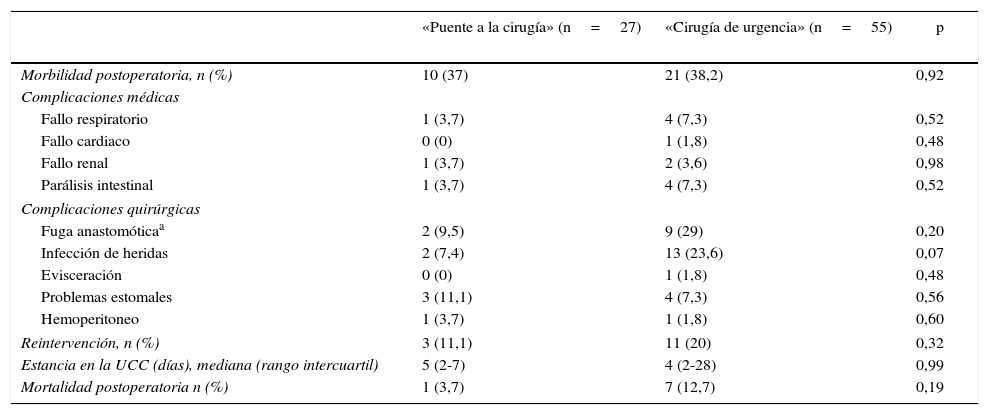
Complicaciones postoperatorias
| «Puente a la cirugía» (n=27) | «Cirugía de urgencia» (n=55) | p | |
|---|---|---|---|
| Morbilidad postoperatoria, n (%) | 10 (37) | 21 (38,2) | 0,92 |
| Complicaciones médicas | |||
| Fallo respiratorio | 1 (3,7) | 4 (7,3) | 0,52 |
| Fallo cardiaco | 0 (0) | 1 (1,8) | 0,48 |
| Fallo renal | 1 (3,7) | 2 (3,6) | 0,98 |
| Parálisis intestinal | 1 (3,7) | 4 (7,3) | 0,52 |
| Complicaciones quirúrgicas | |||
| Fuga anastomóticaa | 2 (9,5) | 9 (29) | 0,20 |
| Infección de heridas | 2 (7,4) | 13 (23,6) | 0,07 |
| Evisceración | 0 (0) | 1 (1,8) | 0,48 |
| Problemas estomales | 3 (11,1) | 4 (7,3) | 0,56 |
| Hemoperitoneo | 1 (3,7) | 1 (1,8) | 0,60 |
| Reintervención, n (%) | 3 (11,1) | 11 (20) | 0,32 |
| Estancia en la UCC (días), mediana (rango intercuartil) | 5 (2-7) | 4 (2-28) | 0,99 |
| Mortalidad postoperatoria n (%) | 1 (3,7) | 7 (12,7) | 0,19 |
Se encontró una diferencia marginalmente significativa en cuanto a la tasa de anastomosis primarias, siendo mayor en el grupo PC en comparación al grupo CU (77,8% frente a 56,4%; p=0,05). Más llamativo fue que únicamente en 4 de los 30 pacientes (13,3%) sometidos al procedimiento de Hartmann se restauró la continuidad intestinal: 0/6 pacientes en el grupo PC y 4/24 pacientes en el grupo CU (p=0,24). Los motivos de la no reconstrucción en el grupo PC fueron la progresión de la enfermedad (n=5) y la muerte postoperatoria (n=1). En el grupo CU los motivos fueron la progresión de la enfermedad (n=2), la muerte postoperatoria (n=2) y la comorbilidad del paciente (n=16). La tasa de estomas definitivos fue del 22,2% en el grupo PC y del 36,4% en el grupo CU (p=0,21). Los datos quirúrgicos se detallan en la tabla 2.
Datos quirúrgicos
| «Puente a la cirugía» (n=27) | «Cirugía de urgencia» (n=55) | p | |
|---|---|---|---|
| Intervención quirúrgica, n (%) | |||
| Laparotomía | 25 (92,6) | 55 (100) | 0,17 |
| Laparoscopia | 2 (7,4) | 0 | |
| Intervención realizada, n (%) | |||
| Anastomosis primaria | 21 (77,8) | 31 (56,4) | 0,05 |
| Hartmann | 6 (22,2) | 24 (43,6) | |
| Tiempo quirúrgico (minutos), mediana (rango intercuartil) | 220 (170-240) | 190 (150-240) | 0,50 |
| Tiempo de reintervención (minutos), mediana (rango intercuartil) | 120 (90-150) | 120 (90-150) | 0,99 |
| Estancia hospitalaria (días), mediana (rango intercuartil) | 16 (12-25) | 11 (8-16) | 0,005 |
Al analizar la morbilidad global postoperatoria no observamos diferencias significativas entre los dos grupos (37% en el grupo PC frente a 38% en el grupo CU; p=0,92). Al detallar las complicaciones individuales encontramos en el grupo CU una tendencia hacia el aumento de las infecciones de la herida (7,4% en el grupo PC frente a 23,6% en el grupo CU; p=0,10) y fuga anastomótica (9,5% en el grupo PC frente a 29% en el grupo CU; p=0,20), aunque las diferencias no fueron estadísticamente significativas. Tres pacientes (11,1%) fueron re-intervenidos en el grupo PC (2 fugas anastomóticas y un desprendimiento de la colostomía), y 11 (20%) en el grupo CU (9 fugas anastomóticas, una evisceración y un hemoperitoneo) (p=0,32).
La mortalidad postoperatoria en el grupo PC fue del 3,7% (neumonía nosocomial, n=1) y del 12,7% en el grupo CU (neumonía nosocominal, n=2; shock séptico por dehiscencia de sutura, n=3; fístula enterocutánea, n=1, e isquemia de colon con fallo multiorgánico, n=1) (p=0,19) (tabla 3).
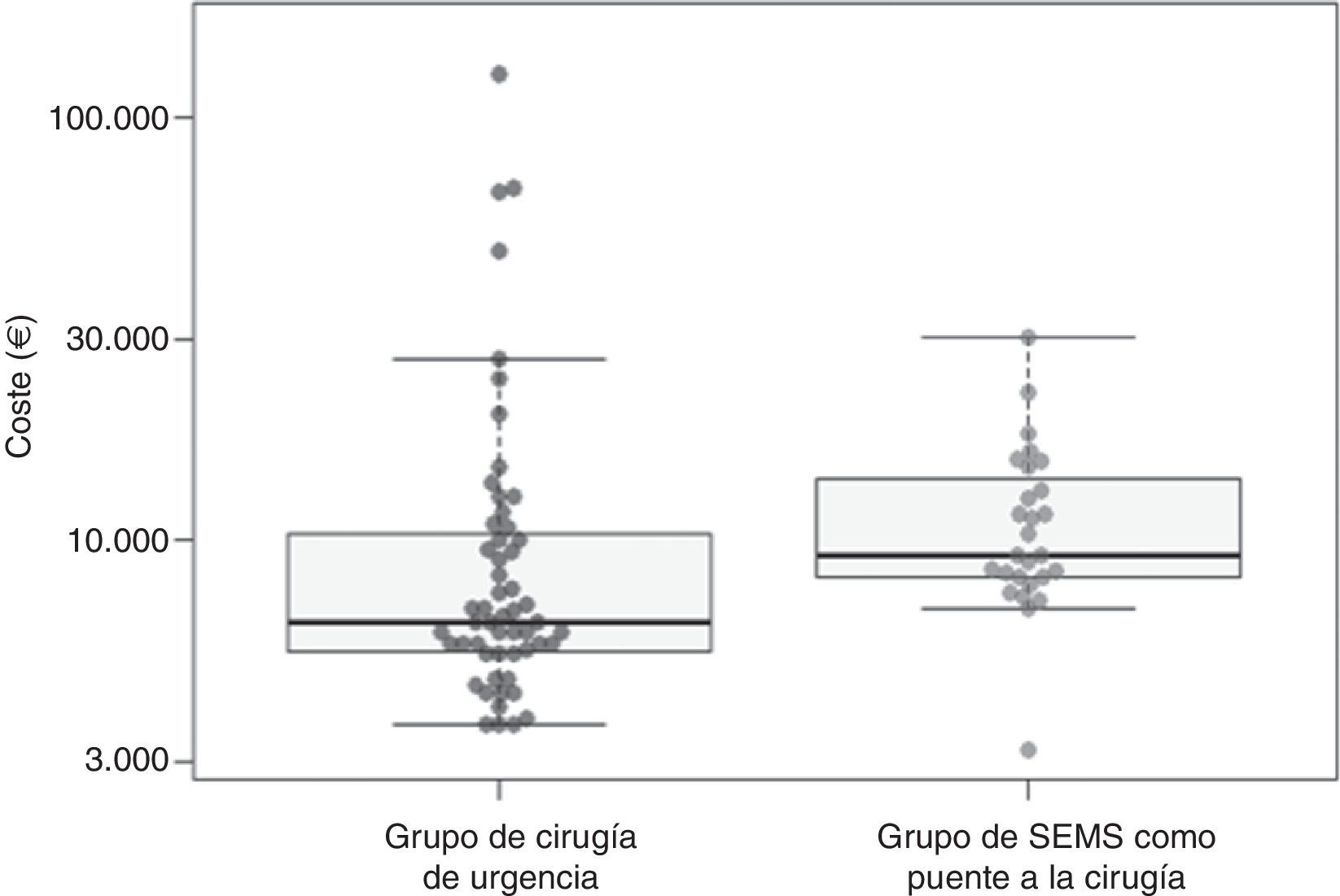
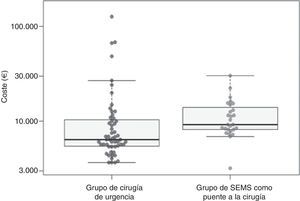
CostesAl considerar los costes medios, el tratamiento en el grupo CU tuvo un coste medio de 13.059,1€ (DE=20.359,2€) y en el grupo PC de 11.547,9€ (DE=5.543,5€); por tanto, el coste en el grupo CU fue superior en 1.391,9€ al del grupo PC. Sin embargo, esta diferencia no fue estadísticamente significativa (p=0,11 con transformación logarítmica y prueba t y p=0,36 con aleatorización muestral no paramétrica) (tabla 4, fig. 2).
Costes
| «Puente a la cirugía» (n=27) | «Cirugía de urgencia» (n=55) | Diferencia de coste total (CT «intervención de urgencia»-CT «puente a la cirugía») | |
|---|---|---|---|
| Coste total, € | |||
| Media (DE) | 11.547,9 (5.543,5) | 13.059,1 (20.359,2) | 1.391,9; IC 95% [−3.536,8 a 7.838,1]; p=0,36 |
| Mediana (rango intercuartil) | 9.209,3 (8.203,4-14.011,2) | 6.369,- (5.447,3-10.400,8) | −2.840,-; IC 95% [−4.515,6 a −1.433,9]; p=0,002 |
CT: coste total.
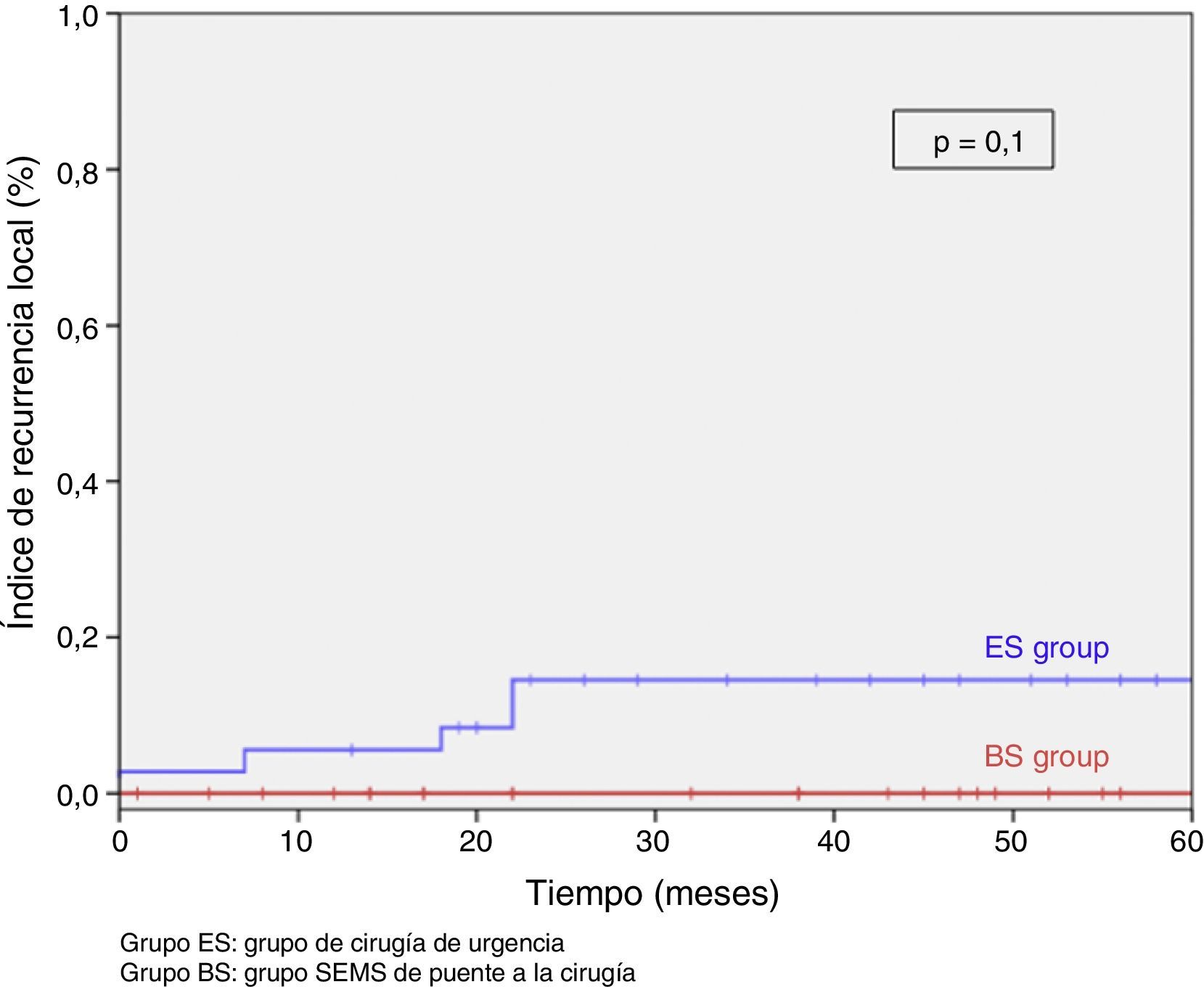
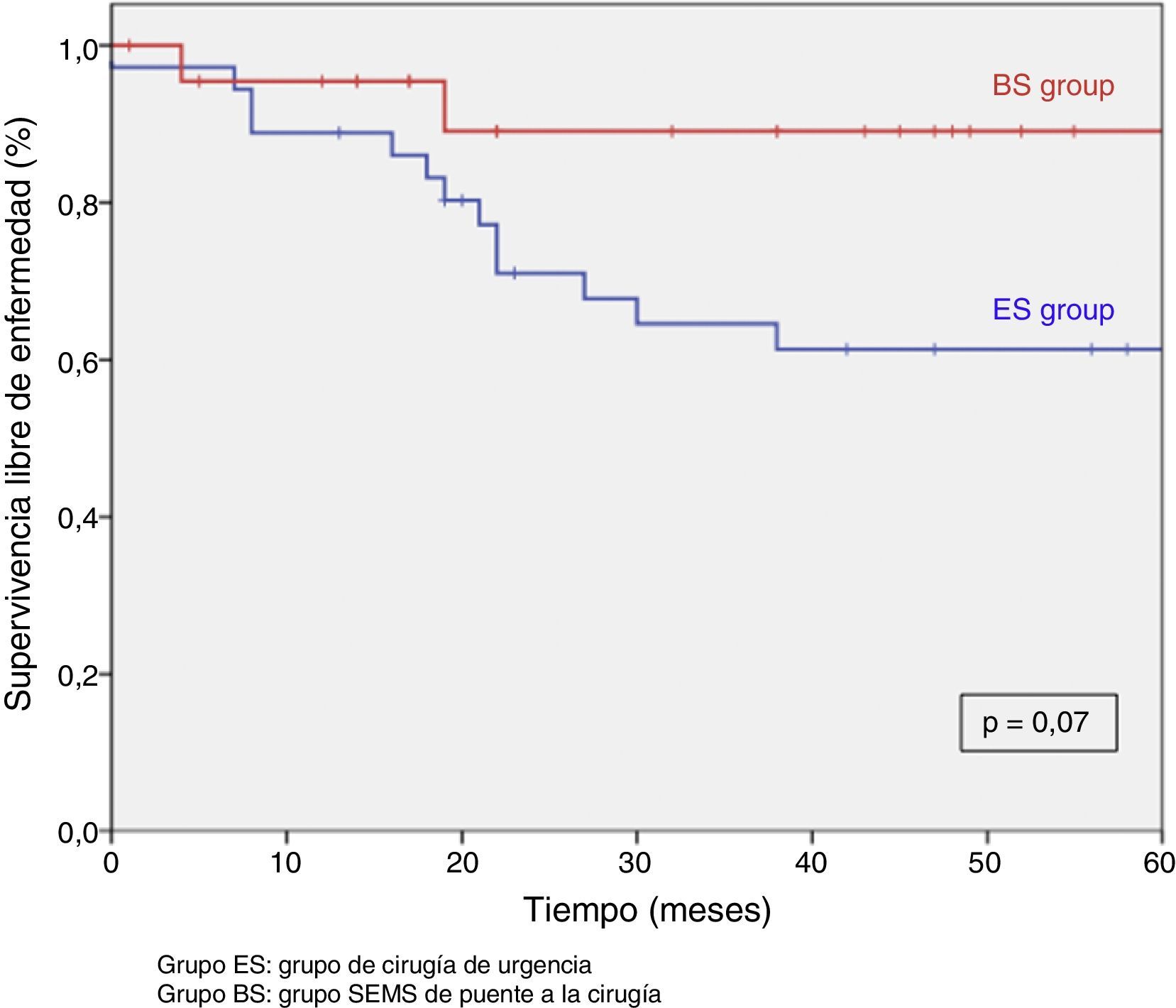
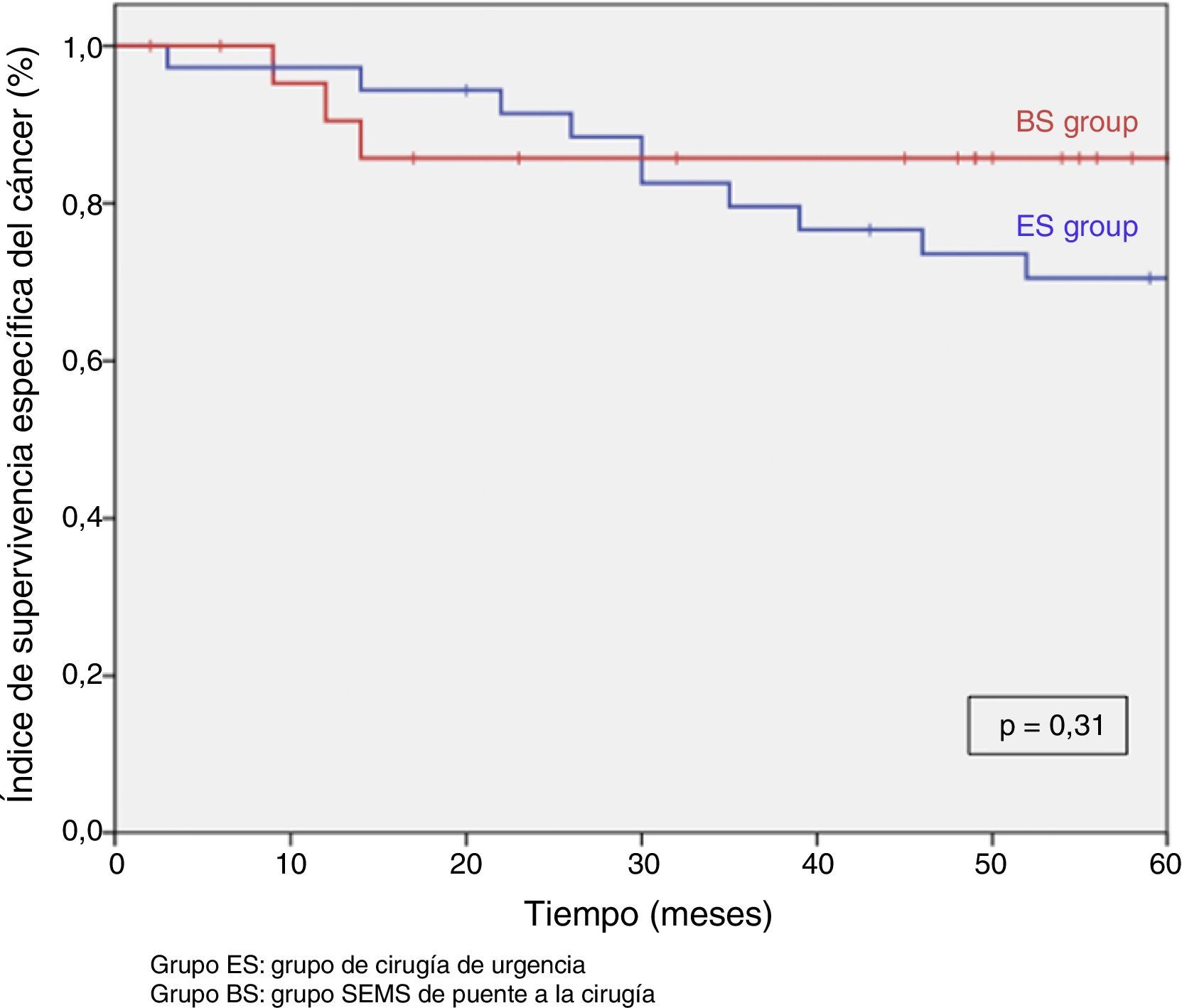
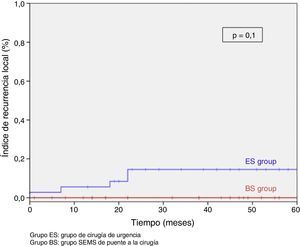
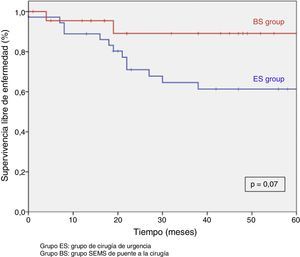
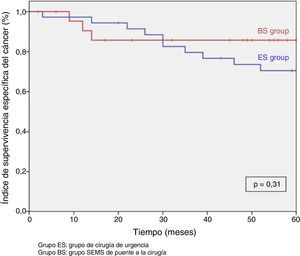
Tras excluir los pacientes metastásicos (n=17) y las muertes postoperatorias (n=8) el seguimiento medio fue de 58 (30-75) meses. Se produjeron 5RL de entre los 59 pacientes restantes (8,5%). No observamos ninguna diferencia estadísticamente significativa en cuanto a RL, supervivencia libre de enfermedad o supervivencia específica del cáncer. Sin embargo, durante el seguimiento a 5años hay que destacar que el índice actuarial de RL en el grupo PC fue del 0%, y del 14,5% en el grupo CU (p=0,1) (fig. 3). La supervivencia libre de enfermedad en el grupo PC fue del 89,1%, siendo del 61,3% en el grupo CU (p=0,07) (fig. 4). La supervivencia específica del cáncer fue del 85,7% en el grupo PC y del 70,5% en el grupo CU (p=0,31) (fig. 5).
DiscusiónLa obstrucción de colon secundaria a neoplasia maligna es un problema clínico frecuente y requiere un tratamiento urgente para su resolución, como puede ser la cirugía urgente o la utilización de una endoprótesis como PC electiva15. La mejor indicación para la colocación del stent es en aquellos tumores distales a la flexura esplénica hasta recto superior (una distancia mínima del margen anal de 11cm). La colocación de stents en el colon proximal al ángulo esplénico es posible, pero su realización no está tan extendida, con menos de un 4% de los casos8,22,23, ya que la CU de colon derecho tiene una morbimortalidad similar a la cirugía electiva24.
Con la introducción de las endoprótesis o stents y la cirugía diferida se intenta reducir la morbimortalidad postoperatoria y la formación de estomas. Martinez-Santos et al.6 demostraron que la colocación de stents previa a la cirugía electiva, en comparación a la resección quirúrgica de urgencia, se asociaba a una mayor tasa de anastomosis primarias, menores complicaciones, menor estancia en la unidad de cuidados críticos y menor estancia hospitalaria. Además, se han encontrado resultados oncológicos similares en términos de supervivencia general7. Un metaanálisis reciente reflejó que la colocación de endoprótesis como PC en el cáncer de colon en oclusión incrementaba la tasa de anastomosis primarias y disminuía la formación de estomas. Igualmente, existe evidencia de menores complicaciones que en la cirugía urgente, aunque la mortalidad postoperatoria no reflejó cambio alguno25.
En nuestro estudio observamos un éxito clínico tras la colocación de stents en 21 de 27 pacientes (77,8%), que es similar a los resultados publicados en otras series19,20,26-28. En estos pacientes, la descompresión colónica por el stent permitió la corrección de las alteraciones hidroelectrolíticas, mejorar el estado nutricional del paciente y completar la estadificación tumoral y, de este modo, someterse a la intervención quirúrgica de forma electiva en unas condiciones óptimas. Al mismo tiempo, observamos un éxito técnico del 88,9%, similar al de otros estudios21-26. La migración y la re-oclusión son dos de las principales complicaciones asociadas a la colocación de stents, aunque la más grave de ellas es la perforación de colon, con una incidencia variable de hasta el 16%19-21,26-28. En nuestro estudio observamos una tasa de perforación del 11,1%. Diversos estudios reportan que las perforaciones podrían tener una repercusión oncológica adversa, favoreciendo la adhesión y la diseminación de las células tumorales, aunque no está claro20,21,26,28. Son necesarios nuevos estudios que demuestren el efecto adverso de la perforación tumoral en la supervivencia de estos pacientes.
Nuestros resultados son comparables a los de otros estudios prospectivos y aleatorizados, y revisiones sistemáticas, en los que se concluye que la colocación de stents como PC es segura y efectiva, asociándose a una menor morbimortalidad22,29-32. Por contra, Pirlet et al.20 reportaron en un estudio controlado, aleatorizado y multicentro que la colocación de stents como PC de cáncer de colon en oclusión no es más segura ni más eficaz que la CU. No pudieron demostrar que la colocación de stents reduzca significativamente la necesidad de estomas. Tuvieron que interrumpir el ensayo debido al elevado índice de fallos técnicos (perforación intestinal) que se produjo en el grupo PC25. Se han reportado hallazgos similares como causa de discontinuidad de un estudio aleatorizado, debido a la morbimortalidad sustancial que se produjo en el grupo de stents26. El elevado índice de fallos técnicos puede reflejar la experiencia del endoscopista. El volumen y la experiencia se correlacionan con los resultados, y la implantación de stents intestinales no es una excepción33. Esto podría explicar los resultados negativos de la colocación de endoprótesis en los estudios anteriores.
Nosotros no observamos diferencias significativas en cuanto al índice de complicaciones postoperatorias entre ambos grupos (37% frente al 38,2%), de manera similar a otros estudios22. En cuanto a la mortalidad postoperatoria, no se reflejó diferencia estadísticamente significativa en ambos grupos (3,7% frente al 12,7%). Las muertes en el grupo «PC» fueron causadas por problemas médicos postoperatorios y no por complicaciones derivadas de la colocación de los stents. Sin embargo, las muertes acaecidas dentro de los 30días siguientes a la CU se debieron a problemas quirúrgicos, ya que estos pacientes se enfrentan a una cirugía con una inadecuada preparación y optimización del paciente.
El uso de endoprótesis en el cáncer de colon en oclusión permite programar la intervención para que pueda ser realizada por un cirujano colorrectal. Anteriormente se ha demostrado que este hecho implica un uso más amplio de la laparoscopia, la cual permite mejores resultados a corto plazo y una recuperación postoperatoria más rápida20,22,28. Además, junto con un mejor estatus del paciente, pueden justificar la mayor tasa de anastomosis primarias hallado en el grupo PC en el presente estudio (77,8% vs 56,4%), evitándose numerosos estomas.
En este estudio, si tenemos en cuenta el coste medio, encontramos un coste más elevado en el grupo CU, aun cuando no existan diferencias estadísticamente significativas. Dicha diferencia se debe a los índices superiores de complicaciones médicas y quirúrgicas en el grupo CU. Por otro lado, el coste más elevado de la estancia hospitalaria en los pacientes del grupo PC se debe a la inclusión del tiempo entre la inserción del stent y la cirugía electiva, y no a la prolongación de la estancia hospitalaria. Una estrategia de hospitalización diferente, con altas a los pacientes entre el momento de la inserción del stent y la realización de la cirugía, podría reducir los costes del grupo PC. Debemos considerar también que en el grupo CU existe una mayor tasa de estomas, lo que incrementa el uso de recursos médicos y financieros. Alcántara et al.18, en un análisis similar, mostraron resultados parecidos al evaluar el coste quirúrgico y la duración de la estancia, no hallando diferencia alguna entre ambos grupos. Sin embargo, encontraron una diferencia al comparar el coste incluyendo los materiales utilizados, reflejando el grupo PC un coste superior. Esto contradice a otros estudios, que concluyen que la colocación de stents es un procedimiento rentable que reduce la estancia hospitalaria y los costes, en comparación a la CU34-36.
Si nos centramos en los resultados oncológicos, no observamos diferencias significativas en cuanto a las tasas de RL, supervivencia libre de enfermedad o supervivencia global entre los dos grupos. Esto puede deberse al pequeño tamaño de la muestra de estudio. Otro hecho importante es que no se observó RL en ninguno de los 3 pacientes en los que el stent perforó el colon. Nuestros datos contrastan con los publicados por Sabbagh et al.34, que observan que la supervivencia global y a los 5años es significativamente más baja en el grupo al que se le coloca el stent que en el grupo cirugía urgente (p=0,0003), con una tasa de mortalidad debida por cáncer significativamente más alta en el grupo del stent que en el de cirugía urgente (48% vs 21%, respectivamente; p=0,02). También encuentran diferencias estadísticamente significativas en la supervivencia libre de enfermedad, la tasa de recurrencia y la media de tiempo hasta la recurrencia, siendo mejor en el grupo de cirugía urgente.
Las limitaciones del presente estudio son que se ha realizado en un único centro, con un pequeño tamaño de muestra, y que no es de naturaleza aleatorizada. También existe un riesgo de sesgo de selección, ya que la decisión sobre el tratamiento está influenciada por la preferencia del cirujano y por la disponibilidad de endoscopista de guardia. Sin embargo, el largo plazo del seguimiento del estudio es de gran utilidad para demostrar que los stents no se asocian a resultados oncológicos adversos a largo plazo.
En conclusión, el presente estudio pone de manifiesto que la colocación de endoprótesis como PC es una opción segura para el tratamiento del cáncer de colon izquierdo en oclusión, con resultados a corto y a largo plazo similares a la cirugía directa, menores costes medios y que permite reducir el número de estomas. Se requieren estudios prospectivos adicionales, con un mayor tamaño de muestra, para demostrar el efecto beneficioso de la colocación de endoprótesis como PC.
FinanciaciónLos autores declaran que no han recibido financiación alguna para el presente estudio.
AutoríaDiseño del estudio: Flor-Lorente, Frasson, E. García-Granero.
Adquisición de datos: Baguena, A. García-Granero, Sanchiz, Peña, Espí.
Análisis e interpretación de los resultados: Flor-Lorente, Frasson, E. García-Granero, Cervantes, Esclapez.
Preparación del manuscrito: Flor-Lorente, Baguena.
Revisión crítica y aprobación del manuscrito: todos los autores.
Conflicto de interesesLos autores declaran no tener conflicto de intereses alguno.
Al Departamento Financiero del Hospital Clínico Universitario de Valencia (Sra. Marisa Román) por facilitar los datos económicos, así como el cálculo de los costes.