En la evolución de los pacientes con infecciones intra-abdominales complicadas la peritonitis terciaria constituye la forma más tardía y grave. La mayor dificultad radica en dar una definición común, precisa y consensuada para conocer cuándo realizar su diagnóstico y cómo poder evitarla y/o tratarla. Esta entidad requiere un tratamiento quirúrgico precoz y repetido, una terapia antibiótica de amplio espectro frente a microorganismos multirresistentes y unas medidas de soporte sistémico intensivo. A pesar de todo ello el pronóstico es malo ya que presenta una mortalidad que puede llegar hasta el 60% siendo la prevención la medida más importante para evitar su desarrollo. En este artículo hemos realizado una revisión específica de la peritonitis terciaria, de las definiciones aceptadas, de los factores de riesgo, de su fisiopatología, de la flora microbiológica implicada y de su tratamiento.
Tertiary peritonitis is the most delayed and severe outcome of patients with complicated intra-abdominal infections. The major difficulty lies in giving a common, precise and consensus definition in order to know when to make its diagnosis and how it can be avoided and/or treated. This condition requires early and repeated surgery, wide spectrum antibiotic therapy against multi-resistant bacteria and intensive systemic support measures. Despite all this, the prognosis is extremely poor since it has a mortality which can reach up to 60%, with preventions being the most important measure to avoid it developing. In this article, we have made a specific review of tertiary peritonitis, of the accepted definitions, the risk factors, its pathophysiology, the microbiological flora involved, and its treatment.
La peritonitis se define como un proceso inflamatorio causado por algún irritante o algún microorganismo como bacterias, hongos, virus, granulomas, fármacos o cuerpos extraños. La infección intra-abdominal se define como las manifestaciones locales que ocurren como consecuencia de la peritonitis. La sepsis intra-abdominal engloba las manifestaciones sistémicas de una inflamación peritoneal grave1,2.
En la peritonitis después de un estímulo inflamatorio inicial por un microorganismo se produce una respuesta local con hiperemia de la vasculatura subyacente, aumento de exudado de fluido en el peritoneo con un influjo de macrófagos durante las 2-4 primeras horas. Después de 4 horas existe un aumento de neutrófilos mediado por la producción de citoquinas IL-1, IL-6, TNF, leucotrienos, factor activador de plaquetas, C5a y C3a. Esta cascada inflamatoria produce además de un intento de destrucción bacteriana, una respuesta pro-coagulante generando una malla de fibrina por la producción de fibrinógeno de las células mesoteliales y macrófagos para formar una barrera física para contener la infección formando un absceso. Si no se puede contener la infección se produce lo que se denomina peritonitis difusa. Si la inflamación es muy intensa y las bacterias y endotoxinas alcanzan el torrente sanguíneo se desencadena una respuesta sistémica que es lo que se define como sepsis intra-abdominal1–3.
Las peritonitis se pueden clasificar en comunitarias o nosocomiales según el lugar de adquisición y según su mecanismo de producción, etiología y fisiopatología como se indica en la tabla 14.
Clasificación de las peritonitis
| Peritonitis primaria |
| Peritonitis secundaria |
| Peritonitis por perforación |
| Comunitaria |
| Nosocomial |
| Peritonitis postoperatoria |
| Dehiscencia de sutura |
| Perforación iatrogénica |
| Peritonitis postraumática |
| Peritonitis terciaria |
| Persistencia de peritonitis secundaria postoperatoria |
| Sin agentes patógenos |
| Fúngica |
| Bacterias de baja patogenicidad |
| Absceso peritoneal |
En este artículo se pretende realizar una revisión sobre una entidad frecuente y extremadamente grave dentro de las peritonitis como es la peritonitis terciaria. Debido al conflicto que existe tanto en su definición, como en su diagnóstico y tratamiento, la evidencia de la que se dispone es muy escasa ya que los criterios de inclusión de los pacientes son muy diferentes debido a que las definiciones de la citada dolencia son muy heterogéneas y por tanto los resultados son enormemente variables. Además prácticamente no existen estudios prospectivos centrados en pacientes con peritonitis terciaria excepto uno de reciente publicación en el año 20095. Por tanto se intentará clarificar en la medida de lo posible esta dolencia aunque será imposible resolver todas las dudas existentes ya que son necesarios en el futuro consensos y estudios mejor diseñados.
DefiniciónUna de las mayores dificultades radica en dar una definición de peritonitis terciaria adecuada, ausente de ambigüedad y consensuada. Como dicen Evans et al para su diagnóstico en la evolución de los pacientes con peritonitis se puede requerir más arte que ciencia6. Ya en 1990 se intenta definir lo que denominan «peritonitis persistentes» como un síndrome de elevada mortalidad que evoluciona a una disfunción multiorgánica debido a la persistencia o recurrencia de una infección abdominal en la que la reintervención quirúrgica puede no demostrar con certeza un proceso infeccioso, aunque sí se encuentra con frecuencia cierto grado de tejido y líquido inflamatorio. Esta nueva cirugía no mejora de manera rápida la condición clínica del paciente y los resultados microbiológicos de las muestras recogidas en la intervención muestran el crecimiento de organismos de significado incierto y diferentes de los hallados en la peritonitis secundaria7. Poco después Reemst et al ya definen la peritonitis terciaria como una peritonitis difusa sin patógenos, o con hongos o con bacterias de baja patogenicidad, en ausencia de un foco infeccioso bien definido8. Posteriormente Nathens et al la definen como la infección intra-abdominal probada por cultivo persistente o recurrente al menos 48 horas después del tratamiento aparentemente adecuado de la peritonitis bacteriana secundaria9. Malangoni por su parte considera que se trata de una infección recurrente de la cavidad peritoneal que sigue a un episodio de peritonitis primaria o secundaria10. Algunos autores se apoyan para definirla en el número necesario de intervenciones quirúrgicas para el control del foco infeccioso desde que es suficiente con más de una re-intervención quirúrgica para unos a los que creen que es necesaria una persistencia de la infección intra-abdominal después de la tercera operación2,11. A medida que surgen estudios de peritonitis terciaria se intentan dar definiciones más completas apoyándose en las previas. En ellas se considera esta entidad más como un síndrome que como un proceso patológico específico en pacientes con una infección abdominal persistente que precisan re-intervenciones quirúrgicas en las que se objetivan colecciones exudativas difusas más que abscesos y que a nivel sistémico se manifiesta como un proceso séptico persistente con disfunción multiorgánica y una elevada mortalidad a pesar de un tratamiento antimicrobiano y quirúrgico agresivo2,12–14. En el año 2005 en la Conferencia Consenso Internacional se da por fin una definición para homogeneizar opiniones y se denomina la peritonitis terciaria como una inflamación peritoneal que persiste o recurre después de 48 horas, con signos clínicos de irritación peritoneal, tras un tratamiento aparentemente adecuado que sigue a una peritonitis secundaria y producida por patógenos nosocomiales. Se divide en microbiológicamente confirmada, probable y posible. Confirmada es aquella en que se aíslan uno o más patógenos nosocomiales del líquido peritoneal o de la sangre en un contexto clínico apropiado tras 48 horas de tratamiento de una peritonitis primaria o secundaria. La flora nosocomial patógena incluye entre otros Stafilococci plasmacoagulasa negativo, Candida species, Enterococci, Pseudomonas, Enterobacter, etc. y está asociada con el sobre-crecimiento en el tracto gastrointestinal de los mismos microorganismos. Probable se define como la enfermedad clínica compatible con una peritonitis secundaria documentada con inflamación peritoneal persistente (más de 500 leucocitos/ml de líquido peritoneal) en ausencia de confirmación microbiológica. Posible es aquella en que persisten signos de inflamación sistémica pero sin una clara evidencia documentada de inflamación persistente del espacio peritoneal después de una peritonitis bacteriana secundaria15. A pesar de todos estos intentos de dar una definición adecuada, en la práctica clínica diaria es difícil llegar a un consenso de cuál es el momento en que etiquetamos la peritonitis terciaria ya que la mayor complicación resulta en delimitar cuándo el paciente pasa de padecer una peritonitis secundaria a una terciaria ya que existe una continuidad de una con otra6. Probablemente el mayor punto de conflicto aparece a la hora de decidir qué se entiende por «tratamiento aparentemente adecuado» fundamentalmente en lo que se refiere al manejo quirúrgico del foco infeccioso ya que no se especifica en la mayoría de estudios y definiciones de peritonitis terciaria y que resulta en la inclusión de pacientes muy distintos entre unos estudios y otros, lo que deriva en resultados clínicos muy diferentes. Prácticamente sólo Chromik et al puntualizan este aspecto y para clasificar a un paciente con peritonitis terciaria se requiere un «control aparentemente adecuado del foco quirúrgico» que viene definido por una completa erradicación del foco quirúrgico. Por tanto, según ellos no debe existir una disrupción o defecto anatómico de una víscera hueca gastrointestinal ni un «problema técnico» de la cirugía previa como dehiscencia de un muñón o anastomosis o cualquier otro problema técnico que derive en la pérdida de integridad física de las vísceras huecas gastrointestinales, en cuyo caso definen el proceso como peritonitis secundaria en curso5. Debido a la falta de consenso respecto a este último criterio quirúrgico y a la dificultad que entraña en la práctica clínica, lo que para unos autores puede ser una peritonitis secundaria postoperatoria complicada para otros ya se trata de una peritonitis terciaria.
Factores de riesgoLos factores de riesgo para el desarrollo de peritonitis terciaria son la malnutrición, comorbilidad, una puntuación elevada en escalas de gravedad APACHE II y SAPS II, la presencia de microorganismos resistentes al tratamiento antibiótico y el fallo orgánico5,10. La edad avanzada también parece estar relacionada con la probabilidad de desarrollar peritonitis terciaria en algunos estudios aunque en otros no se aprecia esta relación10,16. También se ha objetivado que aquellos pacientes con infecciones fúngicas pueden tener mayor propensión al desarrollo de peritonitis terciaria16,17. Desde el punto de vista quirúrgico no se aprecia especial predisposición a su desarrollo según el lugar anatómico donde se originó la peritonitis secundaria, únicamente en un estudio se encontró una mayor asociación en pacientes con peritonitis a partir de una pancreatitis necrosante, dehiscencia del muñón duodenal o peritonitis tras cirugía hepatobiliar como dolencia inicial5,10,18. Por otra parte sí parece que el desarrollo de peritonitis terciaria está asociado a una puntuación inicial elevada en la escala Mannheim Peritonitis Index (MPI) recogida en el momento de intervención quirúrgica por peritonitis secundaria5,16,17. Algunos autores incluso dan puntos de corte de puntuación a partir de los cuales existe mayor riesgo de desarrollo de peritonitis terciaria como es un MPI de 22 en el momento de la cirugía de la peritonitis secundaria y un SAPS II de 39 en el segundo día de postoperatorio5. En algunos estudios se ha objetivado que la falta de mejoría en la puntuación de algunas escalas como la de Goris o SOFA en los días 3 o 4 sugiere la presencia de sepsis abdominal persistente y puede apoyar la necesidad de re-exploración quirúrgica19. Como explicábamos previamente el hecho de que no haya consenso y resulte difícil la separación entre peritonitis secundaria postoperatoria complicada y peritonitis terciaria hace que los factores de riesgo de evolución desfavorable de la peritonitis secundaria y de desarrollo de una u otra sean prácticamente superponibles5,10,20,21.
FisiopatologíaDurante la infección se producen citoquinas pro-inflamatorias que actúan reclutando células inflamatorias para combatir contra patógenos, limpiar el tejido dañado y estimular la cicatrización de heridas. Como protección del daño inflamatorio contra el huésped se generan a su vez citoquinas anti-inflamatorias que disminuyen la capacidad de los monocitos para producir mediadores y para presentar antígenos mediante la expresión del HLA-DR22. Por tanto se produce un equilibrio como resultado de una respuesta inmune balanceada. En la peritonitis terciaria la cascada anti-inflamatoria prevalece produciéndose un estado de inmunoparálisis que se define como un número de monocitos con expresión del HLA-DR (CD 14) inferior al 30%18,22. Como consecuencia existe un estado de alteración de la inflamación peritoneal que da lugar a la ausencia de colecciones purulentas y abscesos claros. Esto se traduce en una dificultad en la cicatrización de heridas y en la recuperación orgánica. Los factores predisponentes a este estado de inmunoparálisis son dependientes tanto del paciente (edad, desnutrición, deficiencias genéticas, inmunes...), de la enfermedad de base (malignidad, neutropenia...) como de las intervenciones sobre el paciente (cirugía, transfusiones, fármacos inmunosupresores...)22. Ante esta situación los microorganismos pueden acceder a la cavidad peritoneal por contaminación durante las intervenciones quirúrgicas, por la selección del inóculo polimicrobiano peritoneal inicial por el tratamiento antibiótico, o por traslocación de la flora intestinal. Esta traslocación puede ser favorecida por isquemia intestinal, endotoxemia, malnutrición, o por la proliferación de flora intestinal resistente por la presión antibiótica23.
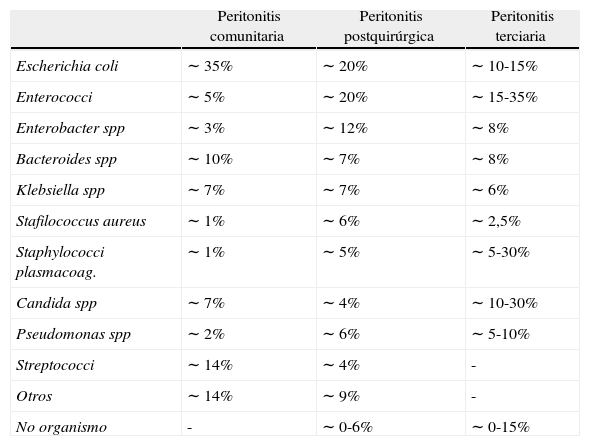
MicrobiologíaEn el tracto digestivo humano coexisten entre 400 y 600 especies microbianas y la concentración bacteriana aumenta progresivamente desde 104bacterias/ml de secreción intestinal en el tracto superior hasta 1011 en el tracto inferior y por su parte los microorganismos grampositivo del tracto superior van desapareciendo predominando los gramnegativo y anaerobios que son en el tracto inferior 1.000 veces más frecuentes que los aerobios24. La microbiología implicada en la peritonitis terciaria varía progresivamente desde la peritonitis comunitaria y postquirúrgica (tabla 2) debido a la presión antibiótica que en general ha recibido el paciente, las intervenciones quirúrgicas repetidas y al estado de inmunoparálisis peritoneal del mismo por lo que en general la flora encontrada suelen ser microorganismos nosocomiales multirresistentes como Pseudomonas, Enterococci, Staphylococci, Candida species, enterobacterias productoras de betalactamasas de espectro extendido (BLEE) o de AmpC, etc. Además el aislamiento en gran parte de las ocasiones es monomicrobiano e incluso a veces no se consigue aislar ningún microorganismo3,9,18,20,21,25.
Microbiología de las peritonitis
| Peritonitis comunitaria | Peritonitis postquirúrgica | Peritonitis terciaria | |
| Escherichia coli | ∼ 35% | ∼ 20% | ∼ 10-15% |
| Enterococci | ∼ 5% | ∼ 20% | ∼ 15-35% |
| Enterobacter spp | ∼ 3% | ∼ 12% | ∼ 8% |
| Bacteroides spp | ∼ 10% | ∼ 7% | ∼ 8% |
| Klebsiella spp | ∼ 7% | ∼ 7% | ∼ 6% |
| Stafilococcus aureus | ∼ 1% | ∼ 6% | ∼ 2,5% |
| Staphylococci plasmacoag. | ∼ 1% | ∼ 5% | ∼ 5-30% |
| Candida spp | ∼ 7% | ∼ 4% | ∼ 10-30% |
| Pseudomonas spp | ∼ 2% | ∼ 6% | ∼ 5-10% |
| Streptococci | ∼ 14% | ∼ 4% | - |
| Otros | ∼ 14% | ∼ 9% | - |
| No organismo | - | ∼ 0-6% | ∼ 0-15% |
Los tres pilares fundamentales en el tratamiento de la peritonitis terciaria son el tratamiento antimicrobiano, el tratamiento quirúrgico y las medidas de soporte sistémico10.
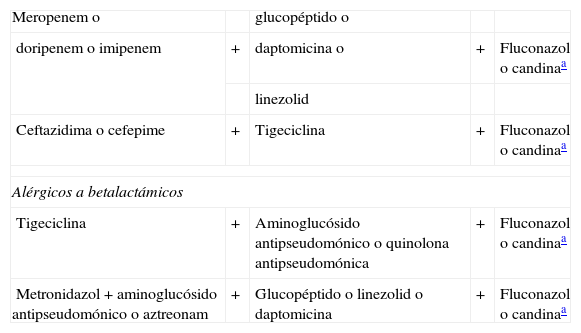
Tratamiento antibióticoEn el tratamiento antibiótico empírico de la peritonitis secundaria no existe evidencia sobre un solo régimen antibiótico eficaz26. Si bien, es cierto que en el caso de peritonitis comunitaria grave o con factores de riesgo de mala evolución, o en el caso de peritonitis nosocomial, postquirúrgica, en pacientes inmunodeprimidos o que han recibido tratamiento antibiótico de amplio espectro durante más de 72 horas previas a la peritonitis, se considera que es conveniente el inicio de una terapia antibiótica de amplio espectro20,21,27–36. La gravedad se puede definir por una puntuación elevada en la escala APACHE II mayor de 15 o por cumplir criterios de sepsis grave, y los factores de riesgo de mal pronóstico incluyen la edad mayor de 65 años, desnutrición, comorbilidad como insuficiencia cardiaca, diabetes, insuficiencia renal crónica y cirrosis hepática, y peritonitis de más de 24 horas de evolución20,21,27. Estos factores y criterios de gravedad son comunes a los que se presentan para el riesgo de desarrollo y establecimiento de la peritonitis terciaria10. Por tanto en el tratamiento antibiótico empírico de la peritonitis terciaria se debe establecer un régimen antimicrobiano de amplio espectro semejante al de la peritonitis postquirúrgica grave con cobertura para enterobacterias BLEE y frente a cocos grampositivos resistentes a betalactámicos y la asociación de terapia antifúngica frente a las especies de Candida más habituales 20,21,27–40. En la tabla 3 se muestran las posibles combinaciones en la terapia antimicrobiana de la peritonitis terciaria y las alternativas en el caso de pacientes alérgicos a betalactámicos20,21,27–41. Una vez obtenido el resultado microbiológico de los cultivos de las muestras peritoneales extraídas en las intervenciones quirúrgicas durante la peritonitis terciaria se recomienda desescalar reduciendo el espectro antibiótico ajustándolo a las sensibilidades según el antibiograma correspondiente1,9,24,29,33.
Tratamiento antimicrobiano empírico en la peritonitis terciaria
| Meropenem o | glucopéptido o | |||
| doripenem o imipenem | + | daptomicina o | + | Fluconazol o candinaa |
| linezolid | ||||
| Ceftazidima o cefepime | + | Tigeciclina | + | Fluconazol o candinaa |
| Alérgicos a betalactámicos | ||||
| Tigeciclina | + | Aminoglucósido antipseudomónico o quinolona antipseudomónica | + | Fluconazol o candinaa |
| Metronidazol + aminoglucósido antipseudomónico o aztreonam | + | Glucopéptido o linezolid o daptomicina | + | Fluconazol o candinaa |
En casos de riesgo de Pseudomonas aeruginosa resistente se debe añadir un segundo antimicrobiano antipseudomónico.
El objetivo del tratamiento quirúrgico en la peritonitis es eliminar la causa de contaminación, reducir el inóculo bacteriano y prevenir la persistencia o recurrencia de sepsis2. En el control quirúrgico se pueden realizar re-laparotomías a demanda o programadas mediante diversas técnicas. Aunque no se ha objetivado superioridad en cuanto a supervivencia entre estas dos modalidades, las re-laparotomías a demanda presentan una reducción significativa tanto de la morbilidad como de la duración de ventilación mecánica, estancia en UCI y hospitalaria, y una disminución de los costes sanitarios2,24,42,43. En la peritonitis terciaria estas re-laparotomías no deben continuarse una vez que se objetiva que la cavidad peritoneal se halla macroscópicamente limpia, ya que re-intervenciones innecesarias pueden aumentar las complicaciones y causar un mayor deterioro en la respuesta inmune local22.
Tratamiento de soporte y coadyuvanteEl tratamiento precoz antimicrobiano, quirúrgico y de soporte adecuado de la peritonitis secundaria grave es la mejor manera de prevenir el desarrollo de peritonitis terciaria. Tanto en la peritonitis secundaria y terciaria como en otros estados de sepsis grave la aplicación de protocolos de monitorización y resucitación hemodinámica precoz adecuados y de soporte sistémico siguiendo las guías de la Campaña para sobrevivir a la Sepsis Grave tendrán un impacto beneficioso en la supervivencia2,10,44.
La descontaminación digestiva selectiva del tracto digestivo puede ser una opción adecuada para eliminar las bacterias y los hongos potencialmente patógenos del tracto intestinal y así evitar el riesgo de traslocación. Un soporte nutricional adecuado, por vía enteral si es posible, es importante para la preservación, restauración y mantenimiento de la barrera intestinal22.
La manipulación inmunológica puede ser en el futuro la llave para tratar y evitar la progresión hacia la peritonitis terciaria. La aplicación selectiva de terapias inmunomoduladoras puede ser beneficiosa en el tratamiento de este estado de inmunoparálisis peritoneal6,22.
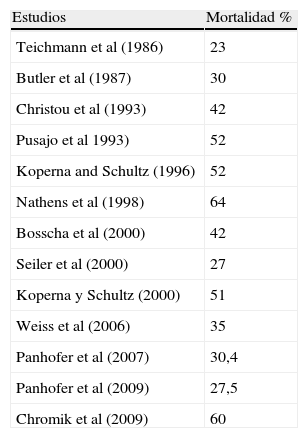
Pronóstico y conclusionesA pesar de un tratamiento antibiótico y quirúrgico adecuado, la mortalidad de la peritonitis terciaria es muy elevada por lo que parece que está más en relación con el tipo de población en el que se produce que con la gravedad del proceso patológico por sí mismo45. La mortalidad se encuentra en un rango entre el 30 y el 60% según los diferentes estudios (tabla 4). Por tanto parece más importante intentar prevenir su desarrollo con medidas diagnósticas, terapéuticas y de soporte, adecuadas y precoces, que intentar tratarla una vez que se ha instaurado. Como comentan en sus estudios Nathens et al los pacientes mueren más «con» que «de» peritonitis terciaria, pudiendo ser esta dolencia simplemente una manifestación de un estado terminal de disfunción orgánica9.
Mortalidad de la peritonitis terciaria
| Estudios | Mortalidad % |
| Teichmann et al (1986) | 23 |
| Butler et al (1987) | 30 |
| Christou et al (1993) | 42 |
| Pusajo et al 1993) | 52 |
| Koperna and Schultz (1996) | 52 |
| Nathens et al (1998) | 64 |
| Bosscha et al (2000) | 42 |
| Seiler et al (2000) | 27 |
| Koperna y Schultz (2000) | 51 |
| Weiss et al (2006) | 35 |
| Panhofer et al (2007) | 30,4 |
| Panhofer et al (2009) | 27,5 |
| Chromik et al (2009) | 60 |
Como conclusión podemos resumir que en general se acepta que la peritonitis terciaria es un síndrome de respuesta inflamatoria sistémica con disfunción orgánica causado por un estado de inflamación peritoneal que persiste después de 48 horas de un tratamiento aparentemente adecuado de una peritonitis secundaria. Su desarrollo está condicionado por la gravedad del cuadro clínico inicial, por la comorbilidad previa del paciente y por su capacidad de respuesta inmunológica. Precisa de medidas de tratamiento de soporte intensivo y de una terapia antimicrobiana empírica de amplio espectro con cobertura para patógenos nosocomiales multirresistentes que suelen estar involucrados en esta dolencia. El punto clave probablemente es llegar a un consenso para definir que se considera como «manejo quirúrgico aparentemente adecuado del foco infeccioso». Aunque comprendemos que en la práctica clínica puede resultar muy difícil definir este concepto resulta necesario para concretar cuál es el punto de transición entre una peritonitis postoperatoria complicada y una peritonitis terciaria. De está manera se podrán homogeneizar criterios de inclusión para poder realizar en el futuro estudios mejor diseñados que valoren con mejor especificidad cuáles son los factores de riesgo, el pronóstico y las medidas de prevención y eficacia en el tratamiento de la peritonitis terciaria.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.