Recientes estudios destacan la presencia del dolor intenso en las extremidades inferiores postsafenectomía. A pesar de que la infiltración local con bupivacaína en el tratamiento del dolor posquirúrgico está extendido en muchas cirugías, hasta el momento en la de revascularización coronaria no se ha empleado. Nos marcamos como objetivo evaluar la infiltración local de bupivacaína en el manejo del dolor postsafenectomía.
MétodoEstudio prospectivo con 2 cohortes de pacientes que se incluyeron de forma aleatoria en 2 grupos: grupo control (GC), donde se trató de forma convencional el cierre de la herida quirúrgica postsafenectomía, y grupo intervención (GI), donde se infiltraron tras el cierre 50mg de bupivacaína extendida a lo largo de la herida quirúrgica postsafenectomía. Se analizaron el perfil de los pacientes, las variables intraquirúrgicas y la intensidad del dolor con la escala visual analógica (EVA), entre otras. Consentimiento informado y análisis de datos con el paquete estadístico SPSS versión 22.0.
ResultadosSobre el miembro inferior seleccionado postsafenectomía el GC fue el que mayor dolor intenso presentó con el movimiento (EVA ≥ 4) durante las 2 (p=0,043), 4 (p=0,001) y 12 (p=0,017) h del postoperatorio. Sin embargo, fue el GI el que mayor complicación de la herida quirúrgica presentó (hematomas, p=0,016), (infección, p=0,019).
ConclusionesLos pacientes que fueron infiltrados con 50 mg de bupivacaína extendida por la herida quirúrgica postsafenectomía presentaron menor intensidad de dolor del miembro inferior seleccionado, tanto en reposo como en movimiento durante el postoperatorio, en comparación con los que no se les infiltró nada.
Recent studies emphasise the presence of severe pain in the lower extremities post-saphenectomy. Although local infiltration in the treatment of surgical pain is widespread in many surgeries, it has not been used in coronary artery bypass grafting so far. The aim of this study was to evaluate the local infiltration of bupivacaine in the management of post-saphenectomy pain.
MethodA prospective study was conducted with two cohorts of patients that were randomly included in two groups: control group (CG) where the surgical wound closure after the saphenectomy was treated in a conventional manner, and the intervention group (GI) where it was infiltrated after the closure with 50mg of bupivacaine throughout the post-saphenectomy surgical wound. The patient profile, iterative variables, and intensity of pain were analysed using a Visual Analogue Scale (VAS). Informed consent was obtained and the data was analysed using the SPSS statistical package version 22.0.
ResultsOn the lower limb selected post-saphenectomy, the CG experienced the greatest severe pain (VAS ≥ 4) at two (P=.043), four (P=.001), and twelve (P=.017) hours post-operative. However, it was the GI that suffered the most complications of the surgical wound (haematomas, P=.016, and (infections, P=.019).
ConclusionsPatients who received an injection of 50mg of bupivacaine into the post-saphenectomy surgical wound presented with a lower intensity pain in the lower limb selected both at rest and with movement during the post-operative period compared to those who did not receive one.
La revascularización coronaria se puede realizar por tratamiento percutáneo que en muchos casos es indicado por la idoneidad de la cirugía coronaria o quirúrgica al ser considerada el estándar del tratamiento efectivo en casos de enfermedad coronaria extensa1. Las Guías clínicas europeas de revascularización remarcan la adecuada selección de los injertos para conseguir una buena durabilidad de la revascularización2. Dentro de los injertos, el gold standard sigue siendo la arteria mamaria interna, aunque también existe una preponderancia en la evidencia científica que avala el empleo del injerto con vena safena (VS)3. Dado que la VS continúa siendo el injerto más empleado en la revascularización de cirugía coronaria, se han desarrollado diversas líneas de investigación encaminadas a la búsqueda de controlar el dolor del paciente4 en las extremidades inferiores postsafecnectomía. Este dolor intenso se define según la International Asociation for Study of Pain como una experiencia sensorial y emocional desagradable asociada con una lesión presente potencial5. Actualmente, existe cierta dificultad en el control del dolor postoperatorio dado los resultados de adherencia en el tratamiento del dolor6, aunque un régimen analgésico multimodal combinado es el mejor enfoque para tratarlos7, incluida la infiltración del agente anestésico bupivacaína al 0,5% en la herida quirúrgica8,9, que según diversos estudios disminuye el dolor y los requerimientos analgésicos10. A pesar de que la infiltración local con bupivacaína en el tratamiento del dolor posquirúrgico está extendido en diferentes especialidades quirúrgicas con resultados beneficiosos tanto para el paciente como para el profesional11, hasta el momento, en cirugía de revascularización coronaria no se ha empleado por lo que tras safenectomía el paciente experimenta dolor intenso en su postoperatorio según la evidencia existente12.
El objetivo del presente trabajo fue evaluar la eficacia de la infiltración local de bupivacaína en el manejo del dolor postsafenectomía.
MétodosEl diseño del estudio fue controlado aleatorizado, con una cohorte prospectiva de pacientes intervenidos de forma programada por nuestro hospital para cirugía de revascularización coronaria en el periodo comprendido del 1 de mayo del 2016 al 1 de mayo del 2017 (ambos inclusive). La razón de asignación de la muestra fue de forma intencionada a simple ciego mediante la aplicación de un muestreo aleatorio sistematizado, donde a la primera paciente seleccionada se otorgó el número «1», asignada al grupo «A» (grupo intervención), donde se infiltró anestésico local (50mg bupivacaína) en la extensión del cierre de la herida quirúrgica del miembro inferior donde se extrajo la VS, mientras que la siguiente paciente se tomó como la número «2» asignada al grupo «B» (grupo control), donde se realizó el cierre de la herida quirúrgica de forma convencional. Así todos los pacientes con números impares fueron los del grupo intervención y los que tenían números pares, los del grupo control. La secuencia aleatoria, la reclusión y la asignación de los pacientes en ambos grupos fueron realizadas por el investigador principal.
Los criterios de inclusión fueron: mayores de 18 años y programados para cirugía de revascularización coronaria con la firma del consentimiento informado tras exposición verbal y por escrito del propósito del estudio. Los criterios de exclusión fueron: deterioro cognitivo incapaz de comunicarse en lengua española o inglesa con antecedentes de reacción alérgica a cualquier tipo de anestésico local, periodo de intubación superior a las primeras 12 h postoperatorias y reintervenidos porque enmascaran los datos recogidos durante dicho periodo. Y aquellos en que no se realizó la extracción de la VS para anastomosis porque no se adecua a los objetivos del presente estudio. Todos los datos se recogieron en el Servicio de Cirugía Cardiovascular y Área del Corazón y en la Unidad de Cuidados Intensivos del hospital. En todo momento, se informó al paciente de forma verbal y por escrito las características propias del estudio que tras aclaración de las dudas que pudieran surgir aceptaron y firmaron el consentimiento informado. De igual forma, se mantuvo la confidencialidad profesional en el tratamiento de la información de los datos de los pacientes al amparo del cumplimiento de la Ley 15/1999 de 13 de diciembre de protección de datos personales y el reglamento que la desarrolla en su Real Decreto 1720/2007 de 21 de diciembre, además de obtener el dictamen favorable por el Comité Ético y de Investigación del hospital.
La preparación quirúrgica de los pacientes en ambos grupos fue similar y de forma convencional bajo el mismo régimen estandarizado de anestesia general, cuya dosis de fármacos por vía intravenosa fue en proporción al peso y las características propias del paciente. Mismo régimen estandarizado de cirugía coronaria (esternotomía media longitudinal para acceder al corazón) con uso de un circuito extracorpóreo (se canuló los grandes vasos previa administración de heparina sódica con tiempos de Hemochron® superior a 200 s), o sin derivación cardiopulmonar (se utilizó el estabilizador cardiaco Octopus®4 de Medtronic [DEMEDIC SA, Buenos Aires, Argentina). Se confeccionó las anastomosis con suficientes garantías de permeabilidad. La finalización de la cirugía se realizó en todos los casos de forma similar, atendiendo al uso o no de un circuito extracorpóreo. Quienes realizaron la práctica de la cirugía coronaria programada para los pacientes de nuestro estudio fueron 2 cirujanos cardiovasculares con los mismos preparativos e idénticas técnicas quirúrgicas empleadas.
La realización de la safenectomía en ambos grupos se hizo bajo la técnica convencional: paciente colocado en posición decúbito supino con la pierna seleccionada semiflexionada, se realizó apertura completa de la piel en todo su trayecto y tras localización de la VS magna distal se comenzó la disección del maléolo hasta la rodilla en el mismo recorrido de la vena. Las ramas colaterales se electrocoagularon con bisturí eléctrico bipolar de baja intensidad o con ligaduras del 4/0 (Premichron®, B/Braun Surgical, SA, Rubí, Barcelona, España). Tras extracción del injerto de VS, se procedió a ligar todas las ramas colaterales bajo un aplicador de múltiples clips para mantenerla permeable en todo su trayecto. Posteriormente, se depositó en suero fisiológico el tiempo necesario hasta la realización de anastomosis. Para el cierre de la herida del miembro inferior seleccionado se suturó con seda muscular del número 0 (Novosin®, B/Braun Surgical, SA, Barcelona, España) con aguja triangular además de grapas, realizando finalmente cura plana con apósito estéril. Además, en el grupo intervención se infiltró 50mg de bupivacaína extendida a lo largo del cierre incisional. Quienes realizaron la extracción y el posterior cierre de la herida quirúrgica de todos los pacientes incluidos fueron el mismo médico residente de cirugía cardiovascular (4 años) y el cirujano adjunto cardiovascular, que utilizaron las mismas técnicas quirúrgicas para el procedimiento de extracción de VS y el cierre de herida. Durante el postoperatorio, se administró en ambos grupos el mismo protocolo analgésico por vía intravenoso estandarizado para nuestro servicio.
Los pacientes fueron sometidos a la evaluación de la intensidad del dolor en su miembro inferior, en que se realizó la safenectomía, a través de la escala visual analógica (EVA) graduada numéricamente, donde «0» no indica dolor y «10» indica dolor insoportable, señalando en una regla de 10cm el punto que según el paciente represente el dolor que manifiesta. EVA ≥ 4 fue considerado dolor intenso13. Se evaluó el dolor del paciente en reposo (dolor estático, es decir, sin movimiento) y movimiento (dolor dinámico, como, por ejemplo, cambio postural o ligera flexión de los miembros inferiores). Quien utilizó la escala EVA fue el investigador principal donde observador y pacientes estaban cegados al tipo de estrategia determinada.
Las variables del estudio fueron: edad (años), sexo (género), peso (kg) y talla (cm) antes de entrar en el quirófano a través de su historia clínica digitalizada. Variables de cirugía coronaria con necesidad de utilizar un circuito extracorpóreo y sin necesidad: tiempo de cirugía (minutos), tiempo de extracción y disección de la VS (minutos) al término de la cirugía programada mediante la hoja quirúrgica digitalizada propia de nuestro hospital. Intensidad del dolor (reposo y movimiento) a las 2, 4 y 12 h del postoperatorio a través de la escala EVA. Complicaciones de la herida quirúrgica (hematomas e infección) del miembro seleccionado y rescate de analgésico durante el postoperatorio mediante la recogida de datos en su historia clínica digitalizada y en el documento ad hoc.
Para la estimación del cálculo muestral se tuvo que realizar previamente un estudio piloto al no existir evidencia que determine el dolor postsafenectomía. Por ello, se obtuvo la intensidad del dolor de la herida quirúrgica en el grupo control con una EVA ≥ 4 tras los resultados del estudio piloto. Por lo que la exposición se consideró un factor de riesgo si el riesgo relativo es al menos de 4, con una significación de un 5% y una potencia estadística del 80%. Usando una razón de un expuesto por cada no expuesto. Se utilizó el programa estadístico EPIDAT para el cálculo de la «n»’ de cada grupo según los valores anteriormente mencionados.
Los análisis estadísticos utilizados se expresaron mediante frecuencia absolutas o relativas, porcentaje (%), medias de tendencia central (media) y desviación estándar (DE). Las variables categóricas fueron comparadas mediante el test de la chi al cuadrado y las continuas mediante el test de la t de Student. Se consideró significativo un valor p inferior a 0,05.
ResultadosDel 100% de los pacientes (n=143) programados para cirugía de revascularización coronaria, se incluyó el 67% de los pacientes (n=96), de los cuales el 39% de ellos (n=56) pertenecían al grupo control y el 28% restantes (n=40) al grupo intervención.
Se excluyó del estudio al 37% de los pacientes (n=47) por presentar un 15% (n=21) intubación prolongada durante las 12 primeras horas, un 4% (n=6) motivos de reintervención quirúrgica y un 14% (n=20) por no proceder a la extracción y la disección de la VS.
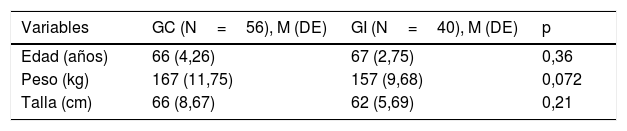
En cuanto a las características de los pacientes, predominó el sexo masculino, siendo en el grupo control del 75% de los pacientes (n=42) y con un 25% (n=14) del sexo femenino. En el grupo intervención, el 70% de los pacientes (n=28) fueron masculino y un 30% (n=12) del sexo femenino (p=0,09). El perfil de los pacientes estudiados se presenta en la tabla tabla 1.
Perfil de los pacientes estudiados en ambos grupos
| Variables | GC (N=56), M (DE) | GI (N=40), M (DE) | p |
|---|---|---|---|
| Edad (años) | 66 (4,26) | 67 (2,75) | 0,36 |
| Peso (kg) | 167 (11,75) | 157 (9,68) | 0,072 |
| Talla (cm) | 66 (8,67) | 62 (5,69) | 0,21 |
GC: grupo control; GI: grupo intervención; M (DE): media (desviación estándar).
Existieron diferencias estadísticamente significativas cuando p<0,05.
Respecto a la utilización de un circuito extracorpóreo para cirugía coronaria, en el 98% de los pacientes (n=94) se utilizó la máquina extracorpórea con uno tiempo de cirugía que varió en el grupo control de 237±127 min y en el grupo intervención de 226±93 min (p=0,360). En un 100% de los pacientes (n=96) se diseccionó y extrajo la VS del miembro seleccionado, en un tiempo que en el grupo control de 63±20 min y en el grupo intervención de 80±27 min (p=0,288).
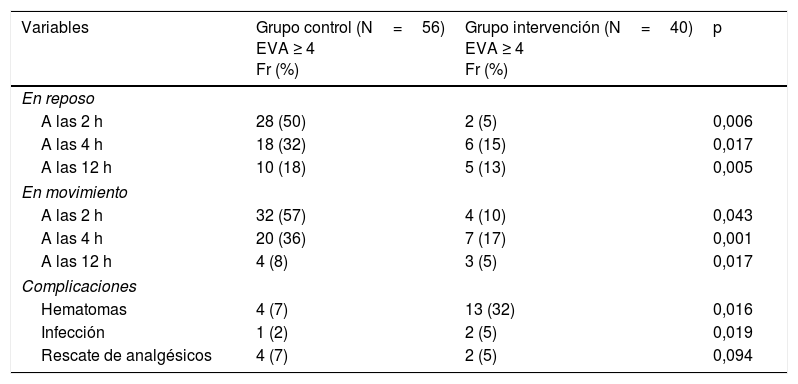
En relación con las variables del postoperatorio, la intensidad del dolor del miembro inferior seleccionado postsafenectomía fue mayor en el grupo control que en el grupo intervención, tanto en reposo, con una EVA ≥ 4 en el 50% de los pacientes (n=28) a las 2 h, el 32% de los pacientes (n=18) y 18% de los pacientes (n=10) a las 12 h del postoperatorio, como en movimiento, con un EVA ≥ 4 en el 57% de los pacientes (n=32) a las 2 h, el 36% de los pacientes (n=20) a las 4 h y solo el 8% de los pacientes (n=4) a las 12 h del postoperatorio. Sin embargo, el grupo intervención reportó mayores complicaciones de la herida quirúrgica frente al grupo control, con un 32% de los pacientes (n=13) que presentaron hematomas y el 5% de los pacientes (n=2) que presentó infección. No hubo diferencias significativas en el rescate de analgésicos para paliar el dolor entre los 2 grupos (tabla 2).
Intensidad del dolor, complicaciones de la herida quirúrgica y rescate de analgésicos de los participantes durante el postoperatorio
| Variables | Grupo control (N=56) EVA ≥ 4 Fr (%) | Grupo intervención (N=40) EVA ≥ 4 Fr (%) | p |
|---|---|---|---|
| En reposo | |||
| A las 2 h | 28 (50) | 2 (5) | 0,006 |
| A las 4 h | 18 (32) | 6 (15) | 0,017 |
| A las 12 h | 10 (18) | 5 (13) | 0,005 |
| En movimiento | |||
| A las 2 h | 32 (57) | 4 (10) | 0,043 |
| A las 4 h | 20 (36) | 7 (17) | 0,001 |
| A las 12 h | 4 (8) | 3 (5) | 0,017 |
| Complicaciones | |||
| Hematomas | 4 (7) | 13 (32) | 0,016 |
| Infección | 1 (2) | 2 (5) | 0,019 |
| Rescate de analgésicos | 4 (7) | 2 (5) | 0,094 |
EVA: escala visual analógica (0 indica no dolor y 10 indica dolor insoportable); Fr (%): frecuencias absolutas (porcentajes).
Existieron diferencias estadísticamente significativas entre los grupos p<0,05.
Los resultados del presente estudio permitieron comparar la intensidad del dolor del miembro seleccionado tras la extracción y la disección de la VS mediante la escala EVA a las 2, 4 y 12 horas del postoperatorio, tanto en el grupo control como en el grupo intervención, cuyos resultados clave exponen una disminución considerable de la intensidad del dolor en el grupo intervención durante su postoperatorio. Su justificación se debe al uso del fármaco anestésico infiltrado en la herida quirúrgica, cuya acción produce un bloqueo reversible de la conducción de los impulsos nerviosos impidiendo la propagación de los potenciales de acción en los axones de las fibras nerviosas autónomas, sensitivas y motoras, disminuyendo así el dolor en el paciente.
Cierto es que los tiempos de extracción y disección de la VS entre los grupos son diferentes, pero el hecho de no realizar el procedimiento un único y mismo cirujano cardiovascular pudiera incidir en los tiempos quirúrgicos, ya que las habilidades y la pericia profesional de cada profesional desempeñan un importante papel en los tiempos. Además, la disección y extracción de la VS puede incidir en los tiempos quirúrgicos debido a su disposición anatómica y localización en cada paciente.
La evidencia señala que la VS se considera idónea para la revascularización coronaria al presentar un único compartimento sin afluente paralelo14, además de la permeabilidad significativa que proporciona15,16, con resultados clínicos satisfactorios para el inicio, el medio y el largo plazo17. Sin embargo, son escasos los estudios que señalan el dolor del paciente tras su extracción y disección. Un estudio de Eisenberg et al.18 analizó la prevalencia y las características del dolor de los pacientes tras injertos; el mismo concluye que el dolor está presente durante meses e incluso años interfiriendo en las actividades la vida diaria de manera importante para algunos pacientes. Los mismos resultados exponen otras investigaciones19. Otros estudios incorporan nuevas técnicas de extracción y disección de la VS, como la técnica videoasistida, que indudablemente aporta beneficios para los pacientes al plantear una menor agresión y una menor incidencia de complicaciones sépticas y no sépticas de la herida20. Pero en ninguno de ellos estudian la intensidad del dolor del miembro inferior seleccionado postsafenectomía en pacientes de cirugía cardiaca. Actualmente, existen investigaciones que tratan el dolor localizado posquirúrgico con agentes infiltrantes anestésicos, como el de Chou et al.21 y el de Huang y Sakat22 en pacientes cardiacos, o Contreras et al.23 en pacientes de otras especialidades quirúrgicas, pero no existen datos que pongan de manifiesto el uso de infiltración local de bupivacaína en la herida quirúrgica postsafenectomía en respuesta al dolor posquirúrgico.
El estudio de Cenk et al.24 destaca que la bupivacaína al 0,5% proporciona un inicio más rápido de bloqueo sensorial y motor en comparación con otros fármacos infiltrante anestésicos. Aunque Liisananttii et al.25 no hallaron diferencias significativas en el uso de bupivacaína al 0,5% con respecto a otros agentes anestésicos infiltrantes en los minutos 5, 10 y 15, y solo destacaron que hubo una tasa más elevada de obtención de anestesia al nivel deseado en el minuto 45 con bupivacaína. Recientemente, Can y Bilgin26, en su estudio aleatorizado y prospectivo donde se incluyó a 90 pacientes distribuidos en 3 grupos, donde a uno de ellos se infiltró bupivacaína al 0,5% en la herida quirúrgica como tratamiento para determinar los efectos indeseados tras su administración, concluyeron que no obtuvieron efectos adversos y añadieron que su uso fue efectivo y seguro. Las mismas conclusiones exponen otras investigaciones27,28. Sin embargo, en ninguno de esos estudios se determinaron la intensidad del dolor del paciente, cuándo se les infiltraba y cuándo no, por lo que se limitan solo a destacar las propiedades del fármaco sin identificar cuándo acontece con mayor o menor efectividad.
Hasta el momento, la infiltración de bupivacaína al 0,5% es efectiva según la evidencia existente, pero no existen estudios que la asocien directamente con la intensidad del dolor en pacientes que han sufrido una extracción y disección de su VS para injerto coronario, y sobre todo evaluando las primeras horas del postoperatorio, tal y como muestra nuestra investigación.
La falta de conocimiento científico en esta materia deja al descubierto que los pacientes intervenidos de cirugía de revascularización coronaria, a los que se les extraen injertos de la VS, presentarán dolor postoperatorio severo, tal y como muestra el estudio de Roca et al.5, lo que dificulta una pronta recuperación del paciente ya que, según Pelaez et al.29, el mantener el dolor agudo aumenta la prevalencia de que se vuelva crónico, además de provocar liberación de catecolaminas por medio del estímulo nociceptivo del propio paciente, lo que incrementa el gasto cardiaco, aumenta el consumo de oxígeno y dificulta los movimientos respiratorios, con el riesgo de aparición de atelectasias30, lo que dificulta la correcta evolución del paciente31.
Basado en nuestros resultados, se recomienda el uso de infiltración local de 50mg de bupivacaína en la extensión de la herida quirúrgica postsafenectomía en respuesta al dolor del paciente durante el postoperatorio, ya que existen diferencias estadísticamente significativas entre los grupos estudiados. Además, su uso permite obtener un beneficio doble; por un lado, a nivel cardiorrespiratorio, donde disminuye el consumo miocárdico de oxígeno a consecuencia del aumento del gasto cardiaco, evitando la aparición de posibles atelectasias según lo anteriormente detallado, y por otro lado, se beneficia el paciente, ya que al experimentar menor dolor inhibe la respuesta nociceptiva propia para combatir el dolor.
Sin embargo, se alerta que el grupo que presentó mayores complicaciones de la herida quirúrgica fue grupo intervención (grupo al que se infiltró bupivacaína), reportando hematomas e infección, aunque de incidencia fútil. A pesar de que la infiltración de bupivacaína en la herida quirúrgica ha sido documentada como analgésico eficaz y se usa ampliamente para el alivio del dolor postoperatorio, los efectos del propio fármaco para la infiltración en la incisión quedan limitados con resultados controversiales32. El hecho de reportar un aumento de complicaciones en el grupo intervención puede justificarse en que existen estudios experimentales que indican que la bupivacaína inhibe la síntesis de colágeno causando edema, vascularización e inflamación significativas, por lo que existe un aumento de riesgo de complicación de la herida quirúrgica, aunque los investigadores enfatizan que estos resultados necesitan ser verificados33.
No obstante, nuestra conclusión aporta que los pacientes a los que se infiltraron 50mg de bupivacaína extendida en la herida quirúrgica postsafenectomía presentaron menor intensidad de dolor del miembro inferior seleccionado, tanto en reposo como en movimiento durante el postoperatorio respecto de aquellos que no se infiltraron.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesNinguno.