El medidor de flujo permite conocer 2 parámetros: el flujo medio del bypass coronario y el índice de pulsatilidad. Estos 2 parámetros, cuando están alterados, pueden indicar una estenosis de la anastomosis del bypass distal. Factores distintos de la suficiencia de la anastomosis, como la calidad de lecho coronario, pueden condicionar el flujo del bypass y dificultar su interpretación. El objetivo de nuestro estudio es analizar los predictores independientes del flujo de los bypass aorto-coronarios.
MétodosRecogimos de forma retrospectiva una serie consecutiva de 90 pacientes intervenidos de revascularización miocárdica aislada por el mismo cirujano desde enero del 2014 hasta agosto del 2016. A partir de esta serie, elaboramos una base de datos electrónica donde cada registro correspondía a un injerto. Construimos, por lo tanto, una base de datos de 185 injertos. De estos, 8 injertos no fueron analizados por no haberse medido el flujo correctamente. Por los tanto, los valores de flujo y de índice de pulsatilidad de 177 injertos fueron utilizados para nuestro análisis estadístico.
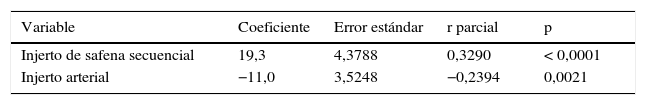
ResultadosEl análisis de regresión lineal múltiple detectó 2 predictores independientes del flujo de los bypasses: injerto de vena safena secuencial (valor r parcial: 0,32; p < 0,0001) e injerto arterial (valor r parcial: –0,23; p 0,0021). Por lo tanto, nuestro modelo objetivó una correlación directa entre la utilización de injerto de safena con técnica secuencial y flujo del bypass, y una correlación inversa entre la utilización de injerto arterial y flujo del bypass.
ConclusionesLos predictores del flujo de los bypasses aorto-coronarios son la utilización de un injerto arterial (coeficiente negativo) y la utilización de un injerto venoso secuencial (coeficiente positivo). Nuestro modelo estadístico no ha identificado como predictor el SYNTAX score ni analizado como variable continua ni como variable dicotómica.
The transit time flowmeter allows knowing two parameters: the mean bypass flow and pulsatility index. These two parameters, when altered, can suggest a bypass stenosis. Factors other than the permeability of the anastomosis, as the quality of coronary bed, may alter the flow of bypass and complicates its interpretation. The aim of our study is to analyze the independent predictors of the mean flow of aorto-coronary bypasses.
MethodsWe collected a retrospective series of 90 consecutive patients who underwent isolated coronary artery bypass grafting by the same surgeon from January 2014 to August 2016. From this series, we have built an electronic database where each record corresponds to one graft and the correspondent single or multiple bypasses. Therefore, we built a database including 185 grafts. Of these, 8 grafts were not analyzed because the flow had not been correctly measured. Therefore, the flow and pulsatility index values of 177 grafts were available for our statistical analysis.
ResultsMultiple linear regression analysis detected two independent predictors of bypass flow: sequential saphenous vein graft (partial r value: 0.32; P<.0001) and arterial graft (partial r-value: –0.23; P=.0021). Therefore, our model showed a direct correlation between use of saphenous graft with sequential technique and bypass flow and an inverse correlation between arterial graft use and bypass flow.
ConclusionsThe predictors of aorto-coronary bypass flow are the use of an arterial graft (negative coefficient) and the use of a sequential venous graft (positive coefficient). Our statistical model has not identified as a predictor the SYNTAX score nor analyzed as a continuous variable nor as a dichotomous variable.
El SYNTAX score es un parámetro elaborado desde el SYNTAX Trial1, un estudio aleatorizado diseñado para comparar resultados de revascularización percutánea frente a cirugía de revascularización miocárdica en el tratamiento de la enfermedad arterial coronaria. El SYNTAX score proporciona un valor que refleja, considerando parámetros de la anatomía coronaria evaluada mediante angiografía, la severidad de la enfermedad arterial coronaria del paciente2. Básicamente, el SYNTAX score es actualmente utilizado para estratificar pacientes con enfermedad coronaria, siendo aquellos con score más altos, y por tanto, reflejo de una enfermedad coronaria severa, más probablemente beneficiados de revascularización quirúrgica que de tratamiento percutáneo.
Unos de los parámetros clave en la realización de una correcta revascularización quirúrgica es la elaboración de bypass perfectamente permeables. El dispositivo más usado en quirófano para comprobar la permeabilidad del bypass es el medidor de flujo (MF)3, cuya utilización está recomendada por la guía europea de revascularización miocárdica4. Se trata de una sonda con 2 transductores de ultrasonidos y un reflector acústico que analiza el tiempo que tarda la sangre en pasar entre los dos transductores. El MF permite conocer, entre otros, 2 parámetros fundamentales: el flujo medio del bypass, cuya curva suele ser prevalentemente diastólica, y el índice de pulsatilidad (IP), que es la diferencia entre el flujo máximo y el mínimo dividida por el flujo medio5. El IP proporciona una estimación de la resistencia al flujo ofrecida por el injerto y por el vaso diana6. Valores de flujo medio inferiores a 15-20ml/min y de IP por encima de 5 pueden indicar una estenosis del bypass6,7. Factores distintos de la permeabilidad de la anastomosis, como la calidad de lecho coronario, pueden alterar el flujo del bypass y dificultar su interpretación8. El objetivo de nuestro estudio es analizar los predictores del flujo del bypass aorto-coronario y analizar el posible impacto del SYNTAX score.
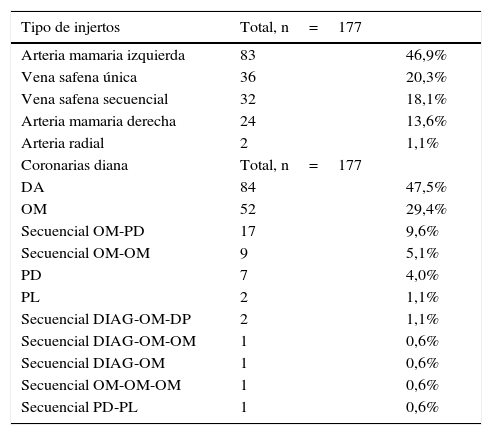
MétodosPacientesRecogimos una serie consecutiva retrospectiva de 90 pacientes intervenidos en nuestro centro hospitalario de cirugía de revascularización miocárdica aislada electiva o urgente o emergente, desde enero del 2014 hasta mayo del 2016 por el mismo cirujano (S. U.). Los datos clínicos y quirúrgicos fueron obtenidos de las bases de datos electrónica del Servicio de Cirugía Cardiaca del Hospital Universitario Doctor Negrín. De esta serie consecutiva de pacientes, hemos elaborado una base de datos electrónica donde cada registro correspondía a un injerto. Hemos, por lo tanto, obtenido una base de datos de 185 injertos. De estos, 8 injertos no fueron analizados por no haberse medido correctamente el flujo con el MF. Por los tanto, los valores de flujo y de IP de 177 injertos fueron utilizados para nuestro análisis estadístico. El tipo de injerto usado y las características clínicas de los pacientes se resumen en las tablas 1 y 2, respectivamente.
Tipo de injertos utilizados y coronarias diana
| Tipo de injertos | Total, n=177 | |
|---|---|---|
| Arteria mamaria izquierda | 83 | 46,9% |
| Vena safena única | 36 | 20,3% |
| Vena safena secuencial | 32 | 18,1% |
| Arteria mamaria derecha | 24 | 13,6% |
| Arteria radial | 2 | 1,1% |
| Coronarias diana | Total, n=177 | |
| DA | 84 | 47,5% |
| OM | 52 | 29,4% |
| Secuencial OM-PD | 17 | 9,6% |
| Secuencial OM-OM | 9 | 5,1% |
| PD | 7 | 4,0% |
| PL | 2 | 1,1% |
| Secuencial DIAG-OM-DP | 2 | 1,1% |
| Secuencial DIAG-OM-OM | 1 | 0,6% |
| Secuencial DIAG-OM | 1 | 0,6% |
| Secuencial OM-OM-OM | 1 | 0,6% |
| Secuencial PD-PL | 1 | 0,6% |
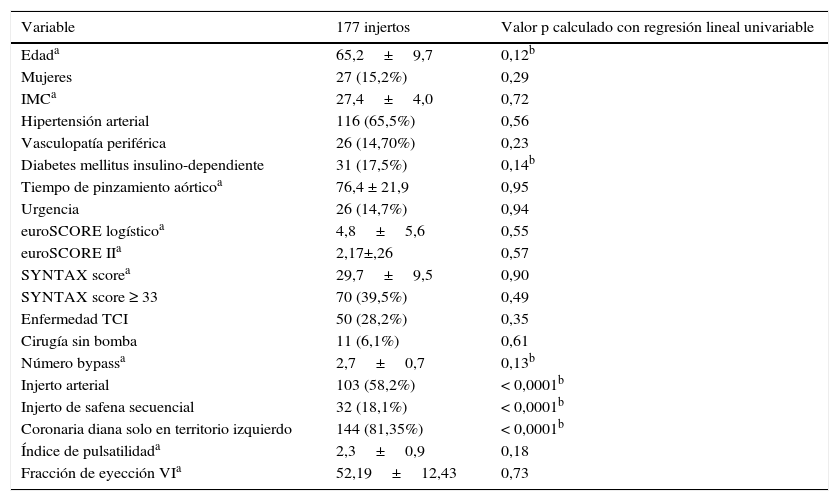
Distribución de los datos preoperatorios y operatorios
| Variable | 177 injertos | Valor p calculado con regresión lineal univariable |
|---|---|---|
| Edada | 65,2±9,7 | 0,12b |
| Mujeres | 27 (15,2%) | 0,29 |
| IMCa | 27,4±4,0 | 0,72 |
| Hipertensión arterial | 116 (65,5%) | 0,56 |
| Vasculopatía periférica | 26 (14,70%) | 0,23 |
| Diabetes mellitus insulino-dependiente | 31 (17,5%) | 0,14b |
| Tiempo de pinzamiento aórticoa | 76,4 ± 21,9 | 0,95 |
| Urgencia | 26 (14,7%) | 0,94 |
| euroSCORE logísticoa | 4,8±5,6 | 0,55 |
| euroSCORE IIa | 2,17±,26 | 0,57 |
| SYNTAX scorea | 29,7±9,5 | 0,90 |
| SYNTAX score ≥ 33 | 70 (39,5%) | 0,49 |
| Enfermedad TCI | 50 (28,2%) | 0,35 |
| Cirugía sin bomba | 11 (6,1%) | 0,61 |
| Número bypassa | 2,7±0,7 | 0,13b |
| Injerto arterial | 103 (58,2%) | < 0,0001b |
| Injerto de safena secuencial | 32 (18,1%) | < 0,0001b |
| Coronaria diana solo en territorio izquierdo | 144 (81,35%) | < 0,0001b |
| Índice de pulsatilidada | 2,3±0,9 | 0,18 |
| Fracción de eyección VIa | 52,19±12,43 | 0,73 |
EPOC: enfermedad pulmonar crónica obstructiva; IMC: índice de masa corporal; TCI: tronco común izquierdo; VI: ventrículo izquierdo.
La vía de abordaje quirúrgico fue la esternotomía longitudinal media. La cirugía fue realizada mediante circulación extracorpórea en el 94% de los casos, en los cuales se mantuvo un flujo entre 2,4-3,2 l/m2/min bajo hipotermia sistémica ligera (34°C). El volumen de cebado fue de un litro. Como norma general, el nivel de hemodilución mínimo fue del 20% de hematocrito. La protección miocárdica fue llevada a cabo mediante cardioplejía hemática fría anterógrada y retrógrada de forma intermitente, y frío local mediante suero congelado. El 6% de los casos restantes en los que no se utilizó circulación extracorpórea, los procedimientos quirúrgicos y anestésicos fueron realizados acorde a los protocolos descritos en www.opcab.eu.
Como norma, en los pacientes en los que se utilizaron las 2 arterias mamarias internas, estas se destinaron a ramas de la coronaria izquierda realizando bypass no secuenciales (arteria mamaria izquierda a descendente anterior y arteria mamaria derecha a rama marginal). La arteria mamaria derecha se ha anastomosó proximalmente a la arteria mamaria izquierda, a la aorta ascendente o se utilizó in situ, tal como se describe en la tabla 1. En el caso de pacientes donde se prefirió usar solo una arteria mamaria, la vena safena fue usada para revascularizar el territorio lateral o posterior de forma no secuencial o secuencial.
El flujo de lo bypass se midió con el MF (Medistim BF 2004, Medistim, Oslo, Noruega) en 2 ocasiones: une vez completadas todas las anastomosis, estando todavía el paciente en circulación extracorpórea, y una vez terminada la circulación extracorpórea. Los valores de esta última medición fueron introducidos en nuestra base de datos y se obtuvieron manteniendo una presión arterial media de entre 70 y 80mmHg. Para que la medición haya sido definida como correcta, la sonda del MF tuvo que acoplarse correctamente con el injerto. La sonda del MF se aplicó en todos los bypass en el segmento medio del injerto, y en el caso de bypass secuencial, la medición se realizó solo proximalmente a la primera anastomosis distal. En 4 pacientes fue necesario, debido a valores de flujo inadecuados, rehacer la anastomosis distal del bypass. En estos casos los valores de flujo y de pulsatilidad introducidos en nuestra base de datos fueron los derivados de la medición realizada después de la corrección de las anastomosis.
Análisis estadísticoLas variables continuas fueron expresadas como media ± desviación estándar. Las variables dicotómicas se indicaron como frecuencia absoluta (porcentaje). El flujo medio de los bypasses se analizó como variable continua. El SYNTAX score se analizó como variable continua y como variable categórica dicotómica: SYNTAX score ≥ 33 (que define en el estudio SYNTAX la categoría de paciente de alto riesgo2) y SYNTAX score < 33. Con respecto al territorio revascularizado, los injertos se dividieron en los que revascularizaban exclusivamente la cara izquierda («coronaria diana solo en territorio izquierdo») y los que revascularizaban el territorio derecho o ambos territorios.
En primer lugar, todas las variables descritas en la tabla 2 fueron analizadas, mediante regresión lineal univariable, siendo la variable dependiente el flujo del bypass. Todas las variables con un valor p ≤ 0,15 en análisis univariable fueron introducidas en un modelo de regresión lineal múltiple, hacia adelante (valor de corte para el ingreso de la variable en el modelo p<0,15; valor de corte para la eliminación de la variable del modelo p>0,20) (tabla 3).
De este modelo de regresión lineal múltiple obtuvimos los predictores independientes del flujo del bypass coronario. El valor R2 se usó para la evaluar la bondad de ajuste del modelo de regresión múltiple. Un valor de p ≤ 0,05 se consideró estadísticamente significativo. Los análisis estadísticos fueron desarrollados usando MedCalc Statistical Software versión 16.1 (MedCalc Software bvba, Ostend, Bélgica; https://www.medcalc.org; 2016).
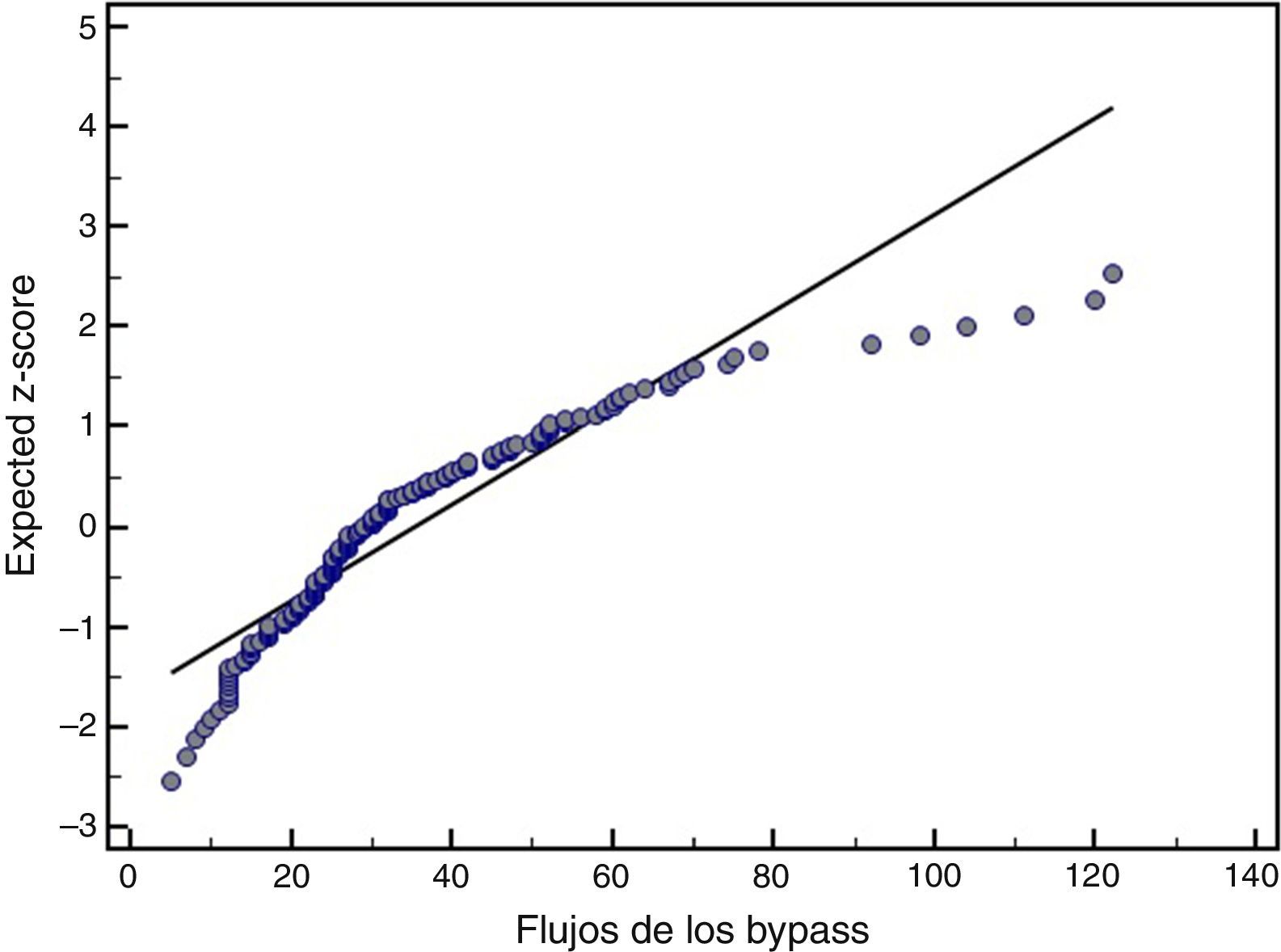
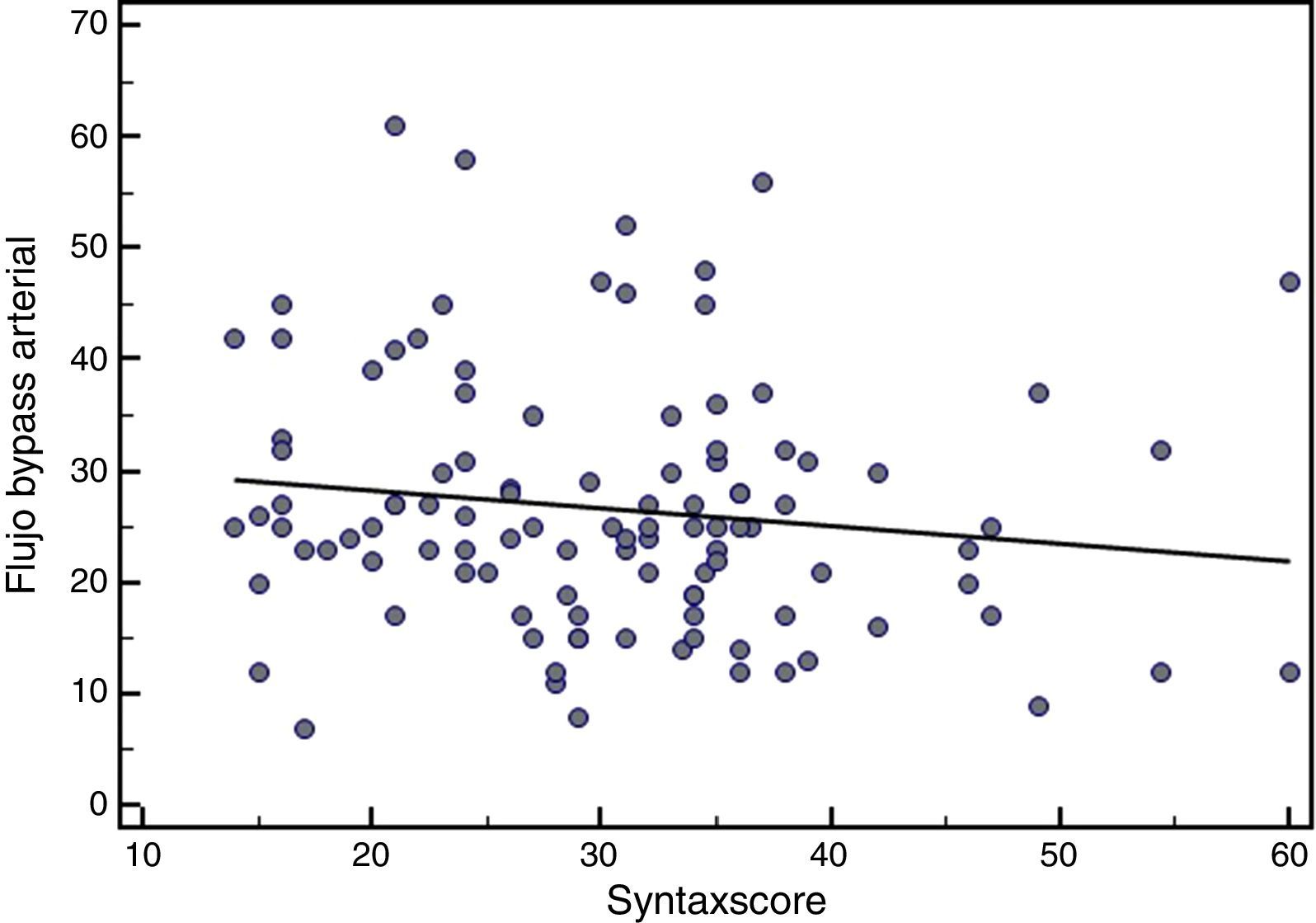
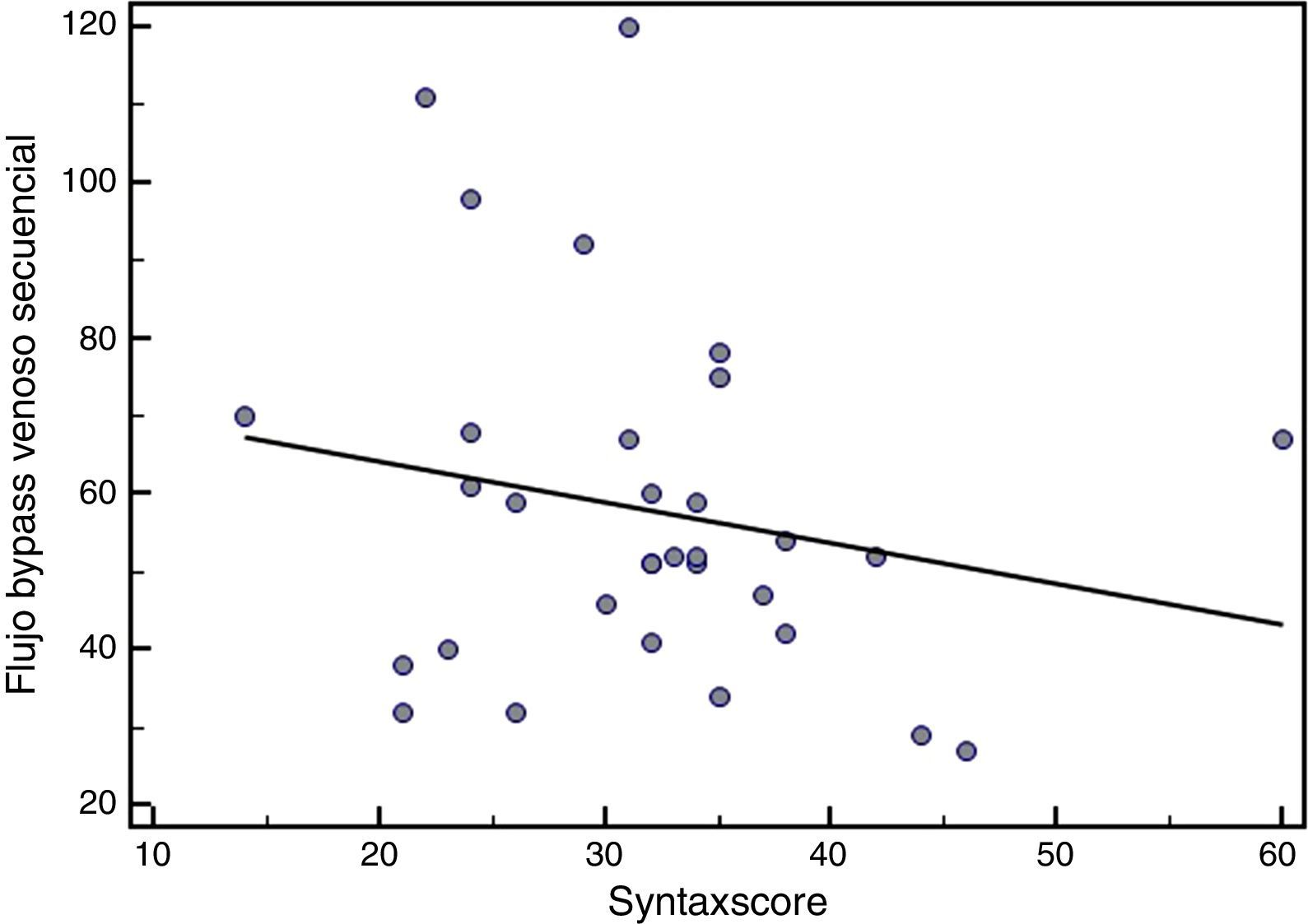
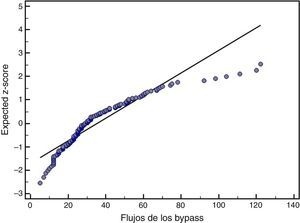
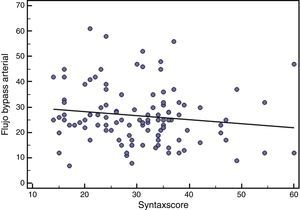
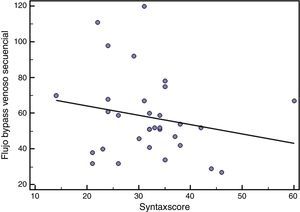
ResultadosLa mortalidad a los 30 días fue del 1,2% (n=1). El flujo medio de los 177 injertos fue de 34,8±20,8ml/min. La figura 1 muestra su distribución normal. El IP medio de los injertos fue de 2,2±0,9. El análisis mediante diagrama de dispersión (figs. 2 y 3) documentó una correlación inversa entre SYNTAX score y el flujo de injertos arteriales y venosos secuenciales.
El análisis de regresión múltiple detectó 2 predictores independientes del flujo de los bypasses: injerto de vena safena secuencial (valor r parcial: 0,32; p < 0,0001) e injerto arterial (valor r parcial: –0,23; p = 0,0021). Por lo tanto, nuestro modelo objetivó una correlación directa entre la utilización del injerto de safena con técnica secuencial y flujo del bypass, y una correlación inversa entre la utilización del injerto arterial y flujo del bypass.
El SYNTAX score analizado como variable continua (p = 0,90) o como variable dicotómica (SYNTAX score ≥ 33: p = 0,49) mediante la regresión lineal univariable, no se asoció de forma estadísticamente significativa al flujo coronario, por lo tanto, no se introdujo en el modelo de regresión lineal múltiple.
DiscusiónEl flujo de los bypasses aorto-coronarios depende de una serie de factores, algunos propios del injerto, como su diámetro o su composición histológica, otros relacionados con el territorio coronario donde se realiza la anastomosis, como el run-off distal, la presencia de flujo competitivo o problemas técnicos de la anastomosis8. Nuestro estudio ha documentado que existe una correlación inversa entre el flujo del bypass e injertos arteriales. Lo que no nos sorprende si consideramos que los injertos arteriales suelen tener un calibre menor de los injertos venosos y presentan una pared con un componente muscular liso, sensible a mediadores vasoactivos, bien demarcada por la lámina elástica interna y externa9. Estos 3 componentes, muy poco representados en el conducto venoso, confieren a los injertos arteriales una capacidad activa de adaptarse al flujo hemático ofreciendo al mismo una resistencia variable en función de estímulos vasoactivos, lo que no ocurre en los injertos venosos10, considerados como conductos «pasivos». Estos 2 factores, menor calibre y mayor desarrollo del componente muscular liso de los injertos arteriales, podrían explicar por qué estos proporcionan menores flujos que los de safena. Nuestro análisis ha además documentado una correlación directa entre flujo del bypass e injerto de vena secuencial. El hecho que los injertos de vena safena secuenciales se asocien a un mayor flujo ha sido previamente documentado en literatura11. Si consideramos constante la resistencia ofrecida al flujo hemático por un injerto venoso (ya que su calibre no se modifica en relación a estímulos vasoactivos), el mayor determinante de su flujo será el diámetro del mismo y la resistencia ofrecida por el lecho coronario. Por lo tanto, a mayor número de anastomosis realizadas con el mismo injerto, corresponde una menor resistencia periférica, y, consecuentemente, un mayor flujo. Este factor hemodinámico podría explicar los mejores resultados en términos de permeabilidad a largo plazo de los injertos secuenciales11 comparados con los no secuenciales y sus excelentes resultados clínicos12.
Son múltiples los factores determinantes de flujo del bypass que no dependen de los injertos. Entre ellos, los más importantes son factores cuantitativos del lecho coronario (diámetro de la coronaria, extensión de su territorio distal), factores cualitativos (severidad de le enfermedad de la arteria coronaria), hemodinámicos (presencia de flujo competitivo) y técnicos (ejecución de la anastomosis)13.
De todos estos factores, el SYNTAX score ofrece una puntuación que podría reflejar los factores cualitativos de la coronaria diana14,15. Para proceder con el cálculo del SYNTAX score hay que considerar significativa toda lesión superior al 50% que se visualice en una arteria con diámetro superior a 1,5mm (http://www.syntaxscore.com/). Las lesiones están evaluadas según la clasificación del American College of Cardiology/American Heart Association16. Puntos clave del proceso de puntuación es la identificación de lesiones que producen oclusiones totales, que involucren los ostium coronarios, bifurcaciones o trifurcaciones o que se asocian a calcificaciones, tortuosidad del vaso o trombos. En nuestro estudio, sin embargo, el análisis de regresión lineal no ha detectado algún impacto del SYNTAX score, ni analizado como variable continua ni como variable categórica, sobre el flujo del bypass, lo que podría indicar que el SYNTAX score, diversamente de lo que ocurre en la revascularización percutánea, no afecta a la calidad de la revascularización quirúrgica.
LimitacionesNuestro estudio ha analizado una muestra relativamente limitada de injertos, no ha evaluado el posible impacto de factores relacionados con la arteria coronaria diana (porcentaje de estenosis, diámetro de la coronaria en el sitio de la anastomosis) y no ha analizado la posible asociación entre flujo coronario e incidencia de estenosis del bypass durante el seguimiento.
ConclusionesLos predictores del flujo de los bypasses aorto-coronarios son la utilización de un injerto arterial (coeficiente negativo) y la utilización de un injerto venoso secuencial (coeficiente positivo). Nuestro modelo estadístico no ha identificado como predictor el SYNTAX score ni analizado como variable continua ni como variable dicotómica.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores del presente estudio no tienen conflicto de intereses.