Analizar la morfología del arco aórtico en pacientes sometidos a cirugía híbrida por patología de arco y aorta torácica descendente, así como evaluar los resultados a corto y a medio plazo.
Pacientes y métodosCatorce pacientes consecutivos (78,6% varones, con edad media de 61,9±10,1años y euroSCORE logístico medio 19,2±9,6%) operados mediante cirugía híbrida (derivación carótido-subclavia izquierda, 7casos; translocación de 2troncos, 2casos; translocación de 3troncos, 5casos) fueron incluidos en el estudio. Se analizaron los diámetros aórticos, la longitud de las zonas de anclaje, la distancia entre troncos supraaórticos, la angulación y el radio de curvatura del arco.
ResultadosLa longitud media de la zona de anclaje proximal aumentó de 5,9±5,3 a 36,3±9,6mm tras cirugía de troncos supraaórticos. El radio de curvatura medio del arco fue de 48,7±19,9mm con angulación media de 84,6±29,1°. Cuatro pacientes presentaron un radio de curvatura <40mm. No hubo mortalidad intrahospitalaria ni complicaciones neurológicas. La supervivencia media fue del 100% a 1 y 2años y del 83,3% a 4años. La supervivencia libre de endofugas fue del 100% a un año y del 90,9% a 2 y 4años. El diámetro aórtico máximo disminuyó de 65,2±17,9 a 50,9±14,2mm.
ConclusionesUna adecuada valoración morfológica del arco aórtico es fundamental para seleccionar la mejor estrategia híbrida y prevenir la aparición de complicaciones en el implante de endoprótesis a ese nivel. Una angulación <70° y un radio de curvatura <40mm del arco aórtico recomienda incrementar la longitud de la zona de anclaje proximal a >2,5cm para evitar defectos de aposición en la curvatura menor del arco y endofugas tipoia.
To analyze the morphology of the aortic arch in patients undergoing hybrid surgery due to pathology of the aortic arch and descending thoracic aorta, as well as to assess the short and mid-term outcomes.
Patients and methodsThe study enrolled fourteen consecutive patients (78.6% males, mean age 61.9±10.1 years and mean logistic euroSCORE 19.2%±9.6%) operated on with hybrid techniques (left carotid-subclavian by-pass, 7cases; 2supraaortic vessels transposition, 2cases; total supraaortic debranching, 5cases). All aortic diameters, lengths of landing zones, distances between supraaortic vessels, aortic arch angulation and curvature ratio were assessed.
ResultsMean proximal landing zone lengths increased from 5.9±5.3mm to 36.3±9.6mm after the supraaortic vessels surgery. Mean arch curvature ratio was 48.7±19.9mm, whereas mean angulation was 84.6±29.1°. Four patients presented a curvature ratio <40mm. There was neither in-hospital mortality nor neurological complications. Kaplan-Meier survival rate was 100% at 1 and 2years and 83.3% at 4years. Freedom from redo and endoleak was 100% at 1year and 90.9% at 2 and 4years. Maximum aortic diameter decreased from 65.2±17.9mm to 50.9±14.2mm.
ConclusionsAn adequate assessment of the aortic arch morphology is of paramount importance in order to select the best hybrid approach in patients sustaining complex arch pathologies, as well as to avoid complications related to aortic endografting at the level of the aortic arch. In those cases with an aortic arch angulation <70° and a curvature ratio <40mm, it is advaisable to increase the proximal landing zone length >2.5mm to avoid typeia endoleaks.
El tratamiento endovascular de numerosas patologías de la aorta torácica descendente es una alternativa eficaz y segura a la cirugía convencional1–3. En caso de afectación del arco aórtico, se han desarrollado diferentes técnicas de derivación o translocación de troncos supraaórticos para preservar la circulación cerebral y permitir el tratamiento endovascular a ese nivel4,5. Sin embargo, el arco aórtico todavía representa un reto para la generación actual de endoprótesis aórticas, fundamentalmente por la magnitud de las fuerzas hemodinámicas a las que se ven sometidas. Recientemente se ha señalado que el principal factor implicado en el fracaso de las endoprótesis aórticas en el arco es la propia morfología de este, sobre todo por su angulación6,7.
Una óptima definición de la morfología del arco aórtico es fundamental para seleccionar la técnica adecuada de reparación, ya sea endovascular o híbrida, y para valorar su posterior resultado. El objetivo de este estudio es analizar la morfología del arco aórtico de los pacientes sometidos a distintos tipos de cirugía híbrida por patología del arco y aorta torácica descendente, así como evaluar el éxito técnico y clínico a corto y a medio plazo de dichas técnicas. El éxito técnico fue definido por la ausencia de endofugas, trombosis, migración de los dispositivos intravasculares o la necesidad de reconversión a cirugía convencional. El éxito clínico se definió como la ausencia de muerte de causa aórtica o relacionada, así como la ausencia de expansión aneurismática o rotura.
Pacientes y métodosEntre 2008 y 2013, 17pacientes con patología de arco aórtico y aorta torácica descendente fueron operados de forma consecutiva mediante transposición o derivación de troncos supraaórticos e implante de endoprótesis aórticas. Tres pacientes fueron excluidos por carecer de un adecuado examen radiológico preoperatorio. Las indicaciones de tratamiento de la patología aórtica de los 14pacientes (78,6% varones; edad media, 61,9±10,1años) incluidos fueron: 7aneurismas fusiformes ateroscleróticos, 4disecciones aórticas tipoB crónicas complicadas con dilatación aneurismática de la falsa luz, una disección aórtica tipoB aguda complicada con malperfusión visceral y 2aneurismas saculares postraumáticos de arco distal. Todos los pacientes fueron clasificados claseiv de la American Society of Anaesthesiologists (ASA). La mortalidad quirúrgica estimada mediante el European System for Cardiac Operative Risk Evaluation (EuroSCORE) logístico fue de 19,2±9,6%.
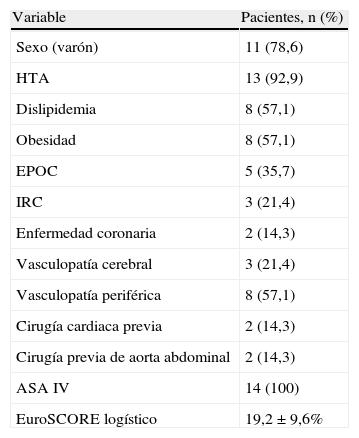
La selección de los pacientes candidatos a un abordaje combinado se realizó en función de su edad y comorbilidades, así como por su riesgo quirúrgico estimado. Las características clínicas y los factores de riesgo quirúrgico de los pacientes figuran en la tabla 1.
Características clínicas y demográficas de los pacientes incluidos en el estudio
| Variable | Pacientes, n (%) |
| Sexo (varón) | 11 (78,6) |
| HTA | 13 (92,9) |
| Dislipidemia | 8 (57,1) |
| Obesidad | 8 (57,1) |
| EPOC | 5 (35,7) |
| IRC | 3 (21,4) |
| Enfermedad coronaria | 2 (14,3) |
| Vasculopatía cerebral | 3 (21,4) |
| Vasculopatía periférica | 8 (57,1) |
| Cirugía cardiaca previa | 2 (14,3) |
| Cirugía previa de aorta abdominal | 2 (14,3) |
| ASA IV | 14 (100) |
| EuroSCORE logístico | 19,2±9,6% |
ASA: American Society of Anaesthesiologists; EPOC: enfermedad pulmonar obstructiva crónica; EuroSCORE: European System for Cardiac Operative Risk Evaluation; HTA: hipertensión arterial; IRC: insuficiencia renal crónica.
Las características anatómicas de la aorta fueron evaluadas en todos los pacientes mediante estudios con contraste de tomografía computarizada multidetector (TCMD) Lightspeed™ VCT General Electric Company (NYSE: GE)8. En todos los estudios se generaron reconstrucciones multiplanares y reconstrucciones tridimensionales para analizar la geometría del arco aórtico. Se registraron los diámetros aórticos medios en las zonas de anclaje proximal (ZAP) y distal (ZAD) y máximo aneurismático, extensión proximal y distal de la lesión aórtica y presencia de trombo mural. Los diámetros aórticos fueron medidos a nivel de la unión sinotubular y en el origen del tronco braquiocefálico, de la arteria carótida común izquierda (ACCI) y de la arteria subclavia izquierda (ASI) en un plano perpendicular a la línea central luminal. Asimismo, se determinó la longitud de la ZAP previa a transposición o derivación y posterior a la misma. Se consideró una longitud de la ZAP mínima de 15mm a nivel de la curvatura menor para lograr un adecuado sellado endovascular. Se registraron también las distancias entre los troncos supraaórticos medidas de borde a borde en la curvatura mayor del arco.
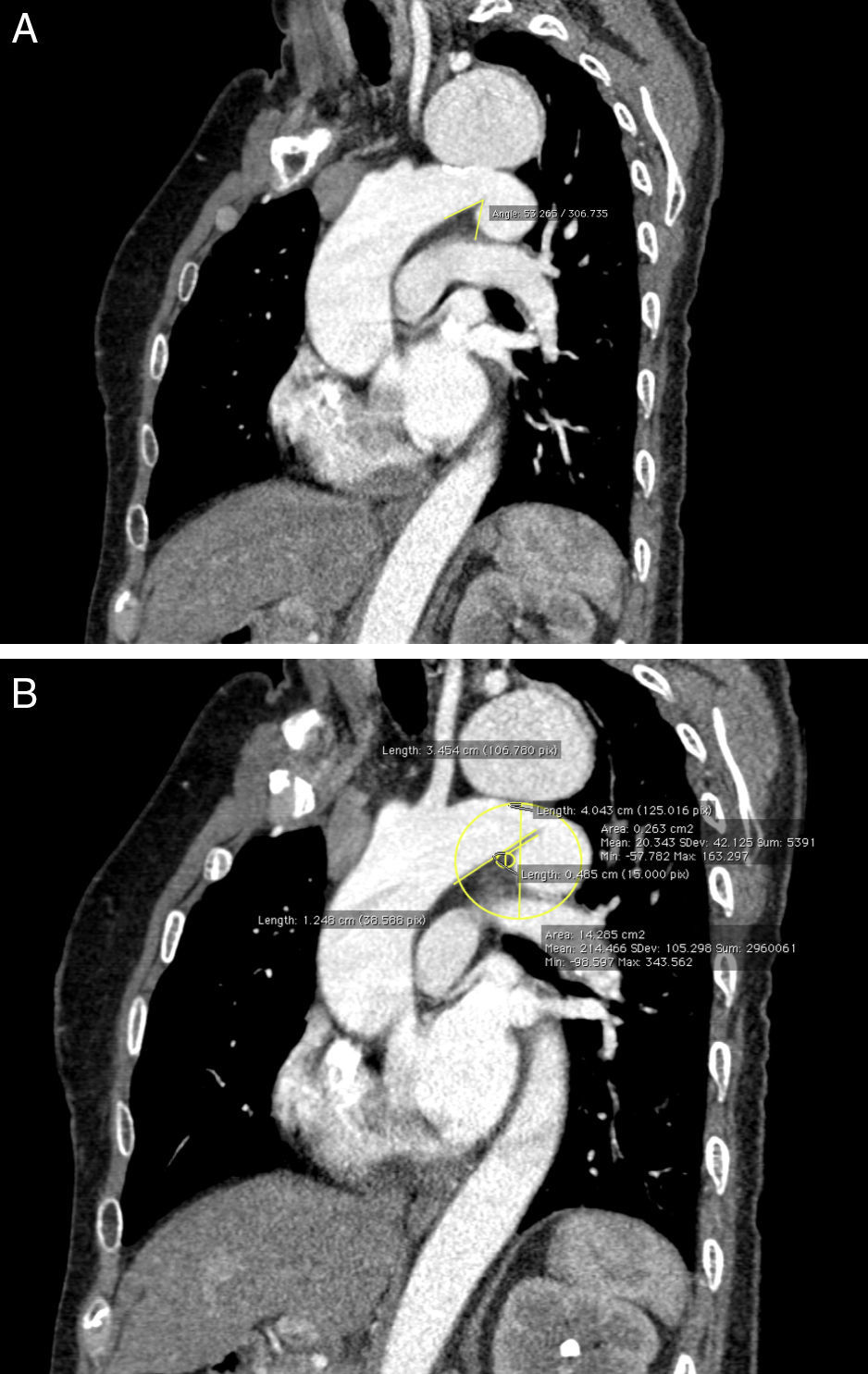
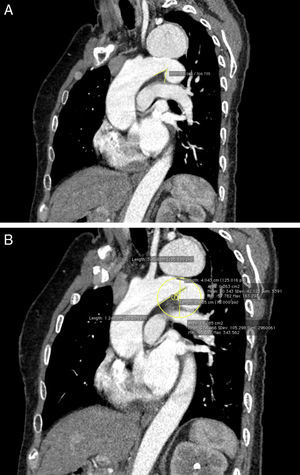
De acuerdo con criterios previamente publicados por otros autores7,9, se efectuó un estudio tanto de la angulación (fig. 1A) como del radio de curvatura del arco aórtico (fig. 1B). La angulación del arco aórtico se determinó a nivel del plano horizontal que pasa por el origen de la ASI, como ha sido previamente descrito por otros autores7. El radio de curvatura se cuantificó calculando la media aritmética del radio de la curvatura menor y la curvatura mayor a nivel del istmo aórtico. Así, radios de curvatura pequeños representan curvaturas aórticas más severas y asocian un mayor riesgo de endofuga tipoi, especialmente cuando son <40mm9.
El protocolo de seguimiento radiológico incluyó la realización de un TCMD a 1, 6 y 12meses y, posteriormente, resonancia magnética cardiovascular de forma bianual.
Cirugía de troncos supraaórticosLa cirugía realizada sobre los troncos supraaórticos incluyó la derivación carótido-subclavia izquierda en 7casos; la translocación de la ACCI y de la ASI en 2casos, y la translocación de los 3troncos supraaórticos en 5casos.
En todos los casos de translocación o de derivación de troncos supraaórticos se realizó monitorización arterial invasiva de arteria radial derecha y arteria radial o femoral izquierda, así como control de la oximetría cerebral intraoperatoria en ambos hemisferios mediante espectroscopia cercana al infrarrojo con el Invos 3100 (Somanetics Co, Troy, Michigan, EE.UU.).
El posterior implante de endoprótesis se efectuó en el mismo acto quirúrgico en todos los casos excepto en uno, en el que se realizó un implante diferido.
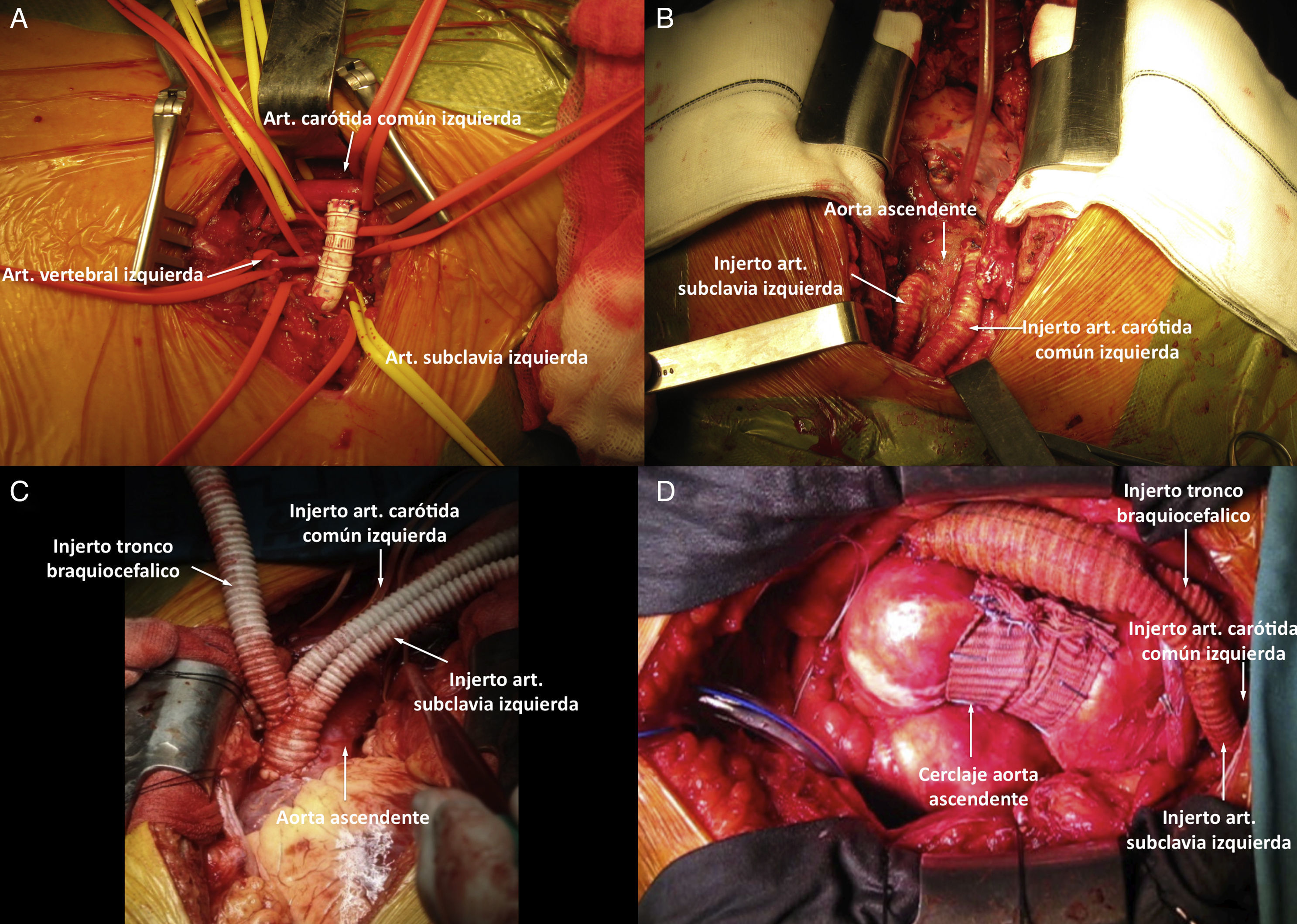
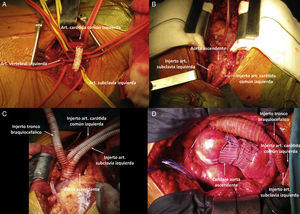
Derivación carótido-subclavia izquierdaSe efectuó un abordaje estándar a través de una incisión paralela a la clavícula izquierda. La anastomosis se efectuó con un injerto de GoreTex® anillado de 6 u 8mm entre la cara posterolateral de la ACCI y la cara superoanterior de la ASI distal al origen de la arteria vertebral izquierda (fig. 2A). En aquellos pacientes en los que el pinzamiento carotídeo conllevó una disminución significativa de la oximetría cerebral izquierda y/o una presión distal al pinzamiento <50mmHg se utilizó un shunt carotídeo 3×30mm Javid™ (Bard Peripheral Vascular Inc, AZ, EE.UU.) (vídeo 1).
A)Derivación carótido-subclavia izquierda con injerto GoreTex® anillado de 8mm. B)Translocación a aorta ascendente de arteria carótida común izquierda y de arteria subclavia izquierda con 2 injertos independientes de dacrón de 8 y 10mm, respectivamente. C)Translocación de los 3troncos supraaórticos con injerto de dacrón trifurcado 16-10-8-8mm. D)Translocación de los 3troncos supraaórticos con injerto de dacrón trifurcado 18-9-9-9mm y remodelado de aorta ascendente dilatada.
En los pacientes con derivación carótido-subclavia izquierda el origen de la ASI se embolizó con coils de acero 0,35”-5cm-10mm Mreye Steal® (Cook Medical, Bloomington, IN, EE.UU.) hasta 2009, y posteriormente con coils de platino de 0,035”-7cm-12mm Nester® (Cook Medical, Bloomington, IN, EE.UU.) para evitar una endofuga tipoii.
Doble transposición de arteria carótida común y subclavia izquierdaSe realizó un abordaje mediante esternotomía media convencional y translocación independiente de la ACCI y la ASI a través de 2injertos de dacrón de 8mm mediante pinzamiento lateral de la cara anterolateral y anterior de aorta ascendente, respectivamente (fig. 2B).
Translocación completa de troncos supraaórticosCuando la patología aórtica se extendía hasta el origen del tronco innominado, se requirió una translocación de los 3troncos supraaórticos para lograr una adecuada ZAP. En dichos casos se empleó un injerto de dacrón bifurcado, preferiblemente 16-8-8 o 18-9-9 en nuestra experiencia, al que se le anastomosó una tercera rama para completar la derivación (fig. 2C). El abordaje fue a través de una esternotomía media, seguida de la anastomosis del cuerpo del injerto de dacrón a la cara anterolateral de la aorta ascendente mediante pinzamiento lateral. Posteriormente se realizó la anastomosis termino-terminal de los troncos supraaórticos en orden: tronco innominado, ACCI y ASI. El muñón vascular en el origen de cada tronco supraaórtico se cerró mediante sutura continua reforzada con parche de teflón.
En los casos con dilatación de aorta ascendente superior a 40mm (2casos) se asoció un remodelado sin circulación extracorpórea de la aorta ascendente (vídeo 2) con injerto de dacrón construido específicamente con marcas radiopacas (fig. 2D) según la técnica descrita previamente por Chen et al.10.
Implante de endoprótesisEl implante de endoprótesis se realizó en un quirófano de cirugía cardiaca con anestesia general en todos los casos. Los procedimientos fueron controlados mediante un arco móvil de fluoroscopia Philips BV Pulsera™ (Philips Medical Systems, Best, Países Bajos) con angiografía por sustracción digital.
Las endoprótesis empleadas fueron Valiant® (Medtronic, World Medical Manufacturing Corp, Sunrise, FL, EE.UU.) en 5pacientes, Valiant® Captivia (Medtronic, World Medical Manufacturing Corp, Sunrise, FL, EE.UU.) en 8pacientes, y Relay™ Plus (Bolton Medical, Sunrise, FL, EE.UU.) en un caso.
Las dimensiones de las endoprótesis se calcularon mediante las imágenes de TCMD, buscando una sobredimensión del 10 al 15% en relación al diámetro de las zonas de anclaje, excepto en los pacientes con disección y/o hematoma intramural aórtico, en los que se sobredimensionó <5%. La longitud de las endoprótesis empleadas fue como mínimo 30 a 40mm más larga que la lesión aórtica para garantizar un adecuado sellado circunferencial en las zonas de anclaje. En 7pacientes se requirió más de una endoprótesis para cubrir la lesión aórtica, manteniendo aproximadamente un 50% de superposición.
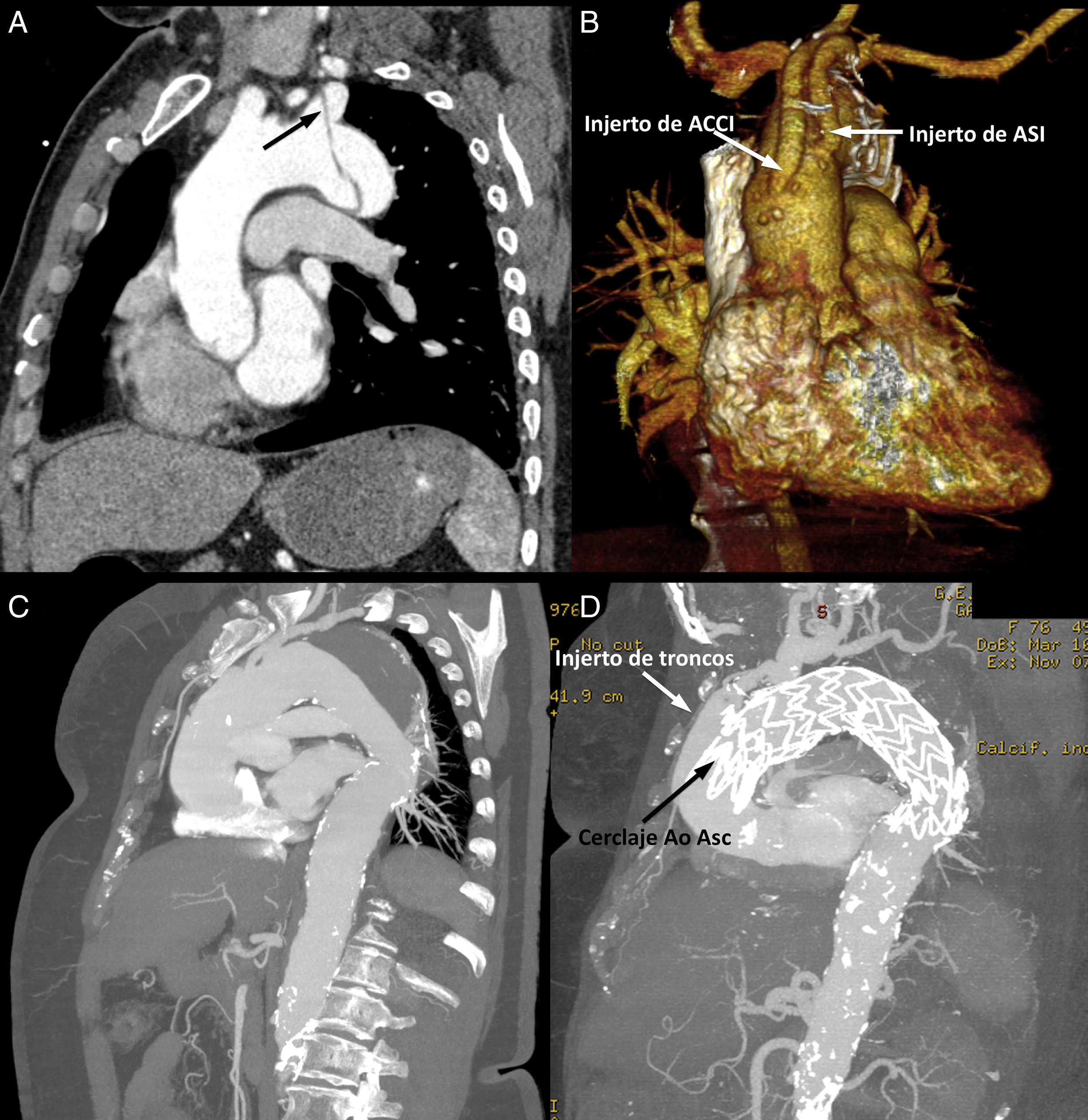
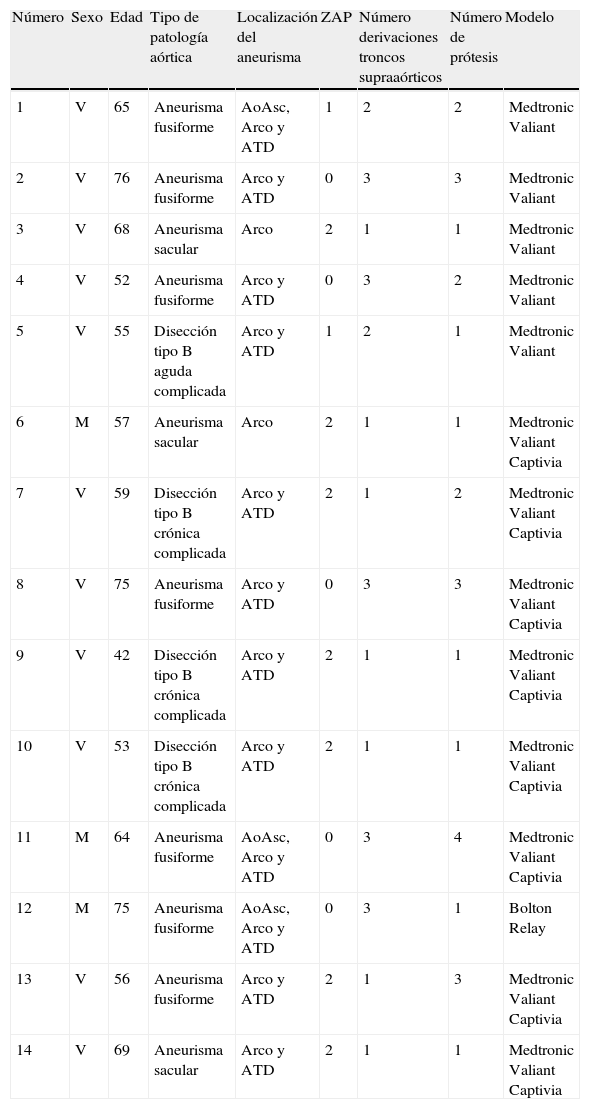
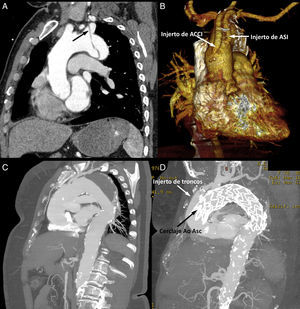
De acuerdo con la clasificación del arco aórtico propuesta por Mitchell et al.11, la ZAP en el arco aórtico fue la zona0 en 5casos, la zona1 en 2casos y la zona3 en 7casos (fig. 3). Los datos relativos al tratamiento endovascular de cada paciente se reflejan en la tabla 2.
A)Reconstrucción multiplanar de disección de aorta tipoB aguda, que afectaba al origen de la arteria subclavia izquierda (flecha) y causaba malperfusión visceral (paciente5). B)Reconstrucción tridimensional tras translocación de arteria carótida común izquierda y de arteria subclavia izquierda e implante de endoprótesis en zona1 (paciente5). C y D)Reconstrucciones multiplanares preoperatoria (C) y postoperatoria (D) de aneurisma fusiforme de arco y torácica descendente tratado mediante translocación de los 3troncos supraaórticos (zona0) y creación de neocuello en aorta ascendente dilatada (paciente12).
Características del procedimiento intravascular en cada paciente
| Número | Sexo | Edad | Tipo de patología aórtica | Localización del aneurisma | ZAP | Número derivaciones troncos supraaórticos | Número de prótesis | Modelo |
| 1 | V | 65 | Aneurisma fusiforme | AoAsc, Arco y ATD | 1 | 2 | 2 | Medtronic Valiant |
| 2 | V | 76 | Aneurisma fusiforme | Arco y ATD | 0 | 3 | 3 | Medtronic Valiant |
| 3 | V | 68 | Aneurisma sacular | Arco | 2 | 1 | 1 | Medtronic Valiant |
| 4 | V | 52 | Aneurisma fusiforme | Arco y ATD | 0 | 3 | 2 | Medtronic Valiant |
| 5 | V | 55 | Disección tipo B aguda complicada | Arco y ATD | 1 | 2 | 1 | Medtronic Valiant |
| 6 | M | 57 | Aneurisma sacular | Arco | 2 | 1 | 1 | Medtronic Valiant Captivia |
| 7 | V | 59 | Disección tipo B crónica complicada | Arco y ATD | 2 | 1 | 2 | Medtronic Valiant Captivia |
| 8 | V | 75 | Aneurisma fusiforme | Arco y ATD | 0 | 3 | 3 | Medtronic Valiant Captivia |
| 9 | V | 42 | Disección tipo B crónica complicada | Arco y ATD | 2 | 1 | 1 | Medtronic Valiant Captivia |
| 10 | V | 53 | Disección tipo B crónica complicada | Arco y ATD | 2 | 1 | 1 | Medtronic Valiant Captivia |
| 11 | M | 64 | Aneurisma fusiforme | AoAsc, Arco y ATD | 0 | 3 | 4 | Medtronic Valiant Captivia |
| 12 | M | 75 | Aneurisma fusiforme | AoAsc, Arco y ATD | 0 | 3 | 1 | Bolton Relay |
| 13 | V | 56 | Aneurisma fusiforme | Arco y ATD | 2 | 1 | 3 | Medtronic Valiant Captivia |
| 14 | V | 69 | Aneurisma sacular | Arco y ATD | 2 | 1 | 1 | Medtronic Valiant Captivia |
ATD: aorta torácica descendente; M: mujer; V: varón; ZAP: zona de anclaje proximal.
Tras la administración de 1,5mg/kg de heparina i.v. para un tiempo de coagulación activado >240s, se realizó el abordaje vascular retrógrado a través de una arteria femoral común en 10casos y de una arteria ilíaca común en un caso, mientras que en 3casos se efectuó un abordaje intravascular anterógrado desde un injerto de dacrón anastomosado a la aorta ascendente.
La liberación de las endoprótesis se realizó con hipotensión arterial controlada (presión arterial sistólica <60mmHg) mediante inducción de una taquicardia ventricular a 180-200lpm a través de un electrodo ventricular intravenoso transitorio. En todos los casos se efectuó una arteriografía intraoperatoria de control al final del procedimiento (vídeo 3).
Se siguió un protocolo específico para prevención de la isquemia medular, manteniendo una presión arterial media tras la liberación de las endoprótesis mayor de 90mmHg y drenaje de líquido cefalorraquídeo con límite de presión en 10cm de agua durante las primeras 48h postoperatorias.
Análisis estadísticoLos datos han sido expresados como media±desviación estándar, mediana y rango, frecuencia de distribución, o simplemente porcentaje, según procediese. Las variables cuantitativas continuas fueron comparadas mediante el test de la t de Student para datos emparejados. Las variables discretas se presentan como porcentajes y se las comparó mediante la prueba de Fisher. Un valor de p<0,05 se consideró estadísticamente significativo. La correlación lineal entre variables cuantitativas fue determinada mediante el test rho de Spearman. La supervivencia actuarial se calculó mediante el análisis de Kaplan-Meier. Se empleó el paquete informático SPSS (versión 15.0, SPSS Inc., Chicago, Ilinois, EE.UU.) para el análisis estadístico.
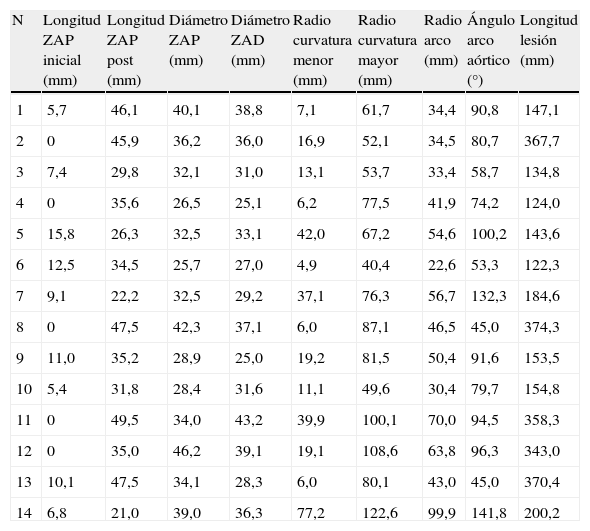
ResultadosGeometría del arco aórticoLa tabla 3 recoge los datos procedentes del análisis morfológico del arco aórtico. En la planificación preoperatoria, la longitud media de la ZAP en ausencia de cirugía de derivación o translocación fue de 5,9±5,3mm, mientras que la longitud media de la ZAP estimada tras asociar cirugía de derivación ascendió a 36,3±9,6mm. El diámetro medio de la ZAP y la ZAD fue de 34,2±6,1 y 32,9±5,7mm, respectivamente. En 9pacientes la distancia entre la ASI y la ACCI fue ≤15mm; en 3pacientes se situó entre 15-20mm, y solo en 2pacientes superó los 20mm.
Datos procedentes del análisis morfológico y geométrico mediante tomografía computarizada multidetector
| N | Longitud ZAP inicial (mm) | Longitud ZAP post (mm) | Diámetro ZAP (mm) | Diámetro ZAD (mm) | Radio curvatura menor (mm) | Radio curvatura mayor (mm) | Radio arco (mm) | Ángulo arco aórtico (°) | Longitud lesión (mm) |
| 1 | 5,7 | 46,1 | 40,1 | 38,8 | 7,1 | 61,7 | 34,4 | 90,8 | 147,1 |
| 2 | 0 | 45,9 | 36,2 | 36,0 | 16,9 | 52,1 | 34,5 | 80,7 | 367,7 |
| 3 | 7,4 | 29,8 | 32,1 | 31,0 | 13,1 | 53,7 | 33,4 | 58,7 | 134,8 |
| 4 | 0 | 35,6 | 26,5 | 25,1 | 6,2 | 77,5 | 41,9 | 74,2 | 124,0 |
| 5 | 15,8 | 26,3 | 32,5 | 33,1 | 42,0 | 67,2 | 54,6 | 100,2 | 143,6 |
| 6 | 12,5 | 34,5 | 25,7 | 27,0 | 4,9 | 40,4 | 22,6 | 53,3 | 122,3 |
| 7 | 9,1 | 22,2 | 32,5 | 29,2 | 37,1 | 76,3 | 56,7 | 132,3 | 184,6 |
| 8 | 0 | 47,5 | 42,3 | 37,1 | 6,0 | 87,1 | 46,5 | 45,0 | 374,3 |
| 9 | 11,0 | 35,2 | 28,9 | 25,0 | 19,2 | 81,5 | 50,4 | 91,6 | 153,5 |
| 10 | 5,4 | 31,8 | 28,4 | 31,6 | 11,1 | 49,6 | 30,4 | 79,7 | 154,8 |
| 11 | 0 | 49,5 | 34,0 | 43,2 | 39,9 | 100,1 | 70,0 | 94,5 | 358,3 |
| 12 | 0 | 35,0 | 46,2 | 39,1 | 19,1 | 108,6 | 63,8 | 96,3 | 343,0 |
| 13 | 10,1 | 47,5 | 34,1 | 28,3 | 6,0 | 80,1 | 43,0 | 45,0 | 370,4 |
| 14 | 6,8 | 21,0 | 39,0 | 36,3 | 77,2 | 122,6 | 99,9 | 141,8 | 200,2 |
ZAD: zona de anclaje distal; ZAP: zona de anclaje proximal.
El diámetro máximo aórtico tratado fue de 65,2±17,9mm, hallándose el máximo diámetro aórtico a nivel del arco en 11pacientes (78,5%).
El radio de curvatura medio del arco aórtico se situó en 48,7±19,9mm, con una angulación media de 84,6±29,1°. El 50% de los pacientes (7) presentaron una angulación del arco aórtico <90°, con 4pacientes con un ángulo inferior a 60°. Asimismo, 4pacientes presentaron un radio de curvatura <40mm. El radio de curvatura presentó una buena correlación con la angulación del arco aórtico, con un coeficiente rho de Spearman de +0,71.
Resultados quirúrgicosNo se produjo mortalidad intrahospitalaria ni se registraron complicaciones neurológicas permanentes (paraplejía y/o accidente cerebrovascular). La mediana de estancia en la UCI fue de 2días (rango, 1 a 27días), mientras que la mediana de estancia hospitalaria total fue de 6días (rango, 4 a 40días). Dos pacientes requirieron estancia prolongada en la UCI y postoperatoria total. El primero fue el paciente5, operado de urgencia por una disección aórtica aguda complicada con severa isquemia mesentérica, renal y de miembro inferior izquierdo en la que la puerta de entrada se hallaba entre la ASI (disecada) y la ACCI. El segundo caso con estancia prolongada fue la paciente12, que presentó en el postoperatorio inmediato múltiples episodios tromboembólicos venosos debido a una trombocitopenia severa inducida por la presencia de anticuerpos antiheparina.
Todos los procedimientos intravasculares se efectuaron en el mismo procedimiento que la cirugía de troncos supraaórticos, salvo en un caso. En dicho caso, dada la arteriopatía difusa de los troncos supraaórticos y la edad del paciente (paciente8), se decidió realizar el procedimiento en 2fases para asegurar la ausencia de lesiones neurológicas graves tras la cirugía de derivación. No se produjeron complicaciones relacionadas con el procedimiento endovascular. Se registraron 2infecciones quirúrgicas superficiales en el punto de acceso vascular inguinal y una infección quirúrgica superficial en la incisión supraclavicular de un by-pass carótido-subclavio. La mediana de endoprótesis empleadas fue de 2, siendo la longitud más empleada la de 150mm y los calibres proximales más utilizados, 34 y 36mm.
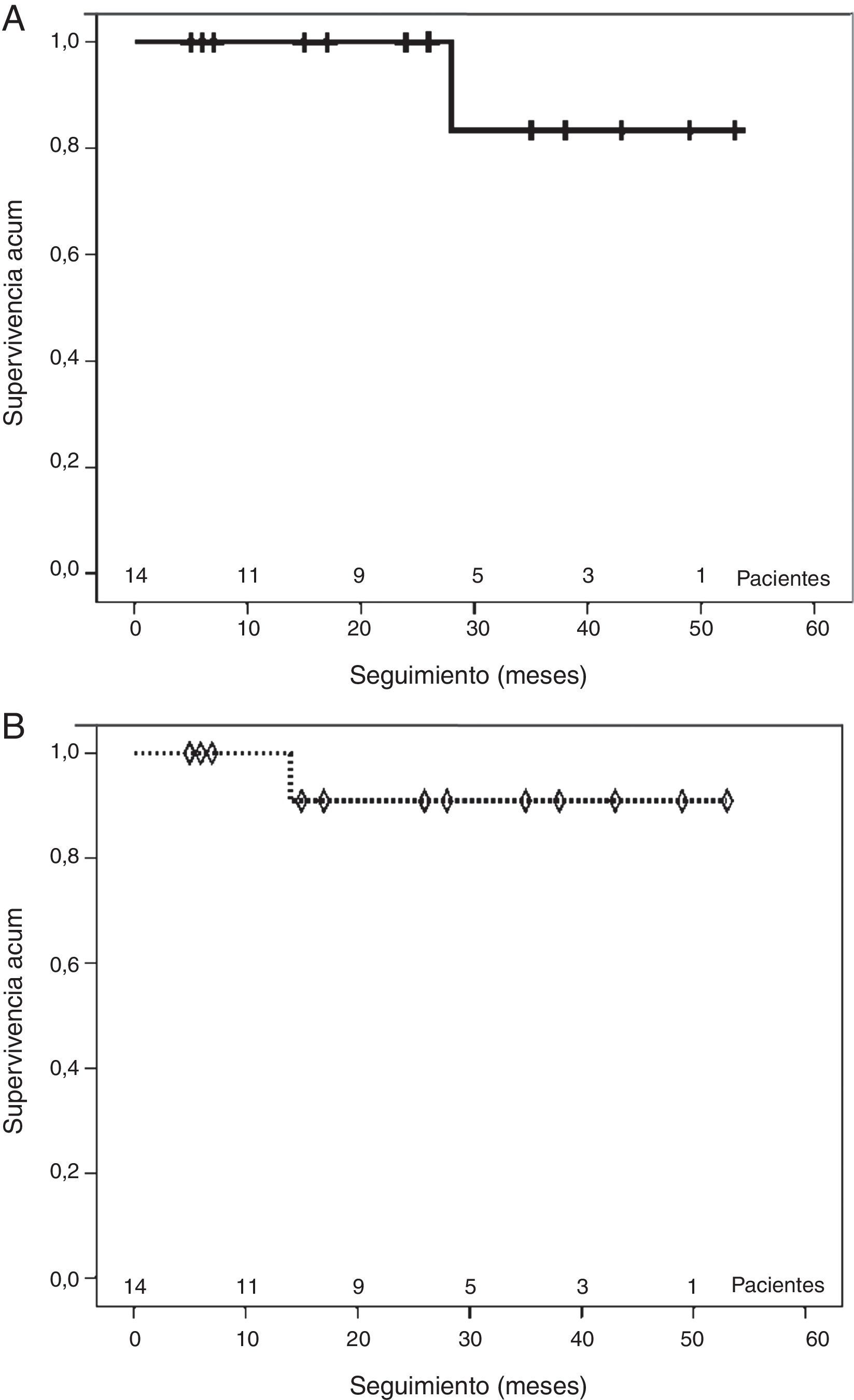
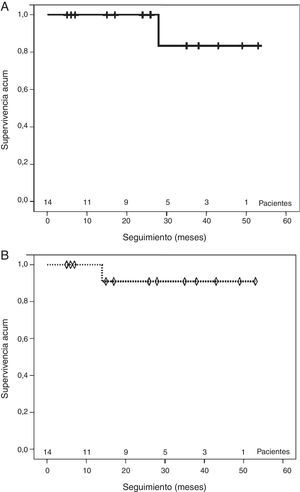
SeguimientoEl seguimiento medio fue de 26,6±15,6meses. La supervivencia media fue del 100% a 1 y 2años y del 83,3% a 4años (fig. 4A). No se registraron muertes de origen cardiovascular durante el seguimiento. Únicamente ocurrió un fallecimiento tardío a los 28meses de la cirugía por insuficiencia respiratoria en un paciente con EPOC estadioiii.
Se registró una reducción del diámetro aórtico máximo de 65,2±17,9mm preoperatorio a 50,9±14,2mm (p<0,001). Esto es, se observó una reducción porcentual media del 19,7±16,4% tras el tratamiento intravascular.
La supervivencia media libre de endofuga y reintervención fue del 100% a un año y del 90,9% a 2 y 4años (fig. 4B). Se registró un caso de endofuga durante el seguimiento a los 14meses de la cirugía. En un paciente con disección tipoB crónica complicada operado mediante derivación carótido-subclavia izquierda e implante de una endoprótesis se produjo una endofuga por rotura distal del tabique intimal que condujo a la presurización de la falsa luz a nivel toracoabdominal. Dicho paciente fue operado con éxito mediante cirugía abierta de un aneurisma toracoabdominal Crawford tipoii.
DiscusiónLa planificación del tratamiento endovascular sobre el arco aórtico requiere un conocimiento adecuado de la morfología del arco aórtico y de los troncos supraaórticos. Aunque algunos autores han publicado estudios radiológicos sobre las variantes en la configuración espacial del arco aórtico7,12,13, todavía no se han correlacionado los distintos parámetros morfológicos del arco aórtico con los resultados del tratamiento endovascular a ese nivel. Nuestro estudio aporta una refinada revisión de los parámetros morfológicos del arco aórtico, así como un estricto seguimiento clínico y radiológico de los pacientes operados mediante cirugía híbrida.
A nivel del arco aórtico hemos de considerar 3factores: morfología, fuerzas hemodinámicas y presencia de los troncos supraaórticos. Estos 3factores explican la incidencia incrementada de complicaciones, fundamentalmente endofugas, tras el tratamiento endovascular de la patología del arco aórtico14-16. Aunque la influencia relativa de cada parámetro morfológico está todavía por determinar, la angulación del arco aórtico se presenta como uno de los principales determinantes del fracaso de algunos casos de tratamiento intravascular del arco aórtico. La angulación aguda, en general <90° y sobre todo <70°, conduce a una inadecuada aposición de las endoprótesis a la curvatura menor del arco y, por tanto, a la posible aparición de endofugas7,17,18. La angulación media en nuestra serie fue de 84,6±29,1°, destacando un 50% de los pacientes con una angulación del arco aórtico <90° y 4pacientes con un ángulo <60°. Por otra parte, 4pacientes en nuestra serie presentaron un radio de curvatura <40mm y <45mm en 6casos, valores que han sido recientemente asociados por Sze et al.9 con una aposición deficiente de las endoprótesis aórticas a la curvatura menor del arco aórtico (defecto en «pico de pájaro») y a una incidencia aumentada de endofugas tipoi9.
El cálculo inadecuado de la longitud de la ZAP en la curvatura menor puede conllevar un defecto en la fijación proximal de la endoprótesis y, en consecuencia, una endofuga tipoia. En nuestra serie, la adecuada valoración preoperatoria nos permitió indicar la cirugía híbrida para pasar de una longitud media de la ZAP de 5,9±5,3 a 36,3±9,6mm y evitar la aparición de endofugas tipoia.
A pesar de una angulación hostil en un número importante de pacientes de nuestra serie, no se produjeron endofugas tipoi por aposición inadecuada de la endoprótesis al arco aórtico. Una posible explicación es el haber buscado mayores longitudes de ZAP mediante la derivación o translocación de uno o varios troncos supraaórticos. Asimismo, el empleo de endoprótesis con un stent no recubierto proximal, el Floppy Freeflo de la Valiant® y Valiant® Captivia (Medtronic, World Medical Manufacturing Corp, Sunrise, FL, EE.UU.), que es altamente flexible y adaptable, permite una liberación de la porción cubierta enrasada con el origen de los troncos, aprovechando así al máximo la longitud de la ZAP8.
Los excelentes resultados del tratamiento endovascular a nivel del arco aórtico en nuestra serie se reflejan en la reducción porcentual del 19,7±16,4% en el diámetro máximo aórtico.
En un metaanálisis realizado por Koullias y Wheatley19 que en la muestra final incluyó 463pacientes procedentes de 15estudios, los procedimientos híbridos de arco aórtico fueron clasificados en 2grupos dependiendo, fundamentalmente, del empleo o no de circulación extracorpórea. El grupoi, que englobó 324pacientes, estuvo constituído por aquellas cirugías híbridas en las que se utilizó circulación extracorpórea con o sin hipotermia profunda y parada circulatoria. Dichas técnicas híbridas implican una sustitución quirúrgica abierta del arco aórtico y reimplante de troncos supraaórticos, que se completa mediante un dispositivo endovascular (puro o mixto dacrón-intravascular) para reparar los segmentos distales de aorta torácica descendente no accesibles a la sustitución abierta. Este tipo de procedimientos como variantes de la «trompa de elefante», y sobre todo la «trompa de elefante congelada», han demostrado resultados excelentes en la literatura, como recientemente han publicado Mestres et al.20 en 113pacientes procedentes del International E-Vita Open® Registry con patología aneurismática compleja de arco aórtico y aorta torácica descendente. En esta última publicación, Mestres et al.20 obtuvieron una mortalidad intrahospitalaria y una supervivencia a 5años del 12 y del 78%, respectivamente, así como una tasa libre de reintervención intravascular y abierta del 88 y del 90%, respectivamente.
Por otra parte, en el metaanálisis conducido por Koullias y Wheatley19, el grupo de la estrategia tipoii, con 139pacientes operados sin soporte de circulación extracorpórea, englobó las técnicas híbridas basadas en la exclusión de la patología del arco aórtico y aorta descendente mediante endoprótesis, asociando alguna técnica de transposición o de derivación extraanatómica de los troncos supraaórticos para preservar su flujo. Como se concluye en el metaanálisis19, no se hallaron diferencias significativas entre ambas estrategias (tipoi y ii) híbridas en términos de morbimortalidad a corto plazo.
En espera de resultados a más largo plazo, parece razonable optar por la estrategia tipoi con sustitución abierta de aorta ascendente y arco en aquellos pacientes en los que la aorta ascendente (zona de anclaje0) sea patológica (diámetro >40mm) debido a la mayor durabilidad en el tiempo de la sustitución aórtica abierta. No obstante, en los 2pacientes con dilatación de aorta ascendente de nuestra serie (pacientes8 y 12) optamos por una estrategia tipoii asociando una técnica de remodelado de la aorta ascendente como la descrita por Chen et al.10 por tratarse de enfermos añosos de alto riesgo con severa afectación ateromatosa de los troncos y otras comorbilidades, como insuficiencia renal crónica, que aconsejaban evitar el empleo de circulación extracorpórea y parada circulatoria con hipotermia.
A pesar de la seguridad y de la reproducibilidad de la cirugía híbrida del arco aórtico, persisten riesgos que deben ser considerados antes de indicar estos procedimientos. En primer lugar, cualquier manipulación de la aorta ascendente y/o de los troncos supraaórticos puede producir embolismos de placas ateroscleróticas. En consecuencia, es recomendable minimizar la manipulación de estas estructuras durante la cirugía de derivación o translocación. Asimismo, una inadecuada orientación o longitud de los injertos supraaórticos puede conducir a la torsión o compresión y subsiguiente oclusión de las derivaciones vasculares. Por ello, es fundamental realizar un exhaustivo estudio morfológico del arco aórtico y los troncos antes de realizar estos procedimientos. La manipulación endovascular tanto de guías como de endoprótesis a nivel del arco puede conducir igualmente a complicaciones embólicas potencialmente graves.
El cálculo inadecuado de la longitud de la ZAP en la curvatura menor puede conllevar un defecto en la fijación proximal de la endoprótesis y, en consecuencia, una endofuga tipoia. En los casos con afectación del arco aórtico, incluso a nivel distal, que presenten una marcada angulación (<70°) y un reducido radio de curvatura del arco aórtico (<40mm) se recomienda incrementar la longitud de la zona de anclaje proximal a >2,5cm. En nuestra serie, la adecuada valoración preoperatoria nos permitió indicar la cirugía híbrida para pasar de una longitud media de la ZAP de 5,9±5,3 a 36,3±9,6mm y evitar la aparición de endofugas tipoia.
Finalmente, es importante destacar que en los pacientes con una aorta ascendente >40mm que vaya a emplearse como ZAP (zona0), se debe asociar la sustitución de aorta ascendente mediante injerto de Dacron5,21 o bien, sobre todo en pacientes de muy alto riesgo quirúrgico, alguna técnica de remodelado de la aorta ascendente sin circulación extracorpórea10.
ConclusionesEl adecuado conocimiento de la morfología y anatomía radiológica del arco aórtico es fundamental para seleccionar la mejor estrategia terapéutica en los pacientes con patología compleja del arco, así como para prevenir la aparición de complicaciones en el implante de endoprótesis a ese nivel. En los casos con afectación del arco aórtico, incluso a nivel distal, que presenten una marcada angulación (<70°) y un reducido radio de curvatura del arco aórtico (<40mm) se recomienda incrementar la longitud de la zona de anclaje proximal a >2,5cm para evitar defectos de aposición de las endoprótesis en la curvatura menor del arco y, por tanto, endofugas tipoia. Las endoprótesis de tercera generación presentan una gran adaptabilidad a angulaciones severas y radios de curvatura importantes con excelentes resultados a medio plazo. El tratamiento híbrido de la patología del arco aórtico requiere un abordaje multidisciplinar y amplía las opciones de tratamiento, principalmente en pacientes de alto riesgo quirúrgico.
LimitacionesA pesar de tratarse de un estudio prospectivo, este estudio presenta como principal limitación el número de pacientes incluidos, lo que podría reducir su poder estadístico para identificar variables de potencial interés.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.