El uso de prótesis no soportadas se asocia con menores gradientes transvalvulares y rápida regresión de la masa ventricular izquierda (MVI). En estudios recientes se sugiere que no existen diferencias respecto a las soportadas. No existe una comparativa en poblaciones con predominio de anillos aórticos pequeños. Analizamos la supervivencia, la clase funcional y la regresión del índice de masa ventricular izquierda (IMVI) en aquellos pacientes con anillo aórtico menor o igual a 21mm.
MétodosEstudio analítico retrospectivo ajustado mediante puntuación de propensión, de 72 pacientes intervenidos de sustitución valvular aórtica aislada por estenosis aórtica severa, con anillos de 19-21mm (24 no soportadas Freedom, 48 soportadas Mitroflow, Sorin Group).
ResultadosEl seguimiento medio fue 51,4±22 meses. No se detectaron diferencias en la clase funcional, la supervivencia, ni en la regresión del IMVI (44±22g/m2 soportadas, 39,4±19g/m2 no soportadas, p=0,86).
ConclusionesEn pacientes con anillo aórtico pequeño de 19-21mm no encontramos diferencias estadísticamente significativas entre bioprótesis.
The use of Stentless bioprosthesis is associated with lower transvalvular gradients and rapid regression in left ventricular mass (LVM). Recent studies suggest that there are no differences regardingt Stented bioprosthesis. There is no comparison in populations with small aortic annulus prevalence. We analysed survival, functional class status and left ventricular mass regression index (LVMRI) in patients with an aortic annulus equal or smaller than 21mm.
MethodsRetrospective analytical study of 72 patients matched with propensity score who underwent scheduled isolated aortic valve replacement due to severe aortic stenosis from March 2003 to February 2010 with small aortic annulus 19-21mm (24 Stentless Freedom versus 48 Stented Mitroflow, Sorin Group).
ResultsMean follow-up was 51.4±22 months. No significant differences were detected in functional class, survival nor mean LVMRI (44±22g/m2 in Stented, 39,4±19g/m2 in Stentless (p=0.86).
ConclusionsIn small aortic annulus patients (19-21mm), no statistical significant differences were found between bioprosthesis.
La estenosis valvular aórtica es actualmente el tipo más frecuente de valvulopatía en Europa y Norteamérica1. El único tratamiento definitivo para la estenosis valvular aórtica severa es la sustitución valvular aórtica (SVAo).
Las prótesis soportadas (PS) se relacionan con una hemodinámica más obstructiva y gradientes transaórticos más elevados en los tamaños pequeños2, mientras que el uso de prótesis no soportadas (PNS, desde 1965)3 se ha asociado con una excelente hemodinámica, menores gradientes y rápida regresión de la masa ventricular izquierda (MVI). Sin embargo en los estudios más recientes se sugiere que no existen diferencias respecto a las PS2–10.
Ambas prótesis son utilizadas en nuestro medio, no existiendo una comparativa en una población no anglosajona con predominio de anillos aórticos pequeños. Como objetivos principales perseguimos analizar la regresión del índice de masa ventricular izquierda (IMVI), la supervivencia y la clase funcional en aquellos pacientes con anillo aórtico menor o igual a 21mm.
Población y métodosEstudio analítico retrospectivo de pacientes intervenidos de SVAo programada aislada con prótesis biológicas por estenosis valvular aórtica severa sintomática desde marzo de 2003 hasta febrero de 2010. Se excluyeron los que presentaban enfermedad coronaria, otra valvulopatía o procedimiento asociado, o los que recibieron una bioprótesis >21mm.
En dicho periodo se intervinieron un total de 162 pacientes, de los cuales 82 (50,6%) presentaban anillo aórtico pequeño menor o igual a 21mm de diámetro medido por ecocardiografía transtorácica (ETT). Debido a la presencia de diferencias estadísticamente significativas preoperatorias en la edad (77,3±5,3 PS vs. 73,7±5,7 años PNS, p=0,04) y en el riesgo preoperatorio (EuroScore I logístico, 10,5% PS vs. 8,5% PNS, p=0,035) se realizó un pareado mediante puntuación de propensión, obteniéndose una muestra final de 72 pacientes con un ratio 2:1 (PS:PNS).
En 48 de ellos se implantó una PS de última generación, la Mitroflow (Sorin Group Canada Inc, Mitroflow division), y otros 24 recibieron una PNS, la Pericarbon Freedom (Sorin Group Biomedica, Saluggia, Italia), ambas de pericardio bovino.
Técnica quirúrgicaSe accedió a mediastino a través de esternotomía media. El circuito de CEC se estableció mediante canulación arterial en aorta ascendente, y venosa en aurícula derecha, accediendo mediante aortotomía transversa a la válvula aórtica.
Todos los pacientes fueron intervenidos por el mismo equipo quirúrgico. Las PNS se implantaron según la técnica de implante subcoronario con dos líneas de sutura continua, mientras que las PS se implantaron en posición supraanular con puntos discontinuos. La elección del tamaño se realizó utilizando los medidores específicos de cada bioprótesis. La elección del tipo de bioprótesis fue a elección del cirujano responsable.
SeguimientoTodas las variables preoperatorias e intraoperatorias se obtuvieron de las historias clínicas. En caso de supervivencia durante el seguimiento, se realizó una entrevista personal y una ETT de control. Las ETT del seguimiento fueron realizadas por dos expertos ecocardiografistas de nuestro centro, utilizando el mismo equipo (Acuson Siemens-Sequoia C-256, Estados Unidos). En caso de fallecimiento, se revisó la historia clínica para obtener los datos de la última ETT realizada y determinar la causa del mismo. Se consideraron complicaciones precoces cardíacas y cerebrovasculares mayores la mortalidad de causa cardíaca, el infarto agudo de miocardio, accidente vascular cerebral no transitorio, y endocarditis precoz. Para la medición de la MVI se utilizó el método de cálculo ASE11.
Análisis estadísticoLas variables cualitativas se expresan codificadas como frecuencias absolutas o relativas, y las variables cuantitativas como media±desviación estándar (DE). La comparación de las variables cualitativas se realizó mediante la prueba de Chi-cuadrado (χ2), y el test exacto de Fisher. Las variables cuantitativas fueron comparadas mediante la t de Student para muestras independientes o U de Mann-Whitney. El análisis y los gráficos de supervivencia se realizaron siguiendo el método de Kaplan-Meier (Log Rank de Mantel-Cox).
Las puntuaciones de propensión se estimaron con un modelo de regresión logística que predecía el estado de tratamiento a partir de 10 covariables preoperatorias observadas, incluidas varias interacciones (edad y riesgo preoperatorio estimado por ejemplo). Los autores indentificaron a los 24 pacientes con PNS y buscaron una pareja para cada caso siguiendo un ratio PS:PNS de 2:1 utilizando el algoritmo «Nearest neighbour matching», mediante macros para SPSS (SPSS Inc., Chicago, IL, USA) 15.0 (SPSSPropensityMatching_Example and SPSSPropensity_Análisis).
Se consideró estadísticamente significativa la diferencia entre variables cuando el valor de p era inferior o igual a 0,05.
ResultadosSe analizaron un total de 72 SVAo con bioprótesis en el periodo anteriormente referido, repartidas en 2 grupos: grupo Mitroflow (n=48, PS) y grupo Freedom (n=24, PNS).
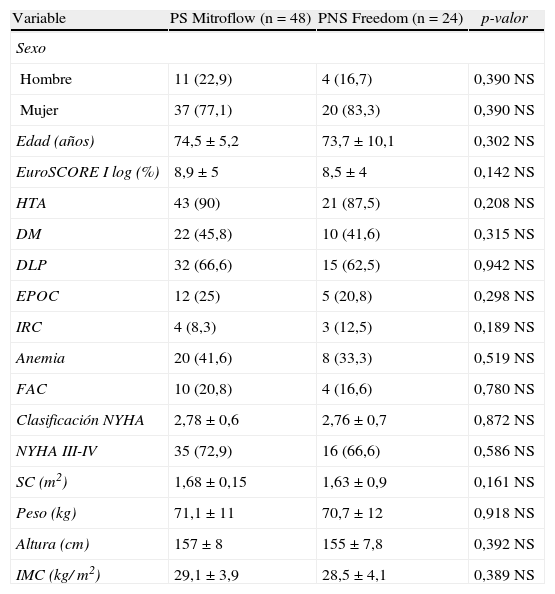
Las características clínicas preoperatorias y ecocardiográficas quedan resumidas en las tablas 1 y 2 (apartado A). Gracias al emparejamiento mediante puntuación de propensión, no se encontraron diferencias significativas en ninguna de las variables preoperatorias.
Características basales preoperatorias pareadas
| Variable | PS Mitroflow (n=48) | PNS Freedom (n=24) | p-valor |
| Sexo | |||
| Hombre | 11 (22,9) | 4 (16,7) | 0,390 NS |
| Mujer | 37 (77,1) | 20 (83,3) | 0,390 NS |
| Edad (años) | 74,5±5,2 | 73,7±10,1 | 0,302 NS |
| EuroSCORE I log (%) | 8,9±5 | 8,5±4 | 0,142 NS |
| HTA | 43 (90) | 21 (87,5) | 0,208 NS |
| DM | 22 (45,8) | 10 (41,6) | 0,315 NS |
| DLP | 32 (66,6) | 15 (62,5) | 0,942 NS |
| EPOC | 12 (25) | 5 (20,8) | 0,298 NS |
| IRC | 4 (8,3) | 3 (12,5) | 0,189 NS |
| Anemia | 20 (41,6) | 8 (33,3) | 0,519 NS |
| FAC | 10 (20,8) | 4 (16,6) | 0,780 NS |
| Clasificación NYHA | 2,78±0,6 | 2,76±0,7 | 0,872 NS |
| NYHA III-IV | 35 (72,9) | 16 (66,6) | 0,586 NS |
| SC (m2) | 1,68±0,15 | 1,63±0,9 | 0,161 NS |
| Peso (kg) | 71,1±11 | 70,7±12 | 0,918 NS |
| Altura (cm) | 157±8 | 155±7,8 | 0,392 NS |
| IMC (kg/ m2) | 29,1±3,9 | 28,5±4,1 | 0,389 NS |
DLP: dislipemia; DM: diabetes mellitus; EPOC: enfermedad pulmonar obstructiva crónica; FAC: fibrilación auricular crónica; HTA: hipertensión arterial; IMC: índice de masa corporal; IRC: insuficiencia renal crónica; NS: no significativo; NYHA: New York Heart Association; PNS: prótesis no soportada; PS: prótesis soportada; SC: superficie corporal. Variables cuantitativas representadas como media±DE, variables cualitativas como número y porcentaje[n (%)].
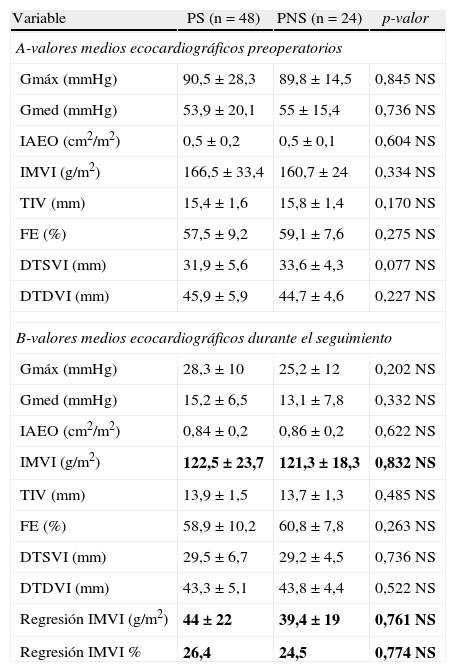
Variables ecocardiográficas
| Variable | PS (n=48) | PNS (n=24) | p-valor |
| A-valores medios ecocardiográficos preoperatorios | |||
| Gmáx (mmHg) | 90,5±28,3 | 89,8±14,5 | 0,845 NS |
| Gmed (mmHg) | 53,9±20,1 | 55±15,4 | 0,736 NS |
| IAEO (cm2/m2) | 0,5±0,2 | 0,5±0,1 | 0,604 NS |
| IMVI (g/m2) | 166,5±33,4 | 160,7±24 | 0,334 NS |
| TIV (mm) | 15,4±1,6 | 15,8±1,4 | 0,170 NS |
| FE (%) | 57,5±9,2 | 59,1±7,6 | 0,275 NS |
| DTSVI (mm) | 31,9±5,6 | 33,6±4,3 | 0,077 NS |
| DTDVI (mm) | 45,9±5,9 | 44,7±4,6 | 0,227 NS |
| B-valores medios ecocardiográficos durante el seguimiento | |||
| Gmáx (mmHg) | 28,3±10 | 25,2±12 | 0,202 NS |
| Gmed (mmHg) | 15,2±6,5 | 13,1±7,8 | 0,332 NS |
| IAEO (cm2/m2) | 0,84±0,2 | 0,86±0,2 | 0,622 NS |
| IMVI (g/m2) | 122,5±23,7 | 121,3±18,3 | 0,832 NS |
| TIV (mm) | 13,9±1,5 | 13,7±1,3 | 0,485 NS |
| FE (%) | 58,9±10,2 | 60,8±7,8 | 0,263 NS |
| DTSVI (mm) | 29,5±6,7 | 29,2±4,5 | 0,736 NS |
| DTDVI (mm) | 43,3±5,1 | 43,8±4,4 | 0,522 NS |
| Regresión IMVI (g/m2) | 44±22 | 39,4±19 | 0,761 NS |
| Regresión IMVI % | 26,4 | 24,5 | 0,774 NS |
DTDVI: diámetro telediastólico del ventrículo izquierdo; DTSVI: diámetro telesistólico del ventrículo izquierdo; FE: fracción de eyección; Gmáx: gradiente máximo transaórtico; Gmed: gradiente medio transaórtico; IAEO: índice del área efectiva del orificio; IMVI; índice de masa ventricular izquierda; NS: no significativo; PNS: prótesis no soportada; PS: prótesis soportada; TIV: tabique interventricular. Variables cuantitativas representadas como media±DE.
En negrita, el objetivo primario.
Referente a las variables operatorias, existieron diferencias estadísticamente significativas en favor de las PS, que precisaron de 10 minutos menos de isquemia miocárdica para su implante (61,1±14,7min PS, 71,2±8,7min PNS, p=0,003), y 11,5 minutos menos de circulación extracorpórea (73,5±19min PS, 85±13min PNS, p=0,012). En cuanto a los tamaños protésicos valvulares medios implantados, no hubo diferencias significativas (20,3±0,8mm PS, 20,6±1mm PNS, p=0,228). Tampoco en la estancia en UCI (4,4±2,8 días PS, 4,7±2,5 PNS, p=0,50), estancia total (12,8±8,4 días PS, 12,1±4,4 PNS, p=0,11) complicaciones precoces cardíacas y cerebrovasculares mayores (10,4% PS vs. 12,5% PNS, p=0,78) ni mortalidad precoz (3 casos PS vs. 2 PNS p=0,42).
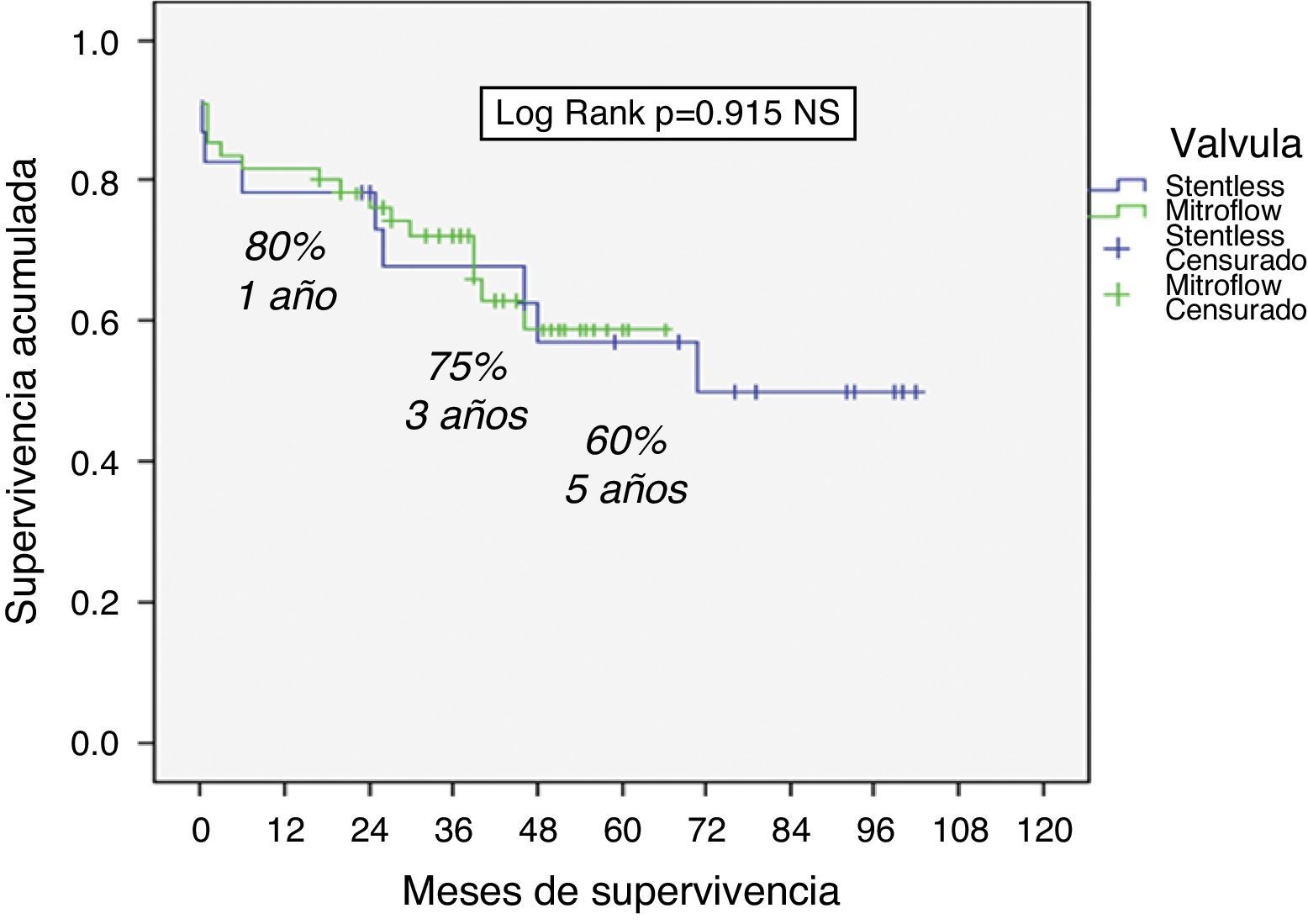
El seguimiento medio fue de 51,4±22 meses (mediana 44,.5, rango intercuartílico 30-53 meses). No existieron diferencias en la clase funcional New York Heart Association (NYHA) (media 1,78±0,5 PNS, 1,72±0,.6 PS, p=0,616, con más del 95% de los pacientes de ambos grupos en clase funcional NYHA I-II) ni en la supervivencia (Log Rank p=0,915), con un 75% de supervivencia global a 3 años y un 60% a 5 años (fig. 1).
Los valores medios ecocardiográficos durante el seguimiento medio (tabla 2, [apartado B]) no arrojan diferencias estadísticamente significativas entre grupos en ninguna de las variables analizadas, haciendo especial hincapié en el índice de MVI (IMVI, PS 122,5±23,7 g/m2, PNS 121,5±18,3 g/m2, p=0,832), en los gradientes medios (PS 15,2±6,5mmHg, PNS 13,1±7,8mmHg, p=0,332) y en el índice de área efectiva del orificio (IAEO) (IAEO, PS 0,84±0,2 cm2/m2, PNS 0,86±0,2 cm2/m2, p=0,622). Por tanto, no hubo diferencias en la regresión de la hipertrofia ventricular izquierda (HVI), medida utilizando el IMVI (valor medio PS 44,2±22g/m2[26,4%], PNS 39,4±19g/m2[24,5%] p=0,761).
No existieron diferencias significativas entre los IAEO medios entre bioprótesis, aunque se detectó una tendencia favorable para las PNS (0,84 cm2/ m2 PS, 0,89cm2/ m2 PNS p=0,48)
DiscusiónEl presente estudio es el primero en realizar una comparativa entre PS y PNS en un medio con predominio de pacientes con anillos aórticos pequeños como el nuestro. A la vista de los resultados obtenidos, presentamos el mayor riesgo preoperatorio, los valores más bajos de SC y el porcentaje de pacientes con anillo aórtico pequeño más extenso (50,6%, frente al 10-23%) de toda la literatura comparativa revisada2–10
El tiempo de isquemia miocárdica fue menor y estadísticamente significativo en las PS (media de 61,1±14,.7 minutos), frente a los 10,1 minutos de más que precisó el grupo de PNS. El porcentaje de complicaciones postquirúrgicas, complicaciones precoces cardíacas y cerebrovasculares mayores fue de aproximadamente el 10% en ambos grupos, con una mortalidad observada inferior a la esperada (EuroScore log 8,7%, observada 6,9%).
Los objetivos principales del estudio fueron determinar si existían diferencias significativas en la regresión del IMVI (considerado actualmente el factor más importante para determinar la eficacia de la SVAo4,8,10) la supervivencia y la clase funcional. En el presente estudio se aprecian efectos similares en la regresión del IMVI en ambos grupos. También hemos observado que las PNS presentan una leve tendencia favorable en los gradientes medios transvalvulares y en los IAEO a pesar de la falta de significación estadística, aspecto confirmado en otros estudios con prótesis de mayor tamaño4–7. Estas diferencias suelen presentarse habitualmente dentro de los primeros 6-12 meses, desapareciendo posteriormente, sin llegar a repercutir en la regresión de la HVI ni en la clase funcional NYHA a largo plazo2–10.
Datos extraídos de la literatura científica4 indican que por cada 20g/m2 de incremento en la HVI se incrementa un 50% el riesgo relativo de morbimortalidad de causa cardiovascular, por lo que una regresión de 20g/m2 en el IMVI se considera clínicamente relevante. La regresión media en el IMVI respecto de su valor preoperatorio medio fue del 26,4% para las PS y del 24,5% para las PNS (p=0,761). La presencia de HTA no controlada en el seguimiento puede ser un sesgo independiente en este punto.
El pronóstico vital de los pacientes intervenidos es similar al de la población general, con una mejoría funcional excelente, encontrándose el 95% en clase funcional NYHA I-II, con una supervivencia del 75% a 3 años y del 60% a 5 años, resultados similares a otras series3–10 sin diferencias entre grupos.
Los primeros estudios habían apreciado mayor regresión del IMVI con las PNS5. Sin embargo, el resto de los ensayos clínicos2,4,6,7 y metaanálisis8,10 realizados desde entonces, concluyeron que la regresión de la MVI es independiente del tipo valvular empleado. Todos estos estudios fueron realizados en poblaciones anglosajonas con una SC media de 1,85 m2 frente a los 1,65 m2 del presente estudio3–10.
Al ser el implante de las PNS más dificultoso y precisar de mayores tiempos de isquemia, no creemos justificado su uso como primera elección, exceptuando casos concretos (depresión severa de la FE y gran HVI, intensa actividad física, elección del paciente)3–5.
El presente trabajo tiene las limitaciones propias de los estudios retrospectivos a pesar de realizarse un pareado mediante puntuación de propensión. Los resultados de los análisis mediante esta técnica están limitados por la posible presencia de sesgos debido a variables no medidas, interdependientes u ocultas. El bajo tamaño muestral condicionado por la escasa frecuencia de implante de PNS puede ser la causa de no detectar diferencias significativas.
Creemos que en las válvulas de menor tamaño, las diferencias entre bioprótesis no son lo suficientemente importantes como para provocar diferencias significativas en la regresión de la MVI, como ocurre en las bioprótesis de mayor tamaño.
Para confirmar estos hallazgos en nuestro medio, creemos precisos estudios prospectivos aleatorizados a largo plazo, utilizando modernas técnicas de medición de HVI como la resonancia magnética para confirmar definitivamente nuestros resultados.
ConclusiónEn pacientes con anillo aórtico pequeño de 19-21mm no encontramos diferencias estadísticamente significativas entre ambas bioprótesis en cuanto a supervivencia, clase funcional NYHA ni regresión del IMVI durante el seguimiento.
Son precisos estudios prospectivos aleatorizados para confirmar con mayor fiabilidad estos datos en nuestro medio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Premio Mejor Comunicación del XI Congreso Andaluz de Cirugía Cardiovascular 2011.