La rápida expansión de los procedimientos percutáneos dirigidos al tratamiento de diferentes patologías cardiacas, incluyendo la cardiopatía estructural, ha sido paralela al desarrollo de nuevas modalidades de imagen tridimensional. La tomografía computarizada y el ecocardiograma transesofágico en 3dimensiones proporcionan una gran resolución espacial y temporal, y al ser utilizados como apoyo en el intervencionismo conducen a la obtención de mayores tasas de éxito técnico y clínico, junto con una disminución del tiempo de radiación. En esta revisión abordamos el papel de la tomografía computarizada y el ecocardiograma transesofágico en 3dimensiones en procedimientos percutáneos como la valvuloplastia mitral, la reparación mitral mediante clip, la sustitución valvular aórtica y pulmonar, el cierre de dehiscencia periprotésica, la oclusión de la orejuela auricular izquierda y el cierre de la comunicación interauricular e interventricular.
The rapid expansion of transcatheter cardiovascular procedures for a wide range of cardiovascular conditions, including structural cardiac diseases, has been paralleled by novel three-dimensional approaches to imaging. Computed tomography and three dimensional transoesophageal echocardiography have high spatial and temporal resolution, and they help guide interventional procedures, leading to safer procedures with higher technical success, reduced radiation exposure, and improved patient outcomes. In this review, we discuss the roles of computed tomography and three dimensional transoesophageal echocardiography in percutaneous procedures such as mitral balloon valvuloplasty, mitral valve repair with clips, aortic and pulmonary valve replacement, paravalvular leak occlusion, left atrial appendage occlusion, and atrial and ventricular septal defect closure.
En los últimos años hemos asistido a una gran expansión del tratamiento percutáneo en cardiopatía estructural, habiéndose desarrollado y extendido técnicas que permiten la corrección de numerosas valvulopatías y de otras condiciones patológicas congénitas o adquiridas.
Las técnicas de imagen tradicionalmente empleadas en cardiología, principalmente la ecocardiografía en 2dimensiones y la fluoroscopia, permiten únicamente la adquisición de un limitado número de proyecciones bidimensionales que no pueden ser modificadas tras la fase de adquisición. La información así aportada será con frecuencia insuficiente para la planificación, la realización y la evaluación posterior al tratamiento percutáneo. La complejidad técnica de estos procedimientos exige un apoyo basado en la visualización detallada de las estructuras cardiacas y sus relaciones espaciales, lo cual puede ser proporcionado por las nuevas técnicas de imagen como son el ecocardiograma transesofágico en 3dimensiones (ETE3D), la tomografía computarizada (TC) y la resonancia magnética (RM) cardiaca. Estas permiten obtener tras la adquisición de imágenes un número infinito de cortes bidimensionales además de reconstrucciones tridimensionales.
El objetivo del trabajo que aquí presentamos es exponer el relevante papel que desempeñan actualmente las modernas técnicas de imagen cardiaca —principalmente el ETE3D y la TC— en el tratamiento percutáneo de los distintos tipos de cardiopatía estructural. De este modo abordaremos el tratamiento percutáneo de la estenosis y la regurgitación mitral, el implante de prótesis percutáneas en posición aórtica y pulmonar, el cierre de la dehiscencia periprotésica, la oclusión de la orejuela auricular izquierda y el cierre del foramen oval permeable, de la comunicación interauricular y de la comunicación interventricular.
Tratamiento percutáneo de la estenosis mitralLa valvuloplastia con balón constituye una alternativa eficaz y segura a la cirugía de sustitución valvular en pacientes seleccionados con valvulopatía mitral reumática.
La adecuada selección de pacientes es fundamental para el éxito del procedimiento. El método más validado es el score introducido por Wilkins, que evalúa mediante ecocardiograma transtorácico la extensión y la severidad de la calcificación de las valvas, su movilidad y la afectación del aparato subvalvular1. Cada ítem se puntúa de 1 a 4puntos, habiéndose relacionado una suma total mayor a 8puntos con pobres resultados tras la valvuloplastia. Además es necesario, de existir regurgitación mitral, cuantificarla de manera precisa ya que, como demostraron Palacios et al., un grado de regurgitación mitral ≥2+ se relaciona con peores resultados2.
No obstante, nuevas técnicas de imagen pueden mejorar la comprensión de la afectación de la estructura valvular. El ecocardiograma 3D permite, mediante visualización directa de la válvula mitral, analizar en detalle tanto la fusión de comisuras, que suele ser asimétrica, como la existencia de deformidad en el orificio mitral, que traduce con frecuencia afectación del aparato subvalvular y calcificación y/o cicatrización de las valvas, siendo todo ello determinante para el éxito del procedimiento. Además, la ausencia de trombos en la orejuela izquierda deberá ser asegurada mediante ecocardiograma transesofágico (ETE) antes de la realización de la valvuloplastia3.
Durante el procedimiento, la localización de la punción transeptal, que ha sido tradicionalmente guiada por fluoroscopia, puede ser mucho más precisa con ayuda de nuevas técnicas de imagen, evitando así el daño de estructuras cardiacas adyacentes. La punción puede ser dirigida mediante ETE3D, que permite visualizar múltiples planos simultáneos en 2D —especialmente útiles son el plano bicaval para determinar la altura de la punción y el eje corto a nivel de válvula aórtica para evaluar la distancia a la aorta— o bien la visión tridimensional, que permite visualizar el septo interauricular desde la perspectiva de la aurícula derecha, quedando la vena cava superior a las 12h y la vena cava inferior a las 6h4.
Asimismo, la adquisición de una TC cardiaca previa al procedimiento también permite elegir el lugar más apropiado para la punción transeptal. Además, la posterior fusión de estas imágenes (tabla 1) con la fluoroscopia permite, durante el procedimiento, guiar los catéteres hacia dicho punto, permitiendo el paso del balón a través del septo por el lugar más adecuado5.
Proceso de obtención de tomografía computarizada (TC) tridimensional y fusión con fluoroscopia en el laboratorio de hemodinámica
| 1. Adquisición de TC cardiaca y reconstrucción de las imágenes en 3 dimensiones |
| 2. Transferencia de imágenes a la estación de trabajo en el laboratorio de hemodinámica |
| 3. Marcar las áreas anatómicas de interés sobre la TC (p.ej., dehiscencia paravalvular, anillo valvular, defecto septal, zona de punción transapical…) |
| 4. Adquisición de imagen en fluoroscopia bidimensional |
| 5. Superponer estructuras radiopacas visibles en fluoroscopia (p.ej., cerclaje de esternotomía, válvulas mecánicas, soportes de válvulas biológicas, calcificaciones valvulares…) con las mismas estructuras identificadas en la TC |
| 6. Obtención de un plano de fluoroscopia ortogonal al primero |
| 7. Superposición de las mismas estructuras en este segundo plano con las imágenes de la TC |
Una vez en la válvula mitral, el correcto posicionamiento del balón durante el inflado puede ser valorado ecocardiográficamente. Para ello, las modalidades más empleadas son de nuevo las tridimensionales, mediante la adquisición de 2planos 2D ortogonales simultáneos o bien mediante la vista «de cirujano» —en la que observamos la válvula mitral desde la cara auricular, siendo la aorta rotada a la posición de las 12h y quedando la orejuela a las 9h—. Esta visión tridimensional ofrece la ventaja de poder rotar la imagen y obtener vistas del balón desde múltiples posiciones sin necesidad de cambiar el ángulo o sonda4.
Inmediatamente tras la valvuloplastia, el ETE es capaz de evaluar el éxito del procedimiento estimando área y gradientes mitrales, evaluando la existencia de regurgitación mitral, su cuantía y lugar de origen, así como la presencia de otras complicaciones, como derrame pericárdico. Puesto que en el momento post-valvuloplastia los gradientes transmitrales son poco fiables debido al cambio brusco de las condiciones hemodinámicas, la planimetría mediante ecocardiografía 3D aporta una medida más fidedigna3.
Tratamiento percutáneo de la regurgitación mitralHasta la fecha, el dispositivo más validado para el tratamiento de la regurgitación mitral es el clip mitral (Evalve, Inc., Menlo Park, California), que replica la técnica quirúrgica introducida por el Dr. Alfieri. Este sistema ha sido evaluado en los ensayos EVERESTI y II. En este último el dispositivo fue comparado con la cirugía reparadora mitral. Aunque el clip mitral resultó menos efectivo que la cirugía en cuanto a la reducción del grado de regurgitación, los resultados clínicos y la disminución del tamaño del ventrículo izquierdo fueron similares, siendo, además, el riesgo del procedimiento percutáneo bajo.
La selección de pacientes es crucial, ya que el dispositivo solo se considera adecuado para un perfil determinado de regurgitación mitral, con características similares a las que fueron incluidas en los ensayos mediante los que se ha testado el dispositivo5 (tabla 2).
Criterios anatómicos de elegibilidad para el estudio EVEREST II(Endovascular Valve Edge-to-Edge Repair Study)
| Regurgitación mitral funcional |
| Mecanismos |
| Dilatación del anillo |
| Restricción secundaria a remodelado ventricular izquierdo |
| Longitud de coaptación entra ambas valvas: ≤2mm |
| Profundidad de coaptación con respecto al anillo mitral: <11mm |
| Regurgitación mitral degenerativa por prolapso oflail |
| Profundidad del flail: <11mm |
| Anchura del flail en eje corto: <15mm |
El procedimiento de colocación del clip mitral es muy exigente y requiere una adecuada colaboración entre el cardiólogo intervencionista y el ecocardiografista. En este caso, el ecocardiograma 3D ofrece claras ventajas sobre el 2D, ya que el primero ofrece una mejor resolución espacial, lo que permite la correcta evaluación de la anatomía de cada uno de los segmentos valvulares además de la visualización de las guías, de los catéteres y del propio clip mitral.
La punción transeptal, que se puede realizar guiada ecocardiográficamente o por TC, tal y como se ha descrito en el procedimiento anterior, se realiza idealmente en una posición posterior y superior del tabique interauricular. Tras dilatar el orificio, el clip se avanza a la aurícula izquierda. El dispositivo de liberación debe alinearse paralelo al flujo mitral anterógrado, para lo cual se emplea en el eco 3D la visión «de cirujano» desde la perspectiva de la aurícula izquierda. La obtención de 2planos bidimensionales simultáneos —intercomisural a 50-70° y eje largo en este caso— es de gran utilidad para la alineación del clip mitral. Además, el dispositivo de liberación debe colocarse sobre la zona donde se origina la máxima regurgitación4.
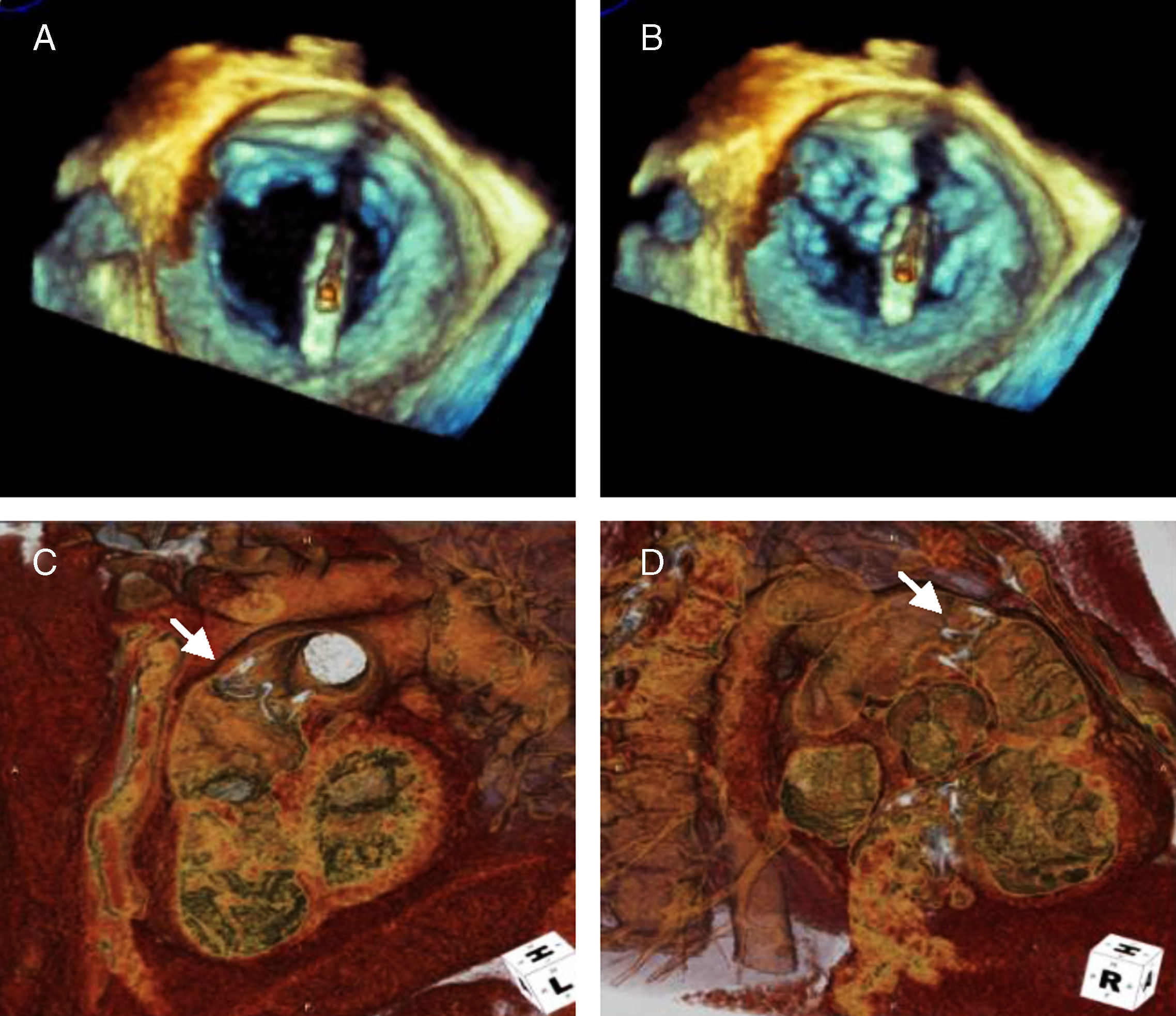
Una vez posicionado el dispositivo, los brazos del clip son desplegados y este es avanzado hacia el ventrículo izquierdo donde, empleando las vistas ecocardiográficas antes descritas, se reevalúa la correcta orientación y posición, siendo entonces liberado el dispositivo (fig. 1).
Tras la aproximación de ambas valvas, la severidad de la regurgitación mitral es de nuevo valorada. En caso de no haber disminuido considerablemente, el clip es recapturado y devuelto a la aurícula izquierda, iniciándose de nuevo el procedimiento de alineación y posicionamiento. En cambio, si la regurgitación mitral ha disminuido, el clip es liberado y se vuelve a cuantificar el grado de regurgitación mitral y la posible estenosis mitral que haya podido aparecer tras la colocación del dispositivo. Además, complicaciones como derrame pericárdico o defecto interauricular mayor del esperado deben ser valoradas.
Si la regurgitación residual fuese importante (>2+) y el gradiente transmitral no estuviera sustancialmente elevado, podría considerarse la colocación de un nuevo clip mitral3.
Otra posible opción para el tratamiento percutáneo de la regurgitación mitral, actualmente en fase de experimentación, es la introducción de un dispositivo de cerclaje en el seno coronario que trata de fruncir el anillo mitral del mismo modo que una anuloplastia quirúrgica. En este procedimiento, mostrar la longitud del seno coronario y su relación con estructuras vecinas como la arteria circunfleja es complicado por ETE, por lo que se realiza guiado mediante fluoroscopia y angiografía del seno coronario. Es posible que la TC fusionada con fluoroscopia pueda tener un papel en el futuro para establecer dichas relaciones.
Implante percutáneo de prótesis valvularesImplante valvular en posición aórticaEl implante transcatéter de válvula aórtica es actualmente una alternativa a la cirugía para el tratamiento de la estenosis aórtica en pacientes con alto riesgo quirúrgico. Hasta la fecha hay 2 dispositivos aprobados en Europa: la Edwards SAPIENS y la Medtronic CoreValve. Ambas son válvulas de tejido pericárdico suturadas respectivamente a un stent metálico montado sobre un balón o a una estructura de nitinol autoexpandible.
La selección de los pacientes en fundamental, ya que el diámetro del anillo valvular y el diámetro luminal de las arterias periféricas son los principales condicionantes que determinan la factibilidad del procedimiento.
El tamaño del anillo valvular se estima en la mayoría de los casos utilizando ecocardiografía bidimensional, aunque técnicas de imagen tridimensional como el ecocardiograma 3D, la TC o la RM han demostrado mayor precisión a la hora de medir el anillo aórtico. Recientemente, Ng et al. demostraron que, usando la TC como método de referencia, la ecocardiografía tendía a infraestimar el tamaño del anillo, siendo esta infraestimación mayor para el eco 2D (16,4%) que para el 3D (9,6%)6. Esto podría implicar diferencias a la hora de elegir el tamaño de prótesis a emplear en la práctica aunque, hasta la fecha, la mayoría de las series han empleado ecocardiografía bidimensional y sus resultados son buenos7.
La medición de los otros elementos de la raíz aórtica —senos de Valsalva, unión sinotubular y aorta tubular— pueden ser estimados de manera precisa por ecocardiografía, aunque la altura de los ostium coronarios es en ocasiones dificultosa por este método. La TC ha demostrado mayor resolución espacial para establecer su relación con los elementos del aparato valvular, siendo una altura de los ostium con respecto al anillo mayor de 10mm deseable para evitar la oclusión de los primeros durante el procedimiento.
El diámetro de las arterias periféricas es fundamental para planificar el abordaje del procedimiento. Aunque la angiografía es método de referencia, la pared de la arteria puede no ser evaluada de manera precisa y otras técnicas de imagen como la TC y el ETE —este último limitado a aorta torácica— pueden poner de manifiesto placas ateroscleróticas que, en caso de ser grandes (>4mm) y/o móviles, podrían contraindicar la vía de abordaje8.
Durante el procedimiento, la fluoroscopia sigue siendo el principal método para guiar el implante, usando la calcificación aórtica como principal marca de referencia. La mayor limitación de este método es la pobre resolución de los tejidos blandos, por lo que la combinación con otras técnicas de imagen permite una mayor precisión durante la colocación de la prótesis. La ecocardiografía es la técnica adyuvante de elección y permite, gracias a técnicas tridimensionales, una visualización simultánea del eje largo y corto valvular en tiempo real. El interés por las técnicas de fusión de fluoroscopia con TC o RM está creciendo y su empleo permite la identificación precisa del lugar idóneo para la liberación protésica así como de las estructuras adyacentes5. Un correcto posicionamiento de la prótesis permite evitar complicaciones como migración de la válvula, interferencia en la movilidad de la valva anterior mitral, del sistema de conducción cardiaco o de los ostium coronarios4.
Tras la liberación de la prótesis, la ecocardiografía permite valorar los gradientes transvalvulares así como la presencia de regurgitación valvular. En caso de regurgitación significativa se puede considerar la postdilatación con balón, el implante de una segunda válvula o, en caso de la CoreValve, también el reposicionamiento de la prótesis.
Durante el seguimiento, la ecocardiografía es también la técnica más empleada, tanto para la evaluación de la posición de la prótesis como su función, regurgitación y cambios en morfología del ventrículo izquierdo. La TC, gracias a su mayor resolución espacial, puede evaluar de manera más precisa la posición de la prótesis, ayudando a comprender mejor los mecanismos que subyacen a la regurgitación valvular7.
Implante valvular en posición pulmonarActualmente, la válvula disponible para implante percutáneo en posición pulmonar es la Medtronic Melody Transcatheter Pulmonary Valve, y es empleada fundamentalmente en pacientes con cardiopatías congénitas.
La ecocardiografía es la técnica de elección para la evaluación de los pacientes pre y post-procedimiento. Durante el implante, la fluoroscopia es la técnica de imagen de elección, aunque se han publicado casos en los que se han usado otras técnicas como la fusión de fluoroscopia con otras modalidades de imagen o la ecocardiografía intracardiaca, aunque su empleo no está aún estandarizado (fig. 1).
Cierre de la dehiscencia periprotésicaUn elevado porcentaje de las prótesis aórticas y mitrales presentan algún grado de insuficiencia periprotésica secundaria a dehiscencia de la sutura. Aunque en la mayoría de los casos este hecho se muestra clínicamente silente, del 1 al 3% de los pacientes con dehiscencia presentan síntomas secundarios, principalmente insuficiencia cardiaca congestiva y/o hemólisis. El tratamiento clásico es el cierre quirúrgico de la dehiscencia, pero este procedimiento se asocia en ocasiones a una elevada morbimortalidad en función de la comorbilidad del paciente. En estos casos aparece como una alternativa atractiva el cierre percutáneo del defecto periprotésico, que se ha mostrado factible, seguro técnicamente y efectivo a corto y largo plazo en el tratamiento de los síntomas asociados a la dehiscencia9.
En primer lugar, para la planificación del procedimiento es crucial la exacta localización de la dehiscencia, así como la definición de su forma y de su tamaño. De la localización dependerá la vía de abordaje inicial por la que se intentará atravesar el defecto, siendo las principales la arterial femoral, la transeptal y la transapical. Se recomienda, para estandarizar el modo de localización del defecto y así facilitar el entendimiento entre cardiólogo intervencionista y experto en técnicas de imagen, el uso del sistema de localización por horas del reloj. Por este método, la imagen de la válvula mitral será rotada hasta que la válvula aórtica se posicione a las 12h y la orejuela auricular izquierda a las 9h. La forma y el tamaño de la dehiscencia determinarán el tipo de dispositivo elegido inicialmente. Hay que tener en cuenta que no existen dispositivos diseñados específicamente para el cierre de los defectos paravalvulares, usándose generalmente el Amplatzer Patent Ductus Arteriosus en los de pequeño tamaño, y el Amplatzer Ventricular Septal Defect en los mayores. Para obtener el máximo de información en esta fase previa al procedimiento es recomendable integrar los datos procedentes de distintas técnicas de imagen, como son la TC con reconstrucción en 4dimensiones, el ecocardiograma transesofágico en 2dimensiones (ETE2D), y el ETE3D en las modalidades de tiempo real, zoom en tiempo real y volumen completo4.
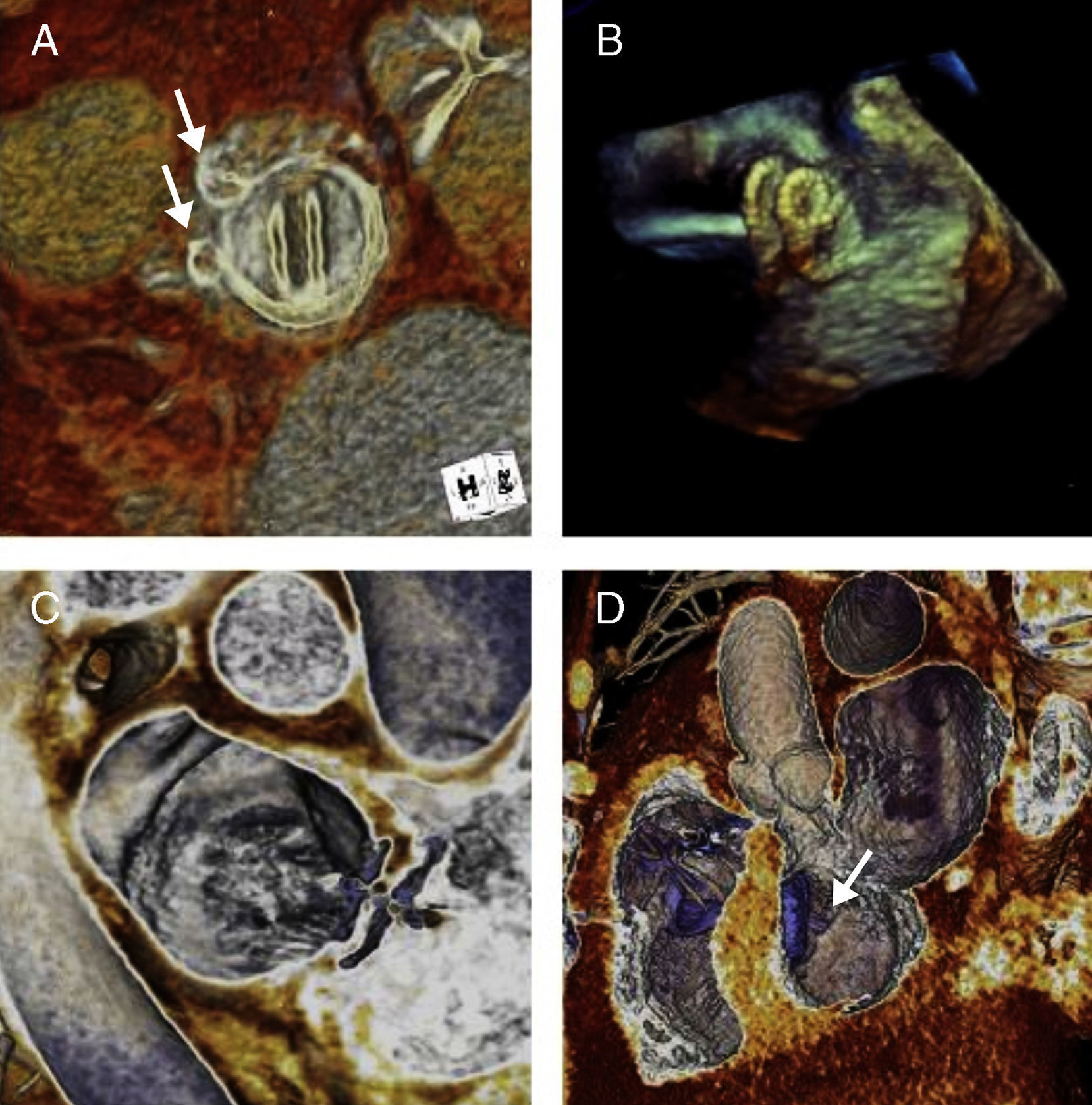
Durante el procedimiento será necesario guiar el catéter y el dispositivo a través de la dehiscencia periprotésica. El éxito de este paso depende en gran medida de la habilidad del operador y de la calidad de la información aportada por las técnicas de imagen, mostrándose como especialmente útiles el ETE3D en tiempo real, y la TC mediante su fusión con la fluoroscopia (fig. 2).
A)La imagen de TC muestra 2dispositivos de cierre de leak paravalvular aórtico. B)Imagen de ETE3D intraprocedimiento de cierre percutáneo de foramen oval permeable. C)Imagen de TC postprocedimento de cierre percutáneo de foramen oval permeable. D)La imagen de TC muestra cierre percutáneo de comunicación interventricular.
Posteriormente a la inserción del dispositivo, y antes de dar por finalizado el procedimiento, será necesaria la aportación del ETE3D en tiempo real para evaluar la presencia de regurgitación paravalvular residual que aconseje la inserción de un nuevo dispositivo oclusor, y descartar la interferencia del dispositivo con el funcionamiento de la prótesis valvular. Durante el seguimiento tras el procedimiento, el ETE2D y el ETE3D permitirán evaluar las posibles complicaciones secundarias, como son el desarrollo de una nueva dehiscencia periprotésica, la embolización del dispositivo y la citada interferencia con la prótesis valvular.
Oclusión de la orejuela auricular izquierdaLa oclusión percutánea de la orejuela auricular izquierda en pacientes con fibrilación auricular no valvular es una estrategia segura y eficaz para la prevención del ictus, la embolia sistémica y la muerte cardiovascular. Actualmente se encuentran en uso 2tipos de dispositivos: el Watchman y el Amplatzer Cardiac Plug. Aunque el papel exacto de esta técnica no está completamente definido, son candidatos a la oclusión los pacientes en los que a un elevado riesgo trombótico se añade un alto riesgo hemorrágico o alguna contraindicación absoluta para la anticoagulación oral a largo plazo.
La evaluación previa al procedimiento mediante ecocardiograma transesofágico y/o TC es necesaria para determinar la elegibilidad de los pacientes. El principal criterio de exclusión es la presencia de trombo en la orejuela auricular izquierda. Es fundamental la medición del ostium y de la longitud máxima de la orejuela, lo cual puede realizarse mediante ETE2D a través de múltiples planos, o de manera más sencilla con ETE3D, usando el modo zoom en tiempo real y posicionando la orejuela en el centro de la imagen, la válvula mitral a las 6h y la vena pulmonar superior izquierda a las 12h. Esta última modalidad proporciona además información adicional en los casos de morfología atípica o de ostium irregular. De este modo se realiza una estimación inicial del tamaño del dispositivo de cierre, cuyo diámetro ha de ser algo superior al del ostium para evitar complicaciones como la embolización del mismo, o el flujo residual2. Respecto a esta evaluación inicial, se ha propuesto que el ETE2D infraestima el tamaño del ostium de la orejuela al compararlo con el ETE3D, y que este último se correlaciona bien con la TC10.
Una vez iniciado el procedimiento, tanto la TC mediante fusión con la fluoroscopia como el ETE3D permiten guiar la punción transeptal y evaluar la correcta localización del dispositivo, siendo necesario comprobar el perfecto sellado del ostium de la orejuela, así como la ausencia de interferencia con el flujo de las venas pulmonares o con la válvula mitral.
Tras el implante, se recomienda un seguimiento ecocardiográfico al mes, a los 6meses y anualmente. La imagen 3D en modo zoom en tiempo real permite una visualización del volumen de la orejuela y su relación espacial con el dispositivo oclusor, lo cual potencialmente podría optimizar el diagnóstico precoz de complicaciones como la existencia de comunicación residual, trombosis o desplazamiento del dispositivo.
Cierre de la comunicación interauricular y del foramen oval permeableEl cierre percutáneo de la comunicación interauricular es un procedimiento que ha mostrado excelentes resultados a corto y a largo plazo, evitando además las complicaciones derivadas de la cirugía abierta, de modo que se ha convertido en una alternativa a esta última.
El ETE2D se ha usado tradicionalmente durante la evaluación previa al procedimiento, determinando la localización, la forma y el tamaño del defecto septal y el tamaño del tejido residual adyacente a los bordes, siendo esto último de crucial importancia para la factibilidad del cierre percutáneo. El ETE3D en tiempo real permite una mejor caracterización del tamaño y de la morfología del defecto e identifica con facilidad defectos complicados, como es el caso de la presencia de múltiples fenestraciones en el tabique interauricular. Se ha publicado escasa información acerca del papel de la TC en la planificación previa al procedimiento. En el trabajo publicado por Ko et al.11 la TC ofreció una medición más precisa del eje largo del defecto septal que la ETE2D en niños.
El procedimiento de cierre percutáneo se realiza casi exclusivamente con guía ecocardiográfica, clásicamente mediante ETE2D o mediante ecocardiografía intracardiaca. Actualmente, el ETE3D en tiempo real ha optimizado la elección intraprocedimiento del tamaño del dispositivo de cierre, pues permite comprobar, mediante la ausencia de flujo por Doppler color, que el balón inflado ha obliterado totalmente la comunicación. Además, es la única modalidad ecocardiográfica que permite asegurar que la liberación del dispositivo se realiza de manera completamente perpendicular al plano del defecto (fig. 2). De este modo, se ha publicado que el ETE3D en tiempo real puede disminuir el tiempo de fluoroscopia respecto al ETE2D12.
Tras el implante, el ETE3D en tiempo real permite la visualización con gran precisión de ambas caras del dispositivo y su tejido adyacente, comprobando la ausencia de flujo residual a través del septo, la correcta alineación del dispositivo y la ausencia de interferencia del mismo con respecto a las estructuras anatómicas vecinas.
Cierre de la comunicación interventricularLa aproximación percutánea ha aparecido como una alternativa segura y efectiva al cierre quirúrgico de la comunicación interventricular. La vía no invasiva presenta un especial interés, debido al elevado riesgo quirúrgico, en los casos de etiología adquirida (postinfarto de miocardio) y en los casos de origen congénito que han presentado una cirugía cardiaca previa.
La evaluación previa al procedimiento mediante ETE3D en tiempo real permite examinar el defecto y sus bordes desde ambas caras ventriculares, determinando la localización, la forma y el área del mismo con mayor precisión que el ETE2D, permitiendo establecer la factibilidad del cierre percutáneo y realizar una aproximación preliminar para la elección del dispositivo necesario para el cierre4. La evidencia presentada en la bibliografía acerca de la utilidad de la TC para la planificación del cierre percutáneo de la comunicación interventricular es escasa, aunque su utilidad se presume elevada, en virtud de la gran información anatómica que aporta esta técnica debido a su resolución espacial.
Durante el procedimiento, el ETE3D en tiempo real permite la completa visualización de los catéteres situados en las cámaras cardiacas, facilitando la navegación del dispositivo oclusor y su posterior colocación a través del defecto septal. Esta operación puede ser guiada también por TC mediante la tecnología de la fusión que, como se explicó anteriormente, permite superponer la imagen previamente adquirida en el tomógrafo con la obtenida mediante fluoroscopia (fig. 2).
Una vez finalizado el procedimiento, el ETE3D permite evaluar, con mayor precisión que el ETE2D, la posición y la alineación del dispositivo, la presencia de flujo residual entre ambos ventrículos por Doppler color, y la posible interferencia del dispositivo con las estructuras adyacentes.
ConclusiónLa rápida expansión del tratamiento percutáneo en cardiopatía estructural debe ir paralela al desarrollo de nuevas técnicas de imagen tridimensional que proporcionen la información necesaria para la planificación y la realización del procedimiento. En este contexto, la ecocardiografía transesofágica en 3dimensiones y la tomografía computarizada se han convertido en herramientas fundamentales para garantizar el éxito de un procedimiento, y se postulan además como base necesaria para el desarrollo de nuevas técnicas percutáneas para el tratamiento de otros tipos de cardiopatía estructural.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.