Comparar, utilizando fuentes secundarias, sensibilidad, especificidad y eficiencia, entre Mantoux y técnicas de inmunoferón-γ.
DiseñoEstudio de revisión bibliográfica con fuentes de información de alta evidencia científica.
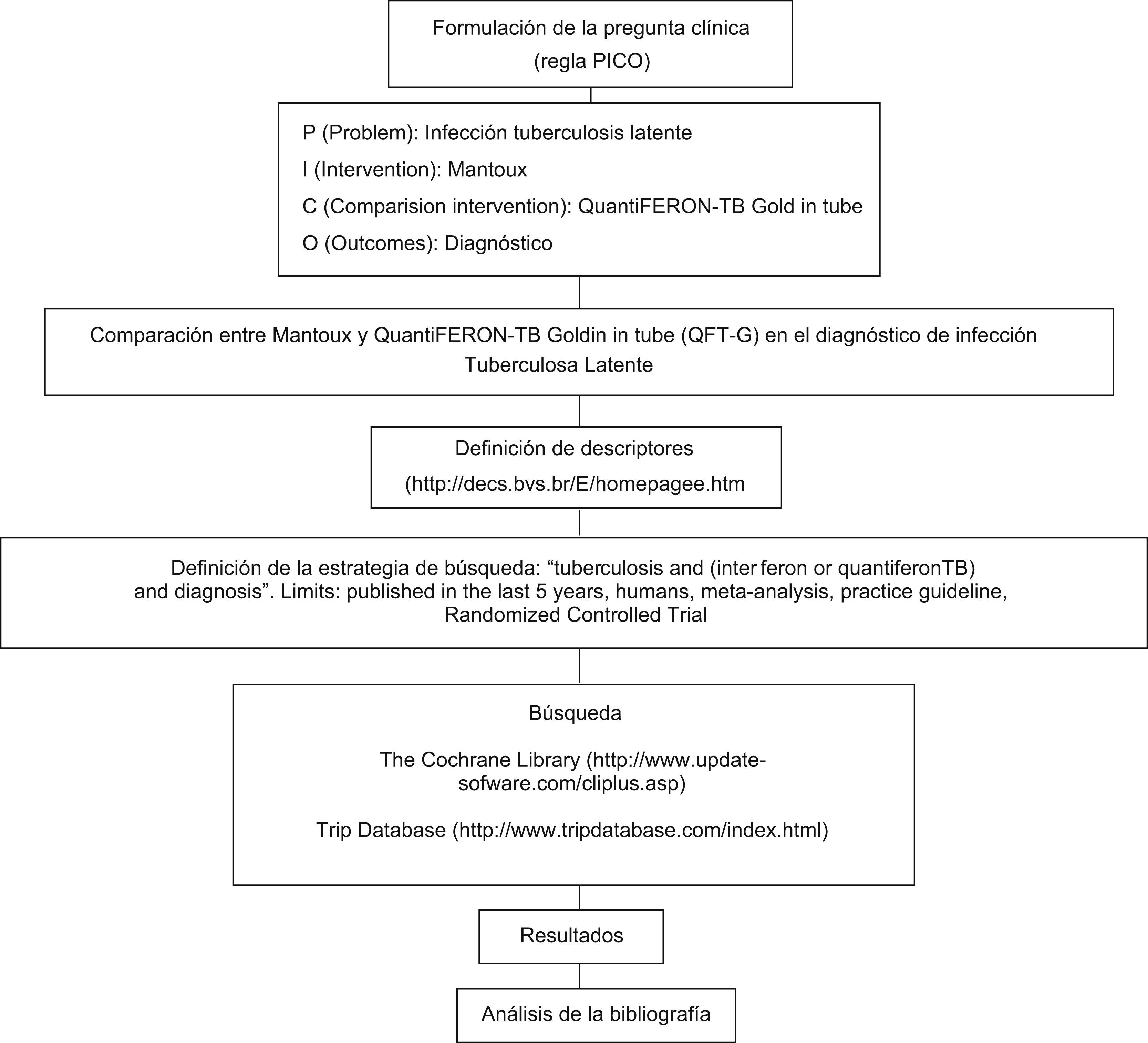
Fuentes de datosBúsqueda bibliográfica en las bases de datos Cochrane y Trip Database. Estrategia de búsqueda: «tuberculosis and (interferon or quantiferon or quantiferonTB) and diagnosis». Límites: publicado en los últimos 5 años, seres humanos, metaanálisis, guía de práctica clínica, Ensayo aleatorio controlado. Se concluye la búsqueda en octubre de 2009.
Selección de los estudiosLocalizamos 3 guías de práctica clínica y 9 artículos que incluyen una revisión sistemática, un metaanálisis, un artículo sobre sensibilidad de las nuevas técnicas, 3 estudios sobre coste-eficiencia y 3 estudios prospectivos sobre el papel de la liberación de inmunoferón-γ en el diagnóstico de tuberculosis.
ResultadosLas nuevas técnicas presentan mayor especificidad que el Mantoux para diagnóstico de la infección tuberculosa latente en contactos vacunados en infancia con BCG. La estrategia diagnóstica más coste-efectiva para la infección tuberculosa latente fue screening con Mantoux y confirmación con QuantiFERON-Gold in tube.
ConclusiónDeberían coordinarse los recursos y limitar su uso en los estudios de contactos a adultos inmunocompetentes vacunados con BCG, con Mantoux superior a 5mm o casos con tuberculina dudosa.
To compare the sensitivity, specificity and efficiency between Mantoux and Interferon-gamma techniques, using secondary sources.
DesignStudy of the published literature with a high evidence-based sources of scientific information.
Data sourcesA bibliographic search in the Cochrane database and Trip-database.
Study selectionWe found three Clinical Practice Guidelines and nine articles, which included one Systematic Review, one Meta-analysis, one article on the sensitivity of the new techniques, three cost-efficiency studies, and three prospective studies on the role of interferon-gamma release in the diagnosis of TB.
ResultsThe new techniques have a higher specificity than Mantoux for the diagnosis of LTBI in contacts vaccinated in childhood with BCG. The most cost-effective diagnostic strategy for LTBI was Mantoux screening and confirmation with QFT-G.
ConclusionResources should be coordinated, limiting its use in studies of contacts in immunocompetent adults vaccinated with BCG, with Mantoux>5mm or Tuberculin doubtful cases.
Como se recoge en protocolos y guías de práctica clínica, en el control de la tuberculosis (TBC) se dispone, entre otras medidas, del diagnóstico precoz, el aislamiento respiratorio, la instauración del tratamiento y el estudio de contactos para detectar y tratar la infección tuberculosa latente (ITL); se detiene así el avance de la enfermedad en la comunidad. La prueba de screening clásica en los protocolos de estudios de convivientes con TBC es el Mantoux, que evidencia un estado de hipersensibilidad frente a proteínas del bacilo tuberculoso que aparece tras una infección por Mycobacterium tuberculosis. Se realiza mediante inoculación intradérmica de 2 unidades de tuberculina PPD RT-23 o 5 unidades de PPD CT-6816-18, ambas dosis bioequivalentes a 5 unidades de PPD-S, tuberculina preparada en 1939 por Seibert y aceptada como estándar internacional en 19511. En la dermis se produce una reacción inflamatoria con infiltración celular, lo que da lugar a una induración medida en milímetros tras 72h. No obstante, esta técnica puede dar falsos positivos en vacunados con BCG (vacuna para TBC fabricada con bacilos vivos atenuados de una cepa de Mycobacterium bovis o bacilo de Calmette-Guerin que deja inmunidad parcial). Esta vacuna no se utiliza en España desde 1980 (1974 en Cataluña), y se mantiene sólo en el País Vasco. Así, en nuestra población, los contactos de determinada edad han podido vacunarse y han producido falsos positivos. El fenómeno de la inmigración hace que determinadas enfermedades puedan aumentar su incidencia2, y hay que tener en cuenta que en determinados países del Magreb es habitual la BCG dentro del calendario de vacunación, lo que aumenta los falsos positivos. En nuestra área, Campo de Gibraltar, la inmigración del Magreb tiene destacada influencia en aspectos socioeconómicos de la población. El protocolo de estudio de convivientes vigente en la Comunidad Autónoma de Andalucía no se actualiza desde 20023. Hay propuestas de actualización a nivel nacional por parte del Grupo de Trabajo de Expertos en Tuberculosis y del Grupo de Trabajo en Comunidades para el tratamiento clínico de la TBC y su prevención4.
Desde hace poco se investiga con test basados en la detección del inmunoferón (IFN) γ liberado por las células de serie blanca sensibilizadas tras incubación de sangre completa con el antígeno determinado. Entre estos test tenemos el QuantiFERON-TB test® (QFT) y el QuantiFERON-Gold in tube (QFT-G), que usan diferentes antígenos para estimular liberación de IFN-γ. El QFT está indicado como ayuda en el diagnóstico de la ITL y el QFT-G está indicado tanto en ayuda para diagnóstico de la ITL como de la TBC. Otro test es T-SPOT.TB, donde la interpretación se basa en el recuento de linfocitos T productores de IFN-γ (en unidades denominadas SPOT) y la diferencia de producción entre sujetos sanos y sujetos en estudio.
Los Centers for Disease Control and Prevention (CDC) norteamericanos, en su última actualización de protocolos de estudios de contactos con TBC5, tratan el papel de estas técnicas, especialmente en caso de contactos vacunados en infancia, y su influencia en mejorar la especificidad. También la última actualización de la Sociedad Española de Neumología y Cirugía Torácica introduce las técnicas de IFN-γ dentro del capítulo de diagnóstico de la ITL, y las utiliza junto con Mantoux. En su algoritmo utilizan screening con tuberculina y confirmación con IFN-γ solo en pacientes vacunados6. Sin embargo, los protocolos utilizados en Atención Primaria no incluyen estas pruebas y su acceso se limita a proyectos de investigación. Las dudas sobre efectividad y eficiencia podrían limitar su instauración generalizada.
ObjetivoComparar utilizando fuentes secundarias, Mantoux y las técnicas de IFN-γ en términos de sensibilidad, especificidad y eficiencia.
Material y métodoLas bases de datos escogidas para nuestra búsqueda fueron Cochrane Library (disponible en: http://www.update-software.com/Clibplus/ClibPlus.asp) y el metabuscador Trip Database (disponible en: http://www.tripdatabase.com/index.html). El motivo de elección de ambas bases fue el hecho de que solo incluyen trabajos filtrados, analizados por su nivel de evidencia científica, y facilitan de esta forma el acceso a información de alta calidad7. No se utiliza el buscador PubMed (disponible en: http://www.ncbi.nlm.nih.gov/pubmed) al no realizar este filtro, lo que complica, por tanto, el proceso de selección.
Para definir nuestros descriptores, utilizamos el recurso disponible en http://decs.bvs.br/E/homepagee.htm, enlace de la Biblioteca Virtual en Salud (disponible http://en:bvs.isciii.es/E/index.php) del Instituto Carlos III para encontrar el descriptor en castellano y su equivalente inglés.
La estrategia de búsqueda utilizada fue «tuberculosis and (interferon or quantiferon or quantiferonTB) and diagnosis». Límites: publicado en los últimos 5 años, seres humanos, meta-análisis, guía de práctica clínica, Ensayo aleatorio controlado. Se concluye la búsqueda en octubre de 2009.
ResultadosLas publicaciones halladas de esta forma incluyen 3 guías de práctica clínica y 9 artículos que contienen una revisión sistemática y un metaanálisis.
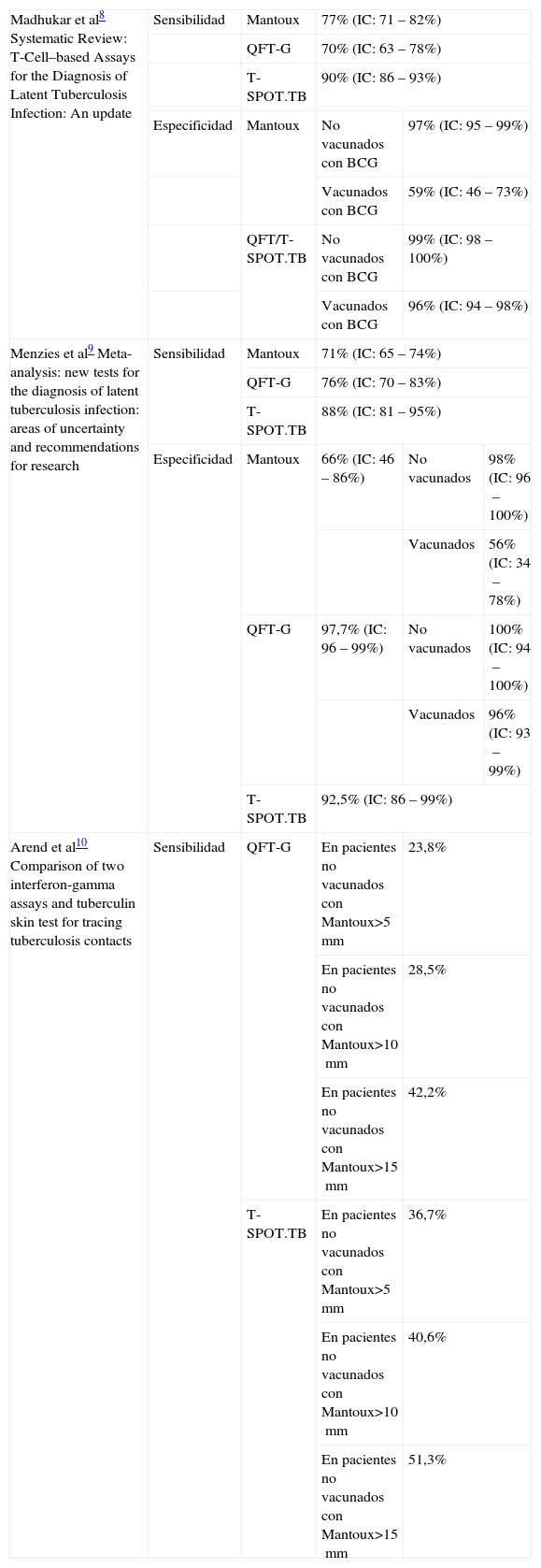
Esta revisión sistemática compara los nuevos test con Mantoux para el diagnóstico de la ITL. Incluye 38 artículos con un total de 1.879 pacientes hasta el 31-03-2008. Por su lado, el metaanálisis encontrado también para el diagnóstico de la ITL incluye 58 estudios con 8.751 individuos; la búsqueda finaliza el 31-10-2006. Ambos estudios se centran en la sensibilidad y la especificidad de estas pruebas al compararlas con Mantoux. Sus resultados se resumen en la tabla 1. El trabajo de Arend et al, realizado en un estudio de contactos de un paciente con TBC pulmonar bacilífera con 785 sujetos no vacunados con BCG en población alemana, estudia la sensibilidad para las técnicas de liberación IFN-de γ y relaciona esta sensibilidad con diferentes puntos de corte en el resultado del Mantoux de los sujetos (tabla 1).
Resultados sobre sensibilidad y especificidad para Mantoux y técnicas de liberación de inmunoferón-γ en la bibliografía consultada
| Madhukar et al8 Systematic Review: T-Cell–based Assays for the Diagnosis of Latent Tuberculosis Infection: An update | Sensibilidad | Mantoux | 77% (IC: 71–82%) | ||
| QFT-G | 70% (IC: 63–78%) | ||||
| T-SPOT.TB | 90% (IC: 86–93%) | ||||
| Especificidad | Mantoux | No vacunados con BCG | 97% (IC: 95–99%) | ||
| Vacunados con BCG | 59% (IC: 46–73%) | ||||
| QFT/T-SPOT.TB | No vacunados con BCG | 99% (IC: 98–100%) | |||
| Vacunados con BCG | 96% (IC: 94–98%) | ||||
| Menzies et al9 Meta-analysis: new tests for the diagnosis of latent tuberculosis infection: areas of uncertainty and recommendations for research | Sensibilidad | Mantoux | 71% (IC: 65–74%) | ||
| QFT-G | 76% (IC: 70–83%) | ||||
| T-SPOT.TB | 88% (IC: 81–95%) | ||||
| Especificidad | Mantoux | 66% (IC: 46–86%) | No vacunados | 98% (IC: 96–100%) | |
| Vacunados | 56% (IC: 34–78%) | ||||
| QFT-G | 97,7% (IC: 96–99%) | No vacunados | 100% (IC: 94–100%) | ||
| Vacunados | 96% (IC: 93–99%) | ||||
| T-SPOT.TB | 92,5% (IC: 86–99%) | ||||
| Arend et al10 Comparison of two interferon-gamma assays and tuberculin skin test for tracing tuberculosis contacts | Sensibilidad | QFT-G | En pacientes no vacunados con Mantoux>5mm | 23,8% | |
| En pacientes no vacunados con Mantoux>10mm | 28,5% | ||||
| En pacientes no vacunados con Mantoux>15mm | 42,2% | ||||
| T-SPOT.TB | En pacientes no vacunados con Mantoux>5mm | 36,7% | |||
| En pacientes no vacunados con Mantoux>10mm | 40,6% | ||||
| En pacientes no vacunados con Mantoux>15mm | 51,3% | ||||
BCG: vacuna antituberculosa; IC: intervalo de confianza; QFT-G: QuantiFERON-Gold in tube.
Sobre eficiencia encontramos 3 estudios:
El trabajo alemán sobre coste-eficiencia de Diel et al, donde contrastan 4 cohortes con diferentes métodos diagnósticos para ITL. Un grupo utiliza Mantoux con criterio diagnóstico de 10mm de induración, un segundo grupo utiliza Mantoux con 5mm de induración y otro grupo utiliza QFT-G. En el cuarto grupo utilizan un proceso en 2 pasos: primero screening con Mantoux de 5mm y después QFT-G para confirmación. El grupo más coste-efectivo fue el de 2 pasos. El NNT para prevenir un caso de ITL fue de 40 para Mantoux de 10mm, de 96 para Mantoux de 5mm y de 22 para los 2 pasos y QFT-G. Los mismos autores presentan un estudio de cohortes de contactos de TBC en un período de 2 años. Se comparan los costes para el servicio de salud pública alemán entre Mantoux y QFT-G para el diagnóstico de ITL. Se utilizaron 3 grupos. El primero utilizó solo QFT-G, el segundo utilizó Mantoux como screening y QFT-G como confirmación, y el tercero utilizó los 2 pasos pero en pacientes vacunados. Al utilizar los 2 pasos se redujeron los costes en un 43% entre los pacientes no vacunados y un 39% entre los vacunados. El ahorro estimado al utilizar 2 pasos (independientemente de la vacuna) fue de 29,77 euros/paciente, asumiendo un gasto de 91,06 euros/paciente al utilizar solo Mantoux.
Otro estudio de coste-eficiencia canadiense compara varias estrategias diagnósticas para descartar TBC activa en población inmigrante. El procedimiento más eficiente fue radiografía de tórax frente al Mantoux y el QFT. Sin embargo, entre pacientes vacunados, el QFT pareció ser más coste-efectivo.
Encontramos 3 guías de práctica clínica:
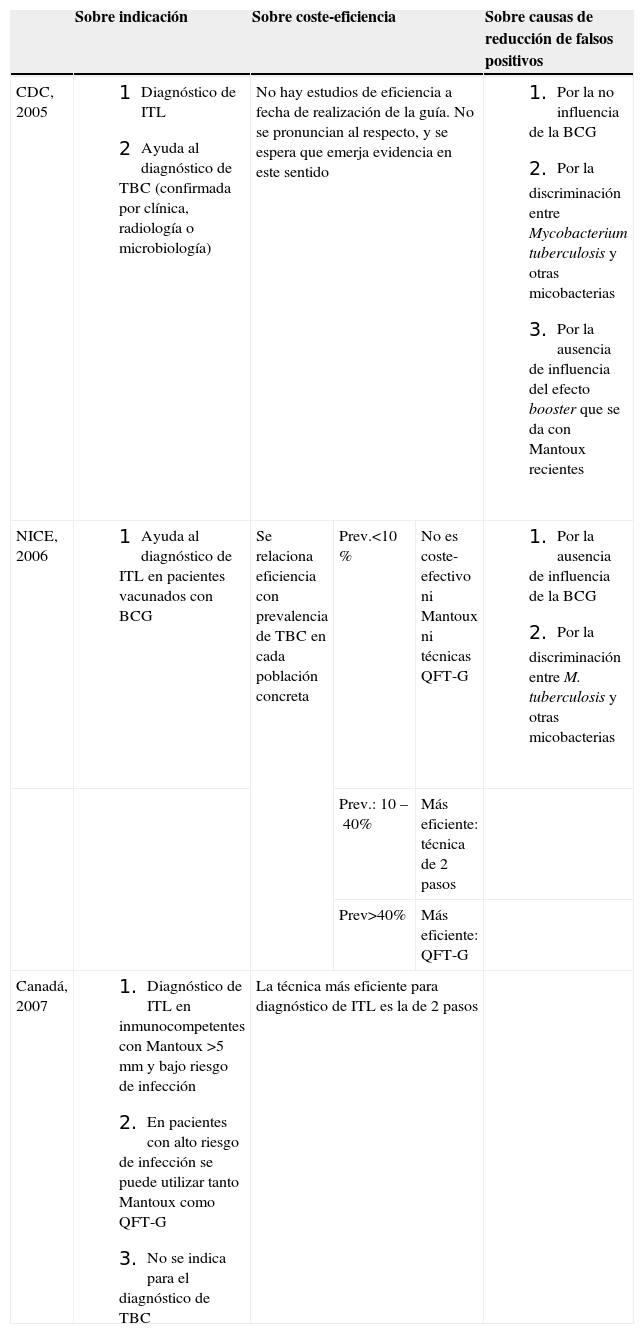
La guía de los CDC estadounidenses específica para el diagnóstico de ITL de 2005, la guía inglesa de TBC NICE de 2006 y la guía sobre técnicas de liberación de IFN-γ del Canadian Tuberculosis Committee de 2007. Las guías CDC y NICE especifican un descenso de falsos positivos en el diagnóstico de la ITL con la utilización de estas técnicas. Las principales diferencias sobre indicación, coste-eficiencia y causas de la reducción en el número de falsos positivos entre estas guías están reflejadas en la tabla 2.
Diferencias encontradas en las guías de práctica clínica localizadas en nuestra búsqueda sobre la utilización de técnicas de liberación de inmunoferón-γ
| Sobre indicación | Sobre coste-eficiencia | Sobre causas de reducción de falsos positivos | |||
| CDC, 2005 |
| No hay estudios de eficiencia a fecha de realización de la guía. No se pronuncian al respecto, y se espera que emerja evidencia en este sentido |
| ||
| NICE, 2006 |
| Se relaciona eficiencia con prevalencia de TBC en cada población concreta | Prev.<10 % | No es coste-efectivo ni Mantoux ni técnicas QFT-G |
|
| Prev.: 10–40% | Más eficiente: técnica de 2 pasos | ||||
| Prev>40% | Más eficiente: QFT-G | ||||
| Canadá, 2007 |
| La técnica más eficiente para diagnóstico de ITL es la de 2 pasos | |||
BCG: vacuna antituberculosa; CDC: Centers for Disease Control and Prevention; ITL: infección tuberculosa latente; NICE: National Institute for Clinical Excellence; Prev.: prevalencia; QFT-G: QuantiFERON-Gold in tube; TBC: tuberculosis.
Encontramos 3 estudios prospectivos referentes al papel que representa el IFN-γ en el diagnóstico de la TBC pulmonar bacilífera. En el trabajo de Kang et al con 144 pacientes en Seúl se encuentra que tanto el QFT-G como el T.SPOT.TB presentan alto valor predictivo negativo y bajo valor predictivo positivo para el diagnóstico de TBC. En los resultados de otro estudio multicéntrico de 148 pacientes, Mazurek et al hallan que tanto el Mantoux como el QFT y el GFT-G tienen la misma sensibilidad para el diagnóstico de TBC, pero tanto con tuberculina como con IFN-γ no se podría descartar TBC en caso de resultado negativo. Gerogianni et al encuentran que solo un 68% de 191 pacientes con baciloscopias positivas presentó positivos los Mantoux y los QFT-G.
DiscusiónLos datos de la revisión sistemática de Madhukar Pai et al8 muestran que tanto Mantoux como estas técnicas presentan una sensibilidad aceptable y, en concreto, el T-SPOT.TB fue superior a la tuberculina, mientras que el QFT-G fue similar. Sin embargo, en el caso de la especificidad, parece superior para los nuevos test en pacientes vacunados y similar entre pacientes no vacunados.
Por otro lado, en el metaanálisis de Menzies et al9 las sensibilidades tanto del QFT-G como del T-SPOT.TB se parecen, como muestran los intervalos de confianza. Al compararlos con el Mantoux, nuevamente el T-SPOT.TB presenta una sensibilidad mayor, mientras que no hay apenas diferencias con respecto al QFT-G. Se observa otra vez cómo presentan mayor especificidad las nuevas técnicas al compararlas con Mantoux, fundamentalmente en pacientes vacunados.
El estudio de Arend et al10 presenta una sensibilidad muy baja de estas técnicas, si bien hay que tener en cuenta que se realiza en pacientes no vacunados con BCG y que la población de referencia presenta una reducida prevalencia de ITL.
En coste-eficiencia11–13, la mayor eficiencia de los 2 pasos se explicaría por el descenso de falsos positivos, lo que implicaría menos tratamientos innecesarios. Así, en el trabajo de Diel et al hay disminución de falsos positivos en un 77% al comparar los 2 pasos y un Mantoux de 5mm. También la guía del Canadian Tuberculosis Committee y el NICE determinan como estrategia diagnóstica más coste-efectiva en su medio los 2 pasos, de hecho, en la población inglesa el gasto de esta estrategia fue de 26 libras per quality-adjusted life-year en contraposición a 150 libras per quality-adjusted life-year del QFT-G.
A pesar de la mayor especificidad de estas técnicas en las guías de práctica clínica consultadas14–16 por la no influencia de la BCG, la desaparición del efecto booster al no exponer al paciente a ningún antígeno y la discriminación con otras micobacterias tienen limitaciones.
No hay suficientes evidencias para usarlas en pacientes con VIH, inmunodeprimidos o tratados con antagonistas TNF-α. No obstante, la guía canadiense comenta que en estos pacientes se puede utilizar IFN-γ para confirmar un Mantoux positivo, pero no descartaría infección si el IFN-γ fuera negativo. La guía NICE solo encuentra un estudio favorable al QFT-G en VIH, pero con problemas metodológicos en su diseño. Tampoco existen suficientes evidencias, según las guías, para recomendar su uso en pediatría, y en estos casos se utiliza tuberculina.
Otro problema que apuntan los CDC es que el QFT-G no solventa el problema del período ventana que plantea el Mantoux. Esto obliga a repetir la prueba en 8-10 semanas si es negativa y a instaurar quimioprofilaxis hasta confirmar el resultado.
Para los CDC, la sensibilidad del QFT-G es inferior que la del Mantoux, pero ese inconveniente puede solventarse con los 2 pasos, con los que se gana sensibilidad con el Mantoux en el primer paso y especificidad con el QFT-G en el segundo paso.
La guía canadiense no recomienda su utilización para screening de TBC en poblaciones expuestas, trabajadores sanitarios, presos o personal de prisiones, pues la evidencia científica es escasa. En estos casos recomiendan Mantoux. Esta guía no recomienda la utilización ni de tuberculina ni de IFN-γ para screening de enfermedad entre inmigrantes, solo se realizaría screening con Mantoux al presentar características clínicas o epidemiológicas que impliquen factores de riesgo para TBC. El estudio de Mazurek et al17 tampoco las indica para diagnóstico de TBC, al tener la misma sensibilidad que el Mantoux, y tampoco Gerogianni et al18 las recomiendan para este fin por su baja especificidad.
Por los datos de la guía NICE y el estudio de Kang et al19, sería importante obtener datos sobre la prevalencia de la TBC y valorar la idoneidad de introducir QFT-G en cada población, de hecho, para la población de Seúl la alta prevalencia de TBC limita su uso. Para este fin serían de ayuda estudios epidemiológicos de la zona en concreto a fin de obtener datos sobre contactos que por edad u origen pudieran haberse vacunado.
En la bibliografía consultada no encontramos referencias al papel del IFN en reinfecciones tuberculosas. En un estudio de convivientes podemos encontrar pacientes infectados en estudios anteriores ya tratados correctamente. Un nuevo Mantoux será positivo y solo un aumento en milímetros con respecto al Mantoux anterior o aspectos epidemiológicos del tipo de contacto nos hará sospechar nueva infección y plantearnos nuevo tratamiento. Al no quedar esta cuestión resuelta, la indicación de tratamiento continúa siendo una cuestión clínica y epidemiológica. El actual protocolo recomienda no instaurar tratamientos si el paciente cumplió correctamente uno previo.
- •
Para diagnosticar infección tuberculosa latente, el test clásico es el Mantoux.
- •
Hay nuevas publicaciones sobre técnicas basadas en detección de inmunoferón-γ.
- •
Los protocolos utilizados en Atención Primaria no incluyen estas pruebas. Las dudas sobre efectividad y eficiencia podrían limitar su instauración generalizada.
- •
Las nuevas técnicas de liberación de inmunoferón-γ presentan, según la evidencia científica disponible, mayor especificidad que el Mantoux para el diagnóstico de la infección tuberculosa latente en el caso de contactos con tuberculosis pulmonar activa vacunados en la infancia con BCG.
- •
La estrategia diagnóstica más coste-efectiva para la infección tuberculosa latente consiste en screening con Mantoux y confirmación con QuantiFERON-Gold in tube.
- •
Deberían coordinarse los recursos y limitar su uso en los estudios de contactos a adultos inmunocompetentes vacunados de BCG, con Mantoux superior a 5mm o casos con tuberculina dudosa.