Introducción
La diabetes mellitus (DM) es una enfermedad crónica que cursa con una lenta degeneración del sistema vascular. Una de sus complicaciones es el pie diabético, y la isquemia, un factor etiopatogénico esencial. La glucación no enzimática de proteínas de la membrana basal endotelial altera, entre otras funciones, la síntesis de heparán sulfato1, notable activador endógeno de la antitrombina III, que parece desempeñar un papel fundamental en el mantenimiento de la homeostasis y la función endotelial2, responsable, al menos en parte, de la angiopatía y de las úlceras del pie diabético.
Es característica la mala evolución de la lesión3. Un tercio de los pacientes será amputado al cabo de 3 años4.
La heparina estimula la síntesis de heparán sulfato en cultivos de células endoteliales5. Su efecto en la angiopatía diabética ha sido estudiado en animales de experimentación y se han evidenciado cambios positivos en la membrana basal endotelial6,7. En humanos se ha observado una disminución del número de exudados duros en pacientes diabéticos con retinopatía8 y una disminución de la proteinuria9. Diversos autores han estudiado el efecto en el pie diabético, con resultados controvertidos10,11.
Los pacientes con úlcera diabética, excepto cuando se complican, siguen al cuidado del equipo de atención primaria. Las observaciones realizadas previamente por los investigadores12, la escasa pero existente bibliografía y el excelente perfil de seguridad de las heparinas de bajo peso molecular (HBPM) nos animan a realizar esta investigación con la intención de mejorar la evolución de las úlceras, disminuir la incidencia de sus terribles consecuencias, aumentar la calidad de vida del paciente y, eventualmente, reducir los costes sociales y sanitarios de este problema de salud.
Objetivos
Principal
Establecer el grado de eficacia del tratamiento con una HBPM (bemiparina) durante 3 meses, en la mejoría de las úlceras tórpidas del pie diabético.
Secundarios
Comparar los dos grupos de tratamiento en cuanto a:
Evolución de la proteinuria.
Evolución de los exudados duros, microhemorragias y microaneurismas de la retinopatía diabética.
Incidencia de amputaciones.
Evolución de la calidad de vida.
Seguridad del tratamiento.
Método
Diseño
Ensayo clínico fase III de evaluación de eficacia y seguridad en una nueva indicación de un fármaco ya comercializado, paralelo de dos grupos, aleatorizado, triple ciego y controlado con placebo.
Emplazamiento
Los pacientes fueron captados en los 39 centros de salud de Mallorca, lo que supone un denominador poblacional de 547.000 personas mayores de 18 años. Las visitas se realizaron en los centros de atención primaria o en el domicilio del paciente. Al inicio y final del tratamiento se realizaron controles hospitalarios (analíticas, retinografías, etc.).
Criterios de inclusión/exclusión
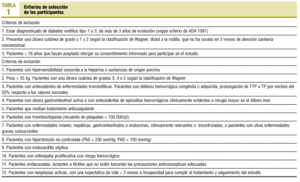
Los criterios de inclusión y exclusión de pacientes en el estudio se exponen en la tabla 1.
Selección de sujetos
Los sujetos fueron reclutados a partir de los equipos de atención primaria, previa solicitud de notificación de los casos conocidos en cada cupo, que fueron incluibles a priori. Posteriormente, se confirmó el cumplimiento de los criterios de inclusión/exclusión y se procedió a la firma del consentimiento informado.
Cálculo del tamaño muestral
No se ha hallado bibliografía sobre la evolución, en un plazo de 3 meses, de las úlceras tórpidas en el pie diabético. Existen datos sobre la evolución hacia la amputación. Tampoco existen datos publicados sobre la eficacia de las HBPM en este tipo de lesiones. A pesar de ello, se plantea la hipótesis como unilateral de eficacia a partir de dos argumentos: los resultados preliminares de un ensayo similar que se está llevando a cabo en el Karolinska Institute (Suecia), y de la información preliminar de pacientes diabéticos con úlceras tórpidas que fueron tratados con HBPM como profilaxis de trombosis venosa profunda, por miembros del grupo investigador, que revelaron resultados esperanzadores en la mayoría de los pacientes12.
Aunque no pueden sentarse las bases de una hipótesis cuantificada de eficacia, se ha optado por plantear un ensayo suficiente para evidenciar eficacia cuando la diferencia de efecto en el grupo tratado obtenga respuestas favorables en un 30% más de pacientes que en el grupo control, para la situación de máxima indeterminación (Pintervención = 0,65; Pcontrol = 0,35), asumiendo un error tipo I del 0,05 y error tipo II del 0,2. Bajo este supuesto, el número de sujetos por grupo se ha calculado en 34, que se ha aumentado hasta 42 pacientes en previsión de un 20% de pérdidas. Por tanto, se requiere en total 84 pacientes.
Tras la exploración preliminar en cuatro centros de salud con 52.000 habitantes mayores de 18 años, había 24 casos de DM diagnosticados con úlceras, lo que supone una prevalencia conocida de aproximadamente 46/100.000 mayores de 18 años, de los que al menos dos tercios cumplen criterios de inclusión y si la mitad de ellos acepta participar, se estima que en la isla de Mallorca, en un año podrá haberse completado la inclusión.
Formación de los grupos
Una vez comprobado que los pacientes cumplen los criterios de inclusión y no los de exclusión, y han firmado el consentimiento informado, el paciente es asignado al grupo experimental o al grupo control de forma aleatoria y equiprobable. Se genera informáticamente, mediante números seudoaleatorios, siguiendo un sistema de bloques de tamaño cuatro. Este método garantiza la heterogeneidad de tratamiento administrado en grupos consecutivos de pacientes, asegurando que en un intervalo corto exista similar número de pacientes en ambos grupos.
Intervenciones
Fármaco experimental: bemiparina, administrado en inyección subcutánea, a una dosis inicial de 3.500 U/día durante 10 días. La dosis de mantenimiento fue de 2.500 U/día durante 80 días.
Fármaco control: suero fisiológico, administrado en inyección subcutánea en volumen necesario para su enmascaramiento.
Las úlceras reciben los cuidados estandarizados, supervisados por la enfermera del estudio, basados en recomendaciones extraídas de consenso de expertos: limpieza con agua y jabón neutro, retirada de esfacelos y material necrótico si lo hubiere, hidratación con suero fisiológico y oclusión simple no compresiva con gasa.
Si la úlcera presenta signos de infección según los criterios expuestos en el protocolo de curas (dos o más signos de rubor, calor, dolor, edema, exudación y pérdida de la función) se trata con antibióticos sistémicos.
Seguimiento de los sujetos
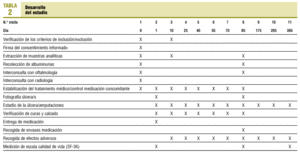
El tratamiento duró 3 meses y se realizó seguimiento hasta completar el año. Los controles y determinaciones en cada uno de ellos se exponen en la tabla 2. Todo el trabajo de campo (captación, seguimientos, extracciones, controles, etc.), fue realizado por el investigador principal y la enfermera, con el apoyo de la secretaría de estudio. Un monitor externo, contratado por Laboratorios Farmacéuticos Rovi S.A., llevó a cabo la supervisión de la realización del estudio.
Definiciones de las variables principales y métodos de medida
La variable principal de efecto fue la úlcera. Se midió el área a partir de una fotografía digital, calculada por método computarizado; el estadio fue valorado por el equipo investigador. En el caso de presentar más de una úlcera, se eligió la de mayor tamaño o estadio más grave.
Definimos como «efecto» (parámetro de valoración), respecto a la evolución favorable de la úlcera, una reducción en, al menos, un 50% en el área de su superficie y/o una variación favorable del estadio en un grado entre el control al iniciar el tratamiento y la valoración final a los 3 meses.
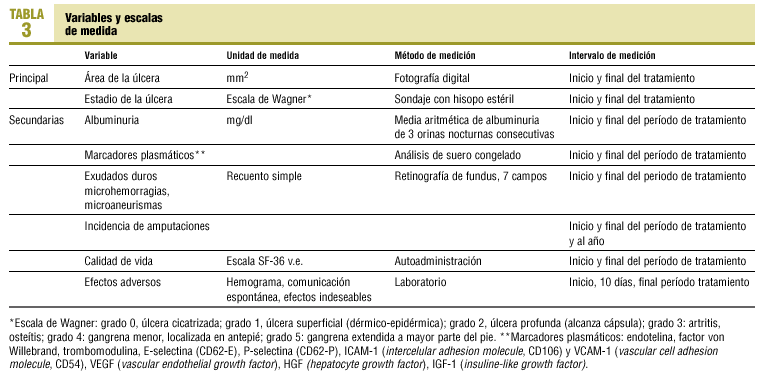
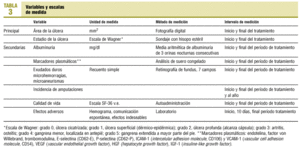
En la tabla 3 se presentan las variables, definiciones, escalas de clasificación y momento en los que se valoraron. Las retinografías se realizaron en el hospital de referencia. Los marcadores plasmáticos se midieron en la unidad de investigación en diabetes del Hospital Vall d'Hebron (Universidad Autónoma de Barcelona).
Se ha elaborado y pilotado un cuaderno de recogida de datos (CRD) que servió de base para la mecanización de datos con un programa de minimización de errores, con doble introducción de las variables centrales del estudio, identificación y modificación de discrepancias.
Estrategia de análisis
El estadístico desconoce la asignación de tratamientos. El análisis se llevó a cabo en la Unidad de Investigación de Atención Primaria de Mallorca.
Tras finalizar la asignación se comprobó si, a pesar de utilizar un sistema de asignación aleatoria compensada, existía homogeneidad de los dos grupos para las variables personales, tipo y tiempo de evolución de la diabetes y los valores basales de las variables de estudio (tamaño inicial de las úlceras y estadio, albuminuria, retinopatía, SF-36).
Se llevó un primer análisis crudo, por diferencia de proporciones en la variable principal de efecto y cálculo de eficacia mediante 1-RR con sus respectivos intervalos de confianza del 95%.
Se efectuó un análisis estratificado ajustado por cada variable independiente. Al aparecer diferencias entre el RR crudo y RR ajustado, se valoró la homogeneidad entre categorías para establecer si la variable es modificadora del efecto o confusora. Se estableció la probabilidad de respuesta por un modelo de regresión logística de las variables predictoras.
El análisis de los datos se realizará por intención de tratar.
Los objetivos secundarios se analizarán comparando proporciones entre grupos de tratamiento.
Se realizará la descripción de los efectos adversos recogidos en ambos grupos.
Discusión
Limitaciones del diseño
Es posible que se produzcan más abandonos (se trata de una administración diaria por vía subcutánea) en caso de evolución desfavorable de las úlceras. El análisis por intención de tratar intenta compensar este sesgo y, en todo caso, favorecer la hipótesis nula.
El seguimiento con controles cada 2 semanas mientras dura el tratamiento pretende homogeneizar los cuidados de la úlcera, mejorar el cumplimiento y aumentar las posibilidades de detectar efectos adversos de la medicación. Ello confiere mayor control del desarrollo del estudio y evita sobrecarga asistencial.
Aunque la posibilidad de efectos locales en el lugar de inyección de estas heparinas, administradas adecuadamente, es mínima, pueden provocar una pérdida de enmascaramiento en casos contados.
Respecto a la calidad de vida, se ha optado por una medida genérica y bien conocida (SF-36), ya que no se ha hallado un cuestionario específico para el problema del pie diabético.
Respecto al calendario del estudio, 9 visitas en 3 meses, puede superar el tratamiento «habitual» de estos enfermos y afectar a la validez externa para garantizar la máxima validez interna.
Respecto de la duración del tratamiento, no hay suficientes elementos para determinar si 3 meses es el período suficiente, pero parece el adecuado para establecer efecto. Sería discutible, desde el punto de vista ético, ampliar el período de tratamiento sin datos del efecto de las HBPM en estas úlceras.
No se dispone de datos que nos permitan cuantificar de forma contrastada la hipótesis establecida, lo que provoca la incertidumbre en cuanto a que el tamaño de muestra sea suficiente para detectar un efecto en caso de haberlo. De producirse una falta de potencia con la muestra prevista, si observamos una tendencia clara, clínicamente relevante hacia la eficacia de la intervención, se propondrían estudios con mayor tamaño de muestra.
Aplicabilidad práctica
La diabetes afecta al 6-8% de la población española. Sus complicaciones crónicas son conocidas y afectan en mayor o menor grado a todos los pacientes. De demostrarse eficacia en el tratamiento de úlceras del pie diabético, con una relación beneficio/riesgo aceptable, podrían evitarse parcialmente al paciente las consecuencias de las mismas, que tanto afectan a la calidad de vida y que evolucionan a menudo hacia la amputación, con los consiguientes costes personales, sanitarios y sociales. Los objetivos secundarios son igualmente importantes en lo referente a la retinopatía y nefropatía diabética. Es una línea de investigación que puede ofrecer alternativas a los enfoques terapéuticos actuales.
Se trata de un ensayo surgido de los profesionales de primaria que diseñan un proyecto en coordinación con profesionales de especializada, promovido por la GAP.
Correspondencia: Manel Rullán García. Unidad de Investigación de Atención Primaria de Mallorca. Reina Esclaramunda, 9. 07003 Palma de Mallorca. España. Correo electrónico: mrullang@hotmail.com
El promotor es la Gerencia de Atención Primaria de Mallorca (ib-salut). Laboratorios Farmacéuticos ROVI S.A. provee la medicación enmascarada, el seguro de responsabilidad civil y compensa al promotor en cuanto a los costes de sustitución del médico investigador y la enfermera del proyecto, los cuales no reciben remuneraciones directas de ningún tipo por parte del laboratorio. El proyecto está cofinanciado por el FIS, expediente PI: 021704.
El protocolo ha sido aprobado por la Agencia Española del Medicamento y por el CEIC de Balears.
Manuscrito recibido el 9 de abril de 2002.
Manuscrito aceptado para su publicación el 18 de noviembre de 2002.