Introducción
La enfermedad pulmonar obstructiva crónica (EPOC) afecta al 9% de la población adulta1 y posiblemente su incidencia continúe aumentando en los próximos años, para pasar a ser la tercera causa de muerte en el mundo occidental en el año 20202. El principal objetivo del tratamiento es aliviar los síntomas y disminuir las agudizaciones. Para conseguir alguna mejoría sintomática el uso de broncodilatadores es la medida más eficaz3. El papel de los corticoides inhalados sigue sujeto a controversia4-6. Recientemente se ha publicado un estudio esperanzador con un inhibidor de la fosfodiesterasa IV, el cilomilast7, aunque su uso clínico parece poco probable a corto plazo. Por tanto, los principales fármacos continúan siendo los broncodilatadores, fundamentalmente anticolinérgicos y betamiméticos. Para valorar la eficacia del tratamiento se han ido añadiendo nuevos parámetros como cuestionarios de calidad de vida, escalas de disnea o tests de esfuerzo, pero la espirometría forzada aún es una de las pruebas más importantes en el control del paciente con EPOC. Los primeros broncodilatadores de acción sostenida fueron los betamiméticos de acción larga, que llevan ya varios años en el mercado. Diversos trabajos han demostrado cierta eficacia de estos fármacos, tanto en la mejoría de la función pulmonar como en la calidad de vida y tolerancia al esfuerzo, comparados con placebo8,9 o con ipratropio10. Últimamente se ha incorporado un nuevo broncodilatador, el bromuro de tiotropio, un anticolinérgico con una serie de características que lo convierten en un fármaco de primera línea. Existen diversos estudios que han comprobado su eficacia, tanto comparado con placebo como con ipratropio11,12, e incluso se ha mostrado superior a salmeterol13. Se ha publicado un trabajo que demuestra la superioridad de la asociación de fluticasona y salmeterol sobre ambos por separado14 y otro que comprobó una mayor eficacia de la budesonida y el formoterol sobre la budesonida aislada15, pero no conocemos ninguno que haya asociado un betamimético de acción larga y tiotropio, lo que a priori parecería la combinación más razonable en pacientes con EPOC de grado grave.
Para conocer la eficacia broncodilatadora de esta asociación hemos diseñado un estudio preliminar en el que comparamos la utilización conjunta de salmeterol y tiotropio con ambos fármacos por separado en pacientes con EPOC de grado moderado-grave.
Pacientes y métodos
Pacientes
Se invitó a participar en el estudio a 22 pacientes diagnosticados de EPOC --volumen espiratorio forzado en el primer segundo (FEV1) < 70% y FEV1/capacidad vital forzada (FVC) < 0,70-- seguidos en nuestra consulta. Todos estaban utilizando un corticoide inhalado y un betamimético de acción larga como tratamiento de base, y bromuro de ipratropio como medicación de rescate. Este tratamiento se había mantenido estable al menos en los 3 meses previos. Se requirió un mínimo de 30 días sin agudizaciones en el momento de la inclusión. Ningún paciente era fumador activo y todos habían sido instruidos en nuestra consulta de enfermería en el manejo de sus dispositivos de inhalación. En todos los casos la mejoría del FEV1 tras 1.000 µg de terbutalina era inferior al 15%. Las características de los pacientes pueden verse en la tabla I. Se excluyó a los pacientes con enfermedades pulmonares diferentes de la EPOC, enfermedades cardiovasculares, enfermedades neurológicas importantes, hiperplasia de próstata, intolerancia conocida a alguno de los fármacos o incapacidad para realizar correctamente las pruebas funcionales. El comité de ética local aprobó el estudio y todos los pacientes dieron su consentimiento por escrito para participar en él tras recibir información al respecto.
Protocolo de estudio
Se utilizó un diseño aleatorio, doble ciego, cruzado y controlado con placebo. Tras comprobar la correcta inhalación, se estableció un período de 2 semanas de lavado durante las cuales el tratamiento fue exclusivamente con 500 µg/12 h de fluticasona y terbutalina a demanda. Se establecieron 3 asociaciones: a) fluticasona en sistema Accuhaler (500 µg/12 h) más salmeterol en sistema Accuhaler (50 µg/12 h) y placebo (similar a tiotropio); b) fluticasona más tiotropio (18 µg/24 h) y placebo (similar a salmeterol), y c) fluticasona más salmeterol y tiotropio. Para diferenciar fármaco de placebo el inhalador disponía de un número identificativo, sin que hubiera diferencias en el aspecto o en el peso del dispositivo. Cada una de las asociaciones de inhaladores se entregaba al paciente en un sobre cerrado que se había codificado previamente. De forma aleatoria todos los pacientes fueron tratados durante una semana con cada una de ellas, dejando 48 h sólo con fluticasona y terbutalina a demanda entre las diferentes asociaciones. En cada visita se recogía el tratamiento previo, se comprobaban las dosis utilizadas y se entregaba el siguiente.
Flujo-pico
Se instruyó a los pacientes para que registraran todos los días, hacia las 9.00 h, antes de la inhalación de los fármacos, el flujo-pico en un diario. Se usó un medidor Personal Best y se realizaban 3 mediciones, de las que se escogía la mejor.
Espirometría
Efectuó la espirometría una enfermera del Laboratorio de Pruebas Funcionales con amplia experiencia, que desconocía la medicación que había recibido el paciente la semana previa. Se utilizó un espirómetro Collins GS Plus y se realizó un mínimo de 3 maniobras, de acuerdo con la normativa de la Sociedad Española de Neumología y Cirugía Torácica16. La espirometría valle se realizó entre las 8.30 y las 9.00 h, antes de la dosis matutina de los fármacos; 120 min después de la inhalación de la combinación de inhaladores objeto de estudio se repitió la espirometría.
Análisis de los datos
El objetivo principal fue la diferencia entre el FEV1 alcanzado con la combinación de salmeterol y tiotropio respecto a ambos por separado, tanto valle como a las 2 h de la inhalación. Se estableció como objetivo secundario la diferencia en el flujo-pico promedio de una semana. Se desestimaron para el análisis los 2 valores extremos y se escogieron los 5 centrales. Todos los valores se expresan como media ± desviación estándar. Para las comparaciones del FEV1 se utilizaron tanto los valores absolutos como el porcentaje del cambio respecto a los valores de referencia, que en pacientes con EPOC de grado moderado-grave parece ser más significativo. Se realizó el análisis de la variancia en el caso de muestras normales y posteriormente se aplicó la prueba de comparaciones múltiples de Bonferroni; en el caso de muestras con distribución no normal se utilizó el test de Wilcoxon. El límite de la significación se estableció en un valor de p inferior a 0,05.
Resultados
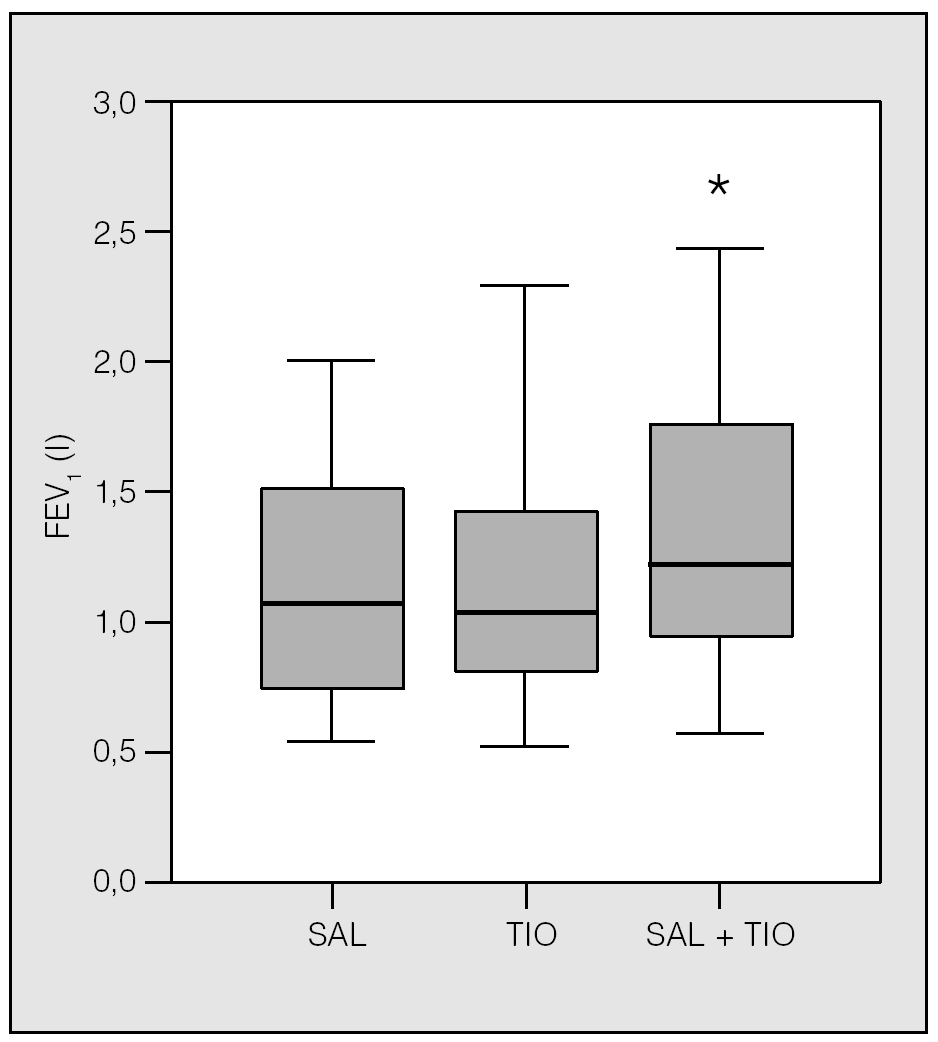
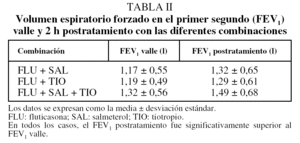
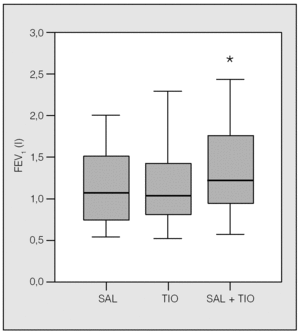
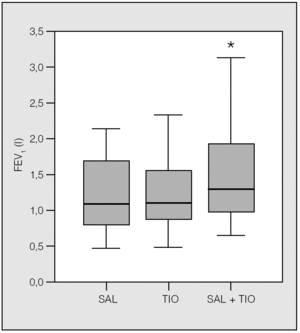
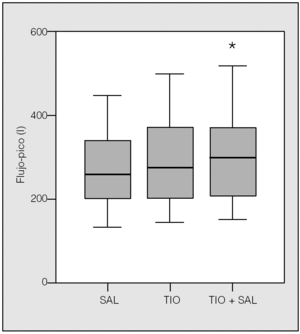
Los 22 pacientes completaron el protocolo. Todos los tratamientos fueron bien tolerados. Sólo 2 de los pacientes, cuyas características pueden verse en la tabla I, eran mujeres. Se excluyó del estudio a los fumadores activos. El FEV1 basal medio (± desviación estándar) fue de 1,16 ± 0,56 l (un 43 ± 14% del teórico) y el flujo-pico promedio fue de 274 l/m. El FEV1 postratamiento fue significativamente mayor que el FEV1 valle en todos los casos desde el punto de vista estadístico. Se alcanzó una mejoría superior al 10% aproximadamente en la mitad de los pacientes, sin diferencias notables entre las 3 pautas (tabla II). No hubo diferencias significativas entre la combinación fluticasona más salmeterol y fluticasona más tiotropio ni en el FEV1 basal ni en el flujo-pico. La combinación de salmeterol más tiotropio (tabla III) fue superior a cualquiera de ellos por separado tanto pre como postratamiento, como se observa en las figuras 1 y 2 (p < 0,03 en todos los casos). El flujo-pico fue también significativamente mejor con la combinación de los 2 broncodilatadores (345 ± 179 frente a 291 ± 126 l/m con salmeterol y 311 ± 151 l/m con tiotropio, en ambos casos p < 0,04). No hubo diferencias entre salmeterol y tiotropio (fig. 3). Ningún paciente refirió intolerancia a las diferentes combinaciones o efectos secundarios reseñables.
Fig. 1. Volumen espiratorio forzado en el primer segundo (FEV1) pretratamiento. Los valores obtenidos con salmeterol (SAL) y tiotropio (TIO) no mostraron diferencias significativas. *p < 0,03.
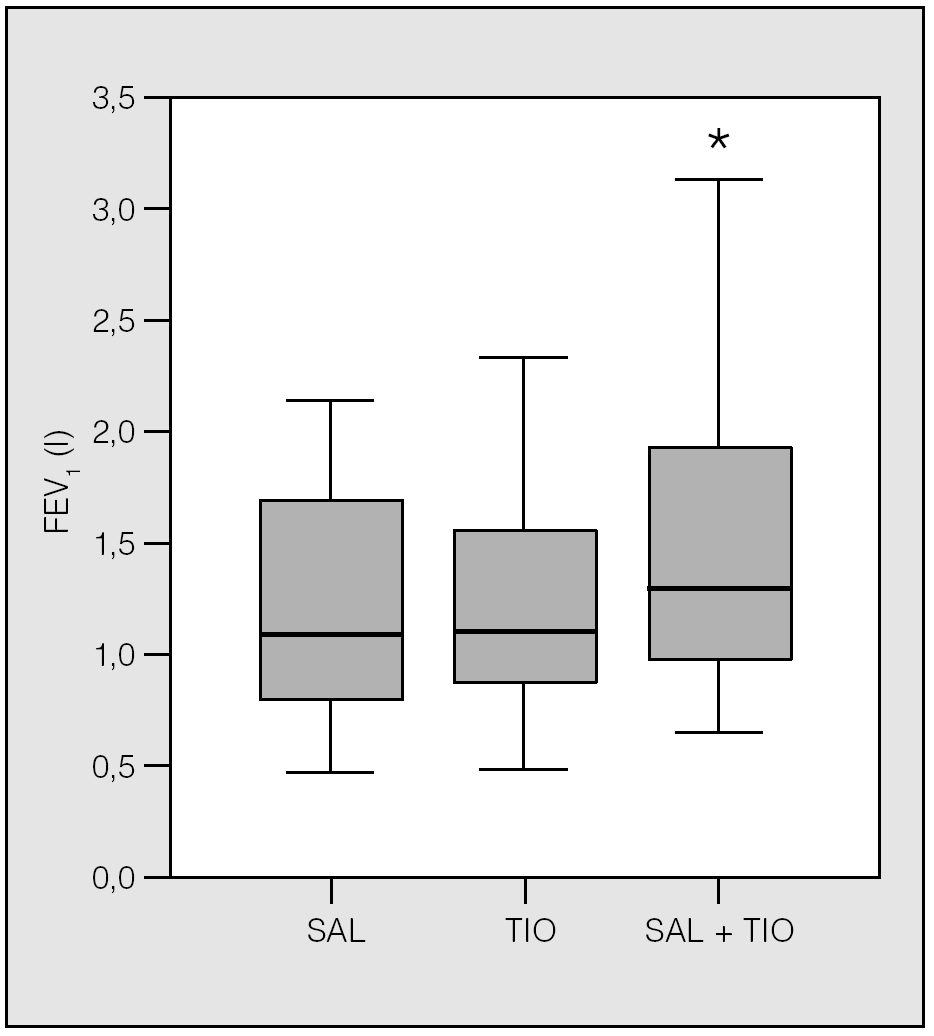
Fig. 2. Al igual que en el caso del volumen espiratorio forzado en el primer segundo (FEV1) valle, el obtenido postratamiento no mostró diferencias entre salmeterol (SAL) y tiotropio (TIO), y la asociación de ambos fue estadísticamente superior. *p < 0,001.
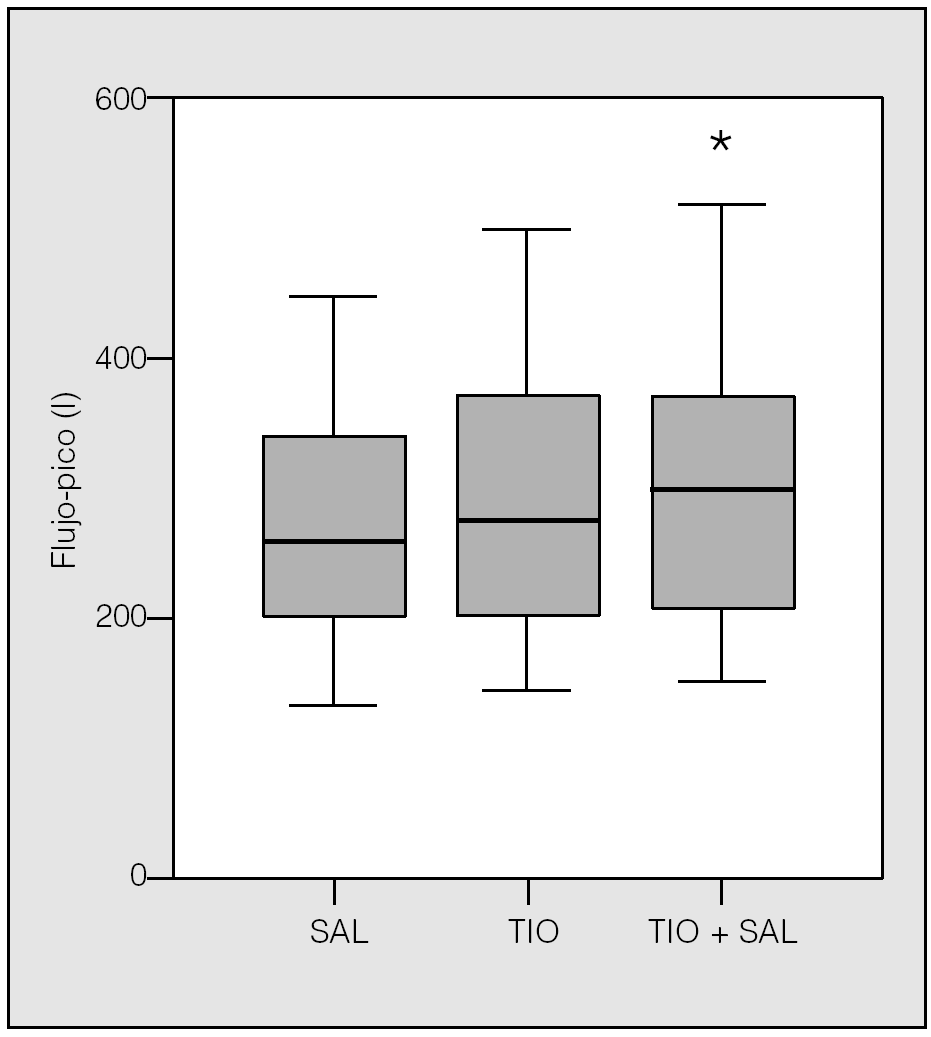
Fig. 3. Los valores del pico-flujo se expresan como la media de los 5 valores centrales (véase texto). En este caso también se mostró superior la combinación de broncodilatadores, aunque con menor significación. SAL: salmeterol; TIO: tiotropio. *p < 0,04.
Discusión
Este estudio preliminar parece mostrar la superior eficacia broncodilatadora de la asociación de tiotropio y salmeterol respecto a cada uno por separado. La EPOC continúa ofreciendo grandes retos terapéuticos. El papel de los corticoides inhalados suscita mucha controversia, y en todo caso sus resultados son modestos. Los β2 de larga duración parecen mejorar la calidad de vida, pero por el momento no se ha demostrado que tengan un impacto positivo en la pérdida de función pulmonar a largo plazo17. Recientemente se ha añadido al arsenal terapéutico el bromuro de tiotropio, un anticolinérgico con efectos broncodilatadores prolongados y selectividad dinámica para los receptores M3. Diversos estudios comparativos han demostrado la superioridad de este fármaco respecto al bromuro de ipratropio e incluso ciertas ventajas cuando se compara con salmeterol11-13. Actualmente se está realizando un estudio de gran amplitud para conocer su impacto a largo plazo en la pérdida de función pulmonar de los pacientes con EPOC. Hasta el momento no conocemos ningún trabajo que haya asociado un β2 de acción sostenida y bromuro de tiotropio. Las evidencias de que disponemos apuntan a que éste sería probablemente el tratamiento de elección en los casos con enfermedad grave, debido a que ambos fármacos poseen mecanismos de acción diferentes y a la larga unión a sus respectivos receptores, que permite una broncodilatación sostenida.
Cuando se aborda la eficacia de un fármaco para el tratamiento de la EPOC existen varios objetivos posibles a estudiar: mejoría global de la calidad de vida en relación con la enfermedad, disminución de las agudizaciones, aumento de la esperanza de vida y también mejoría funcional. No existe una relación absolutamente lineal entre calidad de vida y parámetros funcionales, sobre todo FEV1, pero en general los individuos con mayor obstrucción en la espirometría tienen peor puntuación en los cuestionarios que miden la calidad de vida, presentan mayor número de agudizaciones y, sobre todo en la EPOC de grado grave, tienen una menor esperanza de vida. Hace ya bastantes años que se ha demostrado que la reversibilidad en los pacientes con obstrucción en las vías respiratorias tiene implicaciones pronósticas18. El cuestionario St. George, uno de los más utilizados, muestra una muy buena correlación con el FEV119. Por tanto, parece razonable que conseguir una mejoría significativa en el FEV1 sea un objetivo terapéutico. En ese sentido, nuestro trabajo apoya claramente la utilización de salmeterol y tiotropio en pacientes con EPOC de grado moderado-grave. Existen algunos datos que por su significación conviene resaltar. En todos los casos el FEV1 postratamiento fue significativamente mayor que el pretratamiento desde el punto de vista estadístico, aunque en el caso del tiotropio la media del grupo no alcanzó la significación clínica (± 8%). Aunque existieron variaciones importantes entre los diversos pacientes, el número de ellos que consiguieron una broncodilatación clínicamente significativa fue bastante similar (11 pacientes en el grupo salmeterol, 9 en el de tiotropio y 12 en la combinación) y quizá en una muestra mayor incluso la homogeneidad se incrementaría. Otro dato reseñable es que no hubo diferencias en el FEV1 valle y postratamiento entre salmeterol y tiotropio. Esto contradice en cierto modo los resultados ofrecidos por Donohue et al13, que obtuvieron unos datos claramente favorables al tiotropio en todas las pruebas espirométricas realizadas, lo que también se asoció a la mejoría en la calidad de vida. Estas diferencias no se pueden achacar al grado de afectación funcional, ya que fue similar en los 2 estudios (FEV1 del 40 ± 12 frente al 43 ± 14%).
La medición del flujo-pico matutino tiene un valor limitado en el control de la EPOC. No obstante, en un estudio eminentemente funcional como el nuestro, creemos que tenía interés incluirlo como un dato añadido. Los resultados se comportaron de forma similar al FEV1, sin diferencias significativas entre salmeterol y tiotropio, y con cifras claramente superiores al asociarlos, aunque con menor significación estadística.
En la actualidad es difícil que un paciente con EPOC grave no incluya en su tratamiento un corticoide inhalado. Estos fármacos revierten en parte la pérdida de eficacia que presentan los betamiméticos con su uso mantenido. Por tanto, se decidió que en todas las combinaciones figurara la fluticasona. Con ello, los diferentes tratamientos se acercaban mucho más a la realidad clínica habitual que si no la hubiéramos incluido.
Existen varias limitaciones en este trabajo preliminar. La primera, obviamente, es el tamaño de la muestra. Es posible que la inclusión de un mayor n& uacute;mero de pacientes modificara algo los resultados. Sin embargo, no es probable que los datos variaran de forma sustancial. Otros trabajos que exploran las respuestas broncodilatadoras han utilizado incluso un menor número de casos20,21. Para minimizar este problema hemos escogido a pacientes que conocían bien la técnica correcta de realización de la espirometría y a los que se explicó de forma detallada los objetivos del estudio. Todas las pruebas fueron realizadas por la misma enfermera, también con una amplia experiencia en pruebas funcionales respiratorias. Éste es un estudio que explora únicamente la vertiente funcional, por lo que lo consideramos preliminar, pero los resultados obtenidos apoyan el diseño de otro proyecto más ambicioso para conocer el impacto de la asociación de un β2 de acción sostenida y bromuro de tiotropio en la calidad de vida, las agudizaciones y la pérdida de función pulmonar a largo plazo.
En conclusión, de este trabajo se desprende la mayor eficacia broncodilatadora de la asociación de salmeterol y bromuro de tiotropio en pacientes con EPOC de grado moderado-grave respecto a ambos por separado, lo que abre las puertas a su utilización en la práctica clínica por este tipo de pacientes.
Agradecimientos
Este trabajo no habría sido posible sin la inestimable colaboración de Mercedes Garalt, técnico del Laboratorio de Pruebas Funcionales.