La enfermedad de Parkinson (EP) carece de escalas neuropsicológicas específicas para valorar las alteraciones cognitivas más relevantes en la EP, lo que ha condicionado la utilización de criterios subjetivos o de instrumentos diseñados para otras patologías, dificultando la comparación entre estudios o el seguimiento de los pacientes. Recientemente se ha validado un test de cribado para la demencia en la EP (Parkinson's Disease Dementia-Short Screen [PDD-SS]). Evaluar el grado de satisfacción de los pacientes e investigadores con el uso del PDD-SS en la práctica clínica habitual.
Pacientes y métodosEstudio observacional, transversal, multicéntrico y nacional en 471 pacientes con EP. El grado de satisfacción de los pacientes se midió mediante un cuestionario cuyos ítems puntuaban según una escala analógica-visual de 0-10 puntos (0 = totalmente en desacuerdo, 10 = completamente de acuerdo), mientras que en los investigadores se determinó según una escala Likert de 1-5 puntos (1 = totalmente en desacuerdo, 5 = completamente de acuerdo).
ResultadosEl 36,3% (n=171) de los pacientes presentó demencia asociada a EP según el PDD-SS, considerándose un 77,3% satisfechos con su uso. La satisfacción medida total de los investigadores fue de 3,6±0,6 puntos. El 90% (n=45) de ellos reportó una puntuación global > 3 puntos en el cuestionario de satisfacción. La valoración media de la percepción de aplicabilidad, manejabilidad y fiabilidad del PDD-SS entre los investigadores fue de 3,5±0,7; 3,7±0,6 y 3,1±0,5 puntos, respectivamente.
ConclusiónLos pacientes con EP, así como la mayoría de los investigadores se mostraron satisfechos con el uso del PDD-SS en la práctica clínica habitual.
Parkinson disease (PD) has no specific neuropsychological scales for assessing the most significant cognitive impairment in PD, which has determined the use of subjective criteria or instruments designed for other diseases, making difficult the comparison between studies or the follow-up of patients. A screening test for dementia in PD (Parkinson's Disease Dementia-Short Screen [PDD-SS]) has recently been validated. To assess the degree of satisfaction of patients and researchers through the use of PDD-SS in clinical practice.
Patients and methodsAn observational, cross-over, multicentre and national study was conducted on 471 patients with PD. The degree of patient satisfaction was measured using a questionnaire in which the items scored from 0 to 10 on a visual analogue scale (0 = strongly disagree, 10 = completely agree), while the researchers were determined on a 1-5 point Likert scale (1 = strongly disagree, 5 = completely agree).
ResultsA total of 171 patients (36.3%) patients had dementia associated with PD according to the PDD-SS, of whom 77.3% said they were satisfied with its use. The overall measurement of researcher satisfaction was 3.6±0.6 points. Ninety per cent (n=45) of them reported an overall score >3 points in the satisfaction questionnaire. The mean values of perception of applicability, usability and reliability of PDD-SS among researchers was 3.5±0.7, 3.7±0.6 and 3.1±0.5 points, respectively.
ConclusionsPD patients, as well as most of the researchers, were satisfied with the use of PDD-SS in clinical practice.
La enfermedad de Parkinson (EP) es un trastorno neurodegenerativo que afecta aproximadamente a 3 millones de pacientes en Europa y Norteamérica y se caracteriza por un fenotipo básico de déficits motores (acinesia, rigidez, temblor y alteraciones posturales) junto con otras complicaciones neurológicas que se desarrollan durante la larga progresión de la enfermedad1. Entre éstas destacan las alteraciones de tipo cognitivo, afectivo y conductual, que pueden aparecer desde los estadios tempranos de la enfermedad y llegar a ser más difíciles de abordar que las manifestaciones motoras2.
La prevalencia de demencia en los pacientes con EP oscila entre el 20 y el 40%3, mientras que el riesgo de desarrollar demencia durante el curso de la enfermedad es entre 4 y 6 veces mayor que en la población control de la misma edad4,5. Además, una proporción importante de pacientes con EP sin demencia pueden presentar grados variables de alteraciones cognitivas que aparecen en etapas tempranas de la enfermedad o incluso en pacientes recién diagnosticados6. El deterioro cognitivo leve en la enfermedad de Parkinson suele manifestarse inicialmente con alteraciones más o menos sutiles de la atención, memoria, funciones visuoespaciales y funciones ejecutivas. Un subgrupo de pacientes puede presentar desde fases tempranas alteraciones de lenguaje7.
La ausencia de una escala neuropsicológica apropiada para valorar estas alteraciones cognitivas en la EP ha condicionado que cada experto utilice una metodología distinta y que, por lo tanto, no puedan compararse unos perfiles con otros8.
Cabe señalar que hasta hace poco tiempo los tests utilizados para detectar alteraciones cognitivas en la EP estaban centrados principalmente en la detección de déficits fronto-subcorticales, pero no eran sensibles para la detección de disfunciones corticales9,10. Este es el caso de instrumentos no específicos para la EP como el test MDRS (Mattis Dementia Rating Scale) validado recientemente para su aplicación en la demencia asociada a EP11, o de tests específicos para la EP como la escala SCOPA-Cog12. Para subsanar esta carencia se desarrolló la escala Parkinson's Disease-Cognitive Rating Scale (PD-CRS), un instrumento cuyo desarrollo clinimétrico ha demostrado que resulta un test válido, fiable y útil para diagnosticar de forma precisa el deterioro cognitivo asociado a EP13. Esta escala se ha mostrado útil para discriminar pacientes con EP sin deterioro cognitivo, de aquellos que presentan deterioro cognitivo leve, y estos últimos, de los que presentan demencia asociada a EP. La utilidad comparativa de éste y de otros instrumentos utilizados en la valoración cognitiva de la EP ha sido revisada recientemente9.
La PD-CRS, que ha sido validada de manera independiente por otro grupo14, es apropiada tanto para cribado, como para diagnóstico de demencia y ensayos terapéuticos, sin embargo, por su tiempo medio de aplicación de unos 15min no es un test rápido de cribado de demencia en EP como, p. ej. el Memory Impairment Screen15 o el Mini-Cog16 que se aplican en la enfermedad de Alzheimer.
Dado que es bien conocido que un consumo de tiempo elevado es un factor limitante en la aplicación de escalas neuropsicológicas17 en la práctica clínica diaria se ha considerado conveniente llenar el vacío de un instrumento breve, específico para EP, capaz de ser utilizado como instrumento breve de cribado de demencia en pacientes con deterioro cognitivo asociado a la EP. En este sentido se ha validado muy recientemente18 el test “Parkinson's Disease Dementia-Short Screen” (PDD-SS). Este instrumento, el primero desarrollado para el diagnóstico de demencia asociada a EP, muestra una exactitud diagnóstica excelente, comparable a la de la MDRS, pero con un tiempo de aplicación significativamente más corto que en su versión final: sólo ocupa entre 5 y 7min.
Como complemento a otros datos clinimétricos en el desarrollo de los instrumentos de valoración neuropsicológica es sumamente importante conocer cómo funcionan en la práctica clínica habitual. Así, el presente estudio DIFUSION fue diseñado con los objetivos de valorar la aplicabilidad y aceptabilidad del PDD-SS. Para ello un grupo amplio de neurólogos españoles utilizó la versión inicial de la PDD-SS en una muestra de 471 pacientes con EP reclutados en las diferentes comunidades autónomas y representativos de la población con EP.
Pacientes y métodosSe llevó a cabo un estudio epidemiológico, transversal, multicéntrico y nacional en el que participaron pacientes de servicios de Neurología y Unidades de Parkinson de España, así como de consulta ambulatoria extrahospitalaria. Durante un período de reclutamiento de 6 meses, se incluyeron en el estudio pacientes ambulatorios de ambos sexos, de entre 40 y 85 años de edad, diagnosticados de EP según los criterios diagnósticos del Brain Bank of London19. Como criterios de elegibilidad, se requirió también la ausencia de cambios en la medicación antiparkinsoniana durante el mes previo y la capacidad para realizar la batería de pruebas neuropsicológicas, incluyendo todos los componentes motores asociados.
Como instrumentos de medida de la función cognitiva, se administró a todos los pacientes el Mini-Examen Cognitivo (MEC)20, versión adaptada del Mini-Mental State Examination (MMSE)21, y la versión inicial de la escala PDD-SS. El PDD-SS inicial consta de 8 dimensiones: memoria verbal de fijación, fluencia verbal fonética, fluencia verbal alterante, cuestionario compuesto por cinco preguntas con respuesta dicotómica, dibujo del reloj, memoria verbal diferida por evocación libre, memoria verbal de reconocimiento recodificada y funciones ejecutivas. La puntuación total de este test se obtuvo a partir de la suma de las puntuaciones obtenidas en cada uno de los ítems, siendo el rango de puntuación de la versión larga del test de 0 a 31 puntos e indicando los 0 puntos el máximo deterioro cognitivo y 31 puntos la ausencia de deterioro cognitivo. El punto de corte para el cribado de demencia se estableció en los 15,5 puntos, por lo que puntuaciones del PDD-SS menores o iguales a 15,5 se consideraron indicativas de demencia. Este punto de corte tiene una sensibilidad del 91% y especificidad del 85%18.
La satisfacción de los pacientes con el uso del PDD-SS se evaluó mediante un cuestionario compuesto por 6 preguntas (1: el test me ha parecido fácil de hacer; 2: el test me ha parecido rápido de hacer; 3: el test me ha parecido agradable de hacer; 4: los materiales de apoyo son apropiados; 5: las preguntas me hacen sentir incómodo; 6: dificultad para comprender órdenes), valorada cada una de ellas mediante una escala analógica-visual de 10 puntos (0: mínima satisfacción; 10: máxima satisfacción). En una séptima pregunta se pedía a los pacientes que señalaran en que apartado del test habían experimentado dificultades. La puntuación total del cuestionario se obtuvo a partir de la suma de las preguntas 1, 2, 3 y 5 (en este caso se invirtió la puntuación). La puntuación máxima del test eran 40 puntos, se consideraron satisfechos aquellos pacientes con una puntuación superior o igual a 22 (55%).
En cuanto a la valoración de la satisfacción en el uso del PDD-SS por parte de los médicos, cada uno de los investigadores que participaron en el estudio cumplimentó un cuestionario de satisfacción sobre el PDD-SS de 17 preguntas. Las respuestas a las cuestiones planteadas al investigador fueron registradas mediante una escala tipo Likert, con cinco opciones de respuesta (1: totalmente en desacuerdo; 2: más bien en desacuerdo; 3: indiferente; 4: más bien de acuerdo; 5: totalmente de acuerdo). El cuestionario se dividió en tres bloques en los cuáles se valoró la percepción de manejabilidad, aplicabilidad y fiabilidad del PDD-SS. Para cada investigador se calculó un promedio de la puntuación total resultante de las respuestas a los 17 ítems del cuestionario. Se realizó el promedio de la puntuación global del cuestionario de satisfacción y la obtenida en cada bloque de preguntas.
Todos los análisis estadísticos fueron realizados usando el paquete estadístico SAS© System para Windows, versión 8.2 o posterior.
El estudio recibió la aprobación de un Comité Ético de Investigación Clínica y todos los pacientes firmaron un consentimiento informado antes de ser incluidos en el estudio.
ResultadosDe los 471 pacientes incluidos en el estudio, 288 fueron varones (61,2%) y 182 mujeres (38,6%). La media de edad fue de 70,9±9,1 años (± DE). En cuanto a las características sociodemográficas de los pacientes, el 17,8% manifestó no tener estudios o bien no haber completado los estudios primarios (n=84). Por su parte, el 54,8% de los pacientes manifestó tener estudios primarios (n=258), el 17,6%, estudios secundarios (n=83) y el 9,1%, estudios superiores (n=43).
El 68,6% (n=323) de los pacientes participantes en el estudio presentaban antecedentes clínicos o patología relevante asociada. El antecedente clínico más frecuente en la población de estudio fue la hipertensión arterial, presente en el 38% (n=179) de los pacientes. Seguidamente, destacan los trastornos psiquiátricos, en el 24% de los pacientes (n=113), y las dislipemias en el 23,1% (n=109) de los pacientes.
El tratamiento más frecuente para la enfermedad de Parkinson fue la combinación de levodopa + carbidopa (70,7%, n=333). En orden de frecuencia le siguieron: pramipexol (32,5%, n=153); levodopa + carbidopa + entacapona (21,7%, n=102); rasagilina (17%, n=80) y ropirinol (10,4%, n=49).
De los 52 investigadores, el 61,5% fueron varones (n=32) y el 38,5% mujeres (n=20). En cuanto a su especialización, el 36,5% eran neurólogos generales de hospital (n=19), el 30,8% (n=16) trabajaban en unidades de Parkinson o de trastornos del movimiento y, finalmente, el 9,6% (n=5) eran neurólogos generales de consulta extrahospitalaria. El 21,2% de los investigadores (n=11) incluidos en el análisis declararon tener más de una especialización.
La puntuación total media del Mini-Examen Cognitivo en la muestra de pacientes del estudio fue de 29,0±5,4 puntos. Se observaron diferencias significativas (p<0,0001) en la proporción de pacientes con posible deterioro cognitivo según la edad: el 19,8% en los pacientes mayores de 65 años y el 7,1% de los pacientes menores de 65 años. En cuanto al PDD-SS, la puntuación total media obtenida fue de 18,5±6,3 puntos. El 36,3% (n=171) de los pacientes presentó demencia asociada a la enfermedad de Parkinson según la puntuación de este test. Se detectó una elevada correlación, estadísticamente significativa, entre las puntuaciones obtenidas en el MEC y en el PDD-SS (r=0,73; p<0,0001). La concordancia de los resultados obtenidos en ambos tests fue del 76,86%.
La puntuación media del cuestionario de satisfacción de los pacientes fue de 27,6±7,4 puntos. La proporción de pacientes que se mostraron satisfechos con el uso del PDD-SS, ascendió al 77,3%. En la tabla 1 se muestra la valoración de cada uno de los ítems del cuestionario de satisfacción de los pacientes.
Valoración de cada uno de los ítems del cuestionario de satisfacción de los pacientes (para cada ítem: 0 puntos: mínima satisfacción; 10 puntos: máxima satisfacción)
| Total | |
| Ítem 1: el test me ha parecido fácil de hacer | |
| n | 456 |
| Media | 6,47 |
| DE | 2,69 |
| Ítem 2: el test me ha parecido rápido de hacer | |
| n | 454 |
| Media | 6,47 |
| DE | 2,71 |
| Ítem 3: el test me ha parecido agradable de hacer | |
| n | 460 |
| Media | 7,84 |
| DE | 2,22 |
| Ítem 4: los materiales de apoyo son apropiados | |
| n | 454 |
| Media | 7,98 |
| DE | 2,15 |
| Ítem 5: las preguntas me hacen sentir incómodo | |
| n | 455 |
| Media | 6,74 |
| DE | 3,47 |
| Ítem 6: dificultad para comprender órdenes | |
| n | 456 |
| Media | 6,15 |
| DE | 3,42 |
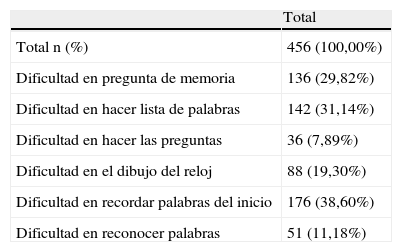
En cuanto al apartado del test en el cual los pacientes habían experimentado dificultades, un 37,7% de los pacientes no encontró dificultad alguna en ninguno de los apartados del test, el 22,6% encontró dificultades en un único apartado, y sólo el 1,8% encontró dificultades en todos los apartados. Una elevada proporción de pacientes, el 38,6% declaró haber tenido dificultades en el apartado del test en el que se pedía recordar palabras aprendidas previamente (tabla 2). De forma similar, el apartado de memoria y el del listado de palabras fueron considerados difíciles por el 29,8% y el 31,1% de los pacientes, respectivamente.
Apartados del PDD-SS en los cuáles los pacientes han presentado alguna dificultad
| Total | |
| Total n (%) | 456 (100,00%) |
| Dificultad en pregunta de memoria | 136 (29,82%) |
| Dificultad en hacer lista de palabras | 142 (31,14%) |
| Dificultad en hacer las preguntas | 36 (7,89%) |
| Dificultad en el dibujo del reloj | 88 (19,30%) |
| Dificultad en recordar palabras del inicio | 176 (38,60%) |
| Dificultad en reconocer palabras | 51 (11,18%) |
Se observaron diferencias significativas en la puntuación del PDD-SS entre el grupo de pacientes satisfechos y el grupo de pacientes no satisfechos. Así, la puntuación del test fue más alta en el grupo de pacientes satisfechos, 19,7±5,9 frente a 15,0±5,9 puntos, respectivamente (p<0,0001). En concordancia, en un análisis de regresión logística aparecieron como factores explicativos de la satisfacción/insatisfacción de los pacientes en el uso del PDD-SS dos variables: la puntuación obtenida en el test y la dificultad reportada por los pacientes. Los pacientes con una puntuación más alta del PDD-SS presentaron un riesgo inferior de insatisfacción con el test (OR=0,9); por tanto, cuanto menor era el grado de demencia del paciente, mayor era su satisfacción con el PDD-SS. Otro factor explicativo de la satisfacción/insatisfacción de los pacientes en el uso del PDD-SS fue la dificultad encontrada en su realización: los pacientes que presentaron una menor dificultad en la realización del PDD-SS, presentaron un riesgo inferior de insatisfacción (OR=0,8).
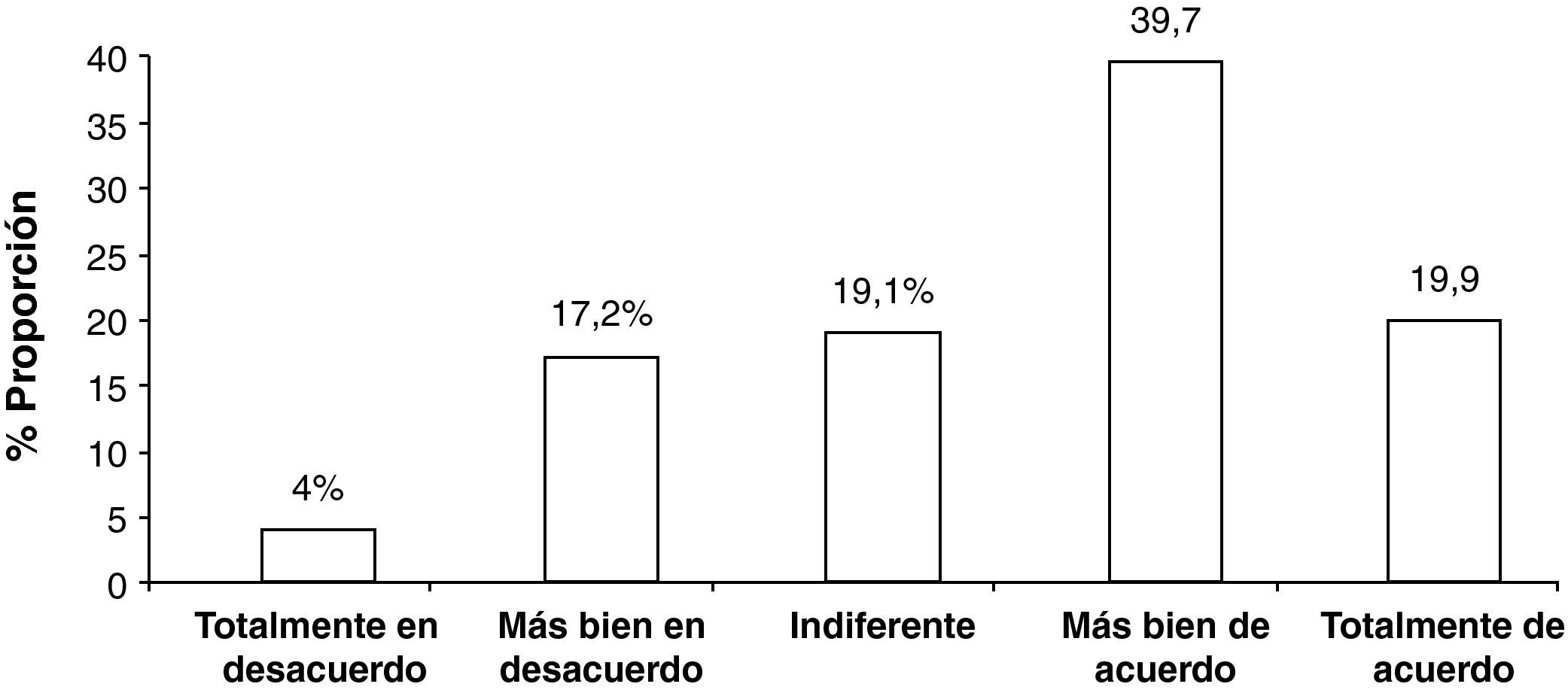
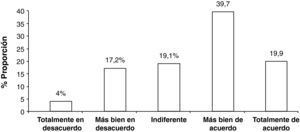
Con respecto a la valoración de la satisfacción de los investigadores con el uso del PDD-SS (n=50), en todos los ítems del cuestionario de satisfacción se obtuvo una puntuación media superior a tres puntos (sobre un máximo de 5), es decir, una puntuación positiva, con una satisfacción media total de 3,6±0,6 puntos. Para el total de respuestas, la valoración o respuesta más frecuente fue el valor 4 («más bien de acuerdo»), que constituyó el 39,7% de las valoraciones, seguida por el valor 5 («totalmente de acuerdo») con un 19,9% de valoraciones (fig. 1).
La gran mayoría de los investigadores (90%, n=45) presentó una puntuación global positiva (3 o más puntos) en el cuestionario de satisfacción y un 26% (n=13) de los investigadores presentó una valoración superior o igual a 4 puntos. Solamente un 10% de los investigadores (n=5) otorgó una puntuación global inferior a 3 en el cuestionario de satisfacción.
La valoración media de la percepción de aplicabilidad del PDD-SS entre los investigadores participantes en el estudio fue de 3,5±0,7 puntos. El 78% (n=39) de los investigadores presentaron una puntuación superior a 3 puntos en la valoración de la aplicabilidad del PDD-SS. Respecto a la percepción de manejabilidad del test, la valoración media entre los investigadores participantes fue de 3,7±0,6 puntos; el 86% (n=43) de los investigadores declararon una puntuación superior a 3 puntos en la valoración de la manejabilidad y comodidad de uso del PDD-SS. Los investigadores consideraron el test como un instrumento que requiere pocos materiales de apoyo y en el que éstos son manejables para la detección de demencia en la enfermedad de Parkinson. La valoración media de la percepción de fiabilidad fue de 3,1±0,5 puntos. El 70% (n=35) de los investigadores valoraron el PDD-SS como un test fiable para la detección de demencia en la enfermedad de Parkinson.
DiscusiónEl PDD-SS es una herramienta específica para detectar las alteraciones cognitivas de la EP. Este test permite, dada su sencillez y rápida ejecución, una primera criba en los pacientes con EP dentro de la práctica clínica habitual del especialista, facilitando un abordaje precoz de estas alteraciones, deseable desde el punto de vista clínico y que, además, resulta económicamente rentable22.
A falta de experiencia en la utilización del PDD-SS, el presente estudio fue diseñado y realizado con el objetivo de evaluar algunos aspectos prácticos relativos a la aplicación del mismo, como el grado de satisfacción del paciente y del médico en el uso del PDD-SS en la práctica clínica habitual, consolidando así la reciente validación18.
Los resultados obtenidos en el presente estudio muestran claramente la satisfacción de los pacientes con el PDD-SS. Cabe señalar que el grupo de pacientes satisfechos con el test obtuvo una puntuación más alta en el PDD-SS. Es decir, los pacientes con un grado menor de demencia son los que declaran estar más satisfechos con el test. Los resultados de este estudio han demostrado la aplicabilidad del PDD-SS, que reúne los requisitos de aplicación exigidos en cuanto a simplicidad, rapidez, coste, facilidad de uso e interpretación y uso de materiales cotidianos no extraños al ambiente en el que se desarrolla la práctica clínica habitual22. En cuanto a la valoración realizada por los investigadores, ésta fue positiva en todos los ítems del cuestionario. Se obtuvieron valores similares en las tres dimensiones evaluadas: aplicabilidad, manejabilidad y fiabilidad.
Asimismo, este estudio ha permitido obtener datos comparativos sobre el uso del PDD-SS y el MEC de Lobo, que es hasta la fecha la herramienta más frecuentemente utilizada por los especialistas españoles para el cribado de la demencia en pacientes con EP. Cabe señalar, que en el presente estudio el uso del PDD-SS ha permitido detectar un porcentaje de pacientes con demencia asociada a la EP superior que con el uso del MEC. Estos resultados sugieren que si bien ambos tests son adecuados para la detección de alteraciones cognitivas, la aplicación del PDD-SS sería la herramienta más idónea y específica para la detección de demencia en pacientes con EP.
El uso de cuestionarios para evaluar la satisfacción del paciente es una metodología establecida que se usa con frecuencia en investigación clínica23 y, en particular, en pacientes con EP24–26 y permite identificar aquellas áreas deficitarias del paciente y también los resultados de los cuidados27. En este estudio los cuestionarios utilizados han sido sencillos y precisos, requisitos necesarios para este tipo de evaluación23.
Con el estudio DIFUSION se han aportado más detalles para la interpretación cualitativa mediante datos comparativos de una muestra representativa de la población, así como por la contextualización de las puntuaciones en las condiciones clínicas de población en estudio. En resumen se puede afirmar que los datos obtenidos sobre el PDD-SS en la práctica médica habitual permiten confirmar la utilidad del test para detectar alteraciones cognitivas en pacientes con EP.
Investigación experimental en humanosEl presente estudio se llevó a cabo siguiendo los principios éticos basados en la última versión vigente de la Declaración de Helsinki y recibió la aprobación de un Comité Ético de Investigación Clínica.
FinanciaciónEste estudio ha recibido soporte económico sin restricciones por parte de Novartis Farmacéutica, S.A. y Esteve, S.A.
Este trabajo ha sido presentado en la Reunión de la SEN 2008.
Conflicto de interesesEl doctor J. Kulisevsky ha recibido compensaciones económicas por su participación como ponente o ‘advisory boards’ por parte de Novartis, Lundbeck, Esteve, Boheringer, Pfizer, GSK, UCB, Merck-Serono, Solvay y Merz. El doctor B. Hernández es empleado de Novartis Farmacéutica S.A. Los restantes autores declaran no tener ningún conflicto de intereses.
El apoyo financiero y material de la presente investigación ha corrido a cargo de Novartis Farmacéutica S.A. y Esteve S.A. Agradecemos la colaboración en la elaboración del presente manuscrito a Marta Muñoz Tudurí de Trial Form Support, España.
E. Agüera Morales, H. R. Sofía; M. Álvarez Saúco, H. Gral. Univ. de Elche; G. Amer Ferrer, H. Son Dureta; F.J. Barrero Hernández, H. Clínico; J.A. Bruguera Hernández, H. La Fe; A. Ares Luque, Complejo Hospitalario; J.J. Asencio Marchante, H. Pto. Real; A. Ávila Ribera, H. General; C. Badia, H. Dr. Peset; J.J. Baiges Octavio, H. Virgen de la Cinta; F. Barriga Hernández, H. Alcorcón; M.J. Catalán Alonso, H. Clínico; A. Castro García, H. Clínico; E. Cebrián, H. Prov. de Pontevedra; E. Cubo Delgado, H. General Yagüe; A. del Olmo, H. Dr. Peset; M.D. Martínez Lozano, H. General; C. Durán Herrera, H. S. Pedro de Alcántara; J. Escudero Torrella, H. General; A. Esquivel López, H. Gregorio Marañón; M. Garcés Redondo, H. Virgen de la Cinta; P. García Ruiz, Fundación J. Díaz; E. Gil Neciga, H. Virgen del Rocío; E. Gómez, Fundación J. Díaz; M. Goñi Imizcoz, H. Divino Vallés; P. Granes Ibáñez, H. Arnau de Lleida; J. Hernández Vara, H. Vall d¿Hebrón; B. Indakoetxea, H. Donostia; P. de Juan Hernández, H. Clínico Univ.; P. Latorre Murillo, H. Can Ruti; E. Lezcano García, H. de Cruces; J.J. López Lozano, H. Puerta de Hierro; S. López Pousa, H. Santa Caterina; J. Marey López, H. Juan Canalejo; M.E. Marta Moreno, H. Miguel Servet; F. Martí, H. Clínico; R. Martín González, H. Sant Joan; C. Martínez Parra, H. Macarena; C. Martínez Rodríguez, H. Cabueñas; J.C. Martínez Castrillo, H. Ramón y Cajal; O. Morsi Hassan, H. Arrixaca; T. Ojea Ortega, H. C. Haya; J. Olazaran Rodríguez, Centro de Especialidades Hermanos Sangro; J. Olivares Romero, H. Torrecadenas; A. Oterino Durán, H. Univ. Valldecilla; B. Pascual Sedano, H. San Pau; L.F. Pascual Millán, H. Clínico; J. Peña Casanova, H. del Mar; N. Rodríguez Fernández, H. General; C. Salvador Aguiar, H. Central de Asturias; F. Sánchez Caballero, H. Valme; V. Serrano Castro, H. Clínico; J. Vaamonde Gamo, H. General de Ciudad Real; A. Villarejo Galende, H. 12 de Octubre; N. Villares, H. Puerta de Hierro y F. Vivancos Matellano, H. La Paz.
La relación de los Miembros del Grupo de Investigadores del estudio DIFUSION se presenta al final del trabajo.