INTRODUCCION
El 75% de las mujeres padece una candidiasis vaginal (CVV) durante su época reproductiva1 y el 5% una candidiasis vulvovaginal recidivante (CVVR). Candida albicans en la mujer asintomática se aisla en el 20% (10,55%). El 25-40%, con cultivos positivos a Candida, son portadoras asintomáticas, con blastosporas. Los micelios son la forma invasora en los tejidos, y aparecen en la enfermedad asintomática. Hay una dependencia hormonal de la infección.
Existe germinación de la Candida, colonización e invasión de los tejidos. Los Lactobacillus producen bacteriocina, que inhibe el crecimiento de los hongos.
Las candidiasis son la primera infección vaginal en Europa, y han aumentado en la última década. Como señaló Gardner: las vaginitis causan más infelicidad en la tierra que otras enfermedades ginecológicas, y el costo es astronómico»2.
Los factores de riesgo para las CVV son1,3: embarazo, diabetes, antibióticos, corticoides, contraceptivos orales (DIU, diafragma, espermicidas), infección por VIH, productos comerciales de higiene, colonización gastrointestinal, contagio sexual, defectos inmunológicos, dieta, estrés, etc. Aunque en un estudio caso-control4, observando los factores de riesgo, se descartó la influencia de los tampones, las bragas de tejido sintético, la dieta y el estrés. Tampoco influirán las relaciones sexuales, con nueva pareja o con parejas múltiples.
Otro estudio caso-control con estudiantes universitarias5 indica que la CVV aumenta con mujeres en edad joven, con sexo oral 2 semanas antes (odds ratio, OR = 3,5), con la contracepción oral (OR = 1,68), con el uso de espermicidas (OR = 3,3), con diagnóstico previo de CVV en el año anterior (OR = 3), y en la raza negra (OR = 3) y otras (OR = 2,2) frente a la blanca.
Hablamos de CVVR cuando hay 3 o más episodios al año6. Aún con tratamiento recurre en el 50%. En la patogenia de CVVR se habla de reinfección, a partir del tracto gastrointestinal, o por transmisión sexual; y de recurrencia, por la virulencia del organismo, con Candidas no albicans, por resistencia antimicótica, y por los factores del huésped, inmunes o no inmunes. En realidad, hay más recurrencia que reinfección, debido a cambios en los mecanismos de defensa protectores del huésped en la mucosa vaginal.
En las vaginitis crónicas, de las que son responsables muchas veces Candidas no albicans resistentes a fluconazol, por ejemplo, los cultivos tienen valor, para ayudar al diagnóstico y para la selección de la terapia apropiada7. Además, un cultivo negativo tampoco excluye la infección vaginal.
En las CVVR un aspecto importante es la actividad sexual, y se han señalado como significativas las siguientes conductas8: edad precoz al primer coito, sexo casual con parejas en el mes previo, sexo durante la menstruación, sexo oral regular, experiencia de coito anal, sexo oral en el último mes, y frecuencia de sexo oral.
El 40% de mujeres con CVV tendrán una o más recurrencias. El tratamiento de la pareja no evita la recidiva de CVV en la mujer.
Ante esta panorámica, el objetivo de nuestro trabajo, prospectivo y multicéntrico a un año, ha sido estudiar CVV comparando dos tratamientos de dosis única, fenticonazol (Loxomexin, Laurimic) frente a sertaconazol (Ginedermofix), para tratar un episodio agudo o recidivante de la infección. Hemos hecho una evaluación al año para ver la curación clínica y el porcentaje de recidivas, así como los efectos secundarios, siguiendo la misma metodología de nuestros dos trabajos anteriores9,10.
MATERIAL Y MÉTODOS
Durante los años 2000 y 2001, en la consulta de Ginecología de Liria (G-L), dependiente del Hospital Arnau de Vilanova de Valencia (grupo A), en la consulta de Planificación Familiar de Liria (PF-L) (grupo B), y en la consulta de Planificación Familiar de Sueca (PF-S) (grupo C), se ha estudiado un total de 327 pacientes afectadas de candidiasis vulvovaginal.
Se aleatorizaron para el tratamiento comparativo de dos productos: fenticonazol y sertaconazol, durante un año, con dosis única. Fenticonazol nitrato, un óvulo de 600 mg, y sertaconazol nitrato, un comprimido vaginal de 500 mg. Con fenticonazol se trataron 136 casos, y con sertaconazol, 191 casos.
En el estudio, en la primera visita, se practicó anamnesis y exploración ginecológica, con toma de muestra para citología y flujo en fresco (grupos B y C) con KOH al 10% para ver micelios y esporas. En todos los grupos también se tomó muestra para cultivo de hongos, cuando se consideró necesario. Se indicó el tratamiento de forma aleatoria, y la necesidad de una nueva visita si no mejoraban las molestias. La segunda visita o final fue al año de la primera. Nos interesaba ver la curación clínica y la incidencia de recidivas. En esa visita se valoraron también los efectos secundarios del tratamiento.
No se trató a la pareja sexual, pero a cada paciente se le proporcionaron por escrito consejos de higiene, incluyendo la abstinencia de coito o el uso de preservativo durante los procesos agudos de infección. Cuando existía en la paciente una vulvovaginitis florida, se asoció en ocasiones la correspondiente crema de uso tópico del mismo producto.
La respuesta clínica se definió como: a) curación, con desaparición de síntomas y signos, y b) fracaso, con ausencia de cambios, sin mejora o empeoramiento, y como recidiva antes del año.
Como la mayoría de las pacientes (aproximadamente el 75%) habían tenido episodios previos de CVV, se les aconsejó que en caso de recidiva durante el año acudieran de nuevo a la consulta.
En el estudio estadístico, se analizan porcentajes para los datos cualitativos y para los datos cuantitativos: la t de Student para la comparación de medias. El test de Pearson del X2 se utilizó para la significación estadística del tratamiento, considerando significativa una p < 0,05.
RESULTADOS
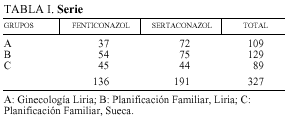
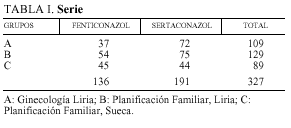
En la tabla I se presentan los casos correspondientes a cada grupo. En total, 327 casos, 136 en tratamiento con fenticonazol (F) y 191 en tratamiento con sertaconazol (S).
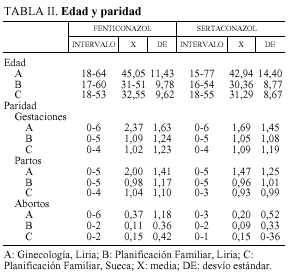
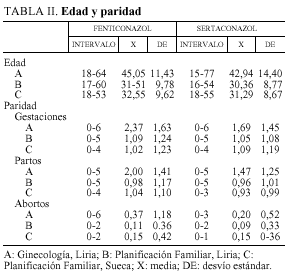
En la tabla II se presenta la edad y la paridad, como gestaciones, partos y abortos. Con datos de intervalo, media y desvío stándar. En la edad, no hubo diferencias significativas entre tratamientos por grupo. Sí, entre grupos, dado que en el G-L son mujeres más mayores, mientras que en los grupos PF son mujeres más jóvenes que buscan anticoncepción. En la paridad, hubo diferencias significativas, en las gestaciones entre F y S, en el grupo A, p < 0,02; y en los partos también en el grupo A entre F y S, p < 0,05.
La edad media de la serie fue 35,40 años. La paridad media de la serie fue 1,20 partos. Eran nuligestas 125 casos, 38,2%.
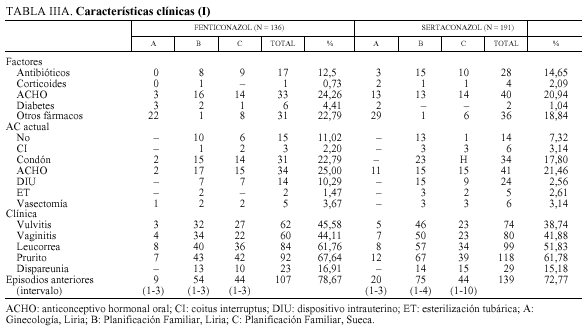
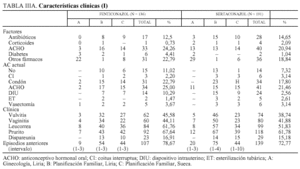
En la tabla IIIA, de características clínicas, se indican los factores causales o predisponentes, la anticoncepción actual, la clínica, los episodios anteriores y su intervalo. No hubo diferencias significativas entre F y S. Globalmente, usaban anticoncepción hormonal oral el 22%, habían tomado antibióticos el 13,76%, eran diabéticas el 2,44%, y tomaban otros fármacos el 20,48%, usualmente terapia hormonal sustitutiva de la menopausia, sobre todo en G-L, grupo A. Hubo 2 casos VIH+.
Clínicamente, la vulvovaginitis suele ir asociada, pero no siempre. Existía vulvitis en el 41,59%, vaginitis en el 42,81%, leucorrea en el 56%, prurito en el 64% y dispareunia en el 16%.
Los episodios anteriores de candidiasis ocurrieron en el 75% de las mujeres, oscilando entre 1 y 10 (media, 3).
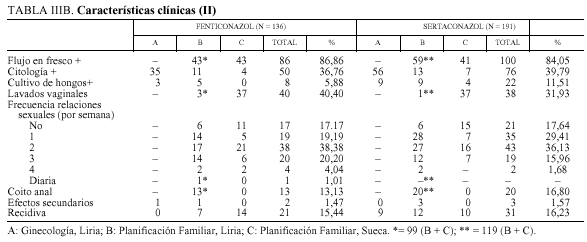
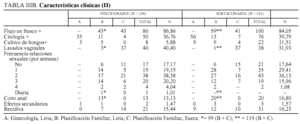
En la tabla IIIB, de características clínicas (continuación), se indica el n.o de casos con flujo en fresco+, las citologías y los cultivos de hongos+, la utilización de lavados vaginales comerciales, la frecuencia de relaciones sexuales por semana, la práctica de coito anal, los efectos secundarios del tratamiento y el n.o de recidivas.
En el grupo A de G-L, no se hizo toma de flujo en fresco, por problemas técnicos de infraestructura y agobio asistencial. Fue positivo en el 85% de los grupos B y C. La citología vaginal fue positiva en el 38%. Dio positiva con mayor frecuencia en el grupo A de G-L, donde se realizó el diagnóstico de muchos casos asintomáticos que se trataron. Hubo atipias reac tivas en 2 casos.
En los grupos B y C de PF, usan lavados vaginales comerciales en el 40,4 y 32%, respectivamente.
La frecuencia de relaciones sexuales por semana, en los grupos B y C, la más usual es de 2 veces por semana, sin diferencias significativas. El coito anal, en los grupos B y C, fue del 13,13 y del 16,80%, respectivamente.
Los efectos secundarios del tratamiento son muy escasos. Con F, 1,47%, y con S, 1,57%. No existen diferencias significativas. Se señalaron picor y escozor tras la inserción del óvulo o comprimido vaginal.
Las recidivas fueron 15,44% para F y 16,23% para S. No hubo diferencias significativas. La curación clínica a corto plazo puede considerarse total, 100%, pero no siempre hay curación microbiológica. En los cultivos de hongos, al inicio, no hubo diferencias significativas, con F, 5,88%, y con S, 11,51%. Candida albicans fue mayoritaria. Candida glabrata se encontró en 1/12 casos en el grupo A. Pero se detectaron otros gérmenes, como Trichomonas vaginalis, Gardnerella vaginalis, Streptococcus agalactie, etc., en el cultivo bacteriológico.
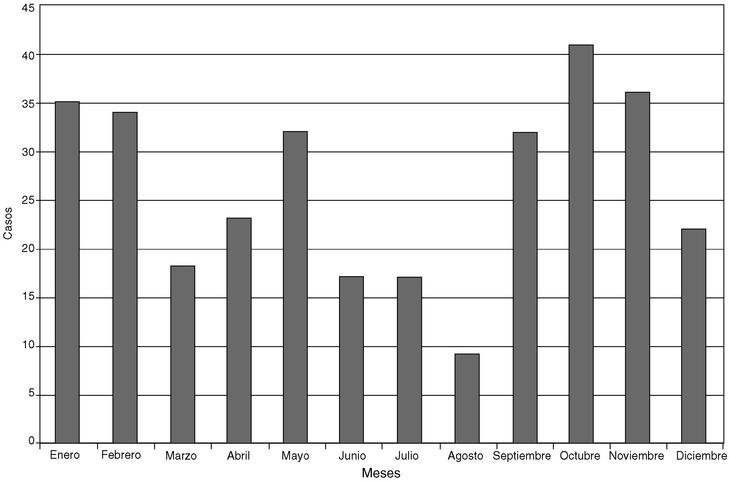
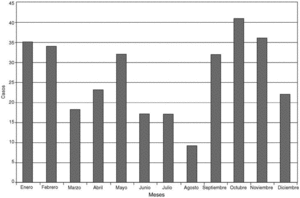
En la figura 1, histograma de frecuencias, se representa la distribución anual de las vulvovaginitis. Hay unos picos de enero-febrero y octubre-noviembre. El punto más bajo, en agosto, es ficticio, se debe a que las consultas están cerradas por vacaciones, pero sabemos que en verano son infecciones más frecuentes, por mayor posibilidad de contaminación en playas y piscinas, y debido al aumento de relaciones sexuales. De todas formas, las infecciones ocurren en cualquier momento del año.
Fig. 1. Distribucón Anual de Candidiasis Vulvovaginal.
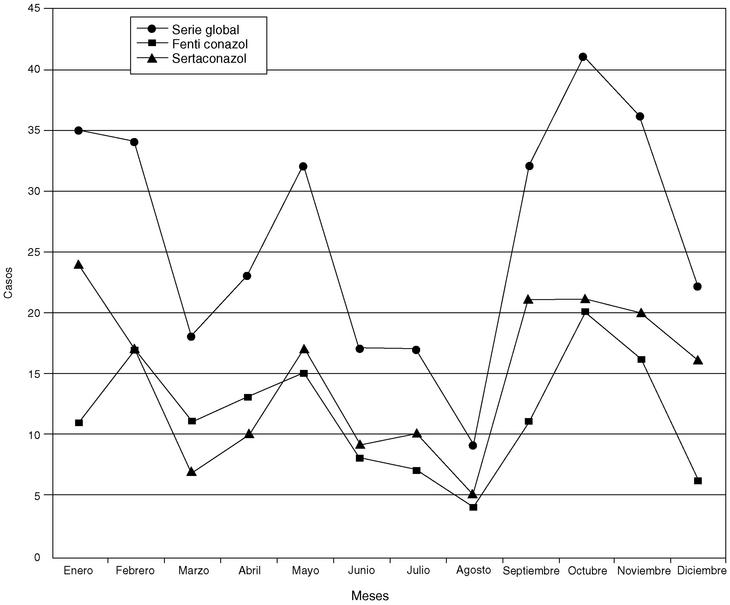
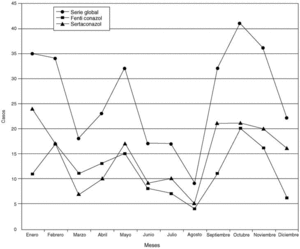
En la figura 2, se representa en líneas quebradas la serie global, y las líneas de los tratamientos F y S, que son bastante superponibles, lo que indica que la incidencia es independiente de las muestras, y se mantiene durante el año.
Fig. 2. Serie global y tratamiento.
DISCUSION
El F es un imidazol, con actividad antibacteriana sobre grampositivos y poder germicida sobre gramnegativos. Es antimicótico en dermatófitos, levaduras y hongos dimórficos. Tiene máxima actividad frente a levaduras a pH = 4-5 (que es el habitual de la vagina), y tiene rápida acción fungicida11.
En el tratamiento de la CVV con F, hay diversos estudios. Comparando un óvulo de 100 mg de F, 15 casos, con un óvulo de miconazol de 100 mg, 15 casos, ambos 2 veces al día12, y con cultivos antes y después del tratamiento, todos los casos se curaron, pero F fue más rápido (86,6%) a 1-2 semanas de tratamiento.
Comparando F crema 1%, 27 casos, con clotrimazol crema 2%, 27 casos, una vez al día, 7 días13, en ambos tratamientos hubo reducción clínica de los síntomas y eliminación de Candidas en el 95%. La curación a los 6 meses con F fue del 92,3%, con clotrimazol del 92%. Hubo 4 recidivas con F, con clotrimazol ninguna. La tolerancia fue excelente, sin síntomas locales.
Se estudió F, en 60 casos, con 3 dosis en mujeres de 17-71 años: 3 grupos de 20 casos, tratados con 200 mg/día, 3 días, 600 mg/día, 1 día, y 1.000 mg/día, 1 día14. Hubo esterilización micológica en el 75-80%, y no recidivas. Las 3 dosis fueron igual de efectivas y bien toleradas. Sólo se produjo quemazón vaginal en un caso con 200 mg y en 2 casos con 1.000 mg.
Los mismos autores15 comparan F, óvulo de 600 mg, 1 día, 40 casos, con clotrimazol de 500 mg, comprimido vaginal, 1 día, 40 casos. Se realizan controles, clínico y cultivo a los 7 días, y en los casos curados se observan recidivas a las 4-5 semanas. Ambos productos eliminan Candida albicans en el 90%. Tolerancia excelente en ambos, e igual eficacia y seguridad en los síntomas. No hubo efectos secundarios. Recurrencias, con F, 2/35, y con clotrimazol, 5/37.
Comparando F, un óvulo de 200 mg, 3 días, con crema vaginal, 2 veces al día, 3 días, en 20 casos de CVVR, con Candida albicans16, con cultivos antes, a los 7 y 21 días postratamiento, los cultivos se negativizaron en el 100%. Los resultados clínicos fueron buenos en el 90%. Sin efectos secundarios. En 2 casos, hubo recidiva a los 30 días.
F en 43 casos de CVV (con 11 CVVR), a dosis única, óvulo de 1.000 mg, y controles a 1 semana, clínico y cultivo17. El cultivo fue negativo en el 69,05%. Tolerancia buena en el 92,85%. La dosis única produce un mejor cumplimiento del tratamiento y tiene ventajas respecto a tratamientos prolongados. Los efectos secundarios se producen en 4 casos: 3 con prurito (el cultivo fue positivo, con persistencia de la infección), y en 1, sequedad vaginal.
Los mismos autores18, en 46 casos de CVV, comparan óvulo único de 600 mg, 28 casos, con crema vaginal 2%, 2 veces al día, 7 días, en 18 casos. La tolerancia fue buena. Y a 1 semana, los cultivos negativos fueron el 89,3% con el óvulo, y el 77,8% con la crema.
Otro estudio19, 10 casos con placebo (grupo C), un óvulo 3 días, y otros 3 días con F, un óvulo de 100 mg. En otros 10 casos (grupo B), F, óvulo de 200 mg, 3 días; y en otros 10 casos (grupo A), F, óvulo de 100 mg, 6 días. La pauta más eficaz fue la del grupo B. No hubo efectos secundarios.
Con 153 casos de CVV, 75 se trataron con F, óvulo de 600 mg ± crema 2% vulvar, y 78 se trataron con clotrimazol, 1 tableta vaginal de 500 mg ± crema 1% vulvar. La dosis única es altamente eficaz y bien tolerada20. Quedaron libres de enfermedad con F, el 83,6%, y con clotrimazol, el 62,9%, al mes del tratamiento, sin diferencias significativas. Efectos secundarios, con F en 5 casos, quemazón y leucorrea.
En otro estudio21, con 174 mujeres de edad media 33 años, se trataron con un óvulo de 600 mg, y si no mejoraban a los 3-5 días, otro óvulo. Con afectación vulvar también se daba crema. Hubo curación clínica en el 88% a los 7-10 días, y curación microbiológica en el 92%. El escozor vaginal mejoró en 2 días en el 80% de los casos, lo que sugiere rapidez de acción.
F tiene una concentración inhibitoria mínima (CIM) de 5-40 µg/ml, dependiendo del pH del medio de cultivo. Es activo frente a bacterias grampositivas (Staphylococcus y Streptococcus). A las 3 h, no hay correlación dosis-concentración con 600 mg, pero a las 12 h sí. Las dosis altas producen reserva intravaginal y es efectivo por período más largo22.
Del estudio multicéntrico italiano23, comparando 337 casos con óvulo de 200 mg, 3 días, y 51 casos de crema al 2%, una vez al día, hubo buenos resultados clínicos en 90%. Los cultivos fueron negativos en la primera visita a los 15 días, el 70% con crema y el 82,6% con óvulo; y en la segunda visita a los 36 días, 89,1% con crema y el 91,9% con óvulo. Hubo efectos secundarios en 12 casos (3,1%): 9 con óvulo y 3 con crema, locales: quemazón, eritema o reacción alérgica local.
El S es otro imidazol, que inhibe la síntesis de ergosterol. Produce cambios en la permeabilidad del plasmolema, las células se redondean y aumentan de volumen. Hay alteraciones en las mitocondrias y acumulación de vesículas. Y plasmólisis, como se ha observado con el microscopio electrónico (ME). Los cambios en la Candida albicans, con S24, es un efecto destructivo en las células, hay alteraciones después de 12 h a concentración 10-6 M, con acción máxima a 10-3 M, y fuerte actividad fungicida a 10-4 M.
Si tiene también actividad antibacteriana25; en un estudio con 174 bacterias de infecciones dermatológicas o vaginales, S tuvo elevada actividad, con CIM entre 0,25 y 8 µg/ml, contra las bacterias grampositivas. Las infecciones fúngicas tópicas pueden ser colonizadas por bacterias. De ahí la importancia de este hecho.
In vitro, con 150 cepas, de 6 especies de Candida, se comparó S con econazol y bifonazol26. S fue el más activo, C. parapsilosis fue la más suceptible, y C. tropicalis, la menos. S inhibe la síntesis de ergosterol y daña la membrana celular del hongo. Tiene buena actividad in vitro, y baja toxicidad en uso tópico. Y eficacia en modelos animales de dermatofitosis.
Al haber pocos trabajos clínicos de su uso en ginecología, nosotros lo hemos empleado para el tratamiento de las CCV.
De nuestro trabajo, con 327 casos de CVV, tratadas 136 con F y 191 con S, concluimos que:
1.La curación clínica a corto plazo es el 100% en ambos grupos. Y a largo plazo, en F, el 84,56% y en S el 83,77%.
2. Los efectos secundarios del tratamiento son muy escasos: en F, el 1,47% y en S, el 1,57%, sin diferencias significativas.
3. Las recidivas fueron el 15,44% para F y el 16,23% para S, sin diferencias significativas.
En definitiva, ambos son buenos productos, con dosis única para el tratamiento de la CVV. Y a la vista de nuestra experiencia, recomendaríamos en caso de CVVR, el tratamiento con la misma dosis única mensual (posmenstrual) al menos durante 6 meses, y mejor un año, para evitar nuevas recidivas.
RESUMEN
Se presenta un estudio prospectivo y multicéntrico, durante 2 años, de candidiasis vulvovaginales en 327 mujeres, comparando un óvulo vaginal de 600 mg de fenticonazol (136 casos) frente a un comprimido vaginal de 500 mg de sertaconazol (191 casos), en dosis única.
Al año del tratamiento, observando la curación clínica, se evaluaron la incidencia de recidivas y de efectos secundarios. No hubo diferencias significativas entre ambos productos, con unos resultados muy satisfactorios. Con fenticonazol hubo curación clínica en el 85,56%, recidivas en el 15,44% y efectos secundarios en el 1,47%. Con sertaconazol, las cifras fueron, respectivamente: 83,77, 16,23 y 1,57%.