O updated Glasgow Aneurysm Score (uGAS), projetado para prever a mortalidade/morbilidade perioperatórias após rAAA, revelou ser um bom preditor de resultados a curto prazo após o tratamento com cirurgia convencional (CC) e Endovascular Aneurysm Repair (EVAR). Os objetivos foram caracterizar os doentes operados a Aneurisma da Aorta Abdominal roto (AAAr) e avaliar a aplicabilidade do uGAS na população de doentes de uma instituição terciária nacional, com capacidade de rEVAR.
MétodosFizemos uma análise retrospetiva dos doentes operados, no nosso serviço, a AAAr entre fevereiro/2011 e fevereiro/2015. As variáveis foram obtidas através da pesquisa numa base de dados de AAAr da instituição e incluíram: idade, sexo, presença de doença cardíaca, doença cerebrovascular, doença renal aguda/crónica e existência de choque pré‐operatório. Foi obtida a mortalidade perioperatória (30 dias ou intra‐hospitalar). O score de risco foi aplicado retrospetivamente e a mortalidade esperada foi comparada com a mortalidade obtida.
ResultadosForam incluídos 89 doentes. Quarenta e nove (55%) foram tratados por CC e os restantes 40 (45%) por EVAR. Trinta e cinco por cento apresentavam doença cardíaca, 12% doença cerebrovascular, 45% doença renal e 25% choque pré‐operatório. O uGAS médio foi de 90,6±16,7. Não se encontraram diferenças estatisticamente significativas entre doentes submetidos a CC e EVAR, relativamente ao uGAS (p=0,105). A mortalidade aos 30 dias foi de 39,8%, tendo sido significativamente menor nos doentes submetidos a EVAR do que nos submetidos a CC (20 vs. 55%; p=0,001).
Os doentes que morreram eram significativamente mais jovens (70 vs. 76 anos; p=0,031), apresentavam maior prevalência de doença renal (55 vs. 45%; p=0,008), choque (59 vs. 41%; p=0,033) e um uGAS mais elevado (100±12,5 vs. 84,6±16,3; p<0,001). A mortalidade dos doentes com uGAS<=85 foi 14,3% e dos doentes com uGAS>85 foi 56,6%.
ConclusãoOs resultados demonstram a aplicabilidade do score uGAS para estratificação do risco num coorte nacional de doentes com AAAr em que o EVAR é uma alternativa disponível. Contudo, uma vez que não foi possível identificar um cut‐off capaz de prever uma mortalidade de 100%, ressalvamos que a utilização de scores compreende o risco de recusa de tratamento a doentes que poderiam eventualmente sobreviver. Adicionalmente, estes resultados sugerem que o tratamento dos AAAr por EVAR se associa a melhores resultados.
The updated Glasgow Aneurysm Score (uGAS), designed to predict mortality/morbidity perioperative after rAAA, proved to be a good predictor of short term results after treatment with conventional surgery (CC) and EVAR. The objectives were to characterize patients operated at rAAA and evaluate the applicability of uGAS in the population of a national tertiary institution with rEVAR capacity.
MethodsWe did a retrospective analysis of patients operated in our service to rAAA between February/2011 to February/2015. The variables were obtained through a search in a database of the institution and included age; sex; presence of heart disease, cerebrovascular disease, acute/chronic kidney disease and preoperative shock. Perioperative mortality (30‐day or in‐hospital) was obtained. The risk score was applied retrospectively and expected mortality compared with the mortality that was obtained.
Results89 patients were included. 49 (55%) were treated by CC and the remaining 40 (45%) by EVAR. 35% had heart disease, 12% cerebrovascular disease, kidney disease 45% and 25% preoperative shock. The average uGAS was 90.6±16.7. There were no statistically significant differences between patients undergoing EVAR or CC respecting to uGAS (p=0,105). Mortality at 30 days was 39.8% and was significantly lower in patients undergoing EVAR than in those undergoing CC (20% vs 55%; p=0.001).
Patients who died were significantly younger (70 vs. 76 years, p=0.031), had a higher prevalence of kidney disease (55% vs 45%; p=0.008), shock (59% vs 41%; p=0.033) and a higher uGAS (100±12,5 vs 84.6±16,3; p<0.001). The mortality of patients with uGAS <=85 was 14.3% and patients with uGAS >85 was 56.6%.
ConclusionThe results demonstrate the applicability of the uGAS score for risk stratification in a National cohort of patients with RAAA that EVAR is an alternative available. However, since it was not possible to identify a cut‐off able to provide a mortality of 100% We point out that the use of scores comprises the risk of treating patients refusing that could possibly survive. Additionally, these results suggest that treatment of RAAA by EVAR is associated with better outcomes.
A taxa de mortalidade global dos doentes com aneurisma da aorta abdominal roto (AAAr) é estimada em cerca de 74%1. Entre aqueles que chegam com vida ao hospital, nem todos são tratados cirurgicamente devido a um risco inaceitável, pela existência de comorbilidades e/ou idade avançada. Os critérios para cirurgia, no entanto, variam significativamente, de acordo com a avaliação inicial do doente, a experiência do cirurgião e preferência do doente. Nos estudos IMPROVE2 e AJAX3, a percentagem de doentes que não foram submetidos a tratamento foi de 20,6% (263/1.275 doentes) e 11% (57/520 pacientes), respetivamente. Estes valores denotam uma diferença considerável nos critérios para cirurgia. Assim, o uso de um modelo que preveja os resultados de modo fidedigno evita a necessidade da realização de uma avaliação subjetiva por parte dos médicos e o custo de cirurgias desnecessárias. Uma vez que a alternativa ao tratamento do doente é geralmente a morte, apenas a utilização de um modelo muito fidedigno é aceitável.
Vários modelos têm sido desenvolvidos para prever a morte após a intervenção nos doentes com um AAAr: Glasgow Aneurysm Score4 (GAS), score de Vancouver5, o Edinburgh Ruptured Aneurysm Score6 e o índex Hardman7. Estes sistemas de pontuação foram concebidos antes da introdução do tratamento endovascular dos aneurismas da aorta abdominal (EVAR) e apenas o GAS foi atualizado, de modo a incluir o tipo de intervenção realizado como variável. Num estudo de validação recente8, o updated GAS (uGAS) demonstrou ser o modelo que, de modo mais preciso, previa a mortalidade após o tratamento por cirurgia convencional (CC) e EVAR dos doentes com AAAr.
Os objetivos do nosso trabalho foram caracterizar os doentes operados a AAAr e avaliar a aplicabilidade do uGAS na população de doentes de uma instituição terciária nacional, com capacidade de realizar rEVAR.
Esperamos que este trabalho contribua no processo de tomada de decisão por parte do cirurgião vascular, sobre se deve prosseguir com o tratamento ou recusá‐lo.
MétodosFizemos uma análise retrospetiva dos doentes operados no nosso serviço a AAAr, entre fevereiro de 2011 a fevereiro de 2015.
Foram incluídos todos os doentes com evidência intraoperatória de AAAr e os doentes submetidos a EVAR com evidência em angio‐TC de hematoma retroperitoneal ou extravasamento de contraste.
Os aneurismas aórticos com envolvimento supra e pararrenal e os doentes sintomáticos, mas sem evidência de rutura em angio‐TC foram excluídos.
As variáveis em estudo foram obtidas através da pesquisa numa base de dados de AAAr da instituição (Microsoft Access) e incluíram: idade, sexo, presença de doença cardíaca (definida como história prévia de enfarto do miocárdio, cirurgia cardíaca, angina de peito ou arritmia), doença cerebrovascular (definida como história prévia de acidente vascular cerebral ou acidente isquémico transitório), doença renal aguda/crónica (definida como uma taxa de filtração glomerular<60ml/min/1,73m2 ou aumento absoluto da creatinina sérica igual ou superior a 0,3mg/dL, em relação ao basal) ou um aumento igual ou superior a 50% em relação ao valor da creatinina sérica pré‐operatória), existência de choque pré‐operatório (TAS pré‐operatória<80mmHg ou necessidade de administração de aminas para controlo tensional).
O cálculo do uGAS4 foi realizado segundo a fórmula: idade (anos)+7 (se presença de doença cardíaca),+10 (se presença de doença cerebrovascular),+17 (se presença de choque),+14 (presença de doença renal aguda/crónica),+7 (se submetido a CC).
O score de risco foi aplicado retrospetivamente e foram calculadas diferenças no score médio e nas categorias que o compõem, entre sobreviventes e não sobreviventes, e entre doentes submetidos a CC ou EVAR.
A mortalidade perioperatória é definida como morte aos 30 dias pós‐cirurgia ou intra‐hospitalar.
Consideração técnicaNo nosso serviço, o EVAR é, habitualmente, a 1.ª opção de tratamento dos AAAr. A CC é normalmente reservada para os doentes com contraindicação anatómica para EVAR – colo aórtico infrarrenal proximal inferior a 15mm de extensão, colo proximal de diâmetro superior a 30mm, angulação proximal maior que 60 graus, presença de trombo abundante ao nível do colo e doença oclusiva/pré‐oclusiva ao nível dos vasos ilíacos (diâmetro inferior a 7mm). Apesar disso, a opção final de qual o tratamento escolhido é tomada pelos médicos que se encontram de urgência.
Foi utilizado balão de oclusão intra‐aórtico em doentes muito instáveis. Quando possível, os procedimentos endovasculares foram realizadas sob anestesia local.
Análise estatísticaA análise estatística foi realizada com o programa SPSS versão 23.0 (SPSS, Chicago, Estados Unidos da América [EUA]). Dados paramétricos contínuos são apresentados como média do valor e desvio padrão; os dados categóricos são apresentados como valores absolutos e percentuais. Os dados não paramétricos são apresentados como mediana e intervalo interquartil. A análise estatística foi realizada aplicando os testes Mann Whitney, qui‐quadrado, Fisher e correlação de Spearman. Um valor de p<0,05 foi considerado estatisticamente significativo.
ResultadosForam operados, durante o período em estudo, 89 doentes, com idade média de 72,5±10,3 anos [45‐92], sendo 83 (93%) do sexo masculino.
Quarenta e nove (55%) foram tratados por CC e os restantes 40 (45%) por EVAR. Foram colocadas 27 endopróteses aorto bi‐ilíacas e 13 endopróteses aorto mono‐ilíacas (nestes últimos casos, realizou‐se bypass femoro‐femoral cruzado após oclusão da artéria ilíaca comum contralateral). Foram usadas as seguintes endopróteses: 5 Gore Excluder (Gore, Newark, DE, EUA), 33 Endurant e Endurant II (Medtronic, Minneapolis, EUA) e 2 Zenith (Cook, Bloomington, IN, EUA).
Trinta e um (34,8%) doentes apresentavam doença cardíaca, 11 (12,4%) doença cerebrovascular prévia, 40 (44,9%) doença renal e 22 doentes (24,7%) apresentavam‐se em choque pré‐operatório.
O uGAS médio foi de 90,6±16,7 [48‐125].
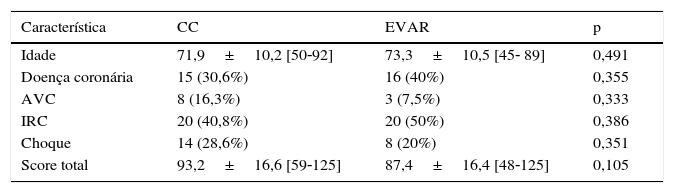
Não se encontraram diferenças estatisticamente significativas entre doentes submetidos a CC e EVAR relativamente ao uGAS (p=0,105), nem em relação a qualquer um dos parâmetros que o compõem (tabela 1).
A mortalidade aos 30 dias foi de 39,8% (35 doentes), tendo sido significativamente menor nos doentes submetidos a EVAR do que nos submetidos a CC (EVAR: 20% vs. CC: 55%; p=0,001).
Os doentes que morreram eram significativamente mais jovens (70,4 anos vs. 75,9 anos; p=0,031), apresentavam maior prevalência de doença renal (morte: 62,9% vs. não morte: 33,3%; p=0,008), choque (morte: 37,1% vs. não morte: 16,7%; p=0,033) e um uGAS mais elevado (morte: 100±12,5 [73‐125] vs. não morte: 84,6±16,3 [48‐125]; p<0,001).
A mortalidade dos doentes com uGAS <=85 foi 14,3% (5/35 doentes) e dos doentes com uGAS >85 foi 56,6% (30/53doentes) (p<0,001).
DiscussãoA decisão de tratar ou não tratar um doente com um AAAr é uma decisão complexa e de elevada responsabilidade.
Devido à inevitável mortalidade associada a esta patologia, a existência de uma ferramenta simples que ajude a prever quais os doentes que têm uma alta probabilidade de morte ou sobrevivência seria muito útil. Apesar dos avanços tecnológicos, da aplicação de programas de triagem e do tratamento eletivo de um cada vez maior número de doentes, o AAAr é responsável pela morte de quase 15 mil doentes/ano nos EUA9. O tratamento desta patologia por EVAR tem sido realizado com cada vez maior frequência9. Em muitos centros, incluindo o nosso, é dada preferência à reparação do AAAr infrarrenal por EVAR se as condições clínicas o permitirem. Esta técnica é muitas vezes realizada sob anestesia local, o que, por si só, demonstrou reduzir a agressão fisiológica por comparação com a técnica cirúrgica convencional10.
No nosso estudo, reportamos uma percentagem de AAAr tratados por EVAR (45%) bastante superior à da maioria dos estudos observacionais11,12.
É de ressalvar que a mortalidade aos 30 dias (39,8%) é semelhante à obtida noutros trabalhos2,11.
Ao contrário das diferenças obtidas em ensaios clínicos randomizados2,3, na nossa população a mortalidade foi significativamente inferior nos doentes submetidos a EVAR (p<00,5). Os valores obtidos são concordantes com outros trabalhos11, nomeadamente o de Mehta13, onde os valores obtidos são semelhantes aos nossos.
Não se encontraram diferenças estatisticamente significativas entre doentes submetidos a CC e EVAR relativamente ao uGAS (p=0,105), nem em relação a qualquer um dos parâmetros que o compõem. Assim, as diferenças obtidas ao nível dos resultados poderão estar relacionadas com um viés de seleção, uma vez que os doentes submetidos a CC são tendencialmente aqueles que apresentam anatomia desfavorável para EVAR, nomeadamente colo proximal de reduzido comprimento. No entanto, apesar de não ser possível recolher dados individuais para cada caso, existe a noção empírica de que foram tratados doentes por EVAR que não apresentariam capacidade para tolerar uma CC.
Outro fator confundidor poderá ser o facto de se recorrer à CC, numa tentativa de realizar uma clampagem da aorta abdominal em doentes emergentes, em quem não haverá tempo de realizar o planeamento de um EVAR.
O índice uGAS apresenta como principal vantagem a sua simplicidade de aplicação, sendo mais fácil de utilizar do que qualquer outro score. Contudo, uma vez que o seu cálculo não depende exclusivamente de dados objetivos e mensuráveis, a sua aplicabilidade em doentes cujos antecedentes são desconhecidos ou impossíveis de obter não é possível.
No nosso caso, o índice de Glasgow demonstrou apresentar boa capacidade discriminativa entre os doentes que sobreviveram ou não. Os doentes que morreram apresentavam um uGAS significativamente mais elevado (p<0,001). Além disso estabelecendo um valor de cut‐off de 85, percebemos que aqueles que apresentam um valor de uGAS inferior têm uma probabilidade de cerca de 85% de sobreviver. Pelo contrário, os que apresentam um valor superior a 85 têm uma probabilidade de sobrevivência de apenas 43%. Podemos, assim, estabelecer que a um aumento do valor de uGAS está associado um aumento da mortalidade. Contudo, este score apresenta teoricamente um baixo valor preditivo positivo e, como tal, não é capaz de identificar com segurança os doentes com alto risco e a quem o tratamento não traria benefício. De ressalvar que um dos doentes com valor de uGAS mais elevado (total=125) sobreviveu.
ConclusãoOs resultados obtidos neste trabalho demonstram a aplicabilidade do score uGAS para estratificação do risco num coorte nacional de doentes com AAAr em que o EVAR é uma alternativa disponível. Contudo, uma vez que não foi possível identificar um cut‐off capaz de prever uma mortalidade de 100%, ressalvamos que a utilização de scores compreende o risco de recusa de tratamento a doentes que poderiam eventualmente sobreviver e, por conseguinte, não pode suportar com fiabilidade a decisão de não intervir.
Responsabilidades éticasProteção de pessoas e animaisOs autores declaram que para esta investigação não se realizaram experiências em seres humanos e/ou animais.
Confidencialidade dos dadosOs autores declaram que não aparecem dados de pacientes neste artigo.
Direito à privacidade e consentimento escritoOs autores declaram que não aparecem dados de pacientes neste artigo.
Conflito de interessesOs autores declaram não haver conflito de interesses.