Estudiar los factores que influyen en el pronóstico vital y funcional global de los pacientes con isquemia crítica de extremidades inferiores (IC), englobando cualquier sector afectado y modalidad de tratamiento.
Material y métodosEstudio de cohortes prospectivo en pacientes con IC. Se registraron: datos demográficos, factores de riesgo cardiovascular, comorbilidad, parámetros analíticos, cuestionario Mini Nutritional Assesment, tratamiento realizado y evolución. Se estudiaron las tasas de mortalidad, salvamento de extremidad y tiempo libre de reingreso y el impacto de los parámetros descritos sobre estas variables resultado mediante las curvas de Kaplan-Meier y la regresión de Cox.
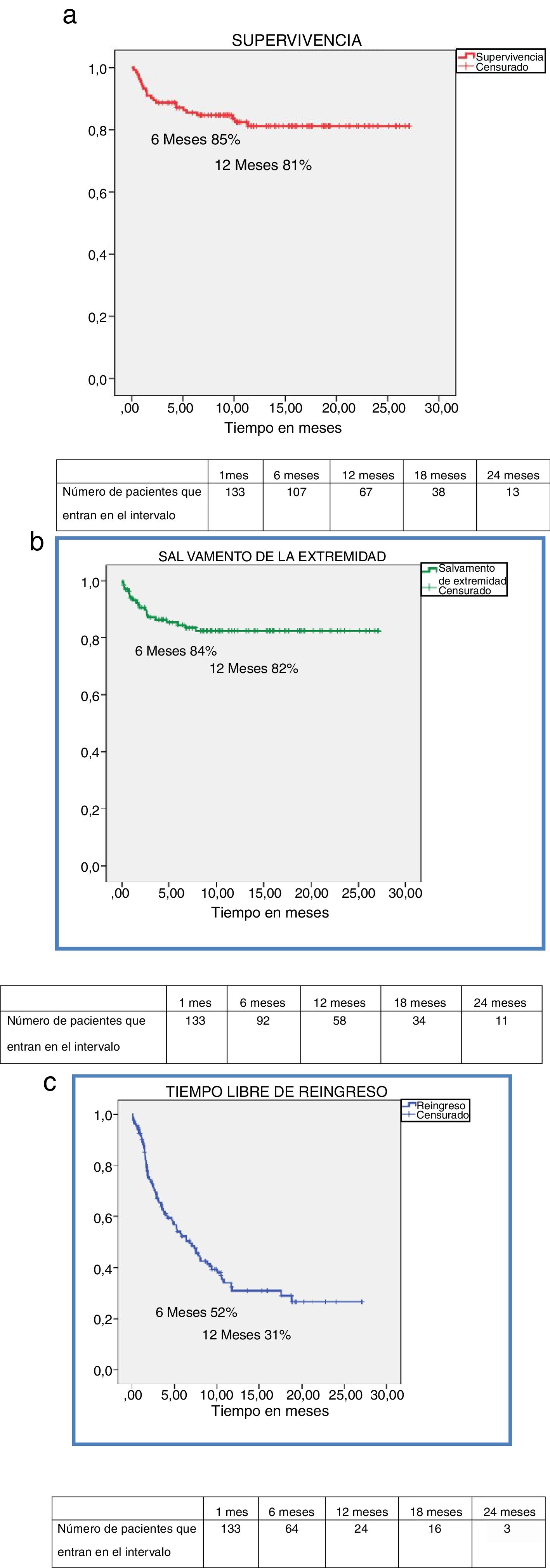
ResultadosIncluimos 133 pacientes, 103 (77,4%) hombres, con edad media de 74,8 años (DS 10,4; rango 52-93). En 97 casos (72,9%) presentaban lesiones tróficas. Se revascularizaron 87 pacientes (65,4%), 48 mediante técnicas abiertas y 39 endovasculares, 5 (3,8%) sufrieron una amputación mayor primaria, tratándose 41 (30,8%) de forma conservadora o mediante amputación menor. La supervivencia fue 85% y 81% a los 6 y 12 meses, con tasas de salvamento de extremidad de 84% y 82% y tiempo libre de reingreso de 52% y 31% para los mismos tiempos. La hipoalbuminemia aumentó el riesgo de mortalidad (p=0,024) y una puntuación baja en el Mini Nutritional Assesment incrementó el riesgo de amputación mayor (p=0,021). Hubo más reingresos en pacientes revascularizados mediante técnicas endovasculares (p=0,001) y en los que presentaban lesiones tróficas (p=0,001).
ConclusionesLa malnutrición es un factor muy prevalente, potencialmente tratable, y determinante en el pronóstico, vital y funcional, de los pacientes con isquemia crítica de extremidades inferiores.
To study the factors that affect the vital and overall functional prognosis of patients with lower limb critical ischaemia (LLCI), including any diseased sector and treatment methods.
Material and methodsA prospective cohort study was conducted on patients with LLCI. A record was made of their demographic data, cardiovascular risk factors, comorbidity, blood test parameters, Mini Nutritional Assessment (MNA) questionnaire, treatment, and outcome. An analysis was made on the mortality, limb salvage, and freedom from re-admission (FRR) rates, as well as the impact of the described parameters on these outcome variables, using Kaplan-Meier curves and Cox regression.
ResultsA total of 133 patients were included, 103 (77.4%) men, with a mean age of 74.8 years (SD 10.4; range 52-93). There was tissue loss in 97 (72.9%) cases. A total of 87 (65.4%) patients were revascularised, 48 using open techniques and 39 endovascular. A primary major amputation was performed on 5 (3.8%) patients, and 41 (30.8%) were treated conservatively, with or without minor amputation. Survival rates were 85% and 81% at 6 and 12 months, respectively, with limb salvage rates of 84% and 82% and FRR of 52% and 31%, respectively, for the same time periods. Hypoalbuminaemia increased the risk of death (P=.024) and a low score in the MNA questionnaire was associated with increased risk of limb loss (P=.021). More re-admissions were observed among patients revascularised with endovascular techniques (P=.001) and those with initial tissue loss (P=.001).
ConclusionsMalnutrition is a very prevalent and potentially treatable factor, which has great impact on the vital and functional prognosis of patients with lower limb critical ischaemia.
Los pacientes afectados de isquemia crítica de las extremidades inferiores (definida como los grados iii y iv de la clasificación de Fontaine) suelen tener una edad avanzada y múltiples comorbilidades. A menudo se asocia con el tabaquismo, la diabetes mellitus, la hipertensión arterial, la dislipidemia, la obesidad y el síndrome metabólico. La incidencia aproximada de esta enfermedad se estima entre 500 y 1.000 casos al año por cada millón de habitantes, y su mortalidad es muy elevada, prácticamente un 20% de los pacientes fallece y el 30% sufre una amputación mayor durante el primer año después del diagnóstico. A los 5 años la mortalidad llega al 50%1,2.
En los pacientes con enfermedad arterial periférica en cualquier grado se ha observado una alta prevalencia de varios déficits nutricionales, provocados por una ingesta baja de fibra, magnesio, ácido fólico y vitamina E, y rica en colesterol, grasas saturadas y sodio3,4. Durante el proceso de recuperación de una enfermedad o de una intervención quirúrgica se produce un aumento de los requerimientos metabólicos, por lo que un correcto estado nutricional es esencial para la buena evolución de los pacientes con isquemia crítica de las extremidades inferiores5,6. Un estudio detallado sobre el estado nutricional de estos pacientes podría detectar aquellos que se beneficiarían del tratamiento con suplementos nutricionales y variación en los hábitos dietéticos6,7.
En los últimos años se han dado importantes cambios en el manejo de los pacientes con isquemia crítica de las extremidades inferiores. Aumenta de forma exponencial el tratamiento endovascular de sus lesiones arteriales, a la vez que disminuye el número de procedimientos abiertos8. Los indicadores de éxito comunes a ambos tipos de procedimientos incluyen la mortalidad y el salvamento de la extremidad, pero difieren en las variables de permeabilidad para los procedimientos abiertos frente a las tasas libres de revascularización o reestenosis de la lesión diana para las técnicas endovasculares, lo que en ocasiones hace compleja la comparación de los resultados de unas y otras.
Habitualmente los estudios sobre el tratamiento de dichos pacientes se centran en subgrupos divididos según técnicas concretas de revascularización o el sector afectado. Nuestro objetivo es analizar el pronóstico vital, el salvamento de la extremidad y la incidencia de reingresos en todos los pacientes afectos de isquemia crítica de las extremidades inferiores de forma global, independientemente del sector afectado o la modalidad de tratamiento. Tratamos además de identificar los principales factores de riesgo (dentro de los parámetros demográficos, la comorbilidad, el estado nutricional y el tratamiento realizado) que puedan influir en dicho pronóstico.
Material y métodosRealizamos un estudio de cohortes prospectivo en el que se incluyeron de forma consecutiva los pacientes ingresados por isquemia crítica de las extremidades inferiores en nuestro servicio entre octubre de 2013 y octubre de 2015. Se excluyeron los pacientes con isquemia aguda de origen embólico o traumático, reingreso por isquemia crítica de un paciente que ya había sido incluido previamente y los pacientes que rechazaron entrar en el estudio.
Se registraron al ingreso los datos demográficos (edad y sexo), los factores de riesgo cardiovascular (tabaquismo, hipertensión arterial, diabetes mellitus e hipercolesterolemia), las principales comorbilidades (cardiopatía, enfermedad cerebrovascular [ECV], enfermedad pulmonar obstructiva crónica [EPOC], insuficiencia renal crónica [IRC] y neoplasia), el sector anatómico principalmente afectado (aortoiliaco, femoropoplíteo [FP] o infrapoplíteo) y el índice tobillo/brazo (ITB).
Dentro del tabaquismo se incluyó a los fumadores activos y a los exfumadores. Se consideró un paciente hipertenso si tomaba medicación hipotensora o precisó la introducción de novo de fármacos antihipertensivos durante el ingreso. Se catalogó un paciente como diabético si tomaba antidiabéticos orales y/o insulina o si sus cifras basales de glucemia superaban los 126mg/dl sin diabetes previamente conocida. Se definió hipercolesterolemia como cifras basales de colesterol total >200mg/dl y/o LDL>100mg/dl y/o el/la paciente estaba en tratamiento con fármacos hipolipidemiantes. La cardiopatía registrada incluía antecedentes de cardiopatía isquémica (angina de pecho, infarto de miocardio, revascularización percutánea o abierta), arritmia, miocardiopatía no isquémica y valvulopatía. La ECV incluía la estenosis carotídea >50%, sintomática o no, la reparación previa, quirúrgica o endovascular, de una estenosis carotídea, y los eventos isquémicos cerebrales (transitorio, ictus menor e ictus mayor). Los pacientes etiquetados como EPOC debían haber sido diagnosticados previamente por un neumólogo y seguir tratamiento y/o revisiones. La IRC fue definida por cifras de aclaramiento renal <60ml/min en la analítica del ingreso. El registro de neoplasia incluía las activas y las previas en remisión.
Se realizó una analítica sanguínea completa a los pacientes a su ingreso, recogiendo los niveles de creatinina (mg/dl), glucemia (mg/dl), hemoglobina (g/dl), hemoglobina glucosilada (%), colesterol total (mg/dl), triglicéridos (mg/dl), LDL (mg/dl), HDL (mg/dl), hierro sérico (pg/dl), albúmina (mg/dl), ácido fólico (pg/dl), vitamina B12 (mg/dl) y vitamina D (mg/dl).
También se realizó al ingreso el cuestionario Mini Nutritional Assessment (MNA), mediante el cual se catalogó a cada paciente como: malnutrido (puntuación 0-7), en riesgo de malnutrición (puntuación 8-11) o con estado nutricional normal (puntuación 12-14).
Se registraron adicionalmente: el tratamiento realizado (revascularización, quirúrgica o endovascular, amputación mayor primaria o manejo médico conservador con o sin amputación menor), las complicaciones, médicas o vasculares, que aparecieron durante el ingreso y los fallecimientos en los primeros 30 días.
Los pacientes fueron seguidos tras el alta con revisiones clínicas al mes, a los 6 y a los 12 meses, con ITB de control en caso de revascularización, y eco-Doppler adicional en caso de revascularización mediante bypass o stent recubierto. Se registraron: los fallecimientos tardíos, las amputaciones mayores tardías y los reingresos por cualquier causa, excluyendo aquellos reingresos programados dentro del tratamiento del proceso isquémico por el que se les incluyó en el estudio (amputaciones menores programadas en un segundo tiempo, revascularizaciones secuenciales dentro del mismo plan de tratamiento, etc.).
Las variables resultado en las que se centró el estudio fueron las tasas de supervivencia, de salvamento de la extremidad y el tiempo libre de reingreso en estos pacientes. También se estudió el impacto de los parámetros demográficos, la comorbilidad, el estado nutricional y el tratamiento realizado sobre estas variables resultado.
Los datos fueron introducidos y analizados en una base de datos SPSS 20. Se han expresado las variables cualitativas como número y porcentaje, y las variables cuantitativas mediante sus respectivas medias, desviaciones estándar (DS) y rangos, y se han utilizado las curvas de Kaplan-Meier y la regresión de Cox para los análisis uni y multivariantes, considerando resultados significativos aquellos con valores de p≤0,05.
ResultadosSe incluyeron en el estudio 133 pacientes, con edad media de 74,8 años (DS 10,4; rango 52-93) y de los cuales 103 (77,4%) eran hombres. La prevalencia de los principales factores de riesgo cardiovascular y de la comorbilidad se detalla en la tabla 1. Destaca una elevada prevalencia de cardiopatía, la mitad de los casos de origen isquémico (41; 30,8%), con revascularización coronaria previa en 26 pacientes (19,5%). También la prevalencia de EPOC, IRC y ECV era elevada, afectando aproximadamente a una cuarta parte de la muestra. Antes del ingreso 80 pacientes (60,2%) estaban ya en tratamiento antiagregante, 96 (72,2%) con estatinas, 38 (28,6%) recibían tratamiento anticoagulante y 110 (82,7%) tomaban al menos un fármaco antihipertensivo.
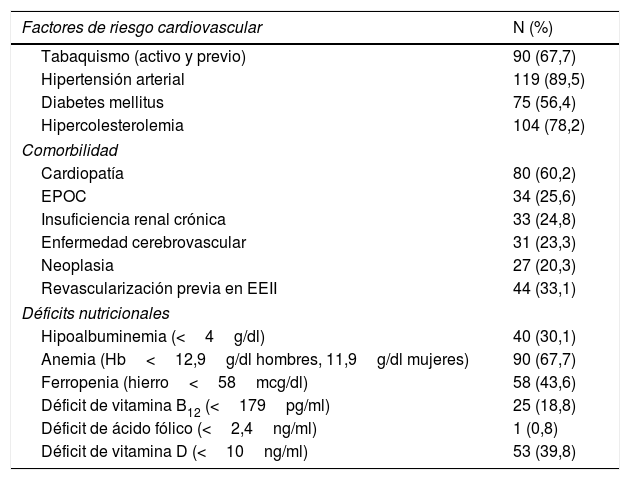
Características clínicas de la muestra a estudio (factores de riesgo cardiovascular y comorbilidad y prevalencia de los principales déficits nutricionales hallados en la analítica realizada al ingreso)
| Factores de riesgo cardiovascular | N (%) |
|---|---|
| Tabaquismo (activo y previo) | 90 (67,7) |
| Hipertensión arterial | 119 (89,5) |
| Diabetes mellitus | 75 (56,4) |
| Hipercolesterolemia | 104 (78,2) |
| Comorbilidad | |
| Cardiopatía | 80 (60,2) |
| EPOC | 34 (25,6) |
| Insuficiencia renal crónica | 33 (24,8) |
| Enfermedad cerebrovascular | 31 (23,3) |
| Neoplasia | 27 (20,3) |
| Revascularización previa en EEII | 44 (33,1) |
| Déficits nutricionales | |
| Hipoalbuminemia (<4g/dl) | 40 (30,1) |
| Anemia (Hb<12,9g/dl hombres, 11,9g/dl mujeres) | 90 (67,7) |
| Ferropenia (hierro<58mcg/dl) | 58 (43,6) |
| Déficit de vitamina B12 (<179pg/ml) | 25 (18,8) |
| Déficit de ácido fólico (<2,4ng/ml) | 1 (0,8) |
| Déficit de vitamina D (<10ng/ml) | 53 (39,8) |
EEII: extremidades inferiores; EPOC: enfermedad pulmonar obstructiva crónica.
Noventa y siete (72,9%) pacientes presentaban lesiones tróficas (isquemia crónica grado iv según la clasificación de Fontaine), el resto (n=36; 27,1%) dolor en reposo (grado iii). El diagnóstico de enfermedad arterial periférica, en estado avanzado, fue realizado de novo en el ingreso en 38 pacientes (28,6%), sin haber presentado previamente clínica de claudicación intermitente. El sector aorto-iliaco fue el principalmente afectado en 29 pacientes (21,8%), el FP en 73 (54,9%) y el infrapoplíteo en 31 (23,3%). El ITB al ingreso no detectó flujo en 24 pacientes (18,1%), fue menor de 0,4 en 23 (17,3%), entre 0,4 y 0,7 en 35 (26,3%), mayor de 0,7 en 6 (4,5%) y no colapsaba en 45 (33,8%).
La puntuación en el test MNA fue patológica (malnutrición o riesgo de malnutrición) en 83 pacientes (64,8%). En la tabla 1 se recogen los diferentes déficits nutricionales hallados en la analítica al ingreso. Destacan muy elevadas prevalencias de anemia y ferropenia, con el 67,7% y 43,6% respetivamente, seguidas de déficit de vitamina D e hipoalbuminemia.
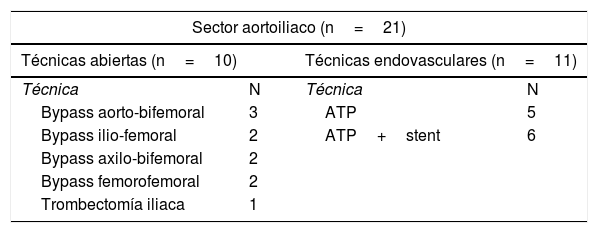
Se revascularizaron 87 pacientes (65,4%), 48 de ellos mediante técnicas abiertas (55,2%) y 39 mediante técnicas endovasculares (44,8%). Cinco (3,8%) sufrieron una amputación mayor primaria, tratándose 41 (30,8%) de forma conservadora, con amputación menor asociada en 25 pacientes (18,8%). En la tabla 2 se recogen los tipos de cirugía realizada por sector afectado. Durante el ingreso se registraron complicaciones en 50 pacientes (37,6%), principalmente médicas (n=32; 24,1%) (hemorragia digestiva, íleo paralítico, diarrea, insuficiencia cardiaca, síndrome coronario agudo, neumonía, fracaso renal, infección urinaria, retención aguda de orina, cuadro confusional, gota, epistaxis, lumbociatalgia, hiponatremia, hiperpotasemia y tromboembolismo pulmonar), seguidas de las de heridas quirúrgicas (n=12; 9%) (hematoma, sobreinfección, dehiscencia y linforrea) y vasculares (n=6; 4,5%) (fracaso hemodinámico/oclusión de la técnica, pseudoaneurisma del punto de punción y fístula arteriovenosa yatrogénica).
Procedimientos quirúrgicos de revascularización (abierta y endovascular) realizados
| Sector aortoiliaco (n=21) | |||
|---|---|---|---|
| Técnicas abiertas (n=10) | Técnicas endovasculares (n=11) | ||
| Técnica | N | Técnica | N |
| Bypass aorto-bifemoral | 3 | ATP | 5 |
| Bypass ilio-femoral | 2 | ATP+stent | 6 |
| Bypass axilo-bifemoral | 2 | ||
| Bypass femorofemoral | 2 | ||
| Trombectomía iliaca | 1 | ||
| Sector FP (n=53) | |||
|---|---|---|---|
| Técnicas abiertas (n=35) | Técnicas endovasculares (n=18) | ||
| Técnica | N | Técnica | N |
| Endarterectomía femoral/profundoplastia | 8 | ATP | 14 |
| Bypass FP 1.ª porción | 12 | ATP+stent | 4 |
| Bypass FP 3.ª porción con vena safena | 8 | ||
| Bypass FP 3.ª porción con PTFE | 2 | ||
| Bypass femorotibial con vena safena | 2 | ||
| Endarterectomía poplítea | 1 | ||
| Bypass poplíteo-distal con vena safena | 1 | ||
| Trombectomía FP | 1 | ||
| Sector infra-poplíteo (n=13) | |||
|---|---|---|---|
| Técnicas abiertas (n=3) | Técnicas endovasculares (n=10) | ||
| Técnica | N | Técnica | N |
| Bypass poplíteo-distal con vena safena | 3 | ATP | 10 |
ATP: angioplastia transluminal percutánea; FP: femoropoplíteo; PTFE: politetrafluoroetileno.
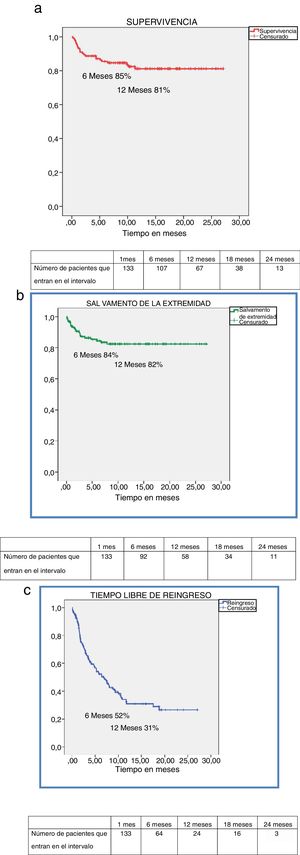
El tiempo medio de seguimiento fue de 12,1 meses (DS 7,3; rango: 0,21-27,1). Las tasas de supervivencia en nuestra muestra fueron de 85% y 81% a los 6 y 12 meses (fig. 1a). Treinta pacientes fallecieron durante el seguimiento por causas: cardiaca (n=3; 3,8%); cerebrovascular (n=4; 3%); respiratoria (n=3; 2,3%); digestiva (n=2; 1,5%); fracaso multiorgánico (n=2; 1,5%); renal (n=1; 0,8%); neoplasia (n=1; 0,8%); tratamiento sedoanalgésico paliativo (n=11; 8,3%) y desconocida (n=1; 0,8%). Las tasas de salvamento de la extremidad fueron de 84% y 82% para los mismos periodos (fig. 1b), realizándose 18 amputaciones supracondíleas y 3 infracondíleas. Las tasas de reingreso fueron de 48% y 69% a los 6 y 12 meses (fig. 1c). En total 79 pacientes (59,4%) reingresaron durante el periodo de seguimiento, de ellos: 37 (46,8%) por isquemia crítica de la misma extremidad inferior que ocasionó el ingreso basal (progresión de la isquemia, fracaso hemodinámico u oclusión de la técnica realizada), 10 (12,6%) por complicaciones relacionadas con las lesiones tróficas originales o las heridas quirúrgicas o los lechos de las amputaciones menores (soreinfección, dehiscencia); 4 (5,1%) por cuadros de isquemia aguda o crónica de la extremidad inferior contralateral; 9 (11,4%) por otros eventos cardiovasculares (insuficiencia cardiaca congestiva, ictus, tromboembolismo pulmonar, endarterectomía carotídea electiva); y 19 (24,1%) por eventos no cardiovasculares (hemorragia digestiva, diarrea, pancreatitis aguda, hematuria, uropatía obstructiva, cistolitotricia programada, insuficiencia renal crónica, EPOC descompensada, mononeuritis, fiebre de origen desconocido, descompensación glucémica, crisis parciales complejas, cuadro psicótico, disminución del nivel de conciencia).
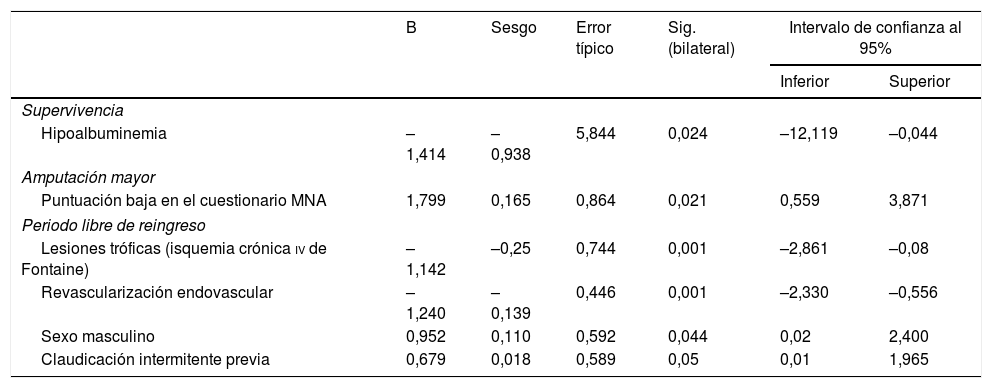
En el análisis univariante los factores asociados a mayor mortalidad fueron la edad (p=0,019), la cardiopatía (p=0,029), la IRC (p=0,027), la hipoalbuminemia (p=0,02) y el déficit de vitamina D (p=0,037). En el análisis multivariante tan solo la hipoalbuminemia se asoció con mayor riesgo independiente de mortalidad (p=0,024) (tabla 3).
Análisis multivariante: a) supervivencia; b) amputación mayor; y c) periodo libre de reingreso en los pacientes del estudio (regresión de Cox)
| B | Sesgo | Error típico | Sig. (bilateral) | Intervalo de confianza al 95% | ||
|---|---|---|---|---|---|---|
| Inferior | Superior | |||||
| Supervivencia | ||||||
| Hipoalbuminemia | –1,414 | –0,938 | 5,844 | 0,024 | –12,119 | –0,044 |
| Amputación mayor | ||||||
| Puntuación baja en el cuestionario MNA | 1,799 | 0,165 | 0,864 | 0,021 | 0,559 | 3,871 |
| Periodo libre de reingreso | ||||||
| Lesiones tróficas (isquemia crónica iv de Fontaine) | –1,142 | –0,25 | 0,744 | 0,001 | –2,861 | –0,08 |
| Revascularización endovascular | –1,240 | –0,139 | 0,446 | 0,001 | –2,330 | –0,556 |
| Sexo masculino | 0,952 | 0,110 | 0,592 | 0,044 | 0,02 | 2,400 |
| Claudicación intermitente previa | 0,679 | 0,018 | 0,589 | 0,05 | 0,01 | 1,965 |
El único factor asociado a una tasa más elevada de amputación mayor, tanto en el análisis univariante como en el multivariante, fue la puntuación baja en el MNA (p=0,021) (tabla 3).
En el análisis tanto univariante como multivariante los factores asociados a mayor tasa de reingreso fueron la presencia de lesiones tróficas (p=0,001), la revascularización endovascular comparada con la cirugía abierta (p=0,001) y el sexo femenino (p=0,044). La presencia de claudicación intermitente previa se asoció a menor tasa de reingresos (p=0,05) (tabla 3).
DiscusiónLa prevalencia de déficits nutricionales en los pacientes con isquemia crítica de las extremidades inferiores es elevada y su presencia se asocia a peor pronóstico9–12. En nuestro medio ya describimos previamente prevalencias especialmente elevadas de anemia (49,5%) y ferropenia (31,9%) en pacientes con isquemia crítica de extremidades inferiores, en un amplio estudio transversal13. En contraste, estas prevalencias eran mucho menores en pacientes con grados más leves de enfermedad periférica (9,8% de anemia y 6,7% de ferropenia entre claudicantes). Estas cifras se han reproducido en un reciente estudio multicéntrico realizado a lo largo de la geografía española, arrojando una prevalencia de anemia preoperatoria del 53,8% global en pacientes sometidos a revascularización aortoiliaca e infrainguinal, ascendiendo al 66,9% entre aquellos con isquemia crítica de las extremidades inferiores11. La malnutrición global se ha descrito como de alrededor del 20% en claudicantes pero >70% en pacientes con isquemia crítica13,14. La rentabilidad diagnóstica de la búsqueda sistemática de déficits nutricionales entre pacientes claudicantes es más escasa, pero es importante en pacientes con isquemia crítica dada la implicación pronóstica de su presencia13.
Nuestra práctica clínica se asemeja a otras a lo largo del país e internacionalmente, con un aumento de las técnicas endovasculares en detrimento de las abiertas, con un uso del 50% aproximadamente de unas y otras en el momento actual y una cifra baja de amputación primaria. Las tasas de supervivencia y salvación de la extremidad al año son buenas, >80% para ambos parámetros, algo mejores que los porcentajes históricos1.
Clásicamente se asocian a mayor mortalidad precoz y tardía factores clínicos como la edad, la cardiopatía, la IRC y la EPOC15. En nuestro estudio encontramos esta asociación también con los 3 primeros, no así con la EPOC. Adicionalmente, la hipoalbuminemia emerge como un factor de riesgo independiente, con un efecto aún mayor que los previos. Se ha descrito cómo la presencia de hipoalbuminemia se asocia a mayor incidencia de infarto de miocardio, accidente cerebrovascular y muerte en pacientes con isquemia crítica de las extremidades inferiores sometidos a revascularización abierta o endovascular15–17. La malnutrición severa, valorada mediante cuestionarios nutricionales como el MNA, aumentó el riesgo de mortalidad 5 veces en pacientes con isquemia crítica de extremidades inferiores en un reciente registro francés14. La anemia, que recientemente está demostrando un efecto negativo en el pronóstico de los pacientes quirúrgicos11,12, no demostró este efecto en nuestro estudio. Esto puede deberse, al menos en parte, a que nuestro análisis incluye todos los pacientes tratados por isquemia crítica, incluidos aquellos manejados de forma conservadora.
El riesgo de pérdida de extremidad también se ha asociado con la anemia12. En nuestro estudio solamente la puntuación baja en el MNA suponía un riesgo incrementado independiente de amputación mayor. Este hallazgo es similar al descrito por Salomon en su reciente estudio14.
Los reingresos aumentan la morbimortalidad de los pacientes y suponen una carga económica importante para el sistema sanitario18–20. La tasa de reingreso se considera un parámetro de calidad asistencial y se contempla como un factor a tener en cuenta para el reembolso económico en sistemas privados de salud18,19. Registramos tasas de reingreso muy elevadas en nuestra cohorte de pacientes, del 48% y 69% a los 6 y 12 meses respectivamente. Cifras similares, con un 47,7% de reingreso no programado a los 6 meses se describe en el estudio de Agarwal de 201718. La principal causa de reingreso era la isquemia crítica inicial. En este estudio describen como factores predictores de reingreso: la edad, el sexo femenino, la raza negra o latina, la amputación previa, el índice de comorbilidad de Charlson y la necesidad de soporte médico o rehabilitación al alta. La revascularización de cualquier tipo reducía los reingresos no programados, con mayor impacto protector de la cirugía abierta (OR 0,36; IC 95% 0,34-0,36) frente a la revascularización endovascular (0,76; IC 95% 0,73-0,78)18. En nuestro estudio las mujeres también presentaron mayores tasas de reingreso, sin que se reprodujeran el resto de factores descritos. Sí aumentaron el riesgo, sin embargo, la presencia de lesiones tróficas o el tratamiento endovascular. Estos factores también se describen en el estudio de Reed publicado en 201619, centrado en los reingresos específicamente tras el tratamiento endovascular de pacientes con isquemia crítica de extremidades inferiores. En este estudio se recogió una incidencia de reingresos del 56%, la mitad de ellos en los primeros 6 meses. La causa más frecuente de reingreso se relacionaba con la mala evolución de las lesiones tróficas (43%), seguida de causas no cardiovasculares (hemorragia gastrointestinal, infección urinaria, etc.) (34%) y finalmente causas cardiovasculares (isquemia de la misma extremidad o contralaterales, eventos cardiacos o cerebrovasculares y tromboembolismo venoso) (23%). Los factores de riesgo independientes que identificaron para el reingreso fueron la edad, el sexo femenino, la presencia de lesiones tróficas, la hemodiálisis y el antecedente de insuficiencia cardiaca. A su vez, los reingresos suponían un factor de riesgo para la pérdida de extremidad y/o mortalidad19. Se ha descrito, por otro lado, que la persistencia de anemia tras el alta hospitalaria es un factor que aumenta el riesgo de reingreso antes de los 30 días, y en una medida directamente proporcional a la severidad de la anemia21. En contraste, en un estudio centrado en pacientes sometidos a bypass aortocoronario, no se reprodujo este riesgo incrementado de reingreso precoz22. Tampoco en nuestra cohorte hemos identificado específicamente la anemia como un factor que aumente la incidencia de reingreso.
El antecedente previo de claudicación intermitente ha actuado como un factor protector de reingreso. Es posible que esto se deba a un mejor control médico y de los factores de riesgo cardiovascular, tratamiento farmacológico más completo y precoz, y a una mayor concienciación de los pacientes ante la enfermedad, con derivación hospitalaria más precoz ante la progresión a isquemia crítica.
La mayor limitación de este estudio es su pequeño tamaño muestral. Se trata de los resultados iniciales de un registro prospectivo iniciado en octubre de 2013, por lo que, con el tiempo, podremos no solo ampliar su número, sino también el tiempo de seguimiento, lo que nos permitirá profundizar en el estudio de estos hallazgos preliminares. Queda fuera del alcance del presente estudio evaluar el impacto de la suplementación nutricional específica sobre el pronóstico de los pacientes y la relación de coste-efectividad de dicha intervención.
Los datos son prospectivos y abarcan el espectro completo de pacientes con isquemia crítica de extremidades inferiores. Consideramos este enfoque muy útil para una perspectiva más global de estos pacientes. Parámetros como la tasa de reingreso pueden resultar interesantes en la evaluación de la historia natural de los pacientes y la calidad asistencial que se les ofrece.
Concluimos que la malnutrición es un factor muy prevalente, potencialmente tratable y que tiene una clara implicación en el pronóstico vital y funcional de los pacientes con isquemia crítica de las extremidades inferiores. Por ello, recomendamos una evaluación nutricional de los pacientes con esta enfermedad mediante el cuestionario MNA y una analítica específica.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses..
Agradecemos a la Sociedad Española de Angiología y Cirugía Vascular la organización del tercer curso Cómo escribir y publicar un artículo científico, y a los organizadores y ponentes que en él participaron, especialmente al Dr. Rodrigo Rial Horcajo, por su papel como tutor durante dicho curso.
Este trabajo fue presentado como comunicación oral en el 62 Congreso Nacional de la SEACV, en Sitges, el 7-10 de junio de 2016.